AIRTIDE 500 mcg/50 mcg inhilasyon için toz içeren kapsül Farmakolojik Özellikler
{ Flutikazon + Salmeterol }
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grubu: Kortikosteroidler ve Diğer İlaçlar ile Kombine Adrenerjikler (Antikolinerjik Kombinasyonları Hariç)
ATC Kodu: R03AK06
Etki mekanizması
AİRTİDE farklı etki şekline sahip salmeterol ve flutikazon propiyonat içermektedir. İki etkin maddenin ilgili etki mekanizmaları aşağıda tartışılmaktadır.
Salmeterol
Salmeterol, reseptörün sekonder bağlanma bölgesine bağlanan bir uzun yan zinciri olan, selektif uzun etkili (12 saat) bir betaadrenoreseptör agonistidir. Salmeterol klasik kısa etkili betaagonistlerin önerilen dozlarına kıyasla en az 12 saat süren daha uzun süreli bronkodilatasyon sağlamaktadır.
Flutikazon propiyonat,
Önerilen dozlarda inhalasyon yoluyla verilen flutikazon propiyonat akciğerlerde bir glukokortikoid antienflamatuvar etkiye sahiptir ve bu etki kortikosteroidler sistemik yolla uygulandığında görülenden daha az yan etkiyle semptomlarda ve astım alevlenmelerinde azalma sağlamaktadır.
Klinik etkililik ve güvenlilik
Flutikazon propiyonat/Salmeterol astım klinik çalışmaları
Uzun süreli astımlı 3416 erişkin ve adolesanda yapılan 12 aylık bir çalışmada (Optimal Astım Kontrolünü Sağlanması, GOAL) astım tedavisi hedeflerinin erişilebilir olup olmadığının belirlenmesi için tek başına inhale kortikosteroidler (Flutikazon Propiyonat) ile Flutikazon propiyonat/Salmeterol'ün etkililik ve güvenliliği karşılatırılmıştır. Tedavi dozu **Toplam kontrol sağlanana veya çalışma ilacının en yüksek dozuna erişilene kadar 12 haftada bir artırılmıştır. GOAL, Flutikazon propiyonat/Salmeterol verilen hastadan tek başına inhale kortikosteroid (IKS) verilen hastalara kıyasla daha fazla hastalarda astım kontrolü sağlandığı ve bu kontrolün daha düşük kortikosteroid dozunda elde edildiğini göstermiştir.
*İyi kontrol altına alınmış astım, tek başına IKS'ye kıyasla Flutikazon propiyonat/Salmeterol ile daha hızlı şekilde elde edilmiştir. Bireysel olarak iyi kontrolün sağlandığı haftanın elde edilmesi için hastaların %50'sindeki tedavi süresi Flutikazon propiyonat/Salmeterol için 16 gün ve IKS grubu için 37 gündü. Daha önce steroid tedavisi alamayan bir hasta alt grubunda bireysel iyi kontrol altına alınmış haftaya kadar geçen süre Flutikazon propiyonat/Salmeterol ile 16 gün olurken IKS ile 23 gün olmuştur.
Genel çalışma bulguları aşağıdakileri göstermiştir:
12 Ayda *İyi Kontrol Altına Alınmış (WC) ve **Tam Olarak Kontrol Altına Alınmamış (TC) Astımlı Hastaların Oranı | ||||
Çalışma Öncesi Tedavi | Salmeterol/FP | FP | ||
WC | TC | WC | TC | |
IKS yok (tek başına kısa etki süreli beta agonisti SABA) | %78 | % 50 | %70 | %40 |
Düşük doz IKS (≤500mcg beklometazon dipropiyonat (BDP) veya eşdeğer/gün) | %75 | %44 | %60 | %28 |
Orta doz IKS (>500-1000mcg dipropiyanat BDP veya eşdeğer/gün) | %62 | %29 | %47 | %16 |
3 tedavi düzeyinde birleştirilmiş bulgular | %71 | %41 | %59 | %28 |
*Yeterli düzeyde kontrol altına alınan astım; >1 semptom skoru ile ≤ 2 gün (semptom skoru 1, ‘gün içinde bir kısa süreli semptom' şeklinde tanımlanır), ≤2 gün ve haftada ≤4 SABA kullanımı, ≥ %80 öngörülen sabah pik ekspiratuar akımı, gece uyanmalarının olmaması, alevlenmelerin olmaması ve tedavi değişikliği gerektiren yan etkilerin olmaması
**Tam kontrol altına alınan astım; semptomların olmaması, SABA kullanımının olmaması, ≥ %80 öngörülen sabah pik ekspiratuar akışı, gece uyanmalarının olmaması, alevlenmelerin olmaması ve tedavi değişikliği gerektiren yan etkilerin olmaması
Bu çalışmadaki bulgular günde iki kez Salmeterol/Flutikazon 50/100 mikrogram dozunun, hızlı astım kontrolünün gerekli olduğu düşünülen orta şiddette dirençli astım hastalarında ilk idame tedavisi olarak değerlendirilebileceğini düşündürmektedir.
≥18 yaşındaki dirençli astım hastası 318 kişide yapılan bir çift kör, randomize, paralel gruplu çalışmada iki haftalık sürede günde iki kez iki inhalasyonla (çift doz) Flutikazon propiyonat/Salmeterol kullanımının güvenlilik ve tolerabilitesi değerlendirilmiştir. Bu çalışma 14 güne kadar her Flutikazon propiyonat/Salmeterol dozu inhalasyonunun iki katına çıkarılmasının günde iki kez tek inhalasyona kıyasla beta agonist ile ilişkili yan etkilerde küçük bir artışa (tremor; 0'a karşı 1 hasta [%1], palpitasyon; 1 hastaya [<%1] karşı 6 [%3], kas krampları; 1 [<%1] hastaya karşı 6 [%3] ) ve inhale kortikosteroid ile ilişkili yan etkilerde benzer bir insidansa neden olduğunu göstermiştir (örn, oral kandidiyazis; 16 hastaya [%8] karşı 6 [%6], ses kısıklığı; 4 hastaya [%2] karşı 2 [%2] ). Flutikazon propiyonat/Salmeterol dozunun ek kısa süreli (14 güne kadar) inhale kortikosteroid tedavisine ihtiyaç duyulan erişkin hastalarda iki katına çıkarılması düşünülürse beta agonist ile ilişkili yan etkilerdeki küçük artış dikkate alınmalıdır.
Astım
Çok Merkezli Salmeterol Astım Araştırma Çalışması
Çok Merkezli Salmeterol Astım Araştırma Çalışması, yetişkin ve ergen gönüllülerde olağan tedaviye salmeterol veya plasebo eklenmesinin güvenliliğini karşılaştıran 28 haftalık bir ABD çalışmasıydı. Solunum ile ilişkili ölüm ve solunum ile ilişkili yaşamı tehdit eden olayların kombine sayısı olan primer sonlanım noktası açısından anlamlı farklılık olmasa da, çalışma salmeterol alan hastalarda astımla ilişkili ölüm sayısında anlamlı artış göstermiştir (salmeterol ile tedavi edilen 13.176 hastada 13 ölüme kıyasla plasebo alan 13.179 hastada 3 ölüm). Çalışma eş zamanlı inhale kortikosteroid kullanımının etkisini değerlendirmek için tasarlanmamıştır ve gönüllülerin yalnızca
%47'si başlangıçta İKS kullanımını bildirmiştir.
Astımda salmeterol+flutikazon propiyonat ile tek başına flutikazon propiyonatın güvenliliği ve
etkililiği
Salmeterol+flutikazon propiyonat ile tek başına flutikazon propiyonat'ın güvenliliği ve etkililiğini karşılaştırmak için biri yetişkin ve ergen gönüllülerde (AUSTRI çalışması), diğeri 4-11 yaşlarında pediyatrik gönüllülerde (VESTRI çalışması) olmak üzere iki tane çok merkezli 26 haftalık çalışma yürütülmüştür. Her iki çalışmaya dahil edilen gönüllülerin bir önceki yılda astımla ilişkili hastaneye yatış veya astım alevlenmesi ile birlikte orta ile şiddetli inatçı astımı vardı. İki çalışmanın da primer hedefi tek başına İKS'ye (flutikazon propiyonat) kıyasla İKS tedavisine LABA eklenmesinin (salmeterol+flutikazon propiyonat) astımla ilişkili olaylar (astımla ilişkili hastaneye yatış, endotrakeyal entübasyon ve ölüm) açısından non- inferioriteyi değerlendirmekti. Çalışmanın ikincil hedefi ciddi astım alevlenmesi (astımın kötüye gitmesi nedeniyle en az 3 gün sistemik kortikosteroid kullanımına gerek olması veya sistemik kortikosteroid kullanımı gerektiren astım nedenli hastaneye veya acile yatış olarak tanımlanmıştır) açısından İKS+LABA'nın (salmeterol+flutikazon propiyonat) tek başına İKS tedavisine (flutikazon propiyonat) üstünlüğünü değerlendirmekti.
AUSTRI ve VESTRI çalışmalarına sırasıyla 11.679 ve 6.208 hasta randomize edilmiş ve tedavi görmüştür. Primer sonlanma noktası güvenlilik için, her iki çalışmada da non- inferiorite gösterilmiştir (bkz. aşağıda tablo)
26 haftalık AUSTRI ve VESTRI çalışmalarında astımla ilişkili ciddi olaylar
| AUSTRI | VESTRI | ||
| Salmeterol+ | Tek başına | Salmeterol+ | Tek başına |
Flutikazon | flutikazon | Flutikazon | flutikazon | |
propiyonat | propiyonat | propiyonat | propiyonat | |
(n=5.834) | (n=5.845) | (n=3.107) | (n=3.101) | |
Birleşik sonlanma noktası (astımla ilişkili hastaneye yatış, endotrakeyal entübasyon ve ölüm) | 34 (%0.6) | 33 (%0.6) | 27 (%0.9) | 21 (%0.7) |
Salmeterol+flutikazon | 1.029 |
| 1.285 |
|
propiyonat/flutikazon | (0.638-1.622) | (0.726-2.272) | ||
propiyonat risk oranı (GA: |
|
| ||
%95) |
|
| ||
Ölüm | 0 | 0 | 0 | 0 |
Astımla ilişkili hastaneye yatış | 34 | 33 | 27 | 21 |
Endotrakeyal entübasyon | 0 | 2 | 0 | 0 |
verilmiştir
İkincil etkililik sonlanma noktası için, flutikazon propiyonat'la karşılaştırıldığında salmeterol+flutikazon propiyonat'ta ilk astım alevlenmesine kadar geçen sürede azalma her iki çalışmada da görülmüştür, ancak yalnızca AUSTRI'de istatistiksel olarak anlamlı fark sağlanmıştır:
| AUSTRI | VESTRI | ||
| Salmeterol+ | Tek başına | Salmeterol+ | Tek başına |
Flutikazon | flutikazon | Flutikazon | flutikazon | |
propiyonat | propiyonat | propiyonat | propiyonat | |
(n=5.834) | (n=5.845) | (n=3.107) | (n=3.101) | |
Astım alevlenmesi olan gönüllülerin sayısı | 480 (%8) | 597 (%10) | 265 (%9) | 309 (%10) |
Salmeterol+flutikazon | 0.787 | 0.859 | ||
propiyonat/flutikazon | (0.698, 0.888) | (0.729, 1.012) | ||
propiyonat risk oranı (GA: |
|
| ||
%95) |
|
| ||
KOAH
Kısa etkili beta-agonistlerine % 10 reversibilite kısıtlaması olmayan semptomatik KOAH hastaları:
6 ay boyunca yürütülen plasebo kontrollü klinik çalışmalar, 50/250 mikrogram ve 50/500 mikrogram'lık Flutikazon propiyonat/Salmeterolün düzenli kullanımının akciğer fonksiyonunu hızlı ve anlamlı derecede düzelttiğini, nefes darlığını ve rahatlatıcı ilaç kullanımını anlamlı derecede azalttığını göstermiştir. Aynı zamanda hastaların sağlık durumunda da anlamlı derecede düzelme olmuştur.
Kısa etkili beta-agonistlerine % 10'dan daha az reversibilite gösteren semptomatik KOAH hastaları:
6 ve 12 ay boyunca yürütülen plasebo kontrollü klinik çalışmalar, 50/500 mikrogram Flutikazon propiyonat/Salmeterol'ün düzenli kullanımının akciğer fonksiyonunu hızlı ve anlamlı derecede düzelttiğini, nefes darlığını ve rahatlatıcı ilaç kullanımını anlamlı derecede azalttığını göstermiştir. 12 aylık periyod boyunca KOAH alevlenme riski ve ilave oral kortikosteroid ihtiyacı anlamlı derecede azalmıştır. Aynı zamanda hastaların sağlık durumunda da anlamlı derecede düzelme olmuştur.
Flutikazon propiyonat/Salmeterol 50/500 mikrogram hem tedavi sırasında sigara içen, hem de sigarayı bırakmış hastalarda akciğer fonksiyonunu ve sağlık durumunu düzeltmede ve KOAH alevlenme riskini azaltmada etkili bulunmuştur.
TORCH çalışması (TOwards a Revolution in COPD Health; KOAH'ta devrime doğru): TORCH, KOAH hastalarında, günde 2 kez 50/500 mikrogram Flutikazon propiyonat/Salmeterol, günde 2 kez 50 mikrogram salmeterol, günde 2 kez 500 mikrogram FP (flutikazon propiyonat) veya plasebo ile yapılan tedavinin tüm nedenlere bağlı ölümler üzerindeki etkisini değerlendirmek için yapılan 3 yıllık bir çalışmadır. Başlangıç (bronkodilatatörden önce) FEV'i beklenen normal değerin % 60'ından az olan orta-şiddetli ve şiddetli KOAH hastaları çift-kör tedavi almak üzere randomize edilmiştir. Çalışma boyunca, diğer inhale kortikosteroidler, uzun etkili bronkodilatörler ve uzun süre sistemik kortikosteroidler dışında, her zamanki KOAH tedavilerini almalarına izin verilmiştir. 3 yıllık sağkalım durumu, çalışmadan çıkıp çıkmadıklarına bakılmaksızın hastaların tümü için tespit edilmiştir. Primer sonlanma noktası, plaseboya kıyasla Flutikazon propiyonat/Salmeterol için 3 yılda tüm nedenlere bağlı ölümlerin azaltılmasıdır. (Tablo 1)
Tablo 1
| Plasebo N = 1524 | Salmeterol 50 N = 1521 | FP 500 N = 1534 | Flutikazon propiyonat/ Salmeterol 50/500 N = 1533 |
3 yılda tüm nedenlere bağlı ölüm | ||||
Ölüm sayısı | 231 | 205 | 246 | 193 |
(%) | (% 15,2) | (% 13,5) | (% 16,0) | (% 12,6) |
Plaseboya karşı risk oranı |
|
|
|
|
(GA) | Geçerli | 0.879 | 1,060 | 0,825 |
p değeri | değil | (0.73, 1,06) 0,180 | (0,89, 1,27) | (0,68, 1,00) 0,052 |
|
|
| 0,525 |
|
Risk oranı, | Geçerli | 0,932 | 0,774 | Geçerli |
komponentlerine karşı Flutikazon | değil |
|
| değil |
propiyonat/Salmeterol 50/500 |
| (0,77, 1,13) | (0,64, |
|
(GA) p değeri |
| 0,481 | 0,93) 0,007 |
|
1. birincil etkinlik karşılaştırılması üzerinde yapılmış 2 ara analizin sigara içme durumu açısından gruplandırılmış bir log-rank analizi için ayarlanmış P değeri.
Flutikazon propiyonat/Salmeterol'ün, plaseboya kıyasla 3 yıl içinde herhangi bir zamanda ölüm riskini % 17,5 oranında azalttığı görülmüştür. (Risk Oranı 0,825 (% 95 GA 0,68, 1,00, p = 0,052; tümü ara analizler için ayarlanmıştır). Plaseboya kıyasla, üç yıllık süre içinde herhangi bir zamanda herhangi bir nedenden dolayı gerçekleşen ölümlerde, salmeterol ile % 12 azalma (p = 0,180) ve FP ile % 6 artış (p = 0,525) olmuştur. (Tablo 1)
Cox'un Orantısal Risk modelinin kullanıldığı destekleyici bir analiz, plaseboya kıyasla 3 yıl içinde herhangi bir zamanda ölüm riskinde % 19 azalma gösteren Flutikazon propiyonat/Salmeterol için 0,811'lik (% 95 GA 0,670, 0,982, p = 0,031) bir risk oranı olduğunu göstermiştir. Model önemli faktörler (sigara içme durumu, yaş, cinsiyet, bölge, başlangıç FEVve Vücut Kitle İndeksi) için ayarlanmıştır. Tedavi etkilerinin bu faktörlere göre değiştiğine dair kanıt yoktur. (Tablo 1)
Üç yıl içinde KOAH'a bağlı nedenlerden dolayı ölen hastaların yüzdesi plasebo için % 6, salmeterol için % 6,1, FP için % 6.9 ve Flutikazon propiyonat/Salmeterol için % 4,7'dir. (Tablo 1)
Plaseboya kıyasla Flutikazon propiyonat/Salmeterol, orta şiddetli ve şiddetli alevlenmeleri % 25 (% 95 GA: % 19 ve % 31 arasında; p < 0.001) oranında azaltmıştır Flutikazon propiyonat/Salmeterol alevlenme oranını, salmeterol ile karşılaştırıldığında % 12 (% 95 GA: % 5 ve % 19 arasında; p = 0.002), FP ile karşılaştırıldığında da % 9 (% 95 GA: % 1 ve % 16 arasında; p = 0.024) oranında azaltmıştır. Plaseboya kıyasla salmeterol ve FP alevlenme oranını anlamlı derecede sırasıyla % 15 (% 95 GA: % 7 ve % 22 arasında; p < 0,001) ve % 18 (% 95 GA: % 11 ve % 24 arasında; p <
0,001) oranında azaltmıştır.
St George Solunum Anketi (SGSA) ile ölçülen Sağlıkla İlişkili Yaşam Kalitesi, plaseboya kıyasla tüm aktif tedavi yöntemleri ile düzelmiştir. Üç yıl boyunca Flutikazon propiyonat/Salmeterol ile sağlanan ortalama düzelme plaseboya kıyasla – 3,1 birim (% 95 GA: - 4,1 ve – 2,1 arasında; p <
0,001), salmeterole kıyasla - 2.2 birim (p < 0,001) ve FP'ye kıyasla - 1.2 birimdir (p = 0,017).
Üç yıllık tedavi süresi boyunca, FEVdeğerleri Flutikazon propiyonat/Salmeterol ile tedavi edilenlerde plasebo ile tedavi edilenlerden daha yüksektir (3 yıl boyunca ortalama fark 92 mL, % 95 GA: 75 - 108 mL; p < 0,001). FEVüzerinde Flutikazon propiyonat/Salmeterol salmeterolden veya FP'den daha etkilidir (salmeterol için ortalama fark 50 mL, p < 0,001 ve FP için 44 mL'dir, p
< 0.001).
Advers olay olarak bildirilen pnömoninin 3 yıllık tahmini olasılığı plasebo için % 12.3, salmeterol için % 13.3, FP için % 18.3 ve Flutikazon propiyonat/Salmeterol için % 19,6'dır (Flutikazon propiyonat/Salmeterol'ün plaseboya karşı risk oranı: 1,64, % 95 GA: 1,33 ve 2,01 arasında, p < 0,001). Pnömoni ile ilişkili ölümlerde artış olmamıştır; tedavi sırasında birincil olarak pnömoniye bağlı oldukları düşünülen ölümler plasebo için 7, salmeterol için 9, FP için 13 ve Flutikazon propiyonat/Salmeterol için 8 olarak tespit edilmiştir. Kemik kırılma olasılığında anlamlı farklılık yoktur (plasebo % 5,1, salmeterol % 5,1, FP % 5,4 ve Flutikazon propiyonat/Salmeterol % 6,3; plaseboya karşı Flutikazon propiyonat/Salmeterol için risk oranı: 1,22, % 95 GA: 0,87 ve 1,72 arasında, p = 0.248). Göz bozuklukları, kemik bozuklukları ve hipotalamus-hipofiz-adrenal eksen bozuklukları ile ilgili advers olayların insidansı düşüktür ve tedaviler arasında farklılık gözlenmemiştir. Salmeterol alan tedavi gruplarında kardiyak advers olaylarında artış olduğuna dair kanıt yoktur.
Pediyatrik popülasyon:
SAM101667 çalışmasında, 6 ila 16 yaşlarında semptomatik astımı olan 158 çocukta, semptom kontrolü ve akciğer fonksiyonu açısından salmeterol/flutikazon propiyonat kombinasyonu flutikazon propiyonat dozunun ikiye katlanmasıyla eşit etkililikte bulunmuştur. Bu çalışma alevlenme üzerine etkileri araştırmak için tasarlanmamıştır.
4 ila 11 yaşlarında çocukların (n=257), her ikisi de günde iki defa olmak üzere salmeterol/flutikazon propiyonat 50/100 veya salmeterol 50mcg + flutikazon propiyonat 100mcg ile tedavi edildiği 12 haftalık bir çalışmada, her iki tedavi kolunda pik ekspiratuar akımda %14'lük bir gelişme ile semptom skoru ve kurtarıcı salbutamol kullanımında iyileşmeler görülmüştür. İki tedavi kolu arasında farklılık bulunmamıştır. İki tedavi kolu arasında güvenlilik parametreleri açısından farklılık bulunmamıştır.
4 ila 11 yaşlarında persistan astımı olan ve inhale kortikosteroid tedavisindeyken semptomatik olan çocukların (n=203) dahil edildiği randomize paralel grup çalışmasında güvenlilik primer hedef olmuştur. Çocuklara günde iki defa tek başına salmeterol/flutikazon propiyonat (50/100mcg) veya tek başına flutikazon propiyonat (100mcg) tedavisi verilmiştir. Salmeterol/flutikazon propiyonat alan iki çocuk ve flutikazon propiyonat alan beş çocuk astımın kötüleşmesi nedeniyle çalışmadan ayrılmıştır. 12 hafta sonunda çalışmanın her iki kolunda da 24 saatlik üriner kortizol atılımı anormal olan çocuk bulunmamıştır. Çalışma kolları arasında güvenlilik profili açısından fark bulunmamıştır.
Gebelik sırasında astımda flutikazon propiyonat içeren ilaçların kullanımı
Majör konjenital malformasyon (MKM) riskini değerlendirmek için, Birleşik Krallık elektronik sağlık kayıtları kullanılarak birinci trimesterde tek başına inhale flutikazon propiyonat ve salmeterol+flutikazon propiyonat ile flutikazon propiyonat içermeyen İKS maruziyetinin karşılaştırıldığı, gözlemsel retrospektif epidemiyolojik kohort çalışması yürütülmüştür. Bu çalışmaya karşılaştırma amaçlı plasebo dahil edilmemiştir.
Birinci trimesterde İKS-maruziyeti olan 5362 gebeden oluşan astım kohortunda, 131 tanı konmuş
MKM belirlenmiştir; flutikazon propiyonat veya salmeterol+flutikazon propiyonat maruziyeti olan 1612'sinden (%30) 42'sinde MKM tanısı konulduğu belirlenmiştir. 1. yılda flutikazon propiyonat ile flutikazon propiyonat olmayan İKS maruziyeti karşılaştırıldığında kadınlarda tanı konulmuş MKM'ler için ayarlanmış olasılık oranı orta şiddette astımlılarda 1,.1 (%95 GA: 0.5 – 2,3) ve şiddetli astımlılarda 1,2 (%95 GA: 0,7 – 2,0) olmuştur. İlk trimesterde tek başına flutikazon propiyonat ile salmeterol+flutikazon propiyonat maruziyeti karşılaştırıldığında MKM riskinde farklılık görülmemiştir. Astım şiddet basamaklarında mutlak MKM riskleri flutikazon propiyonat maruziyeti olan 100 gebelikte 2,0 ila 2,9 arasında değişmektedir. Bu da Pratisyen Hekimlik Araştırma Veritabanında astım tedavisine maruziyeti olmayan 15,840 gebelikte yürütülen çalışmanın sonuçlarıyla karşılaştırılabilir olmuştur (100 gebelikte 2,8 MKM).
5.2. Farmakokinetik özellikler
Genel özellikler
Hayvanlarda veya insanlarda inhalasyon yoluyla birlikte uygulanan salmeterol ve flutikazon propiyonatın birbirlerinin farmakokinetiğini etkilediğine dair herhangi bir bulgu yoktur.
Bu nedenle farmakokinetik açıdan her iki bileşen ayrı ayrı düşünülebilir.
Salmeterol
Salmeterol akciğerlerde lokal olarak etki eder, bu nedenle plazma seviyeleri terapötik etkinin belirleyicisi değildir. Terapötik dozlarda inhalasyondan sonra çok düşük plazma konsantrasyonları gösterdiği için (yaklaşık 200 pg/ml veya daha az) plazmadaki ilaç miktarının tayini teknik olarak zor olduğundan salmeterolün farmakokinetiği ile ilgili sadece sınırlı veriler bulunmaktadır.
Flutikazon propiyonat
Emilim:
Sağlıklı gönüllülerde inhalasyon yoluyla alınan tek doz flutikazon propiyonatın mutlak biyoyararlanımı, kullanılan inhalasyon cihazına göre nominal dozun yaklaşık %5-11'i arasında değişmektedir. Astımlı hastalarda inhale flutikazon propiyonata sistemik maruziyetin daha düşük düzeyde gözlenmiştir. Sistemik emilim temelde akciğerlerde meydana gelmekte olup ilk başta hızlı ve sonrasında uzun sürelidir. İnhale dozun kalanı yutulabilir ancak düşük suda çözünürlük ve presistemik metabolizma nedeniyle sistemik maruziyete minimum katkıda bulunur ve oral biyoyararlanımının %1'den az olmasını sağlar. Sistemik maruziyet, inhale dozun artışıyla lineer şekilde artar.
Dağılım:
Flutikazon propiyonatın dispozisyonu, yüksek plazma klirens (1150 ml/dak), kararlı durumda yüksek dağılım hacmi (300 L) ve yaklaşık 8 saat olan terminal yarılanma ömrü ile karakterizedir.
Flutikazon propiyonatın plazma proteinlerine bağlanma oranı % 91'dir. Biyotransformasyon:
Flutikazon propiyonat başlıca sitokrom P450 enzimi CYP3A4 tarafından inaktif karboksilik asite
metabolize edilir.
Eliminasyon:
Flutikazon propiyonat sistemik dolaşımdan çok hızlı temizlenir. Flutikazon propiyonatın renal
klirensi önemsiz düzeydedir. Dozun %5'inden daha azı idrarda temelde metabolitler olarak atılmaktadır. Dozun büyük bir bölümü feçeste metabolitler ve değişmemiş olarak atılmaktadır.
Hastalardaki karakteristik özellikler Böbrek/Karaciğer yetmezliği:
Veri bulunmamaktadır. Değişik yaş grupları:
Pediyatrik popülasyon
4 ila 77 yaş arası 350 hastayı (hastaların 174'ü 4-11 yaş) içeren, farklı cihazların (DISKUS, ölçülü inhalasyon cihazı) kullanıldığı, kontrol gruplarına yer verilen 9 çalışmadan bildirilen verilerin kullanıldığı bir popülasyon farmakokinetiği analizinde, flutikazon propiyonat 100 ile karşılaştırıldığında Flutikazon propiyonat /salmeterol 50/100 ile tedavi sonrasında daha yüksek flutikazon propionat sistemik maruziyeti görülmüştür.
Çocuklarda ve Adölesan/Erişkin Popülasyonlarda flutikazon propionat karşısında
Salmeterol/flutikazon propiyonat karşılaştırması için Geometrik Ortalama Oranı [%90 GA]
Tedavi (test karşısında referans) | Popülasyon | EAA | C |
Salmeterol/ flutikazon propiyonat 50/100 flutikazon propiyonat 100 | Çocuklar (4– 11yaş) | 1.20 [1.06 – 1.37] | 1.25 [1.11 – 1.41] |
Salmeterol/ flutikazon propiyonat 50/100 flutikazon propiyonat 100 | Adölesan/Erişki n (≥12 yaş) | 1.52 [1.08 – 2.13] | 1.52 [1.08 – 2.16] |
21 günlük Flutikazon propiyonat/salmeterol inhaler 25/50 mikrogram (spacer ile birlikte veya spacer olmaksızın günde iki kez 2 inhalasyon) veya Flutikazon propiyonat/salmeterol US 50/100 mikgrogram (günde iki kez 1 inhalasyon) tedavilerinin etkisi 4 ila 11 yaşlarında hafif astımlı 31 çocukta değerlendirilmiştir. Flutikazon propiyonat/salmeterol inhaler, spacer ile birlikte Flutikazon propiyonat/salmeterol inhaler ve Flutikazon propiyonat/salmeterol için salmeterol sistemik maruziyeti benzer olmuştur (sırasıyla 126pg sa/mL [%95 GA: 70, 225], 103pg sa/mL [%95 GA: 54,
200] ve 110 pg sa/mL [%95 GA: 55, 219]). Flutikazon propiyonat sistemik maruziyeti spacer ile birlikte kullanılan Flutikazon propiyonat/salmeterol inhaler ile (107pg sa/mL [%95 GA: 45.7, 252.2]) ve Flutikazon propiyonat/salmeterol'de (138pg sa/mL [%95 GA: 69.3, 273.2]) benzer olmştur, ancak Flutikazon propiyonat/salmeterol inhaler için daha düşüktür (24pg sa/mL [%95 GA: 9.6, 60.2]).
5.3. Klinik öncesi güvenlilik verileri
Ayrı şekilde verilen salmeterol ve flutikazon propiyonatın hayvan çalışmalarına göre insanlarda kullanıma yönelik güvenlilikle ilişkili tek endişe farmakolojik etkilerin artmasıyla ilişkili etkiler olmuştur.
Hayvan üreme çalışmalarında glukokortikoidlerin, malformasyonlara (yarık damak, iskelet
bozuklukları) neden olduğu gösterilmiştir. Bununla birlikte bu hayvan deneylerinin önerilen dozların verildiği insanlar için anlamlı olduğu düşünülmemektedir. Salmeterol ksinafoat ile yapılan hayvan çalışmaları sadece yüksek maruziyet düzeylerinde embriyofetal toksisite göstermiştir. Birlikte uygulanımı takiben bilinen glukokortikoid kaynaklı anomalilerle ilişkilendirilen dozlarda sıçanlarda artan transpoze umblikal arter ve ossipital kemikte eksik osifikasyon insidansı tespit edilmiştir. Salmeterol ksinafoat veya flutikazon propioynat genetik toksisite potansiyeli göstermemiştir.
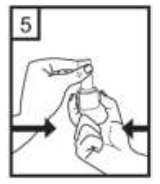
Cihazı dik tutun, kenardaki düğmelere sadece bir kez tam olarak basın ve bırakın. Kapsül her iki
ucundan delinecektir.
Nefes almanız sırasında küçük jelatin kapsül parçaları ağzınıza gelebilir. Jelatin parçaları zararsızdır ve yutulduktan sonra sindirileceklerdir. Küçük jelatin parçalarının oluşma riski kapsülün ambalajından çıkarılır çıkarılmaz hemen kullanılması ve düğmelere sadece bir kez basılması ile azalır.
 Mide Kanseri
Mide kanseri genellikle mideyi tümüyle kaplayan ve mukus üretmekle görevli hücrelerde başlar. Bu kanser tipine adenokarsinom denir.
Mide Kanseri
Mide kanseri genellikle mideyi tümüyle kaplayan ve mukus üretmekle görevli hücrelerde başlar. Bu kanser tipine adenokarsinom denir. |
 Aşırı Alkol Kullanımı, Alkolizm
Alkol bağımlılığı, alkol kullanımı ve alkol sorunları arasındaki farkı açıklamak güçtür.
Örneğin, geçmişte alkol kullanmış olan bir kimsenin mutlaka alkol bağımlısı olması
gerekmez.
Aşırı Alkol Kullanımı, Alkolizm
Alkol bağımlılığı, alkol kullanımı ve alkol sorunları arasındaki farkı açıklamak güçtür.
Örneğin, geçmişte alkol kullanmış olan bir kimsenin mutlaka alkol bağımlısı olması
gerekmez. |
İLAÇ GENEL BİLGİLERİ
Humanis Sağlık Anonim Şirketi
| Geri Ödeme Kodu | A16069 |
| Satış Fiyatı | 895.94 TL [ 1 Dec 2025 ] |
| Önceki Satış Fiyatı | 895.94 TL [ 24 Nov 2025 ] |
| Original / Jenerik | Jenerik İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8680760150270 |
| Etkin Madde | Flutikazon + Salmeterol |
| Yerli ve Beşeri bir ilaçdır. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| Eşdeğer bir ilaç bulunamadı |
 |
Lösemi Kan Kanseri Lösemi, kan kanseridir ve vücudunun kan oluşturan dokularının hastalanması anlamına gelir. Birçok lösemi türü vardır; bazı lösemi türleri çocuklarda bazıları da yetişkinlerde sık görülür. |
 |
Şizofrenlik Şizofrenliğin psikiatrik teşhisi hakkında çok fazla anlaşmazlık vardır. Bu sayfadaki bilgiler, şizofrenliğin teşhisi, nedenleri ve tedavisi hakkındaki faklı teoriler hakkında bilgi verecektir. |
 |
Kalp Krizi Kalbe giden kan akışı durduğunda kalp krizi meydana gelir. |