ALLOPRE 5 G inf�zyonluk ��zelti haz�rlamak i�in toz (5 flakon) K�sa �r�n Bilgisi
{ Treosulfan }
1. BE�ER� TIBB� �R�N�N ADI
ALLOPRE 5 g inf�zyonluk ��zelti haz�rlamak i�in toz
Steril, Sitotoksik
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Her bir flakon 5 g treosulfan i�erir.
Suland�r�ld�ktan sonra 1 ml ��zelti 50 mg treosulfan i�erir.
Yard�mc� maddeler
Yard�mc� maddeler i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
�nf�zyonluk ��zelti haz�rlamak i�in tozBeyaz, kristalimsi topak veya toz.
Uygun koruyucu g�zl�k, maske ve giysiler kullan�lmal�d�r.
�ift u�lu kan�l�n bir ucu su �i�esinin kau�uk t�pas�na yerle�tirilir. Daha sonra ALLOPRE �i�esi alt� �ste gelecek �ekilde kan�l�n di�er ucuna tak�l�r. T�m d�zenek ters �evrilir ve suyun alttaki �i�eye girmesi sa�lan�r; bu s�rada �i�e yava��a �alkalan�r.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
ALLOPRE, aktif tedavi se�eneklerini t�ketmi� relaps veya metastatik epitelyal over kanser hastalar�nda endikedir.
Eri�kinlerin malign ve nonmalign hastal�klar�nda, 1 aydan b�y�k pediyatrik hastalar�n malign hastal�klar�nda allojenik k�k h�cre nakli �ncesi fludarabin ile kombine olarak haz�rl�k rejiminde kullan�m� endikedir.
4.2. Pozoloji ve uygulama �ekli
Pozoloji:
Over kanseri
Monoterapi olarak kullan�ld���nda treosulfan�n dozaj� 5-8 g/m²'dir.
Daha �nce miyelosupresif ajanlarla tedavi veya radyoterapi ve azalm�� performans durumu gibi risk fakt�rlerinin mevcut oldu�u hastalarda doz 6 g/m²'ye veya daha d���k bir doza indirilmelidir.
Tedavi 3-4 haftada bir tekrarlanmal�d�r.
Sisplatin ile kombinasyonda treosulfan 5 g/m² dozunda uygulanmal� ve tedavi k�rleri 3-4
haftada bir tekrarlanmal�d�r.
Tedavi s�resi
Genellikle treosulfan ile 6 tedavi k�r� verilmektedir.
Progresif hastal�k durumunda ve/veya tolere edilemeyen advers olaylar�n varl���nda tedavi durdurulmal�d�r.
Doz de�i�ikli�i
E�er treosulfan uyguland�ktan sonra beyaz kan h�cre say�s� 1,000/μl'nin alt�na d��erse ve/veya trombosit say�s� 25,000/μl'nin alt�na d��erse sonraki doz 1 g/m² azalt�lmal�d�r.
�� hafta sonra beyaz kan h�cre say�s� 3,500/μl'den az ise veya trombosit say�s� 100,000/μl'den d���kse tedavi verilmemelidir. Bir hafta sonra kan say�m� tekrarlanmal�d�r ve hematolojik parametreler tatminkar ise tedavi yeniden ba�lat�labilir.
E�er bundan sonra de�erlerde hala bir de�i�iklik olmazsa treosulfan dozu monoterapi durumunda 6 g/m²'ye ve sisplatin ile kombinasyonda 3 g/m²'ye d���r�lmelidir.
E�er tedavi s�ras�nda beyaz kan h�cre say�s� 3,500/μl'nin alt�na d��mezse ve/veya trombosit say�s� 100,000/μl'nin alt�na inmezse, sonraki tedavi k�r�nde doz 1 g/m² artt�r�labilir.
Allojenik k�k h�cre nakli �ncesi haz�rl�k rejimi
Treosulfan, haz�rlay�c� tedavi ve takiben allojenik HKHT (hematopoetik k�k h�cre transplantasyonu) konusunda deneyimli bir hekim g�zetiminde uygulanmal�d�r.
Malign hastal��� olan yeti�kinler
Treosulfan, fludarabin ile kombinasyon halinde verilir. Tavsiye edilen uygulama dozu ve plan� ��yledir:
Treosulfan g�nde 10 g/m² v�cut y�zey alan� (VYA) k�k h�cre inf�zyonundan (0.g�n) �nce pe�pe�e �� g�n (-4, -3, -2.g�nler) iki saatlik intraven�z inf�zyon �eklinde verilir. Toplam treosulfan dozu 30 g/m²'dir;
4.3. Kontrendikasyonlar
Etkin madde
�iddetli ve devam eden kemik ili�i depresyonu. Emzirme
Kontrol alt�nda olmayan aktif enfeksiyon hastal���
A��r e� zamanl� kalp, akci�er, karaci�er ve b�brek hastal��� Fanconi anemisi ve di�er DNA k�r��� onar�m bozukluklar� Hamilelik (bkz. B�l�m 4.6)
Canl� a�� uygulanmas�
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Over kanseri
Enfeksiyon riski
Enfeksiyonlar�n (mikotik, viral, bakteriyel) riski artar.
Hematolojik etkiler ve kan say�m� takibi
Treosulfan�n doz s�n�rlay�c� yan etkisi, genellikle geri d�n��l� olan miyelosupresyondur. Miyelosupresyon l�kositlerde ve trombositlerde d���� ve hemoglobinde azalma ile kendini g�sterir. L�kositler ve trombositler genellikle 28 g�n sonra ba�lang�� d�zeylerine geri d�ner.
Kemik ili�i fonksiyonunun inhibisyonu k�m�latif oldu�undan, kan say�m� ���nc� tedavi k�r�nden itibaren daha k�sa aral�klarla takip edilmelidir.
Treosulfan kemik ili�i fonksiyonunu bask�layan di�er tedavi formlar�yla (�rn., radyoterapi) kombine kullan�l�rsa bu �zellikle �nemlidir.
Malignite riski
Oral treosulfan dozlar�yla uzun d�nemli tedavi s�ras�nda sekiz hastada (553 hastan�n %1.4'�) akut non-lenfositik l�semi geli�mi�tir. Risk treosulfan�n k�m�latif dozuna ba�l� olarak
de�i�mi�tir. �lave olarak miyelom, miyeloproliferatif bozukluk ve miyelodisplastik sendromun tekil vakalar� raporlanm��t�r.
Kardiyak toksisite
Bir kardiyomiyopati vakas�n�n treosulfan ile ili�kili oldu�u tamamen d��lanamamaktad�r.
Pulmoner toksisite
E�er alerjik alveolit veya pulmoner fibroz geli�irse treosulfan kal�c� olarak kesilmelidir.
Sistit riski
Muhtemel hemorajik sistit geli�imi nedeniyle hastalara intraven�z inf�zyondan sonra 24 saate kadar daha fazla s�v� t�ketmeleri s�ylenmelidir.
B�brek fonksiyon bozuklu�u
Treosulfan b�brekler yoluyla at�ld���ndan, kan say�mlar� b�brek fonksiyon bozuklu�u olan hastalarda dikkatle izlenmeli ve doz uygun �ekilde ayarlanmal�d�r (bkz. B�l�m 4.2).
Canl� a��lar ile birlikte kullan�m
Sitostatik tedavi canl� a��lar�n kullan�ld��� ba����klamadan sonra yayg�n enfeksiyon riskini artt�rabilir. Bu nedenle, treosulfan alan hastalarda canl� a��lar kullan�lmamal�d�r.
Ekstravazasyon
�nf�zyon s�ras�nda hatas�z bir teknik kullan�lmas�na dikkat edilmelidir ��nk� treosulfan ��zeltisinin civardaki dokuya ekstravazasyonu sonucunda a�r�l� enflamatuvar reaksiyonlar meydana gelebilir.
Gebeli�in �nlenmesi
�ocuk do�urma potansiyeli bulunan kad�nlar tedavi s�resince ve tedaviden sonraki ilk 6 ay boyunca etkili bir do�um-kontrol y�ntemi kullanmal�d�r (bkz. B�l�m 4.6).
Allojenik k�k h�cre nakli �ncesi haz�rl�k rejimi
Miyelosupresyon
Pansitopeni ile birlikte derin miyelosupresyon treosulfana dayal� haz�rl�k rejiminin istenen tedavi etkisidir ve t�m hastalarda g�r�l�r. Bu nedenle, hematopoetik sistem toparlan�ncaya kadar kan h�cre say�lar�n�n s�k aral�klarla izlenmesi �nerilir.
�iddetli n�tropeni fazlar� s�ras�nda (n�tropenik periyodun medyan s�resi yeti�kinlerde 14- 17.5 g�n ve pediyatrik hastalarda 21-24 g�nd�r) enfeksiyon riski artar. Dolay�s�yla profilaktik veya ampirik antienfektif tedavi (bakteriyel, viral, fungal) d���n�lmelidir. B�y�me fakt�rleri (G-CSF, GM-CSF), trombosit ve/veya k�rm�z� kan h�cresi deste�i endike olan �ekilde verilmelidir.
Sekonder maligniteler
Sekonder maligniteler allojenik HKHT'den sonra uzun s�re hayatta kalan hastalarda iyi bilinen komplikasyonlard�r. Treosulfan�n bunlar�n ortaya ��kmas�na ne derece katk�da bulundu�u bilinmemektedir. Olas� bir ikinci bir malignite olu�mas� riski hastaya a��klanmal�d�r. �nsan verileri esas al�narak treosulfan Uluslararas� Kanser Ara�t�rmalar� Ajans� (IARC) taraf�ndan bir insan karsinojeni olarak s�n�fland�r�lm��t�r.
Mukozit
Oral mukozit (y�ksek �iddet derecesi dahil) treosulfana dayal� haz�rl�k ve takiben allojenik HKHT'den sonra �ok yayg�n bir istenmeyen etkidir (bkz. B�l�m 4.8). Mukozit profilaksisinin kullan�m� (�rn., topikal antimikrobiyaller, bariyer koruyucular, buz ve yeterli a��z hijyeni) �nerilir.
A��lar
Canl� zay�flat�lm�� a��lar�n�n e� zamanl� kullan�m� �nerilmez. Fertilite
Treosulfan fertiliteyi olumsuz etkileyebilir. Dolay�s�yla, treosulfan tedavisi alan erkeklere tedavi s�ras�nda ve tedaviden 6 ay sonras�na kadar baba olmamalar� ve treosulfan tedavisine ba�l� geri d�n��s�z infertilite olas�l��� nedeniyle tedaviden �nce spermlerinin dondurularak saklanmas� konusunda hekim tavsiyesi almalar� �nerilir.
Premenopozal hastalarda over supresyonu ve amenore ile birlikte menopoz semptomlar� yayg�n bi�imde g�r�lmektedir (bkz. B�l�m 4.6).
Pediyatrik pop�lasyon
N�betler
Primer imm�n yetmezlikleri olan bebeklerde (≤ 4 ayl�k) fludarabin veya siklofosfamid ile kombine olarak treosulfan ile haz�rl�k tedavisinden sonra n�betlere dair tekil raporlar al�nm��t�r. Bu nedenle, 4 ayl�k veya daha b�y�k bebekler n�rolojik advers reaksiyon belirtileri a��s�ndan izlenmelidir. Bunlar�n nedeninin treosulfan oldu�u kan�tlanamam��sa da, 1 ya��ndan k���k �ocuklarda klonazepam profilaksisi d���n�lebilir.
Solunum, g���s ve mediastin hastal�klar�
Treosulfana dayal� haz�rl�k tedavisi alan pediyatrik hastalarda ya� ile solunum toksisitesi aras�nda anlaml� bir ili�ki saptanm��t�r.
Bir ya��ndan k���k �ocuklarda (esas olarak malign olmayan hastal�klar, �zellikle imm�n yetmezlikleri olanlar) III/IV. derece solunum toksisitesi daha fazla ortaya ��km��t�r; bunun muhtemel nedeni haz�rl�k tedavisine ba�lanmadan �nce mevcut olan akci�er enfeksiyonlar�d�r.
Bebek bezi dermatiti
Treosulfan�n idrarla at�lmas� nedeniyle k���k �ocuklarda bebek bezi dermatiti g�r�lebilir. Bu nedenle her bir treosulfan inf�zyonundan sonra bebek bezleri s�k s�k, 6–8 saatte bir de�i�tirilmelidir.
Ekstravazasyon
Treosulfan tahri� edici madde olarak kabul edilir. �ntraven�z uygulama g�venli bir teknik kullan�larak yap�lmal�d�r. Ekstravazasyondan ��phelenilmesi halinde genel g�venlik tedbirleri uygulanmal�d�r. Hi�bir spesifik �nlemin �nerilebilir nitelikte oldu�u kan�tlanmam��t�r.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Bir hastada ibuprofen/klorokinin etkisi e� zamanl� treosulfan uyguland���nda azalm��t�r.
Y�ksek doz kemoterapide treosulfan�n hi�bir etkile�imi g�zlenmemi�tir.
Detayl� in vitro �al��malar treosulfan�n y�ksek plazma konsantrasyonlar� ile CYP3A4, CYP2C19 veya P-gp substratlar� aras�nda potansiyel etkile�imleri tamamen d��lamam��t�r. Bu nedenle, terap�tik indeksi dar CYP3A4, CYP2C19 veya P-gp substratlar� olan t�bbi �r�nler treosulfan tedavisi s�ras�nda verilmemelidir.
Treosulfan�n fludarabinin farmakokineti�i �zerindeki etkisi bilinmemektedir.
4.6. Gebelik ve laktasyon
Genel tavsiye
Gebelik Kategorisi: X
�ocuk do�urma potansiyeli bulunan kad�nlar/ Do�um kontrol� (Kontrasepsiyon)
�ocuk do�urma potansiyeli olan cinsel aktif kad�nlar ve erkekler tedavi s�resince ve tedavinin ard�ndan 6 aya kadar etkili do�um kontrol� uygulamak zorundad�rlar.
Gebelik d�nemi
Treosulfan�n gebe kad�nlarda kullan�m�na ili�kin hi�bir veri yoktur. Hayvan �al��malar� �reme toksisitesi a��s�ndan yetersizdir (bkz. B�l�m 5.3). Treosulfan gebelik d�neminde uyguland��� takdirde ciddi do�um kusurlar�na yol a�t���ndan ��phelenilmektedir. ALLOPRE gebelik d�neminde kontrendikedir (bkz. B�l�m 4.3). �nsanlarda Treosulfan ile elde edilen deneyime g�re, t�m alkilleyici ajanlar mutajenik potansiyele sahiptir. E�er tedavi s�ras�nda veya sonras�nda gebelik meydana gelirse, genetik dan��manl�k olas�l��� d���n�lmelidir.
Laktasyon d�nemi
Treosulfan�n anne s�t�ne ge�ip ge�medi�i bilinmemektedir. Bu �r�n emziren kad�nlarda kullan�lmamal�d�r.
�reme yetene�i/ Fertilite
Treosulfan kad�nlarda ve erkeklerde fertiliteyi olumsuz etkileyebilir. Geri d�n��s�z infertilite olas�l��� nedeniyle erkekler tedaviden �nce spermlerinin dondurularak saklanmas� konusunda hekim tavsiyesi almal�d�r.
Haz�rl�k rejimlerinde kullan�lan di�er alkilleyici ajanlar i�in de bilindi�i gibi, treosulfan premenopozal kad�nlarda over supresyonu ve amenore ile birlikte menopoz semptomlar�na yol a�abilir.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
Treosulfan ara� ve makine kullanma becerisi �zerinde orta derecede etkiye sahiptir. Treosulfan�n bulant�, kusma veya ba� d�nmesi gibi belirli advers reaksiyonlar�n�n bu i�levleri etkileme olas�l��� vard�r.
4.8. �stenmeyen etkiler
G�venlilik profilinin �zeti
Over kanseri
En s�k bildirilen istenmeyen etkiler miyelosupresyon ve gastrointestinal �ikayetlerdir. Bu olaylar genellikle hafiftir ve treosulfan tedavisinden sonra d�zelir. Kemik ili�i supresyonu treosulfan�n doz s�n�rlay�c� etkisidir.
Allojenik k�k h�cre nakli �ncesi haz�rl�k rejimi
Derin miyelosupresyon/pansitopeni haz�rl�k rejiminin istenen tedavi etkisidir ve t�m hastalarda g�r�l�r. Kan h�cre say�lar� HKHT'den sonra genellikle normale d�ner.
Treosulfana dayal� haz�rl�k rejimini takiben allojenik HKHT sonras�nda en yayg�n bi�imde g�zlenen advers reaksiyonlar (yeti�kinler/pediyatrik hastalar) enfeksiyonlar (%13.1/%11.4), gastrointestinal bozukluklar (bulant� [%39.5/%30.7], stomatit [%36.0/%69.3], kusma [22.5%/43.2%], diyare [%15.6/%33.0], abdominal a�r� [%10.4/%17]), yorgunluk (%15.1/%2.3), febril n�tropeni (%11.3/%1.1), �dem (%7.8/%0), d�k�nt� (%7.2/%12.5) ve alanin transaminaz (ALT [%5.1/%9.1]), aspartat transaminaz (AST [%4.4/%8.0]), gama- glutamil transferaz (γGT [%3.7/%2.3]) ve bilir�bin (%18.8/%5.7) y�kselmelerini i�erir.
Advers etkiler tablosu S�kl�k
�ok yayg�n (≥ 1/10), yayg�n (≥ 1/100 ila <1/10), yayg�n olmayan (≥ 1/1,000 ila <1/100), seyrek (≥ 1/10,000 ila < 1/1,000), �ok seyrek (< 1/10,000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor)
Over kanseri
Her bir s�kl�k gruplamas�nda, istenmeyen etkiler azalan ciddiyet s�ras�na g�re sunulmaktad�r.
Organ S�n�f� | S�kl�k |
Enfeksiyonlar ve enfestasyonlar | Yayg�n: Enfeksiyonlar (mikotik, viral, bakteriyel)
�ok seyrek: Sepsis |
Neoplazmlar, benign, malign ve tan�mlanmam�� (kistler ve polipler dahil) | Yayg�n olmayan: Tedaviye ba�l� sekonder maligniteler (akut non- lenfositik l�semi, miyelodisplastik sendrom, miyelom, miyeloproliferatif bozukluk) |
Kan ve lenf sistemi hastal�klar� | �ok yayg�n: Miyelosupresyon (l�kositopeni, trombositopeni, anemi)
Seyrek: Pansitopeni |
Ba����kl�k sistemi hastal�klar� | Seyrek: Alerjik reaksiyonlar |
Endokrin hastal�klar | �ok seyrek: Addison hastal��� |
Metabolizma ve beslenme bozukluklar� | �ok seyrek: Hipoglisemi |
Sinir sistemi hastal�klar� | �ok seyrek: Parestezi |
Kardiyak hastal�klar | �ok seyrek: Kardiyomiyopati |
Solunum, g���s ve mediastin hastal�klar� | �ok seyrek: Pulmoner fibroz, alveolit, pn�moni |
Gastrointestinal hastal�klar | �ok yayg�n: Kusma, bulant� |
Deri ve deri alt� doku hastal�klar� | �ok yayg�n: Sa� d�k�lmesi (genellikle hafif), bronz deri pigmentasyonu
�ok seyrek: Skleroderma, psoriazisin tetiklenmesi, eritem, �rtiker |
B�brek ve idrar yolu hastal�klar� | �ok seyrek: Hemorajik sistit |
Genel rahats�zl�klar ve uygulama yerindeki durumlar | �ok seyrek: Grip benzeri �ikayetler, lokal a�r�l� enflamatuvar reaksiyonlar (ekstravazasyon durumunda) |
Allojenik k�k h�cre nakli �ncesi haz�rl�k rejimi
Yeti�kinler
Advers reaksiyonlar�n tablola�t�r�lm�� listesi
A�a��daki tabloda sunulan advers reaksiyonlar�n s�kl�klar� treosulfan ile fludarabin kombinasyonunun yeti�kin hastalarda allojenik HKHT'den �nce haz�rl�k tedavisi olarak ara�t�r�ld��� 5 klinik �al��madan (toplam 564 hastay� i�eren) al�nm��t�r. Treosulfan arka arkaya 3 g�n 10-14 g/m² VYA doz aral���nda uygulanm��t�r.
Sistem Organ S�n�f� (SOC) | T�m Advers Reaksiyonlar /S�kl�k | Derece 3-4 Advers Reaksiyonlar / S�kl�k |
Enfeksiyonlar ve enfestasyonlar* | �ok yayg�n Enfeksiyonlar (bakteriyel, viral, fungal) Yayg�n Sepsis Bilinmiyor Septik �ok | Yayg�n Enfeksiyonlar (bakteriyel, viral, fungal), sepsis Bilinmiyor Septik �ok |
Neoplazmlar, benign, malign ve | Bilinmiyor Tedaviyle ili�kili ikinci malignite | Bilinmiyor Tedaviyle ili�kili ikinci |
tan�mlanmam�� (kistler ve polipler dahil)* |
| malignite |
Kan ve lenf sistemi hastal�klar�* | �ok yayg�n Miyelosupresyon, pansitopeni, febril n�tropeni | �ok yayg�n Miyelosupresyon, pansitopeni, febril n�tropeni |
Ba����kl�k sistemi hastal�klar�* | Yayg�n A��r� duyarl�l�k |
|
Metabolizma ve beslenme bozukluklar� | Yayg�n ��tah azalmas� Yayg�n olmayan Hiperglisemi Bilinmiyor Asidoz, glukoz tolerans bozuklu�u, elektrolit dengesizli�i | Yayg�n ��tah azalmas� Yayg�n olmayan Hiperglisemi Bilinmiyor Asidoz, glukoz tolerans bozuklu�u, elektrolit dengesizli�i |
Psikiyatrik bozukluklar | Yayg�n Uykusuzluk Yayg�n olmayan Konf�zyon hali Bilinmiyor Ajitasyon | Seyrek Konf�zyon hali |
Sinir sistemi hastal�klar� | Yayg�n Ba� a�r�s�, ba� d�nmesi Yayg�n olmayan Periferik duysal n�ropati Bilinmiyor Ensefalopati, intrakranyal kanama, ekstrapiramidal bozukluk, senkop, parestezi | Seyrek Ba� a�r�s�, Periferik duysal n�ropati Bilinmiyor Ensefalopati, intrakranyal kanama, senkop |
G�z hastal�klar� | Bilinmiyor G�z kurulu�u |
|
Kardiyak hastal�klar* | Yayg�n Kardiyak aritmiler (�rn., atriyal fibrilasyon, sin�s aritmisi) Bilinmiyor Kardiyak arrest, kalp yetmezli�i, miyokard enfarkt�s�, perikardiyal ef�zyon | Yayg�n olmayan Kardiyak aritmiler (�rn., atriyal fibrilasyon, sin�s aritmisi) Bilinmiyor Kardiyak arrest, miyokard enfarkt�s� |
Vask�ler hastal�klar | Yayg�n Hipertansiyon, y�z ve boyunda k�zar�kl�k, k�zarma Yayg�n olmayan Hematom, hipotansiyon Bilinmiyor Emboli, kanama | Yayg�n olmayan Hipertansiyon Bilinmiyor Emboli, kanama |
Solunum, g���s ve mediastin hastal�klar� | Yayg�n Dispne, burun kanamas� | Yayg�n olmayan Dispne, plevra ef�zyonu, |
| Yayg�n olmayan Pn�monit, plevra ef�zyonu, farenks veya larenks enflamasyonu, �ks�r�k, laringeal a�r�, h��k�r�k Bilinmiyor Orofaringeal a�r�, hipoksi, disfoni | farenks veya larenks enflamasyonu Seyrek Burun kanamas�, pn�monit Bilinmiyor Hipoksi |
Gastrointestinal bozukluklar* | �ok yayg�n Stomatit/mukozit, diyare, bulant�, kusma, abdominal a�r� Yayg�n A��z b�lgesinde a�r�, gastrit, dispepsi, konstipasyon, disfaji Yayg�n olmayan A��zda kanama, abdominal distansiyon, �zofageal veya gastrointestinal a�r�, a��z kurulu�u Bilinmiyor Gastrointestinal kanama, n�tropenik kolit, �zofajit, anal enflamasyon, a��zda �lserle�me | Yayg�n Stomatit/mukozit, diyare, bulant�, abdominal a�r� Yayg�n olmayan Kusma, a��z b�lgesinde a�r�, disfaji, a��zda kanama, �zofageal veya gastrointestinal a�r� Bilinmiyor Gastrointestinal kanama, n�tropenik kolit |
Hepatobiliyer hastal�klar* | Yayg�n olmayan Veno-okl�zif karaci�er hastal���, hepatotoksisite Bilinmiyor Karaci�er yetmezli�i, hepatomegali, hepatik a�r� | Seyrek Veno-okl�zif karaci�er hastal���, hepatotoksisite Bilinmiyor Karaci�er yetmezli�i |
Deri ve deri alt� doku hastal�klar� | Yayg�n Makulo-pap�ler d�k�nt�, purpura, eritem, palmar-plantar eritrodisestezi sendromu, ka��nt�, sa� d�k�lmesi Yayg�n olmayan Eritema multiforme, akneiform dermatitis, d�k�nt�, a��r� terleme Bilinmiyor Yayg�n eritem, dermatit, deri nekrozu veya �lseri, deride hiperpigmentasyon, cilt kurulu�u | Yayg�n olmayan Makulo-pap�ler d�k�nt�, purpura, eritem Bilinmiyor Deri nekrozu |
Kas-iskelet sistemi ve ba� dokusu hastal�klar� | Yayg�n Ekstremitelerde a�r�, s�rt a�r�s�, kemik a�r�s�, eklem a�r�s�, kas a�r�s� Bilinmiyor Kas g��s�zl��� | Seyrek Ekstremitelerde a�r�, kemik a�r�s� |
B�brek ve �riner sistem hastal�klar� | Yayg�n Akut b�brek hasar�, hemat�ri Bilinmiyor B�brek yetmezli�i, sistit, diz�ri | Yayg�n olmayan Akut b�brek hasar�, hemat�ri |
Genel rahats�zl�klar ve uygulama yerindeki | �ok yayg�n Astenik durumlar (yorgunluk, asteni, | Yayg�n Yorgunluk |
durumlar | letarji) Yayg�n �dem, pireksi, ���me Yayg�n olmayan Kalple ili�kili olmayan g���s a�r�s�, a�r� Bilinmiyor Enjeksiyon b�lgesinde reaksiyon, ���me hissi | Seyrek Kalple ili�kili olmayan g���s a�r�s�, �dem, pireksi |
Ara�t�rmalar | �ok yayg�n | Yayg�n |
| Bilir�bin art��� | Bilir�bin art���, |
| Yayg�n | transaminazlarda (ALT/AST) |
| Transaminazlarda (ALT/AST) | y�kselme, γGT art��� |
| y�kselme, γGT art���, kanda alkalin | Yayg�n olmayan |
| fosfataz art���, C-reaktif protein | Kanda alkalin fosfataz art���, |
| art���, kilo kayb�, kilo art��� | C-reaktif protein art��� |
| Bilinmiyor | Bilinmiyor |
| Kanda kreatinin d�zeyinde art��, | Kanda LDH art��� |
| kanda laktat dehidrojenaz (LDH) |
|
| d�zeyinde art�� |
|
* A�a��daki detayl� b�l�mlere bak�n�z
Se�ili advers reaksiyonlar�n tarifi Enfeksiyonlar
Enfeksiyonlar�n toplam insidans� %13.1'di (74/564). En s�k g�r�len enfeksiyon t�r� akci�er enfeksiyonuydu (12/74 [%16.2]). Patojenler bakterileri (�rn., Staphylococcus, Enterococcus, Corynebacterium), vir�sleri (�rn., sitomegalovir�s [CMV], Epstein-Barr vir�s� [EBV], herpes) ve mantarlar� (�rn., Candida) i�ermi�tir. Enfeksiyon oran� -4. g�nden -2.g�ne kadar g�nde 10 g/m² treosulfan doz rejimiyle tedavi edilen hastalarda en d���kt� (%7.7).
Benign, malign ve tan�mlanmam�� neoplazmlar (kistler ve polipler dahil)
564 yeti�kin hastadan 1'inde (%0.2) ikinci bir malignite (meme kanseri) geli�mi�tir. Treosulfana dayal� haz�rl�k rejiminden sonra az say�da ikinci malignite vakas� ba�ka ara�t�rmac�lar taraf�ndan raporlanm��t�r. Solid t�m�rleri olan hastalarda oral treosulfan�n klasik dozlar�yla uzun s�reli tedaviden sonra 553 hastan�n %1.4'�nde akut miyeloid l�semi g�zlenmi�tir.
Kan ve lenf sistemi hastal�klar�
Kan hastal�klar� 564 yeti�kin hastadan 67'sinde (%11.9) g�zlenmi�tir. En s�k g�r�len advers reaksiyon febril n�tropeniydi (%11.3). En d���k insidans -4.g�nden -2.g�ne kadar uygulanan g�nde 10 g/m² doz rejimiyle kaydedilmi�tir (%4.1).
Medyan (%25/%75 persentiller) n�tropeni s�resi 10 g/m² treosulfan dozuyla 14 (12, 20) g�n
ve 14 g/m² treosulfan dozuyla 17.5 (14, 21) g�nd�.
Kardiyak hastal�klar
25 hastada (%4.4) kardiyak hastal�klar g�zlenmi�tir. En s�k raporlanan advers reaksiyonlar atriyal fibrilasyon (%1.2), sin�s ta�ikardisi (%0.9), supraventrik�ler ta�ikardi (%0.4) ve ventrik�ler ekstrasistol� (%0.4) i�eren kardiyak aritmilerdi. Kardiyak arrest, kalp yetmezli�i ve miyokard enfarkt�s�n�n tekli vakalar� bildirilmi�tir. Kardiyak hastal�klar�n en d���k s�kl���
-4.g�nden -2.g�ne kadar uygulanan g�nde 10 g/m² doz rejimiyle g�zlenmi�tir (%2.7).
Gastrointestinal bozukluklar
Gastrointestinal hastal�klar 357 hastada (%63.3) g�zlenmi�tir. En s�k bildirilen advers reaksiyonlar bulant� (%39.5), stomatit (%36), kusma (%22.5), diyare (%15.6) ve abdominal a�r�yd� (%10.4). Bu advers reaksiyonlar�n en d���k s�kl�klar� -4.g�nden -2.g�ne kadar uygulanan g�nde 10 g/m² doz rejimiyle g�r�lm��t�r (s�ras�yla %20.4, %30.3, %13.1, %5.0 ve
%5.5).
Hepatobiliyer hastal�klar
Veno-okl�zif karaci�er hastal���n�n (VOH) toplam insidans� %0.9'du (5/564). VOH yaln�zca g�nde 14 g/m² doz rejimiyle meydana gelmi�tir. Bu vakalar�n hi�biri �l�mle sonu�lanmam�� veya hayati tehlikeye yol a�mam��t�r.
Pediyatrik pop�lasyon
Advers reaksiyonlar�n tablola�t�r�lm�� listesi
A�a��daki tabloda sunulan advers reaksiyonlar malign veya non-malign hastal�klar� olan pediyatrik hastalara treosulfan�n fludarabin ile birlikte (ve �o�unlukla ilave olarak tiyotepa ile) allojenik HKHT'den �nce haz�rl�k tedavisi olarak uyguland��� toplam 88 hastay� i�eren iki klinik �al��madan elde edilmi�tir (medyan ya� 8 [aral�k 0–17 ya�]). Treosulfan arka arkaya �� g�n 10-14 g/m² VYA doz aral���nda uygulanm��t�r.
Sistem Organ S�n�f� (SOC) | T�m Advers Reaksiyonlar /S�kl�k | Derece 3-4 Advers Reaksiyonlar / S�kl�k |
Enfeksiyonlar ve enfestasyonlar* | �ok yayg�n Enfeksiyonlar (bakteriyel, viral, fungal) | Yayg�n Enfeksiyonlar (bakteriyel, viral, fungal) |
Neoplazmlar, benign, malign ve tan�mlanmam�� (kistler ve polipler dahil)* | Bilinmiyor Tedaviyle ili�kili ikinci malignite | Bilinmiyor Tedaviyle ili�kili ikinci malignite |
Kan ve lenf sistemi hastal�klar�* | �ok yayg�n Miyelosupresyon, pansitopeni Bilinmiyor Febril n�tropeni | �ok yayg�n Miyelosupresyon, pansitopeni Bilinmiyor |
|
| Febril n�tropeni |
Metabolizma ve beslenme bozukluklar� | Bilinmiyor Alkaloz, elektrolit dengesizli�i, hipomagnezemi | Bilinmiyor Alkaloz |
Sinir sistemi hastal�klar�* | Bilinmiyor Ba� a�r�s�, parestezi, n�bet | Bilinmiyor Parestezi |
G�z hastal�klar� | Bilinmiyor Konjunktiva kanamas�, g�z kurulu�u |
|
Vask�ler hastal�klar | Bilinmiyor Kapiler s�z�nt� sendromu, hipertansiyon, hipotansiyon | Bilinmiyor Kapiler s�z�nt� sendromu, hipertansiyon, hipotansiyon |
Solunum, g���s ve mediastin hastal�klar� | Yayg�n Orofaringeal a�r�, burun kanamas� Bilinmiyor Hipoksi | Bilinmiyor Hipoksi |
Gastrointestinal hastal�klar* | �ok yayg�n Stomatit/mukozit, diyare, bulant�, kusma, abdominal a�r� Yayg�n Disfaji, a��z b�lgesinde a�r� Bilinmiyor N�tropenik kolit, anal enflamasyon, dispepsi, proktit, gastrointestinal a�r�, konstipasyon | �ok yayg�n Stomatit/mukozit, bulant� Yayg�n Disfaji, diyare, kusma, abdominal a�r� Bilinmiyor N�tropenik kolit |
Hepatobiliyer hastal�klar | Bilinmiyor Veno-okl�zif karaci�er hastal���, hepatomegali, hepatotoksisite | Bilinmiyor Veno-okl�zif karaci�er hastal��� |
Deri ve deri alt� doku hastal�klar� | �ok yayg�n Ka��nt� Yayg�n Eksfoliyatif dermatit, makulo- papuler d�k�nt�, d�k�nt�, eritem, cilt a�r�s�, deride hiperpigmentasyon, sa� d�k�lmesi Bilinmiyor Deri �lseri, eritema multiforme, �rtiker, b�ll�z dermatit, akneiform dermatit, palmar-plantar eritrodisestezi sendromu, bebek bezi dermatiti | Yayg�n Eksfoliyatif dermatit, makulo-papuler d�k�nt�, eritem |
Kas-iskelet sistemi ve ba� dokusu hastal�klar� | Bilinmiyor Ekstremitelerde a�r� |
|
B�brek ve �riner sistem hastal�klar� | Bilinmiyor Akut b�brek hasar�, b�brek yetmezli�i, nonenfektif sistit | Bilinmiyor Akut b�brek hasar�, b�brek yetmezli�i |
�reme sistemi ve meme hastal�klar� | Bilinmiyor Skrotal eritem |
|
Genel rahats�zl�klar ve uygulama yerindeki durumlar | �ok yayg�n Pireksi Bilinmiyor ���me, yorgunluk, a�r� |
|
Tetkikler | Yayg�n Transaminazlarda (ALT/AST) y�kselme, bilir�bin art��� Bilinmiyor γGT art��� | Yayg�n Bilir�bin art��� Yayg�n olmayan Transaminazlarda (ALT/AST) y�kselme Bilinmiyor γGT art��� |
* A�a��daki detayl� b�l�mlere bak�n�z
Se�ili advers reaksiyonlar�n tarifi Enfeksiyonlar
88 pediyatrik hastada enfeksiyonlar�n toplam insidans� %11.4'd� (10/88) ve yeti�kin hastalardaki insidans ile benzerdi. Enfeksiyon s�kl��� 12–17 ya� aras� pediyatrik ya� grubunda (6/35 [%17.1]) daha k���k �ocuklara k�yasla daha y�ksekti (4/53 [%7.5]).
Benign, malign ve tan�mlanmam�� neoplazmlar (kistler ve polipler dahil)
Treosulfana dayal� haz�rl�k tedavisinden sonra ikinci bir maligniteye ili�kin be� vaka (miyelodisplastik sendrom, akut lenfoblastik l�semi, Ewing sarkomu) ba�ka ara�t�rmac�lar taraf�ndan raporlanm��t�r. Be� pediyatrik hastan�n t�m� primer imm�n yetmezlikler yani neoplazi riski zaten artm�� olan hastal�klar i�in allojenik HKHT alm��t�r.
Kan ve lenf sistemi hastal�klar�
Medyan (%25/%75 persentiller) n�tropeni s�resi malign hastal�klar� olan pediyatrik
hastalarda 21 (16, 26) g�n ve non-malign hastal�klar� olan hastalarda 24 (17, 26) g�nd�.
Sinir sistemi hastal�klar�
88 pediyatrik hastadan 1'inde ensefalit enfeksiyonu kapsam�nda n�bet bildirilmi�tir. Primer imm�n yetmezlikleri olan �ocuklarda y�r�t�len, ara�t�rmac� taraf�ndan ba�lat�lan bir �al��madan al�nan bir rapor treosulfana dayal� di�er haz�rl�k rejimlerinden sonra meydana gelen 4 n�bet vakas�n� listelemektedir (bkz. B�l�m 4.4).
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirilmesi gerekmektedir (www.titck.gov.tr; e-posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz a��m� ve tedavisi
Treosulfan�n esas toksik etkisi derin miyeloablasyon ve pansitopenidir. Ek olarak asidoz, deri toksisitesi, bulant�, kusma ve gastrit ortaya ��kabilir. Hematopoetik k�k h�cre transplantasyonu yoklu�unda, �nerilen treosulfan dozu doz a��m� te�kil edecektir. Treosulfan doz a��m�n�n spesifik hi�bir antidotu bilinmemektedir. Hematolojik durum yak�ndan izlenmeli ve yo�un destekleyici �nlemler t�bben endike olan �ekilde al�nmal�d�r.
Uzun s�reli veya a��r� terap�tik dozlar, nadiren geri d�n��� olmayan kemik ili�i depresyonu ile sonu�lanabilir. T�bbi �r�n geri �ekilmeli ve kan transf�zyonu ile birlikte genel destekleyici �nlemler uygulanmal�d�r.
T�bbi �r�n�n kazayla g�zlerle temas etmesini �nlemek i�in tedbirler al�nmal�d�r. ��zeltinin ciltle veya g�zlerle temas etmesi halinde, etkilenen b�lge bol miktarda su veya normal serum fizyolojik ile y�kanmal�d�r. Ciltteki ge�ici batma hissini yat��t�rmak i�in tahri� etmeyen bir krem kullan�labilir. G�zler etkilenirse bir hekime ba�vurulmal�d�r.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Antineoplastik ajanlar, alkilleyici ajanlar, alkil s�lfonatlar
ATC kodu: L01 AB02
Etki mekanizmas�
Treosulfan hematopoetik �nc�l h�crelerde sitotoksik aktiviteye sahip �ift fonksiyonlu bir alkilleyici ajan�n bir �n ilac�d�r. Treosulfan�n aktivitesi bir monoepoksit ara maddesine ve L- diepoksib�tana spontan d�n���me ba�l�d�r (bkz. B�l�m 5.2).
Olu�an epoksitler deoksiribon�kleik asidin (DNA) n�kleofilik merkezlerini alkiller ve k�k h�crelerin t�ketiminden ve antineoplastik etkilerden sorumlu oldu�u d���n�len DNA �apraz ba�lar�n� ind�kler.
�lk �nce olu�an monoepoksidin in vivo ko�ullarda DNA'n�n n�kleofilik bir merkezini alkilleyebildi�i �nemlidir. Bu alkilasyon ikinci epoksit halkas� olu�madan �nce bile�i�i kimyasal reaksiyonla bu merkeze sabitler.
Farmakodinamik etkiler
Treosulfan geni� kapsaml� antineoplastik ve antil�semik aktiviteye sahiptir. Antineoplastik aktivite transplantasyon yap�lm�� fare ve s��anlarda lenfomalar/l�semiler, sarkomalar ve hepatomlar, insan t�m�r zenograftlar�, insan t�m�r biyopsileri ve h�cre dizilerine kar�� g�sterilmi�tir. Treosulfan intraperitoneal, intraven�z ve ayr�ca oral yolla uyguland���nda in vivo etkilidir.
Treos�lfan�n imm�nosupresif etkileri, ilkel ve kararl� progenit�r h�crelere, T ve NK h�crelerine kar�� toksisitesine, primer ve sekonder lenfatik organlar�n h�creselli�inin azalmas�na ve Graft-versus-Host-Hastal���'n�n (GvHD) geli�iminden �nce gelen ve ilgili olan 'sitokin f�rt�nas�' �zerindeki �nleyici etkisine ba�lan�r ve venooklusif hastal���n patogenezinde yer al�r.
Klinik etkinlik ve g�venlilik
Over Kanseri
Sisplatin ile kombinasyonda treosulfan�n klinik etkinli�i b�y�k bir randomize klinik �al��mada over kanserli hastalarda g�sterilmi�tir. Toplam 519 hasta sisplatin (70 mg/m²) ile birlikte treosulfan (5 g/m²; PT rejimi) veya siklofosfamid (1 g/m²; PC rejimi) almak �zere randomize edilmi�tir.
Her iki rejim 4 haftal�k aral�klarla verilmi�tir. Medyan 5 y�l takipten sonra, 366 hasta (PC: 179; PT: 187) etkinlik ve 290 hasta (PC: 135; PT: 155) g�venlilik y�n�nden de�erlendirilebilmi�tir.
Progresyona kadar ge�en medyan s�re (primer sonlan�m noktas�) sisplatin/treosulfan kombinasyonuyla daha uzun olmu�tur (20.6 aya kar�� 15.1 ay); ancak bu fark istatistiksel olarak anlaml� de�ildi (P = 0.3).
Her iki tedavi rejimi aras�nda yan�t oranlar� bak�m�ndan farklar saptanmam��t�r.
Genel sa�kal�m tedavi kollar� aras�nda farkl� bulunmam��t�r (29.4 aya kar�� 33.5 ay; P = 0.8). PC kolunda anlaml� olarak daha fazla sa� d�k�lmesi g�zlenirken (P = 0.0001), PT kolunda daha fazla l�kositopeni g�zlenmi�tir (P = 0.01). Treosulfan i�eren rejimle tedavi edilen hastalarda ya�am kalitesi daha iyiydi.
Treosulfan monoterapisinin (5 - 7 g/m²; 4 haftada bir) intraven�z uygulanmas�n�n etkinli�i ilerlemi� over kanseri olan, daha �nce tedavi alm�� 88 hastada (etkinlik y�n�nden 80'i de�erlendirilebilmi�tir) y�r�t�len bir faz II �al��mada g�sterilmi�tir. �ki tam yan�t ve 13 k�smi yan�t saptanm�� ve objektif yan�t oran� %19 bulunmu�tur. Yan�t veren hastalarda medyan sa�kal�m s�resi 41 ayd�. Hastalar�n %34'�nde hastal�k stabildi ve medyan sa�kal�m s�resi 18 ayd�.
Primer tedaviden sonraki 12 ayda progresif hastal�k sergileyen 48 kad�nda %19'luk yan�t oran� ve %31'inde stabil hastal��a ula��labilmi�tir. Toksik yan etkiler seyrek g�r�lm�� ve orta �iddette olmu�tur. Ya�am� tehdit eden miyelosupresyon, tedaviye diren�li emezis ve sa� d�k�lmesi g�zlenmemi�tir.
Allojenik k�k h�cre nakli �ncesi haz�rl�k rejimi
Referans niteli�indeki faz III �al��mada, akut miyeloid l�semi (AML) veya miyelodisplastik sendromu (MDS) olan ve daha ileri ya� (≥ 50 ya�) veya komorbiditeler (hematopoetik h�cre transplantasyonu komorbidite indeksi [HCT-CI] skoru >2) nedeniyle standart haz�rl�k tedavileri i�in artm�� risk ta��yan yeti�kin hastalar 3 × 10 g/m² treosulfan ile birlikte fludarabin (FT; n = 220) i�eren bir haz�rl�k rejimi veya intraven�z busulfan (toplam dozSaklamaya y�nelik �zel tedbirler tedbirler mg/kg) ile birlikte fludarabin (FB2; n = 240) rejimini takiben allojenik HKHT almak �zere randomize edilmi�tir. Hastalar�n %64'�nde AML ve %36's�nda MDS mevcuttu. Hastalar�n medyan ya�� 60'd� (aral�k 31–70 ya�); hastalar�n %25'i 65 ya� �zeriydi.
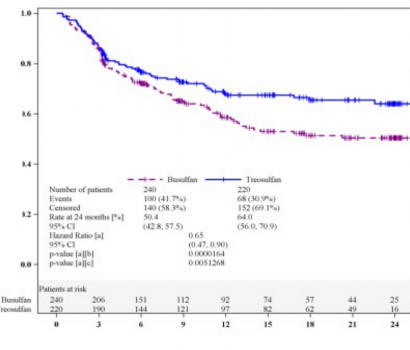
Bu �al��man�n birincil sonlan�m noktas� 2 y�l sonra olays�z sa�kal�md� (EFS). Olaylar hastal�k relaps�, greft yetmezli�i veya �l�m (hangisi �nce ger�ekle�irse) olarak tan�mlanm��t�r. FTrejiminin referans FB2'den daha geride olmad��� (non-inferiorite) istatistiksel olarak kan�tlanm��t�r (�ekil 1).
Risk alt�ndaki hastalar
Zaman (aylar)
Olays�z sa�kal�m oran�
�ekil 1: Olays�z sa�kal�ma ili�kin Kaplan-Meier tahminleri (Tam Analiz Seti)
�nceden tan�mlanm�� �e�itli alt gruplarda (don�r tipi, risk grubu, hastal�k, ya� grubu, HCT-CI skoru, �al��maya giri�te remisyon durumu ve bu parametrelerin �e�itli kombinasyonlar�)
2.y�lda yap�lan EFS analizleri sadece bir istisnayla (MDS hastalar�n�n olu�urdu�u risk grubu I; HR 1.14 [%95 GA 0.48, 2.63]) her zaman treosulfan rejiminin lehine bulunmu�tur (FB2'ye g�re FTtehlike oran� [HR] <1),.
Detayl� sonu�lar Tablo 1'de sunulmaktad�r.
Tablo 1: 24.aydaki tedavi sonu�lar� (Tam analiz seti)
Parametre | Treosulfan | Busulfan | Tehlike oran� (%95 GA) | P de�eri |
Hasta say�s� | 220 | 240 |
|
|
Genel sa�kal�m; % (%95 GA) | 71.3 (63.6, 77.6) | 5Saklamaya y�nelik �zel tedbirler tedbirler (48.4, 63.6) | 0.61 (0.42, 0.88) | 0.0082 |
K�m�latif relaps/progressyon insidans�; % (%95 GA) | 24.6 (17.8, 31.3) | 23.3 (17.6, 29.0) | 0.87 (0.59, 1.30) | 0.5017 |
Nakille ili�kili mortalitenin k�m�latif insidans�; % (%95 GA) |
12.1 (8.1, 17.7) |
28.2 (21.4, 36.5) |
0.54 (0.32, 0.91) |
0.0201 |
GvHD sonu�lar� Tablo 2'de g�sterilmektedir.
Tablo 2: K�m�latif GvHD insidans� (Tam analiz seti)
Parametre | Treosulfan | Busulfan | P de�eri |
Hasta say�s� | 220 | 240 |
|
Akut GvHD, t�m Dereceler; % (%95 GA) | 52.1 (45.5, 58.7) | 58.8 (52.5, 65.0) | 0.1276 |
Akut GvHD, Derece III/IV; % (%95 GA) | 6.4. Saklamaya y�nelik �zel tedbirler(3.2, 9.6) | 9.6 (5.9, 13.3) | 0.2099 |
Kronik GvHD; % (%95 GA) | 60.1 (49.8, 70.3) | 60.7 (53.1, 68.4) | 0.5236 |
Yayg�n kronik GvHD; % (%95 GA) | 18.4 (12.0, 24.8) | 26.1 (19.2, 33.1) | 0.1099 |
Non-malign hastal�klar� (NMH) olan yeti�kin hastalarda treosulfana dayal� haz�rl�k rejimine (FTrejimi ± tiyotepa; bkz. B�l�m 4.2) ili�kin s�n�rl� bilgi mevcuttur. NMH'li yeti�kin hastalarda treosulfan haz�rl�k rejimiyle allojenik HKHT i�in ana endikasyonlar hemoglobinopatilerdir (�rn., orak h�cre hastal���, talasemi major [TM]), primer imm�n yetmezlik, hemofagositik bozukluk, imm�n reg�lasyon bozuklu�u ve kemik ili�i yetmezli�i).
Bir �al��mada NMH'li 31 hasta FTrejimi ve anti-timosit globulin ile tedavi edilmi�tir. Hastalar�n ya�� 0.4 ile 30.5 aras�nda de�i�iyordu ve %29'unun HCT-CI skorlar� > 2'ydi. T�m hastalara greftleme yap�lm��t� ve n�trofil greftlemesine kadar ge�en medyan s�re 21 g�nd� (aral�k, 12–46). �ng�r�len iki y�ll�k genel sa�kal�m oran� %90'd�. Klinik semptomlar ve laboratuvar tetkikleriyle �l��len tam hastal�k yan�tlar� 28 hastada (%90) g�zlenmi�tir (Burroughs LM et al., Biology of Blood and Marrow Transplantation 2014; 20(12):1996- 2003).
�talya'daki bir grup ara�t�rmac� 60 TM hastas�n� (ya� aral��� 1-37; 12 yeti�kin dahil) FTve
tiyotepa rejimiyle tedavi etmi�tir. Bir hasta hari� t�m hastalara greftleme yap�lm�� ve bu hasta
+11.g�n �lm��t�r; n�trofil ve trombositlerin toparlanmas�na kadar ge�en medyan s�re 20 g�nd�. Medyan 36 ayl�k takip s�resiyle (aral�k, 4-73), 5 y�ll�k genel sa�kal�m olas�l��� %93 (%95 GA %83-97) bulunmu�tur. �ocuklar ve yeti�kinler aras�nda sonu� bak�m�ndan hi�bir fark g�zlenmemi�tir (Bernardo ME et al.; Blood 2012; 120(2):473-6).
Yeti�kin hastalarda treosulfana dayal� haz�rl�k rejimini (n = 16) busulfana dayal� haz�rl�k rejimiyle (n = 81) kar��la�t�ran geriye d�n�k bir �al��ma olduk�a benzer sa�kal�m oranlar�n� ortaya koymu�tur (%70.3 ± 15.1'e kar�� %69.3 ± 5.5); bununla birlikte akut GvHD riski treosulfan grubunda daha d���kt� (olas�l�k oran� 0.28; %95 GA 0.12-0.67; P = 0.004) (Caocci G et al.; American Journal of Hematology 2017; 92(12):1303-1310).
Pediyatrik pop�lasyon
Treosulfana dayal� haz�rl�k rejiminin etkinli�i ve g�venlili�i tiyotepa ile birlikte (n = 65) veya tiyotepa olmaks�z�n (n = 5) treosulfan ve fludarabin i�eren bir haz�rl�k rejimi alan akut lenfoblastik l�semi (ALL), AML, MDS veya juvenil miyelomonositik l�semisi (JMML) olan
70 hastada de�erlendirilmi�tir (bkz. B�l�m 4.2). Toplam 37 hasta (%52.9) 12 ya��ndan
k���kt�.
Hi�bir hasta primer greft yetmezli�i ya�amam�� ancak ALL'li bir hastada sekonder greft yetmezli�i geli�mi�tir. Tam don�r tipi kimerizm insidans� +28.g�ndeki vizitte %94.2 (%90
GA %87.2-98.0), +100.g�ndeki vizitte %91.3 (%90 GA %83.6-96.1) ve 12.aydaki vizitte
%91.2 (%90 GA %82.4-96.5) olarak saptanm��t�r.
12.ayda genel sa�kal�m %91.4'd�r (%90 GA %83.9-95.5). 70 hastadan toplam 7'si (%10.0) �lm��t�r; �l�m nedeni iki hastada relaps/progresyon, �� hastada transplantasyonla ili�kili bir neden ve geri kalan iki hastada ba�ka nedenlerdi. HKHT'den sonra +100.g�ne kadar nakille ili�kili mortalite yoklu�u (birincil sonlan�m noktas�) oran� %98.6'd�r (%90 GA %93.4–99.7) ��nk� 70 hastadan biri HKHT'den sonra +100.g�ne kadar nakil/tedaviyle ili�kili bir nedenle �lm��t�r. 12.ayda nakille ili�kili mortalite oran� %2.9'dur (%90 GA %0.9 –8.9). 11 hasta relaps/progresyon ya�am��t�r. K�m�latif relaps/progresyon insidans� +12.ayda %15.7'dir (%90 GA %8.6-22.9).
5.2. Farmakokinetik �zellikler
Genel �zelliklerTreosulfan fizyolojik ko�ullarda (pH 7.4; 37 °C) bir monoepoksit ara maddesine ve L- diepoksib�tana kendili�inden d�n��en ve yar� �mr� 2.2 saat olan bir �n ila�t�r.
Emilim:
Treosulfan�n oral emilimi m�kemmeldir ve biyoyararlan�m� %100'e yak�nd�r.
�ntraven�z uygulamadan sonra, pik plazma d�zeylerine inf�zyon s�resinin sonunda ula��l�r. Yeti�kin hastalarda 10, 12 veya 14 g/m² treosulfan 2 saatlik inf�zyonla verildikten sonra maksimum plazma d�zeyleri (ortalama ± SD) s�ras�yla 306 ± 94 µg/mL, 461 ± 102 µg/mL ve 494 ± 126 µg/mL'ydi.
Da��l�m:
�ntraven�z uygulamadan sonra treosulfan v�cutta h�zla da��l�r; ancak treosulfan�n kan-beyin bariyerinden ge�i�i olduk�a s�n�rl�d�r (bkz. B�l�m 5.3). Yeti�kin hastalarda da��l�m hacmi yakla��k 20–30 litredir. Arka arkaya �� g�n boyunca �nerilen g�nl�k tedaviyle doz birikimi g�zlenmemi�tir. Treosulfan plazma proteinlerine ba�lanmaz.
Biyotransformasyon:
Fizyolojik ko�ullarda (pH 7.4, s�cakl�k 37 °C), treosulfan�n farmakolojik y�nden inaktif treosulfan aktif monoepoksit ara maddesine (S,S-EBDM = (2S,3S)-1,2-epoksib�tan-3,4-diol- 4-metan s�lfonat) ve son olarak da L-diepoksib�tana (S,S-DEB = (2S,3S)-1,2:3,4- diepoksib�tan) spontan olarak (enzimatik olmayan bi�imde) d�n���r.
100 µM'ye kadar konsantrasyonlarda, treosulfan CYP1A2, 2C9, 2C19, 2D6 veya 3A4'�n aktiviteleri �zerinde in vitro hi�bir kesin etkiye sahip de�ildir. Dolay�s�yla treosulfan�n in vivo ko�ullarda CYP450 arac�l� potansiyel etkile�imlere kat�lmas� veya katk�da bulunmas� olas�l��� yoktur.
Eliminasyon:
Over kanseri
�ntraven�z yolla uygulanan treosulfan�n (8 g/m²) ortalama (± SD) terminal yar�-�mr� (t1/2ß)
1.94 ± 0.99 saattir ve de�i�memi� treosulfan�n k�m�latif renal eliminasyonu yakla��k %25'dir (aral�k, %5-%49).
Allojenik k�k h�cre nakli �ncesi haz�rl�k rejimi
Treosulfan�n plazma konsantrasyonlar� �ssel bi�imde katlanarak azal�r ve iki kompartmanl� modele uyan, birinci dereceden eliminasyon s�reciyle en iyi �ekilde tarif edilir.
�ntraven�z yolla uygulanan treosulfan�n (47 g/m²'ye kadar) terminal yar� �mr� (T) yakla��k 2 saattir. Treosulfan dozunun yakla��k %25–40'� 24 saat i�inde idrarla de�i�meden at�l�r ve yakla��k %90'� uygulamadan sonraki ilk 6 saatte at�l�r.
Do�rusall�k/do�rusal olmayan durum
Treosulfan dozuna kar�� i�aretlenen grafikte e�ri alt�nda kalan alan�n (EAA) regresyon analizi do�rusal bir korelasyonu g�stermi�tir.
B�brek ve karaci�er fonksiyon bozuklu�u
A��r b�brek veya karaci�er yetmezli�i olan hastalarda treosulfan ile hi�bir farmakokinetik �al��mas� yap�lmam��t�r ��nk� bu t�r hastalara genellikle allojenik HKHT uygulanmaz. Treosulfan�n yakla��k %25–40'� idrarla at�l�r; bununla birlikte treosulfan�n b�brek klirensi �zerinde b�brek fonksiyonunun bir etkisi g�zlenmemi�tir.
Pediyatrik pop�lasyon
Basit�e VYA'ya dayanan klasik doz hesaplamalar� ergenler veya yeti�kinlere k�yasla d���k VYA'l� bebekler ve k���k ya�taki �ocuklarda anlaml� olarak daha y�ksek maruz kal�ma (EAA) yol a�ar. Bu nedenle, pediyatrik hastalarda treosulfan dozaj�n�n VYA'ya g�re ayarlanmas� gerekir (bkz. B�l�m 4.2).
Treosulfan�n ortalama belirgin terminal yar� �mr� farkl� ya� gruplar� aras�nda benzer bulunmu� ve 1.3 - 1.6 saat aras�nda de�i�mi�tir.
5.3. Klinik �ncesi g�venlilik verileri
Alkilleyici etki mekanizmas� nedeniyle treosulfan, kanserojen potansiyele sahip genotoksik bir bile�ik olarak karakterize edilir. Hayvanlarda treosulfan �zerinde spesifik �reme ve geli�imsel toksisite �al��malar� yap�lmam��t�r. Bununla birlikte, s��anlarda yap�lan kronik toksisite testleri s�ras�nda spermatogenez ve yumurtal�k fonksiyonu �nemli �l��de etkilenmi�tir. Yay�nlanm�� literat�r verileri, puberte �ncesi ve puberte erkek ve di�i farelerde treosulfan�n gonadotoksisitesini raporlar.
Fare ve s��anlar�n L-diepoksib�tan (treosulfan�n alkilleyici transformasyon �r�n�) ile tedavisine ili�kin yay�nlanm�� veriler, do�urganl�k, rahim-yumurtal�k ve sperm geli�iminde bozulma oldu�unu ortaya ��karm��t�r.
J�venil hayvan �al��malar�
J�venil s��an toksisite �al��malar�nda treosulfan, fiziksel geli�mede hafif bir gecikmeye ve di�ilerde biraz gecikmeli bir vajinal a��lma zaman noktas�na neden olmu�tur. S��anlarda treosulfan taraf�ndan �ok d���k bir kan-beyin bariyeri penetrasyonu g�zlenmi�tir. Beyin dokusundaki treosulfan konsantrasyonlar� plazmadakinden %95-98 daha d���k olmu�tur. Bununla birlikte, gen� s��anlar�n beyin dokusunda gen� yeti�kinlere k�yasla yakla��k 3 kat daha y�ksek maruziyet bulunmu�tur.
Akut toksisite
Farelerde oral LDv�cut a��rl���n�n kg'� ba��na 3360 mg treosulfand�r ve intraven�z LD
v�cut a��rl���n�n kg'� ba��na >2500 mg treosulfand�r.
S��anlarda oral LDv�cut a��rl���n�n kg'� ba��na 2575 mg treosulfan ve intraperitoneal LDv�cut a��rl���n�n kg'� ba��na > 2860 mg treosulfand�r.
Subakut toksisite
Subakut bir doz (56-111 mg/kg/g�n) alan maymunlarda hematopoetik sistem hasar g�rm��t�r. Daha y�ksek dozlarda (222-445 mg/kg/g�n) diyare, anoreksi ve belirgin v�cut a��rl��� kayb� da kaydedilmi�tir.
Kronik toksisite
Treosulfan�n s��anlara yedi ay boyunca uygulanmas� erkek s��anlarda spermiyogenezde azalmaya ve di�i s��anlarda menstr�el siklus bozukluklar�na yol a�m��t�r. Di�er t�m organlarda hi�bir de�i�iklik olmam��t�r.
T�m�rijenik ve mutajenik potansiyel
Oral treosulfan dozlar�yla uzun s�reli tedavide hastalar�n %1.4'�nde akut non-lenfositik l�semi g�zlenmi�tir. Alkilleyici �zellikler ta��yan di�er sitostatik ajanlarda oldu�u gibi treosulfan da mutajenik potansiyele sahiptir. Bu nedenle �ocuk sahibi olma potansiyeli bulunan kad�n hastalar�n tedavi s�resince etkili kontrasepsiyon uygulamalar� zorunludur.
�reme toksisitesi
Treosulfan hayvan �al��malar�nda �reme toksisitesi y�n�nden test edilmemi�tir. Bununla birlikte, s��anlarda kronik toksisite testleri s�ras�nda gecikmi� spermiyogenez ve korpora lutea ve folik�l yoklu�u saptanm��t�r.
Sitotoksik preparatlar gebe olabilecek personel taraf�ndan haz�rlanmamal�d�r.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Yok
6.2. Ge�imsizlikler
Bu t�bbi �r�n B�l�m 6.6'da belirtilenler d���nda di�er t�bbi �r�nler ile kar��t�r�lmamal�d�r.
6.3. Raf �mr�
24 ay
Suland�r�lm�� ��zeltiler
��kelti olu�umuna neden olabilece�inden, suland�r�lm�� �r�n� buzdolab�nda saklamay�n�z (2
- 8°C). ��kelti belirtileri g�steren ��zeltiler kullan�lmamal�d�r. Buzdolab�nda saklamay�n�z.
Kullan�m s�ras�nda kimyasal ve fiziksel stabilite 30°C'de 12 saat i�in g�sterilmi�tir. Mikrobiyolojik a��dan, haz�rlama y�ntemi mikrobiyolojik kontaminasyon riskini ortadan kald�rm�yorsa �r�n hemen kullan�lmal�d�r. Hemen kullan�lmamas� halinde kullan�m an�ndaki saklama s�releri ve ko�ullar� kullan�c�n�n sorumlulu�undad�r.
6.4. Saklamaya y�nelik �zel tedbirler
(3.2, 9.6)
25°C alt�ndaki oda s�cakl���nda saklay�n�z.
T�bbi �r�n suland�r�ld�ktan sonraki saklama ko�ullar� i�in bkz. B�l�m 6.3.
6.5. Ambalaj�n niteli�i ve i�eri�i
20 mm ge�meli kapakl�, 20 mm bromob�til kau�uk t�payla kapat�lm�� kal�planm��, liyofilize
edilmi�, renksiz 100 ml Tip-I cam flakon.
Flakonlar plastik shrink sleeve/taban (destek) ile giydirilmi� olabilir veya olmayabilir. Bu plastik kaplama m�stahzar ile temas etmez ve sevkiyat s�ras�nda ilave koruma sa�lama amac�n� ta��r. Bu, t�bbi �r�n�n hem sa�l�k mesle�i mensuplar� hem de ila� personeli taraf�ndan g�venli uygulanmas�n� artt�r�r.
ALLOPRE 1 veya 5 flakon i�eren karton kutularda takdim edilmektedir.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
ALLOPRE 100 ml enjeksiyonluk suda ��zd�r�ld�kten sonra intraven�z inf�zyon i�in kullan�l�r.
Suland�r�lan ��zelti berrak, renksiz bir ��zeltidir.
Kullan�mdan �nce ��zeltiyi g�zle kontrol ediniz. Yaln�zca i�erisinde partik�ller bulunmayan berrak ��zeltiler kullan�lmal�d�r.
��kelti belirtileri g�steren suland�r�lm�� ��zeltiler kullan�lmamal� ve tehlikeli at�klar�n bertaraf edilmesine ili�kin yasal zorunluluklara uygun �ekilde imha edilmelidir (bkz. a�a��).
Tek kullan�ml�kt�r; kullan�lmayan flakon i�eri�ini at�n�z.
“Sitotoksik ve sitostatik be�eri t�bbi �r�nlerin kullan�mlar� sonucu bo�alan i� ambalajlar�n�n at�klar� TEHL�KEL� ATIKTIR ve bu at�klar�n y�netimi 2/4/2015 tarihli ve 29314 say�l� Resmî Gazetede yay�mlanan At�k Y�netimi Y�netmeli�ine g�re yap�l�r”
T�m sitotoksik maddeler i�in oldu�u gibi, ALLOPRE'nin haz�rlanmas� s�ras�nda uygun �nlemler al�nmal�d�r.
Antineoplastik ajanlar�n g�venli haz�rlanmas�na dair talimatlar:
T�bbi �r�n� e�itimli personel haz�rlamal�d�r.
Sitotoksik ila�lar�n haz�rlanmas�nda kullan�lan ara�-gere�lerin (enjekt�rler, i�neler vb.) bertaraf edilmesinde uygun �nlemler al�nmal� ve dikkatli olunmal�d�r.
 Depresyonu Anlamak
Depresyon farkl� ki�ileri farkl� bi�imlerde etkiler. Duygusal veya fiziksel
olmak �zere geni� alanda belirtilere sebep olabilir.Depresyona neler sebep olur?
Depresyonu Anlamak
Depresyon farkl� ki�ileri farkl� bi�imlerde etkiler. Duygusal veya fiziksel
olmak �zere geni� alanda belirtilere sebep olabilir.Depresyona neler sebep olur? |
 Mide Kanseri
Mide kanseri genellikle mideyi t�m�yle kaplayan ve mukus �retmekle g�revli h�crelerde ba�lar. Bu kanser tipine adenokarsinom denir.
Mide Kanseri
Mide kanseri genellikle mideyi t�m�yle kaplayan ve mukus �retmekle g�revli h�crelerde ba�lar. Bu kanser tipine adenokarsinom denir. |
 |
Kolon, Rektum yada Ba��rsak Kanseri Ba��rsak kanseri kolon veya rektumda (arka ge�it) herhangi bir b�lgede ortaya ��kabilir.Kolorektal kanser erken safhalarda te�his edilmesi halinde daha kolay ve daha ba�ar�l� bir �ekilde tedavi edilir. |
 |
Y�ksek Tansiyon Hipertansiyon s�rekli anormal derecede y�ksek olan kan bas�nc�d�r. Tansiyon atardamarlar�n�zdaki kan�n bas�nc�d�r. |
 |
Artrit Artrit, olduk�a yayg�n bir hastal�kt�r ancak iyi anla��lamam��t�r. Asl�nda �artrit� tek bir hastal���n ad� de�ildir; eklem a�r�s� veya eklem hastal�klar�n� adland�rman�n gayri resmi yoludur. |
�LA� GENEL B�LG�LER�
Ideogen �la� Sanayi A.�
| Sat�� Fiyat� | 45712.01 TL [ 1 Dec 2025 ] |
| �nceki Sat�� Fiyat� | 45712.01 TL [ 24 Nov 2025 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8680952000062 |
| Etkin Madde | Treosulfan |
| �thal ( ref. �lke : Yunanistan ) ve Be�eri bir ila�d�r. |