BRAFTOVI 75 mg sert kaps�l (42 adet) K�sa �r�n Bilgisi
{ Enkorafenib }
1. BE�ER� TIBB� �R�N�N ADI
BRAFTOVI 75 mg sert kaps�l
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Enkorafenib 75 mg
Yard�mc� maddeler
in tam listesi i�in b�l�m 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Sert kaps�l (kaps�l)
Kapakta stilize “A” ve g�vdede “LGX 75mg” bask�l�, ten rengi opak kapak ve beyaz opak g�vde. Kaps�l�n uzunlu�u yakla��k 23 mm'dir.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Enkorafenib:
-Binimetinib ile kombinasyon halinde, daha �nce herhangi bir RAF yola�� inhibit�r� kullanmam��, ECOG performans skoru 0 veya 1 olan, BRAF V600 mutasyonu olan, rezeke edilemeyen veya metastatik malign melanomlu yeti�kin hastalar�n tedavisinde endikedir (bkz. b�l�m 4.4 ve 5.1).
-Setuksimab ile kombinasyon halinde, ECOG performans skoru 0 veya 1 olan, daha �nce en az bir basamak sistemik tedavi alm�� BRAF V600E mutasyonlu metastatik kolorektal kanserli (KRK) yeti�kin hastalar�n tedavisinde endikedir (bkz. b�l�m 4.4 ve 5.1).
4.2. Pozoloji ve uygulama �ekli
Enkorafenib tedavisi, antikanser ila�lar�n kullan�m�nda deneyimli bir hekimin sorumlulu�unda ba�lat�lmal� ve g�zetimi alt�nda tutulmal�d�r.
Pozoloji
Melanom
�nerilen enkorafenib dozu, binimetinib ile birlikte kullan�ld���nda g�nde bir kez 450 mg'd�r (alt� adet 75 mg kaps�l).
Kolorektal kanser
Setuksimab ile birlikte kullan�ld���nda �nerilen enkorafenib dozu g�nde bir kez 300 mg'd�r (d�rt adet 75 mg kaps�l).
Doz modifikasyonlar�
Melanom
Advers reaksiyonlar�n y�netimi, enkorafenibin dozunun azalt�lmas�n�, ge�ici olarak kesilmesini veya tedavinin kesilmesini gerektirebilir (bkz. Tablo 1, 3 ve 4).
Binimetinib'in pozolojisi ve �nerilen doz de�i�iklikleri hakk�nda bilgi i�in binimetinib K�B, b�l�m
4.2'ye bak�n�z.
Enkorafenib i�in doz azaltma �nerileri Tablo 1'de sunulmu�tur.
Tablo 1: Melanom endikasyonunda binimetinib ile kombinasyon halinde kullan�ld���nda enkorafenib i�in �nerilen doz de�i�iklikleri
Doz seviyesi | Enkorafenib dozu binimetinib ile birlikte kullan�ld���nda |
Ba�lang�� dozu | 450 mg g�nde bir kez |
1. doz azaltma | 300 mg g�nde bir kez |
2. doz azaltma | 225 mg g�nde bir kez |
Sonraki de�i�iklik | Dozun g�nde bir kez 100 mg'a d���r�lmesi i�in s�n�rl� veri vard�r. Hasta g�nde bir kez 100 mg'� tolere edemiyorsa, enkorafenib kal�c� olarak kesilmelidir. |
Enkorafenib'in tek bir ajan olarak g�nde bir kez 450 mg dozda uygulanmas� �nerilmez. Binimetinibe ge�ici olarak ara verilirse, enkorafenib, bir doz olarak 450 mg'l�k dozda iyi tolere edilmedi�inden, binimetinib dozuna ara verildi�i s�rada g�nde bir kez 300 mg'da enkorafenib azalt�lmal�d�r (binimetinib K�sa �r�n Bilgisi [K�B] b�l�m 4.2'ye bak�n). Binimetinib kal�c� olarak kesilirse, enkorafenib kesilmelidir.
Enkorafenib ge�ici olarak kesilirse (bkz. Tablo 3 ve 4), binimetinibe ara verilmelidir. Enkorafenib kal�c� olarak kesilirse, binimetinib kesilmelidir.
Tedaviye ba�l� toksisiteler meydana gelirse, enkorafenib ve binimetinib dozu azalt�lmal�, ara verilmeli veya kesilmelidir. Binimetinib i�in doz de�i�iklikleri sadece a�a��dakiler i�in gereklidir (�ncelikle binimetinib ile ilgili advers reaksiyonlar): Retina pigment epitel dekolman� (RPED), retinal ven t�kan�kl��� (RVT), interstisyel akci�er hastal���/pn�moni, kardiyak fonksiyon bozuklu�u, kreatin fosfokinaz (KK) y�kselmesi ve rabdomiyoliz ve ven�z tromboembolizm (VTE).
Bu toksisitelerden biri meydana gelirse, binimetinib doz modifikasyon talimatlar� i�in bkz.
binimetinib K�sa �r�n Bilgisi (K�B), b�l�m 4.2.
Kolorektal kanser
Advers reaksiyonlar�n y�netimi, enkorafenibin dozunun azalt�lmas�n�, ge�ici olarak kesilmesini veya tedavinin kesilmesini gerektirebilir (bkz. Tablo 2, 3 ve 4).
Setuksimab�n pozolojisi ve �nerilen doz de�i�iklikleri hakk�nda bilgi i�in setuksimab K�B, b�l�m
4.2'ye bak�n�z.
Enkorafenib i�in doz azaltma �nerileri Tablo 2'de sunulmu�tur.
Tablo 2: KRK endikasyonunda setuksimab ile kombinasyon halinde kullan�ld���nda enkorafenib i�in �nerilen doz modifikasyonlar�
Doz seviyesi | Enkorafenib dozu setuksimab ile birlikte kullan�ld���nda |
Ba�lang�� dozu | 300 mg g�nde bir kez |
1. doz azaltma | 225 mg g�nde bir kez |
2. doz azaltma | 150 mg g�nde bir kez |
Enkorafenib kal�c� olarak kesilirse, setuksimab kesilmelidir. Setuksimab kal�c� olarak kesilirse, enkorafenib kesilmelidir.
Melanom ve kolorektal kanser
Advers reaksiyonlar durumunda doz de�i�iklikleri a�a��da ve Tablo 3 ve 4'te verilmi�tir.
Yeni primer kutan�z maligniteler i�in: Enkorafenib i�in doz modifikasyonu gerekli de�ildir.
Yeni primer kutan�z olmayan RAS mutasyonu pozitif maligniteler i�in: Enkorafenib'in kal�c� olarak kesilmesi d���n�lmelidir.
Tablo 3: Se�ilmi� advers reaksiyonlar i�in binimetinib ile kombinasyon halinde veya setuksimab ile kombinasyon halinde kullan�ld���nda enkorafenib i�in �nerilen doz modifikasyonlar�
Advers reaksiyonun ciddiyeti | Enkorafenib |
Deri reaksiyonlar� | |
Enkorafenib'e devam edilmelidir. D�k�nt� tedavi ile 2 hafta i�inde k�t�le�ir veya d�zelmezse, enkorafenib Derece 0 veya 1'e kadar kesilmeli ve ard�ndan ayn� dozda yeniden ba�lat�lmal�d�r. | |
Derece 0 veya 1'e iyile�ene kadar enkorafenib'e ara verilmeli ve ilk ortaya ��kmas� durumunda ayn� dozda yeniden ba�lanmal� veya Derece 3'�n tekrarlanmas� durumunda azalt�lm�� dozda devam edilmelidir. | |
Enkorafenib kal�c� olarak kesilmelidir. | |
Palmar-plantar eritrodisestezi sendromu (PPES) | |
Enkorafenib'e devam edilmeli ve topikal tedavi gibi destekleyici �nlemler al�nmal�d�r. 2 hafta i�inde destekleyici tedaviye ra�men d�zelme olmazsa, Derece 0 veya 1'e d�zelene kadar enkorafenib durdurulmal� ve tedaviye ayn� doz seviyesinde veya azalt�lm�� bir dozda devam edilmelidir. | |
Enkorafenib verilmemeli, topikal tedavi gibi destekleyici �nlemler al�nmal� ve hasta haftal�k olarak yeniden de�erlendirilmelidir. Enkorafenib, Derece 0 veya 1'e y�kseltildi�inde ayn� doz seviyesinde veya azalt�lm�� doz seviyesinde yeniden ba�lat�lmal�d�r. | |
�veit dahil iritis ve iridosiklit | |
Derece 1 veya 2 �veit veya Derece 3 �veit spesifik (�rn. topikal) ok�ler tedaviye i�in yan�t vermiyorsa, enkorafenib verilmemeli ve 2 hafta i�inde oftalmik izleme tekrarlanmal�d�r. �veit Derece 1 ise ve Derece 0'a d�zeliyorsa tedaviye ayn� dozda devam edilmelidir. �veit Derece 2 veya 3 ise ve Derece 0 veya 1'e iyile�irse, tedaviye azalt�lm�� bir dozda devam edilmelidir. 6 hafta i�inde d�zelme olmazsa, oftalmik izleme tekrarlanmal� ve enkorafenib kal�c� olarak kesilmelidir. | |
Enkorafenib kal�c� olarak kesilmeli ve oftalmolojik izleme ile takip yap�lmal�d�r. | |
Derece 2
Derece 3
Derece 4
Derece 2
Derece 3
Derece 1-3
Derece 4
Advers reaksiyonun ciddiyeti | Enkorafenib |
QTc Uzamas� | |
Enkorafenib verilmemelidir (bkz. B�l�m 4.4'teki izleme) QTcF ≤ 500 ms oldu�unda enkorafenib azalt�lm�� dozda yeniden ba�lat�lmal�d�r.
Birden fazla tekrarlayan durum olursa enkorafenib kesilmelidir. | |
artm�� > 60 ms tedavi �ncesi de�erden | Enkorafenib kal�c� olarak kesilmelidir (bkz. b�l�m 4.4'teki izleme). |
Karaci�er testleri anormallikleri | |
Enkorafenib'e devam edilmelidir. 4 hafta i�inde iyile�me olmazsa, Derece 0 veya 1'e veya tedavi �ncesi/ba�lang�� seviyelerine iyile�ene kadar enkorafenib durdurulmal� ve ard�ndan ayn� dozda yeniden ba�lat�lmal�d�r. | |
ve kan bilirubin > 2x ULN) | Enkorafenib 4 haftaya kadar kesilmelidir. |
Enkorafenib 4 haftaya kadar kesilmelidir.
Veya enkorafenib kal�c� olarak kesilmelidir. | |
Enkorafenib 'in kal�c� olarak kesilmesi d���n�lmelidir. | |
Enkorafenib kal�c� olarak kesilmelidir. | |
QTcF > 500 ms ve de�i�im ≤ 60 ms tedavi �ncesi
QTcF > 500 ms ve
Derece 2 aspartat aminotransferaz (AST) veya alanin aminotransferaz (ALT) > 3x ≤ 5x normalin �st s�n�r� (ULN)
Derece 3'�n ilk olu�umu (AST veya ALT > 5x ULN
Derece 0 veya 1'e veya ba�lang�� d�zeyine y�kselirse, binimetinib azalt�lm�� dozla devam ettirilmelidir.
E�er d�zelme olmazsa, enkorafenib kal�c� olarak kesilmelidir.
Derece 4'�n ilk olu�umu (AST veya ALT > 20 ULN)
Derece 0 veya 1'e veya ba�lang�� d�zeyine y�kselirse, enkorafenib azalt�lm�� doz seviyesinde devam ettirilmelidir.
E�er d�zelme olmazsa, enkorafenib kal�c� olarak kesilmelidir.
Tekrarlayan Derece 3 (AST veya ALT > 5x ULN ve kan bilirubin > 2x ULN)
Tekrarlayan Derece 4 (AST veya ALT > 20 ULN)
Tablo 4: Di�er advers reaksiyonlar i�in binimetinib veya setuksimab ile kombinasyon halinde kullan�ld���nda enkorafenib i�in �nerilen doz de�i�iklikleri
Advers reaksiyonun ciddiyeti | Enkorafenib |
Enkorafenib 4 haftaya kadar kesilmelidir. | |
Enkorafenib 4 haftaya kadar kesilmelidir.
Veya enkorafenib kal�c� olarak kesilmelidir. | |
Enkorafenib 'in kal�c� olarak kesilmesi d���n�lmelidir. | |
Enkorafenib kal�c� olarak kesilmelidir. |
Tekrarlayan veya tolere edilemeyen Derece 2 advers reaksiyonlar
Derece 3 advers reaksiyonlar�n ilk ortaya ��k���
Derece 0 veya 1'e veya ba�lang�� d�zeyine y�kselirse, enkorafenib azalt�lm�� dozda yeniden ba�lat�lmal�d�r veya
E�er d�zelme olmazsa, enkorafenib kal�c� olarak kesilmelidir.
Derece 4 advers reaksiyonlar�n ilk ortaya ��k���
Derece 0 veya 1'e veya ba�lang�� d�zeyine y�kselirse, enkorafenib azalt�lm�� dozda yeniden ba�lat�lmal�d�r veya
E�er d�zelme olmazsa, enkorafenib kal�c� olarak kesilmelidir.
Tekrarlayan Derece 3 advers reaksiyonlar
Tekrarlayan Derece 4 advers reaksiyonlar
Tedavi s�resi
Tedavi, hasta art�k fayda g�rmeyene veya kabul edilemez toksisite geli�ene kadar devam etmelidir.
Unutulan doz
Bir enkorafenib dozu atlan�rsa, hasta ancak bir sonraki programlanan doza 12 saatten fazla zaman varsa, ka��r�lan dozu almal�d�r.
Kusma
Enkorafenib uygulamas�ndan sonra kusma durumunda, hasta dozu tekrar almamal� ve planlanan bir sonraki dozu almal�d�r.
Uygulama �ekli
BRAFTOVI a��zdan kullan�m i�indir. Kaps�ller su ile b�t�n olarak yutulmal�d�r. Yemekle birlikte veya yemeksiz al�nabilirler. Enkorafenib'in greyfurt suyu ile birlikte uygulanmas�ndan ka��n�lmal�d�r (bkz. b�l�m 4.4 ve 4.5).
�zel pop�lasyonlar Ya�l� hastalar
65 ya� ve �zeri hastalarda doz ayarlamas� gerekli de�ildir (bkz B�l�m 5.2).
Karaci�er yetmezli�i
Hafif ila �iddetli karaci�er yetmezli�i olan hastalarda enkorafenib maruziyeti artm�� olabilir (bkz. b�l�m 5.2).
Hafif karaci�er yetmezli�i olan hastalarda (Child Pugh S�n�f A) enkorafenib uygulamas� g�nde bir kez 300 mg'l�k bir dozda dikkatle yap�lmal�d�r.
Orta (Child Pugh S�n�f B) veya �iddetli (Child-Pugh S�n�f C) karaci�er yetmezli�i olan hastalarda kullan�lmamal�d�r.
B�brek yetmezli�i
Pop�lasyon farmakokineti�i (PK) analizine g�re hafif veya orta derecede b�brek yetmezli�i olan hastalarda doz ayarlamas� gerekli de�ildir. �iddetli b�brek yetmezli�i olan hastalarda enkorafenib ile ilgili klinik veri yoktur. Bu nedenle, doz ayarlamas� i�in potansiyel ihtiya� belirlenemez. Enkorafenib, �iddetli b�brek yetmezli�i olan hastalarda dikkatli kullan�lmal�d�r (bkz. b�l�m 4.4 ve 5.2).
Pediyatrik pop�lasyon
�ocuklarda ve ergenlerde enkorafenib'in g�venlili�i ve etkilili�i hen�z belirlenmemi�tir, bu pop�lasyona ait veri bulunmamaktad�r.
4.3. Kontrendikasyonlar
Etkin madde
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Enkorafenib, binimetinib ile kombinasyon halinde (BRAF V600 mutant rezeke edilemeyen veya metastatik melanomlu hastalar i�in) veya setuksimab ile kombinasyon halinde (BRAF V600E mutant metastatik kolorektal kanserli hastalar i�in) verilecektir. Binimetinib veya setuksimab tedavisi ile ilgili uyar�lar ve �nlemler hakk�nda ek bilgi i�in binimetinib K�B veya setuksimab K�B'�n 4.4 b�l�m�ne bak�n.
BRAF mutasyon testi
Enkorafenib almadan �nce, hastalarda BRAF V600 mutasyonlu rezeke edilemeyen veya metastatik melanom veya valide edilmi� bir testle do�rulanm�� BRAF V600E mutasyonlu metastatik kolorektal kanser olmal�d�r. Enkorafenib'in etkilili�i ve g�venlili�i yaln�zca BRAF V600E ve V600K mutasyonlar�n� eksprese eden melanom t�m�rleri veya BRAF V600E mutasyonunu ekprese eden kolorektal t�m�rleri olan hastalarda belirlenmi�tir. Enkorafenib, yaban�l tip BRAF malign melanomu veya vah�i tip BRAF kolorektal kanserli hastalarda kullan�lmamal�d�r.
Bir BRAF inhibit�r� ile tedavi s�ras�nda progrese olan hastalarda binimetinib ile kombinasyon halinde enkorafenib
BRAF V600 mutasyonlu, rezeke edilemeyen veya metastatik melanom tedavisi i�in verilen bir BRAF inhibit�r�nde ilerleme g�steren hastalarda enkorafenib ile binimetinib kombinasyonunun kullan�m�na ili�kin s�n�rl� veri bulunmaktad�r. Bu veriler, bu hastalarda kombinasyonun etkinli�inin daha d���k
olaca��n� g�stermektedir.
Beyin metastaz� olan hastalarda binimetinib ile kombinasyon halinde enkorafenib
Beyne metastaz yapm�� BRAF V600 mutant melanomlu hastalarda enkorafenib ve binimetinib kombinasyonunun etkililik verileri s�n�rl�d�r (bkz. b�l�m 5.1).
Sol ventrik�l disfonksiyonu (LVD)
Enkorafenib, binimetinib ile birlikte kullan�ld���nda, ejeksiyon fraksiyonunda semptomatik veya asemptomatik d����ler olarak tan�mlanan LVD bildirilmi�tir. Tedavi s�ras�nda sol ventrik�l ejeksiyon fraksiyonunun (LVEF), enkorafenib ve binimetinib ba�lat�lmadan �nce, ba�lad�ktan bir ay sonra ve ard�ndan yakla��k 3 ayl�k aral�klarla veya klinik olarak belirtildi�i gibi daha s�k aral�klarla ekokardiyogram veya �ok kap�l� edinim (MUGA) taramas� ile de�erlendirilmesi �nerilir. Tedavi s�ras�nda LVD meydana gelirse, binimetinib K�B, b�l�m 4.2'ye bak�n�z.
Enkorafenib ile binimetinib kombinasyonunun g�venli�i, ba�lang�� LVEF'si %50'nin alt�nda veya normalin alt s�n�rlar�n�n alt�nda olan hastalarda belirlenmemi�tir. Bu nedenle, bu hastalarda binimetinib dikkatli bir �ekilde kullan�lmal� ve herhangi bir semptomatik sol ventrik�l disfonksiyonu, Derece 3-4 LVEF azalmas� veya LVEF'nin ba�lang�ca g�re ≥ %10 mutlak azalmas� durumunda, binimetinib ve enkorafenib kesilmeli ve her 2 haftada bir LVEF de�erlendirilmelidir.
Kanama
Enkorafenib uyguland���nda maj�r hemorajik olaylar dahil hemorajiler meydana gelebilir (bkz. b�l�m 4.8). Antikoag�lan ve antiplatelet tedavilerinin birlikte kullan�m� kanama riskini art�rabilir. Derece ≥ 3 hemorajik olaylar�n olu�umu, doza ara verilerek veya tedavi kesilerek (bkz. B�l�m 4.2 Tablo 4) ve klinik olarak endike oldu�u �ekilde y�netilmelidir.
Ok�ler toksisiteler
Enkorafenib uyguland���nda �veit, iritis ve iridosiklit dahil ok�ler toksisiteler ortaya ��kabilir. Binimetinib ile kombinasyon halinde enkorafenib ile tedavi edilen hastalarda da RPED bildirilmi�tir (bkz. b�l�m 4.8).
Hastalar, yeni veya k�t�le�en g�rme bozuklu�u semptomlar� i�in her ziyarette de�erlendirilmelidir. Azalm�� merkezi g�rme, bulan�k g�rme veya g�rme kayb� dahil olmak �zere yeni veya k�t�le�en g�rme bozukluklar�n�n semptomlar� tespit edilirse, derhal bir oftalmolojik muayene �nerilir.
Tedavi s�ras�nda �veit i�eren iridosiklit ve iritis olu�ursa,b�l�m 4.2'ye bak�n�z.
Tedavi s�ras�nda hasta RPED veya RVO geli�tirirse, rehberlik i�in binimetinib K�B, b�l�m 4.2'ye bak�n�z.
QT uzamas�
BRAF inhibit�rleri ile tedavi edilen hastalarda QT Uzamas� g�zlemlenmi�tir. Enkorafenibin QT uzatma potansiyelini de�erlendirmek i�in kapsaml� bir QT �al��mas� yap�lmam��t�r.
Genel olarak, sonu�lar tek ajan enkorafenib'in kalp h�z�nda hafif art��lara neden olma potansiyeline sahip oldu�unu g�stermektedir. �nerilen dozlarda enkorafenib ve binimetinib'in havuzlanm�� kombinasyon �al��malar� ve tek ajanl� bir enkorafenib �al��mas�nda elde edilen sonu�lar, enkorafenib'in QTc aral���nda k���k art��larla sonu�lanma potansiyeline sahip oldu�unu g�stermektedir (bkz. b�l�m 5.1).
Klinik olarak anlaml� maruziyete ba�l� QT uzamas�n� d��lamak i�in yeterli veri yoktur.
QT uzamas� i�in potansiyel risk nedeniyle, tedaviye ba�lamadan �nce ve tedavi s�ras�nda magnezyum ve potasyum dahil serum elektrolit anormalliklerinin d�zeltilmesi ve QT uzamas� i�in risk fakt�rlerinin (�rn. konjestif kalp yetmezli�i, bradiaritmiler) kontrol edilmesi �nerilir.
Enkorafenib ba�lanmadan �nce, ba�land�ktan bir ay sonra ve daha sonra tedavi s�ras�nda yakla��k 3 ayl�k aral�klarla veya klinik olarak belirtildi�i gibi daha s�k aral�klarla bir elektrokardiyogram�n (EKG) de�erlendirilmesi �nerilir. QTc uzamas�n�n ortaya ��kmas�, anormal elektrolitlerin d�zeltilmesi ve risk fakt�rlerinin kontrol� ile dozun azalt�lmas�, kesilmesi veya kesilmesi ile y�netilebilir (bkz. b�l�m 4.2).
Yeni primer maligniteler
BRAF inhibit�rleri ile tedavi edilen hastalarda kutan�z ve kutan�z olmayan yeni primer maligniteler g�zlenmi�tir ve enkorafenib uyguland���nda ortaya ��kabilir (bkz. b�l�m 4.8).
Cilt maligniteleri
Enkorafenib dahil BRAF inhibit�rleri ile tedavi edilen hastalarda keratoakantom dahil kutan�z skuam�z h�creli karsinom (cuSCC) gibi kutan�z maligniteler g�zlenmi�tir.
Enkorafenib dahil BRAF inhibit�rleri ile tedavi edilen hastalarda yeni primer melanom g�zlenmi�tir (bkz. b�l�m 4.8).
Enkorafenib tedavisine ba�lamadan �nce, tedavi s�ras�nda 2 ayda bir ve tedavinin kesilmesini takiben
6 aya kadar dermatolojik de�erlendirmeler yap�lmal�d�r. ��pheli deri lezyonlar� dermatolojik eksizyon ve dermatopatolojik de�erlendirme ile tedavi edilmelidir. Hastalara, yeni cilt lezyonlar� geli�irse derhal doktorlar�n� bilgilendirmeleri s�ylenmelidir. Enkorafenib'e herhangi bir doz de�i�ikli�i yap�lmadan devam edilmelidir.
Deri d��� maligniteler
Etki mekanizmas�na ba�l� olarak, enkorafenib, mutasyon veya di�er mekanizmalar yoluyla RAS aktivasyonu ile ili�kili maligniteleri malignitelerin riskinin artmas�na yol a�abilir. Enkorafenib alan hastalar, klinik olarak uygun �ekilde tedaviye ba�lamadan �nce, tedavi s�ras�nda ve sonunda ba� ve boyun muayenesinden, g���s/kar�n bilgisayarl� tomografisi (BT) taramas�ndan, anal ve pelvik muayeneden (kad�nlar i�in) ve tam kan h�cresi say�mlar�ndan ge�melidir. RAS mutasyonu pozitif kutan�z d��� maligniteler geli�en hastalarda enkorafenibin kal�c� olarak kesilmesi d���n�lmelidir. RAS mutasyonu ile ili�kili daha �nce veya e�zamanl� kanseri olan hastalara enkorafenib uygulanmadan �nce faydalar ve riskler dikkatlice d���n�lmelidir.
Karaci�er testi anormallikleri
Enkorafenib ile AST ve ALT y�kselmeleri dahil karaci�er testi anormallikleri olu�abilir (bkz. b�l�m 4.8). Karaci�er testi de�erleri, enkorafenib ba�lat�lmadan �nce ve tedavinin ilk 6 ay� boyunca en az ayda bir ve daha sonra klinik olarak belirtildi�i �ekilde izlenmelidir. Karaci�er testi anormallikleri doza ara verilerek, azalt�larak veya tedavi kesilerek y�netilmelidir (bkz. B�l�m 4.2).
Karaci�er yetmezli�i
Enkorafenib ba�l�ca karaci�er yoluyla metabolize ve elimine edildi�inden, hafif ila �iddetli karaci�er yetmezli�i olan hastalarda, maruziyet artabilir. (bkz. b�l�m 5.2).
Klinik veri olmamas� nedeni ile, orta veya �iddetli karaci�er yetmezli�i olan hastalarda enkorafenib
�nerilmemektedir.
Hafif karaci�er yetmezli�i olan hastalarda g�nde bir kez 300 mg dozunda enkorafenib uygulamas� dikkatle yap�lmal�d�r (bkz. b�l�m 4.2).
Klinik muayene ve karaci�er fonksiyon testleri dahil olmak �zere hafif karaci�er yetmezli�i olan hastalarda enkorafenib ile ili�kili toksisitelerin daha yak�ndan izlenmesi ve tedavi s�ras�nda klinik olarak uygun olarak EKG'lerin de�erlendirilmesi �nerilir.
B�brek yetmezli�i
�iddetli b�brek yetmezli�i olan hastalarda veri mevcut de�ildir (bkz. b�l�m 4.2 ve 5.2). Enkorafenib, �iddetli b�brek yetmezli�i olan hastalarda dikkatli kullan�lmal�d�r. Enkorafenib ile tek ajan olarak veya binimetinib veya setuksimab ile kombinasyon halinde kreatinin y�kselmesi yayg�n olarak bildirilmi�tir. Akut b�brek hasar� ve b�brek yetmezli�i dahil olmak �zere g�zlenen b�brek yetmezli�i vakalar� genellikle kusma ve dehidratasyon ile ili�kilendirilmi�tir. Di�er fakt�rler ise diyabet ve hipertansiyon'dur. Kan kreatinin klinik olarak belirtildi�i gibi izlenmeli ve kreatinin y�kselmesi doz modifikasyonu veya kesilmesiyle y�netilmelidir (bkz. B�l�m 4.2'deki Tablo 4). Hastalar tedavi s�ras�nda yeterli s�v� al�m�n� sa�lamal�d�r.
Di�er t�bbi �r�nlerin enkorafenib �zerindeki etkileri.
Enkorafenib tedavisi s�ras�nda g��l� CYP3A inhibit�rlerinin e�zamanl� kullan�m�ndan ka��n�lmal�d�r. G��l� bir CYP3A inhibit�r� ile e�zamanl� kullan�m gerekliyse, hastalar g�venlik a��s�ndan dikkatle izlenmelidir (bkz. b�l�m 4.5).
Enkorafenib ile birlikte orta d�zeyde bir CYP3A inhibit�r� uygulan�yorsa dikkatli olunmal�d�r.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Di�er maddelerin enkorafenib �zerindeki etkileri Enkorafenib �ncelikle CYP3A4 taraf�ndan metabolize edilir.
CYP3A4 inhibit�rleri
Sa�l�kl� g�n�ll�lerde orta (diltiazem) ve g��l� (posakonazol) CYP3A4 inhibit�rlerinin tek doz enkorafenib ile birlikte uygulanmas�, konsantrasyon-zaman e�risi (EAA) alt�ndaki alanda s�ras�yla 2 ve 3 kat bir art��a neden olmu�tur. Maksimum enkorafenib konsantrasyonunda (Cmax) s�ras�yla
%44,6'l�k ve %68,3 art�� olmu�tur.
Model tabanl� tahminler, tekrarlanan uygulamalardan sonra posakonazol�n etkisinin EAA i�in benzer (3-kat art��) ve Cmax i�in biraz daha b�y�k (2,7-kat art��) olabilece�ini g�stermektedir. Ketokonazol i�in modele dayal� tahminler, enkorafenib 450 ve 300 mg QD uygulamas�ndan sonra s�ras�yla yakla��k olarak enkorafenib EAA i�in 5 kat ve enkorafenib Cmaks i�in 3 ila 4 kat artm��t�r.
Bu nedenle, enkorafenibin g��l� CYP3A4 inhibit�rleri ile birlikte uygulanmas�ndan ka��n�lmal�d�r (artan enkorafenib maruziyeti ve toksisitedeki potansiyel art�� nedeniyle, bkz. b�l�m 5.2). G��l� CYP3A4 inhibit�rlerinin �rnekleri aras�nda ritonavir, itrakonazol, klaritromisin, telitromisin, posakonazol ve greyfurt suyu yer al�r ancak bunlarla s�n�rl� de�ildir. G��l� bir CYP3A inhibit�r�n�n e�zamanl� kullan�m�ndan ka��n�lmayacaksa, hastalar g�venlik a��s�ndan dikkatle izlenmelidir.
Orta derecede CYP3A4 inhibit�rleri dikkatle birlikte uygulanmal�d�r. Orta dereceli CYP3A4 inhibit�rlerinin �rnekleri aras�nda bunlarla s�n�rl� olmamak �zere amiodaron, eritromisin, flukonazol, diltiazem, amprenavir ve imatinib bulunur. Enkorafenib orta d�zeyde bir CYP3A inhibit�r� ile
birlikte uyguland���nda, hastalar g�venlik a��s�ndan dikkatle izlenmelidir.
CYP3A4 ind�kleyicileri
Enkorafenibin bir CYP3A4 ind�kleyicisi ile birlikte uygulanmas� klinik �al��mada de�erlendirilmemi�tir; bununla birlikte, enkorafenib maruziyetinde bir azalma olas�d�r ve bu da etkilili�in azalmas�na neden olabilir. Orta veya g��l� CYP3A4 ind�kleyicilerinin �rnekleri aras�nda, bunlarla s�n�rl� olmamak �zere karbamazepin, rifampisin, fenitoin ve St. John's Wort bulunur. CYP3A ind�ksiyon potansiyeli olmayan veya minimum d�zeyde olan alternatif ajanlar d���n�lmelidir.
Enkorafenib'in di�er maddeler �zerindeki etkileri
CYP substratlar�
Enkorafenib, CYP3A4'�n hem inhibit�r� hem de ind�kleyicisidir. CYP3A4'�n substratlar� olan ajanlarla (�rn. hormonal kontraseptifler) e�zamanl� kullan�m, bu ajanlar�n toksisitesinin artmas�na veya etkinlik kayb�na neden olabilir. CYP3A4 substratlar� olan ajanlar dikkatle birlikte uygulanmal�d�r.
Enkorafenib, �ridin difosfat glukuronoziltransferaz (UGT) 1A1'in bir inhibit�r�d�r. UGT1A1'in substratlar� olan e� zamanl� ajanlar (�rn. raltegravir, atorvastatin, dolutegravir) artm�� maruziyete sahip olabilir ve bu nedenle dikkatle uygulanmal�d�r.
Enckrafenib'in binimetinib �zerindeki etkisi
Enkorafenib, UGT1A1'in nispeten g��l� bir geri d�n���ml� inhibit�r� olmas�na ra�men, binimetinib ile enkorafenib birlikte uyguland���nda klinik olarak binimetinib maruziyetinde herhangi bir farkl�l�k g�zlenmemi�tir.
Ta��y�c� y�zeyler
Enkorafenib potansiyel olarak bir dizi ta��y�c�y� inhibe eder. OAT1, OAT3, OCT2 renal ta��y�c�lar�n substratlar� olan ajanlar (furosemid, penisilin gibi) veya hepatik ta��y�c�lar�n substratlar� olan ajanlar OATP1B1, OATP1B3, OCT1 (�rne�in atorvastatin, bosentan) veya BCRP substratlar� (metotreksat, rosuvastatin gibi) veya P-gp substratlar� (�rn., posakonazol) y�ksek maruziyete sahip olabilir ve bu nedenle birlikte dikkatle uygulanmal�d�r.
4.6. Gebelik ve laktasyon
Genel tavsiye Gebelik kategorisi: D
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol�
�ocuk do�urma potansiyeli olan kad�nlar enkorafenib tedavisi s�ras�nda ve son dozu takiben en az 1 ay s�reyle etkili do�um kontrol� kullanmal�d�r. Enkorafenib, hormonal kontraseptiflerin etkinli�ini azaltabilir (bkz. b�l�m 4.5). Bu nedenle hormonal kontrasepsiyon kullanan kad�n hastalar�n, enkorafenib tedavisi s�ras�nda ve son dozu takiben en az 1 ay s�reyle bariyer y�ntemi (�rn. kondom) gibi ek veya alternatif bir y�ntem kullanmalar� �nerilir.
Gebelik d�nemi
Gebe kad�nlarda enkorafenib kullan�m�na ili�kin veri bulunmamaktad�r. Hayvanlar �zerinde yap�lan
�al��malar �reme toksisitesi g�stermi�tir (bkz. b�l�m 5.3). Enkorafenib hamilelik s�ras�nda ve do�um kontrol� kullanmayan �ocuk do�urma potansiyeli olan kad�nlarda �nerilmez. Enkorafenib hamilelik s�ras�nda kullan�l�rsa veya hasta enkorafenib al�rken hamile kal�rsa, hasta fet�se y�nelik potansiyel tehlike konusunda bilgilendirilmelidir.
Laktasyon d�nemi
Enkorafenib veya metabolitlerinin insan s�t�ne ge�ip ge�medi�i bilinmemektedir. Yeni do�anlar/bebekler i�in bir risk g�z ard� edilemez. Emzirmenin durdurulup durdurulmayaca��na veya enkorafenib tedavisinin durdurulup durdurulmayaca��na, emzirmenin �ocuk i�in yarar� ve tedavinin anne i�in yarar� g�z �n�nde bulundurularak karar verilmelidir.
�reme yetene�i / Fertilite
Enkorafenib'in insanlarda do�urganl�k �zerindeki etkileri hakk�nda veri yoktur. Hayvanlardaki bulgulara dayanarak, enkorafenib kullan�m� �reme potansiyeli olan erkeklerde do�urganl��� etkileyebilir (bkz. b�l�m 5.3). Bunun klinik �nemi bilinmedi�inden, erkek hastalar bozulmu� spermatogenez i�in potansiyel risk konusunda bilgilendirilmelidir.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
Enkorafenib'in ara� veya makine kullanma yetene�i �zerinde min�r etkisi vard�r. Klinik �al��malar s�ras�nda enkorafenib ile tedavi edilen hastalarda g�rme bozukluklar� bildirilmi�tir. Hastalara, g�rme bozukluklar� veya ara� ve makine kullanma yeteneklerini etkileyebilecek ba�ka herhangi bir advers reaksiyon ya�arlarsa, ara� veya makine kullanmamalar� tavsiye edilmelidir (bkz. b�l�m 4.4 ve 4.8).
4.8. �stenmeyen etkiler
G�venlilik profilinin �zeti
Binimetinib (g�nde iki kez 45 mg oral) ile kombinasyon halinde enkorafenib'in (a��zdan g�nde bir kez 450 mg) g�venlili�i, BRAF V600 mutant rezeke edilmeyen veya metastatik melanomlu (bundan sonra havuzlanm�� Combo 450 pop�lasyonu olarak an�lacakt�r) 274 hastada de�erlendirilmi�tir. Faz II �al��malar� (CMEK162X2110 ve CLGX818X2109) ve bir Faz III �al��mas� (CMEK162B2301, B�l�m 1).
Rezeke edilemeyen veya metastatik melanomlu hastalarda �nerilen dozda (n = 274), binimetinib uygulanan enkorafenib ile tedavi edilen hastalarda meydana gelen en yayg�n advers reaksiyonlar (>%25) yorgunluk, bulant�, diyare, kusma, retina dekolman�, kar�n a�r�s�, artralji, kan kreatin kinaz art��� ve miyaljidir.
Binimetinib (g�nde iki kez 45 mg oral) ile kombinasyon halinde enkorafenib'in (oral olarak g�nde bir kez 300 mg) g�venlili�i, BRAF V600 mutant rezeke edilemeyen veya metastatik melanomlu (bundan sonra Combo 300 pop�lasyonu olarak an�lacakt�r) 257 hastada, Faz III �al��mas�na (CMEK162B2301, B�l�m 2) g�re de�erlendirilmi�tir. Binimetinib ile birlikte 300 mg enkorafenib ile tedavi edilen hastalarda meydana gelen en yayg�n advers reaksiyonlar (>%25), yorgunluk, bulant� ve diyare olmu�tur.
Enkorafenib tek ajan (g�nde bir kez 300 mg oral) g�venlik profili, rezeke edilemeyen veya metastatik BRAF V600-mutant melanomlu 217 hastan�n (bundan sonra havuzlanm�� enkorafenib 300 pop�lasyonu olarak an�lacakt�r) verilerine dayanmaktad�r. Enkorafenib 300 ile bildirilen en yayg�n advers ila� reaksiyonlar� (ADR'ler) (>%25), hiperkeratoz, alopesi, PPES, yorgunluk, d�k�nt�, artralji, kuru cilt, bulant�, miyalji, ba� a�r�s�, kusma ve ka��nt�d�r.
Enkorafenib'in (g�nde bir kez a��zdan 300 mg) setuksimab (K�B'�ne g�re dozlanm��t�r) ile g�venlili�i, BRAF V600E mutant metastatik kolorektal kanserli 216 hastada, faz III �al��mas� ARRAY-818-302'ye g�re de�erlendirilmi�tir. Bu pop�lasyonda bildirilen en yayg�n advers reaksiyonlar (>%25) �unlard�: yorgunluk, bulant�, ishal, akneiform dermatit, kar�n a�r�s�, artralji/kas- iskelet a�r�s�, i�tah azalmas�, d�k�nt� ve kusma.
Setuksimab ile kombinasyon halinde 300 mg enkorafenib ile tedavi edilen hastalarda herhangi bir advers reaksiyon kaynakl� t�m �al��ma ilac�n�n kesilme oran� %1.9'du.
Advers reaksiyonlar�n tablo halinde listesi
S�kl���n s�n�fland�r�lmas� i�in MedDRA s�kl�k kural� ve sistem organ s�n�f� veri taban� kullan�lm��t�r:
�ok yayg�n (≥ 1/10) Yayg�n (≥ 1/100 ila <1/10)
Yayg�n olmayan (≥ 1/1.000 ila <1/100) Seyrek (≥ 1/10.000 ila <1/1.000)
�ok seyrek (<1/10.000)
Bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor)
Her bir s�kl�k gruplamas�nda, advers reaksiyonlar azalan ciddiyet s�ras�na g�re sunulur.
Tablo 5: Advers reaksiyonlar
S�kl�k | Enkorafenib tek ajan 300 mg (n = 217) | Enkorafenib 450 mg, binimetinib ile kombinasyon halinde (n = 274) | Setuksimab ile kombinasyon halinde enkorafenib 300 mg (n = 216) |
�yi huylu, k�t� huylu ve tan�mlanmam�� neoplazmlar | |||
�ok yayg�n | Cilt papillomu* Melanositik nev�s |
| Melanositik nev�s |
Yayg�n | cuSCC Yeni Primer Melanom* | cuSCC Bazal h�creli karsinom* Cilt papillomu* | cuSCC Cilt papillomu Yeni Primer Melanom* |
Yayg�n olmayan | Bazal h�creli karsinom |
| Bazal h�creli karsinom |
Kan ve lenf sistemi hastal�klar� | |||
�ok yayg�n |
| Anemi |
|
Ba����kl�k sistemi hastal�klar� |
| ||
Yayg�n | A��r� duyarl�l�k | A��r� duyarl�l�k | A��r� duyarl�l�k |
Metabolizma ve beslenme bozukluklar� | |||
�ok yayg�n | ��tah azalmas� |
| ��tah azalmas� |
Psikolojik bozukluklar | |||
�ok yayg�n | �nsomnia |
| �nsomnia |
Sinir sistemi hastal�klar� | |||
�ok yayg�n | Ba� a�r�s�* Periferik n�ropati Disguzi* | Periferik n�ropati Ba� d�nmesi* Ba� a�r�s�* | Periferik n�ropati Ba� a�r�s�* |
Yayg�n | Y�z felci | Disguzi* | Ba� d�nmesi* Disguzi |
Yayg�n olmayan |
| Y�z felci |
|
G�z hastal�klar� | |||
�ok yayg�n |
| G�rme bozuklu�u* RPED |
|
Yayg�n |
| �veit* |
|
Yayg�n olmayan | �veit* |
|
|
Kardiyak hastal�klar | |||
Yayg�n | Supraventrik�ler ta�ikardi | Sol ventrik�l disfonksiyonu | Supraventrik�ler ta�ikardi |
Vask�ler hastal�klar |
| ||
�ok yayg�n |
| Hemoraji Hipertansiyon | Hemoraji |
Yayg�n |
| Ven�z tromboembolizm |
|
Gastrointestinal hastal�klar� | |||
�ok yayg�n | Mide bulant�s� Kusma* Kab�zl�k | Mide bulant�s� Kusma* Kab�zl�k Kar�n a�r�s�* Diyare* | Mide bulant�s� Kusma Kab�zl�k Kar�n a�r�s�* Diyare* |
Yayg�n |
| Kolit |
|
Yayg�n olmayan | Pankreatit* | Pankreatit* | Pankreatit* |
Deri ve deri alt� doku hastal�klar� | |||
�ok yayg�n | Palmar-plantar eritrodisestezi sendromu (PPES) Hiperkeratoz* D�k�nt�* Kuru cilt* Ka��nt�* Alopesi* Eritem Cilt hiperpigmentasyonu* | Hiperkeratoz* D�k�nt�* Kuru cilt* Ka��nt�* Alopesi* | Dermatit akneiform* D�k�nt�* Kuru cilt* Ka��nt�* |
Yayg�n | Dermatit akneiform* Cilt soyulmas� I���a duyarl�l�k* | Dermatit akneiform* Palmar-plantar eritrodisestezi sendromu (PPES) Eritem* | Cilt hiperpigmentasyonu Palmar-plantar eritrodisestezi sendromu (PPES) Hiperkeratoz* Alopesi |
|
| Pannik�lit* I���a duyarl�l�k* | Eritem |
Yayg�n olmayan |
|
| Cilt soyulmas� |
Kas-iskelet ve ba� dokusu hastal�klar� | |||
�ok yayg�n | Artralji Miyalji Eksremitede a�r� S�rt a�r�s� | Artralji Kas hastal�klar�/ Miyalji Eksremitede a�r� S�rt a�r�s� | Artralji/Kas-iskelet a�r�s�* Miyopati/Kas bozuklu�u* Ekstremitede a�r� S�rt a�r�s� |
Yayg�n | Artrit * |
|
|
Yayg�n olmayan |
| Rabdomiyoliz |
|
B�brek ve idrar hastal�klar� | |||
Yayg�n | B�rek yetmezli�i | B�rek yetmezli�i | B�rek yetmezli�i |
Genel bozukluklar ve uygulama yerine ili�kin durumlar | |||
�ok yayg�n | Yorgunluk * Ate�* | Yorgunluk * Ate�* Periferal �dem | Yorgunluk * Ate�* |
Ara�t�rmalar |
| ||
�ok yayg�n | Gama-glutamil transferaz (GGT) art���* | Kan kreatin fosfokinaz art��� Gama-glutamil transferaz (GGT) art���* Transaminaz art���* |
|
Yayg�n | Transaminaz art���* Kan kreatinin art���* Lipaz art��� | Kan alkalin fosfataz art��� Kan kreatinin art���* Amilaz art��� Lipaz art��� | Kan kreatinin art���* Transaminaz art���* |
Yayg�n olmayan | Amilaz art��� |
| Amilaz art��� Lipaz art��� |
beyin kanamas� dahil olmak �zere �e�itli b�lgelerdeki kanamay� i�erir
Enkorafenib, CMEK162B2301-B�l�m 2 �al��mas�nda g�nde iki kez 45 mg binimetinib ile kombinasyon halinde g�nde bir kez 300 mg dozda kullan�ld���nda (Combo 300), a�a��daki advers reaksiyonlar i�in s�kl�k kategorisi havuzlanm�� Combo 450 pop�lasyonuna k�yasla daha d���kt�r: anemi, periferik n�ropati, kanama, hipertansiyon, ka��nt� (yayg�n) ve kolit, amilaz art��� ve lipaz art��� (yayg�n olmayan).
Se�ilmi� advers reaksiyonlar�n tan�m�
Deri maligniteleri
Kutan�z skuam�z h�creli karsinom Melanom
Havuzlanm�� Combo 450 pop�lasyonunda, hastalar�n %3.3'�nde (9/274) keratoakantomlar dahil cuSCC g�zlendi. �lk cuSCC olay�n�n ba�lamas�na kadar ge�en medyan s�re (t�m dereceler) 6,5 ayd� (1,0 ila 22.8 ay aral���nda).
Havuzlanm�� encorafenib 300 pop�lasyonunda, cuSCC hastalar�n %7.4'�nde (16/217) rapor edilmi�tir. cuSCC geli�tiren Faz III �al��mas�ndaki (CMEK162B2301) hastalar i�in, ilk cuSCC olay�n�n (t�m dereceler) ba�lamas�na kadar ge�en medyan s�re 2.3 ayd� (0,3 ila 12,0 ay aral���nda).
Kolorektal kanser
Setuksimab ile kombinasyon halinde 300 mg enkorafenib ile tedavi edilen hastalarda, hastalar�n
%1.4'�nde (3/216) keratoakantom dahil cuSCC g�zlenmi�tir. �lk cuSCC olay�na kadar ge�en s�re (t�m dereceler) bu 3 hasta i�in 0,5, 0,6 ve 3,6 ayd�.
Yeni birincil melanom Melanom
Havuzlanm�� enkorafenib 300 pop�lasyonunda, hastalar�n %4.1'inde (9/217) yeni primer melanom olaylar� meydana geldi ve hastalar�n %1.4'�nde (3/217) Derece 1, hastalar�n %2.1'inde (4/217) Derece 2 olarak rapor edildi. hastalar�n %0,5'inde (1/217) Derece 3 ve hastalar�n %0,5'inde (1/217) Derece 4't�r.
Kolorektal kanser
Setuksimab ile kombinasyon halinde 300 mg enkorafenib ile tedavi edilen hastalarda, hastalar�n
%1.9'unda (4/216) yeni primer melanom olaylar� meydana geldi ve hastalar�n %0.9'unda (2/216) Derece 2 ve %0.9'unda Derece 3 olarak bildirildi (2/216).
Ok�ler olaylar Melanom
Havuzlanm�� Combo 450 pop�lasyonunda, hastalar�n %4,4'�nde (12/274) �veit bildirilmi�tir ve
%0,4'�nde (1/274) Derece 1, %3,6's�nda (10/274) Derece 2 ve %0,4'�nde Derece 3 olmu�tur. (1/274). Bulan�k g�rme ve g�rme keskinli�inde azalma dahil g�rme bozuklu�u hastalar�n %21.5'inde (59/274) meydana geldi. �veit ve g�rme bozuklu�u genellikle geri d�n���ml�yd�.
RPED hastalar�n %29.6's�nda (81/274) meydana geldi, bunlar�n �o�unda Derece 1-2 ve %1.8'inde (5/274) Derece 3 olaylar vard�.
�al��ma CMEK162B2301-B�l�m 2'de, Combo 300 kolunda, %0,4 (1/257) Derece 4 olay� olan hastalar�n %12,5'inde (32/257) RPED g�zlenmi�tir.
Sol ventrik�l disfonksiyonu (LVD)
Melanom hastalar�nda enkorafenib binimetinib ile kombinasyon halinde kullan�ld���nda LVD rapor edilmi�tir (bak�n�z binimetinib K�B, b�l�m 4.8).
Kanama Melanom
Havuzlanm�� Combo 450 pop�lasyonundaki hastalar�n %17,9'unda (49/274) hemorajik olaylar g�zlenmi�tir. Olaylar�n �o�u Derece 1 veya 2 (%14.6) ve %3.3'� Derece 3-4 olaylard�. Az say�da hastada doz kesintileri veya doz azaltmalar� gerekmi�tir (%0.7 veya 2/274). Hemorajik olaylar hastalar�n %1,1'inde (3/274) tedavinin kesilmesine neden olmu�tur. En s�k g�r�len hemorajik olaylar hastalar�n %3.3'�nde (9/274) hemat�ri, %2.9'unda (8/274) rektal hemoraji ve hastalar�n %2.9'unda (8/274) hematokezi idi. Bir hastada e�zamanl� �l�m nedeni olarak �oklu organ yetmezli�i ile �l�mc�l mide �lseri kanamas� meydana geldi.
Hastalar�n %1.5'inde (4/274) beyin kanamas� rapor edilmi� ve 3 hastada �l�mc�l sonu� al�nm��t�r. T�m olaylar, yeni veya ilerleyici beyin metastazlar� ortam�nda meydana geldi.
�al��ma CMEK162B2301-B�l�m 2'de, Combo 300 kolunda, hastalar�n %6,6's�nda (17/257) hemorajik olaylar g�zlenmi� ve hastalar�n %1.6's�nda (4/257) Derece 3-4 olmu�tur.
Kolorektal kanser
Enkorafenib ile tedavi edilen hastalar�n %21.3'�nde (46/216) hemorajik olaylar g�zlenmi�tir. Setuksimab ile kombinasyon halinde 300 mg; Hastalar�n %1.4'� (3/216) Derece 3 olaylard� ve bir �l�mc�l vaka rapor edildi. Hastalar�n %1.9'unda (4/216) doza ara verilmesi veya doz azalt�lmas� gerekmi�tir. Hemorajik olaylar 1 hastada (%0.5) tedavinin kesilmesine neden oldu.
En s�k g�r�len hemorajik olaylar hastalar�n %6.9'unda (15/216) burun kanamas�, %2.8'inde (6/216) hematokezya, %2.8'inde (6/216) rektal kanama ve %2.8'inde (6/216) hemat�ri idi.
Hipertansiyon
Melanom hastalar�nda enkorafenib binimetinib ile kombinasyon halinde kullan�ld���nda hipertansiyon bildirilmi�tir (bak�n�z binimetinib K�B, b�l�m 4.8).
Ven�z tromboembolizm (VTE)
Melanom hastalar�nda enkorafenib binimetinib ile kombinasyon halinde kullan�ld���nda VTE rapor edilmi�tir (bak�n�z binimetinib K�B, b�l�m 4.8).
Pankreatit Melanom
Havuzlanm�� Combo 450 pop�lasyonunda, �o�unlukla asemptomatik olan pankreatik enzim y�ksekli�i bildirilmi�tir. Amilaz ve lipaz y�kselmeleri s�ras�yla hastalar�n %3.3'�nde (9/274) ve
%5.1'inde (14/274) rapor edilmi�tir. Hastalar�n %0.7'sinde (2/274) pankreatit bildirilmi�tir. Her iki hasta da 3. Derece olaylar ya�ad�. Pankreatit, hastalar�n 1/274'�nde (%0.4) doz kesintisine neden oldu.
Kolorektal kanser
Setuksimab ile kombinasyon halinde 300 mg enkorafenib ile tedavi edilen pop�lasyonda, 1 hastada (%0.5) lipaz ve amilaz ile birlikte derece 3 pankreatit olaylar� rapor edilmi� ve dozun kesilmesine neden olmu�tur.
Dermatolojik reaksiyonlar D�k�nt�
Melanom
Havuzlanm�� Combo 450 pop�lasyonunda, hastalar�n %19.7'sinde (54/274) d�k�nt� meydana geldi. Olaylar�n �o�u hafifti ve hastalar�n %0.7'sinde (2/274) Derece 3 veya 4 olaylar rapor edildi. D�k�nt�, hastalar�n %0.4'�nde (1/274) ilac�n kesilmesine ve hastalar�n %1.1'inde (3/274) dozun kesilmesine veya doz de�i�ikli�ine yol a�m��t�r.
Havuzlanm�� enkorafenib 300 pop�lasyonunda, hastalar�n %43.3'�nde (94/217) d�k�nt� bildirilmi�tir. Olaylar�n �o�u hafifti ve hastalar�n %4,6's�nda (10/217) Derece 3 veya 4 olaylar rapor edildi. D�k�nt�, hastalar�n %0,5'inde (1/217) ilac�n kesilmesine ve hastalar�n %7,4'�nde (16/217) dozun kesilmesine veya doz de�i�ikli�ine yol a�m��t�r.
Kolorektal kanser
Setuksimab ile kombinasyon halinde 300 mg enkorafenib ile tedavi edilen hastalarda, hastalar�n
%30,6's�nda (66/216) d�k�nt� meydana gelmi�tir. Olaylar�n �o�u hafifti ve hastalar�n %0.5'inde (1/216) Derece 3 olay rapor edildi. D�k�nt�, hastalar�n %0.5'inde (1/216) doz kesintisine yol a�m��t�r.
Palmar-plantar eritrodisestezi sendromu (PPES) Melanom
PPES, havuzlanm�� Combo 450 pop�lasyonundaki hastalar�n %6,2'sinde (17/274) rapor edilmi�tir. T�m PPES advers reaksiyonlar�, Derece 1 (%3.3) veya Derece 2 (%2.9) idi. Hastalar�n %1,1'inde (3/274) doz kesintisi veya doz de�i�ikli�i meydana geldi.
Pivotal �al��man�n 2. K�sm�ndaki Combo 300 kolunda, hastalar�n %0,4'�nde (1/257) bildirilen Derece 3 olan hastalar�n %3,9'unda (10/257) PPES g�zlenmi�tir.
Havuzlanm�� enkorafenib 300 pop�lasyonunda, hastalar�n %51.6's�nda (112/217) PPES bildirilmi�tir. Olaylar�n �o�u hafif-orta derecedeydi: Hastalar�n %12.4'�nde (27/217) Derece 1, hastalar�n
%26.7'sinde (58/217) Derece 2 ve hastalar�n %12.4'�nde (27/217) Derece 3. PPES, hastalar�n
%4.1'inde (9/217) ilac�n kesilmesine ve hastalar�n %23.0'�nda (50/217) dozun kesilmesine veya doz de�i�ikli�ine yol a�m��t�r.
Kolorektal kanser
Setuksimab ile kombinasyon halinde 300 mg enkorafenib ile tedavi edilen pop�lasyonda, hastalar�n
%5.1'inde (11/216) PPES bildirilmi�tir. PPES advers reaksiyonlar�n�n �o�u, %3.7 (8/216) i�inde Derece 1 idi. Hastalar�n %0,9'unda (2/216) Derece 2 olaylar ve hastalar�n %0,5'inde (1/216) Derece 3 olaylar bildirilmi�tir. Doz kesintisi, doz modifikasyonu veya tedavinin kesilmesi gerekmedi.
Dermatit akneiform Melanom
Enkorafenib, binimetinib ile kombinasyon halinde kullan�ld���nda dermatit akneiform bildirilmi�tir (bak�n�z binimetinib K�B, b�l�m 4.8).
Kolorektal kanser
Setuksimab ile kombinasyon halinde 300 mg enkorafenib ile tedavi edilen hastalarda, dermatit akneiform, hastalar�n %33.3'�nde (72/216) meydana geldi ve �o�unlukla Derece 1 (hastalar�n %25.5'i (55/216) veya 2'si (%6.9) (15 / 216) hasta). Hastalar�n %2.3'�nde (5/216) doz azalt�m� veya kesilmesi bildirilmi�tir. Tedavinin kesilmesi bildirilmemi�tir. Dermatit akneiform genellikle geri d�n���ml�yd�.
I���a duyarl�l�k Melanom
Havuzlanm�� Combo 450 pop�lasyonunda, hastalar�n %4.0'�nda (11/274) ����a duyarl�l�k g�zlenmi�tir. Olaylar�n �o�u Derece 1-2 idi, Derece 3 hastalar�n %0.4'�nde (1/274) rapor edildi ve hi�bir olay tedavinin kesilmesine yol a�mad�. Hastalar�n %0.4'�nde (1/274) doz kesintisi veya doz de�i�ikli�i bildirilmi�tir.
Havuzlanm�� enkorafenib 300 pop�lasyonunda, hastalar�n %4,1'inde (9/217) ����a duyarl�l�k bildirilmi�tir. T�m olaylar S�n�f 1-2 idi. Hi�bir olay kesilmeyi, doz de�i�ikli�ini veya ara vermeyi gerektirmez.
Y�z felci Melanom
Havuzlanm�� Combo 450 pop�lasyonunda, hastalar�n %0,4'�nde (1/274) Derece 3 dahil olmak �zere hastalar�n %0,7'sinde (2/274) y�z parezi meydana geldi. Olaylar geri d�n���ml�yd� ve hi�bir olay tedavinin kesilmesine yol a�mad�. Hastalar�n %0.4'�nde (1/274) doz kesintisi veya modifikasyonu bildirilmi�tir.
Havuzlanm�� enkorafenib 300 pop�lasyonunda, hastalar�n %7,4'�nde (16/217) fasiyal parezi g�zlendi. Olaylar�n �o�u hafif-orta �iddetteydi: Derece 1'de %2,3 (5/217); Hastalar�n %3.7'sinde (8/217) Derece 2 ve hastalar�n %1.4'�nde (3/217) Derece 3. �lk fasiyal parezi olay�n�n ba�lamas�na kadar ge�en medyan s�re 0.3 ayd� (aral�k 0.1 ila 12.1 ay). Y�z parezi genellikle geri d�n���ml�yd� ve %0.9 (2/217) oran�nda tedavinin kesilmesine neden oldu. Hastalar�n %3.7'sinde (8/217) doz kesintisi veya modifikasyonu ve %5.1'inde (11/217) kortikosteroidler dahil semptomatik tedavi bildirilmi�tir.
Kreatin kinaz (CK) y�kselmesi ve rabdomiyoliz
Melanom hastalar�nda binimetinib ile kombinasyon halinde enkorafenib kullan�ld���nda CK y�kselmesi ve rabdomiyoliz meydana gelmi�tir (bak�n�z binimetinib K�B, b�l�m 4.8).
B�brek yetmezli�i Melanom
Havuzlanm�� Combo 450 pop�lasyonunda, Combo 450 mg ile tedavi edilen hastalar�n %6.2'sinde
(17/274) hafif, �o�unlukla 1. Derece, asemptomatik kan kreatinin y�kselmesi kaydedildi. Derece 3 veya 4 y�kselme insidans� %0,7 (2/274) idi. Akut b�brek hasar� ve b�brek yetmezli�i dahil b�brek yetmezli�i olaylar�, enkorafenib ve binimetinib ile tedavi edilen hastalar�n %3.3'�nde (9/274) ve hastalar�n %2.2'sinde (6/274) Derece 3 veya 4 olaylar bildirilmi�tir. B�brek yetmezli�i, doz kesintisi, rehidrasyon ve di�er genel destekleyici �nlemlerle genellikle geri d�nd�r�lebilirdi.
Kolorektal kanser
Setuksimab ile kombinasyon halinde 300 mg enkorafenib ile tedavi edilen hastalar�n %2.8'inde (6/216) kan kreatinin y�kselmesi bildirilmi�tir. Derece 4'teki bir olay d���nda hepsi hafifti. B�brek yetmezli�i olaylar� Derece 3 veya 4 idi ve hastalar�n %1,9'unda (4/216) akut b�brek hasar� ve hastalar�n %0,5'inde (1/216) b�brek yetmezli�i olarak rapor edildi.
Karaci�er laboratuvar anormalli�i Melanom
Havuzlanm�� Combo 450 pop�lasyonunda rapor edilen karaci�er laboratuvar anormallikleri insidans� a�a��da listelenmi�tir:
Artan transaminazlar: genel olarak %15,7 (43/274) – Derece 3-4: %5,5 (15/274)
4.9. Doz a��m� ve tedavisi
Belirtiler
G�nde bir kez 600 ila 800 mg aras�ndaki enkorafenib dozlar�nda, 14 hastan�n 3'�nde b�brek fonksiyon bozuklu�u (Derece 3 hiperkreatinemi) g�zlenmi�tir. Uygulanan en y�ksek doz, 1 g�n boyunca g�nde iki kez 600 mg dozda (toplam doz 1200 mg) enkorafenib alan bir hastada doz hatas� olarak meydana geldi. Bu hasta taraf�ndan bildirilen advers reaksiyonlar, 1. Derece bulant�, kusma ve bulan�k g�rme olaylar�d�r; sonradan hepsi d�zelmi�tir.
Tedavi
Doz a��m� i�in �zel bir tedavi yoktur.
Enkorafenib plazma proteinlerine orta d�zeyde ba�land���ndan, enkorafenib ile doz a��m� tedavisinde hemodiyalizin etkisiz olmas� muhtemeldir. Enkorafenib i�in bilinen bir antidot yoktur. Doz a��m� durumunda, enkorafenib tedavisine ara verilmeli ve b�brek fonksiyonu ve advers reaksiyonlar izlenmelidir. Gerekti�inde semptomatik tedavi ve destekleyici bak�m sa�lanmal�d�r.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Antineoplastik ila�, protein kinaz inhibit�rleri ATC kodu: L01EC03
Etki mekanizmas�
Enkorafenib, g��l� ve olduk�a se�ici bir ATP-rekabet�i k���k molek�l RAF kinaz inhibit�r�d�r. Enkorafenibin BRAF V600E, BRAF ve CRAF enzimlerine kar�� inhibe edici konsantrasyon 50 (IC50) s�ras�yla 0.35, 0.47 ve 0.30 nM olarak belirlenmi�tir. Enkorafenib ayr��ma yar� �mr� >30 saattir ve uzun s�reli pERK inhibisyonu ile sonu�lanm��t�r. Enkorafenib, �e�itli mutasyona u�ram�� BRAF kinaz formlar�n� (V600E, D ve K) eksprese eden t�m�r h�crelerinde RAF/MEK/ERK yolunu bask�lar. Spesifik olarak, enkorafenib in vitro ve in vivo BRAF V600E, D ve K mutant melanom h�cre b�y�mesini ve BRAF V600E mutant kolorektal kanser h�cresi b�y�mesini inhibe eder. Enkorafenib, yaban�l tip BRAF eksprese eden h�crelerde RAF/MEK/ERK sinyalini inhibe etmez.
Binimetinib ile kombinasyon
Enkorafenib ve binimetinib (MEK inhibit�r�, bkz. binimetinib K�B, b�l�m 5.1), MAPK yolunu inhibe ederek daha y�ksek anti-t�m�r aktivitesi ile sonu�lan�r.
Ek olarak, enkorafenib ve binimetinib kombinasyonu, in vivo olarak BRAF V600E mutant insan melanom ksenograftlar�nda direncin ortaya ��kmas�n� �nlemi�tir.
Setuksimab ile kombinasyon
BRAF mutant� CRC'nin RAF inhibit�rlerine direncinin ana mekanizmalar�ndan biri, BRAF arac�l���yla sinyal iletimini atlayarak EGFR'nin yeniden aktivasyonu olarak tan�mlanm��t�r. Bir BRAF inhibit�r�, �rn. enkorafenib ve EGFR'yi hedefleyen ajanlar�n kombinasyonlar�, �rn. setuksimab�n klinik olmayan modellerde anti-t�m�r etkinli�ini iyile�tirdi�i g�sterilmi�tir
Klinik etkililik ve g�venlilik
BRAF V600 mutant rezeke edilemeyen veya metastatik melanom
Enkorafenib ile binimetinib kombinasyonunun g�venlili�i ve etkilili�i, bir BRAF testi kullan�larak tespit edilen rezeke edilemeyen veya metastatik BRAF V600 E veya K mutant� melanom olan hastalarda 2 b�l�ml� Faz III, randomize (1:1:1) aktif kontroll�, a��k etiketli, �ok merkezli bir �al��mada de�erlendirilmi�tir (�al��ma CMEK162B2301). Hastalarda histolojik olarak do�rulanm�� kutan�z veya bilinmeyen primer melanom vard�r, ancak uveal veya mukozal melanomu olanlar �al��ma d��� b�rak�lm��t�r. Hastalar�n, rezeke edilemeyen lokal olarak ilerlemi� veya metastatik hastal�k i�in �nceden adjuvan tedavi ve bir �nceki imm�noterapi s�ras� almalar�na izin verilmi�tir. BRAF/MEK inhibit�rleri ile �nceden tedaviye izin verilmemi�tir.
�al��ma CMEK162B2301, B�l�m 1
B�l�m 1'de, �al��madaki hastalar g�nde iki kez a��zdan 45 mg binimetinib art� a��zdan g�nde 450 mg enkorafenib (Combo 450, n = 192), a��zdan g�nde 300 mg enkorafenib (bundan sonra Enco 300, n = 194 olarak an�lacakt�r) veya g�nde iki kez oral yoldan 960 mg vemurafenib (bundan sonra Vem, n = 191 olarak an�lacakt�r) almak �zere randomize edilmi�tir. Tedavi, hastal�k progresyonuna veya
kabul edilemez toksisiteye kadar devam etmi�tir. Randomizasyon, Amerikan Ortak Kanser Komitesi (AJCC) A�amas� (IIIB, IIIC, IVM1a veya IVM1b, IVM1c'ye kar��) ve Do�u ��birli�i Onkoloji Grubu (ECOG) performans durumu (0'a 1) ve rezeke edilemeyen veya metastatik hastal�k i�in �nceki imm�noterapi taraf�ndan katmanlara ayr�lm��t�r. (evet ya da hay�r)
Primer etkililik sonlan�m noktas�, Combo 450'nin vemurafenib ile kar��la�t�r�ld��� ve k�r bir ba��ms�z inceleme komitesi taraf�ndan de�erlendirildi�i progresyonsuz sa�kal�m (PFS) olmu�tur. Ara�t�rmac�lar taraf�ndan de�erlendirildi�i �ekliyle PFS (ara�t�rmac� de�erlendirmesi) destekleyici bir analizdir. �lave ikincil sonlan� noktas�, Combo 450'nin enco 300 ile PFS kar��la�t�rmas�n� i�emektedir. Combo 450 ile vemurafenib veya Enco 300 aras�ndaki di�er ikincil etkinlik kar��la�t�rmalar�, BIRC ve ara�t�rmac� de�erlendirmesi taraf�ndan de�erlendirildi�i �ekliyle genel sa� kal�m (OS), objektif yan�t oran� (ORR), yan�t s�resi (DoR) ve hastal�k kontrol oran�n� (DCR) i�eriyordur.
Hastalar�n medyan ya�� 56 (aral�k 20-89), %58'i erkek, %90'� beyaz �rktand� ve hastalar�n %72'sinin ba�lang�� ECOG performans durumu 0'd�. �o�u hastada metastatik hastal�k vard� (%95) ve Evre IVM1c idi. (%64); Hastalar�n %27'sinde ba�lang�� serum laktat dehidrogenaz (LDH) y�kselmi� ve hastalar�n %45'inde ba�lang��ta t�m�r tutulumu olan en az 3 organ ve %3.5'inde beyin metastaz� vard�. 27 hasta (%5) �nceden kontrol noktas� inhibit�rleri (anti-PD1/PDL1 veya ipilimumab) alm��t� (Combo 450 kolunda 8 hasta (%4); vemurafenib kolunda 7 hasta (%4); Enco 300 kolunda 12 hasta
(6 %) metastatik ortamda 22 hasta (Combo 450 kolunda 6 hasta; vemurafenib kolunda 5 hasta; Enco
300 kolunda 11 hasta) ve adjuvan ortamda 5 hasta (Combo 450 kolunda 2 hasta; vemurafenib kolunda
2 hasta dahil) ; Enco 300 kolunda 1 hasta.
Medyan maruziyet s�resi Combo 450 ile tedavi edilen hastalarda 11.7 ay, 300 mg ekcorafenib ile tedavi edilen hastalarda 7.1 ay ve vemurafenib ile tedavi edilen hastalarda 6.2 ay olmu�tur. Combo 450 i�in medyan r�latif doz yo�unlu�u (RDI), binimetinib i�in %99.6 ve enkorafenib i�in %100 idi; medyan RDI, Enco 300 i�in %86,2 ve vemurafenib i�in %94.5 idi.
CMEK162B2301 �al��mas�n�n 1. B�l�m�, vemurafenib ile tedavi edilen hastalara k�yasla Combo 450 ile tedavi edilen hastalarda PFS'de istatistiksel olarak anlaml� bir iyile�me g�stermi�tir. Tablo 4 ve �ekil 1, k�r bir ba��ms�z radyoloji komitesi taraf�ndan verilerin merkezi olarak g�zden ge�irilmesine dayanan PFS ve di�er etkinlik sonu�lar�n� �zetlemektedir.
Ara�t�rmac� de�erlendirmesine dayal� etkinlik sonu�lar�, ba��ms�z merkezi de�erlendirme ile tutarl�yd�. Katmanla�t�r�lmam�� alt grup analizleri, ba�lang��ta LDH, ECOG performans durumu ve AJCC a�amas� dahil olmak �zere Combo 450 lehine nokta tahminleri g�sterdi.
Tablo 6: �al��ma CMEK162B2301, B�l�m 1: Progresyonsuz sa� kal�m ve onaylanm�� genel yan�t sonu�lar� (ba��ms�z merkezi inceleme)
| Enkorafenib + binimetinib n = 192 (Combo 450) | Enkorafenib
n = 194 (Enco 300) | Vemurafenib
n = 191 (Vem) |
Son tarih: 19 May�s 2016 | |||
PFS (birincil analiz) | |||
Olaylar�n say�s� (�lerleyen hastal�k (PD)) (%) |
98 (51.0) |
96 (49.5) |
106 (55.5) |
Ortalama, ay (%95 CI) | 14.9 (11.0, 18.5) | 9.6 (7.5,14.8) | 7.3 (5.6, 8.2) |
HR (%95 CI) (vs Vem) p de�eri (katmanl� log- a�amas�) | 0.54 (0.41, 0.71) < 0.001 |
|
|
HR (%95 CI) (vs. Vem) Nominal p-de�eri |
| 0.68 (0.52, 0.90) 0.007 |
|
HR (%95 CI) (vs Enco 300) p de�eri (katmanl� log- a�amas�) | 0.75 (0.56, 1.00) 0.051 |
|
|
Onaylanm�� genel yan�tlar | |||
Genel yan�t oran�, n (%) (95 % CI) | 121 (63.0) (55.8, 69.9) | 98 (50.5) (43.3, 57.8) | 77 (40.3) (33.3, 47.6) |
CR, n (%) | 15 (7.8) | 10 (5.2) | 11 (5.8) |
PR, n (%) | 106 (55.2) | 88(45.4) | 66 (34.6) |
SD, n (%) | 46 (24.0) | 53(27.3) | 73 (38.2) |
DCR, n (%) (%95 CI) | 177 (92.2) (87.4, 95.6) | 163 (84.0) (78.1, 88.9) | 156 (81.7) (75.4, 86.9) |
Yan�t s�resi | |||
Ortalama, ay (%95 CI) | 16.6 (12.2, 20.4) | 14.9 (11.1, NE) | 12.3 (6.9, 16.9) |
G�ncellenmi� analiz, son tarih: 07 Kas�m 2017 | |||
PFS | |||
Olaylar�n say�s� (ilerlemi� hastal�k) (%) | 113 (58.9) | 112 (57.7) | 118 (61.8) |
Ortalama ay (%95 CI) | 14.9 (11.0, 20.2) | 9.6 (7.4,14.8) | 7.3 (5.6, 7.9) |
HR (%95 CI) (vs. Vem) Nominal p-de�eri | 0.51 (0.39, 0.67) <0.001 |
|
|
HR (%95 CI) (vs. Vem) Nominal p-de�eri |
| 0.68 (0.52, 0.88) 0.0038 |
|
HR (%95 CI) (vs Enco 300) Nominal p-de�eri | 0.77 (0.59,1.00) 0.0498 |
|
|
CI = g�ven aral���; CR = tam yan�t; DCR = hastal�k kontrol oran� (CR+PR+SD+Non-CR/Non-PD; Non- CR/Non-PD sadece CR'ye ula�amayan veya PD'si olan hedef lezyonu olmayan hastalar i�in ge�erlidir); HR
= risk oran�; NE = tahmin edilemiyor; PFS = progresyonsuz sa� kal�m; PR = k�smi yan�t; SD = stabil hastal�k. Vem = vemurafenib.
�ekil 1: �al��ma CMEK162B2301, B�l�m 1: Kaplan-Meier ba��ms�z merkezi incelemeye g�re progresyonsuz sa� kal�m grafi�i (son tarih 19 May�s 2016)
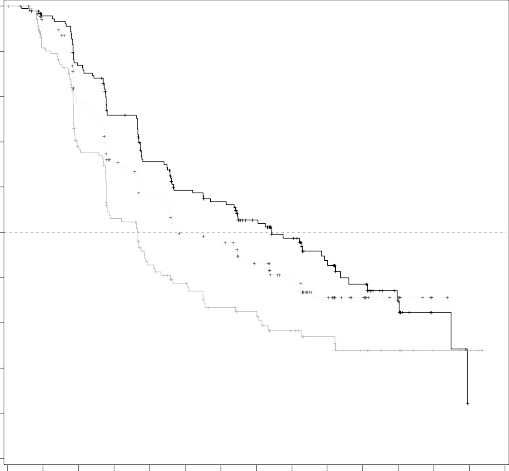
Median PFS (months) 14.9 9.6 7.3
100
90
80
Probability of Progression Free Survival(%)
70
60
50
40
30
20
10
0
0 2 4 6 8 10 12 14 16 18 20 22 24 26 28
Time (months)
|
| ||||||||||||||
| |||||||||||||||
| |||||||||||||||
�al��ma CMEK162B2301 B�l�m 1'in (son tarih 07 Kas�m 2017) bir ara OS analizi, vemurafenib ile kar��la�t�r�ld���nda Combo 450 i�in OS'de istatistiksel olarak anlaml� bir geli�me g�stermi�tir (bkz. Tablo 5 ve �ekil 2).
Her tedavi kolundaki hastalar�n benzer bir oran�, daha sonra kontrol noktas� inhibit�rleriyle, esas olarak pembrolizumab, nivolumab ve ipilimumab ile tedavi g�rm��t�r (%34,4 Combo 450 kolu,
%36,1 enkorafenib kolu, %39,8 vemurafenib kolu).
Tablo 7: �al��ma CMEK162B2301, B�l�m 1: Genel sa� kal�m ara sonu�lar� (son tarih: 7 Kas�m 2017)
| Enkorafenib + binimetinib n = 192 (Combo 450) | Enkorafenib n = 194 (Enco 300) | Vemurafenib n = 191 (Vem) |
OS | |||
Olaylar�n say�s� (%) | 105 (54.7) | 106 (54.6) | 127 (66.5) |
Ortalama ay | 33.6 | 23.5 | 16.9 |
(%95 CI) | (24.4, 39.2) | (19.6, 33.6) | (14.0, 24.5) |
12 ayda sa� kal�m | 75.5% | 74.6% | 63.1% |
(%95 CI) | (68.8, 81.0) | (67.6, 80.3) | (55.7, 69.6) |
24 ayda sa� kal�m | 57.6% | 49.1% | 43.2% |
(%95 CI) | (50.3, 64.3) | (41.5, 56.2) | (35.9, 50.2) |
HR (%95 CI) (vs Vem) | 0.61 (0.47, 0.79) |
|
|
p-de�eri ((katmanl� log- | < 0.0001 | ||
a�amas�) |
| ||
HR (95 % CI) (vs. Enco 300) | 0.81 (0.61,1.06) |
|
|
p-de�eri ((katmanl� log- | 0.061 | ||
a�amas�) |
| ||
�ekil 2: �al��ma CMEK162B2301, B�l�m 1: Kaplan-Meier Genel sa� kal�m (son tarih: 7 Kas�m 2017)
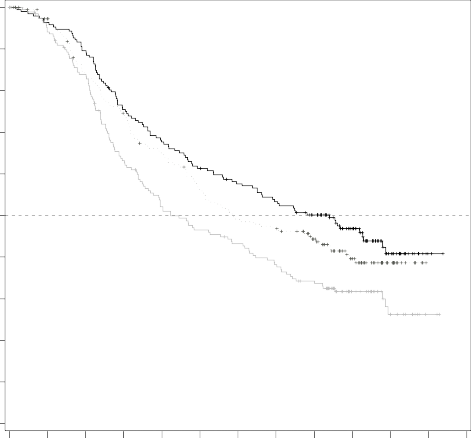
Median OS (months) 33.6 23.5 16.9
| ||||||||||||
| ||||||||||||
Ya�am Kalitesi (QoL) (son tarih: 19 May�s 2016)
Sa�l�kla ilgili Ya�am Kalitesi, i�levsellik, melanom semptomlar� ve tedaviye ba�l� advers reaksiyonun hasta taraf�ndan bildirilen sonu�lar� (PRO) �l��mlerini ara�t�rmak i�in Kanser Tedavisinin Fonksiyonel De�erlendirilmesi-Melanom (FACT M), Avrupa kanser ara�t�rma ve tedavi organizasyon grubu temel ya�am kalitesi anketi (EORTC QLQ C30) ve EuroQoL 5 Boyut-5 D�zey s�nav� (EQ 5D 5L) kullan�ld�. Di�er tedavilere k�yasla Combo 450 ile tedavi edilen hastalarda FACT M ve EORTC QLQ C30'da %10'luk kesin bir bozulma �nemli �l��de gecikmi�tir. FACT M skorunda kesin %10 bozulmaya kadar ge�en medyan s�re, Combo 450 kolunda ula��lmad� ve fark 0.46 (%95 CI: 0.29, 0.72) i�in bir HR ile vemurafenib kolunda 22.1 ayd� (%95 CI: 15.2, NE). EORTC QLQ C30 skorunda %10'luk kesin bozulmaya kadar ge�en s�renin analizi, benzer sonu�lar verdi.
Combo 450 alan hastalar, t�m ziyaretlerde ba�lang�� EQ-5D-5L indeks skorundan ortalama de�i�iklikte herhangi bir de�i�iklik veya hafif bir iyile�me bildirirken, vemurafenib veya enkorafenib alan hastalar t�m ziyaretlerde d����ler bildirmi�tir (istatistiksel anlaml� farkl�l�klar ile). Skordaki zaman i�indeki de�i�imin de�erlendirilmesi, EORTC QLQ C30 i�in ve FACT M i�in t�m ziyaretlerde
ayn� e�ilimi verdi.
�al��ma CMEK162B2301, B�l�m 2
CMEK162B2301 �al��mas�n�n 2. B�l�m�, binimetinibin enkorafenib ve binimetinib kombinasyonuna katk�s�n� de�erlendirmek i�in tasarlanm��t�r.
G�nde iki kez a��zdan 45 mg binimetinib (Combo 300, n = 258) ile kombinasyon halinde kullan�lan g�nl�k 300 mg enkorafenib i�in PFS, Enco 300 i�in PFS (n = 280, B�l�m 1'den 194 hasta ve B�l�m'den 86 hasta dahil) kar��la�t�r�lm��t�r. 2). B�l�m 2'ye kay�t, t�m B�l�m 1 hastalar� randomize edildikten sonra ba�lad�.
9 Kas�m 2016 kapan�� tarihindeki �n B�l�m 2 verileri, Combo 300 i�in 9.2 aya (%95 CI: 7.4, 11.0) k�yasla 12.9 ayl�k (%95 CI: 10.1, 14.0) iyile�tirilmi� medyan PFS tahmini ile binimetinib'in katk�s�n� g�stermi�tir, Enco 300 (B�l�m 1 ve 2) i�in ba��ms�z merkezi incelemesi (BIRC) i�in. Ara�t�rmac� de�erlendirmesi i�in benzer sonu�lar g�zlemlendi.
BIRC i�in teyit edilen ORR, Combo 300 i�in %65.9 (%95 GA: 59.8, 71.7) ve Enco 300 i�in %50,4 (%95 CI 44.3, 5Saklamaya y�nelik �zel tedbirler tedbirler) idi (B�l�m 1 ve 2). BIRC i�in do�rulanm�� yan�tlar i�in medyan DOR, Combo 300 i�in 12.7 ay [%95 GA: 9.3, 15.1] ve Enco 300 i�in 12.9 ay [95 % GA: 8.9, 15.5] idi. Medyan tedavi s�resi, Enco 300, 52.1 hafta vs 31.5 haftaya kar�� Combo 300 i�in daha uzundu.
Kardiyak elektrofizyoloji
G�nde iki kez 45 mg binimetinib ile kombinasyon halinde g�nde bir kez 450 mg enkorafenibin (Combo 450) birle�tirilmi� �al��malar�n�n g�venlilik analizinde, 450 mg enkorafenib art� binimetinib'de yeni QTc uzamas� > 500 msn insidans� %0.7 (2/268) olmu�tur ve enkorafenib tek ajan grubunda %2,5 (5/203). Tedavi �ncesi de�erlere k�yasla > 60 ms'lik QTc uzamas�, enkorafenib ve binimetinib grubunda %4,9 (13/268) hastada ve enkorafenib tek ajan grubunda %3,4 (7/204) g�zlenmi�tir (bkz. B�l�m 4.2 ve 4.4).
BRAF V600E Mutant Metastatik Kolorektal Kanser - �al��ma ARRAY-818-302
Setuksimab ile kombinasyon halinde enkorafenib, randomize, aktif kontroll�, a��k etiketli, �ok merkezli bir �al��mada de�erlendirilmi�tir (ARRAY 818-302 BEACON CRC). Uygun hastalar�n, �nceki 1 veya 2 rejimden sonra ilerlemi� BRAF V600E mutant metastatik kolorektal kansere sahip olmas� gerekiyordu. Kay�tl� hastalar, t�m�r RAS durumu ile ilgili olarak yerel olarak onaylanm�� etikete g�re setuksimab almaya uygundu. RAF inhibit�rlerinin, MEK inhibit�rlerinin veya EGFR inhibit�rlerinin �nceden kullan�m� yasaklanm��t�r. Randomizasyon, Do�u Kooperatif Onkoloji Grubu (ECOG) performans skoruna, irinotekan ve setuksimab kayna��n�n �nceki kullan�m�na g�re katmanlara ayr�lm��t�r.
Toplam 665 hasta, onayl� SmPC'sine (n=220) g�re dozlanan setuksimab ile kombinasyon halinde g�nde 300 mg oral enkorafenib veya oral yoldan 45 mg binimetinib ile kombinasyon halinde g�nde oral olarak 300 mg enkorafenib almak �zere randomize edildi (1:1:1). g�nde iki kez ve setuksimab, onayl� SmPC'sine (n=224) veya Kontrole (setuksimab ile irinotekan veya setuksimab ile irinotekan/5- florourasil/folinik asit (FOLFIRI), n= 221) g�re dozland�. Tedavi, hastal�k progresyonuna veya kabul edilemez toksisiteye kadar devam etti.
Etkililik sonu� �l��tleri, enkorafenib 300 mg ile setuksimab kombinasyonunu Kontrol ile kar��la�t�ran, k�r bir ba��ms�z inceleme komitesi (BIRC) taraf�ndan de�erlendirildi�i �zere genel sa�kal�m (OS) ve genel yan�t oran� (ORR) idi. Di�er etkinlik �l��tleri a�a��daki Tablo 8'de �zetlenmi�tir.
Hastalar�n ortanca ya�� 61 (26-91 aras�), %47'si erkek ve %83'� beyazd�. Hastalar�n %51'inin ba�lang�� ECOG performans durumu 0 idi ve %51'i �nceden irinotekan ald�. Hastalar�n %46.8'inde ba�lang��ta t�m�r tutulumu olan en az 3 organ vard�.
Setuksimab ile kombinasyon halinde 300 mg enkorafenib ile tedavi edilen hastalarda medyan maruziyet s�resi 3.2 ay ve irinotekan/setuksimab veya FOLFIRI/setuksimab (Kontrol kolu) ile tedavi edilen hastalarda 1.4 ay olmu�tur. 300 mg enkorafenib ve setuksimab kombinasyonu ile tedavi edilen hastalarda, medyan ba��l doz yo�unlu�u (RDI) enkorafenib i�in %98 ve setuksimab i�in %93.5 olmu�tur. Kontrol kolunda medyan RDI setuksimab i�in %85.4, irinotekan i�in %75.7 idi ve Folinik asit ve 5-FU alan hasta alt grubunda medyan RDI s�ras�yla %75.2 ve %75 idi.
Setuksimab ile kombinasyon halinde 300 mg enkorafenib, Kontrol ile kar��la�t�r�ld���nda OS, ORR ve PFS'de istatistiksel olarak anlaml� bir iyile�me g�stermi�tir. Etkinlik sonu�lar� Tablo 8 ve �ekil 3 ve 4'te �zetlenmi�tir.
Ara�t�rmac� de�erlendirmesine dayal� etkinlik sonu�lar�, ba��ms�z merkezi de�erlendirme ile tutarl�yd�.
Tablo 8: �al��ma ARRAY-818-302: Etkililik Sonu�lar�
| Setuksimab ile Enkorafenib | Setuksimab ile irinotekan veya setuksimab ile FOLFIRI (Kontrol) |
Son tarih: 11 �ubat 2019 (birincil analiz) | ||
OS | ||
Hasta say�s� | 220 | 221 |
Olaylar�n say�s� (%) | 93 (42.3) | 114 (51.6) |
Ortalama ay (95% CI) | 8.4 (7.5-11.0) | 5.4 (4.8, 6.6) |
HR (95% CI) (vs | 0.60 (0.41-0.88) |
|
Kontrol) |
| |
p-de�eri | 0.0002 | |
Ortalama takip | 7.6 | 7.2 |
s�resi, aylar (95% |
|
|
CI) | (Saklamaya y�nelik �zel tedbirler tedbirler, 9.20) | (6.1, 8.1) |
ORR (BIRC ba��na) | ||
Hasta say�s� | 113 | 107 |
ORR n (%) | 23 (20.4) | 2 (1.9) |
(95% CI) | (13.4, 29.0) | (0.2, 6.6) |
P-de�eri | <0.0001 |
|
CR, n (%) | 6 (5.3) | 0 |
PR, n (%) | 17 (15.0) | 2 (1.9) |
SD, n (%) | 57 (50.4) | 26 (24.3) |
DCR, n (%) | 84 (74.3) | 33 (30.8) |
(95% CI) | (65.3, 82.1) | (22.3, 40.5) |
PFS (BIRC ba��na) | ||
Hasta say�s� | 220 | 221 |
Olaylar�n say�s� (%) | 133 (60.5) | 128 (57.9) |
Ortalama PFS, aylar (95% CI) | 4.2 (3.7, 5.4) | 1.5 (1.5, 1.7) |
HR (95% CI) | 0.40 (0.30, 0.55 |
|
P-de�eri | < 0.0001 | |
G�ncellenmi� analiz, son tarih: 15 A�ustos 2019 | ||
OS | ||
Hasta say�s� | 220 | 221 |
Olaylar�n say�s� (%) | 128 (58.2) | 157 (71.0) |
Ortalama, aylar (95% CI) | 9.3 (8.0, 11.3) | 5.9 (5.1, 7.1) |
HR (95% CI) (vs | 0.61 (0.48, 0.77) |
|
Kontrol) |
| |
p-de�er | < 0.0001 | |
Ortalama takip | 12.3 | 12.9 |
s�resi, aylar (95% |
|
|
CI) | (11.1, 14.1) | (10.9, 14.6) |
ORR (BIRC ba��na) | ||
Hasta say�s� | 220 | 221 |
ORR n (%) | 43 (19.5) | 4 (1.8) |
(95% CI) | (14.5, 25.4) | (0.5, 4.6) |
p-de�er | <0.0001 |
|
CR, n (%) | 7 (3.2) | 0 |
PR, n (%) | 36 (1Saklamaya y�nelik �zel tedbirler tedbirler) | 4 (1.8) |
SD, n (%) | 117 (53.2) | 59 (26.7) |
DCR, n (%) | 167 (75.9) | 69 (31.2) |
(95% CI) | (69.7, 81.4) | (25.2, 37.8) |
PFS (BIRC ba��na) | ||
Hasta say�s� | 220 | 221 |
Olaylar�n say�s� (%) | 167 (75.9) | 147 (66.5) |
Ortalama PFS, aylar | 4.3 | 1.5 |
(95% CI) | (4.1, 5.5) | (1.5, 1.9) |
HR (95% CI) | 0.44 (0.35, 0.55) |
|
P-de�er | < 0.0001 | |
CI = G�ven aral���; CR = Tam yan�t; HR = Tehlike oran�; ORR = Genel yan�t oran�; OS = Genel hayatta kalma; PR = K�smi yan�t; SD = Stabil hastal�k, DCR: Hastal�k kontrol oran� (CR+PR+SD+CR-olmayan/PD- olmayan; CR-olmayan/PD-olmayan, yaln�zca CR'ye ula�amayan veya PD'si olan, �l��lemeyen bir hastal��� olan hastalar i�in ge�erlidir.)
�ekil 3: �al��ma ARRAY-818-302: Kaplan-Meier Genel Sa�kal�m (son tarih: 11 �ubat 2019)
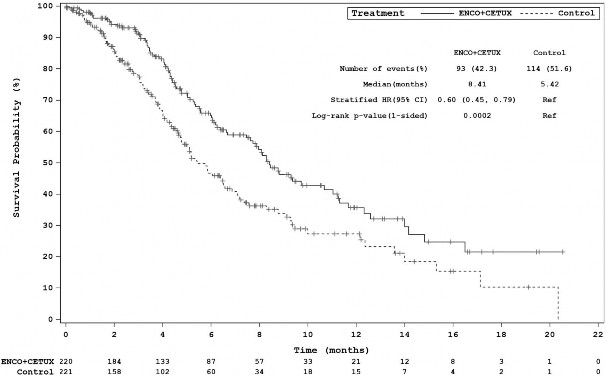
�ekil 4: �al��ma ARRAY-818-302: Genel Sa�kal�m Kaplan-Meier grafi�i (son tarih: 15 A�ustos 2019)
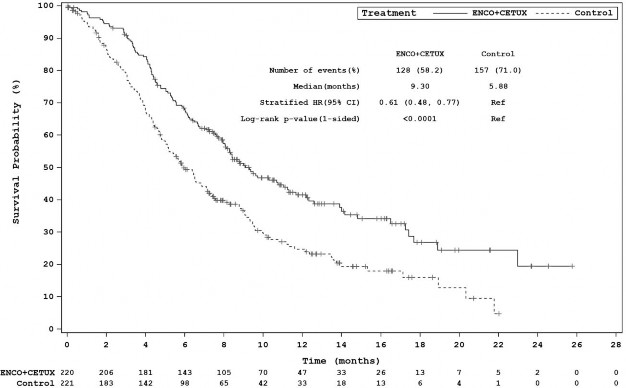
Kardiyak Elektrofizyoloji
Kolorektal endikasyonda ayarlanan Faz 3 (ARRAY-818-302) g�venlik analizinde, tedavi �ncesi ile kar��la�t�r�ld���nda yeni QTcF uzamas� >500 msinsidans� %3.2 (7/216) ve QTcF uzamas� >60 ms idi. de�erleri enkorafenib + setuksimab kolundaki hastalar�n %8,8'inde (19/216) g�zlenmi�tir (bkz. B�l�m 4.2 ve 4.4).
Pediyatrik pop�lasyon
Avrupa �la� Ajans�, melanomda pediyatrik pop�lasyonun bir veya daha fazla alt grubunda enkorafenib ile yap�lan �al��malar�n sonu�lar�n� sunma y�k�ml�l���n� ertelemi�tir (pediyatrik kullan�m hakk�nda bilgi i�in bkz. b�l�m 4.2).
Avrupa �la� Ajans�, kolorektal karsinomda pediyatrik pop�lasyonun t�m alt gruplar�nda enkorafenib ile yap�lan �al��malar�n sonu�lar�n� sunma zorunlulu�undan feragat etmi�tir (pediyatrik kullan�m hakk�nda bilgi i�in bkz. b�l�m 4.2).
5.2. Farmakokinetik �zellikler
Enkorafenibin farmakokineti�i, BRAF V600E veya K mutasyonunu bar�nd�ran ileri ve rezeke edilemeyen veya metastatik kutan�z melanom dahil olmak �zere solid t�m�rl� hastalarda ve sa�l�kl� deneklerde ve BRAF V600E mutasyonlu metastatik kolorektal kanserli eri�kin hastalarda incelenmi�tir. Enkorafenibin farmakokineti�inin, tekli ve �oklu dozlardan sonra yakla��k olarak doz
do�rusal oldu�u g�sterilmi�tir. G�nde bir kez tekrarlanan dozlamadan sonra, 15 g�n i�inde kararl� durum ko�ullar�na ula��ld�. Yakla��k 0,5'lik birikim oran�, muhtemelen CYP3A4'�n otomatik ind�ksiyonundan kaynaklanmaktad�r. EAA'n�n denekler aras� de�i�kenli�i (%CV) %12.3 ile %68.9 aras�nda de�i�mektedir.
Emilim:
Oral uygulamadan sonra enkorafenib, medyan Tde�eri 1.5 ile 2 saatte h�zla emilir. Sa�l�kl� deneklerde tek oral 100 mg [C] binimetinib dozunun ard�ndan enkorafenib dozunun en az %86's� emilmi�tir. Y�ksek ya�l�, y�ksek kalorili bir yemekle birlikte 100 mg'l�k tek bir enkorafenib dozunun uygulanmas�, maksimum binimetinib konsantrasyonunu (C) %36 azalt�rken, konsantrasyon- zaman e�risi (EAA) alt�ndaki alan de�i�memi�tir. Sa�l�kl� g�n�ll�lerde yap�lan bir ila� etkile�imi �al��mas�, mide pH'�n� de�i�tiren bir ajan�n (rabeprazol) varl���nda enkorafenib maruziyet derecesinin de�i�medi�ini g�stermi�tir.
Da��l�m:
Enkorafenib, in vitro olarak insan plazma proteinlerine orta derecede (%86.1) ba�lan�r. Sa�l�kl� g�n�ll�lerde 100 mg'l�k [C] tek oral enkorafenib dozunu takiben, ortalama (SD) kan-plazma konsantrasyon oran� 0,58 (0,02) ve ortalama (%CV) g�r�n�r da��l�m hacmi (Vz/F)'dir. enkorafenib 226 L'dir (%32.7).
Biyotransformasyon:
Sa�l�kl� deneklerde 100 mg [C] tek oral enkorafenib dozunu takiben, metabolizman�n enkorafenib i�in ana klirens yolu oldu�u bulundu (geri kazan�lan radyoaktif dozun yakla��k %88'i). Enkorafenibin bask�n biyotransformasyon reaksiyonu, N-dealkilasyonuydu. Di�er ana metabolik yollar, hidroksilasyon, karbamat hidrolizi, dolayl� glukuronidasyon ve glukoz konjugat olu�umunu i�eriyordu.
Eliminasyon:
Sa�l�kl� deneklerde 100 mg'l�k [C] tek oral enkorafenib dozunun ard�ndan, radyoaktivite hem fe�este hem de idrarda e�it olarak elimine edilmi�tir (ortalama %47.2). �drarda radyoaktivitenin
%1.8'i enkorafenib olarak at�lm��t�r. Enkorafenibin ortalama (%CV) g�r�n�r klerensi (CL/F) 27.9 L/saat (%9.15) olmu�tur. Medyan (aral�k) enkorafenib terminal yar� �mr� (T1/2) 6.32 saat olmu�tur (3.74 ila 8.09 saat).
�la� etkile�imleri
Enkorafenib ve setuksimab aras�nda herhangi bir ila� ila� etkile�imi yoktur.
CYP enzimlerinin enkorafenib �zerindeki etkisi
Enkorafenib, CYP3A4, CYP2C19 ve CYP2D6 taraf�ndan metabolize edilir. �n vitro olarak, CYP3A4'�n insan karaci�er mikrozomlar�nda enkorafenibin toplam oksidatif klirensine katk�da bulunan ana enzim oldu�u (~%83.3), ard�ndan CYP2C19 ve CYP2D6'n�n (s�ras�yla ~%16,0 ve
%0,71) oldu�u tahmin edilmi�tir.
Enkorafenibin CYP substratlar� �zerindeki etkisi
In vitro deneyler, enkorafenib'in UGT1A1, CYP2B6, CYP2C9 ve CYP3A4/5'in nispeten g��l� bir geri d�n���ml� inhibit�r� ve ayr�ca zamana ba�l� bir CYP3A4 inhibit�r� oldu�unu g�stermektedir. Enkorafenib, insan primer hepatositlerinde CYP1A2, CYP2B6, CYP2C9 ve CYP3A4'� ind�kledi. 1. G�n ve 15. G�nde CYP2B6, CYP1A2, CYP2C9, CYP2C19 ve CYP2D6 i�in prob substratlar� ile birlikte uygulanan 450 mg enkorafenib sim�lasyonlar�n�n t�m�, klinik olarak anlaml� etkile�imlerin beklenmedi�ini g�stermi�tir. Ba��rsak ekstraksiyonuna tabi tutulan CYP3A4 ve UGT1A1 substratlar� ile birlikte uygulama i�in, k���k ila orta d�zeyde bir etkile�im beklenir. Binimetinib bir UGT1A1 substrat� olsa da, ba��rsak ekstraksiyonuna u�ramaz ve bu nedenle enkorafenib ile DDI beklenmez. Ek olarak, binimetinib enkorafenib ile birlikte uyguland���nda klinik olarak maruziyette herhangi bir farkl�l�k g�zlenmemi�tir.
Ta��y�c�lar�n encorafenib �zerindeki etkisi
Enkorafenib'in P glikoprotein (P gp) ta��y�c�lar�n�n bir substrat� oldu�u bulundu. Enkorafenib y�ksek i�sel ge�irgenlik g�sterdi�inden, Pgp'nin inhibisyonunun enkorafenib konsantrasyonlar�nda klinik olarak �nemli bir art��la sonu�lanmas� olas� de�ildir. Birka� al�m ta��y�c� ailesinin (OCT1, OATP1B1, OATP1B3 ve OATPB1) kat�l�m�, ilgili ta��y�c� inhibit�rleri kullan�larak in vitro olarak ara�t�r�ld�. Veriler, hepatik al�m ta��y�c�lar�n�n, enkorafenib'in birincil insan hepatositlerine da��l�m�nda yer almad���n� g�stermektedir.
Enkorafenib'in ta��y�c�lar �zerindeki etkisi
Enkorafenib, in vitro olarak hepatik ta��y�c� OCT1'i inhibe etti, ancak klinik olarak etkili bir inhibit�r olmas� olas� de�ildir. �n vitro �al��malara dayanarak, enkorafenibin klinik konsantrasyonlarda renal ta��y�c�lar OCT2, OAT1, OAT3 ve hepatik ta��y�c�lar OATP1B1 ve OATP1B3'� inhibe etme potansiyeli vard�r. Ek olarak, enkorafenib, beklenen klinik konsantrasyonlarda ba��rsakta P-gp'yi ve BCRP'yi inhibe edebilir.
�zel pop�lasyonlar
Geriyatrik Pop�lsyon
Bir dizi farmakokinetik analize dayanarak, ya��n enkorafenib da��l�m hacmi �zerinde �nemli bir ortak de�i�ken oldu�u, ancak y�ksek de�i�kenlik oldu�u bulundu. Bu de�i�ikliklerin k���k boyutu ve y�ksek de�i�kenli�i g�z �n�ne al�nd���nda, bunlar�n klinik olarak anlaml� olmas� olas� de�ildir ve ya�l� hastalar i�in doz ayarlamas�na gerek yoktur.
Cinsiyet
Bir dizi farmakokinetik analize dayanarak cinsiyet, klirens veya da��l�m hacmi �zerinde anlaml� bir model de�i�keni olarak bulunmam��t�r. Sonu� olarak, cinsiyete ba�l� olarak enkorafenib maruziyetinde �nemli bir de�i�iklik beklenmemektedir.
V�cut a��rl���
Bir dizi farmakokinetik analize dayanarak, v�cut a��rl���n�n klerens ve da��l�m hacmi �zerinde �nemli bir model de�i�keni oldu�u bulundu. Bununla birlikte, klirensteki k���k de�i�iklik b�y�kl��� ve modelde tahmin edilen da��l�m hacmindeki y�ksek de�i�kenlik g�z �n�ne al�nd���nda, a��rl���n enkorafenib'in a���a ��kmas� �zerinde klinik olarak anlaml� bir etkisi olmas� olas� de�ildir.
Irk
Asyal�lar ve Asyal� olmayanlar aras�nda enkorafenibin farmakokinet�i a��s�ndan klinik olarak anlaml� farklar yoktur. Di�er �rklarda veya etnik k�kenlerde enkorafenibin maruziyetindeki potansiyel farkl�l�klar� de�erlendirmek i�in yeterli veri yoktur.
Karaci�er yetmezli�i
�zel bir klinik �al��man�n sonu�lar�, hafif karaci�er yetmezli�i olan hastalarda (Child Pugh S�n�f A) normal karaci�er fonksiyonuna sahip g�n�ll�lere k�yasla %25 daha y�ksek toplam enkorafenib maruziyetini g�stermektedir. Bu, ba�lanmam�� enkorafenib maruziyetinde %55'lik bir art�� anlam�na gelir.
Enkorafenib'in farmakokineti�i, orta (Child Pugh S�n�f B) veya �iddetli (Child Pugh S�n�f C) karaci�er yetmezli�i olan hastalarda klinik olarak de�erlendirilmemi�tir. Enkorafenib, Fizyolojik esasl� farmakokinetik (PBPK) modellemesine dayal� olarak �ncelikle karaci�er yoluyla metabolize edildi�inden ve elimine edildi�inden, orta ila �iddetli karaci�er yetmezli�i olan hastalarda, hafif karaci�er yetmezli�i olan hastalardan daha fazla maruziyet art��� olabilir. Orta veya �iddetli karaci�er yetmezli�i olan hastalarda doz �nerisi yap�lamaz (bkz. b�l�m 4.2 ve 4.4).
B�brek yetmezli�i
Enkorafenib, minimal renal eliminasyona u�rar. B�brek yetmezli�inin enkorafenibin farmakokineti�i �zerindeki etkisini de�erlendirmek i�in bir klinik �al��ma yap�lmam��t�r.
Bir dizi farmakokinetik analizde, hafif (eGFR 60 ila 90 mL/dak/1.73 m2) veya orta (eGFR 30 ila 59 mL/dak/1.73 m2) b�brek yetmezli�i olan hastalarda enkorafenibin g�r�nen total v�cut klerensi (Cl/F)'nde belirgin bir e�ilim g�zlenmemi�tir. Normal b�brek fonksiyonu olan denekler (eGFR ≥90 mL/dak/1.73 m2). Hafif ve orta derecede b�brek yetmezli�i olan hastalarda CL/F'de k���k bir d���� (≤%5) �ng�r�lm��t�r, bu da klinik olarak anlaml� olmas� muhtemel de�ildir. Enkorafenibin farmakokineti�i, �iddetli b�brek yetmezli�i olan hastalarda �al���lmam��t�r.
5.3. Klinik �ncesi g�venlilik verileri
4 haftal�k ve 13 haftal�k s��an toksisite �al��malar�nda, klinik belirtiler, v�cut a��rl���nda azalma epididimlerde ve prostat a��rl�klar�nda azalma ve testis, epididim, mide ve deride mikroskobik bulgular kaydedildi. Bu bulgular�n k�smen tersine �evrilebilirli�i, 4 haftal�k bir iyile�me d�neminden sonra kaydedildi. Ek olarak, 13 haftal�k s��an toksisite �al��mas�nda, ≥ 100 mg/kg/g�n dozlarda geri d�n���ml� klinik patoloji de�i�iklikleri kaydedilmi�tir. 4 haftal�k �al��ma i�in NOAEL olu�turulamad�. 13 haftal�k �al��mada belirlenen NOAEL, insan terap�tik maruziyetlerinin 10 kat�ndan fazlayd�.
4 haftal�k ve 13 haftal�k maymun toksisite �al��mas�nda, insan terap�tik maruziyetlerinin biraz �zerinde izole/sporadik kusma ve diyare epizodlar�n�n yan� s�ra oftalmik lezyonlar g�zlenmi�tir. Oftalmik lezyonlar k�smen geri d�n���ml�yd� ve retinada d�� �ubuklar ve koniler tabakas� ile foveadaki merkezi makulada retina pigmentli epitelyum aras�nda bir ayr�lma veya ayr�lmadan olu�uyordu. Bu g�zlem, insanlarda merkezi ser�z benzeri koryoretinopati veya merkezi ser�z retinopati olarak tan�mlanana benzerdi.
Enkorafenib genotoksik de�ildir.
Enkorafenib ile do�urganl�k �al��malar� yap�lmam��t�r. 13 haftal�k s��an toksikolojisi �al��malar�nda, 6 mg/kg/g�n'de (terap�tik dozda insan maruziyetinin 5 kat�ndan fazla doz seviyesi) enkorafenib tedavisi, t�b�ler dejenerasyon ve oligospermi ile testis ve epididim a��rl�klar�n�n azalmas�na neden olmu�tur. 13 haftal�k �al��mada, en y�ksek doz seviyesinde (60 mg/kg/g�n) k�smi tersine �evrilebilirlik kaydedilmi�tir.
S��anlarda yap�lan embriyo-fetal geli�im �al��mas�, enkorafenib'in daha d���k fetal a��rl�klar ve iskelet geli�iminde gecikmeler ile fetal toksisiteye neden oldu�unu g�stermi�tir.
Tav�anlarda yap�lan embriyo-fetal geli�im �al��mas�, enkorafenib'in daha d���k fetal a��rl�klar ve iskelet geli�iminde ge�ici de�i�iklikler ile fetal toksisiteye neden oldu�unu g�stermi�tir. Baz� fet�slerde aort ark�nda dilatasyon g�zlendi.
Enkorafenib, bir in vitro 3T3 N�tr K�rm�z� Al�m Testinde fototoksik olmu�tur. Enkorafenib, in vivo fare duyarl�la�t�rma deneyinde bir duyarl�la�t�r�c� de�ildir. Toplu olarak, bu veriler enkorafenib'in fototoksik potansiyel riskine ve hastalarda terap�tik dozlarda minimal duyarl�l�k riskine sahip oldu�unu g�stermektedir.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Kaps�l i�eri�i Kopovidon Poloksamer 188 Mikrokristalin sel�loz S�ksinik asit Krospovidon
Silika kolloidal susuz Magnezyum stearat
Kaps�l k�l�f�
Jelatin (s���r kaynakl�) Titanyum dioksit K�rm�z� demir oksit Sar� demir oksit
Siyah demir oksit
Bask� �ellak
Siyah demir oksit Propilen glikol
6.2. Ge�imsizlikler
Ge�erli de�ildir.
6.3. Raf �mr�
36 ay
6.4. Saklamaya y�nelik �zel tedbirler
30°C alt�nda saklay�n.
Nemden korumak i�in orijinal ambalaj�nda saklay�n�z.
6.5. Ambalaj�n niteli�i ve i�eri�i
Her paket, poliamid/al�minyum/PVC/al�minyum blisterlerde 42 adet sert kaps�l i�erir.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan t�bbi �r�nler ya da at�k materyaller yerel gerekliliklere uygun olarak imha edilmelidir.
 Belso�uklu�u, Chlamydia ve Frengi
Belso�uklu�u, bakterilerin sebep oldu�u bir enfeksiyondur. Cinsel ili�ki
yoluyla bula��r ve d�lyata�� boynunda, idrar yollar�nda, an�ste, makatta ve
bo�azda enfeksyona sebep olabilir.
Belso�uklu�u, Chlamydia ve Frengi
Belso�uklu�u, bakterilerin sebep oldu�u bir enfeksiyondur. Cinsel ili�ki
yoluyla bula��r ve d�lyata�� boynunda, idrar yollar�nda, an�ste, makatta ve
bo�azda enfeksyona sebep olabilir. |
 Omurilik zedelenmeleri
Omurilik zedelenmesini takip eden birka� g�n i�inde, hi�kimse hasarin ne kadar olacagini tahmin edemez. Buradaki sorun, omuriligin herhangi bir zedelenmesinden hemen sonra, bir omurilik sokunun olusmasidir.
Omurilik zedelenmeleri
Omurilik zedelenmesini takip eden birka� g�n i�inde, hi�kimse hasarin ne kadar olacagini tahmin edemez. Buradaki sorun, omuriligin herhangi bir zedelenmesinden hemen sonra, bir omurilik sokunun olusmasidir. |
 |
Diyabet Hastal��� Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r. |
 |
A��z Kanseri A��z kanserinin en yayg�n t�rleri, dudak, dil, di�etidir. Nadiren yanak i�i veya damak b�lgelerini de i�ine al�r. |
 |
�izofrenlik �izofrenli�in psikiatrik te�hisi hakk�nda �ok fazla anla�mazl�k vard�r. Bu sayfadaki bilgiler, �izofrenli�in te�hisi, nedenleri ve tedavisi hakk�ndaki fakl� teoriler hakk�nda bilgi verecektir. |
�LA� GENEL B�LG�LER�
Pierre Fabre �la� A.�.
| Sat�� Fiyat� | 64904.05 TL [ 21 Feb 2025 ] |
| �nceki Sat�� Fiyat� | 64904.05 TL [ 14 Feb 2025 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | K�s�tlanm�� Beyaz Re�eteli bir ila�d�r. |
| Barkodu | 8699749000055 |
| Etkin Madde | Enkorafenib |
| ATC Kodu | L01EC03 |
| Birim Miktar | 75 |
| Birim Cinsi | MG |
| Ambalaj Miktar� | 42 |
| Antineoplastik ve �mm�nomod�lat�r Ajanlar |
| �thal ( ref. �lke : Italya ) ve Be�eri bir ila�d�r. |