CABOMETYX 60 mg film kaplı tablet Kısa Ürün Bilgisi
{ Kabozantinib }
1. BEŞERİ TIBBİ ÜRÜNÜN ADI
CABOMETYX 60 mg film kaplı tablet
2. KALİTATİF VE KANTİTATİF BİLEŞİM
Etkin madde
Her film kaplı tablette 60 mg kabozantinibe eşdeğer 76,03 mg kabozantinib (S)-malat bulunur.
Yardımcı maddeler
Laktoz… 46,61 mg
Kroskarmeloz sodyum 14,40 mg
Yardımcı maddeler için Bölüm 6.1'e bakınız.
3. FARMASÖTİK FORMU
Film kaplı tablet.
Tabletler sarı renklidir, yuvarlak biçimli, çentiksizdir ve bir yüzünde “XLâ€, diğer yüzünde ise “60†yazısı bulunur.
4. KLİNİK ÖZELLİKLER
4.1. Terapötik endikasyonlar
Renal Hücreli Karsinom (RHK)CABOMETYX, metastatik şeffaf hücreli renal hücreli karsinom (RHK) tanısı almış, ilerlemiş renal hücreli karsinomda monoterapi olarak;
Orta ve yüksek riskli yetişkin hastaların birinci basamak tedavisinde (bkz. Bölüm 5.1),
4.2. Pozoloji ve uygulama şekli
Pozoloji/uygulama sıklığı ve süresi:
CABOMETYX tedavisi yalnızca kanser ilaçlarının uygulamasında deneyimli bir hekim tarafından başlatılmalıdır.
Pozoloji
CABOMETYX tabletler ile kabozantinib kapsüller biyoeşdeğer değildir ve birbirleri yerine kullanılmamalıdır (bkz. Bölüm 5.2).
Monoterapi olarak CABOMETYX
RHK ve HSK için önerilen CABOMETYX dozu günde bir kez alınan 60 mg'dir. Tedavi, hastanın tedaviden daha fazla klinik yarar sağlamadığı zamana kadar veya kabul edilemez toksisite ortaya çıkana kadar sürdürülmelidir.
Birinci basamak ilerlemiş RHK'da nivolumabla kombinasyon halinde CABOMETYX
Önerilen CABOMETYX dozu, her 2 haftada bir 240 mg ya da her 4 haftada bir 480 mg olacak şekilde intravenöz yoldan uygulanan nivolumab ile kombinasyon halinde günde bir kez 40 mg'dır. CABOMETYX tedavisine, hastalık progresyonuna veya kabul edilemez toksisite ortaya çıkana kadar devam edilmelidir. Nivolumaba hastalık progresyonuna, kabul edilemez toksisite ortaya çıkana kadar veya hastalık progresyonu olmayan hastalarda 24 aya kadar devam edilmelidir (nivolumab pozolojisi için Kısa Ürün Bilgisine (KÜB) bakınız).
Tedavi değişikliği
Şüpheli advers ilaç reaksiyonlarının yönetimi, tedavinin geçici olarak durdurulmasını ve/veya CABOMETYX dozunun azaltılmasını gerektirebilir (bkz. Tablo 1). Monoterapide doz azaltımı gerekli olduğunda dozun günde 40 mg'ye ve ardından günde 20 mg'ye düşürülmesi önerilir.
CABOMETYX nivolumab ile kombinasyon halinde uygulandığında, dozun günde bir kez 20 mg CABOMETYX'e ardından iki günde bir 20 mg'ye düşürülmesi önerilir (nivolumab için önerilen tedavi değişikliği konusunda nivolumab KÜB'üne bakınız).
CTCAE derece 3 veya üzeri toksisitelerin veya tolere edilemeyen derece 2 toksisitelerin tedavisi için doza ara verilmesi önerilmektedir. Devam etmesi durumunda ciddileşebilecek veya tolere edilemez hale gelebilecek olaylarda dozun azaltılması önerilmektedir.
Bir dozun atlanması durumunda bir sonraki doza 12 saatten kısa bir süre kaldıysa atlanmış olan doz alınmamalıdır.
Tablo 1: Advers reaksiyonlar için önerilen CABOMETYX doz değişiklikleri
Advers reaksiyon ve şiddeti | Tedavi değişikliği |
Tolere edilebilir ve kolay yönetilir olan derece 1 ve derece 2 advers reaksiyonlar | Genellikle doz ayarlanması gerekli değildir. Gereken şekilde destekleyici bakım uygulanması düşünülmelidir. |
Tolere edilemeyen ve doz azaltımı veya destekleyici bakımla tedavi edilemeyen derece 2 advers reaksiyonlar | Advers reaksiyon derece ≤1'e gerileyene kadar tedaviye ara verilir. Gereken şekilde destekleyici bakım uygulanmalıdır. |
| Tedavinin daha düşük bir dozla yeniden başlatılması düşünülmelidir. |
Derece 3 advers reaksiyonlar (klinik açıdan anlamlı olmayan laboratuvar anormallikleri hariç) | Advers reaksiyon derece ≤1'e gerileyene kadar tedaviye ara verilir. Gereken şekilde destekleyici bakım uygulanmalıdır. Tedavi daha düşük bir dozla yeniden başlatılmalıdır. |
Derece 4 advers reaksiyonlar (klinik açıdan anlamlı olmayan laboratuvar anormallikleri hariç) | Tedaviye ara verilir. Uygun tıbbi bakım başlatılmalıdır. Advers reaksiyon derece ≤1'e gerilerse tedavi daha düşük bir dozla yeniden başlatılmalıdır. Advers reaksiyon gerilemezse CABOMETYX kalıcı şekilde kesilmelidir. |
Nivolumab ile kombinasyon halindeki CABOMETYX ile tedavi edilen RHK hastalarında karaciğer enzimindeki artışlar |
|
ALT veya AST > 3 kat ULN ancak eşzamanlı toplam bilirubin ≥ 2 kat ULN olmadığında ≤10 kat ULN | Advers reaksiyon derece ≤1'e gerileyene kadar CABOMETYX ve nivolumaba ara verilmelidir İmmün bağlantılı reaksiyondan şüpheleniliyorsa kortikosteroid tedavisi düşünülebilir (nivolumab KÜB'üne bakınız). İyileşmeden sonra tek bir ilaçla yeniden başlanması veya her iki ilaca sırayla yeniden başlanması düşünülebilir. Nivolumaba tekrar başlanıyorsa nivolumab KÜB'üne bakınız. |
ALT veya AST > 10 kat ULN ancak | CABOMETYX ve nivolumab kalıcı olarak |
eşzamanlı toplam bilirubin ≥ 2 kat ULN | bırakılmalıdır. |
olduğunda > 3 kat ULN | İmmün bağlantılı reaksiyondan şüpheleniliyorsa kortikosteroid tedavisi düşünülebilir (nivolumab KÜB'üne bakınız). |
Not: Toksisite dereceleri Advers Olaylar için Ulusal Kanser Enstitüsü Ortak Terminoloji Kriterleri, Versiyon 4.0'a (NCI- CTCAE v4) uygundur.
Eş zamanlı tıbbi ürünler
CYP3A4'ü güçlü şekilde inhibe eden eşzamanlı tıbbi ürünler dikkatli şekilde kullanılmalıdır ve CYP3A4'ün güçlü indükleyicileri olan eşzamanlı ürünlerin kronik kullanımından kaçınılmalıdır (bkz. Bölüm 4.4 ve 4.5).
CYP3A4'ü indükleme veya inhibe etme potansiyeli minimal olan veya hiç olmayan alternatif bir eşzamanlı tıbbi ürünün seçilmesi düşünülmelidir.
Uygulama şekli:
CABOMETYX oral kullanıma yöneliktir. Tabletler bütün halde yutulmalı, çiğnenmemelidir. Hastalara CABOMETYX almadan önceki en az 2 saat ve aldıktan sonraki 1 saat süresince hiçbir şey yememesi söylenmelidir.
Özel popülasyonlara ilişkin ek bilgiler:
Böbrek yetmezliği:
Kabozantinib hafif veya orta derecede böbrek yetmezliği bulunan hastalarda dikkatli şekilde kullanılmalıdır. Şiddetli böbrek yetmezliği bulunan hastalarda kabozantinibin güvenlilik ve etkililiği kanıtlanmadığından bu popülasyonda kullanımı önerilmez.
Karaciğer yetmezliği:
Hafif karaciğer yetmezliği olan hastalarda doz ayarlaması gerekmez. Orta derecede karaciğer yetmezliği olan hastalar (Child Pugh B) için sınırlı veri bulunduğundan, herhangi bir doz önerisi sağlanamaz. Bu hastalarda genel güvenliğin yakından takip edilmesi önerilmektedir (bkz. Bölüm 4.4 ve 5.2). Şiddetli karaciğer yetmezliği olan hastalarda (Child Pugh C) klinik deneyim yoktur, bu nedenle bu hastalarda kabozantinib kullanılması önerilmemektedir (bkz. Bölüm 5.2).
Kardiyak yetmezliği:
Kardiyak yetmezliği olan hastalara ilişkin veriler sınırlıdır. Herhangi bir spesifik doz önerisinde bulunulamamaktadır.
Pediyatrik popülasyon:
Kabozantinibin çocuklar ve 18 yaş altı adolesanlardaki güvenliliği ve etkililiği henüz kanıtlanmamıştır. Veri mevcut değildir.
![]()
Geriyatrik popülasyon:
Yaşlı hastalarda (≥ 65 yaş) kabozantinib kullanılırken herhangi bir spesifik doz ayarlaması önerilmez.
Irk:
Etnik kökene göre doz ayarlaması gerekmez (bkz. Bölüm 5.2).
4.3. Kontrendikasyonlar
Etkin madde
4.4. Özel kullanım uyarıları ve önlemleri
Advers reaksiyonların çoğu tedavinin erken dönemlerinde ortaya çıktığından, tedaviyi uygulayan hekim doz değişikliklerinin gerekli olup olmadığını belirlemek için tedavinin ilk sekiz haftasında hastayı yakından değerlendirmelidir. Genel olarak erken dönemde başlayan advers reaksiyonlar arasında hipokalsemi, hipokalemi, trombositopeni, hipertansiyon, palmar- plantar eritrodizestezi sendromu (PPES), proteinüri ve gastrointestinal (Gİ) olaylar (abdominal ağrı, mukozal enflamasyon, konstipasyon, diyare, kusma) yer alır.
Şüpheli advers ilaç reaksiyonlarının yönetimi, kabozantinib tedavisinin geçici olarak durdurulmasını ya da dozun azaltılmasını gerektirebilir (bkz. Bölüm 4.2).
Pivot klinik çalışmada (METEOR) renal hücreli karsinomda önceki vasküler endotelyal büyüme faktörü (VEGF)-hedefli tedaviyi takiben, bir advers olaydan (AO) kaynaklanan doz azaltımı ve doza ara verme olayları kabozantinible tedavi uygulanan hastaların sırasıyla
%59,8'inde ve %70'inde ortaya çıkmıştır. Hastaların %19,3'ünde iki doz azaltımı gerekli olmuştur.
İlk doz azaltımına kadar geçen medyan süre 55 gün, ilk doza ilk ara vermeye kadar geçen medyan süre ise 38 gün olmuştur.
Klinik çalışmada (CABOSUN) daha önce tedavi uygulanmamış renal hücreli karsinomda doz azaltımı ve doz kesme olayları kabozantinible tedavi uygulanan hastaların sırasıyla %46'sında ve %73'ünde ortaya çıkmıştır.
Kabozantinib birinci basamak ilerlemiş renal hücreli karsinomda nivolumab ile kombinasyon halinde kullanıldığında, klinik çalışmada (CA2099ER) bir AO nedeniyle kabozantinib ile doz azaltımı ve doz kesintileri hastaların %54,1 ve %73,4'ünde ortaya çıkmıştır. Hastaların
%9,4'ünde iki doz azaltımı gerekli olmuştur. İlk doz azaltımına kadar geçen medyan süre 106 gün, ilk doz kesintisine kadar geçen medyan süre ise 68 gün olmuştur.
Klinik çalışmada (CELESTIAL), daha önce uygulanmış olan sistemik tedaviyi takiben hepatoselüler karsinomda doz azaltımı ve doz kesme olayları kabozantinib ile tedavi edilen hastaların sırasıyla % 62 ve % 84'ünde ortaya çıkmıştır. Hastaların% 33'ünde iki doz azaltımı gerekmiştir. İlk doz azaltımına kadar geçen medyan süre 38 gün, ilk doz durdurmaya kadar geçen medyan süre ise 28 gün olmuştur. Hafif veya orta derecede karaciğer yetmezliği olan hastaların daha yakından takip edilmesi önerilmektedir.
Hepatotoksisite
Kabozantinib ile tedavi edilen hastalarda karaciğer fonksiyon testlerinde anormallikler (alanin aminotransferaz [ALT], aspartat aminotransferaz [AST] ve bilirubinde artışlar) sıklıkla gözlenmiştir. Kabozantinib tedavisine başlamadan önce karaciğer fonksiyon testlerinin (ALT, AST ve bilirubin) yapılması ve tedavi sırasında yakından izlenmesi önerilmektedir. Kabozantinib tedavisi ile ilgili olduğu düşünülen karaciğer fonksiyon testleri kötüleşen hastalar için (yani alternatif bir neden bulunmadığı durumlarda), Tablo 1'deki doz değişikliği tavsiyesine uyulmalıdır (bkz. Bölüm 4.2).
Cabozantinib, nivolumab ile kombinasyon halinde verildiğinde, ilerlemiş RCC hastalarında kabozantinib monoterapisine göre 3. ve 4. derece ALT ve AST artışlarının daha sık olduğu bildirilmiştir (bkz. Bölüm 4.8). Karaciğer enzimleri tedavi başlamadan önce ve tedavi sırasında periyodik olarak izlenmelidir. Her iki ilacın tıbbi yönetim kılavuzları izlenmelidir (bkz. Bölüm 4.2 ve nivolumab KÜB).
Kabozantinib, esas olarak hepatik yolla elimine edilir. Hafif veya orta dereceli karaciğer yetmezliği olan hastalarda genel güvenliğin daha yakından izlenmesi önerilmektedir (ayrıca bkz. Bölüm 4.2 ve 5.2). Orta derecede karaciğer yetmezliği olan hastaların (Child-Pugh B) göreceli olarak daha yüksek oranında kabozantinib tedavisi ile hepatik ensefalopati gelişmiştir. CABOMETYX'in şiddetli karaciğer yetmezliği olan hastalarda kullanılması önerilmemektedir. (Child-Pugh C, bkz. Bölüm 4.2)
Hepatik ensefalopati
HSK çalışmasında (CELESTIAL), hepatik ensefalopati kabozantinibte plasebo kolundan daha sık rapor edilmiştir. Kabozantinib, diyare, kusma, iştah azalması ve elektrolit anormallikleri ile ilişkilendirilmiştir. Karaciğer yetmezliği olan HSK hastalarında, bu hepatik olmayan etkiler hepatik ensefalopati gelişimi için hızlandırıcı faktör olabilir. Hastalar hepatik ensefalopati bulguları ve semptomları açısından izlenmelidir.
Perforasyonlar ve fistüller
Kabozantinible ciddi, bazen ölümcül olan Gİ perforasyonlar ve fistüller gözlenmiştir. Enflamatuvar bağırsak hastalığı (örneğin Crohn hastalığı, ülseratif kolit, peritonit, divertikülit veya apandisit), Gİ kanalda tümör infiltrasyonu görülen veya daha önce uygulanmış Gİ ameliyatında komplikasyonlar (özellikle gecikmiş veya tam olmayan iyileşme ile ilişkili ise) yaşamış olan hastalar kabozantinib tedavisine başlanmadan önce dikkatli şekilde değerlendirilmelidir ve sonrasında apse ve sepsis dahil perforasyon ve fistül semptomları açısından yakından takip edilmelidir. Tedavi sırasında geçmeyen veya tekrarlayan diyare anal fistül oluşumu açısından bir risk faktörü olabilir. Yeterli düzeyde kontrol altına alınamayan fistül veya Gİ perforasyon görülen hastalarda kabozantinib kesilmelidir.
Gastrointestinal (Gİ) hastalıkları
Diyare, bulantı/kusma, iştah azalması ve stomatit/ağızda ağrı en sık bildirilen Gİ bazılarıdır (bkz. Bölüm 4.8). Dehidrasyonu, elektrolit dengesizliklerini ve kilo kaybını önlemek için antiemetikler, antidiyareik ilaçlar veya antasitler ile destekleyici bakım da dahil olmak üzere, derhal tıbbi tedavi yapılmalıdır. Sürekli veya tekrarlayan önemli Gİ advers reaksiyonları durumunda, doz kesme veya azaltımı veya kabozantinibin kalıcı olarak kesilmesi düşünülmelidir (bkz. Tablo 1).
Tromboembolik olaylar
Kabozantinib ile pulmoner embolizmi ve bazen ölümcül olan arteriyel tromboembolizmi de içeren venöz tromboembolizm olayları gözlenmiştir. Bu olaylar açısından risk altında olan veya bu olayları içeren bir öyküye sahip olan hastalarda kabozantinib dikkatli kullanılmalıdır. HSK çalışmasında (CELESTIAL), bir ölümcül olay da dahil olmak üzere kabozantinib ile portal ven trombozu gözlenmiştir. Portal ven invazyon öyküsü olan hastaların portal ven trombozu gelişme riskinin daha yüksek olduğu görülmüştür. Akut miyokard enfarktüsü veya klinik açıdan anlamlı başka herhangi bir tromboembolik komplikasyon yaşayan hastalarda kabozantinib kesilmelidir.
Hemoraji
Kabozantinib kullanımı ile birlikte bazen ölümcül olan şiddetli hemoraji gözlenmiştir. Şiddetli kanama öyküsüne sahip olan hastalar kabozantinib tedavisine başlanmadan önce dikkatli şekilde değerlendirilmelidir. Şiddetli kanama görülen veya şiddetli kanama riski altında olan hastalara kabozantinib uygulanmamalıdır.
HSK çalışmasında (CELESTIAL), ölümcül hemorajik olayların, plaseboya göre kabozantinib ile daha sık görüldüğü rapor edilmiştir. İlerlemiş HSK popülasyonunda ciddi hemoraji için zemin hazırlayan risk faktörleri, majör kan damarlarının tümör invazyonu ve altta yatan karaciğer sirozu ile sonuçlanan özofagus varislerinin varlığı, portal hipertansiyon ve trombositopeni olabilir. CELESTIAL çalışmasında, birlikte antikoagülasyon tedavisi veya antiplatelet ajanları alan hastalar hariç tutulmuştur. Ayrıca, tedavi edilmemiş veya tamamen tedavi edilmemiş kanamalı veya kanama riski yüksek varisleri olan hastalar da bu çalışmadan dışlanmıştır.
Birinci basamak ilerlemiş RHK'de nivolumabla kombinasyon halindeki kabozantinib çalışmasında (CA2099ER) terapötik dozlarda antikoagülanlar kullanan hastalar dışarıda bırakılmıştır.
Anevrizmalar ve arter diseksiyonları
VEGF yolak inhibitörlerinin, hipertansiyonu olan veya olmayan hastalarda kullanılması, anevrizmalar ve/veya arter diseksiyonlarının oluşumunu kolaylaştırabilir. CABOMETYX başlamadan önce hipertansiyon veya anevrizma öyküsü gibi risk faktörleri olan hastalarda bu risk dikkatle değerlendirilmelidir.
Trombositopeni
HSK çalışmasında (CELESTIAL), trombositopeni ve trombosit azalması bildirilmiştir. Trombosit seviyeleri kabozantinib tedavisi sırasında izlenmeli ve trombositopeninin ciddiyetine göre doz değiştirilmelidir (bkz. Tablo 1).
Yara komplikasyonları
Kabozantinib ile birlikte yara komplikasyonları gözlenmiştir. Kabozantinib tedavisi mümkünse dental cerrahi operasyonlar veya invaziv dental prosedürler dahil olmak üzere planlı cerrahilerden en az 28 gün önce kesilmelidir. Cerrahiden sonra kabozantinib tedavisine devam etme kararı yeterli yara iyileşmesine ilişkin klinik karara göre verilmelidir. Tıbbi müdahale gerektiren yara iyileşmesi komplikasyonları yaşayan hastalarda kabozantinib kesilmelidir.
Hipertansiyon
Kabozantinib kullanımı ile birlikte hipertansiyon gözlenmiştir. Kabozantinib tedavisine başlanmadan önce kan basıncı iyi şekilde kontrol altına alınmalıdır. Kabozantinib tedavisi sırasında tüm hastalar hipertansiyon açısından izlenmeli ve gerektiğinde standart anti- hipertansif tedavi uygulanmalıdır. Anti-hipertansiflerin kullanılmasına karşın devam eden hipertansiyon vakalarında kabozantinib dozu azaltılmalıdır.
Hipertansiyon şiddetliyse ve anti-hipertansif tedavisine ve kabozantinib dozunun azaltılmasına karşın devam ediyorsa kabozantinib kesilmelidir. Hipertansif kriz durumunda kabozantinib kesilmelidir.
Osteonekroz
Kabozantinib kullanımı ile birlikte çene osteonekrozu (ÇON) olayları gözlenmiştir. Kabozantinib tedavisine başlanmadan önce ve kabozantinib tedavisi boyunca periyodik olarak oral muayene yapılmalıdır. Hastalara ağız hijyeni uygulamaları konusunda bilgi verilmelidir. Kabozantinib tedavisi, mümkünse, planlanan diş cerrahisi veya invaziv diş prosedürlerinden en az 28 gün önce durdurulmalıdır. Bifosfonatlar gibi ÇON ile ilişkili ajanları alan hastalarda dikkatli olunmalıdır. ÇON yaşayan hastalarda kabozantinib kesilmelidir.
Palmar-plantar eritrodizestezi sendromu
Kabozantinib kullanımı ile birlikte palmar-plantar eritrodizestezi sendromu (PPES) gözlenmiştir. PPES şiddetli olduğunda kabozantinib tedavisine ara verilmesi düşünülmelidir.
PPES derece 1'e gerilediğinde kabozantinib tedavisi daha düşük bir dozla yeniden başlatılmalıdır.
Proteinüri
Kabozantinib kullanımı ile birlikte proteinüri gözlenmiştir. Kabozantinib tedavisi sırasında idrardaki protein düzeyi düzenli şekilde izlenmelidir. Nefrotik sendrom gelişen hastalarda kabozantinib kullanımı kesilmelidir.
Posterior reversibl ensefalopati sendromu
Kabozantinib kullanımı ile birlikte Posterior Reversibl Ensefalopati Sendromu (PRES) gözlenmiştir. Nöbetler, baş ağrısı, görme bozuklukları, konfüzyon veya zihinsel fonksiyon değişikliklerinin de aralarında olduğu birden fazla semptom sergileyen tüm hastalarda bu sendrom düşünülmelidir. PRES gözlenen hastalarda kabozantinib tedavisi kesilmelidir.
QT aralığında uzama
Kabozantinib QT aralığı uzaması öyküsüne sahip hastalarda, anti-aritmikler alan hastalarda veya önceden mevcut önemli kardiyak hastalık, bradikardi veya elektrolit bozuklukları olan hastalarda dikkatli şekilde kullanılmalıdır. Kabozantinib kullanılırken tedavi sırasında EKG ve elektrolitlerin (serum kalsiyum, potasyum ve magnezyum) izlenmesini de içeren periyodik takip düşünülmelidir.
Tiroid disfonksiyonu
Tüm hastalarda başlangıçta tiroid fonksiyonunun laboratuvar ölçümü önerilir. Önceden hipotiroidizmi veya hipertiroidizmi olan hastalar, kabozantinib tedavisine başlamadan önce standart tıbbi uygulamaya göre tedavi edilmelidir. Kabozantinib tedavisi sırasında tüm hastalar tiroid disfonksiyonunun belirti ve semptomları açısından yakından izlenmelidir. Kabozantinib tedavisi boyunca tiroid fonksiyonu periyodik olarak izlenmelidir. Tiroid disfonksiyonu gelişen hastalar standart tıbbi uygulamaya göre tedavi edilmelidir.
Biyokimyasal laboratuvar test anormallikleri
Kabozantinib, artan elektrolit anormallikleri (hipo ve hiperkalemi, hipomagnezemi, hipokalsemi, hiponatremi dahil) insidansı ile ilişkilendirilmiştir. Kabozantinib tedavisi sırasında biyokimyasal parametrelerin izlenmesi ve gerektiğinde standart klinik uygulamaya göre uygun replasman tedavisi başlatılması önerilmektedir. Kabozantinib tedavisi sırasında biyokimyasal parametrelerin izlenmesi ve gerektiğinde standart klinik uygulamaya göre uygun replasman tedavisi başlatılması önerilmektedir. HSK hastalarında hepatik ensefalopati vakaları elektrolit bozukluklarının gelişmesine bağlanabilir. Sürekli veya tekrarlayan önemli anormallikler olması durumunda doz kesme veya azaltımı veya kabozantinibi kalıcı olarak kesme düşünülmelidir (bkz. Tablo 1).
CYP3A4 indükleyicileri ve inhibitörleri
Kabozantinib bir CYP3A4 substratıdır. Kabozantinibin güçlü CYP3A4 inhibitörü ketokonazolle eş zamanlı uygulanması kabozantinibin plazma maruziyetinde bir artışa neden olmuştur. Kabozantinib güçlü CYP3A4 inhibitörleri olan ajanlarla birlikte uygulanırken
dikkatli olunması gerekmektedir. Kabozantinibin güçlü CYP3A4 indükleyici rifampisinle eş zamanlı uygulanması kabozantinibin plazma maruziyetinde bir düşüşe neden olmuştur. Bu nedenle güçlü CYP3A4 indükleyiciler olan ajanların kronik şekilde kabozantinible birlikte uygulanmasından kaçınılmalıdır (bkz. Bölüm 4.2 ve 4.5).
P-glikoprotein substratları
MDCK-MDR1 hücrelerinin kullanıldığı iki yönlü bir tayinde kabozantinibin P-glikoprotein (P- gp) transportunun substratı değil bir inhibitörü (IC= 7,0 μM) olduğu görülmüştür. Bu nedenle kabozantinib, eşzamanlı uygulanan P-gp substratlarının plazma konsantrasyonlarını artırma potansiyeline sahip olabilir.
Hastalar kabozantinib kullanırken P-gp substratı (örneğin feksofenadin, aliskiren, ambrisentan, dabigatran eteksilat, digoksin, kolşisin, maravirok, posakonazol, ranolazin, saksagliptin, sitagliptin, talinolol, tolvaptan) alımı konusunda uyarılmalıdır (bkz. Bölüm 4.5).
MRP2 inhibitörleri
MRP2 inhibitörlerinin uygulanması, kabozantinibin plazma konsantrasyonlarında artışa yol açabilir. Bu nedenle MRP2 inhibitörlerinin (örneğin siklosporin, efavirenz, emtrisitabin) eşzamanlı kullanımı konusunda dikkatli olunmalıdır (bkz. Bölüm 4.5).
Yardımcı maddelerle ilgili uyarılar
Laktoz
Nadir kalıtımsal galaktoz intoleransı, toplam laktaz yetmezliği ya da glukoz-galaktoz malabsorpsiyon problemi olan hastaların bu tıbbi ürünü kullanmamaları gerekir.
Sodyum
Bu tıbbi ürünün her bir tableti 1 mmol'den (23 mg) daha az sodyum içerir, dolayısıyla esasında sodyum içermediği kabul edilebilir.
4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri
Diğer tıbbi ürünlerin kabozantinib üzerindeki etkileri CYP3A4 inhibitörleri ve indükleyicileri
Güçlü CYP3A4 inhibitörü ketokonazolün (27 gün boyunca her gün 400 mg) sağlıklı gönüllülere uygulanması kabozantinibin klirensini azaltmış (%29 oranında) ve tek doz plazma kabozantinib maruziyetini (EAA) %38 arttırmıştır. Bu nedenle güçlü CYP3A4 inhibitörlerinin (örneğin ritonavir, itrakonazol, eritromisin, klaritromisin, greyfurt suyu) kabozantinib ile birlikte uygulanmasına dikkatle yaklaşılmalıdır.
Güçlü CYP3A4 indükleyici rifampisinin (31 gün boyunca her gün 600 mg) sağlıklı gönüllülere uygulanması kabozantinibin klirensini arttırmış (4,3 kat) ve tek doz plazma kabozantinib maruziyetini (EAA) %77 azaltmıştır. Bu nedenle, güçlü CYP3A4 indükleyicilerin (örneğin fenitoin, karbamazepin, rifampisin, fenobarbital veya sarı kantaron [Hypericum perforatum] içeren bitkisel preparatlar) kabozantinib ile birlikte kronik kullanımından kaçınılmalıdır.
Gastrik pH'ı değiştiren ilaçlar
Sağlıklı gönüllülere proton pompası inhibitörü (PPI) esomeprazolün (6 gün süresince günde 40 mg) 100 mg tek doz kabozantinib ile birlikte uygulanması, plazma kabozantinib maruziyeti (EAA) üzerinde klinik açıdan anlamlı herhangi bir etki ortaya çıkarmamıştır. Gastrik pH'ı değiştiren ajanlar (yani PPI'lar, H2 reseptörü antagonistleri ve antasitler) kabozantinib ile birlikte uygulanırken herhangi bir dozaj ayarlaması endike değildir.
MRP2 inhibitörleri
In vitro veriler kabozantinibin bir MRP2 substratı olduğunu göstermektedir. Bu nedenle MRP2 inhibitörlerinin uygulanması, kabozantinibin plazma konsantrasyonlarında artışlara yol açabilir.
Safra tuzu sekestranları
Kolestiramin ve kolestagel gibi safra tuzu sekestranları kabozantinible etkileşime girebilir ve emilimi (veya yeniden emilimi) etkileyerek potansiyel olarak azalmış maruziyet ortaya çıkarabilir (bkz. Bölüm 5.2). Bu potansiyel etkileşimlerin klinik anlamlılığı bilinmemektedir.
Kabozantinibin diğer tıbbi ürünler üzerindeki etkileri
Kabozantinibin kontraseptif steroidlerin farmakokinetiği üzerindeki etkisi araştırılmamıştır. Kontraseptif etkinin değişmeyeceği garanti edilemeyeceğinden bariyer yöntemi gibi ilave bir kontraseptif yöntem kullanılması önerilir.
Kabozantinibin warfarinin farmakokinetiği üzerindeki etkisi araştırılmamıştır. Warfarin ile bir etkileşim mümkün olabilir. Bu gibi bir kombinasyon durumunda INR değerleri takip edilmelidir.
P-glikoprotein substratları
MDCK-MDR1 hücrelerinin kullanıldığı iki yönlü bir tayinde kabozantinibin P-gp transportunun substratı değil bir inhibitörü (IC= 7,0 μM) olduğu görülmüştür. Bu nedenle kabozantinib, eşzamanlı uygulanan P-gp substratlarının plazma konsantrasyonlarını artırma potansiyeline sahip olabilir. Hastalar kabozantinib kullanırken P-gp substratı (örneğin feksofenadin, aliskiren, ambrisentan, dabigatran eteksilat, digoksin, kolşisin, maravirok, posakonazol, ranolazin, saksagliptin, sitagliptin, talinolol, tolvaptan) alımı konusunda uyarılmalıdır.
4.6. Gebelik ve laktasyon
Gebelik kategorisi: D
Çocuk doğurma potansiyeli bulunan kadınlar/ Doğum kontrolü (Kontrasepsiyon) Hayvan çalışmalarına dayanarak, kabozantinib gebe kadınlara uygulandığında fetusta hasar oluşturabilir. Gebe kalma potansiyeli olan kadınlar kabozantinib tedavisi sırasında gebe kalmaktan kaçınmalıdır.
Çocuk doğurma potansiyeline sahip kadınlar kabozantinib kullandıkları sırada gebelikten kaçınmaları konusunda uyarılmalıdır. Kabozantinib alan erkek hastaların kadın partnerleri de gebelikten kaçınmalıdır. Tedavi sırasında ve tedavinin tamamlanmasını takip eden en az 4 ay süresince erkek ve kadın hastalar ve bunların partnerleri etkili doğum kontrol yöntemleri uygulamalıdır. Oral kontraseptifler belki de “etkili doğum kontrol yöntemleri†olarak kabul edilemeyebileceğinden bariyer yöntemler gibi bir başka yöntemle birlikte kullanılmaları gerekir (bkz. Bölüm 4.5).
Gebelik dönemi
Kabozantinib kullanan hamile kadınlar üzerinde herhangi bir çalışma yapılmamıştır. CABOMETYX'in gebelik ve/veya fetus/yeni doğan üzerinde zararlı farmakolojik etkileri bulunmaktadır. Hayvanlar üzerinde gerçekleştirilen çalışmalar embriyo-fetal ve teratojenik etkiler ortaya koymuştur (bkz. Bölüm 5.3). İnsanlar açısından söz konusu olan risk bilinmemektedir. Hastanın klinik durumu CABOMETYX ile tedaviyi gerekli kılmadığı takdirde kabozantinib hamilelik sırasında kullanılmamalıdır.
Laktasyon dönemi
Emzirilen bebekte ortaya çıkması muhtemel ciddi advers etkiler nedeniyle emziren anne kabozantinib kullanmamalı veya bebeğin emzirilmesine son verilmelidir. Kabozantinib veya metabolitlerinin anne sütüne geçip geçmediği bilinmemektedir. Bebeğin zarar görme potansiyeli nedeniyle anneler CABOMETYX ile uygulanan tedavi sırasında ve tedavinin tamamlanmasını takip eden en az 4 ay süresince emzirmeyi kesmelidir.
Üreme yeteneği/Fertilite
İnsan fertilitesine ilişkin herhangi bir bilgi bulunmamaktadır. Klinik dışı güvenlilik bulguları ışığında, erkek ve kadın fertilitesi CABOMETYX tedavisinden zarar görebilir (bkz. Bölüm 5.3). Hem erkeklere hem de kadınlara bu konuda tavsiye almaları ve tedaviden önce fertilite korumasını düşünmeleri önerilmelidir.
4.7. Araç ve makine kullanımı üzerindeki etkiler
Kabozantinib motorlu taşıt ve makine kullanma becerisi üzerinde çok az etkiye sahiptir. Bitkinlik ve güçsüzlük gibi advers reaksiyonlar kabozantinib ile ilişkilendirilmiştir. Bu nedenle motorlu taşıt ve makine kullanırken dikkatli olunması önerilmelidir.
4.8. İstenmeyen etkiler
Monoterapi olarak kabozantinib
Güvenlilik profilinin özeti
RHK popülasyonunda (≥ %1 insidans) en yaygın ciddi advers ilaç reaksiyonları abdominal ağrı, diyare, bulantı, hipertansiyon, embolizm, hiponatremi, pulmoner embolizm, kusma, dehidratasyon, yorgunluk, asteni, iştah azalması, derin ven trombozu, baş dönmesi, hipomagnezemi ve palmar-plantar eritrodizestezi sendromudur (PPES).
RHK popülasyonunda tüm derecelerden en sık bildirilen advers reaksiyonlar (hastaların en az
%25'i tarafından yaşanan) diyare, yorgunluk, bulantı, iştah azalması, PPES, hipertansiyon,
kilo kaybı, kusma, disguzi, konstipasyonve AST artışıdır. Hipertansiyon, daha önce VEGF- hedefli tedavi görmüş olan RHK hastalarına (%37) kıyasla hiç tedavi uygulanmamış RHK popülasyonunda (%67) daha sık gözlenmiştir.
HSK popülasyonunda (≥ %1 insidans) en yaygın ciddi advers ilaç reaksiyonları hepatik ensefalopati, asteni, yorgunluk, PPES, diyare, hiponatremi, kusma, abdominal ağrı ve trombositopenidir.
HSK popülasyonunda tüm derecelerden en sık bildirilen advers reaksiyonlar (hastaların en az
%25'i tarafından yaşanan) diyare, iştah azalması, PPES, yorgunluk, bulantı hipertansiyon ve kusmadır.
4.8. İstenmeyen etkiler
Monoterapi olarak kabozantinibin klinik çalışmalarında tanımlanan veya kabozantinibin pazarlama sonrası kullanımından sonra bildirilen istenmeyen etkiler, Tablo 2'de MedDRA sistem organ sınıfı ve sıklık kategorilerine göre listelenmiştir. Sıklıklar tüm dereceleri temel almaktadır ve şu şekilde tanımlanmıştır: çok yaygın (≥1/10), yaygın (≥1/100 ila <1/10), yaygın olmayan (≥1/1.000 ila <1/100), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor) Her sıklık derecesi grubunda istenmeyen etkiler azalan ciddiyet sırasına göre sunulmaktadır.
Tablo 2: Klinik çalışmalarda veya monoterapi olarak kabozantinib ile tedavi edilen hastalarda pazarlama sonrası dönemde bildirilen advers ilaç reaksiyonları (AİR'ler)
Enfeksiyon ve enfestasyonlar | |
Yaygın | apse |
Kan ve lenf sistemi hastalıkları | |
Çok yaygın | anemi, trombositopeni |
Yaygın | nötropeni, lenfopeni |
Endokrin hastalıkları | |
Çok yaygın | hipotiroidizm |
Metabolizma ve beslenme hastalıkları | |
Çok yaygın | iştah azalması, hipomagnezemi, hipokalemi, hipoalbuminemi |
Yaygın | dehidrasyon, hipofosfatemi, hiponatremi, hipokalsemi, hiperkalemi, hiperbilirubinemi, hiperglisemi, hipoglisemi |
Sinir sistemi hastalıkları | |
Çok yaygın | disguzi, baş ağrısı, baş dönmesi |
Yaygın | periferik nöropati (duyusal dahil olmak üzere) |
Yaygın olmayan | konvulsiyon |
Bilinmiyor | serebrovasküler olay |
Kulak ve iç kulak hastalıkları | |
Yaygın | tinnitus |
Kardiyak hastalıklar | |
Bilinmiyor | miyokardiyal enfarktüs |
Vasküler hastalıklar | |
Çok yaygın | hipertansiyon, hemoraji |
Yaygın | derin ven trombozu, venöz tromboz, arteriyel tromboz |
Bilinmiyor | anevrizmalar ve arter diseksiyonları |
Solunum, göğüs bozuklukları ve mediastinal hastalıkları | |
Çok yaygın | disfoni, dispne, öksürük |
Yaygın | pulmoner embolizm |
Gastrointestinal hastalıkları | |
Çok yaygın | diyare, bulantı, kusma, stomatit, konstipasyon, abdominal ağrı, dispepsi, üst abdominal ağrı |
Yaygın | gastrointestinal perforasyon, fistül, gastro-özofageal reflü hastalığı, hemoroid, ağızda ağrı, ağız kuruluğu, disfaji, glossodini |
Yaygın olmayan | pankreatit |
Hepato bilier hastalıkları | |
Yaygın | hepatik ensefalopati* |
Yaygın olmayan | Kolestatik hepatit |
Deri ve deri altı doku hastalıkları | |
Çok yaygın | palmar-plantar eritrodizestezi sendromu, döküntü |
Yaygın | kaşıntı, alopesi, cilt kuruluğu, akneiform dermatit, saç rengi değişikliği, hiperkeratoz, eritem |
Kas-iskelet, bağ doku hastalıkları | |
Çok yaygın | ekstremitede ağrı |
Yaygın | kas spazmaları, artralji |
Yaygın olmayan | çene osteonekrozu |
Böbrek ve idrar yolu hastalıkları | |
Yaygın | proteinüri |
Genel bozukluklar ve uygulama bölgesine ilişkin hastalıkları | |
Çok yaygın | Yorgunluk, mukozal enflamasyon, asteni, periferik ödem |
Araştırmalar | |
Çok yaygın | kilo kaybı, serum ALT artışı, AST artışı |
Yaygın | kan ALP artışı, GGT artışı, kan kreatinin artışı, amilaz artışı, lipaz artışı, kan kolesterol artışı, kan trigliseritleri artışı |
Yaralanma, zehirlenme ve girişimsel komplikasyonlar | |
Yaygın olmayan | yara komplikasyonları |
*Seçilen istenmeyen etkilerin daha fazla karakterize edilmiş açıklaması için bkz Bölüm 4.8.
Birinci basamak ilerlemiş RHK'de nivolumabla kombinasyon halinde kabozantinib
Güvenlilik profilinin özeti
Kabozantinib nivolumabla kombinasyon halinde uygulandığında, tedaviye başlamadan önce nivolumab KÜB'üne bakınız. Nivolumab monoterapisinin güvenlilik profili hakkında daha fazla bilgi için lütfen nivolumab KÜB'üne bakınız.
RHK'de (n=320) iki haftada bir 240 mg nivolumab ile kombinasyon halinde günde bir kez 40 mg kabozantinib veri kümesinde, minimum 16 aylık takipte, en yaygın ciddi advers ilaç reaksiyonları (≥% 1 insidans) diyare, pnömonit, pulmoner emboli, pnömoni, hiponatremi, pireksi, adrenal yetmezlik, kusma, dehidrasyondur.
En sık görülen advers reaksiyonlar (≥%25) diyare, yorgunluk, palmar-plantar eritrodizestezi sendromu, stomatit, kas-iskelet ağrısı, hipertansiyon, döküntü, hipotiroidizm, iştahta azalma, bulantı, karın ağrısıdır. Advers reaksiyonların çoğu hafif ila orta şiddetliydi (Derece 1 veya 2).
4.8. İstenmeyen etkiler
Nivolumabla kombinasyon halindeki kabozantinibin klinik çalışmasında tanımlanan advers reaksiyonlar Tablo 3'te MedDRA Sistem Organ Sınıfı ve sıklık kategorilerine göre listelenmiştir. Sıklıklar tüm dereceleri temel almaktadır ve şu şekilde tanımlanmıştır: çok yaygın (≥1/10), yaygın (≥1/100 ila <1/10), yaygın olmayan (≥1/1.000 ila <1/100), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). Her sıklık derecesi grubunda istenmeyen etkiler azalan ciddiyet sırasına göre sunulmaktadır.
Tablo3: Nivolumab ile Kombinasyon Halindeki Kabozantinib için Advers Reaksiyonlar
Enfeksiyon ve enfestasyonlar | |
Çok yaygın | üst solunum yolu enfeksiyonu |
Yaygın | Pnömoni |
Kan ve lenf sistemi hastalıkları | |
Yaygın | eozinofili |
Bağışıklık sistemi bozuklukları | |
Yaygın | aşırı duyarlılık (anfilaktik reaksiyon dahil) |
Yaygın olmayan | infüzyon ilişkili aşırı duyarlılık reaksiyonları |
Endokrin hastalıkları | |
Çok yaygın | hipotiroidizm, hipertiroidizm |
Yaygın | adrenal yetmezlik |
Yaygın olmayan | hipofizit, tiroidit |
Metabolizma ve beslenme hastalıkları | |
Çok yaygın | İştah azalması |
Yaygın | Dehidrasyon |
Sinir sistemi hastalıkları | |
Çok yaygın | disguzi, baş dönmesi, baş ağrısı |
Yaygın | periferik nöropati |
Yaygın olmayan | otoimmün ensefalit, Guillain-Barré sendromu, myastenik sendrom |
Kulak ve iç kulak hastalıkları | |
Yaygın | Tinnitus |
Göz bozuklukları | |
Yaygın | kuru göz, bulanık görme |
Yaygın olmayan | Üveit |
Kardiyak hastalıklar | |
Yaygın | atriyal fibrilasyon, taşikardi |
Yaygın olmayan | miyokardit |
Vasküler hastalıklar | |
Çok yaygın | hipertansiyon |
Yaygın | tromboz |
Bilinmiyor | Anevrizmalar ve arter diseksiyonları |
Solunum, göğüs bozuklukları ve mediastinal hastalıkları | |
Çok yaygın | disfoni, dispne, öksürük |
Yaygın | pnömonit, pulmoner embolizm, epistaksis, plevral efüzyon |
Gastrointestinal hastalıklar | ||
Çok yaygın | Diyare, kusma, bulantı, konstipasyon, stomatit, karın ağrısı, dispepsi | |
Yaygın | kolit, gastrit, oral ağrı, ağız kuruluğu, hemoroid | |
Yaygın olmayan | Pankreatit, ince bağırsak perforasyonu, glosodini | |
Hepato bilier hastalıkları | ||
Yaygın | hepatit | |
Deri ve deri altı doku hastalıkları | ||
Çok yaygın | palmar-plantar eritrodizestezi sendromu, döküntü, prürit | |
Yaygın | alopesi, cilt kuruluğu, eritem, saç rengi değişikliği | |
Yaygın olmayan | psoriasis, ürtiker | |
Kas iskelet ve bağ doku hastalıkları | ||
Çok yaygın | kas iskelet ağrısı, artralji, kas spazmı | |
Yaygın | artrit | |
Yaygın olmayan | miyopati, çene osteonekrozu, fistül | |
Böbrek ve idrar yolu hastalıkları | ||
Çok yaygın | proteinüri | |
Yaygın | renal yetmezlik, akut böbrek hasarı | |
Yaygın olmayan | nefrit | |
Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklar | ||
Çok yaygın | yorgunluk, pireksi, ödem | |
Yaygın | ağrı, göğüs ağrısı | |
Araştırmalar | ||
Çok yaygın | ALT artışı, AST artışı, hipofosfatemi, hipokalsemi, hipomagnezemi, hiponatremi, hiperglisemi, lenfopeni, alkalin fosfataz artışı, lipaz artışı, amilaz artışı, trombositopeni, kreatinin artışı, anemi, lökopeni, hiperkalemi, nötropeni, hiperkalsemi, hipoglisemi, hipokalemi, toplam bilirubin artışı, hipermagnezemi, hipernatremi, kilo kaybı | |
Yaygın | kandaki kolesterolde artış, hipertrigliseridemi | |
Tablo 3'te sunulan advers reaksiyon sıklıkları, tamamen tek başına kabozantinibe bağlanamaz, ancak altta yatan hastalık veya kombinasyon halinde kullanılan nivolumab bunlara katkıda bulunabilir.
Tromboz, portal | ven | trombozu, pulmoner | ven | trombozu, pulmoner tromboz, aortik | ||||||||||||
| tromboz, | arteriel | tromboz, | derin | ven | trombozu, | pelvik | ven | trombozu, | vena | kava | |||||
trombozu, venöz tromboz, uzuv venöz trombozunu kapsayan kompozit bir terimdir | ||||||||||||||||
Ölümle sonuçlanan vakalar bildirilmiştir. |
|
|
|
|
|
|
|
|
|
| ||||||
Döküntü; dermatit, akneli dermatit, bullöz dermatit, eksfoliatif dermatit, eritematöz | ||||||||||||||||
döküntü, foliküler döküntü, makular döküntü, makülo papüler döküntü, papüler döküntü, | ||||||||||||||||
pruritik döküntü ve ilaç erüpsiyonunu kapsayan kompozit bir terimdir | ||||||||||||||||
Kas iskelet ağrısı; sırt ağrısı, kemik ağrısı, kas-iskelet göğüs ağrısı, kas iskelet rahatsızlığı, | ||||||||||||||||
miyalji, boyun ağrısı, ekstremitelerde ağrı, spinal ağrıyı içeren kompozit bir terimdir. | ||||||||||||||||
Laboratuvar | terimlerinin | sıklıkları, | kilo | kaybı, | kanda | kolesterol | artışı | ve | ||||||||
| hipertrigliseridemi | haricinde | laboratuvar | ölçümlerinde | başlangıca | göre | kötüleşme | |||||||||
| yaşayan hastaların oranını yansıtmaktadır. |
|
|
|
| |||||||||||
Seçilen istenmeyen etkilerin açıklaması
Aşağıdaki reaksiyonlarla ilgili veriler, RHK konusunda gerçekleştirilmiş pivot çalışmalarda daha önce uygulanmış olan VEGF-hedefli tedaviyi takiben ve daha önce tedavi uygulanmamış RHK hastaları ile HSK'de önceki sistemik tedavinin ardından monoterapi olarak oral yolla her
gün 60 mg Cabometyx alan hastaları veya birinci basamak RHK'de nivolumabla kombinasyon halinde oral yolla günde bir kez 40 mg CABOMETYX alan hastaları esas almaktadır (bkz. Bölüm 5.1).
Gastrointestinal (Gİ) perforasyon (bkz. Bölüm 4.4)
RHK'de önceki VEGF-hedefli tedaviyi takiben gerçekleştirilmiş olan çalışmada (METEOR), kabozantinible tedavi uygulanan RHK hastalarının %0,9'unda (3/331) Gİ perforasyonlar bildirilmiştir. Olayların Derece 2 veya 3 olduğu belirlenmiştir. Başlangıca kadar geçen medyan sürenin 10 hafta olduğu görülmüştür.
Daha önce tedavi uygulanmamış hastalar üzerinde gerçekleştirilen RHK çalışmasında (CABOSUN) GI perforasyonlar, kabozantinible tedavi uygulanan hastaların %2,6'sında (2/78) bildirilmiştir. Derece 4 veya 5 olaylar.
HSK çalışmasında (CELESTIAL) Gİ perforasyonlar, kabozantinible tedavi uygulanan hastaların %0,9 unda (4/467) bildirilmiştir. Tüm olaylar Derece 3 veya 4 olduğu belirlenmiştir. Başlangıca kadar geçen medyan sürenin 5,9 hafta olduğu görülmüştür.
İleri evre RHK'de birinci basamak tedavide nivolumab ile kombinasyon halinde (CA2099ER), GI perforasyonlarının insidansı tedavi edilen hastalarda %1,3'tü (4/320). Olaylardan biri 3. Derece, iki olay 4. Derece ve bir olay da 5. Dereceydi (ölümcül).
Kabozantinib klinik programında ölümcül perforasyonlar ortaya çıkmıştır. Hepatik ensefalopati ( bkz. Bölüm 4.4)
HSK çalışmasında (CELESTIAL) hepatik ensefalopati (hepatik ensefalopati, ensefalopati, hiperamonemik ensefalopati), kabozantinible tedavi uygulanan hastaların %5,6'unda (26/467); (%2,8'inde Derece 3-4 olayı ve birinde (%0,2) Derece 5) olayı bildirilmiştir. Başlangıca kadar geçen medyan sürenin 5,9 hafta olduğu görülmüştür. RSK çalışmalarında (METEOR, CABOSUN ve CA2099ER) hepatik ensefalopati vakası rapor edilmemiştir.
Diyare (bkz. Bölüm 4.4)
RHK'de önceki VEGF-hedefli tedaviyi takiben gerçekleştirilmiş olan çalışmada (METEOR) diyare, kabozantinible tedavi uygulanan RHK hastalarının %74'ünde (245/331) (%11'inde Derece 3-4 olaylar) bildirilmiştir. Başlangıca kadar geçen medyan sürenin 4,9 hafta olduğu görülmüştür.
Daha önce tedavi uygulanmamış hastalar üzerinde gerçekleştirilen RHK çalışmasında (CABOSUN) diyare, kabozantinible tedavi uygulanan hastaların %73'ünde (57/78) (%10'unda Derece 3-4 olaylar) bildirilmiştir.
HSK çalışmasında (CELESTIAL) diyare, kabozantinible tedavi uygulanan hastaların %54 unda (251/467) (%9,9'unda Derece 3-4 olaylar) bildirilmiştir. Başlangıca kadar geçen medyan sürenin 4,1 hafta olduğu görülmüştür. Diyare sırasıyla 84/467 (%18), 69/467 (%15), 5/467 (%1) oranında doz değişimine, kesilmesine ve kalıcı olarak kesilmesine neden olmuştur.
İleri evre RHK'de birinci basamak tedavide nivolumab ile kombinasyon halinde (CA2099ER), diyare insidansı tedavi edilen hastaların %64,7'ydi (207/320); %8,4'ünde (27/320) olaylar Derece 3-4 şeklindeydi. Tüm olayların başlangıcına kadar geçen medyan süre 12,9 haftaydı. Diyare olan hastaların sırasıyla %26,3'ünde (84/320) doz gecikmesi veya azaltılması ve
%2,2'sinde (7/320) bırakılması meydana gelmiştir. Fistüller (bkz. Bölüm 4.4)
RHK'de önceki VEGF-hedefli tedaviyi takiben gerçekleştirilmiş olan çalışmada (METEOR), kabozantinible tedavi uygulanan hastaların %1,2'sinde (4/331) fistüller bildirilmiştir ve hastaların %0,6'sında (2/331) görülen anal fistüller de buna dahildir. Olaylardan bir tanesinin Derece 3, kalanların ise Derece 2 olduğu saptanmıştır. Başlangıca kadar geçen medyan sürenin 30,3 hafta olduğu görülmüştür. Daha önce tedavi uygulanmamış hastalar üzerinde gerçekleştirilen RHK çalışmasında (CABOSUN) hiç fistül vakası bildirilmemiştir.
HSK çalışmasında (CELESTIAL); HSK hastalarının %1,5'inde (7/467) fistüller bildirilmiştir. Başlangıca kadar geçen medyan sürenin 14 hafta olduğu görülmüştür.
İleri evre RHK'de birinci basamak tedavide nivolumab ile kombinasyon halinde (CA2099ER), fistül insidansı tedavi edilen hastalarda %0,9'du (3/320) ve şiddeti Derece 1'di.
Kabozantinib klinik programında ölümcül fistüller ortaya çıkmıştır. Hemoraji (bkz. Bölüm 4.4)
RHK'de önceki VEGF-hedefli tedaviyi takiben gerçekleştirilmiş olan çalışmada (METEOR), kabozantinible tedavi uygulanan RHK hastalarında şiddetli (Derece ≥ 3) hemorajik olayların insidansının %2,1 (7/331) olduğu belirlenmiştir. Başlangıca kadar geçen medyan sürenin 20,9 hafta olduğu görülmüştür.
Daha önce tedavi uygulanmamış RHK çalışmasında (CABOSUN), kabozantinible tedavi uygulanan RHK hastalarında şiddetli (Derece ≥ 3) hemorajik olayların insidansının %5,1 (4/78) olduğu belirlenmiştir.
HSK çalışmasında (CELESTIAL), kabozantinible tedavi uygulanan hastalarda şiddetli (Derece
≥ 3) hemorajik olayların insidansının %7,3 (34/467) olduğu belirlenmiştir. Başlangıca kadar geçen medyan sürenin 9,1 hafta olduğu görülmüştür.
İleri evre RHK'de birinci basamak tedavide nivolumab ile kombinasyon halinde (CA2099ER), Derece ≥ 3 hemoraji insidansı tedavi edilen hastalarda %1,9'du (6/320).
Kabozantinib klinik programında ölümcül kanamalar ortaya çıkmıştır. Posterior Reversibl Ensefalopati Sendromu (PRES) (bkz. Bölüm 4.4)
METEOR veya CABOSUN veya CA2099ER veya CELESTIAL çalışmasında hiçbir PRES vakası bildirilmemiştir, fakat diğer klinik çalışmalarda (2/4872 gönüllüde, % 0.04) nadiren PRES bildirilmiştir.
RHK'de kabozantinib nivolumab ile kombine edildiğinde karaciğer enzimlerinde artış
Nivolumab ile kombinasyon halinde kabozantinib alan daha önce tedavi edilmemiş RHK'li hastaların klinik bir çalışmasında, ileri evre RCC'li hastalarda kabozantinib monoterapisine göre Derece 3 ve 4 ALT artışı (%10,1) ile AST artışında (%8,2) daha yüksek insidans gözlenmiştir (METEOR çalışmasında ALT %3,6 ve AST %3,3 artmıştır. Derece > 2 ALT veya AST artışı başlangıcına kadar geçen medyan süre 10,1 haftaydı (aralık: 2 ila 106,6 hafta; n=85). Derece > 2 ALT veya AST artışı olan hastalarda, artışlar %91'inde Derece 0-1'e kadar gerilemiş olup, gerilemeye kadar geçen medyan süre 2,29 haftaydı (aralık: 0,4 ila 108,1 hafta).
Tek ajan olarak veya birlikte (n = 25) uygulanan kabozantinib (n = 10) veya nivolumab (n = 10) ile tekrar eprüve edilen Derece ≥2 ALT veya AST artışı olan 45 hasta arasında, kabozantinib alan 4 hastada, nivolumab alan 3 hastada ve hem kabozantinib hem de nivolumab alan 8 hastada Derece ≥2 ALT veya AST artışının tekrarladığı gözlenmiştir.
Hipotiroidizm
RHK'de önceki VEGF-hedefli tedaviyi takiben gerçekleştirilmiş olan çalışmada (METEOR), hipotiroidizm insidansı %21'di (68/331).
Tedavi edilmemiş RHK çalışmasında (CABOSUN), kabozantinib ile tedavi edilen hastalarda hipotiroidizm insidansı %23'tü (18/78).
HSK çalışmasında (CELESTIAL), kabozantinib ile tedavi edilen hastalarda hipotiroidizm insidansı %8,1'di (38/467) ve %0,4'ünde (2/467) olaylar Derece 3'tü.
İleri evre RHK'de birinci basamak tedavide nivolumab ile kombinasyon halinde (CA2099ER), hipotiroidizm insidansı tedavi edilen hastalarda %35,6'ydı (114/320).
Şüpheli advers reaksiyonların raporlanması
Ruhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesine olanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu Türkiye Farmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; eposta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz aşımı ve tedavisi
Kabozantinib doz aşımının herhangi bir spesifik tedavisi yoktur ve doz aşımının olası semptomları belirlenmemiştir.
Doz aşımından şüphelenilmesi durumunda kabozantinib uygulaması durdurulmalıdır ve destekleyici bakım uygulanmalıdır. Herhangi bir olası değişim eğiliminin değerlendirilmesi amacıyla metabolik klinik laboratuar parametreleri en az haftada bir veya klinik açıdan uygun görüldüğü şekilde takip edilmelidir. Doz aşımı ile ilişkili advers reaksiyonlar için semptomatik tedavi uygulanmalıdır.
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: antineoplastik ajan, protein kinaz inhibitörü
ATC kodu: L01EX07.
Etki mekanizması
Kabozantinib tümör büyümesinden, anjiyogenezden, patolojik kemik yeniden modellenmesinden, ilaç direncinden ve metastatik kanser progresyonundan sorumlu birden fazla reseptör tirozin kinazı (RTK) inhibe eden küçük bir moleküldür. Kabozantinib çeşitli kinazlara karşı inhibe edici aktivitesi açısından değerlendirilmiştir ve MET (hepatosit büyüme faktörü reseptörü proteini) ve VEGF (vasküler endotelyal büyüme faktörü) reseptörlerini inhibe ettiği bulunmuştur. Ek olarak kabozantinib GAS6 reseptörü (AXL), RET, ROS1, TYRO3, MER, kök hücre faktörü reseptörü (KIT), TRKB, Fms-benzeri tirozin kinaz-3 (FLT3) ve TIE- 2'nin de aralarında olduğu başka tirozin kinazları da inhibe etmektedir.
Farmakodinamik etkiler
Kabozantinib geniş çeşitlilikte preklinik tümör modellerinde dozla ilişkili tümör büyümesi inhibisyonu ve tümör regresyonu sergilemiştir ve/veya metastazı inhibe etmiştir.
Kardiyak elektrofizyoloji
Medullar tiroid kanseri hastaları üzerinde gerçekleştirilen bir kontrollü klinik çalışmada kabozantinib tedavisine (günde 140 mg dozunda) başlanmasını takiben Fridericia ile düzeltilmiş QT aralığında (QTcF) 29. Günde (fakat 1. Günde değil) başlangıca göre 10 - 15 ms'lik bir artış gözlenmiştir. Bu etki kardiyak dalga formu morfolojisinde bir değişiklikle veya yeni ritimlerle ilişkilendirilmemiştir. Bu çalışmada kabozantinible tedavi uygulanan hastaların veya RHK veya HSK çalışmalarında kabozantinible tedavi uygulanan gönüllülerin hiçbirinde (60 mg dozunda) doğrulanmış QTcF >500 ms gözlenmemiştir.
Klinik etkililik ve güvenlilik
Renal hücreli karsinom (RHK)
Daha önce vasküler endotelyal büyüme faktörü (VEGF) hedefli tedavi gören RHK hastalarındaki randomize çalışma (METEOR)
Önceki vasküler endotelyal büyüme faktörü (VEGF)-hedefli tedaviyi takiben renal hücreli karsinom tedavisinde CABOMETYX'in güvenliliği ve etkililiği randomize, açık etiketli, çok merkezli bir faz 3 çalışmada (METEOR) değerlendirilmiştir. Daha önce en az 1 VEGF reseptörü tirozin kinaz inhibitörü (VEGFR TKI) almış olan berrak hücreli bileşene sahip ilerlemiş RHK hastaları (N=658) CABOMETYX (N=330) veya everolimus (N=328) almak üzere randomize edilmiştir (1/1). Hastaların daha önce sitokinlerin ve VEGF'yi, programlı ölüm 1 (PD-1) reseptörünü veya onun ligandlarını hedef alan antikorların da aralarında olduğu başka tedaviler almış olmasına izin verilmiştir. Beyin metastazları tedavi edilmiş olan hastaların çalışmaya katılmasına izin verilmiştir. Progresyonsuz sağkalım (PFS) körleştirilmiş bir bağımsız radyolojik inceleme kurulu tarafından değerlendirilmiştir ve randomize edilmiş olan ilk 375 gönüllü üzerinde primer analiz gerçekleştirilmiştir. Sekonder etkililik sonlanma noktaları objektif yanıt oranı (ORR) ve genel sağkalım (OS) olarak belirlenmiştir.
Tümör değerlendirmeleri ilk 12 ay süresince 8 haftada bir ve ardından 12 haftada bir gerçekleştirilmiştir.
Başlangıçtaki demografik özellikler ve hastalık özellikleri CABOMETYX ve everolimus kollarında birbiri ile benzerlik sergilemiştir.
Hastaların çoğunun erkek (%75) ve medyan yaşın 62 olduğu belirlenmiştir. Yüzde yetmiş biri (%71) daha önce yalnızca bir VEGFR TKI almıştır; hastaların %41'inin daha önce aldığı tek VEGFR TKI'nın sunitinib olduğu belirlenmiştir. Prognostik risk kategorisine ilişkin Memorial Sloan Kettering Cancer Center kriterlerine göre %46'sının olumlu (0 risk faktörü), %42'sinin orta (1 risk faktörü) ve %13'ünün kötü (2 veya 3 risk faktörü) olduğu görülmüştür. Hastaların
%54'ünün 3 veya daha fazla organında metastatik hastalık tespit edilmiştir ve bu organları akciğer (%63), lenf düğümleri (%62), karaciğer (%29) ve kemikler (%22) oluşturmaktadır. Medyan tedavi süresinin CABOMETYX alan hastalarda 7,6 ay (aralık 0,3 – 20,5), everolimus alan hastalarda ise 4,4 ay (aralık 0,21 – 18,9) olduğu belirlenmiştir.
CABOMETYX için everolimus ile kıyasla PFS'de istatistiksel olarak anlamlı bir iyileşme gösterilmiştir (Şekil 1 ve Tablo 4). PFS analizi sırasında planlı bir OS analizi gerçekleştirilmiştir ve istatistiksel anlamlılığa ilişkin ara sınıra ulaşmamıştır (202 olay, HR=0,68 [0,51, 0,90], p=0,006). Daha sonra gerçekleştirilen planlı olmayan bir ara OS analizinde CABOMETYX'e randomize edilmiş hastalarda everolimusa kıyasla istatistiksel olarak anlamlı iyileşme ortaya konmuştur (320 olay, medyan 21,4 aya karşılık 16,5 ay; HR=0,66 [0,53, 0,83], p=0,0003; Şekil 2). 430 olayda bir takip analizi (tanımlayıcı) ile OS için karşılaştırılabilir bulgular gözlenmiştir.
ITT popülasyon üzerinde gerçekleştirilen keşifsel PFS ve OS analizleri de yaşa (<65 veya ≥65), cinsiyete, MSKCC risk grubuna (olumlu, orta, kötü), ECOG durumuna (0 veya 1), tanıdan randomizasyona kadar geçen süreye (<1 yıl veya ≥1 yıl), tümör MET durumuna (yüksek veya düşük veya bilinmiyor), kemik metastazları (yok veya var), viseral metastazlar (yok veya var), viseral ve kemik metastazları (yok veya var), önceki VEGFR-TKI'ların sayısı (1 veya ≥2), ilk VEGFR-TKI'nın süresi (≤6 ay veya >6 ay) göre oluşturulmuş farklı alt gruplarda everolimusa kıyasla CABOMETYX lehine tutarlı sonuçlar ortaya koymuştur.
Objektif yanıt oranı bulguları Tablo 5'te özetlenmektedir.
Şekil 1: Daha önce uygulanan vasküler endotelyal büyüme faktörü (VEGF)-hedefli tedavinin ardından RHK'li gönüllülerde bağımsız radyolojik inceleme kurulu incelemesiyle elde edilen Kaplan Meier progresyonsuz sağkalım eğrisi (randomize edilen ilk 375 gönüllü) (METEOR)
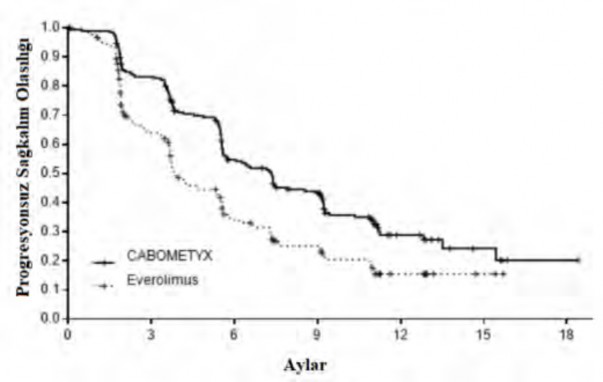
Risk altındaki gönüllülerin sayısı
CABOMETYX 187 | 152 | 92 | 68 | 20 | 6 | 2 |
Everolimus 188 | 99 | 46 | 29 | 10 | 2 | 0 |
Tablo 4: Daha önce uygulanan vasküler endotelyal büyüme faktörü (VEGF)-hedefli tedavinin ardından RHK'li gönüllülerde bağımsız radyolojik inceleme kurulu incelemesiyle elde edilen PFS bulgularının özeti (METEOR)
| Primer PFS analizi popülasyonu | Tedavi amaçlı popülasyon | ||
Sonlanma Noktası | CABOMETYX | Everolimus | CABOMETYX | Everolimus |
| N=187 | N= 188 | N = 330 | N = 328 |
Medyan PFS (%95 GA), ay | 7,4 (5,6, 9,1) | 3,8 (3,7, 5,4) | 7,4 (6,6, 9,1) | 3,9 (3,7, 5,1) |
HR (%95 GA), p değeri | 0,58 (0,45, 0,74), p<0,0001 | 0,51 (0,41, 0,62), p<0,0001 | ||
Şekil 2: Daha önce uygulanan vasküler endotelyal büyüme faktörü (VEGF)-hedefli tedavinin ardından RHK'li gönüllülerde genel sağkalıma ilişkin Kaplan-Meier eğrisi (METEOR)
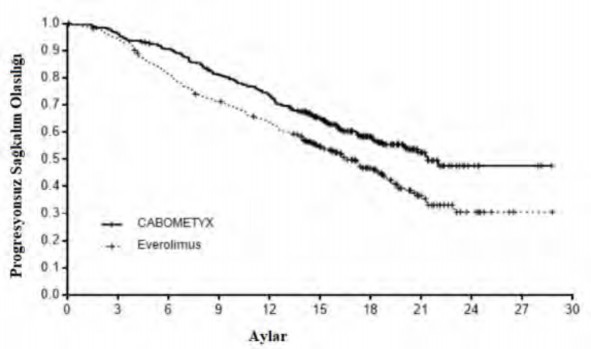
Risk altındaki gönüllülerin sayısı
CABOMETYX | 330 | 318 | 296 | 264 | 239 | 178 | 105 | 41 | 6 | 3 | 0 |
Everolimus | 328 | 307 | 262 | 229 | 202 | 141 | 82 | 32 | 8 | 1 | 0 |
Tablo 5: Daha önce uygulanan vasküler endotelyal büyüme faktörü (VEGF)-hedefli tedavinin ardından RHK'li gönüllülerde bağımsız radyolojik inceleme kurulu (IRC) incelemesiyle elde edilen ORR bulgularının özeti
| Primer analiz ORR tedavi amaçlı popülasyon (IRC) | Araştırmacının incelemesine göre ORR tedavi amaçlı popülasyon | ||
Sonlanma noktası | CABOMETY X | Everolimus | CABOMETYX | Everolimus |
| N = 330 | N = 328 | N = 330 | N = 328 |
ORR (yalnızca kısmi yanıtlar) (%95 GA) | %17 (%13, %22) | %3 (%2, %6) | %24 (%19, %29) | %4 (%2, %7) |
p değeri | P < 0,0001 | P < 0,0001 | ||
Kısm yanıt | %17 | %3 | %24 | %4 |
İlk yanıta kadar geçen medyan süre, ay (%95 GA) | 1,91 (1,6, 11,0) | 2,14 (1,9, 9,2) | 1,91 (1,3, 9,8) | 3,50 (1,8, 5,6) |
En iyi yanıt olarak Sstabil hastalık | %65 | %62 | %63 | %63 |
En iyi yanıt olarak progresif hastalık | %12 | %27 | %9 | %27 |
Daha önce tedavi uygulanmamış renal hücreli karsinom hastalarında randomize çalışma (CABOSUN)
Daha önce tedavi uygulanmamış renal hücreli karsinom tedavisinde CABOMETYX'in güvenliliği ve etkililiği randomize, açık etiketli, çok merkezli bir çalışmada (CABOSUN) değerlendirilmiştir. Daha önce tedavi uygulanmamış, lokal olarak ilerlemiş veya metastatik berrak hücreli bileşene sahip RHK hastaları (N=157) CABOMETYX (N=79) veya sunitinib (N=78) almak üzere randomize edilmiştir (1/1). Hastaların, Uluslararası Metastatik RHK Veri Tabanı Konsorsiyumu (IMDC) risk grubu kategorilerine göre tanımlandığı üzere, orta veya kötü riskli hastalığa sahip olması gerekmiştir.
Hastalar IMDC risk grubuna göre ve kemik metastazı varlığına göre (evet/hayır) basamaklandırılmıştır. Hastaların yaklaşık %75'i tedavinin başlamasının öncesinde bir nefrektomi geçirmiştir.
Orta riskli hastalıkta aşağıdaki risk faktörlerinden bir veya ikisi karşılanmıştır, kötü riskli hastalıkta ise üç veya daha fazla faktör karşılanmıştır: RHK tanısından sistemik tedaviye kadar geçen süre < 1 yıl, Hgb < LLN, Düzeltilmiş kalsiyum > ULN, KPS < %80, nötrofil sayısı > ULN ve trombosit sayısı > ULN.
Primer sonlanma noktası PFS olarak belirlenmiştir. Sekonder etkililik sonlanma noktaları objektif yanıt oranı (ORR) ve genel sağkalım (OS) olarak belirlenmiştir. Tümör değerlendirmeleri 12 haftada bir gerçekleştirilmiştir.
Başlangıçtaki demografik özellikler ve hastalık özellikleri CABOMETYX ve sunitinib kollarında birbiri ile benzerlik sergilemiştir. Hastaların çoğunun erkek (%78) ve medyan yaşın 62 olduğu belirlenmiştir. IMDC risk gruplarına göre hasta dağılımı %81 orta (1-2 risk faktörü) ve %19 kötü (≥3 risk faktörü) olmuştur. Çoğu hastanın (%87) ECOG performans durumunun 0 veya 1; hastaların %13'ünün ise ECOG performans durumunun 2 olduğu görülmüştür. Hastaların %36'sında kemik metastazları tespit edilmiştir.
Körleştirilmiş Bağımsız Radyolojik İnceleme Kurulu (IRC) tarafından retrospektif şekilde değerlendirildiği üzere, CABOMETYX ile sunitinible olana kıyasla PFS'de istatistiksel olarak anlamlı iyileşme ortaya konmuştur (Şekil 3 ve Tablo 6). PFS üzerinde araştırmacı tarafından yapılmış analiz ile IRC tarafından yapılmış analizin sonuçları tutarlılık sergilemiştir.
MET durumu hem pozitif hem de negatif olan hastalar CABOMETYX ile sunitinib ile olana kıyasla olumlu bir etki sergilemiştir ve MET durumu pozitif olan hastalarda MET durumu negatif olan hastalara kıyasla daha fazla aktivite gözlenmiştir (sırasıyla HR=0,32 (0,16 , 0,63) ve 0,67 (0,37 , 1,23)).
CABOMETYX tedavisi sunitinible karşılaştırıldığında daha uzun bir sağkalım yönünde eğilim ortaya çıkarmıştır (Tablo 6). Çalışma, OS analizi için yeterli güce sahip değildi ve veriler olgun değildi.
Objektif yanıt oranı (ORR) bulguları Tablo 6'te özetlenmektedir.
Şekil 3: Daha önce tedavi uygulanmamış RHK'li gönüllülerde IRC değerlendirmesine göre progresyonsuz sağkalıma ilişkin Kaplan-Meier eğrisi
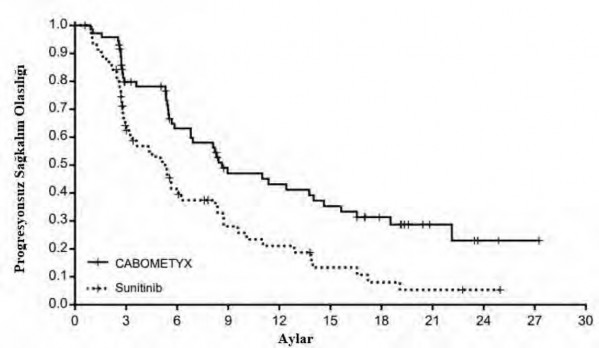
Risk altındaki gönüllülerin sayısı
CABOMETYX | 79 | 51 | 37 | 24 | 22 | 18 | 12 | 5 | 2 | 1 | 0 |
Sunitinib | 78 | 36 | 21 | 12 | 9 | 5 | 3 | 2 | 1 | 0 | 0 |
Tablo 6: Daha önce tedavi uygulanmamış RHK'li gönüllülerde etkililik sonuçları (ITT popülasyon, CABOSUN)
| CABOMETYX (N=79) | Sunitinib (N=78) |
IRC'ye göre progresyonsuz sağkalım (PFS) |
|
|
Ay olarak medyan PFS (%95 GA) | 8,6 (6,2, 14,0) | 5,3 (3,0, 8,2) |
HR (%95 GA); basamaklandırılmış | 0,48 (0,32, 0,73) | |
İki yanlı log-sıra p değeri: basamaklandırılmış | p=0,0005 | |
Araştırmacıya göre progresyonsuz sağkalım (PFS) | ||
Ay olarak medyan PFS (%95 GA) | 8,3 (6,5, 12,4) | 5,4 (3,4, 8,2) |
HR (%95 GA); basamaklandırılmış | 0,56 (0,37, 0,83) | |
İki yanlı log-sıra p değeri: basamaklandırılmış | p=0,0042 | |
Genel sağkalım |
|
|
Ay olarak medyan OS (%95 GA) | 30,3 (14,6, NE) | 21,0 (16,3, 27,0) |
HR (%95 GA); basamaklandırılmış | 0,74 (0,47, 1,14) | |
IRC'ye göre objektif yanıt oranı n (%) |
|
|
Tam yanıtlar | 0 | 0 |
Kısmi yanıtlar | 16 (20) | 7 (9) |
ORR (yalnızca kısmi yanıtlar) | 16 (20) | 7 (9) |
Stabil hastalık | 43 (54) | 30 (38) |
Progresif Hastalık | 14 (18) | 23 (29) |
Araştırmacıya göre Objektif Yanıt Oranı n (%) | ||
Tam yanıtlar | 1 (1) | 0 |
Kısmi yanıtlar | 25 (32) | 9 (12) |
ORR (yalnızca kısmi yanıtlar) | 26 (33) | 9 (12) |
Stabil hastalık | 34 (43) | 29 (37) |
Progresif hastalık | 14 (18) | 19 (24) |
IxRS'ye göre basamaklandırma faktörleri IMDC risk kategorilerinden (orta risk, kötü risk ve kemik metastazı (evet, hayır)) oluşmaktadır.
tehlikeler modeli kullanılarak hesaplanmıştır. Tehlike oranı < 1 kabozantinib lehine progresyonsuz sağkalım göstermektedir
Sunitinib karşısında nivolumab ile kombinasyon halindeki kabozantinib için randomize faz 3 çalışması (CA2099ER)
İleri evre/metastatik RHK'nin birinci basamak tedavisi için 2 haftada bir intravenöz yoldan 240 mg nivolumab ile kombinasyon halinde günde bir kez oral yoldan alınan 40 mg kabozantinibin güvenliliği ve etkililiği, bir faz 3, randomize, açık etiketli çalışmada (CA2099ER) değerlendirilmiştir. Çalışmaya, PD-L1 durumlarına veya IMDC risk grubuna bakılmaksızın, berrak hücreli bileşene sahip ileri evre veya metastatik RHK'li, Karnofsky Performans Durumu (KPS)>%70 ve RECIST v1.1'e göre ölçülebilir hastalığı olan hastalar (18 yaş veya üstü) dahil edilmiştir. Çalışmada, otoimmün hastalığı veya sistemik immünosupresyon gerektiren diğer tıbbi koşulları olan hastalar, daha önce bir anti-PD-1, anti PD-L1, anti-PD-L2, anti-CD137 veya anti-CTLA-4 antikoru ile tedavi görmüş hastalar, antihipertansif tedaviye rağmen hipertansiyonu kontrol edilemeyenler, aktif beyin metastazları ve kontrolsüz adrenal yetmezliği olan hastalar dışarıda bırakılmıştır. Hastalar IMDC prognostik skoru, PD-L1 tümör ekspresyonu ve bölgeye göre katmanlandırılmıştır.
Toplam 651 hasta, her 2 haftada bir intravenöz yoldan uygulanan 240 mg (n =323) nivolumab ile kombinasyon halinde oral olarak günde bir kez 40 mg kabozantinib veya 4 hafta boyunca günde bir kez 50 mg sunitinib (n = 328) ve takiben 2 hafta ara verilerek uygulanacak şekilde randomize edilmiştir. Tedavi, en fazla 24 ay boyunca nivolumab uygulamasıyla hastalık progresyonuna veya kabul edilemez toksisiteye kadar devam etmiştir. Araştırmacı tarafından belirlendiği üzere, hastanın klinik fayda sağlaması ve çalışma ilacını tolere etmesi halinde, araştırmacı tarafından değerlendirilen RECIST versiyon 1.1 ile tanımlanan ilk progresyon sonrasında tedaviye izin verilmiştir. Başlangıç sonrası ilk tümör değerlendirmesi, randomizasyondan sonra 12 haftada (± 7 gün) gerçekleştirilmiştir. Sonraki tümör değerlendirmeleri, 60. Haftaya kadar her 6 haftada bir (± 7 gün), daha sonra radyografik progresyona kadar her 12 haftada bir (± 14 gün) yapılmış ve Körleştirilmiş Bağımsız Merkezi İnceleme (BICR) ile doğrulanmıştır. Primer etkililik sonuç ölçüsü, bir BICR tarafından belirlendiği şekliyle PFS idi. Diğer etkililik ölçüleri arasında kilit sekonder sonlanım noktaları olarak OS ve ORR bulunuyordu.
İki grup arasında başlangıç özellikleri genel olarak dengelenmişti. Medyan yaş 61 olup (aralık: 28-90), %38,4'ü 65 yaşında ve %9,5'i  75 yaşındaydı. Hastaların çoğu erkek (%73,9) ve beyazdı (%81,9). Hastaların yüzde sekizi Asyalıydı, %23,2'si ve %76,5'i, sırasıyla
%70 ila %80 ve %90 ila %100'lük bir başlangıç KPS'sine sahipti. IMDC risk kategorilerine göre hasta dağılımı %22,6 iyi, %57,6 orta ve %19,7 yüksekti. Tümör PD-L1 ekspresyonu açısından, hastaların %72,5'inde PD-L1 ekspresyonu <% 1 veya belirsizdi ve hastaların
%24,9'unda PD-L1 ekspresyonu >% 1'di,. Hastaların %11,5'inde sarkomatoid özellikli tümörler vardı. Tedavinin medyan süresi nivolumab ile birlikte kabozantinible tedavi edilen hastalarda 14,26 ay (aralık: 0,2-27,3 ay) ve sunitinib ile tedavi edilen hastalarda 9,23 aydı (aralık: 0,8-27,6 ay).
Çalışma, nivolumab ile kombinasyon halinde kabozantinibe randomize edilen hastalarda sunitinib ile karşılaştırıldığında PFS, OS ve ORR'de istatistiksel olarak anlamlı bir fayda olduğunu kanıtlamıştır. Önceden belirlenmiş alt gruplarda, IMDC risk kategorileri ve PD-L1 tümör ekspresyon durumunda tutarlı sonuçlar gözlenmiştir.
Primer analizden elde edilen etkililik sonuçları (minimum takip 10,6 ay; medyan takip 18,1 ay) Tablo 7'de gösterilmektedir.
Tablo 7: Etkililik sonuçları (CA2099ER)
| nivolumab + kabozantinib (n = 323) | sunitinib (n = 328) |
BICR'ye göre PFS |
|
|
Olaylar | 144 (%44,6) | 191 (%58,2) |
Tehlike oranı | 0,51 | |
%95 CI | (0,41, 0,64) | |
p-değeri | < 0,0001 | |
Medyan (%95 CI) | 16,59 (12,45, 24,94) | 8,31 (6,97, 9,69) |
OS |
|
|
Olaylar | 67 (%20,7) | 99 (%30,2) |
Tehlike oranı | 0,60 | |
%98,89 CI | (0,40, 0,89) | |
p-değeri | 0,0010 | |
Medyan (%95 CI) | N.E. | N.E. (22,6, N.E.) |
Oran (%95 CI) |
|
|
6 ayda | 93,1 (89,7, 95,4) | 86,2 (81,9, 89,5) |
BICR'ye göre ORR (CR + PR) | 180 (%55,7) | 89 (%27,1) |
(%95 CI) | (50,1, 61,2) | (22,4, 32,3) |
ORR'de Fark (%95 CI) | 28,6 (21,7, 35,6) | |
p-değeri | < 0,0001 | |
Tam yanıt (CR) | 26 (%8,0) | 15 (%4,6) |
Kısmi yanıt (PR) | 154 (%47,7) | 74 (%22,6) |
Stabil hastalık (SD) | 104 (%32,2) | 138 (%42,1) |
Medyan yanıt süresi |
|
|
Ay (aralık ) | 20,17 (17,31, N.E.) | 11,47 (8,31, 18,43) |
Yanıta kadar medyan süre |
|
|
Ay (aralık ) | 2,83 (1,0-19,4) | 4,17 (1,7-12,3) |
IMDC prognostik risk skoru (0, 1-2, 3-6), PD-L1 tümör ekspresyonu (%1'e karşı <% 1 veya belirsiz) ve IRT'ye girildiği gibi bölgeye (ABD/Kanada/Batı Avrupa/Kuzey Avrupa, ROW) göre katmanlandırılmış log-sıra testi.
Sunitinib) katman ayarlı fark
PFS'nin primer analizi, yeni kanser tedavisi için sansürlemeyi içeriyordu (Tablo 7). Yeni kanser tedavisi için sansür içeren ve içermeyen PFS sonuçları tutarlıydı.
Sunitinib karşısında, nivolumab ile kombinasyon halindeki kabozantinib kolunda, tümör PD L1 ekspresyonundan bağımsız olarak PFS yararı gözlenmiştir. Tümör PD L1 ekspresyonu ≥ 1% için medyan PFS, nivolumab ile kombinasyon halinde kabozantinib için 13.08 ay, ve sunitinib kolunda 4,67 aydı (HR = 0,45; %95 CI: 0,29, 0,68). Tümör PD L1 ekspresyonu < 1% için medyan PFS, nivolumab ile kombinasyon halinde kabozantinib için 19.84 ay, ve sunitinib kolunda 9,26 aydı (HR = 0,50; %95 CI: 0,38, 0,65).
Sunitinib karşısında, nivolumab ile kombinasyon halindeki kabozantinib kolunda, tümör (IMDC) risk kategorisinden bağımsız olarak PFS yararı gözlenmiştir. İyi risk grubu için medyan PFS'e, nivolumab ile kombinasyon halinde kabozantinib için erişilmemiştir ve sunitinib kolunda 12,81 aydı (HR = 0,60; %95 CI: 0,37, 0,98). Orta risk grubu için medyan PFS, nivolumab ile kombinasyon halinde kabozantinib için 17,71 ay ve sunitinib kolunda 8,38 aydı (HR = 0,54; %95 CI: 0,41, 0,73). Yüksek risk grubu için medyan PFS, nivolumab ile kombinasyon halinde kabozantinib için 12,29 ay ve sunitinib kolunda 4,21 aydı (HR = 0,36;
%95 CI: 0,23, 0,58).
Güncellenmiş bir PFS ve OS analizi, tüm hastaların minimum 16 aylık bir takip süresi ve 23,5 aylık bir medyan takip süresi dolduğunda gerçekleştirilmiştir (bkz. Şekil 4 ve 5). PFS tehlike oranı 0,52'ydi (%95 CI: 0,43, 0,64). OS tehlike oranı 0,66'ydı (%95 CI: 0,50, 0,87). IMDC risk kategorileri ve PD-L1 ekspresyon seviyeleri için alt gruplarda güncellenmiş etkililik verileri (PFS ve OS) orijinal sonuçları doğrulamıştır. Güncellenen analizle iyi risk grubunda medyan PFS'ye ulaşılmıştır.
Şekil 4: Kaplan-Meier PFS eğrileri (CA2099ER)
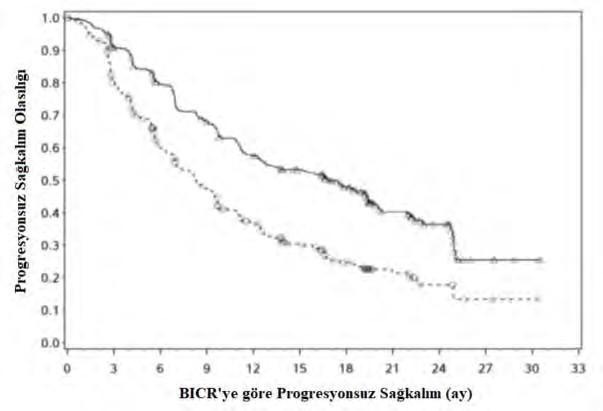
Risk altındaki gönüllülerin sayısı Nivolumab + kabozantinib
323 280 236 201 166 145 102 56 26 5 2 0
Sunitinib
328 230 160 122 87 61 37 17 7 2 1 0
![]()
Nivolumab + kabozantinib (olaylar: 175/323), medyan ve %95 CI : 16,95 (12,58, 19,38)
![]() Sunitinib (olaylar: 206/328), medyan ve %95 CI: 8,31 (6,93, 9,69)
Sunitinib (olaylar: 206/328), medyan ve %95 CI: 8,31 (6,93, 9,69)
Şekil 5: Kaplan Meier OS eğrileri (CA2099ER)
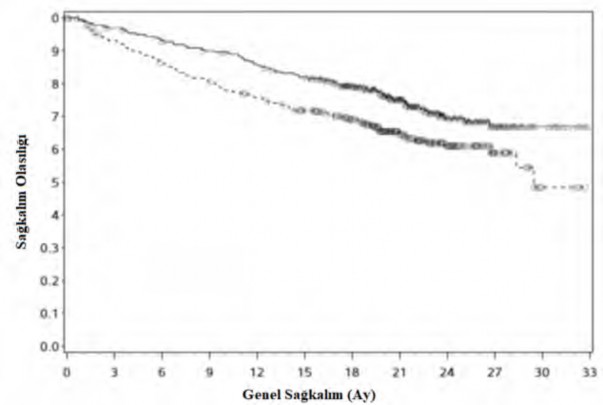
Risk altındaki gönüllülerin sayısı Nivolumab + kabozantinib
323 | 308 | 295 | 283 | 269 | 255 | 220 | 147 | 84 | 40 | 10 | 0 |
Sunitinib |
|
|
|
|
|
|
|
|
|
|
|
328 | 295 | 272 | 254 | 236 | 217 | 189 | 118 | 62 | 22 | 4 | 0 |
![]()
Nivolumab + kabozantinib (olaylar: 86/323), medyan ve %95 CI: NE ![]() Sunitinib (olaylar: 116/328), medyan ve %95 CI: 29,47 (28,35, NE)
Sunitinib (olaylar: 116/328), medyan ve %95 CI: 29,47 (28,35, NE)
Hepatoselüler karsinom
Sorafenib alan hastalarda kontrollü çalışma (CELESTIAL)
CABOMETYX'in güvenliliği ve etkinliği randomize, çift kör, plasebo kontrollü Faz 3 çalışmasında (CELESTIAL) değerlendirilmiştir. Küratif tedaviye uygun olmayan ve daha önce ilerlemiş hastalık için sorafenib alan HSK'lı hastalar (N = 707), CABOMETYX (N = 470) veya plasebo (N = 237) alacak şekilde randomize edilmiştir (2: 1). Hastalar, sorafenibin yanı sıra ilerlemiş hastalık için daha önce bir başka sistemik tedavi almış olabilirler. Randomizasyon, hastalığın etiyolojisi (HBV [HCV ile birlikte olan veya olmayan], HCV [HBV ile olmayan] veya diğer), coğrafi bölge (Asya, diğer bölgeler) ve hastalığın ekstrahepatik yayılımının ve/ veya makrovasküler invazyonun varlığına (Evet, Hayır) göre sınıflara ayrılmıştır.
Primer sonlanma noktası genel sağkalım (OS) olarak belirlenmiştir. Sekonder etkililik sonlanma noktaları progresyonsuz sağkalım (PFS) ve objektif yanıt oranı (ORR) araştırmacı tarafından Katı Tümörlerde Yanıt Değerlendirme Kriterleri (RECIST ) 1.1 kullanılarak belirlenmiştir. Tümör değerlendirmeleri 8 haftada bir gerçekleştirilmiştir. Gönüllüler radyolojik hastalığın ilerlemesinden sonra klinik fayda görürken veya sonraki sistemik veya karaciğer
yönelimli lokal antikanser tedavisine ihtiyaç duyulana kadar kör çalışma tedavisine devam etmişlerdir. Kör tedavi aşamasında plasebodan kabozantinibe çapraz geçişe izin verilmemiştir.
Başlangıçtaki demografik özellikler ve hastalık özellikleri CABOMETYX ve placebo kollarında birbiri ile benzerlik sergilemiştir ve 707 randomize hastanın tümü için aşağıda gösterilmiştir.
Hastaların çoğu erkek (%82) ve medyan yaş 64'tü. Hastaların çoğu (%56) Beyaz ve hastaların
%34'ü Asyalıydı. Hastaların yüzde elli üçünün (%53) ECOG performans durumu (PS) 0 ve
%47'sinin ECOG PS'i 1'di. Hemen hemen tüm hastalar (%99) Child Pugh A ve %1'i Child Pugh B idi. HSK için etiyolojide %38 hepatit B virüsü (HBV), %21 hepatit C virüsü (HCV),
%40 diğer (ne HBV ne de HCV) bulunuyordu. Yüzde yetmiş sekizinde (%78) makroskopik vasküler invazyon ve/veya karaciğer dışı tümör yayılması, %41'inde alfa-fetoprotein (AFP) seviyeleri ≥400μg/L idi, %44'ü lokal-bölgesel transarteryel embolizasyon veya kemoinfüzyon prosedürleriyle tedavi edilmişti ve %37'si kabozantinib tedavisinden önce radyoterapi almıştı. Sorafenib tedavisinin medyan süresi 5,32 aydı. İleri evre hastalık için daha önce hastaların yüzde yetmiş ikisi (%72) 1 ve %28'i 2 sistemik tedavi rejimi almıştır.
OS'de CABOMETYX için plaseboya kıyasla istatistiksel olarak anlamlı bir iyileşme olduğu gösterilmiştir (Tablo 8 ve Şekil 6)
PFS ve ORR bulguları Tablo 8'de özetlenmiştir.
Tablo 8: HSK'da etkililik sonuçları (ITT popülasyon, CELESTIAL)
| CABOMETYX (N=470) | Placebo (N=237) |
Genel sağkalım | ||
Ay olarak medyan OS (%95 GA) | 10,2 (9,1, 12,0) | 8,0 (6,8, 9,4) |
HR (%95 GA) | 0,76 (0,63, 0,92) | |
p-değeri | p=0,0049 | |
Progresyonsuz sağkalım (PFS) | ||
Ay olarak medyan PFS (%95 GA) | 5,2 (4,0, 5,5) | 1,9 (1,9, 1,9) |
HR (%95 GA) | 0,44 (0,36, 0,52) | |
p-değeri | p<0,0001 | |
Kaplan-Meier eğrisine göre 3 ayda olaysız gönüllülerin yüzdesi | ||
% (%95 GA) | %67,0 (%62,2, %71,3) | %33.3 (%27.1, %39.7) |
Objektif yanıt oranı n (%) | ||
Tam yanıtlar (CR) | 0 | 0 |
Kısmi yanıtlar (PR) | 18 (4) | 1 (0,4) |
ORR (CR+PR) | 18 (4) | 1 (0,4) |
p-değeri | p=0,0086 | |
Stabil hastalık | 282 (60) | 78 (33) |
Progresif Hastalık | 98 (21) | 131 (55) |
Şekil 6: Genel sağkalıma ilişkin Kaplan-Meier eğrisi (CELESTIAL)
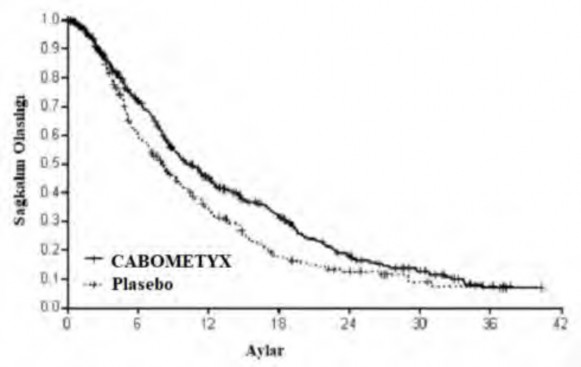
Risk altındaki gönüllülerin sayısı | ||||||||
CABOMETYX | 470 | 281 | 159 | 93 | 44 | 22 | 4 | 0 |
Plasebo | 237 | 117 | 57 | 25 | 15 | 7 | 3 | 0 |
Şekil 7: Progresyonsuz sağkalıma ilişkin Kaplan-Meier eğrisi (CELESTIAL)
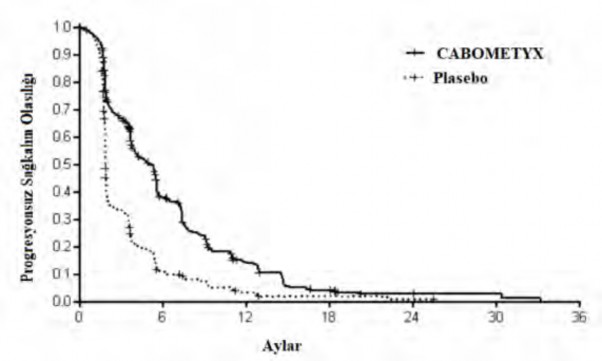
Risk altındaki gönüllülerin sayısı
CABOMETYX | 470 | 131 | 39 | 10 | 3 | 2 | 0 |
Plasebo | 237 | 21 | 5 | 2 | 1 | 0 | 0 |
Sistemik radyasyon dışı ve lokal karaciğere yönelik sistemik protokol olmayan antikanser tedavisi (NPACT) insidansı, kabozantinib kolunda % 26 ve plasebo kolunda %33'tür. Bu tedavileri alan gönüllüler, çalışma tedavisine son vermek zorunda kalmıştır. NPACT kullanımı için sansür uygulayıcı bir inceleme OS analizi, birincil analizi desteklemiştir: tabakalaşma faktörleri (IxRS'e göre) için düzeltilen HR 0.66 (% 95 GA: 0.52, 0.84; tabakalı logrank p-değeri
= 0.0005)'tir. Kaplan-Meier eğrisine göre medyan OS süresi 4.2 aylık fark ile, kabozantinib kolunda 11.1 aya karşılık plasebo kolunda 6.9 ay olarak tahmin edilmiştir.
EuroQoL EQ-5D-5L kullanılarak hastalığa özgü olmayan yaşam kalitesi (QoL) değerlendirilmiştir. CABOMETYX'in plaseboya karşı EQ-5D fayda endeksi skoru üzerinde olumsuz bir etkisi tedavinin ilk haftası boyunca gözlenmiştir. Bu periyot sonunda yalnızca sınırlı QoL verileri elde edilmiştir.
Pediyatrik popülasyon
Avrupa İlaç Ajansı, solid malign tümörlerin tedavisinde pediatrik bir ya da daha fazla alt grubunda CABOMETYX ile yapılan çalışmalardan elde edilen bulguların sunulması zorunluluğunu ertelemiştir. (pediatrik kullanıma ilişkin bilgiler için bkz. Bölüm 4.2).
5.2. Farmakokinetik özellikler
Genel özellikler
Emilim:
Kabozantinibin oral yolla uygulanmasını takiben pik plazma konsantrasyonlarına dozdan 3 ila
4 saat sonra erişilmektedir. Plazma konsantrasyonu-zaman profilleri, kabozantinibin enterohepatik yeniden dolaşıma maruz kaldığına işaret eder şekilde, uygulamadan yaklaşık 24 saat sonra ikinci bir emilim piki olduğunu göstermektedir.
Kabozantinible 19 gün süresince 140 mg dozunda her gün yapılan tekrarlı doz uygulaması tek doz uygulamasına kıyasla yaklaşık 4 ila 5 katlık bir ortalama kabozantinib birikimi ortaya çıkarmıştır (EAA'ya göre); kararlı duruma yaklaşık 15 günde erişilmektedir.
Kabozantinibin 140 mg'lik tek bir oral dozunun uygulandığı sağlıklı gönüllülerde yüksek miktarda yağ içeren bir öğün, açlık durumuna kıyasla, Cmaks ve EAA değerlerini orta düzeyde arttırmıştır (sırasıyla %41 ve %57). Kabozantinib uygulamasından 1 saat sonra alınan gıdaların kesin etkisi konusunda bilgi bulunmamaktadır.
Sağlıklı gönüllülerde 140 mg'lik tek bir dozun ardından kabozantinib kapsül ile tablet formülasyonları arasında biyoeşdeğerlik ortaya konamamıştır. Tablet formülasyonunun Cmaks değerinde kapsül formülasyonuna kıyasla %19'luk bir artış gözlenmiştir. Kabozantinib tablet ve kapsül formülasyonları arasında %10'un altında bir EAA farkı görülmüştür.
Dağılım:
Kabozantinibin in vitro insan plazmasında proteine bağlanma oranı yüksektir (>%99,7). Popülasyon farmakokinetiği (PF) modeline göre merkez bölmenin (Vc/F) dağılım hacminin 212 L olduğu tahmin edilmiştir.
Biyotransformasyon:
Kabozantinib in vivo metabolize edilmiştir. Plazmada ana maddenin %10'undan yüksek maruziyelerde (EAA) dört metabolit tespit edilmiştir: XL184-N-oksit, XL184 amid kleavaj ürünü, XL184 monohidroksi sülfat ve 6-desmetil amid kleavaj ürünü sülfat.
Ana madde kabozantinibin hedefli kinaz inhibisyonu potensinin <%1'ine sahip iki konjuge olmayan metabolitin (XL184-N-oksit ve XL184 amid klevaj ürünü) her biri toplam ilaçla ilişkili plazma maruziyetinin <%10'unu oluşturmaktadır.
Bir nötralize edici CYP3A4 antikoru, NADPH katalizörlü insan karaciğeri mikrozomal (HLM) inkübasyonunda metabolit XL184 N-oksit oluşumunu >%80 inhibe ettiğinden, kabozantinib bir in vitro CYP3A4 metabolizması substratıdır; bunun aksine CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C19, CYP2D6 ve CYP2E1 nötralize edici antikorları kabozantinib metaboliti oluşumu üzerinde herhangi bir etki ortaya çıkarmamıştır. Bir CYP2C9 nötralize edici antikor kabozantinib metaboliti oluşumu üzerinde minimal etki (yani <%20 azalma) sergilemiştir.
Eliminasyon:
1.883 hasta ve 140 sağlıklı gönüllüden toplanan veriler kullanılarak kabozantinib üzerinde gerçekleştirilen bir popülasyon FK analizinde 20 ila 140 mg aralığında dozların oral yolla uygulanmasının ardından kabozantinibin plazma terminal yarı ömrünün yaklaşık 110 saat olduğu görülmüştür. Kararlı durumdaki ortalama klirensin (CL/F) 2,48 L/sa olduğu hesaplanmıştır. Sağlıklı gönüllülere tek doz 14C-kabozantinib uygulanmasını takip eden 48 günlük bir toplama periyodu içinde, %54'ü feçeste, %27'si ise idrarda olmak üzere, uygulanan toplam radiyoaktivitenin yaklaşık %81'i tespit edilmiştir.
Hastalardaki karakteristik özellikler ve farmakokinetik/farmakodinamik ilişkiler
Böbrek yetmezliği:
Tek bir 60 mg dozunda kabozantinib ile yapılan böbrek yetmezliği çalışmasında, toplam plazma kabozantinib, Cmaks ve EAA0-inf değerlerine ilişkin geometrik LS ortalama oranlarının böbrek fonksiyonu normal olan gönüllülere kıyasla hafif derecede böbrek yetmezliği görülen gönüllülerde %19 ve %30 daha yüksek (Cmaks değerine ilişkin %90 GA %91,60 ila %155,51; EAA0-inf %98,79 ila %171,26), orta derecede böbrek yetmezliği görülen gönüllülerde ise %2 ve %6-7 daha yüksek (Cmaks değerine ilişkin %90 GA %78,64 ila %133,52; EAA0-inf %79,61 ila %140,11) olduğu gösterilmiştir. Bağlanmamış plazma kabozantinib EAA0-inf için geometrik LS ortalamaları, normal böbrek fonksiyonu olan gönüllülere kıyasla, hafif böbrek yetmezliği olan gönüllüler için %0,2 daha yüksek (%90 CI %55,9 ila % 180) ve orta derecede böbrek yetmezliği olanlar için %17 daha yüksekti (% 90 CI %65,1 ila %209,7). Ciddi böbrek yetmezliği olan gönüllüler üzerinde çalışma yapılmamıştır.
Karaciğer yetmezliği:
Sağlıklı gönüllülerde ve kanser hastalarında (HSK dahil) kabozantinibin bütünleşik bir popülasyon farmakokinetik analizine dayanarak, normal karaciğer fonksiyonuna (n = 1425) ve hafif karaciğer yetmezliğine sahip (n = 558) deneklerde ortalama kabozantinib plazma maruziyetinde klinik olarak anlamlı bir fark gözlenmemiştir. UKE-ODÇG (Ulusal Kanser Enstitüsü - Organ Disfonksiyonu Çalışma Grubu) kriterlerine göre orta derecede karaciğer yetmezliği (n = 15) olan hastalarda sınırlı veri vardır. Kabozantinibin farmakokinetiği şiddetli karaciğer yetmezliği olan hastalarda değerlendirilmemiştir.
Irk:
Gerçekleştirilmiş olan bir popülasyon FK analizinde kabozantinibin FK'sinde ırk bazında klinik açıdan anlamlı farklılık tespit edilmemiştir.
5.3. Klinik öncesi güvenlilik verileri
Klinik çalışmalarda advers etkiler gözlemlenmemiştir ancak klinik maruz kalma düzeylerine benzer maruz kalma düzeylerinde hayvanlarda advers etkiler gözlemlenmiştir ve bu, muhtemelen klinik kullanım açısından önem taşımaktadır.
Sıçanlar ve köpekler üzerinde 6 aya varan sürelerle gerçekleştirilen tekrarlı doz toksisitesi çalışmalarında toksisite açısından hedef organların Gİ kanal, kemik iliği, lenfoid dokular, böbrek, adrenal dokular ve üreme sistemi dokuları olduğu görülmüştür. Bu bulgular için advers
etki görülmeyen düzeyin (NOAEL) amaçlanan terapötik dozda insanlardaki klinik maruziyet düzeylerinin altında olduğu belirlenmiştir.
Kabozantinib standart bir grup genotoksisite tayininde mutajenik veya klastojenik potansiyel sergilememiştir. Kabozantinibin karsinojenik potansiyeli iki tür üzerinde değerlendirilmiştir: rasH2 transgenik fareler ve Sprague-Dawley sıçanları. Sıçanlar üzerinde gerçekleştirilen 2 yıllık karsinojenisite çalışmasında, insanlardaki amaçlanan maruziyetin oldukça altında kalan maruziyetlerde kabozantinible ilişkili neoplastik bulgular, her iki cinsiyette adrenal medullada tek başına veya malign feokromositoma/kompleks malign feokromositoma ile birlikte selim feokromositoma insidansında artış şeklinde olmuştur. Sıçanlarda gözlenen neoplastik lezyonların klinik anlamı belirsizdir fakat düşük olması olasıdır.
Kabozantinibin insanlarda amaçlanan terapötik maruziyetten hafifçe daha yüksek maruziyetlerde rasH2 fare modelinde karsinojenik olmadığı görülmüştür.
Sıçanlar üzerine yapılan fertilite çalışmaları erkek ve dişi fertilitesinde azalma ortaya koymuştur. Ek olarak, insanlarda amaçlanan terapötik dozda ortaya çıkan klinik maruziyet düzeylerinin altındaki maruziyet düzeylerinde erkek köpeklerde hipospermatogenez gözlenmiştir.
Sıçanlar ve tavşanlar üzerinde embriyofetal gelişim çalışmaları yapılmıştır. Sıçanlarda kabozantinib implantasyon sonrası kayıp, fetal ödem, yarık damak/dil, dermal aplazi ve kıvrık veya rudimenter kuyruk ortaya çıkmasına neden olmuştur. Tavşanlarda kabozantinib fetal yumuşak doku değişikliklerine (dalak boyutunda azalma, akciğer orta lobunun küçük olması veya mevcut olmaması) neden olmuş ve fetal total malformasyon insidansını arttırmıştır. Embriyofetal toksisite ve teratojenik bulgulara ilişkin NOAEL düzeyinin amaçlanan terapötik dozda insanlardaki klinik maruziyet düzeylerinin altında olduğu belirlenmiştir.
Kabozantinib uygulanan juvenil sıçanlar (>2 yaş pediyatrik popülasyon ile karşılaştırılabilir) artmış WBC parametreleri, azalmış hematopoez, pubesent/olgunlaşmamış dişi üreme sistemi (vajinal açılım gecikmesi olmadan), diş anormallikleri, kemik mineral içeriğinde ve yoğunluğunda azalma, karaciğer pigmentasyonu ve lenf düğümü lenfoid hiperplazisi sergilemiştir. Uterustaki/yumurtalıklardaki bulguların ve azalmış hematopoezin geçici olduğu görülmüştür, kemik parametreleri ve karaciğer pigmentasyonu üzerindeki etkiler ise devam etmiştir. Juvenil sıçanlar (<2 yaş pediyatrik popülasyon ile korelasyon sergiler) tedaviyle ilişkili benzer bulgular sergilemiştir fakat karşılaştırılabilir doz düzeylerinde kabozantinible ilişkili toksisiteye karşı daha hassas oldukları görülmüştür.
6. FARMASÖTİK ÖZELLİKLER
6.1. Yardımcı maddelerin listesi
Tablet içeriği Mikrokristalin selüloz
Laktoz (susuz) (sığır sütünden elde edilir) Hidroksipropil selüloz
Kroskarmelloz sodyum Kolloidal silikon dioksit (susuz) Magnezyum stearat
Film kaplama ajanı Opadry Sarı (03K92254) Hipromelloz 2910
Titanyum dioksit (E171) Triasetin
Sarı demir oksit (E172)
6.2. Geçimsizlikler
Bilinen geçimsizliği yoktur.
6.3. Raf ömrü
48 ay.
6.4. Saklamaya yönelik özel tedbirler
25°C'nin altındaki oda sıcaklığında saklayınız.
6.5. Ambalajın niteliği ve içeriği
Çocuk emniyetli polipropilen kapaklı HDPE şişede, üç tane silika jel desikant kanister ve polyester fiber. Her şişede 30 film kaplı tablet bulunur.
6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
Geçerli olduğu takdirde kullanılmamış olan ürünler ya da atık materyaller ‘Tıbbi Atıkların Kontrolü Yönetmeliği' ve ‘Ambalaj Atıklarının Kontrolü Yönetmeliği' ne uygun olarak imha edilmelidir.
Kullanılmayan tıbbi ürün veya atık materyaller yerel gerekliliklere uygun şekilde bertaraf edilmelidir.
 Grip, Soğuk Algınlığı ve Öksürük
Grip ve soğuk algınlığı (nezle) semptomları arasındaki farkı bilmek önemlidir. Soğuk algınlığı gripten daha hafif belirtiler gösteren bir solunum yolu hastalığıdır.
Grip, Soğuk Algınlığı ve Öksürük
Grip ve soğuk algınlığı (nezle) semptomları arasındaki farkı bilmek önemlidir. Soğuk algınlığı gripten daha hafif belirtiler gösteren bir solunum yolu hastalığıdır. |
 Pankreas Kanseri
Pankreas karnın alt kısmında yatay şekilde bulunan bir organdır. Sindirime yardımcı olan enzimleri ve kan şekerini yönetmeye yardımcı olan hormonları vücuda dağıtmakla görevlidir.
Pankreas Kanseri
Pankreas karnın alt kısmında yatay şekilde bulunan bir organdır. Sindirime yardımcı olan enzimleri ve kan şekerini yönetmeye yardımcı olan hormonları vücuda dağıtmakla görevlidir. |
 |
Depresyonu Anlamak Depresyon farklı kişileri farklı biçimlerde etkiler. Duygusal veya fiziksel olmak üzere geniş alanda belirtilere sebep olabilir.Depresyona neler sebep olur? |
 |
Sırt Ağrısı Sırt ağrısı birden bire ortaya çıkıp şiddetli (akut) olabilir veya zamanla gelişip daha uzun süreli sorunlara (kronik) neden olabilir. |
 |
Artrit Artrit, oldukça yaygın bir hastalıktır ancak iyi anlaşılamamıştır. Aslında “artrit” tek bir hastalığın adı değildir; eklem ağrısı veya eklem hastalıklarını adlandırmanın gayri resmi yoludur. |
İLAÇ GENEL BİLGİLERİ
Gen İlaç Ve Sağlık Ürünleri San. Ve Tic. Ltd. Sti.
| Satış Fiyatı | 157985.37 TL [ 17 Mar 2025 ] |
| Önceki Satış Fiyatı | 157985.37 TL [ 7 Mar 2025 ] |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8699783090463 |
| Etkin Madde | Kabozantinib |
| ATC Kodu | L01EX07 |
| Birim Miktar | 60 |
| Birim Cinsi | MG |
| Ambalaj Miktarı | 30 |
| Antineoplastik ve İmmünomodülatör Ajanlar |
| İthal ( ref. ülke : Yunanistan ) ve Beşeri bir ilaçdır. |