COSOPT OFTALMIIK solüsyon 5 ml Kısa Ürün Bilgisi
{ Timolol Maleat + Dorzolamid }
1. BEŞERİ TIBBİ ÜRÜNÜN ADI
COSOPT® Oftalmik Solüsyon2. KALİTATİF VE KANTİTATİF BİLEŞİM
Etkin maddeler:
Her ml’si, 20 mg dorzolamide eşdeğer 22.26 mg dorzolamid hidroklorür, 5 mg timolola eşdeğer 6.83 mg timolol maleat içerir.
Her ml’si 0.075 mg benzalkonyum klorür içerir.
Sodyum hidroksit ve mannitol için bkz. 4.4.
Yardımcı maddeler için 6.1.’e bakınız.
Yardımcı maddeler için 6.1.’e bakınız.
3. FARMASÖTİK FORMU
Göz damlası, solüsyon.
Berrak, renksiz/hemen hemen renksiz, az viskoz oftalmik solüsyon.
4.1. Terapötik endikasyonlar
4.2. Pozoloji ve uygulama şekli
Pozoloji /uygulama sıklığı ve süresi:
Etkilenmiş gÖz(ler)e günde iki kez bir damla COSOPT.
Başka bir topikal oftalmik ajan kullanılıyorsa, COSOPT ve diğer ajan, aralarında en az 10 dakikalık bir süre olacak şekilde uygulanmalıdır.
Başka oftalmik antiglokom ajan(lar)ın yerine COSOPT başlanacağı zaman, diğer ajan(lar) bir günlük uygun dozdan sonra kesilir ve bunu izleyen gün COSOPT başlanır.
Uygulama şekli:
Hastalar uygulamadan önce ellerini yıkamaları ve damlalığın ucunu göz veya göz çevresine değdirmemeleri konusunda bilgilendirilmelidir.
1. Şişeyi ilk kez açarken ön yüzdeki güvenlik etiketinin açılmamamış olmasına dikkat ediniz. Henüz açılmamış şişelerde, kapak ile şişe arasında bir boşluk olması normal bir durumdur.
Açma kapama okları ►
2. Güvenlik etiketini sıyırarak açınız.
Parmakla basılacak alan ►
Boşluk ►
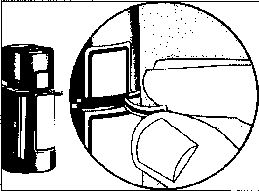
çeviriniz. Kapağı direk olarak çekip çıkartmaya çalışmayınız. Kapağı çekerek çıkartmaya çalışmak şişenin çalışma mekanizmasını bozar.
Parmakla basılacak alan ►
4. Başınızı arkaya doğru eğiniz ve yavaşça alt göz kapağınızı aşağı doğru çekerek göz ile göz kapağı arasında bir boşluk oluşmasını sağlayınız.

5. Şişeyi baş aşağı çeviriniz ve baş veya işaret parmağınızla şişenin üzerindeki parmakla basılacak alana bastırarak doktorunuzun belirttiği şekilde bir damla ilacın göz içine dağılmasını sağlayınız.
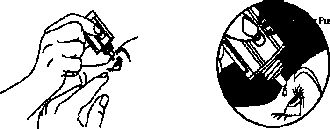
Pusi Parmakla basılacak alan
DAMLALIĞIN UCUNU GÖZ VEYA GÖZ KAPAĞINIZA TEMAS ETTİRMEYİNİZ.
6. Nazolakrimal oklüzyon ya da göz kapaklarında kapanma olduğunda, sistemik emilim azalır. Bu da sistemik yan etkilerde azalmaya ve lokal aktivitede artışa sebep olur.
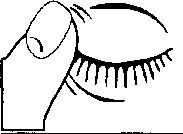
I. COSOPT kullandıktan sonra, gözünüzü bir süre kapayınız ve burun tarafından, gözünüzün köşesine parmağınızla bastırınız ya da 2 dakika boyunca gözkapağınızı kapayınız. Bu, COSOPT’ un gözünüzde kalmasına yardımcı olur.
8. İlacı ilk defa açtığınızda damlatmakta zorlandıysanız kapağı yerine takınız ve kapatınız
# (sıkıştırmayınız), daha sonra kapağın üstündeki okların gösterdiği şekilde kapağı ters yöne
doğru çevirerek açınız.
9. Doktorunuz tarafından belirtilmişse diğer gözünüz için 4 ve 5. basamaklardaki uygulamaları tekrar ediniz.
10. Kapağı şişeye değene dek çevirerek sıkıca kapatınız. İyice kapatmış olduğunuzu anlayabilmeniz için kapağın sol tarafındaki okun, şişenin etiketinde sol tarafta yer alan okla aynı hizada olması gerekmektedir. Olması gerekenden fazla sıkıştırmaya çalışmayınız, şişeye veya kapağa zarar verebilirsiniz.
II. Damlalığın ucu sadece bir damla damlatması için ayarlanmıştır. Damlalığın ucunu genişletmeye çalışmayınız.
12. Kullanmanız gerek dozların tümünü uyguladığınızda hala şişede bir miktar COSOPT kalacaktır. Şişeye ekstra bir miktar ilave edilmiş olduğundan doktorunuzun size reçete ettiği miktarın tamamını kullandıktan sonra kalan kısmını önemsemeyiniz. İlacm şişede kalan kısmını şişeden çıkarmaya çalışmayınız.
fN
Hastalara ilacı kullanmadan önce ellerini yıkamaları ve damlalığın ucunun göz veya gözün etrafına temas etmesinden kaçınmaları gerektiği hakkında bilgi verilmelidir.
Hastalara aynı zamanda göze uygulanan solüsyonlar dikkatli uygulanmadığı takdirde oküler enfeksiyonlara sebep olan sıradan bakterilerle kontamine olabileceği ve sonuçta gözlerde ciddi hasar ve buna bağlı olarak görme kaybı yaşanabileceği hakkında bilgi verilmelidir.
Kontakt Lens Kullananlarda;
Damlanın göze damlatılmasından önce lensler çıkartılmalı ve damla kullanıldıktan sonra en az 15 dakika yeniden takılmamalıdır.
Özel popülasyonlara ilişkin ek bilgiler Böbrek yetmezliği:
COSOPT ile ileri derecede böbrek yetmezliği (kreatinin klerensi <30 ml/dk) olan hastalarda çalışma yapılmamıştır. Dorzolamid esas olarak böbrekler yoluyla atıldığından, COSOPT bu hastalar için önerilmemektedir.
Karaciğer yetmezliği:
COSOPT ile karaciğer yetmezliği olan hastalarda çalışma yapılmamıştır ve bu nedenle bu hastalarda dikkatle kullanılmalıdır.
Pediyatrik popülasyon:
Pediyatrik hastalarda etkinlik ile ilgili yapılmış çalışma yoktur.
2 yaş altı pediyatrik hastalarda güvenlilik incelenmemiştir (> 2 ile < 6 yaş arası pediyatrik hastalann güvenliliği ile ilgili bilgi için bkz. bölüm 5.1.)
Geriyatrik popülasyon:
4.3. Kontrendikasyonlar
COSOPT,
• Reaktif havayolu hastalığı, bronşiyal astımı veya bronşiyal astım öyküsü ya da şiddetli kronik obstrüktif akciğer hastalığı olan hastalarda,
• Sinüs bradikardi si, hasta sinüs sendromu, sino-atriyal blok, ikinci ya da üçüncü derece atriyoventriküler bloğu, belirgin kalp yetmezliği, kardiyojenik şoku olan hastalarda,
• Ciddi renal yetmezlik (kreatinin klerensi <30 ml/dk) veya hiperkloremik asidoz,
• Bu ürünün herhangi bir bileşenine karşı aşırı duyarlılığı olan hastalarda kontrendikedir.
4.4. Özel kullanım uyarıları ve önlemleri
Diğer topikal olarak uygulanan oftalmik ajanlarla olduğu gibi, bu ilaç da sistemik olarak absorbe olabilir. İlacm timolol bileşeni bir beta-blokördür. Bu nedenle beta-blokörlerin sistemik uygulanması sonrasında görülen Prinzmetal anjinanın kötüleşmesi, ciddi periferal ve merkezi dolaşım hastalıklarının kötüleşmesi ve hipotansiyon dahil istenmeyen reaksiyonlar, Topikal uygulama sonrasında da ortaya çıkabilir.
Kardiyo-respiratuvar reaksiyonlar
Timolol maleat bileşeni nedeniyle, COSOPT ile tedaviye başlamadan önce kalp yetmezliği uygun bir şekilde kontrol altına alınmış olmalıdır.
Kalp yetmezliği dahil, kardiyovasküler hastalık geçmişi olan hastalar, bu hastalıkların belirtileri açısından takip edilmeli ve nabız hızları ölçülmelidir, (ör., koroner kalp hastalığı, Prinzmetal anjina).
Birinci derece kalp bloğu olan hastalarda, ileti zamanı üzerine olumsuz etkisi nedeniyle beta-blokörler dikkatle kullanılmalıdır.
Timolol maleat uygulanması sonrasında astımlı hastalarda bronkospazma bağlı ölüm ve nadiren kalp yetmezliğiyle ilişkili ölüm dahil olmak üzere respiratuvar ve kardiyak reaksiyonlar bildirilmiştir.
Hafıf-orta dereceli kronik obstrüktif pulmoner hastalığı olan (KOAH) hastalarda, COSOPT dikkatle, sadece yararın potansiyel risklerin üzerinde olduğu durumlarda kullanılmalıdır.
Vasküler bozukluklar
Şiddetli periferal dolaşım bozukluğu olan hastalar (ör. Raynaud hastalığı ya da Raynaud sendromu) dikkatle tedavi edilmelidir.
Diabetes mellitusTu hastalarda hipoglisemik semptomlann maskelenmesi Beta-adreneıjik blokörler, insülin veya oral hipoglisemik ajan kullanan, spontan hipoglisemisi olan ya da diyabetik hastalarda (özelllikle labil diyabet) dikkatle uygulanmalıdır. Beta-adrenerjik blokör ajanlar akut hipogliseminin işaret ve semptomlarını maskeleyebilir.
Tirotoksikozun maskelenmesi
Beta-adrenerjik blokör ajanlar hipertiroidizmin (ör. taşikardi) bazı klinik belirtilerini maskeleyebilir. Tirotoksikoz geçirmesinden şüphe edilen hastalar, beta-adrenerjik blokör ajan kullanımının beklenmedik şekilde bırakılmasından sonra, tiroid açısından değerlendin lmeldir.
Cerrahi anestezi
Cerrahi öncesi beta-adrenerjik blokör ajanlann bırakılma gerekliliği uygun değildir. Cerrahi sırasında gerekli olduğunda, beta-adreneıjik blokörlerin etkileri adrenerjik agonistlerin yeterli dozlanyla düzeltilebilir. Anestezi uzmanı, hasta timolol kullandığı zaman bilgilendirilmelidir (bkz. bölüm 4.9.).
İmmünoloji ve aşırı duyarlılık
Diğer topikal olarak uygulanan oftalmik ajanlarla olduğu gibi, bu ilaç da sistemik olarak absorbe olabilir. İlacın dorzolamid bileşeni bir sülfonamiddir. Bu nedenle sülfonamidlerin sistemik uygulanması sonrasında görülen istenmeyen etkiler (Stevens-Johnson sendromu ve toksik epidermal nekroliz gibi) topikal uygulanma ile ortaya çıkabilir. Ciddi reaksiyonlar ya da aşırı duyarlılık bulgulan ortaya çıkarsa, bu preparatın kullanılmasına son verilmelidir.
Dorzolamid hidroklorür göz damlası ile benzer lokal oküler istenmeyen etkiler COSOPT ile de gözlemlenmiştir. Bu tür reaksiyonlar meydana gelirse COSOPT uygulamasının sonlandırılması düşünülebilir.
Atopi öyküsü olan ya da çeşitli alerjenlere karşı ileri derecede anafılaktik reaksiyon öyküsü olan hastalar beta-blokör alırlarken, bu aleıjenlerle gerek rastlantı eseri, gerekse tanı ya da tedavi amaçlı nedenlerle tekrarlayan karşılaşmalarda daha da reaktif hale gelebilirler. Bu hastalar, anafılaktik reaksiyonların tedavisinde kullanılan alışılmış adrenalin dozlarına yanıt vermeyebilir.
Eş zamanlı tedavi
Aşağıdaki eş zamanlı tedaviler önerilmemektedir:
Dorzolamid ve oral karbonik anhidraz inhibitörleri Topikal beta-adrenerjik blokör ajanlar
Timolol sistemik beta-blokör ajanla tedavide birarada kullanıldığında, göz-içi basıncı üzerindeki etkisi ya da sistemik beta blokajla birlikte görülen bilinen etkilerinde artış gözlemlenebilir.
Tedavinin kesilmesi
Sistemik beta-blokörlerle olduğu gibi, koroner kalp yetmezliği olan hastalarda oftalmik timolol tedavisinin kesilmesine gerek duyulursa, tedavi kademeli olarak kesilmelidir.
Beta-blokörler ile tedavi, miyastenia gravisin belirtilerini kötüleştirebilir.
Karbonik anhidraz inhibitörlerinin diğer etkileri
Oral karbonik anhidraz inhibitörleriyle tedavi, özellikle daha önceden böbrek taşları gelişme eğilimi olan hastalarda asit-baz bozukluklarına bağlı olarak ürolitiyazis ile ilişkili bulunmuştur. COSOPT ile hiç asit-baz bozukluğu gözlenmemiş olmasına karşın, ürolitiyazis nadiren bildirilmiştir. COSOPT sistemik olarak emilen topikal bir karbonik anhidraz inhibitörü içerdiğinden, daha önce böbrek taşı öyküsü olan hastalar COSOPT kullanırken ürolitiyazis geçirme riskinde artış yaşanabilir.
Diğer
Akut açı kapanması glokomu olan hastalann tedavisi, oküler hipotansif ajanlara ek olarak başka terapötik girişimler de gerektirir. COSOPT ile akut açı kapanması glokomu olan hastalarda çalışma yapılmamıştır.
Daha önceden kronik kornea defektleri olan ve/veya dorzolamid kullanımı sırasında bir intraoküler cerrahi operasyon geçirmiş hastalarda kornea ödemi ve geri dönüşsüz kornea dekompansasyonu bildirilmiştir. Bu tip hastalarda topikal dorzolamid dikkatli kullanılmalıdır,
AkÖz supresan tedavi uygulamasıyla birlikte fıltrasyon prosedürü sonrasında oküler hipotoni ile birlikte koroid ayrılması bildirilmiştir.
Diğer antiglokom ilaçlarının kullanımında olduğu gibi, bazı hastalarda uzun süreli tedaviden sonra oftalmik timolol maleata yanıtta azalma bildirilmiştir. Ancak 164 hastanın en az üç yıl takip edildiği klinik çalışmalarda başlangıçtaki stabilizasyondan sonra ortalama intraoküler basınçta anlamlı fark bulunmamıştır.
Oftalmik beta-blokörler göz kuruluğunu tetikleyebilir. Kornea hastalığı olan hastalar dikkatle tedavi edilmelidir.
Biyolojik test ile etkileşimler
COSOPT, klinik olarak anlamlı elektrolit bozukluklarıyla ilişkili bulunmamıştır.
Yardımcı maddeler:
4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri
COSOPT ile spesifik ilaç etkileşim çalışmaları yapılmamıştır.
Klinik çalışmalarda COSOPT, hiçbir etkileşim olmaksızın sistemik olarak kullanılan aşağıdaki ilaçlarla birlikte kullanılmıştır: ADE-inhibitörleri, kalsiyum kanal blokörleri, diüretikler, aspirin de dahil olmak üzere non-steroid anti-inflamatuvar ilaçlar ve hormonlar (öm., östrojen, insülin, tiroksin).
Bununla birlikte, timolol maleat oftalmik solüsyonunun oral kalsiyum kanal blokörleri, katekolamin depolarını boşaltan ilaçlar ya da beta-adrenerjik bloke edici ajanlar, antiaritmikler (amiodaron dahil), digital glikozitleri, parasempatomimetikler, narkotikler ve monoamin oksidaz (MAO) inhibitörleri ile birlikte kullanılması halinde aditif etki ve hipotansiyon ve/veya belirgin bradikardinin oluşma potansiyeli bulunmaktadır.
CYP2D6 inhibitörleri (ör: kinidin, SSRIs) ve timolol ile kombine tedavi sırasında, sistemik beta-blokör etkide artış (öm., kalp hızında yavaşlama, depresyon) bildirilmiştir.
COSOPT tek başına pupilla büyüklüğüne çok az etki eder ya da hiç etmez. Bazen timolol maleat oftalmik solüsyonu ve epinefrin (adrenalin) birlikte kullanımında midriyazis rapor edilmiştir.
Beta-blokörler antidiyabetik ajanların hipoglisemik etkisini artırabilir.
4.6. Gebelik ve laktasyon
Genel tavsiye
Gebelik kategorisi C.
Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)
COSOPT için, gebeliklerde maruz kalmaya ilişkin klinik veri mevcut değildir.
Gebelik dönemi
COSOPT gebelik dönemi boyunca kullanılmamalıdır.
Dorzolamid
Gebelik döneminde dorzolamide maruz kalımla ilgili yeterli klinik veri yoktur. Tavşanlarda dorzolamid anne için toksik dozlarda teratojenik etkilere yol açmıştır (bkz. bölüm 5.3.).
Timolol
Sistemik beta-blokörlerle yapılan iyi kontrollü epidemiyolojik çalışmalar teratojenik etkilere ilişkin hiçbir bulgu göstermemiştir ancak fetuslarda veya yenidoğanlarda bradikardi gibi bazı farmakolojik etkiler gözlenmiştir. COSOPT doğuma kadar uygulanırsa, yenidoğan yaşamın ilk birkaç gününde dikkatle takip edilmelidir.
Laktasyon dönemi
Dorzolamidin anne sütüne geçip geçmediği bilinmemektedir. Dorzolamid verilen emziren sıçanlarda yavrunun kilo alımında azalma gözlenmiştir. Timolol anne sütüne geçer. COSOPT tedavisi gerekliyse, emzirme önerilmemektedir.
Üreme yeteneği/ Fertilite
4.7. Araç ve makine kullanımı üzerindeki etkiler
4.8. İstenmeyen etkiler
Klinik çalışmalarda COSOPT’a spesifik hiçbir istenmeyen olay gözlenmemiştir; istenmeyen olaylar daha önce, dorzolamid hidroklorür ve/veya timolol ile bildirilenlerle sınırlı olmuştur.
Klinik çalışmalarda 1035 hasta COSOPT ile tedavi edilmiştir. Tüm hastalann yaklaşık %2.4’ü lokal oküler istenmeyen reaksiyonlar nedeniyle tedavisini bırakmıştır; tüm hastaların yaklaşık %1.2’si tedaviyi alerji veya aşırı duyarlılığı (göz kapağı enflamasyonu ve konjunktivit) gösteren lokal istenmeyen reaksiyonlar nedeniyle bırakmıştır.
Aşağıdaki istenmeyen reaksiyonlar klinik çalışmalarda veya pazarlama sonrası deneyimde COSOPT veya bileşenlerinden biriyle bildirilmiştir:
[Çok yaygm (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan (>1/1,000 ila <1/100); seyrek (>1/10,000 ila <1/1000)]
Bağışıklık sistemi hastalıkları:
COSOPT ve timolol maleat göz damlaları:
Seyrek : Anjiyoödem dahil sistemik alerjik reaksiyonların belirtileri, ürtiker, pruritus, döküntü, anafılaksi
Timolol maleat göz damlası, solüsyon:
Seyrek : Anjiyoödem dahil sistemik alerjik reaksiyonların belirtileri, ürtiker, lokal ve genel kızarıklık, anafılaksi Bilinmiyor: Pruritus
Metabolizma ve beslenme hastalıkları:
Timolol maleat göz damlaları:
Bilinmiyor: Hipoglisemi
Psikiyatrik hastalıkları:
Timolol maleat göz damlaları:
Yaygm olmayan; Depresyon*
Seyrek: Uykusuzluk*, kabus görme*, hafıza kaybı
Sinir sistemi hastalıkları:
Dorzolamid hidroklorür göz damlası, solüsyon;
Yaygın: Başağrısı*
Seyrek : Baş dönmesi*, parestezi*
Timolol maleat göz damlası, solüsyon:
Yaygın: Başağnsı*
Yaygın olmayan : Baş dönmesi*, bayılma*
Seyrek : Parestezi*, miyastenia gravis belirtilerinde artış, libidoda düşüş*, serebrovasküler hastalık*, serebral iskemi
Göz hastalıkları:
COSOPT:
Çok yaygın : Yanma ve batma hissi
Yaygın : Konjunktivada kızarıklık, bulanık görme, kornea erozyonu, gözde kaşıntı, göz yaşarması
Dorzolamid hidroklorür göz damlası, solüsyon:
Yaygın : Göz kapağı iltahaplanması*, göz kapağı iritasyonu*
Yaygın olmayan: İridosiklit*
Seyrek : Kızarıklık dahil kaşıntı*, ağrı*, göz kapağının kabuk kaplaması*, geçici miyopluk (tedavi kesilince bu yan etki görülmüyor), korneada ödem*, oküler hipotoni*, koro i dal ayrılma (fıltrasyon cerrahisinin ardından)*
Timolol maleat göz damlası, solüsyon:
Yaygın : Blefarit dahil oküler iltahaplanmanın belirtileri*, keratit*, kornea duyarlılığında azalma ve göz kuruluğu*
Yaygın olmayan : Işığın kırılma değişiklikleri dahil görme bozuklukları (bazı vakalarda miyotik tedavilerin kesilmesinden kaynaklanan)
Seyrek : Pitozis, diplopi, koroidal ayrılma (fıltrasyon cerrahisinin ardından)* (bkz. bölüm
4.4.)
Bilinmiyor: Kaşıntı, göz yaşarması, gözde kızarıklık, bulanık görme, korea erozyonu
Kulak ve iç kulak hastalıkları:
Timolol maleat göz damlası, solüsyon:
Seyrek: Kulak çınlaması*
Kardiyak hastalıklar:
Timolol maleat göz damlası, solüsyon:
Yaygın olmayan: Bradikardi*
Seyrek : Göğüs ağrısı*, çarpıntı*, ödem*, aritmi*, konjestif kalp yetmezliği*, kalp bloğu*, kalp krizi*
Bilinmiyor: Atriyoventriküler blok, kalp yetmezliği
Vasküler hastalıklar:
Timolol maleat göz damlası, solüsyon:
Seyrek: Hipotansiyon*, topallama, Raynaud fenomeni*, ayak ve ellerde soğuma*
Solunum, göğüs bozuklukları ve mediastinal hastalıkları:
COSOPT:
Yaygın: Sinüzit
Seyrek : Nefes darlığı, solunum yetersizliği, rinit, nadiren bronkospazm
Dorzolamid hidroklorür göz damlası, solüsyon:
Seyrek: Burun kanaması*
Timolol maleat göz damlası, solüsyon:
Yaygın olmayan: Dispne*
Seyrek : Bronkospazm (özellikle bronkospastik hastalığa sahip olan hastalarda), solunum güçlüğü, öksürük*
Gastrointestinal hastalıklar:
COSOPT:
Çok yaygın : Disgüzi
Dorzolamid hidroklorür göz damlası, solüsyon:
Yaygın: Bulantı*
Seyrek : Boğazda iritasyon, ağız kuruluğu*
Timolol maleat göz damlası, solüsyon:
Yaygın olmayan : Bulantı*, dispepsi*
Seyrek : Diyare, ağız kuruluğu*
Bilinmiyor: Disgüzi, mide ağrısı, kusma
Deri ve deri altı doku hastalıkları:
COSOPT:
Seyrek: Kontakt dermatit, Stevens-Johnson sendromu, toksik epidermal nekroliz Dorzolamid hidroklorür göz damlası, solüsyon:
Seyrek: Kızarıklık*
Timolol maleat göz damlası, solüsyon:
Seyrek : Alopesi*, psoriyazis benzeri kızarıklık veya psoriyazisin şiddetlenmesi*
Bilinmiyor: Deride döküntü
Kas-iskelet bozukluklar, bağ doku ve kemik hastalıkları:
Timolol maleat göz damlası, solüsyon;
Seyrek : Sistemik lupuz eritematozus Bilinmiyor: Miyalji
Böbrek ve idrar hastalıkları:
COSOPT
Yaygın olmayan: Ürolitiyaz
Üreme sistemi ve meme hastalıkları:
Timolol maleat göz damlası, solüsyon:
Seyrek : Peyronie hastalığı*, libidoda azalma Bilinmiyor: Seksüel disfonksiyon
Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklar:
COSOPT
Seyrek : Anjiyoödem dahil sistemik aleıjik reaksiyonların belirtileri, ürtiker, pruritus, kızanklık, anafılaksi, nadiren bronkospazm Dorzolamid hidroklorür göz damlası, solüsyon:
Yaygın: Asteni/yorgunluk*
Timolol maleat göz damlası, solüsyon:
Yaygın olmayan: Asteni/yorgunluk*
4.9. Doz aşımı ve tedavisi
İnsanlarda COSOPT’un yanlışlıkla ya da bilerek aşırı dozda ağızdan alındığı durumlara ait veriler mevcut değildir.
Semptomlar:
Timolol maleat oftalmik solüsyonun dikkatsizlik sonucunda aşırı dozda kullanılmasının, baş dönmesi, başağrısı, nefes darlığı, bradikardi, bronkospazm ve kardiyak arest gibi sistemik beta-adreneıjik bloke edici ajanlarla görülen etkilere benzer sistemik etkilerle sonuçlandığına dair bildirimler bulunmaktadır. Dorzolamidin aşırı dozda alınması sonucunda en sık beklenecek semptom ve bulgular; elektrolit dengesizliği, asidoz ve olası merkezi sinir sistemi etkileridir.
İnsanlarda dorzolamid hidroklorürün kasıtlı veya kasıtsız alınmasına bağlı doz aşımı hakkında sınırlı bilgiler vardır. Oral kullanımda uyku hali bildirilmiştir. Topikal uygulamada aşağıdaki olaylar bildirilmiştir: bulantı, baş dönmesi, başağrısı, yorgunluk, anormal rüyalar ve disfaji.
Tedavi:
Tedavi semptomatik ve destekleyici olmalıdır. Serum elektrolit düzeyleri (özellikle potasyum) ve kan pH düzeyleri izlenmelidir. Çalışmalar, timololün iyi diyaliz edilmediğini göstermektedir.
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grubu: Oftalmik karbonik anhidrazı inhibe eden bir ilaç ile oftalmik beta-blokör bir ilacın kombinasyonudur.
ATC kodu: S01ED51
Etki mekanizması
COSOPT iki bileşenden oluşmaktadır: dorzolamid hidroklorür ve timolol maleat. Her iki bileşen de aköz hümör salgılanmasını azaltarak yükselmiş intraoküler basıncı azaltır, ancak bu etkilerini farklı etki mekanizmalarıyla gösterir.
Dorzolamid hidroklorür, insan karbonik anhidrazı ITnin güçlü bir inhibitörüdür. Gözün siliyer proseslerindeki karbonik anhidrazın inhibisyonu, olasılıkla sodyum ve sıvı transportunda bir azalma ile sonuçlanacak bikarbonat iyonu oluşmasını yavaşlatarak aköz hümör salgılanmasını azaltır. Timolol maleat nonselektif bir beta-adreneıjik reseptör bloke edici ajandır. Timolol maleatın intraoküler basıncı düşüren kesin etki mekanizması şu anda tam olarak aydınlatılamamıştır ancak bir floresan çalışması ve tonografi çalışmaları baskın etkinin azalmış aköz oluşumuyla ilgili olabileceğini göstermektedir. Bununla birlikte, bazı çalışmalarda dışa akış kolaylığında hafif bir artış da gözlenmiştir. Bu iki ajanın kombine etkileri, her bir bileşenin tek başına, ayrı ayrı uygulandığı durumlarla karşılaştınldığında intraoküler basınçta ek bir azalmayla sonuçlanmaktadır.
Topikal uygulama sonrasında, COSOPT, glokomla ilişkili olsun ya da olmasın, yükselmiş intraoküler basıncı düşürür. Yükselmiş intraoküler basınç, optik sinir hasarı ve glokoma bağlı görme alanı kaybının patogenezinde majör bir risk faktörüdür. COSOPT, gece körlüğü, akomodatif spazm ve pupilla konstriksiyonu gibi, miyotiklerin sık rastlanan yan etkileri olmaksızın intraoküler basıncı düşürür.
Farmakodinamisi Klinik etkiler:
Günde iki kez (sabah-akşam) uygulanan COSOPT’un intraoküler basıncı düşürücü etkisini, birlikte tedavinin uygun bulunduğu glokomlu ya da oküler hipertansiyonlu hastalarda tek başlarına ya da eş zamanlı uygulanan %0.5 timolol ve %2.0 dorzolamid ile karşılaştırmak amacıyla 15 aya kadar süren çalışmalar yürütülmüştür. Burada hem tedavi edilmemiş, hem de timolol monoterapisi ile tam olarak kontrol altına alınamamış hastalar çalışmaya dahil edilmişlerdir. Hastalann büyük bir kısmı çalışmaya katılmadan önce topikal beta-blokör monoterapisi ile tedavi edilmişlerdir. Günde iki kez uygulanan COSOPT’un (koruyucu içeren formülasyon) intraoküler basıncı düşürücü etkisi, günde üç kez uygulanan %2Tik dorzolamid ya da günde iki kez uygulanan %0.5’lik timolol monoterapileriyle elde edilen etkilerden daha fazla bulunmuştur. Günde iki kez verilen COSOPT’un (koruyucu içeren formülasyon) intraoküler basıncı düşürücü etkisi, günde iki kez uygulanan dorzolamid ve günde iki kez uygulanan timololün eş zamanlı tedavisiyle görülen etkiye eşdeğerdir. Günde iki kez uygulanan COSOPT’un (koruyucu içeren formülasyon) intraoküler basıncı gün boyunca düşürücü etkisi gösterilmiş ve bu etki uzun süreli uygulama boyunca devam etmiştir.
Pediyatrik kullanım
5.2. Farmakokinetik özellikler
Dorzolamid hidroklorür
Emilim:
Oral karbonik anhidraz inhibitörlerinin tersine, dorzolamid hidroklorürün topikal yoldan uygulanması, ilacın etkilerini son derece düşük dozlarda doğrudan göz içinde göstermesine ve dolayısıyla sistemik maruz kalmanın daha az olmasına olanak tanımaktadır. Klinik çalışmalarda, bu durum, oral karbonik anhidraz inhibitörlerine özgü elektrolit değişiklikleri veya asit-baz bozuklukları olmaksızın intraoküler basınçta bir azalmaya yol açmıştır.
Dağılım:
Topikal olarak uygulandığında, dorzolamid sistemik dolaşıma ulaşmaktadır. Topikal uygulamanın ardından sistemik karbonik anhidraz (KA) inhibisyonu potansiyelini belirlemek amacıyla, eritrosit ve plazmadaki ilaç ve metabolit konsantrasyonları ve eritrositlerdeki karbonik anhidraz inhibisyonu ölçülmüştür. Dorzolamid kronik doz uygulaması sırasında KA-II’ye selektif bağlanmanın bir sonucu olarak eritrositlerde birikirken, plazmada son derece düşük serbest ilaç konsantrasyonlan sağlanmaktadır.
Bivotransformasvon:
Ana ilaç tek bir N-desetil metaboliti oluşturmaktadır; bu, KA-II’yi ana ilaçtan daha az etkili olarak inhibe etmekle birlikte, daha az aktif olan izoenzimi (KA-I) de inhibe etmektedir. Metabolit de eritrositlerde birikmekte ve temel olarak KA-I’e bağlanmaktadır. Dorzolamidin plazma proteinlerine bağlanması orta düzeydedir (yaklaşık %33).
Eliminasyon:
Dorzolamid başhca idrar yoluyla değişmeden atılır; metaboliti de idrar yoluyla atılır. Doz uygulaması bittikten sonra, dorzolamid eritrositlerden doğrusal olmayan şekilde temizlenir ve bu da başlangıçta ilaç konsantrasyonunda hızlı bir düşüşe yol açar, bunu yaklaşık 4 aylık bir yarılanma ömrü ile daha yavaş bir eliminasyon fazı izler.
Dorzolamid uzun süreli topikal oküler uygulamadan sonraki maksimum sistemik maruz kalımı yansıtan şekilde oral yolla uygulandığında kararlı duruma 13 haftada ulaşılmıştır. Bu amaçla plazma ve eritrositlerdeki (alyuvar) etkin madde ve metabolit konsantrasyonu ile RBC’deki karbonik anhidraz düzeyleri ölçülmüştür. Kararlı durumda plazmada neredeyse hiç serbest etkin madde veya metabolit bulunmamıştır; eritrositlerde KA (karbonik anhidraz) inhibisyonu böbrek fonksiyonu veya solunum üzerinde farmakolojik etki oluşturmak için yeterli olduğu düşünülenden daha azdır. Benzer farmakokinetik sonuçlar dorzolamid hidroklorürün kronik, topikal uygulanmasından sonra da gözlenmiştir. Ancak böbrek fonksiyon bozukluğu olan (hesaplanan kreatin klerensi 30-60 ml/dak) bazı yaşlı hastalann eritrositlerinde metabolit konsantrasyonları daha yüksektir fakat karbonik anhidraz inhibisyonunda anlamlı farklılık olmadığı gibi klinik yönden anlamlı sistemik yan etkilerin hiçbiri bu bulguyla doğrudan ilişkili değildir.
Timolol maleat
Emilim:
Plazma ilaç konsantrasyonu çalışmalannda, %0.5’lik timolol maleat oftalmik solüsyonunun günde iki kez uygulanması sonrasında timolole sistemik olarak maruz kalma oranlan belirlenmiştir. Sabah dozunu izleyen ortalama doruk plazma konsantrasyonu 0.46 ng/ml ve öğleden sonraki dozu izleyen ortalama doruk plazma konsantrasyonu da 0.35 ng/ml olarak belirlenmiştir.
Dağılım:
Timolol plazma proteinlerine çok az oranda bağlanmakta olup, plasenta ve süte geçer. Plazma yarı - ömrü 4 saat olarak bildirilmiştir. Sistemik dolaşıma karışan miktarları ile ilgili herhangi bir veri bulunmamaktadır.
Bivotransformasyon:
Timolol büyük oranda karaciğerde metabolize edilir.
Eliminasyon:
5.3. Klinik öncesi güvenlilik verileri
Her bileşenin oküler ve sistemik emniyet profilleri tamamıyla ortaya konmuştur.
Dorzolamid
Tavşanlarda dorzolamid anneye toksik dozda verildiğinde metabolik asidozun eşlik ettiği, vertebral bölümde malformasyonlar görülmüştür.
Timolol
Hayvan çalışmalarında teratojenik etki göstermemiştir.
Ayrıca dorzolamid hidroklorür ve timolol maleat oftalmik solüsyonuyla topikal olarak tedavi edilen ya da dorzolamid hidroklorür ve timolol maleatm eş zamanlı uygulandığı hayvanlarda göze ait hiç bir istenmeyen yan etki görülmemiştir. Her bir bileşenle yapılan in vitro ve in vivo çalışmalar mutajenik potansiyeli göstermemiştir. Bu nedenle, COSOPT’un terapötik dozlarıyla, insan güvenliği açısından anlamlı risk beklenmemektedir.
6. FARMASÖTİK ÖZELLİKLER
6.1. Yardımcı maddeierin listesi
Benzalkonyum klorür Hidroksietilselüloz Mannitol (E421)
Sodyum sitrat (E331)
Sodyum hidroksit (E524) (pH ayarlaması için)
6.2. Geçimsizlikler
Bilinen bir geçimsizliği yoktur.
6.3. Raf ömrü
24 ay.
6.4. Saklamaya yönelik özel uyarılar
6.5. Ambalajın niteliği ve içeriği
6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
Kullanılmamış olan ürünler ya da atık materyaller "Tıbbi Atıkların Kontrolü Yönetmeliği" ve "Ambalaj ve Ambalaj Atıkları Kontrolü Yönetmeliği "’ne uygun olarak imha edilmelidir.
 Diyabet Hastalığı
Diyabet, insülin hormonu ile ilgili problemlerden kaynaklanan bir hastalıktır.
Diyabet Hastalığı
Diyabet, insülin hormonu ile ilgili problemlerden kaynaklanan bir hastalıktır. |
 Deri Kanseri
Deri kanseri çok rastlanan bir hastalıktır. Üç ana türü bulunur ;genelde kemirici ülser olarak bilinen bazal hücreli karsinom, yassı hücreli karsinom ve kötü huylu tümör.
Deri Kanseri
Deri kanseri çok rastlanan bir hastalıktır. Üç ana türü bulunur ;genelde kemirici ülser olarak bilinen bazal hücreli karsinom, yassı hücreli karsinom ve kötü huylu tümör. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| AZARCOM | 8699844713232 | 158.16TL |
| AZARGA | 8699760710070 | |
| BIMASOPT | 8680199619911 | 464.57TL |
| BRIMO-TIM | 8699844611880 | 171.16TL |
| BRITIL-T | 8680199615579 | 169.76TL |
| Diğer Eşdeğer İlaçlar |
 |
Yüksek Tansiyon Hipertansiyon sürekli anormal derecede yüksek olan kan basıncıdır. Tansiyon atardamarlarınızdaki kanın basıncıdır. |
 |
Yüksek Tansiyon Hipertansiyon sürekli anormal derecede yüksek olan kan basıncıdır. Tansiyon atardamarlarınızdaki kanın basıncıdır. |
 |
İnme İnme, beynin hasar görmesinin sonucudur. Bu hasar, beynin bir kısmındaki ya bir kanama ya da akut kan eksikliği nedeniyle o kısmın geçici ya da kalıcı olarak işlevini yapamamasına yol açar. |
İLAÇ GENEL BİLGİLERİ
Ashfield Sağlık Hizmetleri Tic. Ltd. Şti
| Geri Ödeme Kodu | A02024 |
| Satış Fiyatı | TL |
| Önceki Satış Fiyatı | |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8681608226214 |
| Etkin Madde | Timolol Maleat + Dorzolamid |
| ATC Kodu | S01ED51 |
| Birim Miktar | 5+20 |
| Birim Cinsi | MG+MG |
| Ambalaj Miktarı | 5 |
| Duyu Organları > Göz Tansiyonu İlaçları (Glokom) ve Miyotikler > Timolol Maleat Kombinasyonları |
| İthal ( ref. ülke : Slovakya ) ve Beşeri bir ilaçdır. |