DAPLIG 10 mg film kapl� tablet (28 tablet) K�sa �r�n Bilgisi
{ Dapagliflozin }
1. BE�ER� TIBB� �R�N�N ADI
DAPL�G 10 mg film kapl� tablet
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Dapagliflozin 10 mg
Yard�mc� maddeler
Susuz laktoz (s���r s�t�nden elde edilmektedir) 56,05 mg Yard�mc� maddeler i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Film kapl� tablet
Bir taraf� “10” yaz�l�, sar� veya sar�ms� renkli, elmas �ekilli film kapl� tablet
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Tip 2 diabetes mellitus
DAPL�G eri�kinlerde yetersiz kontrol edilen tip 2 diabetes mellitus tedavisi i�in diyet ve egzersize yard�mc� olarak endikedir.
�ntolerans nedeniyle metformin uygun g�r�lmedi�inde monoterapi olarak
4.2. Pozoloji ve uygulama �ekli
Pozoloji/uygulama s�kl��� ve s�resi:
Tip 2 diabetes mellitus
�nerilen doz g�nde bir defa 10 mg dapagliflozindir.
Dapagliflozin ile ins�lin veya s�lfonil�re gibi ins�lin salg�lat�c� bir ila� kombinasyon halinde kullan�ld���nda, hipoglisemi riskini azaltmak i�in ins�linin veya ins�lin salg�lat�c� ilac�n daha d���k bir dozu d���n�lebilir (bkz. B�l�m 4.5 ve 4.8).
Uygulama �ekli:
DAPL�G g�n�n herhangi bir saatinde yemeklerle birlikte veya a� karn�na g�nde bir defa oral yolla al�nabilir. Tabletler b�t�n olarak yutulmal�d�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
B�brek yetmezli�i:
B�brek fonksiyonuna g�re herhangi bir doz ayarlamas� yap�lmas� gerekli de�ildir.
S�n�rl� deneyim nedeniyle, t�m endikasyonlarda GFR < 25 mL/dak olan hastalarda dapagliflozin tedavisine ba�lanmas� �nerilmez.
Diyabetli hastalarda, glomer�ler filtrasyon h�z� (GFR) < 45 mL/dak oldu�unda dapagliflozinin glikoz d���r�c� etkilili�i azal�r ve �iddetli b�brek yetmezli�i bulunan hastalarda etkililik g�stermemesi olas�d�r. Bu nedenle, GFR'nin 45 mL/dak'�n alt�na d��mesi durumunda, diyabet hastalar�nda ek glikoz d���r�c� tedavi d���n�lmelidir (bkz. B�l�m 4.4, 4.8, 5.1 ve 5.2).
Tablo 1. T�m endikasyonlar i�in eGFR de�erlerine g�re kullan�m �nerileri
eGFR (mL/dak/1,73 m) | Kullan�m �nerisi |
eGFR ≥45 | G�nde bir kez 10 mg a��zdan |
25<eGFR <45 | G�nde bir kez 10 mg a��zdan Dapagliflozinin glikoz d���r�c� etkilili�i azal�r. |
eGFR <25 | Tedavi ba�lanmas� �nerilmez. Muhtemelen dapagliflozinin glikoz d���r�c� etkilili�i yoktur. |
Karaci�er yetmezli�i:
Hafif veya orta derecede karaci�er yetmezli�i olan hastalar i�in herhangi bir doz ayarlamas�na gerek duyulmamaktad�r. A��r derecede karaci�er yetmezli�i olan hastalarda 5 mg ba�lang�� dozu �nerilmektedir. �yi tolere edildi�i takdirde, belirtildi�inde doz 10 mg'a ��kar�labilir (bkz. B�l�m 4.4 ve 5.2).
Pediyatrik pop�lasyon:
Dapagliflozinin 18 ya� alt�nda g�venlili�i ve etkilili�i belirlenmemi�tir. Herhangi bir veri bulunmamaktad�r.
Geriyatrik pop�lasyon (≥ 65 ya�):
Ya�a ba�l� olarak herhangi bir doz ayarlamas�n�n yap�lmas� �nerilmemektedir.
4.3. Kontrendikasyonlar
Dapagliflozin etkin maddesine veya B�l�m 6.1'de listelenen yard�mc� maddelerden herhangi birine kar�� a��r� duyarl�l�k durumunda kontrendikedir.
4.4. �zel kullan�m uyar�lar� ve �nlemleri
B�brek yetmezli�i
S�n�rl� deneyim nedeniyle, GFR <25 mL/dak olan hastalarda dapagliflozin tedavisine ba�lanmas� �nerilmez.
Dapagliflozinin glikoz d���r�c� etkilili�i b�brek fonksiyonuna ba�l� olup, GFR <45 mL/dak olan hastalarda azalmaktad�r ve a��r derecede b�brek yetmezli�i olan hastalarda ise etkililik g�stermemesi olas�d�r (bkz. B�l�m 4.2, 5.1 ve 5.2).
Orta derecede b�brek yetmezli�i olan (GFR <60 mL/dak), tip 2 diyabet hastalar�nda yap�lan bir �al��mada, plasebo ile kar��la�t�r�ld���nda, dapagliflozin ile tedavi edilen hastalar�n daha b�y�k bir k�sm�nda kreatinin, fosfor ve paratiroit hormonu (PTH) art��� ve hipotansiyon gibi advers reaksiyonlar g�zlenmi�tir.
Karaci�er yetmezli�i
Karaci�er yetmezli�i olan hastalarda ger�ekle�tirilen klinik �al��malardan elde edilen deneyim s�n�rl�d�r. Dapagliflozin maruziyeti, a��r derecede karaci�er yetmezli�i olan bireylerde artmaktad�r (bkz. B�l�m 4.2 ve 5.2).
Vol�m deplesyonu ve/veya hipotansiyon riski olan hastalarda kullan�m�
Dapagliflozin etki mekanizmas�na ba�l� olarak, di�rezi artt�r�r ve bu da klinik �al��malarda g�zlenen hafif kan bas�nc� d�����ne yol a�abilir (bkz. B�l�m 5.1). Bu etki, kan glukoz konsantrasyonlar� �ok y�ksek olan bireylerde daha belirgin olabilir.
Anti-hipertansif tedavi almakta olup hipotansiyon �yk�s� olan hastalar ya da ya�l� hastalar gibi, kan bas�nc�nda dapagliflozin kaynakl� bir d�����n risk olu�turabilece�i hastalarda dikkatli olunmal�d�r.
Vol�m deplesyonu yaratabilen e�zamanl� durumlar (�rne�in gastrointestinal hastal�k) mevcut oldu�unda, vol�m deplesyonunun (�rn., fiziksel muayene, kan bas�nc� �l��mleri, hematokrit ve elektrolitleri i�eren laboratuvar testleri) dikkatle izlenmesi �nerilmektedir. Vol�m deplesyonu geli�en hastalarda, kay�p d�zeltilene kadar dapagliflozin tedavisine ge�ici olarak ara verilmesi �nerilmektedir (bkz. B�l�m 4.8).
Diyabetik ketoasidoz
Dapagliflozin dahil olmak �zere sodyum-glukoz ko-transporter 2 (SGLT2) inhibit�rleri ile tedavi edilen hastalarda ya�am� tehdit eden ya da �l�mc�l vakalar dahil olmak �zere nadir diyabetik ketoasidoz (DKA) vakalar� bildirilmi�tir. Baz� vakalarda bu durumun ortaya ��k�� bi�imi atipik olup, kan glukozu de�erleri 14 mmol/L (250 mg/dL) alt�nda olmak �zere sadece orta d�zeyde art�� g�stermi�tir.
Bulant�, kusma, anoreksi, kar�n a�r�s�, a��r� susama, nefes alma g��l���, konf�zyon, al���lmad�k yorgunluk ya da uyuklama gibi spesifik olmayan semptomlar�n ortaya ��kmas� durumunda
diyabetik ketoasidoz riski dikkate al�nmal�d�r. E�er bu semptomlar ortaya ��karsa, kan glukoz d�zeyinden ba��ms�z olarak hastalar derhal ketoasidoz a��s�ndan de�erlendirilmelidir.
Hastalarda DKA ��phesi ya da tan�s� oldu�unda derhal dapagliflozin tedavisi kesilmelidir.
Maj�r cerrahi prosed�rler ya da akut ciddi t�bbi hastal�klar nedeniyle hastaneye yat�r�lan hastalarda tedavi kesilmelidir. Bu hastalarda ketonlar�n izlenmesi �nerilir. Kan keton d�zeylerinin �l��m� idrara tercih edilir. Dapagliflozin tedavisi, keton de�erleri normal oldu�unda ve hastan�n durumu stabilize oldu�unda yeniden ba�lat�labilir.
Dapagliflozin tedavisine ba�lamadan �nce, hasta �yk�s�nde ketoasidoza yatk�nl�k olu�turabilecek fakt�rler g�z �n�nde bulundurulmal�d�r.
Daha y�ksek DKA riski alt�nda olabilecek hastalar, d���k beta-h�cresi fonksiyonu rezervi olan hastalar� (�r. d���k C-peptid bulunan tip 2 diyabet hastalar� ya da eri�kinlerde latent otoimm�n diyabet (LADA) ya da pankreatit �yk�s� bulunan hastalar), k�s�tl� g�da al�m�na neden olan hastal�klar� ya da ciddi dehidratasyon bulunan hastalar�, ins�lin dozlar� azalt�lan hastalar� ve akut t�bbi hastal�k, cerrahi ya da alkol kullan�m�na ba�l� olarak ins�lin gereksinimleri fazla olan hastalar� kapsar. SGLT2 inhibit�rleri bu hastalarda dikkatli �ekilde kullan�lmal�d�r.
SGLT2 inhibit�r� tedavisi alt�ndayken bir DKA ya�ayan hastalarda, ba�ka bir a��k h�zland�r�c� fakt�r belirlenmedik�e ve d�zeltilmedik�e yeniden SGLT2 inhibit�r� tedavisine ba�lanmas� �nerilmez.
Dapagliflozin ile tip 1 diabetes mellitus �al��malar�nda, DKA yayg�n s�kl�kta bildirilmi�tir. Tip 1 diyabeti bulunan hastalar�n tedavisinde dapagliflozin kullan�lmamal�d�r.
Perineal nekrotizan fasiit (Fournier kangreni)
SGLT2 inhibit�rleri kullanan kad�n ve erkek hastalarda pazarlama sonras�nda perineal nekrotizan fasiit (Fournier kangreni olarak da bilinir) vakalar� bildirilmi�tir (bkz. B�l�m 4.8). Bu acil cerrahi m�dahale ve antibiyotik tedavisi gerektiren nadir ancak ciddi ve potansiyel olarak ya�am� tehdit edici bir olayd�r.
Hastalara, ate� veya halsizlik ile birlikte, genital veya perineal b�lgede a�r�, hassasiyet, eritem veya �i�lik semptomlar�n�n bir kombinasyonunu ya�amalar� durumunda t�bbi yard�m almalar� �nerilmelidir. Nekrotizan fasiitin �ncesinde �rogenital enfeksiyon veya perineal apse ortaya ��kabilece�i bilinmelidir. Fournier kangreninden ��phelenildi�i takdirde DAPL�G kesilmeli ve acil tedavi (antibiyotikler ve cerrahi debridman dahil) ba�lat�lmal�d�r.
�drar yolu enfeksiyonlar�
�drarla glukoz at�l�m�, idrar yolu enfeksiyonu riskinde art�� ile ili�kili olabilir; bu nedenle piyelonefrit veya �rosepsis tedavisi s�ras�nda dapagliflozine ge�ici olarak ara verilmesi d���n�lmelidir.
Ya�l� hastalar (≥65)
Ya�l� hastalarda vol�m deplesyonu riski daha fazlad�r ve di�retiklerle tedavi edilme olas�l�klar� daha y�ksektir.
Ya�l� hastalarda b�brek i�lev bozuklu�unun olma olas�l��� ve/veya bu hastalar�n b�brek fonksiyonlar�nda de�i�ikliklere neden olabilecek anjiyotensin d�n��t�r�c� enzim inhibit�rleri (ACE-I) ve anjiyotensin II tip I resept�r blokerleri (ARB) gibi anti-hipertansif t�bbi �r�nlerle tedavi g�r�yor olma olas�l��� daha y�ksektir. T�m hastalarda oldu�u gibi ya�l� hastalarda da b�brek fonksiyonu ile ilgili ayn� �neriler ge�erlidir (bkz. B�l�m 4.2, 4.4, 4.8 ve 5.1).
Kalp yetersizli�i
NYHA s�n�f IV'te dapagliflozin ile deneyim s�n�rl�d�r.
Kronik b�brek hastal���
Alb�m�nirisi olmayan non-diyabetik hastalarda kronik b�brek hastal���n�n tedavisi i�in dapagliflozin ile ilgili deneyim bulunmamaktad�r. Alb�min�risi olan hastalar dapagliflozin tedavisinden daha fazla yarar g�rebilir.
Alt ekstremite amp�tasyonlar�
Bir ba�ka SGLT2 inhibit�r�yle tip 2 diyabette yap�lan uzun s�reli klinik �al��malarda, alt ekstremite amp�tasyon vakalar�nda (esas olarak ayak ba�parma��) bir art�� g�zlenmi�tir. Bunun bir s�n�f etkisi olu�turup olu�turmad��� bilinmemektedir. Diyabetli hastalara rutin �nleyici ayak bak�m� konusunda bilgi verilmesi �nemlidir.
�drar laboratuvar de�erlendirmeleri
Etki mekanizmas� nedeniyle, DAPL�G almakta olan hastalar�n idrarlar�nda glukoz testi pozitif sonu� verecektir.
Laktoz
DAPL�G film kapl� tablet laktoz i�ermektedir. Nadir kal�t�msal galaktoz intolerans�, Lapp laktaz yetmezli�i ya da glukoz-galaktoz malabsorpsiyon problemi olan hastalar�n bu ilac� kullanmamalar� gerekir.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Farmakodinamik etkile�imler
Di�retikler
Dapagliflozin; tiazid ve loop di�retiklerin di�retik etkilerine katk�da bulunabilir ve dehidratasyon ve hipotansiyon riskini art�rabilir (bkz. B�l�m 4.4).
�ns�lin ve ins�lin salg�lat�c� ila�lar
�ns�lin ve s�lfonil�reler gibi ins�lin salg�lat�c� ila�lar hipoglisemiye neden olur. Bu nedenle,
riskinin azalt�lmas� i�in ins�lin veya ins�lin salg�lat�c� ilac�n daha d���k dozunun kullan�lmas� gerekebilir (bkz. B�l�m 4.2 ve 4.8).
Farmakokinetik etkile�imler
Dapagliflozin metabolizmas� ba�l�ca UDP glukuronoziltransferaz 1A9 (UGT1A9) arac�l� glukuronit konjugasyonu yoluylad�r.
�n vitro �al��malarda dapagliflozin; sitokrom P450 (CYP) 1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP3A4'� inhibe etmemi� ya da CYP1A2, CYP2B6,
CYP3A4'� ind�klememi�tir. Bu nedenle, dapagliflozinin, bu enzimler taraf�ndan metabolize olan e�zamanl� uygulanan t�bbi �r�nlerin metabolik klirensini de�i�tirmesi beklenmemektedir.
Di�er t�bbi �r�nlerin dapagliflozin �zerindeki etkisi
Sa�l�kl� bireylerle ger�ekle�tirilen, �zellikle tek doz tasar�m�n kullan�ld��� etkile�im �al��malar�, dapagliflozinin farmakokineti�inin metformin, pioglitazon, sitagliptin, glimepirid, vogliboz, hidroklorotiazit, bumetanid, valsartan ya da simvastatin taraf�ndan de�i�tirilmedi�ini g�stermektedir.
Dapagliflozin ile rifampisinin (�e�itli aktif ta��y�c� ve ila� metabolize edici enzimlerin ind�kleyicisi) e�zamanl� uygulanmas�n� takiben sistemik dapagliflozin maruziyetinde (EAA)
%22'lik bir d���� g�zlenmi�, ancak 24 saatlik �riner glukoz at�l�m�nda klinik olarak anlaml� bir etkisi olmam��t�r. Herhangi bir doz ayarlamas� �nerilmemektedir. Di�er ind�kleyicilerle (�rne�in; karbamazepin, fenitoin, fenobarbital) klinik olarak anlaml� bir etki beklenmemektedir.
Dapagliflozin ile mefenamik asidin (UGT1A9 inhibit�r�) e�zamanl� uygulanmas�n� takiben sistemik dapagliflozin maruziyetinde %55'lik bir art�� g�zlenmi�tir; ancak 24 saatlik �riner glukoz at�l�m�nda klinik olarak anlaml� bir etkisi olmam��t�r. Herhangi bir doz ayarlamas� �nerilmemektedir.
Dapagliflozinin di�er t�bbi �r�nler �zerindeki etkisi
Dapagliflozin renal lityum at�l�m�n� art�rabilir ve kan lityum seviyeleri d��ebilir. Dapagliflozin ba�lat�ld�ktan ve doz de�i�ikliklerinden sonra serum lityum konsantrasyonu daha s�k izlenmelidir. Lityum serum konsantrasyonunu izlemek i�in l�tfen hastay� re�eteye lityum yazan doktora sevk ediniz.
Sa�l�kl� bireylerle ger�ekle�tirilmi� olan, �zellikle tek doz tasar�m�n kullan�ld��� etkile�im �al��malar�nda, dapagliflozin metformin, pioglitazon, sitagliptin, glimepirid, hidroklorotiazit, bumetanid, valsartan, digoksin (P-gp substrat�) ya da varfarinin farmakokineti�ini (S-varfarin; CYP2C9 substrat�), veya varfarinin INR ile �l��ld��� �zere antikoag�lan etkilerini de�i�tirmemi�tir. Tek doz 20 mg dapagliflozin ile simvastatin (CYP3A4 substrat�) kombinasyonu simvastatinin EAA de�erinde %19 art�� ve simvastatin asidin EAA de�erinde
%31 art�� ile sonu�lanm��t�r. Simvastatin ve simvastatin asit maruziyetlerindeki art��lar�n klinikte anlaml� oldu�u d���n�lmemektedir.
1,5-anhidroglusitol (1,5.-AG) Tayini ile Etkile�im
SGLT2 inhibit�rleri alan hastalarda glisemik kontrol�n de�erlendirilmesinde 1,5-AG �l��mleri g�venilir sonu�lar vermedi�inden glisemik kontrol�n 1,5-AG tayini ile izlenmesi �nerilmez. Glisemik kontrol� izlemek i�in alternatif y�ntemlerin kullan�m� �nerilmektedir.
�zel pop�lasyonlara ili�kin ek bilgiler
Herhangi bir etkile�im �al��mas� yap�lmam��t�r.
Pediyatrik pop�lasyon
Etkile�im �al��malar� sadece eri�kinlerde ger�ekle�tirilmi�tir.
4.6. Gebelik ve laktasyon
Gebelik Kategorisi: C
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon) Dapagliflozin ve �strojen/progesteron i�eren kontraseptifler aras�nda, �zel bir ila� etkile�im �al��mas� yap�lmam��t�r. Ancak, metabolizma verisine g�re, dapagliflozinin �strojen/progesteron i�eren kontraseptiflerin farmakokineti�i �zerinde klinik olarak anlaml� bir etkisi beklenmemektedir. �ocuk do�urma potansiyeli olan kad�nlarda �zel bir �nleme gerek yoktur.
Gebelik d�nemi
Gebe kad�nlarda dapagliflozin kullan�m�na ili�kin veri bulunmamaktad�r. S��anlar �zerindeki �al��malarda, insanlardaki gebeli�in ikinci ve ���nc� trimesterlerine kar��l�k gelen d�nemde geli�me s�recindeki b�breklerde toksisite g�zlenmi�tir (bkz. B�l�m 5.3). Bu nedenle gebeli�in ikinci ve ���nc� trimesterlerinde dapagliflozinin kullan�lmas� �nerilmemektedir.
Hayvanlar �zerinde yap�lan ara�t�rmalar �reme toksisitesinin bulundu�unu g�stermi�tir (bkz. B�l�m 5.3). �nsanlara y�nelik potansiyel risk bilinmemektedir.
Gebelik saptand���nda dapagliflozin tedavisi durdurulmal�d�r.
Laktasyon d�nemi
Dapagliflozin ve/veya metabolitlerinin insan s�t� ile at�l�p at�lmad��� bilinmemektedir. Hayvanlardaki mevcut farmakodinamik/toksikolojik veriler, dapagliflozin/metabolitlerinin s�t ile at�ld���n�, ayr�ca emzirilen yavrularda farmakoloji arac�l� etkilerin oldu�unu g�stermi�tir (bkz. B�l�m 5.3). Yenido�anlar/bebekler i�in risk olas�l�k d��� b�rak�lamamaktad�r. Dapagliflozin, emzirme d�neminde kullan�lmamal�d�r.
�reme yetene�i/Fertilite
Dapagliflozinin insanda fertilite �zerindeki etkisi incelenmemi�tir. Erkek ve di�i s��anlarda dapagliflozin, test edilen herhangi bir dozda fertilite �zerinde bir etki g�stermemi�tir.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
DAPL�G'in, ara� ve makine kullanma becerisi �zerinde herhangi bir etkisi bulunmamakta ya da ihmal edilebilir d�zeyde etkileri olabilmektedir. Dapagliflozin, bir s�lfonil�re veya ins�lin ile kombinasyon halinde kullan�ld���nda, hastalara, hipoglisemi riskine kar�� dikkatli olmalar� �nerilmelidir.
4.8. �stenmeyen etkiler
G�venlilik profilinin �zeti
Tip 2 diabetes mellitus
Tip 2 diyabet konulu klinik �al��malarda, 15000'den fazla hasta dapagliflozin ile tedavi edilmi�tir.
G�venlili�in ve tolere edilebilirli�in birincil de�erlendirmesi, plasebo kontroll� 13 k�sa s�reli (24 haftaya kadar) �al��man�n �nceden tan�mlanm�� olan birle�tirilmi� analizinde 2360 hasta 10 mg dapagliflozin ile tedavi edilmi�, 2295 hastaya plasebo uygulanm��t�r.
Tip 2 diyabet konulu dapagliflozin kardiyovask�ler sonlan�mlar �al��mas�nda (DECLARE �al��mas�, bkz. B�l�m 5.1), 48 ayl�k bir medyan maruziyet s�resi ile 8574 hasta 10 mg dapagliflozin, 8569 hasta ise plasebo alm��t�r. Toplamda dapagliflozin maruziyeti 30623 hasta y�l� olmu�tur.
Klinik �al��malarda en s�k bildirilen advers reaksiyon genital enfeksiyonlar olmu�tur.
Kalp yetersizli�i
D���k ejeksiyon fraksiyonuyla seyreden kalp yetersizli�i hastalar�nda y�r�t�len dapagliflozin kardiyovask�ler sonu� �al��mas�nda (DAPA-HF �al��mas�), 18 ayl�k bir medyan maruziyet s�resi boyunca 2368 hasta 10 mg dapagliflozin, 2368 hasta ise plasebo alm��t�r. Hasta pop�lasyonu, tip 2 diyabeti olan ve olmayan hastalar� ve eGFR de�eri ≥ 30 mL/dak/1,73 m olan hastalar� i�ermi�tir.
Dapagliflozinin kalp yetersizli�i g�r�len hastalardaki genel g�venlilik profilinin dapagliflozinin bilinen g�venlilik profili ile tutarl� oldu�u g�r�lm��t�r.
Kronik b�brek hastal���
Kronik b�brek hastal��� bulunan hastalarda yap�lan dapagliflozin renal sonu� �al��mas�nda (DPA-CKD), ortanca 27 ayl�k maruziyette 2149 hasta dapagliflozin 10 mg ve 2149 hasta plasebo ile tedavi edilmi�tir. Hasta pop�lasyonu >25 ile ≤75 mL/dak/1.73 m eGFR'ye sahip
oran� [UACR] ≥ 200 ve ≤ 5000 mg/g) olan hastalardan olu�maktayd�. Tedavi, e�er eGFR 25 mL/dak/1.73 m d�zeyinin alt�na d��m��se devam ettirilmi�tir.
Kronik b�brek hastal��� bulunan hastalarda dapagliflozinin genel g�venlilik profili dapagliflozinin bilinen g�venlilik profili ile uyumlu idi.
A�a��daki advers reaksiyonlar plasebo kontroll� klinik �al��malarda ve pazarlama sonras� g�zlemde tespit edilmi�tir. Bu advers reaksiyonlardan herhangi birinin dozla ba�lant�l� oldu�u bulunmam��t�r. Advers reaksiyonlar sistem organ s�n�f�na ve s�kl��a g�re listelenmektedir. �u terimler ve s�kl�k dereceleri kullan�lm��t�r: �ok yayg�n (≥1/10); yayg�n (≥1/100 ila <1/10); yayg�n olmayan (≥1/1000 ila <1/100); seyrek (≥1/10.000 ila <1/1000); �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Plasebo kontroll� klinik �al��mada ve pazarlama sonras� ortaya ��kan advers reaksiyonlar
Enfeksiyonlar ve enfestasyonlar
Yayg�n*: Vulvovajinit, balanit ve ba�lant�l� genital enfeksiyonlar*, idrar yolu enfeksiyonu*
Yayg�n olmayan**: Mantar enfeksiyonu
�ok seyrek: Perineal nekrotizan fasiit (Fournier Kangreni)
Metabolizma ve beslenme hastal�klar�
�ok yayg�n: Hipoglisemi (SU veya ins�lin ile birlikte kullan�ld���nda) Yayg�n olmayan**: Vol�m deplesyonu, susama hissi**
Seyrek: Diyabetik ketoasidoz (tip 2 diyabette kullan�ld���nda)
Sinir sistemi hastal�klar�
Yayg�n*: Ba� d�nmesini de i�eren sersemlik hali
Gastrointestinal hastal�klar
Yayg�n olmayan**: Konstipasyon**, a��z kurulu�u**
Deri ve deri alt� doku hastal�klar�
Yayg�n*: D�k�nt�
�ok seyrek: Anjiyo�dem
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar�
Yayg�n*: S�rt a�r�s�*
B�brek ve idrar yolu hastal�klar�
Yayg�n*: Dis�ri, poli�ri* Yayg�n olmayan**: Nokt�ri**
�reme sistemi ve meme hastal�klar�
Yayg�n olmayan**: Vulvovajinal ka��nt�**, genital ka��nt�**
Ara�t�rmalar
Yayg�n*: Dislipidemi, hematokrit y�kselmesi, ba�lang�� tedavisi s�ras�nda renal kreatinin klirensinde azalma
Yayg�n olmayan**: Ba�lang�� tedavisi s�ras�nda kanda kreatinin y�kselmesi**, kanda �re y�kselmesi**, kilo verme**
* Hastalar�n ≥ % 2'sinde ve plaseboya k�yasla dapagliflozin 10 mg ile tedavi edilen hastalar�n
≥ %1'inde ve en az 3 hastada daha raporlanm��t�r.
** Ara�t�r�c� taraf�ndan hastalar�n ≥ %0,2'sinde �al��ma tedavisiyle ili�kisi muhtemel, ili�kisi olas� ya da ili�kili olarak bildirilmi�tir ve plaseboya k�yasla ≥ %1 fazla ve en az 3 fazla ki�i dapagliflozin 10 mg ile tedavi edilmi�tir.
Se�ili advers reaksiyonlar�n tan�m�
Vulvovajinit, balanit ve ili�kili genital enfeksiyonlar
13 �al��mal�k g�venlilik havuzunda vulvovajinit, balanit ve ili�kili genital enfeksiyonlar 10 mg dapagliflozin ve plasebo alan g�n�ll�lerin s�ras�yla %5,5 ve %0,6's�nda bildirilmi�tir. Enfeksiyonlar�n �o�unun hafif ila orta �iddetli oldu�u g�r�lm��t�r ve g�n�ll�ler ilk standart tedavi k�r�ne yan�t vermi�tir. Enfeksiyonlar nadiren dapagliflozin tedavisinin kesilmesine neden olmu�tur. Bu enfeksiyonlar�n kad�nlarda daha s�k ortaya ��kt��� g�zlenmi�tir (dapagliflozin ve plasebo ile s�ras�yla %8,4 ve %1,2) ve ge�mi� �yk�ye sahip g�n�ll�lerin rek�rren enfeksiyon ya�ama olas�l���n�n daha y�ksek oldu�u belirlenmi�tir.
DECLARE �al��mas�nda, ciddi genital enfeksiyon advers olaylar� ya�ayan hastalar�n say�lar�n�n d���k ve dengeli oldu�u g�r�lm��t�r: dapagliflozin ve plasebo gruplar�n�n her birinde 2 hasta.
Yap�lan klinik �al��mada, dapagliflozin grubunda hi�bir hasta, ciddi genital enfeksiyonuna ba�l� advers olay bildirmemi�, plasebo grubunda ise bir hasta b�yle bir bildirimde bulunmu�tur. Dapagliflozin grubunda genital enfeksiyonlara ba�l� olarak tedavinin b�rak�lmas�na neden olan advers olaylar 7 (%0,3) hastada g�r�lm��t�r, plasebo grubunda ise b�yle bir olay g�zlenmemi�tir.
Yap�lan ba�ka bir klinik �al��mada, dapagligflozin grubunda genital enfeksiyonlardan olu�an ciddi advers olay bulunan 3 hasta (%0,1) varken, plasebo grubunda yoktur. Dapagliflozin grubunda genital enfeksiyonlar nedeniyle tedavinin b�rak�lmas�na yol a�an advers olay bulunan 3 hasta (%0,1) varken, plasebo grubunda yoktur. Diyabeti olmayan hi�bir hastada genital enfeksiyonlar�n ciddi yan etkileri veya genital enfeksiyonlar nedeniyle tedavinin kesilmesine neden olan yan etkiler bildirilmemi�tir.
Perineumda nekrotizan fasiit (Fournier gangreni)
Dapagliflozin de dahil olmak �zere SGLT2 inhibit�rleri alan hastalarda pazarlama sonras�nda Fournier gangreni olgular� bildirilmi�tir (bkz. B�l�m 4.4).
Tip 2 diabetes mellitus bulunan 17160 hasta ile yap�lan ve medyan maruziyet s�resinin 48 ay oldu�u DECLARE �al��mas�nda, biri dapagliflozin ile tedavi edilen grupta ve 5'i plasebo grubunda olmak �zere 6 Fournier gangreni olgusu bildirilmi�tir.
Hipoglisemi
Hipoglisemi s�kl���n�n diyabet konulu klinik �al��malarda arka plan tedavisinin tipine ba�l� oldu�u g�r�lm��t�r.
Monoterapide, metformine ilave ya da sitagliptine ilave (metforminle veya metforminsiz) dapagliflozin �al��malar� i�in, min�r hipoglisemi epizodlar�n�n s�kl�klar� tedavinin 102. haftas�na kadar plasebo dahil tedavi gruplar� aras�nda benzer olmu�tur (< %5). T�m �al��malarda maj�r hipoglisemi olaylar� yayg�n olmayan s�kl�kta g�zlenmi�tir ve dapagliflozin
tedavilerinin kullan�ld��� �al��malarda hipoglisemi oranlar� daha y�ksek olmu�tur (bkz. B�l�m 4.5).
Glimepiride ilave tedavi �al��mas�nda, 24 ve 48. haftalarda min�r hipoglisemi epizodlar�, plasebo ile glimepirid uygulanan kombinasyon grup (s�ras�yla %2,1 ve %2,1) ile kar��la�t�r�ld���nda 10 mg dapagliflozin ile glimepirid kombinasyonu uygulanan grupta daha s�k (s�ras�yla %6,0 ve %7,9) bildirilmi�tir.
�ns�line ilave �al��mas�nda, maj�r hipoglisemi epizodlar�, 24. ve 104. haftalarda 10 mg dapagliflozin ve ins�lin ile tedavi edilen bireylerin s�ras�yla %0,5'i ve %1,0'� ve 24. ve 104. haftalarda plasebo ve ins�lin ile tedavi edilen bireylerin %0,5'inde bildirilmi�tir. 24. ve 104. haftalarda, min�r hipoglisemi epizodlar� 10 mg dapagliflozin ve ins�lin alan bireylerin s�ras�yla
%40,3'� ve %53,1'i ve plasebo ile ins�lin alan bireylerin %34,0'�nda ve %41,6's�nda bildirilmi�tir.
24 haftaya kadar olan, metformin ve bir s�lfonil�reye ekleme �al��mas�nda, maj�r hipoglisemi epizodu bildirilmemi�tir. 10 mg dapagliflozine ek olarak metformin ve bir s�lfonil�re alan hastalar�n %12,8'inde ve plaseboya ek olarak metformin ve bir s�lfonil�re alan hastalar�n
%3,7'sinde min�r hipoglisemi epizodlar� bildirilmi�tir.
DECLARE �al��mas�nda plasebo ile kar��la�t�r�ld���nda dapagliflozin tedavisiyle maj�r hipoglisemi riskinde art�� g�zlenmemi�tir. Maj�r hipoglisemi olaylar� dapagliflozinle tedavi uygulanan 58 (%0,7) hastada ve plaseboyla tedavi uygulanan 83 (%1,0) hastada bildirilmi�tir.
Yap�lan klinik �al��mada, yaln�zca tip 2 diyabetli hastalarda olmak �zere, hem dapagliflozin hem de plasebo tedavisi gruplar�nda 4 (%0,2) hastada maj�r hipoglisemi olaylar� g�zlemlenmi�tir.
Yap�lan ba�ka bir klinik �al��mada, hipoglisemi maj�r olaylar� dapagliflozin grubunda 14 hastada (%0,7) ve plasebo grubunda 28 hastada (%1,3) bildirilmi� ve sadece tip 2 diyabet bulunan hastalarda g�zlenmi�tir.
Vol�m deplesyonu
13 �al��mal�k g�venlilik havuzunda, vol�m deplesyonuna i�aret eden reaksiyonlar (dehidratasyon, hipovolemi ya da hipotansiyon bildirimlerini i�erir) 10 mg dapagliflozin ve plasebo alan bireylerin s�ras�yla %1,10'unda ve %0,7'sinde bildirilmi�tir; ciddi olaylar bireylerin < %0,2'sinde meydana gelmi� olup 10 mg dapagliflozin ve plasebo aras�nda dengelidir (bkz. B�l�m 4.4).
DECLARE �al��mas�nda vol�m deplesyonuna i�aret eden olaylar ya�ayan hastalar�n say�s�n�n tedavi gruplar� aras�nda dengeli oldu�u g�r�lm��t�r: dapagliflozin ve plasebo gruplar�nda s�ras�yla 213 (%2,5) ve 207 (%2,4). Ciddi advers olaylar dapagliflozin ve plasebo grubunda
s�ras�yla 81 (%0,9) ve 70 (%0,8) g�n�ll�de bildirilmi�tir. Ya�, di�retik kullan�m�, kan bas�nc�
(ARB) kullan�m� alt gruplar�nda olaylar�n genel olarak tedavi gruplar� aras�nda dengeli oldu�u g�r�lm��t�r. Ba�lang��ta eGFR de�eri < 60 mL/dak/1,73 m olan hastalarda dapagliflozin grubunda vol�m deplesyonuna i�aret eden 19 ciddi advers olay, plasebo grubunda ise 13 olay ortaya ��km��t�r.
Yap�lan klinik �al��mada vol�m s�v� dengesine i�aret eden olaylar�n g�r�ld��� hastalar�n say�s� dapagliflozin grubunda 170 (%7,2), plasebo grubunda ise 153 (%6,5) olmu�tur. Vol�m s�v� dengesine i�aret eden ciddi olaylar ya�ayan hastalar�n say�s�n�n, dapagliflozin grubunda (23 [%1,0]) plasebo grubundakine k�yasla (38 [%1,6]) daha d���k oldu�u g�zlenmi�tir. Sonu�lar�n ba�lang��ta diyabet var olup olmamas�ndan ve ba�lang��taki eGFR d�zeyinden ba��ms�z �ekilde birbirine yak�n oldu�u g�zlenmi�tir.
Yap�lan ba�ka bir klinik �al��mada, vol�m s�v� dengesine i�aret eden olaylar�n g�r�ld��� hastalar�n say�s� dapagliflozin grubunda 120 (%5,6), plasebo grubunda ise 84 (%3,9) olmu�tur. Dapagliflozin grubunda vol�m s�v� dengesine i�aret eden ciddi olay semptomlara sahip 16 hasta (%0,7) varken, plasebo grubunda 15 hasta (%0,7) vard�.
Tip 2 diyabette diyabetik ketoasidoz
Medyan maruziyet s�resinin 48 ay oldu�u DECLARE �al��mas�nda, dapagliflozin 10 mg grubunda 27 hastada, plasebo grubunda ise 12 hastada DKA olaylar� rapor edilmi�tir. Olaylar �al��ma periyodu boyunca e�it da��l�ml� olarak ger�ekle�mi�tir. Dapagliflozin grubunda DKA olaylar�n�n g�r�ld��� 27 hastan�n 22'sinin olay s�ras�nda e�zamanl� ins�lin tedavisi almakta oldu�u saptanm��t�r. DKA i�in h�zland�r�c� fakt�rler, bir tip 2 diabetes mellitus pop�lasyonunda beklendi�i �ekilde olmu�tur (bkz. B�l�m 4.4).
Yap�lan klinik �al��mada DKA olaylar� dapagliflozin grubunda tip 2 diyabetli 3 hastada bildirilmi�, plasebo grubunda ise hi�bir hastada bildirilmemi�tir.
Yap�lan ba�ka bir klinik �al��mada DKA olaylar� dapagliflozin grubunda hi�bir hastada bildirilmezken, plasebo grubunda tip 2 diyabeti bulunan 2 hastada bildirilmi�tir.
�drar yolu enfeksiyonlar�
13 �al��mal�k g�venlilik havuzunda, idrar yolu enfeksiyonlar� 10 mg dapagliflozin i�in plaseboya k�yasla daha s�k bildirilmi�tir (s�ras�yla %4,7 kar��s�nda %3,5; bkz. B�l�m 4.4). Enfeksiyonlar�n �o�u hafif ila orta derecede olmu� ve bireyler ilk standart tedavi k�r�ne yan�t vermi�, nadir durumlarda dapagliflozin tedavisinin kesilmesi gerekmi�tir. Bu enfeksiyonlar kad�nlar aras�nda daha s�k g�zlenmi�tir ve �yk�s� olan hastalar�n enfeksiyon n�ks� geli�tirme olas�l��� daha y�ksek olmu�tur.
DECLARE �al��mas�nda idrar yolu enfeksiyonu g�r�len ciddi advers olaylar� 10 mg dapagliflozin ile plasebo ile olandan daha d���k s�kl�kta bildirilmi�tir; s�ras�yla 79 (%0,9) olaya kar��l�k 109 (%1,3) olay ortaya ��km��t�r.
Yap�lan klinik �al��mada ciddi idrar yolu enfeksiyonu advers olaylar�n�n g�r�ld��� hastalar�n say�s� dapagliflozin grubunda 14 (%0,6) , plasebo grubunda ise 17 (%0,7) olmu�tur.
Dapagliflozin ve plasebo gruplar�n�n her birinde idrar yolu enfeksiyonlar�na ba�l� olarak tedavinin b�rak�lmas�na neden olan advers olaylar 5 (%0,2) hastada g�r�lm��t�r.
Yap�lan ba�ka bir klinik �al��mada, ciddi idrar yolu enfeksiyonu advers olaylar�n�n g�r�ld��� hastalar�n say�s� dapagliflozin grubunda 29 (%1,3), plasebo grubunda ise 18 (%0,8) olmu�tur. Dapagliflozin grubunda idrar yolu enfeksiyonlar�na ba�l� olarak tedavinin b�rak�lmas�na neden olan advers olaylar 8 hastada (%0,4) g�r�l�rken, plasebo grubunda ise 3 hastada (%0,1) g�r�lm��t�r.
Kreatinin art���
Kreatinin art���yla ili�kili advers reaksiyonlar gruplanm��t�r (�rn. Renal kreatinin klirensinde azalma, b�brek fonksiyon bozuklu�u, kan kreatininde art�� ve glomer�ler filtrasyon h�z�nda azalma). 13 �al��mal�k g�venlilik havuzunda, bu reaksiyon gruplamas� dapagliflozin 10 mg ve plasebo alan hastalar�n s�ras�yla %3,2 ve %1,8'inde bildirilmi�tir. Normal b�brek fonksiyonu olan ya da hafif b�brek bozuklu�u bulunan hastalarda (ba�lang��ta eGFR ≥ 60 mL/dak/1,73m) bu reaksiyon gruplamas� dapagliflozin 10 mg ve plasebo alan hastalar�n s�ras�yla %1,3 ve
%0,8'inde bildirilmi�tir. Bu reaksiyonlar, ba�lang��ta eGFR ≥ 30 ve < 60 mL/dak/1,73m hastalarda daha yayg�n olmu�tur (dapagliflozin 10 mg ile %1,85 ve plasebo ile %9,3).
B�brek ile ili�kili advers olaylar ya�am�� olan hastalar�n ileri de�erlendirmesi bunlar�n �o�unda ba�lang�ca k�yasla ≤44 mikromol/L (≤ 0,5 mg/dL) kreatinin de�i�iklikleri oldu�unu g�stermi�tir. Kreatinin art��lar� s�rekli tedavi s�ras�nda genellikle ge�ici ya da tedavi b�rak�ld�ktan sonra geri d�n��l� olmu�tur.
Ya�l� hastalar� ve b�brek fonksiyon bozuklu�u (60 mL/dak/1,73 m'den az eGFR) bulunan hastalar� i�eren DECLARE �al��mas�nda, eGFR her iki tedavi grubunda zamanla azalm��t�r. Plasebo grubu ile kar��la�t�r�ld���nda, dapagliflozin grubunda 1.y�lda ortalama eGFR biraz daha d���k olurken, 4. y�lda ortalama eGFR biraz daha y�ksek olmu�tur.
Yap�lan klinik �al��mada hem dapagliflozin grubunda hem de plasebo grubunda eGFR zaman i�inde d��m��t�r. Ortalama eGFR'de ba�lang��ta g�zlenen azalma dapagliflozin grubunda -4,3 mL/dak/1,73 m, plasebo grubunda ise -1,1 mL/dak/1,73 m olmu�tur. Tedavi gruplar�nda eGFR'de ba�lang�ca k�yasla 20. ayda g�zlenen fark�n birbirine yak�n oldu�u g�r�lm��t�r: dapagliflozinle -5,3 mL/dak/1,73 m, plaseboyla -4,5 mL/dak/1,73 m.
Yap�lan ba�ka bir klinik �al��mada, hem dapagliflozin grubunda hem de plasebo grubunda eGFR zaman i�inde d��m��t�r. Ortalama eGFR'deki ilk g�zlenen azalma (14. g�n) dapagliflozin grubunda -4,0 mL/dak/1,73 m, plasebo grubunda ise -0,8 mL/dak/1,73 m olmu�tur. 28.ayda, ba�lang�� eGFR'ye g�re de�i�im, dapagliflozin grubunda -7,4 ml/dk/1,73 m ve plasebo grubunda ise -8,6 ml/dk/1,73 m'dir.
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar / risk dengesinin s�rekli olarak izlenmesine
Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr; e- posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99)
4.9. Doz a��m� ve tedavisi
Dapagliflozin, 500 mg'a (maksimum �nerilen insan dozunun 50 kat�) varan tek oral dozlarda sa�l�kl� bireylerde herhangi bir toksisite g�stermemi�tir. Bu bireylerin idrar�nda, bir s�re boyunca dozla ili�kili olarak (500 mg doz i�in en az 5 g�n) tespit edilir glukoz d�zeyleri g�zlenmi�, dehidratasyon, hipotansiyon ya da elektrolit dengesizli�i bildirimi olmam�� ve QTc aral���nda klinik a��dan anlaml� herhangi bir etki s�z konusu olmam��t�r. Hipoglisemi insidans� plasebo ile benzer olmu�tur. Sa�l�kl� bireylerde ve tip 2 diabetes mellitusu olan bireylere 2 hafta s�reyle 100 mg'a (maksimum �nerilen insan dozunun 10 kat�) varan g�nde tek doz rejiminin uyguland��� klinik �al��malarda, hipoglisemi insidans� plaseboya g�re hafif derecede daha y�ksek olmu� ve dozla ili�kili olmad��� g�r�lm��t�r. Dehidratasyon, hipotansiyon dahil advers reaksiyonlar�n oranlar� plasebo ile benzer olmu�, b�brek fonksiyonu biyolojik g�stergeleri ve serum elektrolitleri gibi laboratuvar parametrelerinde klinik olarak anlaml�, dozla ba�lant�l� de�i�iklikler olmam��t�r.
Doz a��m� durumunda, hastan�n klinik durumunun gerektirdi�i �ekilde uygun destekleyici tedavi ba�lat�lmal�d�r. Dapagliflozinin hemodiyaliz ile v�cuttan uzakla�t�r�lmas� �al���lmam��t�r.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Diyabet tedavisinde kullan�lan ila�lar, sodyum-glukoz ko-transporter 2 (SGLT2) inhibit�rleri
ATC kodu: A10BK01
Etki mekanizmas�
Dapagliflozin y�ksek derecede potent (Ki: 0,55 nM), selektif ve geri d�n���ml� SGLT2 inhibit�r�d�r.
Dapagliflozinle sa�lanan SGLT2 inhibisyonu, sodyum reabsorbsiyonunda e�zamanl� bir azalmayla, proksimal renal t�b�lde glomer�ler filtrattan glukoz reabsorbsiyonunu azalt�r ve �riner glukoz ekskresyonu ve ozmotik di�rez ortaya ��kar�r. Dolay�s�yla dapagliflozin distal t�b�le sodyum ta��nmas�n� artt�r�r ve bu da t�b�loglomer�ler geribildirimi artt�r�r ve intraglomeruler bas�nc� azalt�r. Bu, ozmotik di�rez ile birlikte, a��r� vol�m y�klemesinde azalma, kan bas�nc�nda d���� ve �n y�k ve son y�kte azalma sa�lar ve bunlar kardiyak yeniden modelleme �zerinde yararl� etkiler ortaya ��karabilir. Di�er etkiler aras�nda hematokrit art��� ve v�cut a��rl���nda azalma bulunur. DAPA-HF �al��malar�nda ortaya konmu� oldu�u gibi, dapagliflozinin kardiyak faydalar� yaln�zca kan glukozu d���r�c� etkiye ba��ml� de�ildir.
Dapagliflozin, b�breklerden glukoz reabsorpsiyonunu azaltarak gerek a�l�k gerekse post-
(glukuretik etki) ilk dozdan sonra g�zlenir, 24 saatlik doz uygulama aral��� boyunca s�reklidir ve tedavi s�resince bu etki korunur. B�brek taraf�ndan bu mekanizma ile uzakla�t�r�lan glukoz miktar�, kan glukoz konsantrasyonu ve glomer�ler filtrasyon h�z�na ba�l�d�r. Dolay�s�yla glukoz d�zeyi normal olan g�n�ll�lerde dapagliflozinin hipoglisemiye yol a�ma e�ilimi d���kt�r. Dapagliflozin hipoglisemiye cevaben normal endojen glukoz �retimini bozmaz. Dapagliflozin, ins�lin sekresyonunundan ve ins�lin etkisinden ba��ms�z etki g�sterir. Dapagliflozin ile y�r�t�len klinik �al��malarda beta h�cre fonksiyonu i�in homeostaz model de�erlendirmesinde (HOMA beta h�cre) d�zelme g�zlenmi�tir.
SGLT2 selektif �ekilde b�brekte eksprese olur. Dapagliflozin, periferik dokulara glukoz ta��nmas�nda �nemli di�er glukoz ta��y�c�lar�n� inhibe etmez ve glukoz absorpsiyonundan sorumlu, ba��rsaktaki ba�l�ca ta��y�c� olan SGLT1'e g�re SGLT2 i�in >1400 kat daha se�icidir.
Farmakodinamik etkiler
Sa�l�kl� bireylerde ve tip 2 diabetes mellitusu olan bireylerde dapagliflozin uygulamas�ndan sonra idrarla at�lan glukoz miktar�nda art��lar g�r�lm��t�r. 12 hafta s�reyle tip 2 diabetes mellitusu olan bireylere uygulanan 10 mg/g�n dapagliflozin dozunda g�n ba��na yakla��k 70 g glukoz at�lm��t�r (280 kilokalori/g�n'e e�de�er). �ki y�l boyunca 10 mg/g�n dapagliflozin verilen tip 2 diabetes mellitusu olan bireylerde glukoz at�l�m�n�n korundu�u y�n�nde kan�tlar g�r�lm��t�r.
Tip 2 diabetes mellitusu olan bireylerde dapagliflozin ile sa�lanan �riner glukoz at�l�m� ayr�ca ozmotik di�reze ve idrar hacminde art��a neden olur. 10 mg dapagliflozin ile tedavi edilen tip 2 diabetes mellitusu olan bireylerdeki idrar hacmi art��lar� 12 hafta s�reyle korunmu�tur ve yakla��k 375 mL/g�n d�zeyinde olmu�tur. �drar hacmindeki art��, idrarla sodyum at�l�m�nda, serum sodyum konsantrasyonlar�nda de�i�iklikler ile ba�lant�l� olmayan k���k ve ge�ici bir art�� ile ili�kilendirilmi�tir.
Ayr�ca idrarla �rik asit at�l�m� da ge�ici olarak artm�� (3-7 g�n) ve buna, serum �rik asit konsantrasyonunda s�rekli bir azalma e�lik etmi�tir. 24. haftada serum �rik asit konsantrasyonlar�ndaki d����ler -48,3 mikromol/L ila -18,3 mikromol/L (-0,87 mg/dL ila - 0,33 mg/dL) aral���nda olmu�tur.
Klinik etkililik ve g�venlilik
Tip 2 diabetes mellitus
Glisemik kontrol�n�n iyile�mesi ve kardiyovask�ler morbidite ve mortalitenin azalmas� tip 2 diyabet tedavisinin b�t�nleyici par�alar�d�r.
Dapagliflozinin glisemik etkilili�ini ve g�venlili�ini de�erlendirmek �zere 7056 tip 2 diyabeti olan bireyler ile on d�rt adet �ift k�r, randomize, kontroll� klinik �al��ma ger�ekle�tirilmi�tir: bu �al��malarda 4737 birey dapagliflozin ile tedavi edilmi�tir. On iki �al��mada tedavi s�resi 24
kadar �al��ma s�resi), bir �al��ma 28 hafta tedavi s�resi ve bir �al��ma s�resi 52 hafta olup; 52 haftal�k ve 104 haftal�k uzatma d�nemleri yer alm��t�r (toplam �al��ma s�resi 208 hafta). Ortalama diyabet s�resi 1,4 ila 16,9 y�l aral���nda olmu�tur. �al��maya kat�lan bireylerin
%50'sinde hafif derecede b�brek yetmezli�i ve %11'inde orta derecede b�brek yetmezli�i olmu�tur. Bireylerin %51'i erkek, %84'� Beyaz, %8'i Asyal�, %4'� Siyah ve %4'� di�er etnik gruplardand�r. Bireylerin %81'inde v�cut kitle indeksi (VK�) 27'dir. Ayr�ca, yeterince kontrol alt�na al�namayan tip 2 diyabeti ve hipertansiyonu olan hastalarda iki adet 12-haftal�k, plasebo-kontroll� �al��ma y�r�t�lm��t�r.
Kardiyovask�ler ve renal olaylar �zerindeki etkinin de�erlendirilmesi amac�yla, kan�tlanm�� kardiyovask�ler hastal��� bulunan veya bulunmayan, tip 2 diyabetli 17160 hasta �zerinde plaseboyla kar��la�t�rmal� �ekilde 10 mg dapagliflozin ile bir kardiyovask�ler sonu� �al��mas� (DECLARE) ger�ekle�tirilmi�tir.
Glisemik kontrol
Monoterapi
Yeterli derecede kontrol edilemeyen tip 2 diabetes mellitusu olan bireylerde dapagliflozin ile monoterapinin g�venlili�ini ve etkilili�ini de�erlendirme amac�yla �ift k�r, plasebo kontroll�, 24 hafta s�reli (ek uzatma s�reli) bir �al��ma ger�ekle�tirilmi�tir. Dapagliflozin ile g�nde bir kez tedavi sonucunda HbA1c'de plasebo ile kar��la�t�r�ld���nda istatistiksel olarak anlaml� d����ler sa�lanm��t�r (p < 0,0001) (Tablo 2).
Uzatma d�neminde HbA1c d����� 102. haftaya kadar s�rm��t�r. (10 mg dapagliflozin ve plasebo i�in d�zeltilmi� ba�lang�ca g�re ortalama de�i�iklik s�ras�yla -%0,61 ve -%0,17).
Tablo 2. Monoterapi olarak dapagliflozinin plasebo kontroll� �al��mas�n�n 24. hafta sonu�lar� (LOCF)
Monoterapi | ||
| Dapagliflozin 10 mg | Plasebo |
N | 70 | 75 |
HbA1c (%) Ba�lang�� (ortalama) Ba�lang�ca g�re de�i�iklik Plaseboya g�re fark (%95 GA) |
8,01 -0,89 -0,66 (-0,96, -0,36) |
7,79 -0,23 |
HbA1c < %7'ye ula�an g�n�ll� y�zdesi Ba�lang�ca g�re d�zeltilen |
50,8 |
31,6 |
V�cut a��rl��� (kg) Ba�lang�� (ortalama) Ba�lang�ca g�re de�i�iklik Plaseboya g�re fark (%95 GA) |
94,13 -3,16 -0,97 (-2,20, 0,25) |
88,77 -2,19 |
![]()
�lave kombinasyon tedavisi
52 haftal�k, aktif kontroll� bir e�de�erlik �al��mas�nda (52 ve 104 haftal�k uzatma periyoduna sahip), glisemik kontrol�n yetersiz oldu�u bireylerde (HbA1c > %6,5 ve ≤ %10) metformine ilave tedavi olarak bir s�lfonil�reye (glipizid) kar��, metformine ilave tedavi olarak dapagliflozin de�erlendirilmi�tir. Bulgular, glipizide k�yasla HbA1c'de ba�lang��tan 52. haftaya kadar benzer bir ortalama azalmay� ve b�ylece e�de�erli�i g�stermi�tir (Tablo 3). 104. haftada, HbA1c'de ba�lang�ca g�re d�zeltilmi� ortalama de�i�iklik dapagliflozin i�in -%0,32 ve glipizid i�in -%0,14't�r. 208. haftada, Hb1Ac'de ba�lang�ca g�re d�zeltilmi� ortalama de�i�iklik dapagliflozin i�in %-0,10 ve glipizid i�in 0,20% dir. 52. ve 104. ve 208. haftalarda, glipizid ile tedavi edilen grup ile (s�ras�yla %40,8, %47,0, %50,0) kar��la�t�r�ld���nda dapagliflozin ile tedavi edilen grupta (s�ras�yla %3,5, %4,3 ve %5,0) anlaml� olarak daha d���k bir birey oran�nda en az bir hipoglisemi olay� ya�anm��t�r.104. ve 208. haftada �al��maya devam eden birey oran� dapagliflozin ile tedavi edilen grup i�in %56,2 ve %39,7 ve glipizid ile tedavi edilen grup i�in %50,0 ve %34,6'dir.
Tablo 3. Metformine ilave tedavi olarak dapagliflozin ile glipizidi kar��la�t�ran aktif kontroll� �al��man�n 52. hafta sonu�lar� (LOCF)
Parametre | Dapagliflozin + metformin | Glipizid + metformin |
N | 400 | 401 |
HbA1c (%) Ba�lang�� (ortalama) Ba�lang�ca g�re de�i�iklik Glipizid + metforminden fark� (%95 GA) |
7,69 -0,52 0,00 (-0,11, 0,11) |
7,74 -0,52 |
V�cut a��rl��� (kg) Ba�lang�� (ortalama) Ba�lang�ca g�re de�i�iklik Glipizid + metforminden fark� (%95 GA) |
88,44 -3,22 -4,65 (-5,14, -4,17) |
87,60 1,44 |
![]()
Metformin, glimepirid, metformin ve bir s�lfonil�re, sitagliptin (metforminle veya metforminsiz) ya da ins�line ilave tedavi olarak dapagliflozin, plasebo alan bireyler ile kar��la�t�r�ld���nda 24 haftada HbA1c'de istatistiksel olarak anlaml� d����ler sa�lam��t�r (p < 0,0001; Tablo 4, 5 ve 6).
24. haftada HbA1c'de g�zlenen azalmalar, 48 haftal�k verilere (glimepirid) ve 104 haftal�k verilere (ins�lin) sahip ilave tedavi kombinasyonu �al��malar�nda (glimepirid ve ins�lin) korunmu�tur. 48. haftada sitagliptine ilave edildi�inde (metforminle veya metforminsiz), 10 mg dapagliflozin ve plasebo i�in ba�lang�ca g�re d�zeltilmi� ortalama de�i�iklik s�ras�yla -
%0,30'dur ve %0,38'dir. Metformine ilave edilme �al��mas� i�in, HbA1c'deki azalmalar 102. haftaya kadar korunmu�tur (10 mg dapagliflozin ve plasebo i�in ba�lang�ca g�re d�zeltilmi� ortalama de�i�iklik s�ras�yla -%0,78 ve %0,02). �ns�lin i�in 104. haftada (ilave oral glukoz d���r�c� t�bbi �r�nler varl���nda veya yoklu�unda), HbA1c'deki azalmalara ili�kin olarak 10 mg dapagliflozin ve plasebo i�in ba�lang�ca g�re d�zeltilmi� ortalama de�i�iklik s�ras�yla -
%0,71 ve -%0,06'd�r. 48 ve 104. haftalarda ins�lin dozu 76 IU/g�n'l�k ortalama bir dozda 10 mg dapagliflozin ile tedavi edilen bireylerde ba�lang�ca g�re stabil kalm��t�r. Plasebo grubunda 48 ve 104. haftalarda ba�lang�ca g�re s�ras�yla 10,5 IU/g�n ve 18,3 IU/g�n'l�k (ortalama doz 84 ve 92 IU/g�n) ortalama bir art�� s�z konusudur. 104. haftada �al��mada kalan birey oran� 10 mg dapagliflozin ile tedavi edilen grup i�in %72,4't�r ve plasebo grubu i�in %54,8'dir.
Tablo 4. Metformin ya da sitagliptin (metforminle veya metforminsiz) ile ilave kombinasyon tedavi olarak dapagliflozine y�nelik plasebo kontroll� �al��malar�n 24 haftal�k sonu�lar� (LOCF)
�lave kombinasyon tedavisi | ||||
| Metformin | DPP-4 inhibit�r (sitagliptin) ± metformin | ||
| Dapagliflozin 10 mg | Plasebo | Dapagliflozin 10 mg | Plasebo |
N | 135 | 137 | 223 | 224 |
HbA1c (%) Ba�lang�� (ortalama) Ba�lang�ca g�re de�i�iklik Plaseboya g�re fark (%95 GA ) |
7,92 -0,84 -0,54* (-0,74, -0,34) |
8,11 -0,30 |
7,90 -0,45 -0,48* (-0,62, -0,34) |
7,97 0,04 |
HbA1c < %7'ye ula�an g�n�ll� y�zdesi Ba�lang�ca g�re d�zeltilen |
|
|
|
|
V�cut a��rl��� (kg) |
|
|
|
|
Ba�lang�� (ortalama) | 86,28 | 87,74 | 91,02 | 89,23 |
Ba�lang�ca g�re de�i�iklik | -2,86 | -0,89 | -2,14 | -0,26 |
Plaseboya g�re fark | -1,97* |
| -1,89* |
|
(%95 GA ) | (-2,63, -1,31) |
| (-2,37, -1,40) |
|
*p de�eri < 0,0001; plasebo + oral glukoz d���r�c� t�bbi �r�ne kar�� **p de�eri < 0,05; plasebo + oral glukoz d���r�c� t�bbi �r�ne kar��
| ||||

Tablo 5. 24 haftal�k, plasebo-kontroll�, ek s�lfonil�re (glimepirid) ya da metformin ve bir s�lfonil�re ile kombine dapagliflozin �al��malar�n�n sonu�lar�
Ek kombinasyon
S�lfonil�re (glimepirid)
S�lfonil�re
+metformin
Dapagliflozin 10 mg
Plasebo Dapagliflozin
10 mg
Plasebo
N | 151 | 145 | 108 | 108 |
HbA1c (%) |
|
|
|
|
Ba�lang�� de�eri | 8,07 | 8,15 | 8,08 | 8,24 |
(ortalama) Ba�lang�� seviyesine |
-0,82 |
-0,13 |
-0,86 |
-0,17 |
g�re de�i�im Plaseboya g�re fark� |
-0,68* |
|
-0,69* |
|
(%95 g�ven aral���) | (-0,86,-0,51) |
| (-0,89,-0,49) |
|
HbA1c < 7% (LOCF) |
|
|
|
|
ula�an denekler (%) Ba�lang�� de�erine |
31,7* |
13,0 |
31,8* |
11,1 |
g�re d�zeltilmi� |
|
|
|
|
V�cut a��rl��� (kg) (LOCF) Ba�lang�� de�eri |
80,56 |
80,94 |
88,57 |
90,07 |
(ortalama) |
|
|
|
|
Ba�lang�� seviyesine g�re de�i�im Plaseboya g�re fark� | -2,26
-1,54* | -0,72 | -2,65
-2,07* | -0,58 |
(%95 g�ven aral���) | (-2,17, -0,92) |
| (-2,79, -1,35) |
|
glimepirid 4 mg/g�n; 2Metformin (�abuk- ya da uzat�lm��-sal�ml� form�lasyonlar) >1500 mg/g�n, ek olarak, deneye kat�lmadan �nce en az 8 hafta boyunca, maksimum dozun en az yar�s� olacak �ekilde, maksimumtolereedilebilir dozdabir s�lfonil�re
Ba�lang�� seviyesi ve en az 1 ba�lang�� sonras� etkinlik �l��m� olan randomize ve tedavi
edilen hastalar
1. ve 2. kolonlar; LOCF metoduyla analiz edilmi� HbA1c (bkz. dipnot d); 3. ve 4. kolonlar
LRM metoduyla analiz edilmi� HbA1c (bkz. dipnot e)
Ba�lang�� de�erine g�re d�zeltilmi� en k���k kareler ortalamas�
LOCF: �leri aktar�lan son g�zlem (kurtarma tedavisi yap�lan bireylerde kurtarma �ncesinde)
BT�: Boylamsal tekrarlanm�� �l��mler analizi
*plasebo + oral glukoz-d���r�c� t�bbi �r�n(ler)e g�re p-de�eri < 0,0001
Tablo 6. �ns�lin ile kombinasyon halinde (tek ba��na veya oral glukoz d���r�c� t�bbi �r�nlerle birlikte) dapagliflozine y�nelik plasebo kontroll� �al��mada 24. hafta sonu�lar� (LOCF)
Parametre | 10 mg dapagliflozin + ins�lin ± oral glukoz d���r�c� t�bbi �r�nler | Plasebo + ins�lin ± oral glukoz d���r�c� t�bbi �r�nler |
N | 194 | 193 |
HbA1c (%) Ba�lang�� (ortalama) Ba�lang�ca g�re de�i�iklik Plaseboya g�re fark (%95 GA) |
8,58 |
8,46 |
-0,90 | -0,30 | |
-0,60 |
| |
(-0,74, -0,45) |
| |
V�cut a��rl��� (kg) Ba�lang�� (ortalama) Ba�lang�ca g�re de�i�iklik Plaseboya g�re fark (%95 GA) |
94,63 |
94,21 |
-1,67 | 0,02 | |
-1,68 |
| |
(-2,19, -1,18) |
| |
Ortalama + g�nl�k ins�lin dozu (IU) Ba�lang�� (ortalama) Ba�lang�ca g�re de�i�iklik Plaseboya g�re fark (%95 GA) Ortalama g�nl�k ins�lin dozunda en az %10 d���� olan bireyler (%) |
77,96 |
73,96 |
-1,16 | 5,08 | |
-6,23 |
| |
(-8,84, -3,63) |
| |
19,7 |
11,0 |
![]()
%80'i tek ba��na metformin, %12'si metformin + s�lfonil�re tedavisindedir ve kalanlar di�er oral glukoz d���r�c� t�bbi �r�nler kullanmaktad�r.
�la�-naif hastalarda metformin ile kombinasyon halinde
�la�-naif hastalarda metformin ile kombinasyon halinde dapagliflozin'in (5 mg veya 10 mg) etkililik ve g�venlili�ini her iki ilac�n tek ba��na uygulanmas�na k�yasla de�erlendirmek �zere iki aktif kontroll�, 24 haftal�k �al��maya yeterli d�zeyde kontrol alt�na al�nmayan tip 2 diyabetli (HbA1c ≥ %7,5 ve ≤ %12) toplam 1236 ila�-naif hasta kat�lm��t�r.
Metformin (g�nde 2000 mg'a kadar) ile kombinasyon halinde dapagliflozin 10 mg tedavisi, kombinasyonun ayr� ayr� bile�enlerine k�yasla HbA1c'de anlaml� iyile�me sa�lam�� (Tablo 7) ve a�l�k plazma glukozunda (AK�) (kombinasyonun ayr� ayr� bile�enlerine k�yasla) ve v�cut a��rl���nda (metformine k�yasla) daha fazla d����le sonu�lanm��t�r.
Tablo 7: �la�-naif hastalarda dapagliflozin ve metformin kombinasyonunu ara�t�ran aktif kontroll� bir �al��mada 24. hafta sonu�lar� (LOCF)
| Dapagliflozin 10 mg + metformin | Dapagliflozin 10 mg | Metformin |
Parametre |
|
| |
N | 211 | 219 | 208 |
HbA1c (%) Ba�lang�� (ortalama) Ba�lang��tan itibaren de�i�ime Dapagliflozine k�yasla fark (%95 GA) Metformine k�yasla fark (%95 CGA) |
9,10 |
9,03 |
9,03 |
-1,98 | -1,45 | -1,44 | |
−0,53 |
|
| |
(−0,74, −0,32) |
|
| |
−0,54 | −0,01 |
| |
(−0,75, −0,33) | (−0,22, 0,20) |
|
![]()
Uzat�lm�� sal�ml� eksenatid ile kombinasyon tedavisi
Yirmi sekiz haftal�k �ift k�r, aktif komparat�r-kontroll� bir �al��mada, dapagliflozin ve uzat�lm�� sal�ml� eksenatid (bir GLP-1 resept�r agonisti) kombinasyonu, tek ba��na metformin ile yeterli glisemik kontrol sa�lanamayan (HbA1c ≥%8 ve ≤ %12) hastalarda tek ba��na dapagliflozin ve uzat�lm�� sal�ml� eksenatid ile kar��la�t�r�lm��t�r. T�m tedavi gruplar�nda ba�lang�ca k�yasla HbA1c'de d���� olmu�tur. Dapagliflozin 10 mg ve uzat�lm�� sal�ml� eksenatid kombinasyonu uygulanan grupta, ba�lang�ca g�re HbA1c'de tek ba��na dapagliflozin ve uzat�lm�� sal�ml� eksenatid ile g�r�lenden daha fazla d���� g�zlenmi�tir (Tablo 8).
Tablo 8. Metformin ile kombinasyon halinde tek ba��na dapagliflozin ve uzat�lm�� sal�ml� eksenatide k�yasla dapagliflozin ve uzat�lm�� sal�ml� eksenatid kombinasyonunu ara�t�ran 28 haftal�k �al��ma sonu�lar� (tedavi ama�lanm�� hastalar)
| Dapagliflozin 10 mg QD + uzat�lm�� sal�ml� eksenatid 2 mg QW | Dapagliflozin 10 mg QD + plasebo QW | Uzat�lm�� sal�ml� eksenatid 2 mg QW + plasebo QD |
Parametre |
| ||
N | 228 | 230 | 227 |
HbA1c (%) |
|
|
|
Ba�lang�� (ortalama) | 9,29 | 9,25 | 9,26 |
Ba�lang��tan itibaren de�i�im | -1,98 | -1,39 | -1,60 |
Kombinasyon ve tekli t�bbi �r�n aras�nda ba�lang��tan itibaren de�i�imde ortalama fark (%95 GA) |
|
-0,59* (-0,84, -0,34) |
-0,38** (-0,63, -0,13) |
44,7 | 19,1 | 26,9 | |
V�cut a��rl��� (kg) |
|
|
|
Ba�lang�� (ortalama) | 92,13 | 90,87 | 89,12 |
Ba�lang��tan itibaren de�i�im | -3,55 | -2,22 | -1,56 |
Kombinasyon ve tekli t�bbi �r�n aras�nda ba�lang��tan itibaren de�i�imde ortalama fark (%95 GA) |
|
-1,33* (-2,12, -0,55) |
-2,00* (-2,79, -1,20) |
![]()
QD=g�nde bir kez, QW=haftada bir kez, N=hasta say�s�, GA=g�ven aral���.
a Ayarlanm�� en k���k kareler ortalamalar� (LS Ortalamalar�) ve 28. haftada ba�lang�� de�erlerinden itibaren de�i�imde tedavi gruplar� aras�ndaki farklar, tekrarl� �l��mlere sahip bir kar���k modelle (MMRM) modellenmi� ve bu modelde tedavi, b�lge, ba�lang�� HbA1c grubu (< %9,0 veya ≥% 9,0), hafta ve hafta baz�nda tedavi etkile�imi sabit fakt�rler, ba�lang�� de�erleri ise e�de�i�ken olarak kullan�lm��t�r.
*p < 0,001, **p < 0,01.
P-de�erlerinin t�m� �st katl�l�k i�in ayarlanm�� p-de�erleridir.
Analizler kurtarma tedavisinden sonraki �l��mleri ve �al��ma ilac�n�n erken sonland�r�lmas�ndan sonra yap�lan �l��mleri i�ermez.
A�l�k plazma glukozu
Monoterapi olarak veya metformin, glimepiride, metformin ve bir s�lfonil�re, sitagliptin (metforminle veya metforminsiz) ya da ins�line ilave tedavi olarak 10 mg dapagliflozin ile tedavi sonucunda, AK� d�zeylerinde plasebo ile kar��la�t�r�ld���nda (-0,33 mmol/L ila 0,21 mmol/L [-6,0 mg/dL ila 3,8 mg/dL]) istatistiksel olarak anlaml� d����ler meydana gelmi�tir (- 1,90 mmol/L ila -1,20 mmol/L [-34,2 mg/dL ila -21,7 mg/dL]). Bu etki, tedavinin birinci haftas�nda g�zlenmi�tir ve 104. haftaya kadar uzat�lan �al��malarda devam etmi�tir.
Dapagliflozin 10 mg ve uzat�lm�� sal�ml� eksenatid kombinasyonu 28. hafta AK�'de anlaml� �ekilde daha fazla d����le sonu�lanm��t�r: -3,66 mmol/l (-65,8 mg/dl), tek ba��na dapagliflozin i�in -2,73 mmol/l (-49,2 mg/dl) ile (p < 0,001) ve tek ba��na eksenatid i�in -2,54 mmol/L (-45,8 mg/dl) ile (p < 0,001) kar��la�t�r�lmal�.
Yaln�zca bu konunun ara�t�r�ld��� bir �al��mada eGFR de�eri ≥ 45 ila < 60 mL/dak/1,73 m olan diyabetli hastalarda dapagliflozin ile uygulanan tedavi 24 haftada FPG'de azalmalar ortaya ��karm��t�r: plaseboyla elde edilen -0,27 mmol/L'ye kar��l�k (-4,87 mg/dL) -1,19 mmol/L (- 21,46 mg/dL) (p=0,001).
Post-prandiyal glukoz
Glimepiride ilave olarak 10 mg dapagliflozin ile tedavi sonucunda 24. haftada 2 saatlik post- prandiyal glukoz de�erinde istatistiksel olarak anlaml� d����ler sa�lanm�� olup bu etki 48. haftaya kadar devam etmi�tir.
Sitagliptine (metforminle veya metforminsiz) ilave olarak 10 mg dapagliflozin tedavisi, 24 haftada, 2 saatlik post-prandiyal glukoz d�zeyinde azalmalar ile sonu�lanm�� olup bu etki 48. haftaya kadar devam etmi�tir.
Dapagliflozin 10 mg ve uzat�lm�� sal�ml� eksenatid kombinasyonu, her iki t�bbi �r�n�n tek ba��na uygulamas�na k�yasla 28. haftada 2. saatlik post-prandiyal glukoz d�zeyinde anlaml� �ekilde daha fazla d����le sonu�lanm��t�r.
V�cut a��rl���
Metformin, glimepirid, metformin ve bir s�lfonil�re, sitagliptin (metforminle veya metforminsiz) veya ins�line ilave olarak 10 mg dapagliflozin, 24. haftada v�cut a��rl���nda istatistiksel olarak anlaml� d���� sa�lam��t�r (p < 0,0001, Tablo 4 ve 5). Bu etkiler uzun s�reli �al��malarda korunmu�tur. 48. haftada, plaseboya k�yasla sitagliptine ilave tedavi olarak (metforminle veya metforminsiz) dapagliflozin i�in fark -2,22 kg'd�r. 102. haftada, plaseboya k�yasla metformine ilave tedavi olarak veya plaseboya k�yasla ins�line ilave olarak dapagliflozin i�in fark s�ras�yla -2,14 ve -2,88 kg'd�r.
Aktif kontroll� bir e�de�erlik �al��mas�nda metformine ilave tedavi olarak dapagliflozin, glipizide k�yasla 52. haftada v�cut a��rl���nda -4,65 kg'l�k istatistiksel olarak anlaml� bir azalma (p < 0,0001, Tablo 3) ile sonu�lanm�� ve bu, 104. ve 208. haftada korunmu�tur (s�ras�yla -5,06 kg ve -4,38 kg ).
Dapagliflozin 10 mg ve uzat�lm�� sal�ml� eksenatid kombinasyonu, her iki t�bbi �r�n�n tek ba��na uygulamas�na k�yasla anlaml� �ekilde daha fazla kilo kayb� ile sonu�lanm��t�r (Tablo 8).
V�cut bile�imini de�erlendirmek �zere �ift enerjili X-���n� absorpsiyometrisinin (DXA) kullan�ld���, 182 diyabetik birey ile ger�ekle�tirilen 24 haftal�k bir �al��ma, ya�s�z doku veya s�v� kayb� yerine DXA ile �l��ld���nde, plasebo ve metformin ile kar��la�t�r�ld���nda 10 mg dapagliflozin ve metformin ile s�ras�yla v�cut a��rl���nda ve v�cut ya� k�tlesinde d����lerin oldu�unu g�stermi�tir. Dapagliflozin ve metformin ile tedavi sonucunda, manyetik rezonans g�r�nt�leme alt �al��mas�nda plasebo ve metformin tedavisi ile kar��la�t�r�ld���nda i� organ ya� dokusunda say�sal azalma g�zlenmi�tir.
Kan bas�nc�
13 plasebo kontroll� �al��man�n �nceden tan�mlanm�� olan birle�tirilmi� analizinde, 24. haftada 10 mg dapagliflozin ile tedavi, sistolik kan bas�nc�nda ba�lang�ca g�re -3,7 mmHg ve diyastolik kan bas�nc�nda ba�lang�ca g�re -1,8 mmHg de�i�iklik ile sonu�lan�rken ayn� de�erler plasebo grubu i�in s�ras�yla -0,5 mmHg ve -0,5 mmHg olmu�tur. 104 haftaya kadar benzer azalmalar g�zlenmi�tir.
Dapagliflozin 10 mg ve uzat�lm�� sal�ml� eksenatid kombinasyonu, tek ba��na dapagliflozin (- 1,8 mmHg, p < 0,05) ve tek ba��na uzat�lm�� sal�ml� eksenatide (-1,2 mmHg, p < 0,01) k�yasla
28. haftada sistolik kan bas�nc�nda anlaml� �ekilde daha fazla d����le (-4,3 mmHg) sonu�lanm��t�r.
Yeterince kontrol alt�na al�namayan tip 2 diyabeti ve hipertansiyonu (bir �al��mada bir ACE-I ya da ARB ile �nceden mevcut stabil tedaviye ve di�er �al��mada ACE-I ya da ARB art� bir ilave antihipertansif tedaviye ra�men) olan toplam 1062 hasta, iki adet 12-haftal�k, plasebo- kontroll� �al��mada dapagliflozin 10 mg ya da plasebo ile tedavi edilmi�tir. Her iki �al��mada,
12. haftada dapagliflozin 10 mg art� al���ld�k antidiyabetik tedavi, HbA1c'de d�zelme sa�lam��
ve plasebo a��s�ndan d�zeltilmi� sistolik kan bas�nc�nda s�ras�yla ortalama 3,1 ve 4,3 mmHg
Yaln�zca bu konunun ara�t�r�ld��� bir �al��mada eGFR de�eri ≥ 45 ila < 60 mL/dak/1,73 m olan diyabetli hastalarda dapagliflozin ile uygulanan tedavi 24 haftada oturur pozisyondaki sistolik kan bas�nc�nda azalmalar ortaya ��karm��t�r: plaseboyla elde edilen -1,7 mmHg‘ye kar��l�k -4,8 mmHg (p < 0,05).
Orta derecede b�brek yetmezli�i g�r�len hastalarda glisemik kontrol KBH 3A (eGFR ≥ 45 ila
![]()
< 60 mL/dak/1,73 m)
Dapagliflozinin etkilili�i yaln�zca bu konunun ara�t�r�ld��� bir �al��mada eGFR de�eri ≥ 45 ila
< 60 mL/dak/1,73 m olan ve ola�an bak�mla yeterli glisemik kontrol sa�lanamayan diyabetli hastalarda de�erlendirilmi�tir. Dapagliflozinle uygulanan tedavi HbA1c'de ve v�cut a��rl���nda plaseboya k�yasla azalmalar ortaya ��karm��t�r (Tablo 9).
Tablo 9. eGFR de�eri ≥ 45 ila < 60 mL/dak/1,73 molan diyabetli hastalarda dapagliflozinle yap�lan plasebo kontroll� bir �al��man�n 24. Hafta sonu�lar�
| Dapagliflozin 10 mg | Plasebo |
N | 159 | 161 |
HbA1c (%) |
|
|
Ba�lang�� (ortalama) | 8,35 | 8,03 |
Ba�lang�ca g�re de�i�iklik | -0,37 | -0,03 |
Plaseboya k�yasla fark (%95 GA) | -0,34* (-0,53, -0,15) |
|
V�cut a��rl��� (kg) |
|
|
Ba�lang�� (ortalama) | 92,51 | 88,30 |
Ba�lang�ca g�re de�i�iklik y�zdesi | -3,42 | -2,02 |
Plaseboya k�yasla fark y�zdesindeki de�i�iklik (%95 GA) | -1,43* (-2,15, -0,69) |
|
a .Metformin veya metformin hidroklor�r dapagliflozin ve plasebo gruplar�nda hastalar�n s�ras�yla %69,4'�nde ve %64,0'�nda ola�an bak�m�n bir par�as�yd� b Ba�lang�� de�erine g�re ayarlanm�� en k���k kareler ortalamas� c Ba�lang�� de�erine g�re ayarlanm�� en k���k kareler ortalamas�ndan elde edilmi�tir * p<0,001 | ||
Ba�lang�� HbA1c de�eri ≥ %9 olan hastalar
Ba�lang��ta HbA1c de�eri ≥ %9,0 olan bireylerle ger�ekle�tirilen �nceden tan�mlanm�� olan bir analizde 10 mg dapagliflozin ile tedavi sonucunda 24. haftada HbA1c'de istatistiksel olarak anlaml� d����ler elde edilmi�tir (monoterapi olarak: d�zeltilmi� ba�lang�ca g�re ortalama de�i�iklik: 10 mg dapagliflozin ve plasebo i�in s�ras�yla -%2,04 ve %0,19; metformine ilave tedavi olarak: d�zeltilmi� ba�lang�ca g�re ortalama de�i�iklik: dapagliflozin ve plasebo i�in s�ras�yla -%1,32% ve -%0,53).
Kardiyovask�ler ve renal sonu�lar
Dapagliflozinin Kardiyovask�ler Olaylar �zerindeki Etkisi (DECLARE) �al��mas�, mevcut
plaseboya k�yasla etkisini belirlemek �zere ger�ekle�tirilmi� olan uluslararas�, �ok merkezli, randomize, �ift k�r, plasebo kontroll� bir klinik �al��mayd�. T�m hastalarda tip 2 diyabet ve en az iki ilave kardiyovask�ler risk fakt�r� (erkeklerde ya��n ≥ 55 olmas� veya kad�nlarda ya��n ≥ 60 olmas� ve dislipidemi, hipertansiyon ya da e�zamanl� t�t�n kullan�m� durumlar�ndan bir veya daha fazlas�n�n mevcut olmas�) ya da kan�tlanm�� kardiyovask�ler hastal�k mevcuttu.
Randomize edilen 17160 hastan�n 6974'� (%40,6) kan�tlanm�� kardiyovask�ler hastal��a sahipti, 10186's�nda ise (%59,4) kan�tlanm�� kardiyovask�ler hastal�k mevcut de�ildi. 8582 hasta 10 mg dapagliflozine, 8578'i ise plasebo randomize edildi ve medyan 4,2 y�l s�resince takip edildi.
�al��ma pop�lasyonunun ortalama ya�� 63,9'du ve %37,4'� kad�nd�. Toplamda %22,4'� ≤ 5 y�ld�r diyabetliydi ve diyabetin ortalama s�resi 11,9 y�ld�. Ortalama HbA1c %8,3, ortalama beden k�tle indeksi (BK�) ise 32,1 kg/m'ydi.
Ba�lang��ta hastalar�n %10,0'� kalp yetersizli�i �yk�s�ne sahipti. Ortalama eGFR 85,2 mL/dak/1,73 m'ydi, hastalar�n %7,4'�nde eGFR < 60 mL/dak/1,73 m'ydi, hastalar�n
%30,3'�nde ise mikroalb�min�ri veya makroalb�min�ri (UACR s�ras�yla ≥ 30 ila ≤ 300 mg/g veya > 300 mg/g) mevcuttu.
Hastalar�n �o�u (%98) ba�lang��ta metformin (%82), ins�lin (%41) ve s�lfonil�reyi (%43) i�eren bir ya da daha fazla diyabetik ila� kullanm��t�r.
Birincil sonlan�m noktalar�, kardiyovask�ler �l�m, miyokard infarkt�s� ya da iskemik inmeden (MACE) olu�an ilk olaya kadar ge�en s�re ve kalp yetersizli�i i�in hastane yat��� ya da kardiyovask�ler �l�mden olu�an ilk olaya kadar ge�en s�re olmu�tur. �kincil sonlan�m noktalar� bir renal bile�ik sonlan�m noktas� ve t�m nedenlere ba�l� mortalite olmu�tur.
Maj�r advers kardiyovask�ler olaylar
Dapagliflozin 10 mg, plaseboya kar�� kardiyovask�ler �l�m, miyokard infarkt�s� ya da iskemik inme bile�imi i�in daha k�t� olmam��t�r (tek-tarafl� p < 0,001).
Kalp yetersizli�i veya kardiyovask�ler �l�m
Dapagliflozin 10 mg, kalp yetersizli�ine ba�l� hastane yat��� ya da kardiyovask�ler �l�m bile�iminin �nlenmesinde plaseboya kar�� �st�nl�k g�stermi�tir (�ekil 1). Tedavi etkisindeki farkl�l���n kalp yetersizli�i nedeniyle hastaneye yat��tan kaynakland���na ve kardiyovask�ler �l�m a��s�ndan a��k bir farkl�l�k olmad���na i�aret etmektedir (�ekil 2).
Dapagliflozinin plaseboya k�yasla sahip oldu�u tedavi yarar� hem kan�tlanm�� kardiyovask�ler hastal��� bulunan hem de bulunmayan hastalarda ve hem ba�lang��ta kalp yetersizli�i bulunan hem de bulunmayan hastalarda g�zlenmi�tir. Bu yarar ya�, cinsiyet, b�brek fonksiyonu (eGFR) ve b�lgenin aralar�nda oldu�u kilit alt gruplarda tutarl�l�k sergilemi�tir.
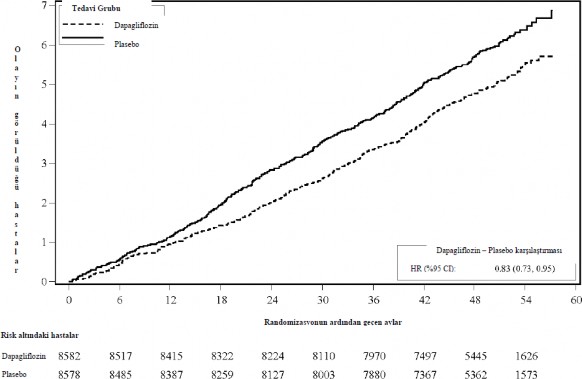
�ekil 1: Kalp yetersizli�i nedeniyle ilk hastaneye yat��a veya kardiyovask�ler �l�me kadar ge�en s�re
Risk alt�ndaki hastalar periyodun ba�lang�c�ndaki risk alt�ndaki hastalar�n say�s�d�r. HR=Tehlike oran� GA=g�ven aral���.
Birincil ve ikincil sonlan�m noktalar�n�n sonu�lar� �ekil 2'de g�sterilmektedir. MACE i�in dapagliflozinin plasebo kar��s�ndaki �st�nl��� g�sterilmemi�tir (p=0,172). Bu nedenle renal bile�ik son nokta ve t�m nedenlere ba�l� mortalite do�rulay�c� test prosed�r�n�n bir par�as� olarak test edilmemi�tir.
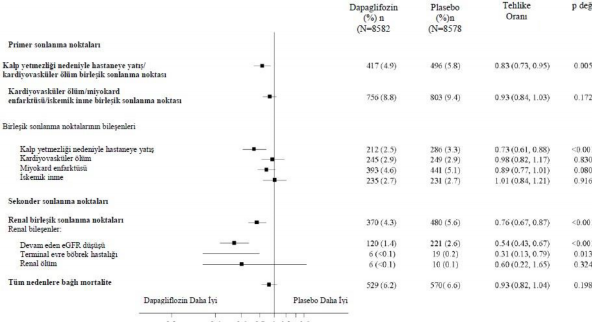
�ekil 2: Primer birle�ik sonlan�m noktalar� ile bunlar�n bile�enleri ve sekonder sonlan�m noktalar� ile bunlar�n bile�enleri �zerindeki tedavi etkileri
Renal birle�ik sonlan�m noktas� �u �ekilde tan�mlanm��t�r: eGFR'de devam eden do�rulanm��
≥ %40'l�k d���� (eGFR <60 mL/dak/1,73m'ye) ve/veya son d�nem b�brek hastal��� (≥ 90 g�n diyaliz veya b�brek nakli, devam eden do�rulanm�� eGFR < 15 mL/dak/1,73m) ve/veya renal ya da kardiyovask�ler �l�m.
p de�erleri primer sonlan�m noktalar� i�in iki yanl� p de�erleridir, sekonder sonlanma noktalar� ve t�m tekli bile�enler i�inse nominal p de�erleridir. �lk olay meydana gelene kadar ge�en s�re Cox orant�l� tehlikeler modeli kullan�larak analiz edilmi�tir. Tekli bile�enler i�in ilk olaylar�n say�s� her bir bile�en i�in ilk olaylar�n ger�ek say�s�d�r ve birle�ik sonlan�m noktas�ndaki olaylar�n say�s�na eklenmez. GA=g�ven aral���.
Nefropati
Dapagliflozin do�rulanm�� devam eden eGFR d�����, son d�nem b�brek hastal���, renal veya kardiyovask�ler �l�m birle�ik olaylar�n�n insidans�n� azaltm��t�r. Gruplar aras�ndaki farkl�l�k renal bile�enler olan devam eden eGFR d�����, son d�nem b�brek hastal��� ve renal �l�mde ortaya ��kan azalmalardan kaynaklanm��t�r (�ekil 2).
Nefropatiye kadar ge�en s�re i�in tehlike oran� (HR) (s�rekli eGFR azalmas�, son evre b�brek hastal��� ve renal �l�m) plaseboya kar�� dapagliflozin i�in 0,53 (%95 GA 0,43, 0,66) olmu�tur.
Ayr�ca, plasebo ile kar��la�t�r�ld���nda dapagliflozin yeni ba�lang��l� s�rekli alb�min�riyi azaltm�� (HR 0,79 [%95 GA 0,72, 0,87]) ve makroalb�min�ride daha fazla gerileme sa�lam��t�r
(HR 1,82 [%95 GA 1,51, 2,20]).
Kalp yetersizli�i
Dapagliflozin ve Kalp Yetersizli�inde Advers Sonu�lar�n �nlenmesi (DAPA-HF) �al��mas�, d���k ejeksiyon fraksiyonu (sol ventrik�ler ejeksiyon fraksiyonu [LVEF] ≤ %40) ile seyreden kalp yetersizli�i (New York Kalp Birli�i [NYHA] fonksiyonel s�n�f� II-IV) g�r�len hastalar �zerinde arka plan standart tedaviye eklenen dapagliflozinin kardiyovask�ler �l�m ve kalp yetersizli�inde k�t�le�me insidans� �zerinde plaseboya k�yasla etkisini belirlemek amac�yla ger�ekle�tirilmi� olan uluslararas�, �ok merkezli, randomize, �ift k�r, plasebo kontroll� bir �al��mayd�.
4744 hastan�n 2373'� 10 mg dapagliflozine, 2371'i ise plaseboya randomize edildi ve medyan 18 ayl�k bir s�re boyunca takip edildi. �al��ma pop�lasyonunun medyan ya�� 66'yd� ve %77'si erkekti.
Ba�lang��ta hastalar�n %67,5'i NYHA s�n�f II, %31,6's� s�n�f III, %0,9'u ise s�n�f IV �eklinde s�n�fland�r�ld�, medyan LVEF %32'ydi, kalp yetmezliklerinin %56's�n�n iskemik, %36's�n�n iskemik d��� oldu�u g�r�ld�, %8'inin ise etiyolojisi belirlenemedi. Her bir tedavi grubundaki hastalar�n %42'si tip 2 diyabet �yk�s�ne sahipti ve her bir gruptaki hastalar�n ilave bir %3'� hem kay�t hem de randomizasyon s�ras�nda ≥ %6,5 seviyesinde HbA1c de�erine dayan�larak tip 2 diyabete sahip �eklinde s�n�fland�r�ld�. Hastalara standart tedavi uygulanmaktayd�; hastalar�n %94'� ACE-I, ARB veya anjiyotensin resept�r�-neprilisin inhibit�r� (ARNI, %11),
%96's� beta-bloker, %71'i mineralokortikoid resept�r antagonisti (MRA), %93'� di�retik ile tedavi g�rmekteydi, %26's�nda ise implante edilebilir bir cihaz (defibrilat�r fonksiyonu ile) bulunmaktayd�.
Kay�t s�ras�nda eGFR de�eri ≥ 30 mL/dak/1,73 m olan hastalar �al��maya dahil edildi. Ortalama eGFR de�eri 66 mL/dak/1,73 m'ydi, hastalar�n %41'inde eGFR < 60mL/dak/1,73 m, %15'inde ise eGFR < 45 mL/dak/1.73 m olarak tespit edildi.
Kardiyovask�ler �l�m ve kalp yetersizli�inde k�t�le�me
Dapagliflozin, kardiyovask�ler �l�m, kalp yetersizli�i nedeniyle hastaneye yat�� veya kalp yetersizli�i nedeniyle acil servis ziyareti primer birle�ik sonlanma noktas�n� �nlemek konusunda plaseboya k�yasla �st�nl�k sergilemi�tir (HR 0,74 [%95 GA 0,65, 0,85], p < 0,0001). Bu etki erken d�nemde g�zlenmi�tir ve �al��ma s�resince varl���n� korumu�tur (�ekil 3).
�ekil 3: Kardiyovask�ler �l�m, kalp yetersizli�i nedeniyle hastaneye yat�� veya kalp yetersizli�i nedeniyle acil hastane ziyaretini i�eren primer birle�ik sonlanma noktas� ilk ortaya ��kana kadar ge�en s�re
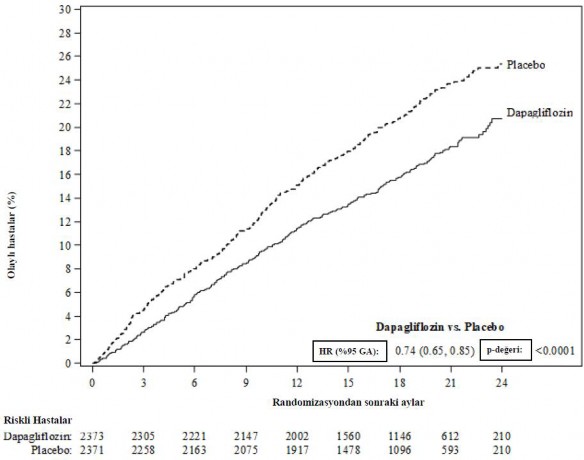
Kalp yetersizli�i nedeniyle acil hastane ziyareti, �rne�in bir acil serviste ger�ekle�tirilen ve kalp yetersizli�inde k�t�le�me (yaln�zca oral di�retiklerde bir art�� �eklinde de�il) nedeniyle tedavi gerektiren, acil, planl� olmayan bir doktor de�erlendirmesi �eklinde tan�mlanm��t�r.
Risk alt�ndaki hastalar periyodun ba�lang�c�nda risk alt�nda olan hastalar�n say�s�d�r.
Primer birle�ik sonlanma noktas�n�n �� bile�eni de tedavi etkisine ayr� ayr� katk�da bulunmu�tur (�ekil 4). Birka� acil kalp yetersizli�i ziyareti olmu�tur.
�ekil 4: Primer birle�ik sonlanma noktas�, onun bile�enleri ve t�m nedenlerden kaynaklanan mortaliteye ili�kin tedavi etkileri
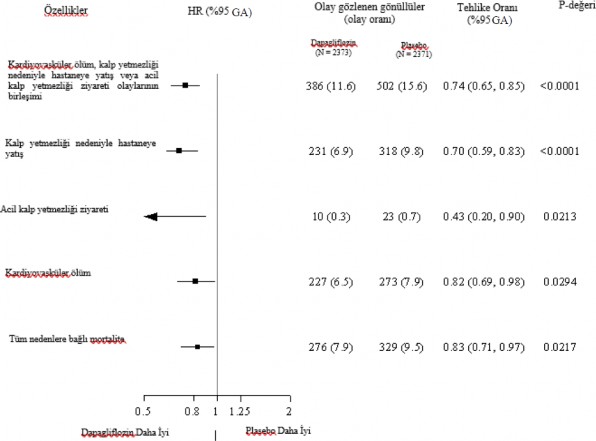
Kalp yetersizli�i nedeniyle acil hastane ziyareti, �rne�in bir acil serviste ger�ekle�tirilen ve kalp yetersizli�inde k�t�le�me (yaln�zca oral di�retiklerde bir art�� �eklinde de�il) nedeniyle tedavi gerektiren, acil, planl� olmayan bir doktor de�erlendirmesi �eklinde tan�mlanm��t�r.
�lk olaylar�n say�s�, her bir bile�ene ili�kin ilk olaylar�n ger�ek say�s�d�r ve toplam� birle�ik sonlanma noktas�ndaki olay say�s�na e�it de�ildir.
Olay oranlar�, 100 hasta y�l� takip ba��na olay g�zlenen g�n�ll�lerin say�s� �eklinde sunulmaktad�r.
Tek tek bile�enlere ve t�m nedenlerden kaynaklanan mortaliteye ili�kin p de�erleri nominaldir.
Dapagliflozin, ayn� zamanda kalp yetersizli�i nedeniyle hastaneye yat�� (ilk ve rek�rren) ve kardiyovask�ler �l�m olaylar�n�n toplam say�s�n� d���rm��t�r; dapagliflozin grubunda 567 olay, plasebo grubunda ise 742 olay ortaya ��km��t�r (Olay Oran� 0,75 [%95 GA 0,65, 0,88], p
< 0,0002).
Dapagliflozinin ortaya ��kard��� tedavi yarar�, tip 2 diyabeti olan ve olmayan kalp yetersizli�i hastalar�nda g�zlenmi�tir. Dapagliflozin, kardiyovask�ler �l�m insidans� ve kalp yetersizli�inde k�t�le�me primer birle�ik sonlanma noktas�n� diyabet hastalar�nda 0,75'lik (%95 GA 0,63, 0,90), bir HRde�eriiled���rm��t�r.
Dapagliflozinin primer sonlanma noktas� �zerinde plaseboya k�yasla sergiledi�i tedavi faydas�, e�zamanl� kalp yetersizli�i tedavisi, b�brek fonksiyonu (eGFR), ya�, cinsiyet ve b�lgenin de aralar�nda oldu�u di�er kilit alt gruplarda da tutarl�l�k g�stermi�tir.
Hasta taraf�ndan bildirilen sonu� – kalp yetersizli�i semptomlar�
Dapagliflozinin kalp yetersizli�i semptomlar� �zerinde ortaya ��kard��� tedavi etkisi, bitkinlik, periferik �dem, dispne ve ortopneyi i�eren kalp yetersizli�i semptomlar�n�n s�kl���n� ve �iddetini �l�en Kansas City Kardiyomiyopati Anketi Toplam Semptom Skoru (KCCQ-TSS) ile de�erlendirilmi�tir. Skor 0 ile 100 aras�nda de�i�mektedir ve daha y�ksek skorlar sa�l�k durumunun daha iyi oldu�unu g�stermektedir.
Dapagliflozinle uygulanan tedavi, KCCQ-TSS'de ba�lang��tan 8. aya kadar meydana gelen de�i�iklikle �l��ld��� �zere, kalp yetersizli�i semptomlar� �zerinde plaseboya k�yasla istatistiksel ve klinik a��dan anlama sahip olan bir yarar ortaya ��karm��t�r (Kazan� Oran� 1,18 [%95 GA 1,11, 1,26]; p < 0,0001). Hem semptom s�kl��� hem de semptom y�k� sonu�lara katk�da bulunmu�tur. Hem kalp yetersizli�i semptomlar�nda iyile�me sa�lanmas� hem de kalp yetersizli�i semptomlar�ndaki k�t�le�menin �nlenmesi konusunda yarar g�zlenmi�tir.
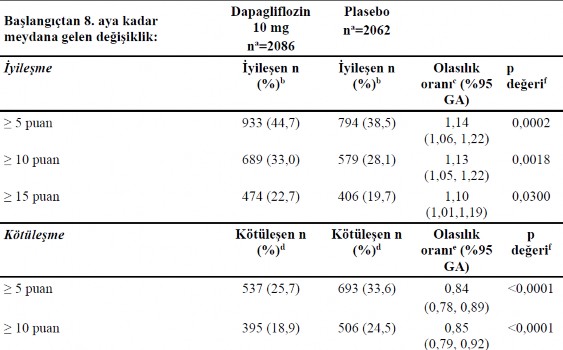
Yan�t veren analizlerinde KCCQ-TSS'de ba�lang��tan 8. aya 5 puan veya daha fazla art�� �eklinde tan�mlanan klinik a��dan anlaml� bir iyile�me g�zlenen hastalar�n oran�n�n dapagliflozin tedavisi grubunda plaseboya k�yasla daha y�ksek oldu�u g�r�lm��t�r. 5 puan veya daha fazla d���� �eklinde tan�mlanan klinik a��dan anlaml� k�t�le�me g�zlenen hastalar�n oran�n�n dapagliflozin tedavisi grubunda plaseboya k�yasla daha d���k oldu�u g�r�lm��t�r. Dapagliflozin ile elde edilen yararlar, klinik a��dan anlaml� daha b�y�k de�i�iklik i�in daha konservatif kesmeler uyguland���nda da varl���n� korumu�tur (Tablo 10).
Tablo 10. KCCQ-TSS'de 8 ayda klinik a��dan anlaml� iyile�me ve k�t�le�me ya�ayan hastalar�n say�s� ve y�zdesi
5.2. Farmakokinetik �zellikler
Genel �zellikler
Emilim:
Dapagliflozin, oral uygulama sonras�nda h�zla ve iyi absorbe edilmektedir. Maksimum dapagliflozin plazma konsantrasyonlar�na (C) genellikle a� karn�na uygulamadan sonraki iki saat i�erisinde ula��lmaktad�r. G�nde bir kez 10 mg dapagliflozin dozlar�ndan sonra geometrik ortalama kararl� durum dapagliflozin Cve EAAde�erleri s�ras�yla 158 ng/mL ve 628 ng s/mL olmu�tur. 10 mg dozunun uygulanmas�ndan sonra dapagliflozinin mutlak oral biyoyararlan�m� %78 olmaktad�r. Y�ksek oranda ya� i�eren bir ���nle birlikte verildi�inde dapagliflozinin Cde�eri %50'ye kadar azalm�� ve Tde�eri yakla��k 1 saat uzam��; ancak a�l�k durumu ile kar��la�t�r�ld���nda EAA de�eri de�i�memi�tir. Bu de�i�iklikler klinik olarak anlaml� kabul edilmemektedir. Bu nedenle DAPL�G a� veya tok karn�na al�nabilir.
Da��l�m:
Dapagliflozin yakla��k %91 oran�nda proteine ba�lanmaktad�r. Proteine ba�lanma oran� farkl� hastal�k durumlar�ndan etkilenmemektedir (�rn. b�brek veya karaci�er yetmezli�i). Dapagliflozinin ortalama kararl� durum da��l�m hacmi 118 L'dir.
Biyotransformasyon:
Dapagliflozin b�y�k �l��de metabolize olarak, ba�l�ca inaktif bir metabolit olan dapagliflozin 3-O-glukuronide metabolize olmaktad�r. Dapagliflozin 3-O-glukuronid veya di�er metabolitler glukoz d���r�c� etkilere katk�da bulunmamaktad�r. Dapagliflozin 3-O-glukuronid olu�umuna karaci�er ve b�brekte bulunan bir enzim olan UGT1A9 arac�l�k eder ve CYP'nin arac�l�k etti�i metabolizma insanda min�r bir klerens yola��d�r.
Eliminasyon:
Dapagliflozinin ortalama plazma terminal yar� �mr� (t) sa�l�kl� bireylere tek oral 10 mg dapagliflozin dozunun uygulanmas�ndan sonra 12,9 saattir. �ntraven�z uygulanan dapagliflozinin ortalama toplam sistemik klerensi 207 mL/dak olarak �l��lm��t�r. Dapagliflozin ve ilgili metabolitleri ba�l�ca idrar yolu ile elimine olur ve bunun %2'den az� de�i�memi� dapagliflozin �eklindedir. 50 mg [C]-dapagliflozin dozunun uygulanmas�ndan sonra %96's� geri kazan�lm�� olup, bunun %75'i idrarda ve %21'i fe�estedir. Fe�este dozun yakla��k %15'i ana ila� olarak at�lm��t�r.
Do�rusal/do�rusal olmayan durum:
Dapagliflozin maruziyeti, 0,1 mg ila 500 mg aral���nda dapagliflozin dozundaki art�� ile orant�l� olarak artm��t�r ve 24 haftaya kadarki tekrarl� g�nl�k doz uygulamalar� ile farmakokineti�inde zaman i�inde de�i�iklik olmam��t�r.
Hastalardaki karakteristik �zellikler
B�brek yetmezli�i:
Kararl� durumda (7 g�n s�reyle g�nde bir kez 20 mg dapagliflozin), tip 2 diabetes mellitusu ve hafif, orta veya a��r derecede b�brek yetmezli�i olan bireylerde (ioheksol plazma klerensi ile belirlenmi�tir) ortalama sistemik dapagliflozin maruziyeti, b�brek fonksiyonu normal olan tip 2 diabetes mellitusu olan bireylere g�re s�ras�yla %32, %60 ve %87 daha y�ksek olmu�tur. Kararl� durumda 24 saatlik �riner glukoz at�l�m�, b�brek fonksiyonu ile y�ksek derecede ili�kili olup tip 2 diabetes mellitusu ve normal b�brek fonksiyonu olan bireylerde veya hafif, orta veya a��r derecede b�brek yetmezli�i olan hastalarda s�ras�yla 85, 52, 18 ve 11 g glukoz/g�n at�l�m� tespit edilmi�tir. Hemodiyalizin dapagliflozin maruziyetine etkisi bilinmemektedir. B�brek fonksiyonundaki azalman�n sistemik maruziyet �zerindeki etkisi, bir pop�lasyon farmakokinetik modelinde incelenmi�tir. �nceki sonu�larla tutarl� olarak, modelin tahmini AUC de�eri normal b�brek fonksiyonuna sahip hastalara k�yasla kronik b�brek hastal��� bulunan hastalarda daha y�ksektir ve tip 2 diyabeti bulunan ve bulunmayan kronik b�brek hastalar� aras�nda anlaml� fark yoktur.
Karaci�er yetmezli�i:
Hafif veya orta derecede karaci�er yetmezli�i olan hastalarda (Child-Pugh s�n�f A ve B), ortalama dapagliflozin Cve EAA de�erleri, sa�l�kl�, benzer �zelliklere sahip kontrol bireylere k�yasla s�ras�yla %12'ye ve %36'ya kadar daha y�ksek olmu�tur. Bu farkl�l�klar�n klinik olarak anlaml� olmad��� kabul edilmi�tir. A��r derecede karaci�er yetmezli�i olan bireylerde (Child-Pugh s�n�f C) dapagliflozinin ortalama Cve EAA de�erleri, benzer �zelliklere sahip sa�l�kl� kontrollerden s�ras�yla %40 ve %67 daha y�ksek bulunmu�tur.
Geriyatrik hastalarda (≥ 65 ya�):
70 ya��na kadarki bireylerde tek ba��na ya�a ba�l� maruziyette klinik olarak anlaml� bir art�� olmamaktad�r. Bununla birlikte, b�brek fonksiyonunda ya�a ba�l� d���� nedeniyle artm�� maruziyet beklenebilir. 70 ya��n �zerindeki hastalarda maruziyet ile ilgili sonu�lara varabilmek i�in yeterli veri bulunmamaktad�r.
Pediyatrik pop�lasyon
Pediyatrik pop�lasyonda farmakokinetik hen�z �al���lmam��t�r.
Cinsiyet
Kad�nlarda ortalama dapagliflozin EAAde�erinin erkeklere oranla %22 daha y�ksek oldu�u tahmin edilmektedir.
Irk
Beyaz, Siyah veya Asyal� �rklar aras�nda sistemik maruziyet a��s�ndan klinik olarak anlaml� herhangi bir farkl�l�k bulunmamaktad�r.
V�cut a��rl���
Dapagliflozin maruziyetinin, artan a��rl�kla d��t��� bulunmu�tur. Bu nedenle d���k v�cut a��rl���na sahip hastalarda maruziyet biraz daha y�ksek olabilir ve y�ksek v�cut a��rl���na sahip hastalarda ise maruziyet biraz daha d���k olabilir. Bununla birlikte maruziyetteki farkl�l�klar klinik a��dan �nemli kabul edilmemektedir.
5.3. Klinik �ncesi g�venlilik verileri
Klinik d��� veriler; g�venlilik farmakolojisi, tekrarl� doz toksisitesi, genotoksisite, karsinojenik potansiyel ve fertiliteyi kapsayan standart �al��malar do�rultusunda insanlar i�in �zel bir tehlike ortaya koymam��t�r. Dapagliflozin farelerde veya s��anlarda, iki y�ll�k karsinojenisite �al��malar�nda de�erlendirilen dozlar�n herhangi birinde t�m�r olu�umuna neden olmam��t�r.
�reme toksisitesi ve geli�imsel toksisite
Yeni s�tten kesilen j�venil s��anlara do�rudan dapagliflozin uygulamas� ve gebelik (insanda b�brek mat�rasyonu a��s�ndan gebeli�in ikinci ve ���nc� trimesterlerine kar��l�k gelen d�nemler) ile emzirme d�nemi s�ras�ndaki dolayl� maruziyet, ayr� ayr�, yavrularda b�brek pelvis ve t�b�ler dilatasyon insidans ve/veya �iddetinde art�� ile ili�kilidir.
J�venil toksisite �al��mas�nda, dapagliflozin gen� s��anlara 21. postnatal g�nden itibaren postnatal 90. g�ne kadar do�rudan uyguland���nda t�m doz d�zeylerinde renal pelvis ve t�b�ler dilatasyonlar bildirilmi�tir; yavrularda, test edilen en d���k dozda maruziyet, maksimum �nerilen insan dozunun ≥ 15 kat� olmu�tur. Bu bulgular, t�m dozlarda g�zlenen dozla ili�kili b�brek a��rl��� art��� ve makroskobik b�brek b�y�mesi ile ili�kilendirilmi�tir. J�venil hayvanlarda g�zlenen renal pelvik ve t�b�ler dilatasyonlar yakla��k 1 ayl�k iyile�me d�neminde tamamen geri d�n���ml� olmam��t�r.
Ba�ka bir prenatal ve postnatal geli�im �al��mas�nda anne s��anlara gebeli�in 6. g�n�nden postnatal 21. g�ne kadar doz uygulanm��t�r ve yavrular intra uterin ve emzirme yoluyla ilaca dolayl� olarak maruz b�rak�lm��t�r (s�tte ve yavrularda dapagliflozin maruziyetini de�erlendirme ama�l� bir ek �al��ma ger�ekle�tirilmi�tir). �la� uygulanan di�i hayvanlar�n eri�kin yavrular�nda renal pelvis dilatasyon insidans�nda veya �iddetinde art�� g�r�lm��; ancak bu etkiler sadece test edilen en y�ksek dozda meydana gelmi�tir (kar��l�k gelen maternal ve yavru dapagliflozin maruziyetleri maksimum �nerilen insan dozunda insan de�erinin s�ras�yla 1415 ve 137 kat �st� olmu�tur). Bunlar d���ndaki geli�imsel toksisite etkileri yavrular�n v�cut a��rl�klar�nda dozla ilgili d����leri ile s�n�rl� olmu� ve sadece ≥ 15 mg/kg/g�n dozlar�nda g�r�lm��t�r (maksimum �nerilen insan dozunda insan de�erlerinin ≥ 29 kat� olan yavru maruziyetleri ile ili�kili). Maternal toksisite sadece test edilen en y�ksek dozda g�r�lm�� ve v�cut a��rl���nda ve dozla birlikte yem t�ketiminde ge�ici azalmalar ile s�n�rl� kalm��t�r. Geli�imsel toksisite a��s�ndan advers etkinin g�r�lmedi�i d�zey (NOAEL), yani test edilen en d���k doz, maksimum �nerilen insan dozunda insan de�erinin yakla��k 19 kat� olan maternal sistemik maruziyet ile ili�kilidir.
S��anlar ve tav�anlardaki ek embriyo-fetal geli�im �al��malar�nda dapagliflozin, her t�rde ba�l�ca organogenez d�nemlerine denk gelen aral�klarda uygulanm��t�r. Tav�anlarda test edilen dozlar�n herhangi birinde maternal ya da geli�imsel toksisite g�zlenmemi�tir; test edilen en y�ksek doz, maksimum �nerilen insan dozunun yakla��k 1191 kat� sistemik maruziyet ile ili�kilidir. Dapagliflozin, s��anlarda, maksimum �nerilen insan dozunun 1441 kat�na kadarki maruziyetlerde embriyoletal ya da teratojenik etki g�stermemi�tir.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Tablet �ekirde�i:
Mikrokristalin Sel�loz, PH105
Susuz Laktoz (s���r s�t�nden elde edilmektedir) Kroskarmelloz Sodyum
Mikrokristalin Sel�loz, PH200 LM Sodyum Stearil Fumarat
Film kaplama maddesi (Opadry® II Yellow 85F220219):
Polivinilalkol k�smi hidrolize
Makrogol / PEG Talk
Sar� Demir Oksit
6.2. Ge�imsizlikler
Bilinen herhangi bir ge�imsizli�i bulunmamaktad�r.
6.3. Raf �mr�
24 ay
6.5. Ambalaj�n niteli�i ve i�eri�i
�r�n�m�z �effaf PVC/Aclar ve aluminyum folyo blister ile ambalajlan�r. Blisterler karton kutular i�erisinde paketlenir. Bir kutu i�erisinde 28 adet film kapl� tablet i�eren blister ambalajlarda kullanma talimat� ile birlikte sunulmaktad�r.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj At�klar�n�n Kontrol� Y�netmelik”lerine uygun olarak imha edilmelidir.
 Diyabet Hastal���
Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r.
Diyabet Hastal���
Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r. |
 Belso�uklu�u, Chlamydia ve Frengi
Belso�uklu�u, bakterilerin sebep oldu�u bir enfeksiyondur. Cinsel ili�ki
yoluyla bula��r ve d�lyata�� boynunda, idrar yollar�nda, an�ste, makatta ve
bo�azda enfeksyona sebep olabilir.
Belso�uklu�u, Chlamydia ve Frengi
Belso�uklu�u, bakterilerin sebep oldu�u bir enfeksiyondur. Cinsel ili�ki
yoluyla bula��r ve d�lyata�� boynunda, idrar yollar�nda, an�ste, makatta ve
bo�azda enfeksyona sebep olabilir. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| DAPADAP | 8681428091713 | 567.67TL |
| DAPGEON | 8699293097334 | 567.67TL |
| DAPITUS | 8680972609160 | 593.80TL |
| DAPLIG | 8699511099171 | 596.98TL |
| FORZIGA | 8699786092730 | 596.98TL |
| Di�er E�de�er �la�lar |
 |
Diyabet Hastal��� Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r. |
 |
Artrit Artrit, olduk�a yayg�n bir hastal�kt�r ancak iyi anla��lamam��t�r. Asl�nda �artrit� tek bir hastal���n ad� de�ildir; eklem a�r�s� veya eklem hastal�klar�n� adland�rman�n gayri resmi yoludur. |
 |
Kalp Krizi Kalbe giden kan ak��� durdu�unda kalp krizi meydana gelir. |
�LA� GENEL B�LG�LER�
Saba �la� Sanayi ve Ticaret A.�.
| Sat�� Fiyat� | 596.98 TL [ 17 Dec 2024 ] |
| �nceki Sat�� Fiyat� | 596.98 TL [ 2 Dec 2024 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699511099171 |
| Etkin Madde | Dapagliflozin |
| ATC Kodu | A10BK01 |
| Birim Miktar | 10 |
| Birim Cinsi | MG |
| Ambalaj Miktar� | 28 |
| Sindirim Sistemi ve Metabolizma > Oral Antidiyabetik �la�lar |
| Yerli ve Be�eri bir ila�d�r. |