DASIKAM 100 mg film kapl� tablet (30 tablet) K�sa �r�n Bilgisi
{ Dasatinib }
1. BE�ER� TIBB� �R�N�N ADI
DASIKAM 100 mg film kapl� tablet
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Her bir film kapl� tablet 100 mg dasatinibe e�de�er 103,693 mg dasatinib monohidrat i�erir.
Yard�mc� maddeler
Laktoz monohidrat (inek s�t� kaynakl�) 131,3 mg Yard�mc� maddeler i�in B�l�m 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Film kapl� tablet.
Beyaz ila beyaz�ms�, oval, k��eleri e�imli ve bir taraf� “100” bask�l� film kapl� tablettir.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
DASIKAM , a�a��daki ko�ullara sahip yeti�kin hastalar�n tedavisinde endikedir:
Yeni tan� konmu� Philadelphia kromozumu pozitif kronik evre kronik miyeloid l�semi (KML),
4.2. Pozoloji ve uygulama �ekli
L�semi tan� ve tedavisinde uzmanla�m�� hekim taraf�ndan tedavi ba�lat�lmal�d�r.
Pozoloji:
Yeti�kin hastalar
DASIKAM'�n kronik faz KML'de �nerilen ba�lang�� dozaj� sabah veya ak�am olmak �zere g�nde bir defa oral yoldan uygulanan 100 mg'd�r. �nerilen dozaja ula�mak i�in DASIKAM
20 mg, 50 mg, 70 mg ve 100 mg'l�k film kapl� tabletler halinde sat��a sunulmu�tur (Bkz. B�l�m 4.4, 4.8 ve 5.1). Kronik faz KML hastalar�nda bir Faz III doz optimizasyon �al��mas�nda plevral ef�zyon, konjestif kalp yetmezli�i/kardiyak fonksiyon bozuklu�u ve miyelosupresyon insidans� g�nde bir kere 100 mg DASIKAM ile tedavi edilen hastalarda daha d���k bulundu�u i�in bu hasta grubunda ba�lang�� dozu g�nde 1 kere 100 mg'd�r.
Tabletler d�zenli olarak sabah ya da ak�amlar� al�nmal�d�r.
DASIKAM'�n akselere, myeloid ya da lenfoid blastik faz (ileri faz) KML ya da Ph+ ALL'de ba�lang�� dozaj� sabah bir tablet ve ak�am bir tablet olmak �zere oral yoldan uygulanan g�nde iki defa 70 mg'd�r. (Bkz. B�l�m 4.8 ve 5.1).
Hastan�n yan�t�na ve tolerans�na g�re doz artt�r�labilir ya da azalt�labilir.
Uygulama s�kl��� ve s�resi:
Ph+ kronik faz KML, h�zlanm��, miyeloid veya lenfoid blastik evredeki (ileri faz) KML veya Ph+ ALL'li yeti�kin hastalarda ve Ph+ kronik faz KML'li pediyatrik hastalarda yap�lan klinik �al��malarda DASIKAM tedavisi hastal���n progresyonuna veya hasta tolere edemeyene kadar devam etmi�tir. Sitogenetik veya molek�ler yan�t [tam sitogenetik yan�t (CCyR), maj�r molek�ler yan�t (MMR) ve MR4.5 gibi] al�nd�ktan sonra tedaviyi kesmenin uzun vadede hastal���n sonucu �zerindeki etkisi ara�t�r�lmam��t�r.
Klinik �al��malarda, Ph+ ALL'li pediyatrik hastalarda DASIKAM tedavisi s�rekli olarak uygulanm�� ve maksimum iki y�l s�reyle as�l ard���k kemoterapi bloklar�na eklenmi�tir. Daha sonra k�k h�cre transplantasyonu yap�lan hastalarda, DASIKAM transplantasyondan sonra ilave bir y�l s�reyle uygulanabilir.
�nerilen dozu elde etmek amac�yla, DASIKAM 20 mg, 50 mg, 70 mg ve 100 mg film kapl� tabletler halinde bulunmaktad�r. Hastan�n yan�t� ve tolerabilitesine g�re dozun azalt�lmas� veya artt�r�lmas� �nerilir.
Uygulama �ekli:
Oral yoldan uygulan�r. Derinin ilaca maruz kalma riskini azaltmak i�in tabletler ezilmemeli ya da kesilmemeli, b�t�n olarak yutulmal�d�r. DASIKAM yemekle birlikte ya da a� karn�na al�nabilir. Kronik faz KML'de g�nl�k doz d�zenli olarak sabah ya da ak�am al�nmal�d�r. �leri faz KML'de ise g�nl�k doz sabah ve ak�am olmak �zere g�nde iki kerede al�nmal�d�r. Tabletleri b�t�n olarak alan hastalara k�yasla eritilmi� tablet alan hastalarda maruziyet daha d���k oldu�undan film kapl� tabletler eritilmemelidir.
DASIKAM a� veya tok karn�na al�nabilir ve d�zenli olarak sabah veya ak�am al�nmal�d�r. DASIKAM greyfurt veya greyfurt suyu ile birlikte al�nmamal�d�r (Bkz. B�l�m 4.5).
Doz art�r�m�:
Yeti�kin kronik faz KML ve Ph+ ALL hastalar�nda yap�lan klinik �al��malarda �nerilen ba�lang�� dozaj�nda hematolojik veya sitogenetik yan�t vermeyen hastalarda dozun g�nde bir kere 140 mg'a (kronik faz KML) veya g�nde bir kere 180 mg'a (ileri faz KML veya Ph+ ALL) art�r�m�na izin verilmi�tir.
G�ncel tedavi k�lavuzlar�na g�re �nerilen d�nemde hematolojik, sitogenetik ve molek�ler yan�t
vermeyen ve tedaviyi tolere eden Ph+ kronik faz KML'li pediyatrik hastalarda a�a��da Tablo1'de belirtilen doz art��lar� tavsiye edilmektedir.
Tablo 1: Ph+ Kronik faz KML'li pediyatrik hastalarda doz art���
| Doz (g�nl�k maksimum doz) | |
Tablet | Ba�lang�� dozu | Y�kseltme |
40 mg | 50 mg | |
60 mg | 70 mg | |
70 mg | 90 mg | |
100 mg | 120 mg | |
Ph+ ALL'li pediyatrik hastalarda DASIKAM kemoterapi ile birlikte uyguland���ndan bu hastalarda dozun art�r�lmas� �nerilmez.
�stenmeyen etkilerde dozun ayarlanmas�:
Miyelosupresyon:
Klinik �al��malarda miyelosupresyon doza ara verilerek, doz azalt�larak ya da �al��ma tedavisi kesilerek tedavi edilmi�tir. Gereken durumlarda trombosit transf�zyonu ve k�rm�z� h�cre transf�zyonu yap�lm��t�r. Diren�li miyelosupresyonu olan hastalarda hematopoetik b�y�me fakt�r� kullan�lm��t�r.
Yeti�kinlerde doz de�i�iklik k�lavuzlar� Tablo 2'de ve Ph+ kronik faz KML'li pediyatrik hastalarda Tablo3'te �zetlenmektedir. Kemoterapi ile kombinasyon tedavisi uygulanan Ph+ ALL'li pediyatrik hastalara y�nelik k�lavuzlar tablolar�n arkas�ndan ayr� bir paragrafta a��klanmaktad�r.
Tablo 2 Yeti�kinlerde n�tropenide ve trombositopenide doz ayarlamalar� | ||
Kronik Faz KML (ba�lang�� dozu: g�nde bir kere 100 mg) |
MNS < 0,5 x 10/L ve/veya Trombositler < 50 x 10/L |
diren�li ya da intoleran hastalar i�in). |
MNS ≥ 1 x 10/L ve trombositler ≥ 50 x 10/L olana kadar tedavi kesilir
4.3. Kontrendikasyonlar
Dasatinib monohidrata veya di�er bile�enlerine kar�� a��r� duyarl�l��� olanlarda kontrendikedir. (Bkz. B�l�m 6.1).
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Klinik �nemi olan etkile�meler:
Dasatinib sitokrom P450 (CYP)3A4'�n bir substrat� ve inhibit�r�d�r. Dolay�s�yla, primer olarak CYP3A4 taraf�ndan metabolize edilen veya onun aktivitesini d�zenleyen t�bbi �r�nlerin e�zamanl� uygulanmas�nda etkile�me potansiyeli vard�r (Bkz. B�l�m 4.5).
Dasatinibin CYP3A4'� kuvvetle inhibe eden t�bbi �r�nler veya maddeler (�rn., ketokonazol, itrakonazol, eritromisin, klaritromisin, ritonavir, telitromisin, greyfurt suyu) ile e�zamanl� kullan�m� Ddasatinib etkinli�ini artt�rabilir. Bu y�zden, DASIKAM alan hastalarda g��l� bir CYP3A4 inhibit�r�n�n e�zamanl� uygulamas� �nerilmez (Bkz. B�l�m 4.5).
Dasatinibin CYP3A4'� ind�kleyen t�bbi �r�nler (�rn., deksametazon, fenitoin, karbamazepin, rifampisin, fenobarbital ya da St. John's Wort diye de bilinen Hypericum perforatum i�eren bitkisel preparatlar) ile e�zamanl� kullan�m� dasatinib al�m�n� kayda de�er oranda azalt�p terap�tik ba�ar�s�zl�k riskini potansiyel olarak artt�rabilir. Bundan dolay�, DASIKAM alan hastalara CYP3A4 ind�ksiyon potansiyeli daha az olan alternatif t�bbi �r�nlerin e�zamanl� uygulamas� se�ilmelidir (Bkz. B�l�m 4.5).
Dasatinib ile bir CYP3A4 substrat�n�n e�zamanl� kullan�m� CYP3A4 substrat� d�zeyini artt�rabilir. Dolay�s�yla, DASIKAM'�n �rne�in astemizol, terfenadin, sisaprid, pimozid, kinidin, bepridil ya da ergot alkaloidleri (ergotamin, dihidroergotamin) gibi terap�tik indeksi dar olan CYP3A4 substratlar� ile e�zamanl� uygulamas� dikkat gerektirir (Bkz. B�l�m 4.5).
Dasatinib ile bir histamin-2(H) blok�r�n (�rn., famotidin), bir proton pompas� inhibit�r�n�n (�rn., omeprazol) ya da al�minyum hidroksitin ve magnezyum hidroksitin e�zamanl� kullan�m� dasatinib d�zeyini azaltabilir. Dolay�s�yla Hblok�rleri ile proton pompas� inhibit�rleri �nerilmez. Al�minyum hidroksit/magnezyum hidroksit �r�nleri ise dasatinibden 2 saat �nce veya 2 saat sonra uygulanmal�d�r (Bkz. B�l�m 4.5).
�zel pop�lasyonlar
Tek doz farmakokinetik �al��ma bulgular�na dayanarak, hafif, orta veya �iddetli karaci�er yetmezli�i olan hastalar �nerilen ba�lang�� dozunu alabilir (Bkz. B�l�m 5.2). Bu klinik �al��man�n s�n�rlamalar�ndan dolay�, karaci�er yetmezli�i olan hastalara dasatinib uygulan�rken dikkatli olunmas� �nerilir.
�nemli istenmeyen ila� reaksiyonlar�
Myelosupresyon: Dasatinib tedavisi anemi, n�tropeni ve trombositopeni ile ili�kilidir. Bu belirtiler, ileri faz KML veya Ph+ ALL hastalar�nda kronik faz KML hastalar�nda oldu�undan daha erken ve daha s�k g�r�l�r. �lk iki ay her hafta tam kan say�m� yap�lmal�, daha sonra ayl�k
olarak veya klinik olarak endike olmas� halinde daha s�k aral�klarla devam edilmelidir. Kronik faz KML hastalar�nda, 12 hafta boyunca her 2 haftada bir ve bundan sonra her 3 ayda bir veya klinik olarak endike oldu�u hallerde tam kan say�m� yap�lmal�d�r.
Myelosupresyon genellikle geri d�n���ml� olmu� ve dasatinib ge�ici olarak kesilerek ya da dozu azalt�larak tedavi edilmi�tir. Kemoterapi ile kombinasyon halinde dasatinib alan Ph+ ALL'li pediyatrik hastalarda, her bir kemoterapi blo�unun ba�lang�c�ndan �nce ve klinik olarak endike olan �ekilde tam kan say�m� ger�ekle�tirilmelidir. Kemoterapi bloklar�n�n konsolidasyonu s�ras�nda, iyile�me g�zlenene kadar 2 g�nde bir tam kan say�m� yap�lmal�d�r (Bkz. B�l�m 4.2 ve 4.8).
Kanama: Kronik faz KML hastalar�ndaki (n=548) dasatinib alan 5 hasta (%1) grade 3 veya 4 kanama geli�tirmi�tir. Dasatinibin �nerilen dozunu almakta olan ileri faz KML hastalar� (n=304) ile yap�lan klinik �al��malarda hastalar�n %1'inde ciddi merkezi sinir sistemi (MSS) kanamas� g�r�lm��t�r. Bir vaka fatal olmu� ve CTC (Common Toxicity Criteria) grade 4 trombositopeni ile ili�kilendirilmi�tir. �leri faz KML hastalar�n�n %6's�nda grade 3 veya 4 gastrointestinal kanama g�r�lm�� ve genellikle ilac�n kesilmesi ve transf�zyon gerekmi�tir. �leri faz KML hastalar�n�n %2'sinde ba�ka grade 3 veya 4 kanamalar ortaya ��km��t�r. Bu hastalarda kanamaya ba�l� olaylar�n �o�u tipik olarak grade 3 veya 4 trombositopeni ile ili�kilidir (Bkz. B�l�m 4.8). Buna ek olarak, in vitro ve in vivo platelet tayinleri Ddasatinib tedavisinin platelet aktivasyonunu reversibl olarak etkiledi�ini �nermektedir.
Hastalar�n trombosit fonksiyonlar�n� inhibe eden t�bbi �r�nler ya da antikoag�lanlar almas� gereken durumlarda dikkatli olmak gerekir.
S�v� retansiyonu: Dasatinib s�v� retansiyonu ile ili�kilidir. Yeni tan� alm�� kronik faz KML hastalar�nda yap�lan Faz III klinik �al��mada, minimum 60 ayl�k bir takip sonucunda dasatinib tedavi grubundaki 13 hastada (%5) ve imatinib tedavi grubundaki 2 hastada (%1) grade 3 veya 4 s�v� retansiyonu bildirilmi�tir (Bkz. B�l�m 4.8). �nerilen dozda dasatinib almakta olan kronik faz KML hastalar�ndan (n=548) 32 hastada (%6) ciddi s�v� retansiyonu g�r�lm��t�r. �nerilen dozda dasatinib almakta olan ileri faz KML hastalar�nda (n=304) yap�lan klinik �al��malarda s�ras� ile hastalar�n %7'sinde ve %1'inde bildirilen grade 3 veya 4 plevral ve perikardiyal ef�zyon dahil, hastalar�n %8'inde grade 3 veya 4 s�v� retansiyonu bildirilmi�tir. Bu hastalarda grade 3 veya 4 pulmoner �dem ve pulmoner hipertansiyon her biri %1 oran�nda bildirilmi�tir.
Dispne ya da kuru �ks�r�k gibi plevral ef�zyonu d���nd�ren semptomlar geli�tiren hastalar g���s r�ntgeni ile de�erlendirilmelidir. Grade 3 veya 4 plevral ef�zyon torasentez ve oksijen tedavisi gerektirebilir. S�v� retansiyonu olaylar� tipik olarak di�retik ve k�sa steroid k�rleri dahil destekleyici tedavi �nlemleri ile iyile�tirilmi�tir. 65 ya� ve �st� hastalarda plevral ef�zyon, dispne, �ks�r�k, perikardiyal ef�zyon ve konjestif kalp yetmezli�i g�r�lme olas�l��� gen� hastalardan daha y�ksek oldu�undan, bu hastalar yak�ndan izlenmelidir. Plevral ef�zyon ile ba�vuran hastalarda da �ilotoraks vakalar� bildirilmi�tir. (Bkz. b�l�m 4.8)
Pulmoner arter hipertansiyonu (PAH): Dasatinib tedavisi ile ba�lant�l� olarak sa� kalp kateterizasyonu ile konfirme edilen pre-kapiler pulmoner arter hipertansiyonu (PAH) bildirilmi�tir (Bkz. B�l�m 4.8). Bu vakalarda PAH dasatinib tedavisine ba�land�ktan sonra bildirilmi�tir ve bir y�ldan daha uzun s�ren tedavileri de i�ermektedir.
Dasatinib tedavisine ba�lamadan �nce hastalar altta yatan kardiyopulmoner hastal�k bulgu ve semptomlar� a��s�ndan de�erlendirilmelidir. Kardiyak hastal�k semptomlar� ile gelen her hastaya tedavi ba�lang�c�nda ekokardiyografi yap�lmal� ve kardiyak ya da pulmoner hastal�k risk fakt�rleri bulunan hastalarda yap�lmas� d���n�lmelidir. Dasatinibe ba�land�ktan sonra dispne ve bitkinlik geli�tiren hastalar plevral ef�zyon, pulmoner �dem, anemi, akci�er infiltrasyonu dahil yayg�n etiyolojiler a��s�ndan de�erlendirilmelidir. Hemotoloji – d��� advers reaksiyonlar�n tedavisi �nerilerine g�re (Bkz. B�l�m 4.2) bu de�erlendirme yap�l�rken dasatinib dozu azalt�lmal� ya da tedaviye ara verilmelidir. Doz azalt�larak veya ara verilerek bir iyile�me sa�lanam�yorsa ya da hi�bir a��klama getirilemiyorsa, PAH te�hisi d���n�lmelidir. Tan� koymak i�in standart uygulama rehberine g�re hareket etmelidir. E�er PAH konfirme edilirse, dasatinib tamamen kesilmelidir. Standart uygulama rehberine g�re takip edilmelidir. Dasatinib tedavisi kesildikten sonra dasatinib ile PAH geli�tiren hastalar�n hemodinamik ve klinik parametrelerinde d�zelme g�zlenmi�tir.
QT Uzamas�: �n vitro veriler dasatinibin kardiyak ventrik�ler repolarizasyonu (QT aral���) uzatma potansiyeli oldu�unu g�stermektedir (Bkz. B�l�m 5.3). Yeni tan� alm�� kronik faz KML hastalar�nda yap�lan Faz III �al��mada, minimum 60 ayl�k takip sonras�nda, dasatinib ile tedavi edilen 258 hastadan ve imatinib ile tedavi edilen 258 hastadan olu�an her iki tedavi grubundaki 1'er hastada (< %1) QTc uzamas� advers reaksiyon olarak bildirilmi�tir. Ba�lang�ca g�re QTcF'teki medyan de�i�iklikler dasatinib ile tedavi edilen hastalarda 3 milisaniye, buna kar��n imatinib ile tedavi edilen hastalarda 8,2 milisaniye idi. Her iki tedavi grubundaki 1'er hastada (< %1) >500 milisaniye QTcF bildirilmi�tir. Dasatinib ile tedavi edilen 865 l�semi hastas�nda yap�lan Faz II klinik �al��malarda QTc aral���nda ba�lang��tan olan ortalama de�i�iklik, Fridericia metodu (QTcF) ile, 4 – 6 milisaniyeydi; ba�lang��tan itibaren b�t�n ortalama de�i�ikliklerin �st %95 g�ven aral�klar� < 7 milisaniye olmu�tur (Bkz. B�l�m 4.8).
�nceki imatinib tedavisine diren�li veya intoleransl� hastalarda yap�lan klinik �al��malarda dasatinib alan 2.182 hastadan 15'inde (%1) advers olay olarak QTc uzamas� bildirilmi�tir. Yirmi bir hastada (%1) > 500 milisaniye QTcF bildirilmi�tir.
QTc uzamas� olan veya bunu geli�tirebilecek durumdaki hastalarda DASIKAM dikkatli uygulanmal�d�r. Hipokalemi veya hipomagnezemili, konjenital uzun QT sendromlu, anti- aritmik ila�lar alan veya QT uzamas�na yol a�an ba�ka t�bbi �r�nler alan ya da k�m�latif y�ksek doz antrasiklin tedavisi g�ren hastalar buna dahildir. Dasatinib uygulamadan �nce hipokalemi veya hipomagnezemi d�zeltilmelidir.
Kardiyak advers reaksiyonlar: Dasatinib, aralar�nda daha �nce kardiyak hastal�k hikayesi olan hastalar�n da bulundu�u 519 yeni tan� alm�� kronik faz KML hastas� ile yap�lan randomize bir �al��mada incelenmi�tir. Konjestif kalp yetmezli�i/kardiyak fonksiyon bozuklu�u, perikardiyal
ef�zyon, aritmi, �arp�nt�, QT uzamas� ve miyokard infarkt�s� (fatal dahil) gibi kardiyak advers reaksiyonlar Dasatinib tedavisi alan hastalarda rapor edilmi�tir. Kardiyak advers olaylar, kardiyak hastal�klar ilgili hikayesi veya risk faktor� olan hastalarda daha yayg�nd�r. Kardiyak hastal�k risk fakt�r� (�r hipertansiyon, hiperlipidemi, diyabet) veya hikayesi (�r. Ge�mi�te perk�tan koroner giri�im, belgelendirilmi� koroner arter hastal��� olan hastalar g���s a�r�s�, nefes darl��� ve a��r� terleme gibi kardiyak disfonksiyon bulgu ve semptomlar� a��s�ndan dikkatlice izlenmeli ve uygun �ekilde de�erlendilmeli ve tedavi edilmelidir.
![]()
E�er bu klinik belirti ve semptomlar geli�irse hekimlerin dasatinib uygulamas�na ara vermeleri ve alternatif KML'ye �zg� tedavi ihtiyac�n� g�z �n�nde bulundurmalar� �nerilmektedir. D�zelme sonras�nda, dasatinib ile tedaviye devam edilmeden �nce i�levsel bir de�erlendirme yap�lmal�d�r. Hafif/orta �iddetli olaylarda (Grade ≤ 2) dasatinibe ba�lang�� dozunda devam edilebilir ve �iddetli olaylarda (Grade ≥ 3) doz d�zeyi azalt�larak (Bkz. B�l�m 4.2) devam edilebilir. Tedaviye devam eden hastalar periyodik olarak izlenmelidir. Kontrol edilemeyen ya da anlaml� kardiyovask�ler hastal��� olan hastalar klinik �al��malara al�nmam��t�r.
Trombotik mikroanjiyopati (TMA)
BCR-ABL tirozin kinaz inhibit�rleri, dasatinib i�in bireysel olgu raporlar� dahil olmak �zere trombotik mikroanjiyopati (TMA) ile ili�kilendirilmi�tir (Bkz. B�l�m 4.8). Dasatinib alan bir hastada TMA ile ili�kili bir laboratuvar bulgusu veya klinik bulgu geli�irse, dasatinib tedavisi sonland�r�lmal� ve ADAMTS13 aktivitesi ve anti-ADAMTS13-antikor tespiti dahil olmak �zere TMA i�in kapsaml� bir de�erlendirme tamamlanmal�d�r. D���k ADAMTS13 aktivitesi ile ba�lant�l� olarak anti-ADAMTS13-antikoru y�kselirse, Dasatinib tedavisi tekrar ba�lat�lmamal�d�r.
Hepatit B reaktivasyonu
Hepatit B vir�s� (HBV) kronik ta��y�c�s� olan hastalarda, BCR-ABL tirozin kinaz inhibit�rleri ile tedavi sonras�, Hepatit B reaktivasyonu ortaya ��km��t�r. Baz� vakalar, karaci�er nakli veya �l�me sebep olan akut karaci�er yetmezli�i veya fulminan hepatit ile sonu�lanm��t�r. DASIKAM tedavisine ba�lanmadan �nce, hastalar HBV enfeksiyonu a��s�ndan test edilmelidir. Pozitif HBV serolojisine sahip (aktif hastal��� olanlar dahil) ve tedavi s�ras�nda HBV enfeksiyonu i�in pozitif test sonucu veren hastalarda, tedavi ba�lat�lmadan �nce karaci�er hastal��� ve HBV tedavisi konusunda uzman hekimlere dan���lmal�d�r. DASIKAM ile tedaviye ihtiya� duyan HBV ta��y�c�lar�, tedavi boyunca ve tedavi sonland�r�ld�ktan sonra birka� ay boyunca aktif HBV enfeksiyonu bulgu ve belirtileri i�in yak�ndan izlenmelidir (Bkz. B�l�m 4.8).
Pediyatrik hastalarda b�y�me ve geli�im �zerinde etkiler
�matinibe diren�li/tolere edemeyen Ph+ kronik faz KML'li pediyatrik hastalarda ve tedavi almam�� Ph+ kronik faz KML'li pediyatrik hastalarda dasatinib ile yap�lan pediyatrik �al��malarda en az 2 y�ll�k tedaviden sonra, biri y�ksek �iddette olmak �zere 6 hastada (%4,6) tedavi ile ili�kili kemik b�y�mesi ve geli�imle ilgili advers olaylar bildirilmi�tir (Grade 3 B�y�me Gerili�i). Bu 6 vaka epifiz f�zyonunda gecikme, osteopeni, b�y�me gerili�i ve
jinekomasti vakalar�n� i�ermi�tir (Bkz. B�l�m 5.1). Bu bulgular�n KML gibi kronik hastal�k ba�lam�nda yorumlanmas� zordur ve uzun d�nem takibi gerekmektedir.
Yeni tan� konan Ph+ ALL'li pediyatrik hastalarda kemoterapi ile kombinasyon halinde dasatinibin incelendi�i �al��malarda en az 2 y�ll�k tedaviden sonra, 1 hastada (%0,6) tedavi ile ili�kili kemik b�y�mesi ve geli�imle ilgili advers olaylar bildirilmi�tir. Bu olgu bir Grade 1 osteopeniydi.
Klinik �al��malarda dasatinib ile tedavi edilen pediyatrik hastalarda b�y�me gerili�i g�zlenmi�tir (Bkz. B�l�m 4.8). Pediyatrik hastalarda kemik b�y�mesinin ve geli�iminin izlenmesi �nerilir.
Laktoz: Bu t�bbi �r�n�n 100 mg'l�k g�nl�k dozu 131,3 mg ve 140 mg'l�k g�nl�k dozu 183,827 mg laktoz monohidrat i�erir. Nadir kal�t�msal galaktoz intolerans�, Lapp laktaz yetmezli�i ya da glukoz-galaktoz malabsorpsiyon problemi olan hastalar�n bu ilac� kullanmamalar� gerekir.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Dasatinibin plazma konsantrasyonlar�n� artt�rabilen aktif maddeler:
In vitro �al��malar dasatinibin bir CYP3A4 substrat� oldu�unu g�stermektedir. Dasatinib ile CYP3A4'� kuvvetle inhibe eden t�bbî �r�nlerin veya maddelerin (�rn., ketokonazol, itrakonazol, eritromisin, klaritromisin, ritonavir, telitromisin, greyfurt suyu) e�zamanl� kullan�m� dasatinibin kan d�zeyini artt�rabilir. Dolay�s�yla, DASIKAM alan hastalarda kuvvetli bir CYP3A4 inhibit�r�n�n sistemik uygulamas� �nerilmez.
In vitro deneylere g�re, dasatinib; klinik olarak �nemli konsantrasyonlarda, plazma proteinlerine yakla��k %96 oran�nda ba�lan�r. Dasatinibin proteinlere ba�lanan di�er t�bbî �r�nler ile olan etkile�imini de�erlendirmek i�in herhangi bir �al��ma yap�lmam��t�r. Yer de�i�tirme (displacement) potansiyeli ve klinik �nemi bilinmemektedir.
Dasatinibin plazma konsantrasyonlar�n� d���rebilen aktif maddeler:
G��l� bir CYP3A4 ind�kleyicisi olan rifampisin 8 ak�am �st�ste 600 mg olarak uyguland�ktan sonra dasatinib uyguland��� zaman, dasatinibin EAA'� %82 azalm��t�r. Keza CYP3A4 aktivitesini ind�kleyen ba�ka t�bbi �r�nler de (�rn., deksametazon, fenitoin, karbamazepin, fenobarbital veya St. John's Wort olarak da bilinen Hypericum perforatum i�eren bitkisel preparatlar) metabolizmay� h�zland�rarak dasatinibin plazma konsantrasyonlar�n� d���rebilirler. Dolay�s�yla, g��l� CYP3A4 ind�kleyicileri ile DASIKAM'�n e�zamanl� kullan�m� tavsiye edilmez. Rifampisinin ya da ba�ka CYP3A4 ind�kleyicisinin endike oldu�u hastalarda, enzim ind�ksiyonu daha az olan t�bbi �r�nler kullan�lmal�d�r.
Zay�f bir CYP3A4 ind�kleyicisi olan deksametazonun dasatinib ile e� zamanl� kullan�m�na izin verilmektedir; dasatinib EAA's�n�n deksametazonla birlikte kullan�ld���nda yakla��k %25 oran�nda azalmas� beklenmektedir ve bu d�����n klinik olarak anlaml� olmas� olas� de�ildir.
Histamin-2 antagonistleri ve proton pompas� inhibit�rleri:
Gastrik asit sekresyonunun Hantagonistleri ya da proton pompas� inhibit�rleri (�rn., famotidin ve omeprazol) ile uzun s�reli supresyonunun dasatinib al�m�n� azaltma olas�l��� vard�r. Sa�l�kl� g�n�ll�lerde yap�lan bir tek doz �al��mas�nda tek doz dasatinibden 10 saat �nce famotidin uyguland��� zaman dasatinib al�m� %61 azalm��t�r. 14 sa�l�kl� g�n�ll� �zerinde ger�ekle�tirilen bir �al��mada denge durumunda 4 g�nl�k 40 mg omeprazol dozunun ard�ndan tek bir 100 mg'lik dasatinib dozunun uygulanmas� dasatinib EAA's�n� %43, Cde�erini ise %42 azaltm��t�r. Dasatinib tedavisi alan hastalarda Hantagonistleri ya da proton pompas� inhibit�rleri yerine antasit kullan�m� d���n�lmelidir (Bkz. B�l�m 4.4).
Antasitler:
Nonklinik veriler dasatinib solubilitesinin pH'a ba�l� oldu�unu kan�tlamaktad�r. Sa�l�kl� g�n�ll�lerde al�minyum/magnezyum hidroksidin dasatinib ile e�zamanl� kullan�m� sonucu tek doz dasatinibin EAA'� %55 ve C'� %58 azalm��t�r. Ancak antasitler tek doz dasatinibden 2 saat �nce uyguland��� zaman dasatinibin konsantrasyonunda ya da al�m�nda �nemli bir de�i�iklik g�zlenmemi�tir. Bu durumda, antiasitler DASIKAM'dan en erken 2 saat �nce veya 2 saat sonra uygulanabilir (Bkz. B�l�m 4.4).
![]()
DASIKAM'�n plazma konsantrasyonlar�n� de�i�tirebilece�i aktif maddeler:
Dasatinibin ve bir CYP3A4 substrat�n�n e� zamanl� kullan�m� CYP3A4 substrat� kan d�zeyini artt�rabilir. Sa�l�kl� g�n�ll�lerde yap�lan bir �al��mada 100 mg'l�k tek bir dasatinib dozu bir CYP3A4 substrat� oldu�u bilinen simvastatinin EAA ve Cal�m�n� s�ras�yla %20 ve %37 artt�rm��t�r. Bu etkinin multipl dasatinib dozlar�ndan sonra daha fazla oldu�u g�r�lm��t�r. Dolay�s�yla, terap�tik indekslerinin dar oldu�u bilinen CYP3A4 substratlar� (�rn., astemizol, terfenadin, sisaprid, pimozid, kinidin, bepridil veya ergot alkaloidleri (ergotamin, dihidroergotamin) DASIKAM alan hastalarda dikkatli uygulanmal�d�r (Bkz. B�l�m 4.4).
In vitro veriler �rne�in glitazonlar gibi CYP2C8 substratlar� ile potansiyel etkile�me riski oldu�unu g�stermektedir.
�zel pop�lasyonlara ili�kin ek bilgiler Pediyatrik pop�lasyon
Etkile�im �al��malar� yaln�zca yeti�kinlerle ger�ekle�tirilmi�tir.
4.6. Gebelik ve laktasyon
Gebelik kategorisi: D
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
�ocuk do�urma potansiyeli olan cinsel olarak aktif erkek ya da kad�n hastalar DASIKAM ile tedavi g�r�rken yeterli kontrasepsiyon kullanmal�d�r.
Gebelik d�nemi
�nsan deneyimlerine dayanarak, dasatinibin hamilelik esnas�nda kullan�ld���nda n�ral t�p defektleri ve fet�s �zerinde zararl� farmakolojik etkileride dahil olmak �zere konjenital malformasyonlara sebep olabilece�i beklenmektedir. Hayvanlarda yap�lan �al��malar �reme toksisitesi g�stermi�tir (Bkz. B�l�m 5.3). Kad�n�n klinik durumu dasatinib ile tedavisini gerektirmedik�e DASIKAM, gebelik d�neminde kullan�lmamal�d�r. E�er DASIKAM gebelikte kullan�lacak ise fet�s�n kar�� kar��ya bulundu�u potansiyel risk hastaya bildirilmelidir.
Dasatinib hamile bir kad�na uyguland���nda fet�se zarar verebilir. Hamilelikleri s�ras�nda Ddasatinib alm�� olan kad�nlarda pazarlama sonras� spontan d���k ve yan� s�ra fet�s ve bebekte anomali bildirimleri yap�lm��t�r.
Laktasyon d�nemi
Dasatinib monohidrat�n insan ya da hayvan s�t� ile at�ld���na ili�kin yetersiz/s�n�rl� bilgi mevcuttur. Bu nedenle emzirilen �ocuk a��s�ndan bir risk oldu�u g�z ard� edilemez.
DASIKAM ile tedavi s�ras�nda emzirme durdurulmal�d�r.
�reme yetene�i/ Fertilite
Hayvanlarla yap�lan �al��malarda, erkek ve di�i s��anlar�n fertilitesi dasatinib tedavisinden etkilenmemi�tir (Bkz. B�l�m 5.3). Doktorlar ve di�er sa�l�k uzmanlar� uygun ya�taki erkek hastalara spermlerin saklanmas� hakk�nda tavsiyeyi de i�eren, DASIKAM'�n fertilite �zerindeki olas� etkileri hakk�nda bilgi vermelidir).
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
DASIKAM'�n ara� ve makine kullanma becerisi �zerinde �ok d���k etkisi vard�r. Dasatinib sersemlik ya da g�rme bulan�kl���na sebep olabilece�inden, hastalar ara� ve makine kullan�rken dikkatli olmalar� konusunda uyar�lmal�d�r.
4.8. �stenmeyen etkiler
G�venlilik profilinin �zeti
A�a��da a��klanan veriler klinik �al��malarda, 324 yeni tan� alm�� kronik faz KML ve 2.388 imatinibe diren�li veya tolere edemeyen kronik veya ileri faz KML veya Ph+ ALL hastas�n� ve
188 pediyatrik hastay� i�eren hastalar�n (N=2.900) tek ajanl� tedavi olarak dasatinib maruziyetini yans�tmaktad�r.
Kronik faz KML, ileri faz KML veya Ph+ ALL hastalar�n� i�eren 2.712 hastada medyan tedavi s�resi 19,2 ay (0- 93,2 ay aral���nda) olmu�tur. Yeni tan� alm�� kronik faz KML hastalar�nda yap�lan randomize �al��mada, medyan tedavi s�resi yakla��k 60 ay olmu�tur. 1.618 yeti�kin kronik faz KML hastas�n�n medyan tedavi s�resi 29 ay (0-92,9 ay aral���nda) olmu�tur. 1.094 yeti�kin ileri faz KML veya Ph+ ALL hastas�nda, hastalar�n medyan tedavi s�resi 6,2 ay (0- 93,2 ay aral���nda) idi. Pediyatrik �al��malardaki 188 hastada tedavi s�resi 26,3 ay olmu�tur (0
ila 99,6 ay aral���nda). Dasatinib ile tedavi edilen 130 kronik faz pediyatrik KML hastas�n� i�eren alt grupta medyan tedavi s�resi 42,3 ay (0,1-99,6 ay aral���nda) olmu�tur.
Dasatinib ile tedavi edilen hastalar�n �o�unlu�u bazen advers reaksiyon ya�am��t�r. Dasatinib ile tedavi edilen 2.712 hastadan olu�an genel pop�lasyonda, 520 (%19) hasta advers reaksiyon ya�am�� ve bunun sonucunda tedavileri kesilmi�tir.
Pediyatrik Ph+ kronik faz KML pop�lasyonunda dasatinibin genel g�venlilik profili, form�lasyondan ba��ms�z �ekilde yeti�kin pop�lasyonda g�zlenene benzer olmu�tur; sadece pediyatrik pop�lasyonda perikardiyal ef�zyon, plevral ef�zyon, pulmoner �dem veya pulmoner hipertansiyon bildirilmemi�tir. Dasatinib ile tedavi edilen kronik faz KML'li 130 pediyatrik hastan�n 2'sinde (%1,5) tedavinin kesilmesine yol a�an advers reaksiyonlar g�r�lm��t�r.
4.9. Doz a��m� ve tedavisi
Dasatinib doz a��m� deneyimi klinik �al��malardaki izole vakalar ile s�n�rl�d�r. Bir hafta boyunca g�nde 280 mg'l�k bir doz a��m� iki hastada bildirilmi�tir ve her iki hastan�n da trombosit say�lar�nda belirgin bir azalma olmu�tur. Dasatinib grade 3 veya 4 myelosupresyon ile ba�lant�l� bulundu�undan (Bkz. B�l�m 4.4), �nerilen dozajdan fazlas�n� alm�� olan hastalar myelosupresyon a��s�ndan yak�ndan g�zlemlenmeli ve uygun destekleyici tedavi uygulanmal�d�r.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Antineoplastik ajanlar, Protein kinaz inhibit�r� ATC kodu: L01EA02
Farmakodinami
Dasatinib c-KIT, efrin (EPH) resept�r kinazlar ve PDGFβ resept�r� dahil bir tak�m ba�ka se�ilmi� onkojen kinazlar ile birlikte BCR-ABL kinaz ile SRC ailesi kinazlar�n�n aktivitesini inhibe eder. Dasatinib potensini 0,6-0,8 nM'de g�steren g��l� bir subnanomolar BCR-ABL kinaz inhibit�r�d�r. BCR-ABL enziminin hem inaktif hem de aktif konformasyonuna ba�lan�r.
Etki mekanizmas�
�matinibe duyarl� ve diren�li hastal�k de�i�kenleri olan l�semi h�cresi serilerinde dasatinib in vitro olarak aktiftir. Bu klinik olmayan �al��malar dasatinibin a��r� BCR-ABL ekspresyonundan, BCR-ABL kinaz par�a mutasyonlar�ndan, SRC ailesi kinazlar� (LYN, HCK) i�eren alternatif sinyal yolaklar�n�n aktivasyonundan, ve �oklu ila� diren� (MDR) geninin a��r� ekspresyonundan kaynaklanan imatinib direncini yenebilece�ini g�stermektedir. Bundan ba�ka, dasatinib SRC ailesi kinazlar�n� subnanomolar konsantrasyonda inhibe eder.
In vivo, fare veya s��an KML modellerinin kullan�ld��� ayr� deneylerde dasatinib kronik KML'nin blastik faza progresyonunu engellemi� ve merkezi sinir sistemi dahil farkl� yerlerde b�y�yen, hastalardan elde edilmi� KML h�cresi serilerini ta��yan farelerde sa�kal�m� uzatm��t�r.
Klinik etkililik ve g�venlilik
Faz I �al��mada, tedavi edilen ve 27 ay takip edilen ilk 84 hastada KML'nin t�m fazlar�nda ve Ph+ ALL'de hematolojik ve sitogenetik yan�tlar g�zlenmi�tir. Yan�tlar KML ve Ph+ ALL'nin t�m fazlar�nda s�rekli olmu�tur.
�matinibe diren�li olan veya tolere edemeyen kronik, h�zlanm�� veya miyeloid blastik evredeki KML'li hastalarda dasatinibin g�venlilik ve etkilili�ini de�erlendirmek �zere d�rt tek kollu, kontrols�z, a��k Faz II klinik �al��ma ger�ekle�tirilmi�tir. Ba�lang��ta 400 veya 600 mg imatinib tedavisi ba�ar�s�z olan kronik fazdaki hastalarda bir randomize, kar��la�t�rmal� olmayan �al��ma y�r�t�lm��t�r. Ba�lang�� dozu g�nde iki kez 70 mg dasatinib idi. Etkinli�in iyile�tirilmesi veya toksisitelerin y�netimi i�in doz de�i�ikliklerine izin verilmi�tir (Bkz. B�l�m 4.2).
G�nde iki kez uygulanan dasatinibe k�yasla g�nde bir kez uygulanan dasatinibin etkilili�ini de�erlendirmek �zere iki randomize, a��k etiketli Faz III �al��ma y�r�t�lm��t�r. Buna ek olarak, yeni kronik faz KML tan�s� konmu� yeti�kin hastalarda bir a��k etiketli, randomize, kar��la�t�rmal� Faz III �al��ma yap�lm��t�r.
Dasatinibin etkilili�i, hematolojik ve sitogenetik yan�t oranlar�na dayal�d�r.
Yan�t s�reklili�i ve tahmini sa�kal�m oranlar�, dasatinibin klinik yarar� a��s�ndan ilave kan�t sa�lamaktad�r.
Klinik �al��malarda toplam 2.712 hasta de�erlendirilmi� olup, bunlar�n %23'� ≥ 65 ya� ve %5'i
≥ 75 ya��ndayd�.
Kronik faz KML – Yeni tan� konmu�
Yeni kronik faz KML tan�s� konmu� yeti�kin hastalarda bir uluslararas�, a��k etiketli, �ok merkezli, randomize, kar��la�t�rmal� Faz III �al��ma yap�lm��t�r. Hastalar g�nde bir kez dasatinib 100 mg veya g�nde bir kez imatinib 400 mg almak �zere randomize edilmi�tir.
Primer sonlanma noktas� 12 ay i�indeki do�rulanm�� tam sitogenetik yan�t oran� (cCCyR) idi. Sekonder sonlanma noktalar� cCCyR'de ge�en s�re (yan�t s�reklili�inin �l��m�), cCCyR'ye kadar ge�en s�re, maj�r molek�ler yan�t (MMR) oran�, MMR'ye kadar ge�en s�re, progresyonsuz sa�kal�m (PFS) ve genel sa�kal�md� (OS). Di�er ili�kili etkililik sonu�lar� CCyR ve tam molek�ler yan�t (CMR) oranlar�n� i�ermi�tir. �al��ma devam etmektedir.
Toplam 519 hasta bir tedavi grubuna randomize edilmi�tir: 259'u dasatinib ve 260'� imatinib grubuna. Ba�lang�� �zellikleri ya� (medyan ya� dasatinib grubunda 46 ve imatinib grubunda 49 olup hastalar�n s�ras�yla %10 ve %11'i 65 ya� veya �zerindeydi), cinsiyet (s�ras�yla %44 ve
%37'si kad�n) ve �rk (s�ras�yla Beyaz %51 ve %55; Asyal� %42 ve %37) a��s�ndan iki tedavi grubu aras�nda iyi �ekilde dengelenmi�tir. Ba�lang��ta, Hasford Skorlar�n�n da��l�m� dasatinib ve imatinib tedavi gruplar�nda benzerdi (s�ras�yla d���k risk: %33 ve %34; orta risk %48 ve
%47; y�ksek risk: %19 ve %19).
En az 12 ayl�k takiple, dasatinib grubuna randomize olan hastalar�n %85'i ve imatinib grubuna randomize olan hastalar�n %81'i halen birinci basamak tedavi almaktayd�. Hastal�k progresyonundan dolay� 12 ay i�inde tedaviyi kesme oran� dasatinib grubunda %3 ve imatinib grubunda %5 idi.
En az 60 ayl�k takiple, dasatinib grubuna randomize olan hastalar�n %60'� ve imatinib grubuna randomize olan hastalar�n %63'� halen birinci basamak tedavi almaktayd�. Hastal�k
progresyonundan dolay� 60 ay i�inde tedaviyi kesme oran� dasatinib grubunda %11 ve imatinib grubunda %14 idi.
Etkililik sonu�lar� Tablo 8'de sunulmu�tur. Tedavinin ilk 12 ay�nda imatinib grubuna k�yasla dasatinib grubundaki hastalar�n istatistiksel olarak anlaml� �ekilde daha y�ksek bir b�l�m�nde cCCyR elde edilmi�tir. Dasatinibin etkilili�i, ya�, cinsiyet ve ba�lang�� Hasford skorlar� dahil farkl� alt gruplarda tutarl� �ekilde g�sterilmi�tir.
Tablo 8: Yeni Tan� Konmu� Kronik Faz KML Hastalar�nda Yap�lan bir Faz 3 �al��madan Al�nan Etkililik Sonu�lar�
| Dasatinib n=259 | �matinib n=260 | p-de�eri |
Yan�t oran� (%95 GA) | |||
Sitogenetik Yan�t |
|
|
|
12 Ayda |
|
|
|
cCCyR | %76,8 (71,2-81,8) | %66,2 (60,1-71,9) | p < 0,007* |
CCyRP | %85,3 (80,4-89,4) | %73,5 (67,7-78,7) | - |
24 Ayda |
|
|
|
cCCyR | %80,3 | %74,2 | - |
CCyR | %87,3 | %82,3 | - |
36 Ayda |
|
|
|
cCCyR | %82,6 | %77,3 | - |
CCyRP | %88 | %83,5 | - |
48 Ayda |
|
|
|
cCCyR | %82,6 | %78,5 | - |
CCyR | %87,6 | %83,8 | - |
60 Ayda |
|
|
|
cCCyR | %83 | %78,5 | - |
CCyR | %88 | %83,8 | - |
Maj�r Molek�ler Yan�t | |||
12 ayl�k | %52,1(45,9-58,3) | %33,8 (28,1-39,9) | p<0,00003* |
24 ayl�k | %64,5(58,3-70,3) | %50 (43,8-56,2) | - |
36 ayl�k | %69,1(63,1-74,7) | %56,2 (49,9-62,3) | - |
48 ayl�k | %75,7 (70–80,8) | %62,7 (56,5-68,6) | - |
60 ayl�k | %76,4 (70,8-81,5) | %64,2 (58,1-70,1) | p=0,0021 |
Risk Oran� (%99,99GA)(12 ayl�k) | |||
cCCyR'a kadar ge�en s�re | 1,55 (1-2,3) | p<0,0001* | |
MMR'a kadar ge�en s�re | 2,01 (1,2-3,4) | p<0,0001* | |
cCCyR s�resi | 0,7 (0,4-1,4) | p<0,035* | |
Risk Oran� (%95 GA)(24 ayl�k) | |||
cCCyR'a kadar ge�en s�re | 1,49 (1,22-1,82) | - |
MMR'a kadar ge�en s�re | 1,69 (1,34-2,12) | - |
cCCyR s�resi | 0,77 (0,55-1,1) | - |
Risk Oran� (%95 GA)(36 ayl�k) | ||
cCCyR'a kadar ge�en s�re | 1,48 (1,22-1,8) | - |
MMR'a kadar ge�en s�re | 1,59 (1,28-1,99) | - |
cCCyR s�resi | 0,77 (0,53-1,11) | - |
Risk Oran� (%95 GA)(48 ayl�k) | ||
cCCyR'a kadar ge�en s�re | 1,45 (1,2-1,77) | - |
MMR'a kadar ge�en s�re | 1,55 (1,26-1,91) | - |
cCCyR s�resi | 0,81 (0,56-1,17) | - |
Risk Oran� (%95 GA)(60 ayl�k) | ||
cCCyR'a kadar ge�en s�re | 1,46 (1,2-1,77) | p=0,0001 |
MMR'a kadar ge�en s�re | 1,54 (1,25-1,89) | p<0,0001 |
cCCyR s�resi | 0,79 (0,55-1,13) | p=0,1983 |
*Hasford Skoru'na g�re ayarlanm�� ve istatistiksel �nemi �nceden belirlenmi� nominal bir �nem d�zeyine g�re g�sterilmi�tir.
GA = g�ven aral���
60 ayl�k takipten sonra, do�rulanm�� CCyR ile cCCyR'ye ula�mak i�in gereken medyan s�re dasatinib grubunda 3,1 ay ve imatinib grubunda 5,8 ay olmu�tur. 60 ayl�k takipten sonra, bir MMR olan hastalarda MMR'ye ula�mak i�in gereken medyan s�re dasatinib grubunda 9,3 ay ve imatinib gubunda 15 ay olmu�tur. Bu sonu�lar 12, 24 ve 36. aylarda g�zlenen sonu�larla uyumludur.
MMR'ye kadar ge�en s�re �ekil 1'de grafik olarak g�sterilmektedir. MMR'ye kadar ge�en s�re dasatinib ile tedavi edilen hastalarda, imatinib ile tedavi edilen hastalara k�yasla tutarl� �ekilde daha k�sa olmu�tur.
�ekil 1. Maj�r molek�ler yan�ta (MMR) kadar ge�en s�renin Kaplan-Meier kestirimi
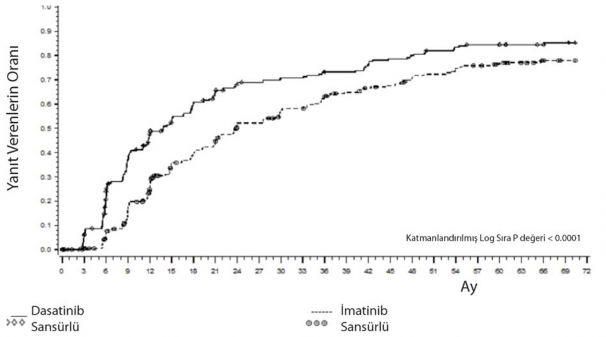
GRUP | # YANIT VERENLER / # RANDOM�ZE ED�LENLER | R�SK ORANI (%95 GA) |
Dasatinib | 198/259 |
|
�matinib | 167/260 |
|
�matinib kar��s�nda dasatinib |
| 1,54 (1,25-1,89) |
Dasatinib ve imatinib tedavi gruplar�nda s�ras�yla 3 ay (%54 ve %30), 6 ay (%70 ve %56), 9 ay
(%75 ve %63), 24 ay (%80 ve %74), 36 ay (%83 ve %77), 48 ay (%83 ve %79) ve 60 ay (%83
ve %79) i�indeki cCCyR oranlar� primer sonlanma noktas� ile uyumluydu. Dasatinib ve imatinib tedavi gruplar�nda s�ras�yla 3 ay (%8 ve %0,4), 6 ay (%27 ve %8), 9 ay (%39 ve %18), 12 ay
(%46 ve %28), 24 ay (%64 ve %46), 36 ay (%67 ve %55), 48 ay (%73 ve %60) ve 60 ay (%76
ve %64) i�indeki MMR oranlar� da primer sonlanma noktas� ile uyumluydu.
Spesifik zaman noktalar�ndaki MMR oranlar� �ekil 2'de grafik olarak g�sterilmektedir. MMR oranlar� dasatinib ile tedavi edilen hastalarda, imatinib ile tedavi edilen hastalara k�yasla tutarl� �ekilde daha y�ksek olmu�tur.
�ekil 2. Zaman i�indeki MMR oranlar� – yeni kronik faz KML tan�s� konmu� hastalarda yap�lan faz 3 �al��maya randomize edilen t�m hastalar
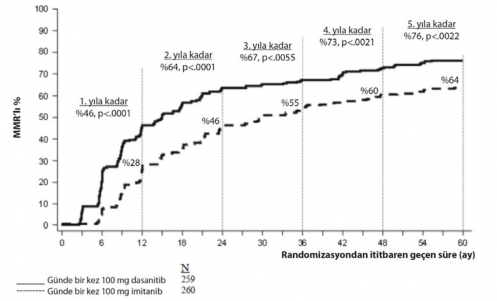
Herhangi bir zamanda BCR-ABL oran� ≤ %0,01 (4-log azalma) olan hastalar�n oran� dasatinib grubunda, imatinib grubuna k�yasla daha y�ksekti (%54,1 kar��s�nda %45). Herhangi bir zamanda BCR-ABL oran� ≤%0,0032 (4,5-log azalma) olan hastalar�n oran� dasatinib grubunda, imatinib grubuna k�yasla daha y�ksekti (%44 kar��s�nda %34).
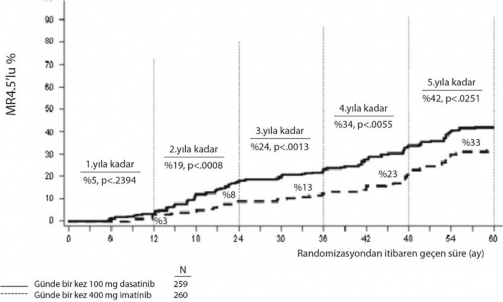
Zaman i�indeki MR 4,5 oranlar� �ekil 3'te grafik olarak g�sterilmektedir. MR 4,5 oranlar� dasatinib ile tedavi edilen hastalarda, imatinib ile tedavi edilen hastalara k�yasla tutarl� �ekilde daha y�ksek olmu�tur.
�ekil 3. Zaman i�indeki MR 4,5 oranlar�–yeni kronik faz KML tan�s� konmu� hastalarda yap�lan faz 3 �al��maya randomize edilen t�m hastalar
Hasford skoru ile belirlenen her bir risk grubunda herhangi bir zamandaki MMR oran� imatinib grubuna k�yasla dasatinib grubunda daha y�ksekti (s�ras�yla d���k risk: %90 ve %69; orta risk:
%71 ve %65; y�ksek risk: %67 ve %54)
Bir ek ara�t�rma analizinde imatinib tedavisi uygulanan hastalarla kar��la�t�r�ld���nda (%64) dasatinible tedavi uygulanan daha fazla say�da hastada (%84) erken molek�ler yan�t (3 ayl�k BCR-ABL seviyelerinin ≤ %10 olmas� �eklinde tan�mlanm��t�r) elde edildi�i g�r�lm��t�r. Tablo 9'da g�r�ld��� gibi, erken molek�ler yan�t elde edilen hastalarda transformasyon riski daha d���k, progresyonsuz sa� kal�m (PFS) oran� ile genel sa� kal�m (OS) oran� daha y�ksekti.
Tablo 9: 3 Ayl�k BCR-ABL d�zeyleri ≤ %10 ve > %10 olan Dasatinib Hastalar�
Dasatinib N = 235 | 3 Ayl�k BCR-ABL Seviyeleri ≤%10 Olan Hastalar | 3 Ayl�k BCR-ABL Seviyeleri ABL > %10 Olan Hastalar |
Hasta Say�s� (%) | 198 (84,3) | 37 (15,7) |
60. Ayda transformasyon, n/N (%) | 6/198 (3) | 5/37 (13,5) |
60. Ayda PFS Oran� (%95 GA) | %92 (89,6, 95,2) | %73,8 (52, 86,8) |
60. Ayda OS Oran� (%95 GA) | %93,8 (89,3, 96,4) | %80,6 (63,5, 90,2) |
Spesifik zaman noktas�yla OS oran� �ekil 4'te grafikle g�sterilmektedir. Dasatinible tedavi uygulanan ve 3 ayda ≤ %10 �eklinde bir BCR-ABL d�zeyine ula�an hastalarda OS oran�n�n ula�mayanlara k�yasla tutarl� �ekilde daha y�ksek oldu�u g�r�lm��t�r.
�ekil 4. Yeni kronik KML tan�s� konmu� olan hastalarda yap�lan bir faz 3 �al��mada 3. ayda BCR-ABL d�zeyine g�re (≤ %10 veya > %10) genel sa�kal�m i�in s�n�r noktas� grafi�i
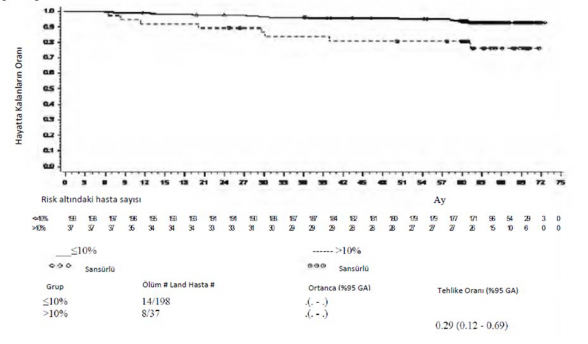
Hastal�k ilerlemesi uygun terap�tik idareye kar��n akyuvar h�crelerinde art��, CHR, k�smi CyR veya CCyR kayb�, h�zlanm�� evreye veya blast evresine ilerleme ya da �l�m �eklinde tan�mlanm��t�r. Tahmin edilen 60 ayl�k PFS oran� dasatinib ve imatinib tedavi grubunun her ikisi i�inde %88,9'dur (GA: %84 - %92,4). 60 ayda, akselere ya da blast faza ge�i� dasatinib (n
= 8; %3) ile tedavi edilen hastalarda imatinib ile tedavi edilen hastalardan (n = 15; %5,8) daha seyrek olarak ger�ekle�mi�tir. Dasatinib ve imatinib ile tedavi edilen vakalardaki tahminî 60 ayl�k sa�kal�m oranlar� s�ras�yla %90,9 (GA: %86,6 - %93,8) ve %89,6 (GA: %85,2 - %92,8) olmu�tur. Dasatinib and imatinib aras�nda OS (Risk Oran� 1,01, %95 GA: 0,58-1,73, p= 0,9800) ve PFS (Risk Oran� 1, %95 GA: 0,58-1,72, p = 0,9998) a��s�ndan herhangi bir fark tespit edilmemi�tir.
Yeni kronik faz KML tan�s� konmu� hastalarla y�r�t�len faz III �al��mas�nda, dasatinib veya imatinib tedavileri kesilen hastalardan al�nan kan �rneklerinde BCR-ABL sekans� yap�lm��t�r. Dasatinib alan hastalarda T315I, F317I/L ve V299L mutasyonlar� saptanm��t�r. �matinib grubunda farkl� bir mutasyon spektrumu saptanmam��t�r. In vitro verilere g�re, dasatinib, T315I mutasyonuna kar�� aktif g�r�nmemektedir.
Kronik faz KML – �nceki �matinib Tedavisine Diren� ya da �ntolerans
�matinibe diren�li ya da intolerans� olan hastalarda iki klinik �al��ma y�r�t�lm��t�r; bu �al��malardaki primer etkinlik sonland�rma kriteri Maj�r Sitogenetik Yan�tt� (MCyR):
�al��ma 1
400 ya da 600 mg imatinib ile ba�lang�� tedavileri ba�ar�s�z olan hastalarda a��k etiketli, randomize, kar��la�t�rmal� olmayan �ok merkezli bir �al��ma y�r�t�lm��t�r. Hastalara randomize olarak (2:1) ya dasatinib (g�nde iki kere 70 mg) ya da imatinib (g�nde iki kere 400 mg) verilmi�tir. Hastada doz de�i�ikli�i ile kontrol alt�na al�nmayan hastal�k progresyonu veya intoleransa dair bir bulgu olmas� durumunda, alternatif tedavi koluna ge�i� yap�lmas�na izin verilmi�tir. Primer sonlanma noktas� 12. haftada MCyR idi. Sonu�lar 150 hasta i�in mevcuttur:
101 hasta dasatinib ve 49 hasta imatinib koluna randomize edilmi�tir (t�m� imatinibe diren�li). Te�histen randomizasyona kadar ge�en medyan s�re dasatinib grubunda 64 ay ve imatinib grubunda 52 ay olmu�tur. T�m hastalar �nceden yo�un tedavi g�rm��t�r. Genel hasta pop�lasyonunun %93'� �nceden imatinibe tam hematolojik yan�t (CHR) vermi�tir. S�ras�yla dasatinib ve imatinib kollar�ndaki hastalar�n�n %28'inde ve %29'unda �nceden imatinibe MCyR g�r�lm��t�r.
Medyan tedavi s�resi dasatinib i�in 23 ay (hastalar�n %44'� g�n�m�ze dek > 24 ay tedavi edilmi�tir) ve imatinib i�in 3 ay (hastalar�n %10'u g�n�m�ze dek > 24 ay tedavi edilmi�tir) olmu�tur.
�apraz ge�i�ten �nce dasatinib kolundaki hastalar�n %93'� ve imatinib kolundaki hastalar�n
%82'sinde bir CHR elde edilmi�tir.
3 ayl�k takipte dasatinib kolunda (%36) imatinib kolundakinden (%29) daha s�k MCyR
g�r�lm��t�r. Dasatinib kolundaki hastalar�n %22'sinde tam sitogenetik yan�t (CCyR) rapor edilmi� ancak imatinib kolunda bu oran yaln�zca %8 olarak bildirilmi�tir. Daha uzun s�reli tedavi ve takiple (medyan 24 ay), �aprazlama �ncesi dasatinib ile tedavi edilen hastalar�n %53'� (%44'�nde CCyR), imatinib ile tedavi edilenlerin %33'�nde (%18'inde CCyR) McyR'ye ula��lm��t�r. �al��maya girmeden �nce 400 mg imatinib alm�� olan hastalar aras�nda dasatinib kolunda hastalar�n %61'inde, imatinib kolunda hastalar�n %50'sinde MCyR'ye ula��lm��t�r.
Kaplan-Meier'in tahminlerine dayanarak, 1 y�l MCyR devam ettiren hastalar�n oran� dasatinib (CCyR %97, %95 GA: [%92-%100]) i�in %92 (%95 GA: [%85-%100]) ve imatinib (CCyR
%100) i�in %74 olmu�tur (95%GA: [%49-%100]). MCyR'yi 18 ay boyunca devam ettiren
hastalar�n oran� Ddasatinib (CCyR %94, %95 GA: [%87-%100]) i�in %90 (%95 GA: [%82-
%98]) ve imatinib (CCyR 100%) i�in %74't� (%95 GA: [%49-%100]).
Kaplan-Meier'in tahminlerine dayanarak, 1 y�l boyunca ilerleme olmadan hayatta kalan [progression-free survival (PFS)] hastalar�n oran� dasatinib i�in %91 (%95 GA: [%85-%97]) ve imatinib i�in %73 olmu�tur (%95 GA: [%54-%91]). �kinci y�lda PFS'ye sahip hastalar�n oran� Ddasatinib i�in %86 (%95 GA: [%78-%93]) ve imatinib i�in %65 (%95 GA: [%43-%87]) olmu�tur.
Dasatinib kolundaki hastalar�n toplam %43'�n�n ve imatinib kolundakilerin %82'sinin tedavileri ba�ar�s�z olmu�tur; yani, ya hastal�klar� ilerlemi�tir ya da di�er tedaviye �apraz ge�i� yapm��lard�r (yan�t al�nmad���, �al��ma ilac� tolere edilmedi�i i�in vs.)
�apraz ge�i� �ncesi maj�r molek�ler yan�t oranlar� (periferik kan �rneklerinde BCR-ABL/ kontrol transkriplerinin RQ-PCR ile <%0,1 olmas� ile tan�mlan�r) dasatinib i�in %29 ve imatinib i�in %12 olmu�tur.
�al��ma 2
�matinibe intolerans veya diren� geli�tiren (yani, imatinib tedavisi s�ras�nda tedaviye devam etmeyi olanaks�z hale getiren �nemli toksisite geli�tiren hastalar) hastalarda a��k etiketli, tek kollu, �ok merkezli bir �al��ma y�r�t�lm��t�r.
Toplam 387 hasta (288'i diren�, 99'u intolerans) g�nde iki kere 70 mg dasatinib alm��t�r. Te�histen tedavinin ba�lang�c�na kadar medyan s�re 61 ay idi. Hastalar�n �o�unlu�u (% 53) 3 y�ldan fazla bir s�re �nce imatinib tedavisi g�rd�. Diren� geli�tiren hastalar�n �o�u (%72) > 600 mg imatinib alm��t�. Imatinibe ilaveten, hastalar�n %35'i daha �nce sitotoksik kemoterapi g�rm��t�, %65'i daha �nce interferon alm��t� ve %10'una �nceden k�k h�cre transplantasyonu yap�lm��t�. Ba�lang��ta hastalar�n %38'inin imatinib direncini olu�turan mutasyonlar� vard�. Dasatinib tedavisinin medyan s�resi 24 ay olmu�, hastalar�n %51'i bug�ne kadar > 24 ay tedavi edilmi�tir. Maj�r sitogenetik yan�t (MCyR) imatinibe diren�li hastalar�n %55'inde, imatinib intolerans hastalar�n %82'sinde geli�mi�tir.
Minimum 24 ay takip s�resinde �nceden MCyR g�steren 240 hastan�n 21'inde ilerleme olmu� ve medyan MCyR s�resine ula��lmam��t�r.
Kaplan-Meier'in tahminlerine dayanarak, hastalar�n %95'i (%95 GA: [%92-%98]) MCyR'yi 1 y�l boyunca ve %88'i (%95 GA: [%83-%93]) 2 y�l boyunca s�rd�rm��lerdir. CCyR'yi 1 y�l boyunca s�rd�ren hastalar�n oran� %97 (%95 GA: [%94-%99]) ve 2 y�l s�rd�ren hastalar�n %90 (%95 GA: [%86-%95]) olmu�tur. Daha �nce imatinibe kar�� hi� MCyR'ye sahip olmayan imatinib diren�li hastalar�n (n= 188) %42'si dasatinib ile MCyR'ye ula�m��t�r.
Bu �al��maya kaydedilen hastalar�n %38'inde 45 farkl� BCR-ABL mutasyonu mevcuttu. T315I hari� olmak �zere imatinib direnci ile ili�kili �e�itli BCR-ABL mutasyonlar� bulunan hastalarda tam hematolojik yan�t veya MCyR elde edilmi�tir. �kinci y�lda MCyR oranlar�, hastalara ba�lang�� BCR-ABL mutasyonu, P-loop mutasyonu olmas�na veya herhangi bir mutasyon bulunmamas�na ba�l� olmaks�z�n benzerdi s�ras�yla %63, %61 ve %62).
�matinibe diren�li hastalar aras�nda tahmin edilen PFS oran� 1 y�lda %88 (%95 GA: [%84-
%92]) ve 2 y�lda %75'ti (%95 GA: [%69-%81]). �matinibi tolere edemeyen hastalar aras�nda
tahmin edilen PFS oran� 1 y�lda %98 (%95 GA: [%95-%100]) ve 2 y�lda %94 (%95 GA: [%88-
%99]) olmu�tur.
24. ayda maj�r molek�ler yan�t oran� %45 idi (imatinibe diren�li hastalar i�in %35 ve imatinibi tolere edemeyen hastalar i�in %74).
Akselere Faz KML
�matinibe diren�li veya intoleran olan hastalarda a��k etiketli, tek kollu, �ok merkezli bir �al��ma yap�lm��t�r. Toplam 174 hasta (imatinib diren�li: 161, intoleransl�: 13) g�nde iki kere
70 mg dasatinib alm��t�r. Te�histen tedavi ba�lang�c�na kadar ge�en medyan s�re 82 ay olmu�tur. Dasatinib tedavisinin medyan s�resi 14 ay olmu�, hastalar�n %31'i bug�ne kadar > 24 ay tedavi edilmi�tir. 24 ayda maj�r molek�ler yan�t oran� %46'd�r (Tam sitogenetik yan�t� (CCyR) olan 41 hastada de�erlendirilmi�tir).
Myeloid Blastik Faz KML
�matinibe intolerans� veya direnci olan hastalarda a��k etiketli, tek kollu, �ok merkezli bir �al��ma yap�lm��t�r. Toplam 109 hasta (imatinib direnci: 99, intolerans�: 10) g�nde iki kere 70 mg dasatinib alm��t�r. Te�histen tedavi ba�lang�c�na kadar ge�en medyan s�re 48 ay olmu�tur. Dasatinib tedavisinin medyan s�resi 3,5 ay olmu�, hastalar�n %12'� bug�ne kadar > 24 ay tedavi edilmi�tir. 24 ayda maj�r molek�ler yan�t oran� %68'dir (Tam sitogenetik yan�t� (CCyR) olan 19 hastada de�erlendirilmi�tir). �lave etkililik bulgular� Tablo 10'da bildirilmi�tir.
Lenfoid Blastik Faz KML ve Ph+ ALL
Daha �nceki imatinib tedavisine diren� veya intolerans geli�tiren lenfoid blastik faz KML veya Ph+ ALL hastalar�nda a��k etiketli, tek kollu, �ok merkezli bir �al��ma yap�lm��t�r. Toplam 48 lenfoid blastik KML hastas� (imatinib diren�li: 42, intoleransl�: 6) g�nde iki kere 70 mg dasatinib alm��t�r. Te�histen tedavi ba�lang�c�na kadar medyan 28 ay ge�mi�tir. Dasatinib tedavisinin medyan s�resi 3 ay olmu�, bug�ne kadar tedavisi > 24 ay s�ren hasta oran� %2 olmu�tur. 24 ayda maj�r molek�ler yan�t oran� %50'dir (Tam sitogenetik yan�t� (CCyR) olan 22 hastada). Ayr�ca 46 Ph+ ALL hastas� da g�nde iki kere 70 mg dasatinib alm��t�r (imatinibe diren�li: 44, intoleransl�: 2). Te�histen tedavi ba�lang�c�na kadar medyan 18 ay ge�mi�tir.
Dasatinib tedavisinin medyan s�resi 3 ay olup bug�ne kadar > 24 ay tedavi edilen hasta oran�
%7 olmu�tur. 24 ayda maj�r molek�ler yan�t oran� %52'dir (Tam sitogenik yan�t� (CCyR) olan 25 hastada). Maj�r hematolojik yan�tlar�n (MaHR) �abuk elde edilmi� olmas� dikkate de�erdir (lenfoid blastik KML hastalar�nda ilk dasatinib uygulamas�ndan itibaren 35 g�n, Ph+ ALL hastalar�nda ise 55 g�n i�inde).
Tablo 10: Faz II Dasatinib tek kollu klinik �al��malar�nda etkililik
| Kronik (N=387) | H�zlanm�� (n=174) | Myeloidblast (n=109) | Lenfoid blast (n=48) | Ph+ALL (n=46) |
Hematolojik yan�t oran� (%) | |||||
MaHR (%95 CI) | n/a | %64 (57-72) | %33 (24-43) | %35 (22-51) | %41 (27-57) |
CHR (%95 CI) | %91 (88-94) | %50 (42-58) | %26 (18-35) | %29 (17-44) | %35 (21-50) |
NEL (%95 CI) | n/a | %14 (10-21) | %7 (3-14) | %6 (1-17) | %7 (1-18) |
MaHR s�resi (%; Kaplan-Meier kestirimleri) | |||||
1 y�l | n/a | %79 (71-87) | %71 (55-87) | %29 (3-56) | %32 (8-56) |
2 y�l | n/a | %60 (50-70) | %41 (21-60) | %10 (0-28) | %24 (2-47) |
Sitogenetik yan�t (%) | |||||
MCyR (%95 CI) | %62 (57-67) | %40 (33-48) | %34 (25-44) | %52 (37-67) | %57 (41-71) |
CCyR (%95 CI) | %54 (48-59) | %33 (26-41) | %27 (19-36) | %46 (31-61) | %54 (39-69) |
Sa�kal�m (%; Kaplan-Meier kestirimleri) | |||||
Progresyonsuz Sa�kal�m | |||||
1 y�l | %91 (88-94) | %64 (57-72) | %35 (25-45) | %14 (3-25) | %21 (9-34) |
2 y�l | %80 (75-84) | %46 (38-54) | %20 (11-29) | %5 (0-13) | %12 (2-23) |
Genel | |||||
1 y�l | %97 (95-99) | %83 (77-89) | %48 (38-59) | %30 (14-47) | %35 (20-51) |
2 y�l | %94 (91-97) | %72 (64-79) | %38 (27-50) | %26 (10-42) | %31 (16-47) |
Bu tabloda a��klanan veriler g�nde iki kez 70 mg'l�k ba�lang�� dozu kullan�lan �al��malardan al�nm��t�r. �nerilen ba�lang�� dozu i�in B�l�m 4.2'ye bak�n�z.
a Koyu renkli karakterlerle verilen rakamlar primer sonlanma noktas� sonu�lar�d�r.
b Hematolojik yan�t kriterleri (t�m yan�tlar 4 hafta sonra do�rulanm��t�r): Maj�r hematolojik yan�t (MaHR) = tam hematolojik yan�t (CHR) + l�semi kan�t� yok(NEL).
CHR (kronik KML): WBC < kurumsal ULN, trombosit < 450.000 W, periferik kanda blast veya promyelositler yok, periferik kanda < %5 miyelositler + metamiyelositler, periferik kanda <%20 bazofiller ve ekstramed�ller tutulum yok.
CHR (ileri evre KML/Ph+ ALL): WBC < kurumsal ULN, ANC>1.000 W, trombosit > 1.000 W, periferik kanda blast veya promyelositler yok, periferik kanda < %5 kemik ili�i blast�, <%5 miyelositler + metamiyelositler, periferik kanda <%20 bazofiller ve ekstramed�ller tutulum yok.
NEL: CHR ile ayn� kriterler ancak ANC > 500 W ve < 1.000 /mm3 veya trombosit > 20.000/mm3 ve <100.000 W.
n/a = ge�erli de�il; GA = g�ven aral���; ULN = normal aral���n �st s�n�r�.
Dasatinibten sonra kemik ili�i transplant� yap�lan hastalar�n sonu�lar� tam olarak de�erlendirilmemi�tir.
�matinibe diren�li veya intoleran olan kronik, akselere ya da myeloid blast faz KML ve Ph+ALL hastalar�nda Faz III Klinik �al��malar
G�nde bir kere uygulanan dasatinib ile g�nde iki kere uygulanan dasatinib etkinli�ini de�erlendirmek �zere randomize, a��k-etiketli iki �al��ma y�r�t�lm��t�r: A�a��daki sonu�lar dasatinib tedavisine ba�lad�ktan sonra minimum 2 y�ll�k ve 7 y�ll�k takiplere dayanmaktad�r.
�al��ma 1
Kronik faz KML �al��mas�nda, primer sonland�rma kriteri imatinibe diren�li hastalarda MCyR't�r. Ba�l�ca sekonder sonland�rma kriteri imatinibe diren�li hastalarda toplam g�nl�k dozda MCyR't�r. Di�er ikincil son noktalar, MCyR, PFS ve genel hayatta kalma s�resini i�ermi�tir. 497'i imatinibe diren�li olan toplam 670 hasta g�nde bir kere 100 mg, g�nde bir kere 140 mg, g�nde iki kere 50 mg ya da g�nde iki kere 70 mg dasatinib grubuna randomize edilmi�tir. En az 5 y�ll�k takip s�resi olan (n=205) halen tedavi g�rmekte olan t�m hastalar i�in medyan tedavi s�resi 59 ayd� (28 – 66 ay aral���nda). T�m hastalar i�in 7 y�ll�k takipte medyan tedavi s�resi 29,8 ay olmu�tur (aral�k <1-92,9 ay).
T�m dasatinib tedavi gruplar�nda etkinlik elde edilmi�tir ve primer sonlan�m noktas�nda g�nde tek doz uygulamas� g�nde iki kere uygulamaya g�re (MCyR fark� %1,9; %95 g�ven aral��� [-
%6,8 - %10,6]) k�yaslanabilir bir etkinlik (daha az olmayan) g�stermi�tir. Ancak, g�nde bir kez 100 mg'l�k rejimde g�venlilik ve tolerabilitede art�� g�zlenmi�tir. Etkililik sonu�lar� Tablo 11 ve 12'de a��klanmaktad�r.
Tablo 11: Faz III Doz Optimizasyon �al��mas�nda Dasatinibin Etkinli�i: �matinibe Diren�li veya �ntolerant Kronik Faz KML (2 y�ll�k sonu�lar)
T�m Hastalar | n=167 |
Imitanibe diren�li hastalar | n=124 |
Hematolojik Yan�t Oran� (%95 GA) |
|
CHR | %92 (86-95) |
Sitogenetik Yan�t (%) (%95 GA) |
|
MCyR |
|
T�m hastalar | %63 (56-71) |
Imatinibe Diren�li Hastalar | %59 (50-68) |
CCyR |
|
B�t�n hastalar | %50 (42-58) |
Imatinibe Diren�li Hastalar | %44 (35-53) |

B�t�n Hastalar
%69 (58-79)
�matinibe Diren�li Hastalar
%72 (58-83)
CCyR Elde Edilen Hastalarda Maj�r Molek�ler Yan�t (%) (%95 GA)
Tam Hematolojik Yan�t (THY) (kronik KML): l�kosit ≤ kurum �st s�n�r�, trombositler <450.000 /mm, periferal kanda blast ya da promyelosit yok, periferal kanda <%5 myelosit art� metamyelosit, periferal kanda bazofil <%20 ve hi� bir ekstramed�ler tutulum yok.
d Maj�r molek�ler yan�t kriterleri: Periferik kan �rneklerinde RQ-PZR ile BCR-ABL/kontrol transkriptin ≤%0,1 olmas�yla tan�mlan�r.
GA = g�ven aral��� ULN = Normal Aral���n �st S�n�r�.
Tablo 12: Dasatinibin Faz III Doz Optimizasyonu �al��mas�ndaki Uzun D�nemli Etkinli�i: �matinibe Diren�li veya �ntolerant Kronik Faz KML Hastalar�
| Minimum Takip S�resi | |||
| 1 y�l | 2 y�l | 5 y�l | 7 y�l |
Maj�r Molek�ler Yan�t | ||||
T�m hastalar | Ge�erli de�il | %37(57/154) | %44 (71/160) | %46 (73/160) |
Imatinibe diren�li hastalar | Ge�erli de�il | %35 (41/117) | %42 (50/120) | %43 (51/120) |
Imatinibe intoleran hastalar | Ge�erli de�il | %43 (16/37) | %53 (21/40) | %55 (22/40) |
Progresyonsuz Sa�kal�m (PFS) | ||||
T�m hastalar | %90 (86, 95) | %80 (73, 87) | %51 (41, 60) | %42 (33, 51) |
Imatinibe diren�li hastalar | %88 (82, 94) | %77 (68, 85) | %49 (39, 59) | %39 (29, 49) |
Imatinibe intoleran hastalar | %97 (92, 100) | %87 (76, 99) | %56 (37, 76) | %51(32, 67) |
Genel Sa�kal�m | ||||
T�m hastalar | %96 (93, 99) | %91 (86, 96) | %78 (72, 85) | %65 (56, 72) |
Imatinibe diren�li hastalar | %94 (90, 98) | %89 (84, 95) | %77 (69, 85) | %63 (53, 71) |
Imatinibe intoleran hastalar | %100 (100, 100) | %95 (88, 100) | %82 (70, 94) | %70 (52, 82) |
Kaplan-Meier tahminlerine dayanarak, g�nde bir defa dasatinib 100 mg ile tedavi edilen ve 18 ay s�reyle MCyR yan�t�n� koruyan hastalar�n oran� %93 idi (%95 GA: [88% - 98%]).
�matinibi tolere edemeyen hastalarda etkililik de de�erlendirilmi�tir. G�nde bir defa 100 mg dozu alan bu hasta pop�lasyonunda, MCyR elde edilen hasta oran� %77 ve CCyR oran� %67 olmu�tur.
�al��ma 2
�leri faz KML ve Ph+ ALL �al��mas�n�n primer sonland�rma kriteri MaHR't�. Toplam 611 hasta ya g�nde bir kere 140 mg ya da g�nde iki kere 70 mg DASIKAM grubuna randomize edilmi�ti. Medyan tedavi s�resi yakla��k 6 ayd� (aral�k 0,03-31 ay).
Primer etkinlik sonlan�m kriterine g�re, g�nde bir kere uygulamas�, g�nde iki kere uygulamas� ile kar��la�t�r�labilir (daha az olmayan) bir etkinlik g�stermi�tir (MaHR fark� %0,8; %95 g�ven aral��� [-%7,1-%8,7]), ancak, g�nde bir kez 140 mg rejimi iyile�mi� g�venlilik ve tolerabilite g�stermi�tir. Yan�t oranlar� Tablo 13'te belirtilmektedir.
Tablo 13: Dasatinibin Faz III Doz Optimizasyonu �al��mas�ndaki Etkinli�i: �leri Faz KML ve Ph+ ALL (2 y�ll�k sonu�lar)
| Akselere (n=158) | Miyeloid Blast (n=75) | Lenfoid Blast (n=33) | Ph+ALL (n=40) |
MaHY | %66 | %28 | %42 | %38 |
(%95 GA) | (59-74) | (18-40) | (26-61) | (23-54) |
THY | %47 | %17 | %21 | %33 |
(%95 GA) | (40-56) | (10-28) | (9-39) | (19-49) |
NEL | %19 | %11 | %21 | %5 |
(%95 GA) | (13-26) | (5-20) | (9-39) | (1-17) |
MSY | %39 | %28 | %52 | %70 |
(%95 GA) | (31-47) | (18-40) | (34-69) | (54-83) |
TSY | %32 | %17 | %39 | %50 |
(%95 GA) | (25-40) | (10-28) | (23-58) | (34-66) |
= tam hematolojik yan�t (THY) + l�semi kan�t� olmamas� (NEL).
THY: l�kosit ≤ kurumun ULN'si, ANC ≥ 1.000 /mm, trombosit ≥ 100.000 /mm, periferik kanda blast ya da promiyelosit yok, kemik ili�inde blast ≤ %5, periferik kanda miyelosit art� metamiyelosit < %5, periferik kanda bazofil <%20 ve kemik ili�i d��� tutulum yok.
NEL: THY ile ayn� kriterler ama ANC ≥ 500/mm ve < 1.000 /mm, ya da trombosit ≥ 20.000 /mm ve ≤ 100.000
/mm
G�nde bir defa 140 mg rejimi ile tedavi uygulanan h�zlanm�� faz CML hastalar�nda medyan MaHR s�resi ve medyan genel sa�kal�ma ula��lmam��t�r ve medyan PFS'nin 25 ay oldu�u tespit edilmi�tir.
G�nde bir defa 140 mg rejimi ile tedavi uygulanan miyeloid blast faz� CML hastalar�nda medyan MaHR s�resinin 8 ay, medyan PFS'nin 4 ay, medyan genel sa�kal�m�n ise 8 ay oldu�u tespit edilmi�tir. G�nde bir defa 140 mg rejimi ile tedavi uygulanan lenfoid blast faz� CML
hastalar�nda medyan MaHR s�resinin 5 ay, medyan PFS'nin 5 ay, medyan genel sa�kal�m�n ise 11 ay oldu�u tespit edilmi�tir.
G�nde bir defa 140 mg rejimi ile tedavi uygulanan Ph+ ALL hastalar�nda medyan MaHR s�resinin 5 ay, medyan PFS'nin 4 ay, medyan genel sa�kal�m�n ise 7 ay oldu�u tespit edilmi�tir. Pediyatrik pop�lasyon
Pediyatrik KML hastalar�
�ki pediyatrik �al��mada tedavi edilen kronik faz KML'li 130 pediyatrik hastada (biri Faz I, a��k etiketli, randomize olmayan doz aral��� bulma �al��mas� ve di�eri Faz II, a��k etiketli, randomize olmayan �al��ma), 84 hasta (sadece Faz II �al��madan kaydedilen) yeni tan� konan kronik faz KML ve 46 hasta (17 hasta Faz I �al��madan ve 29 hasta Faz II �al��madan kaydedilmi�tir) imatinib ile �nceki tedaviye diren�liydi veya bu tedaviyi tolere edememi�tir. Kronik faz KML'li 130 pediyatrik hastan�n 97'si g�nde bir kez dasatinib tablet 60 mg/m ile tedavi edilmemi�tir (y�ksek BSA'l� hastalar i�in g�nde bir defa 100 mg'l�k maksimum doz). Hastalar hastal�k progresyonuna veya kabul edilemez toksisiteye kadar tedavi edilmi�tir.
Kilit etkililik sonlanma noktalar� ��yleydi: tam sitogenetik yan�t (CCyR), maj�r sitogenetik yan�t (MCyR) ve maj�r molek�ler yan�t (MMR). Sonu�lar Tablo 14'te g�sterilmektedir.
Tablo 14: Dasatinibin kronik faz KML'li pediyatrik hastalarda etkilili�i – Minimum takip d�neminde zaman i�inde k�m�latif yan�t
| 3 ay | 6 ay | 12 ay | 24 ay |
CCyR (%95 GA) | ||||
Yeni tan� konan (N=51) | %43,1 (29,3-57,8) %45,7 | %66,7 (52,1-79,2) %71,7 | %96,1 (86,5- 99,5) %78,3 | %96,1 (86,5-99,5) %82,6 |
�nceki imatinib (N=46) | (30,9-61) | (56,5-84) | (63,6-89,1) | (68,6-92,2) |
MCyR (%95 GA) | ||||
Yeni tan� konan (N=51) | %60,8 (46,1-74,2) %60,9 | %90,2 (78,6- 96,7) %82,6 | %98 (89,6- 100) %89,1 | %98 (89,6- 100) %89,1 |
�nceki imatinib (N=46) | (45,4- 74,9) | (68,6- 92,2) | (76,4-96,4) | (76,4-96,4) |
MMR (%95 GA) | ||||
Yeni tan� konan (N=51) | %7,8 (2,2- 18,9) %15,2 | %31,4 (19,1-45,9) %26,1 | %56,9 (42,2-70,7) %39,1 | %74,5 (60,4- 85,7) %52,2 |
�nceki imatinib (N=46) | (6,3- 28,9) | (14,3- 41,1) | (25,1-54,6) | (36,9- 67,1) |
Faz I pediyatrik �al��mada, imatinibe diren�li veya tolere edemeyen kronik faz KML'li hastalar aras�nda en az 7 y�ll�k takipten sonra, medyan PFS s�resi 53,6 ay ve OS oran� %82,4 idi.
Faz II pediyatrik �al��mada, tablet form�lasyonu alan hastalarda yeni tan� alan kronik faz KML'li 51 hasta aras�nda tahmini 24 ayl�k PFS oran� %94 iken (82,6-98) imatinibe
diren�li/tolere edemeyen kronik faz KML'li 29 hastada bu oran� %81,7 (61,4, 92) bulunmu�tur. 24 ayl�k takipten sonra, yeni tan� konan hastalarda OS %100 ve imatinibe diren�li/tolere edemeyen hastalara %96,6 idi.
Faz II pediyatrik �al��mada, yeni tan� konan 1 hastada ve imatinibe diren�li/tolere edemeyen 2 hastada hastal�k blastik faz KML'ye ilerlemi�tir.
Dasatinib oral s�spansiyon haz�rlamaya y�nelik toz form�lasyonu alan (72 mg/m dozunda) 33 yeni tan� konmu� kronik faz KML'li pediyatrik hasta mevcuttu. Bu doz �nerilen doza k�yasla
%30 daha d���k maruziyeti temsil etmektedir. Bu hastalarda, CCyR ve MMR 12. ayda CCyR:
%87,9 [%95 GA: (71,8-96,6)] ve MMR: %45,5 [%95 GA: (28,1-63,6)] olarak bulunmu�tur.
Daha �nce imatinib alm�� olan dasatinib ile tedavi edilen kronik faz KML hastalar� aras�nda, tedavi sonunda �u mutasyonlar tespit edilmi�tir: T315A, E255K ve F317L. Ancak, tedaviden �nce E255K ve F317L de tespit edilmi�tir. Tedavi sonunda yeni tan� konan kronik faz KML hastalar�nda herhangi bir mutasyon tespit edilmemi�tir.
ALL'li pediyatrik hastalar
Dasatinibin kemoterapi ile kombinasyon halinde etkilili�i, yeni tan� konan Ph+ ALL'li bir ya��n �zerindeki hastalarda yap�lan bir pivot �al��mada de�erlendirilmi�tir.
Bu �ok merkezli, tarihsel olarak kontroll�, standart kemoterapiye eklenen dasatinib ile yap�lan Faz II �al��mada, 104'� do�rulam�� Ph+ ALL'ye sahip yeni tan� konmu� Ph+ ALL'li 106 pediyatrik hasta, kemoterapi ile kombinasyon halinde 24 aya varan s�rekli doz rejimi ile g�nl�k 60 mg/m'lik doz alm��t�r. Hastalar�n 82'si sadece dasatinib tablet al�rken 24 hasta en az bir kez dasatinib oral s�spansiyon haz�rlamak i�in toz form�lasyonunu alm��t�r (bunlar�n 8'i sadece dasatinib oral s�spansiyon haz�rlamak i�in toz form�lasyonunu alm��t�r). Arka plandaki kemoterapi rejimi AIEOP-BFM ALL 2000 �al��mas�nda kullan�lanla ayn�yd� (kemoterap�tik standart �ok ajanl� kemoterapi protokol�). Primer etkililik sonlanma noktas� 3 y�ll�k olays�z sa�kal�m olup (EFS), %65,5 olarak bulunmu�tur (55,5, 73,7).
Ig/TCR tekrar d�zenlemesi ile de�erlendirilen minimum rezid�el hastal�k (MRD) negativite oran�, konsolidasyon sonunda tedavi edilen t�m hastalarda %71,7 idi. Bu oran de�erlendirilebilir Ig/TCR de�erlendirmeleri olan 85 hastaya dayand�r�ld���nda, oran %89,4 idi. �nd�ksiyon ve konsolidasyon sonunda ak�� sitometrisi ile �l��len �ekilde MRD negativite oranlar� s�ras�yla %66 ve %84 idi.
5.2. Farmakokinetik �zellikler
Genel �zelliklerDasatinibin farmakokineti�i 229 yeti�kin sa�l�kl� g�n�ll�lerde ve 84 hastada de�erlendirilmi�tir.
Emilim:
Oral uygulamay� takiben hastalar dasatinibi h�zla absorbe ederler, pik konsantrasyonlar 0,5-3 saatte g�r�l�r. Oral uygulamay� takiben, ortalama maruziyetteki art�� (EAA) g�nde iki kere 25 mg - 120 mg aral���ndaki dozlarda doz art���yla yakla��k olarak orant�l�d�r. Dasatinibin genel ortalama terminal yar�lanma �mr� hastalarda yakla��k 5-6 saattir.
�ok ya�l� bir yemekten 30 dakika sonra 100 mg'l�k tek bir dasatinib dozu uygulanan sa�l�kl� g�n�ll�lerde al�nan veriler dasatinibin ortalama EAA'�nda %14 art�� g�stermi�tir.
Dasatinibden 30 dakika �nce yenilen az ya�l� bir yemek Dasatinibin ortalama EAA'�n� %21 artt�rm��t�r. G�dalar�n g�zlenen etkileri ila� al�m�nda klinik a��dan �nem ta��yan de�i�ikliklere yol a�mam��t�r. Dasatinib maruziyetinde g�r�len de�i�kenlik, az ya�l� (%39 CV) ve �ok ya�l� yeme�e (%32 CV) k�yasla a�l�k ko�ullar�nda daha y�ksektir (%47 CV).
Hasta pop�lasyonu FK analizine g�re, dasatinib maruziyetinde g�r�len de�i�kenli�in temelde durumlar aras� biyoyararlan�m de�i�kenli�inden (%44 CV) ve daha d���k �l��de bireyler aras� biyoyararlan�m de�i�kenli�inden ve bireyler aras� klirens de�i�kenliklerinden (s�ras�yla, %30 ve %32) kaynakland��� tahmin edilmi�tir. Maruziyetteki durumlar aras� rastgele de�i�kenli�in k�m�latif maruziyeti ve etkililik veya g�venlili�i etkilemesi beklenmemektedir.
Da��l�m:
Hastalarda dasatinibin g�r�n�r da��l�m hacmi y�ksek olup (2,505 L) varyasyon katsay�s� (%CV
%93) t�bbi �r�n�n ekstravask�ler yerde yayg�n olarak da��ld���n� g�sterir. In vitro deneyimlere g�re, dasatinib klinik olarak �nemli konsantrasyonlarda plazma proteinlerine yakla��k %96 oran�nda ba�lanmaktad�r.
Biyotransformasyon:
Dasatinib insanlarda, metabolitlerin olu�umunda g�rev alan multipl enzimler ile yayg�n olarak metabolize edilir. 100 mg [C] i�aretli dasatinib uygulanan sa�l�kl� g�n�ll�lerde plazmada dola�an radyoaktivitenin %29'u de�i�memi� dasatinib olarak bulunmu�tur. Plazma konsantrasyonu ve �l��len in vitro aktivite dasatinibin metabolitlerinin �r�n�n g�zlenen farmakolojisinde maj�r bir rol oynama olas�l�klar�n�n d���k oldu�unu g�stermektedir. CYP3A4 dasatinibin metabolizmas�ndan sorumlu maj�r enzimdir.
Eliminasyon:
Dasatinib'in ortalama terminal yar� �mr� 3 ila 5 saat aras�ndad�r. Ortalama belirgin oral klirensi 363,8 L/saattir (%CV %81,3).
Eliminasyon ba�l�ca fe�este, �o�unlukla metabolitler halinde ger�ekle�ir. Tek doz [C] i�aretli dasatinib verilmesini takiben, dozun yakla��k %89'u 10 g�n i�inde at�lm��, radyoaktivitenin
%4'� idrarda ve %85'i fe�este bulunmu�tur. �drardaki ve fe�esteki de�i�memi� dasatinib oranlar� s�ras�yla dozun %0,1'i ve %19'u olmu�, dozun kalan� ise metabolit olmu�tur.
Do�rusall�k/ Do�rusal Olmayan Durum:
Yeterli veri mevcut de�ildir.
Hastalardaki karakteristik �zellikler
B�brek yetmezli�i:
Dasatinib ile b�brek fonksiyonlar� azalm�� olan hastalarda herhangi bir klinik �al��ma yap�lmam��t�r (serum kreatinin konsantrasyonu normal aral���n �st s�n�r�n�n >1,5 kat� olan hastalar �al��malara al�nmam��t�r). Dasatinibin ve metabolitlerinin b�brek klerensi <%4 oldu�u i�in, b�brek yetmezli�i olan hastalarda total v�cut klerensinde bir azalma beklenmez.
Dasatinib ve metabolitleri b�breklerden minimal d�zeyde at�lmaktad�r.
Karaci�er yetmezli�i:
![]()
Karaci�er yetmezli�inin dasatinibin tek-doz farmakokineti�i �zerine etkileri, 50 mg uygulanan orta d�zeyde karaci�er yetmezli�i olan 8 hastada ve 20 mg uygulanan �iddetli karaci�er yetmezli�i olan 5 hastada, 70 mg uygulanan e�le�tirilmi� sa�l�kl� g�n�ll�lerle kar��la�t�r�larak de�erlendirilmi�ir. Orta d�zeyde karaci�er yetmezli�i olan hastalar normal karaci�er fonksiyonu olanlarla kar��la�t�r�ld���nda dasatinibin 70 mg doza g�re ayarlanm�� ortalama Cve EAA de�erleri s�ras�yla %47 ve %8 oran�nda azalm��t�r. �iddetli karaci�er yetmezli�i olan hastalar normal karaci�er fonksiyonu olan g�n�ll�ler ile kar��la�t�r�ld���nda dasatinibin 70 mg doza g�re ayarlanm�� ortalama Cve EAA de�erleri s�ras�yla %43 ve %28 oran�nda azalm��t�r. (Bkz. B�l�m 4.2 ve 4.4)
Pediyatrik pop�lasyon
Dasatinib farmakokineti�i l�semi veya solid t�m�rleri olan 104 pediyatrik hastada de�erlendirilmi�tir (tablet form�lasyonu alan 72 ve oral s�spansiyon haz�rlamak i�in toz form�lasyonu alan 32).
Yap�lan bir pediyatrik farmakokinetik �al��mada, doza g�re normalize edilen dasatinib maruziyeti (C, Cve C) kronik faz KML'li 21 hasta ve Ph+ ALL'li 16 hasta aras�nda benzer olmu�tur.
Dasatinib tablet form�lasyonunun farmakokineti�i, tekrarlayan veya diren�li l�semili veya solid t�m�rleri olan 72 pediyatrik hastada g�nde bir defa 60 ila 120 mg/m ve g�nde iki defa 50 ila 110 mg/m aras�nda de�i�en oral dozlarda de�erlendirilmi�tir. Veriler iki �al��mada birle�tirilmi�tir ve dasatinibin h�zla emildi�ini g�stermi�tir. Ortalama T0,5 ve 6 saat aras�nda g�zlenirken ortalama yar� �m�r t�m doz ve ya� gruplar�nda 2 ila 5 saat aras�nda bulunmu�tur. Dasatinibin FK profili, pediyatrik hastalarda maruziyette dozla ili�kili art��la birlikte dozla orant�l� olmu�tur. �ocuklar ve ad�lesanlar aras�nda dasatinib FK profili a��s�ndan anlaml� bir fark g�r�lmemi�tir. Doza g�re normalle�tirilmi� dasatinib C, EAA (0-T) ve EAA
(INF) parametrelerine ait geometrik ortalamalar�n farkl� doz d�zeylerinde �ocuklar ve ad�lesanlar aras�nda benzer oldu�u bulunmu�tur. Bir PFK modele dayal� sim�lasyon, B�l�m
4.2'de tablet i�in �nerilen v�cut a��rl���na dayal� dozlam�n, 60 mg/m tablet form�lasyonu ile benzer bir maruziyet sa�layaca��n� g�stermi�tir.
5.3. Klinik �ncesi g�venlilik verileri
Dasatinibin klinik olmayan g�venlilik profili bir dizi ve farelerde, s��anlarda, maymunlarda ve tav�anlarda yap�lan in vivo ve in vitro �al��mada de�erlendirilmi�tir.
Primer toksisiteler gastrointestinal, hematopoietik ve lenfoid sistemlerde ortaya ��km��t�r. Ba��rsak daima hedeflenen bir organ oldu�u i�in, s��anlarda ve maymunlarda gastrointestinal toksisite dozu s�n�rlam��t�r. S��anlarda eritrosit parametrelerindeki minimal ve hafif d����lere kemik ili�indeki de�i�iklikler e�lik etmi�tir; maymunlarda benzer de�i�iklikler daha d���k bir insidans ile g�r�lm��t�r. S��anlarda lenfoid toksisite lenf nod�llerinde, dalakta ve timusta lenfoid azalmas� ve lenfoid organlar�n a��rl�klar�nda d����ler ile kendini g�stermi�tir. Tedavinin kesilmesini takiben gastrointestinal, hematopoetik ve lenfoid sistemlerdeki de�i�iklikler geri d�n���ml� olmu�tur.
9 aya kadar tedavi edilen maymunlarda arka plan b�brek mineralizasyonunda art�� ile s�n�rl� b�brek de�i�iklikleri g�zlenmi�tir. Maymunlarda ≥ 15 mg/kg akut tek dozun uyguland��� bir oral �al��mada k�tan�z hemoraji g�zlenmi�, fakat ne maymunlarda ne de s��anlarda tekrarlanan dozlar�n uyguland��� �al��malarda g�r�lmemi�tir. S��anlarda dasatinib trombosit agregasyonunu in vitro olarak inhibe etmi� ve t�rnak eti kanamas�n� in vivo olarak uzatm��t�r. Ancak spontan kanama g�r�lmemi�tir.
hERG ve Purkinje lif tayinleri; in vitro dasatinib aktivitesinin kardiyak ventrik�ler repolarizasyonu (QT aral���) uzatma potansiyeli olabilece�ini g�stermi�tir. Ancak bilinci a��k maymunlarda �l��mlenen bir in vivo tek doz �al��mas�nda QT aral���nda veya EKG dalgas� formunda bir de�i�iklik g�r�lmemi�tir.
Dasatinib in vitro bakteri h�cresi tayinlerinde (Ames testi) mutajenik ve bir in vivo s��an mikron�kleus �al��mas�nda genotoksik bulunmam��t�r. B�l�nmekte olan �in hamsteri over h�crelerinde in vitro klastojenik etki g�stermi�tir.
S��an fertilitesi ve erken embriyonik geli�imle ilgili konvansiyonel bir �al��mada dasatinib erkek veya di�ilerin fertilitesini etkilememi�tir ancak insanlardaki klinikte kullan�lan doz seviyelerinde embriyoletaliteyi ind�klemi�tir. Embriyofetal geli�im �al��malar�nda dasatinib benzer �ekilde, s��anlarda yavrular�n boylar�ndaki d���� ve hem s��anlarda hem de tav�anlarda fet�s�n iskeletinde farkl�l�klar ile birlikte olan embriyoletaliteyi ind�klemi�tir. Bu etkiler maternel toksisiteye yol a�mayan dozlarda ortaya ��km��t�r; bu da dasatinibin implantasyondan organojenezin tamamlanmas�na kadar ge�en s�rede selektif reprod�ktif toksik madde oldu�unu g�stermektedir.
Farelerde dasatinib doza ba�l� olan ve doz azalt�larak ve/veya dozaj plan� de�i�tirilerek etkinlikle tedavi edilen immunosupresyonu ind�klemi�tir. Dasatinib fare fibroblastlar�nda y�r�t�len bir in vitro n�tral k�rm�z� uptake fototoksisite tayininde fototoksik potansiyel g�stermi�tir. Dasatinibin di�i t�ys�z farelere tek dozluk oral uygulama sonras� �nerilen standard terap�tik doz ile insan maruziyetinin 3 kat�na kadarki maruziyette (EAA'ya g�re) in vivo olarak non-fototoksik olarak de�erlendirilmi�tir.
�ki y�ll�k bir karsinojenisite �al��mas�nda, s��anlara g�nl�k 0,3, 1 ve 3 mg/kg dozlar�nda oral dasatinib uygulanm��t�r. En y�ksek doz genellikle g�nl�k 100 mg ila 140 mg aras�nda de�i�en �nerilen ba�lang�� dozunda insanlarda g�zlenen maruziyetle e�de�er bir plazma maruziyet (EAA) d�zeyi ile sonu�lanm��t�r. Y�ksek doz uygulanan di�ilerde uterus ve rahimde skuam�z h�creli karsinomalar ve papillomalar�n birle�ik insidans�nda ve d���k doz uygulanan erkeklerde prostat adenomalar�n�n insidans�nda istatistiksel olarak anlaml� bir art�� kaydedilmi�tir. S��anlarda karsinojenisite �al��malar�ndan elde edilen bu bulgular�n insanlar i�in �nemi bilinmemektedir.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Tablet �ekirde�i:
Laktoz monohidrat (inek s�t� kaynakl�) Mikrokristalin sel�loz tip 101 Mikrokristalin sel�loz tip 102
Hidroksipropil sel�loz tip E Kroskarmeloz sodyum tip A Magnezyum stearat
Film kaplama:
Hipromeloz
Titanyum dioksit (E171) Triasetin
6.2. Ge�imsizlikler
Ge�erli de�il.
6.3. Raf �mr�
36 ay
6.4. Saklamaya y�nelik �zel tedbirler
25°C alt�ndaki oda s�cakl���nda saklay�n�z.
6.5. Ambalaj�n niteli�i ve i�eri�i
30 film kapl� tablet i�eren �ocuklar�n a�amayaca�� polipropilen kapakl� y�ksek dansiteli polietilen (HDPE) �i�e.
Her bir HDPE �i�esine bir desikan (1 g) kutusu yerle�tirilir.
Her kartonda bir �i�e vard�r.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
DASIKAM film kapl� tablet sa�l�k profesyonellerinin aktif ila� maddesine maruz kalmalar�n� engelleyecek bir film kaplama ile �evrili bir �ekirdek tabletten olu�ur. Ancak, e�er tabletler ezilir veya k�r�l�rsa, sa�l�k profesyonelleri tek kullan�ml�k kemoterapi eldivenleri giymelidirler.
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj At�klar�n�n Kontrol� Y�netmelik”lerine uygun olarak imha edilmelidir.
 Do�um Sonras� Depresyonu
Do�um sonras� depresyonu, do�umdan sonra her on kad�ndan biri taraf�ndan
tecr�be edilen stresli bir durumdur.
Do�um Sonras� Depresyonu
Do�um sonras� depresyonu, do�umdan sonra her on kad�ndan biri taraf�ndan
tecr�be edilen stresli bir durumdur. |
 Asperger Sendromu
Asperger sendromu, otistik gurubun bir b�l�m� olan bir �z�rd�r. Bu genelde,
gurubun daha ”y�ksek” taraf�nda yer ald��� d���n�len ki�ilere uygun bir tan�d�r.
Asperger Sendromu
Asperger sendromu, otistik gurubun bir b�l�m� olan bir �z�rd�r. Bu genelde,
gurubun daha ”y�ksek” taraf�nda yer ald��� d���n�len ki�ilere uygun bir tan�d�r. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| DASAVEC | 8699828091516 | 18,118.01TL |
| DASIKAM | 8699638095728 | 17,256.55TL |
| MYLORGE | 8699514012757 | 28,119.61TL |
| SPRYCEL | 8699726094206 | 18,119.36TL |
| SPRYTINIB | 8699769090173 | 28,119.61TL |
| Di�er E�de�er �la�lar |
 |
HIV ve Aids HIV, Human Immunodeficiency Virus’d�r (�nsanlarda Ba����kl�k Sistemini Bozan Vir�sd�r). Bu vir�s AIDS hastal���na sebep olur. |
 |
Kolon, Rektum yada Ba��rsak Kanseri Ba��rsak kanseri kolon veya rektumda (arka ge�it) herhangi bir b�lgede ortaya ��kabilir.Kolorektal kanser erken safhalarda te�his edilmesi halinde daha kolay ve daha ba�ar�l� bir �ekilde tedavi edilir. |
 |
Depresyonu Anlamak Depresyon farkl� ki�ileri farkl� bi�imlerde etkiler. Duygusal veya fiziksel olmak �zere geni� alanda belirtilere sebep olabilir.Depresyona neler sebep olur? |
�LA� GENEL B�LG�LER�
TEVA �la�lar� San.Ve Tic.A.�
| Sat�� Fiyat� | 28119.61 TL [ 1 Dec 2025 ] |
| �nceki Sat�� Fiyat� | 28119.61 TL [ 24 Nov 2025 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | K�rm�z� Re�eteli bir ila�d�r. |
| Barkodu | 8699638095780 |
| Etkin Madde | Dasatinib |
| �thal ( ref. �lke : Fransa ) ve Be�eri bir ila�d�r. |