DEXA-SINE SE %0.1 tek kullan�ml�k g�z damlas� ��zelti (10 adet) K�sa �r�n Bilgisi
{ Deksametazon }
1. BE�ER� TIBB� �R�N�N ADI
DEXA-S�NE SE %0.1 tek kullan�ml�k g�z damlas�, ��zelti Steril
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
1 ml ��zelti 1,315 mg deksametazon sodyum fosfat i�erir (1 mg deksametazona e�de�er olarak).
Her tek dozluk kap (0,5 ml) 0,526 mg deksametazon sodyum fosfat i�erir (0,4mg deksametazona e�de�er).
Yard�mc� maddeler
Yard�mc� maddeler i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
G�z damlas�.
Berrak, renksiz-hafif sar� ��zelti.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Konjunktiva, kornea ve g�z�n �n segmentinin steroidlere cevap veren, enfekte olmayan inflamatuvar ve alerjik durumlar�n�n ve cerrahi sonras� inflamasyonun tedavisinde endikedir.
4.2. Pozoloji ve uygulama �ekli
Pozoloji/uygulama s�kl��� ve s�resi:
Topikal olarak konjunktivaya bir veya iki damla uygulan�r.
Ciddi veya akut inflamasyonda, tedavi ba�lang�c�nda, hasta g�z�n/g�zlerin konjunktival keselerine her 30-60 dakikada bir 1 – 2 damla damlat�l�r.
Tedaviye istenilen cevap al�nd�ktan sonra, uygulamalar�n s�kl���, hasta g�z�n/g�zlerin
konjunktival keselerine her 2 – 4 saatte bir 1 – 2 damla olacak �ekilde azalt�lmal�d�r.
�nflamasyon yeteri kadar kontrol alt�na al�n�yorsa, doz g�nde 3 – 4 kere bir damlaya kadar
azalt�labilir.
E�er 3 – 4 g�n i�inde yeterli cevap al�namazsa, sistemik veya subkonjunktival tedavi
eklenebilir.
Kronik inflamasyonda, doz, hasta g�z�n/g�zlerin konjunktival keselerine her 3-6 saatte bir
veya gerekti�i s�kl�kta, bir veya iki damlad�r.
Alerji veya min�r inflamasyonda, doz istenilen yan�t elde edilene kadar, hasta g�z�n/g�zlerin
konjunktival keselerine her 3-4 saatte bir damlat�lan bir veya iki damlad�r. Tedavinin tamamlanmadan kesilmemesi i�in dikkat edilmelidir.
G�z i�i bas�nc�n�n d�zenli olarak �l��lmesi �nerilir.
Uygulama �ekli:
Ok�ler kullan�m i�indir.
Preparat� uygulamadan �nce ellerinizi y�kay�n�z. Kullan�m s�ras�nda tek dozluk damlal�k ucuna dokunmay�n�z, damlal��� g�ze ya da g�z �evresine de�dirmeyiniz.
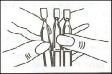
Kullan�lacak olan tek dozluk Dexa-Sine SE di�er tek dozlardan yana do�ru bir �ekme ile ayr�l�r:

Daha sonra �st�ndeki kapa�� d�nd�r�lerek kopar�l�r. Bu i�lemde koparma i�lemini �ekerek yap�lmamal�d�r.
Kapak a��ld�ktan sonra �ok d�zg�n bir a��z ile kar��la��lacakt�r.

Tek dozluk ila� kab� bir elin ba� ve i�aret parmaklar� aras�nda tutularak g�ze yakla�t�r�l�r, ba� hafif�e arkaya e�ilerek kap s�k�lmadan, ancak iki parmak aras�nda hafif bir bas�n�la g�ze damlatma yap�lmal�d�r. Bu i�lem s�ras�nda di�er el ile alt g�z kapa�� a�a�� �ekilmelidir. Kab�n s�k�lmas� ile i�erik g�ze
f��k�rabilir, bu nedenle de kab�n s�k�lmamas�na �ok �zen g�sterilmelidir.
4.3. Kontrendikasyonlar
DEXA-S�NE SE a�a��daki durumlarda kullan�lmamal�d�r:
Etkin madde
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Yaln�zca ok�ler kullan�m i�in
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
DEXA-S�NE SE ile ilgili etkile�im �al��malar� yap�lmam��t�r.
Topikal steroidlerin ve topikal NSA��'lar�n e�zamanl� kullan�m�, kornea iyile�mesi ile ilgili problemlerin ortaya ��kma olas�l���n� artt�rmaktad�r.
Ritonavir ile tedavi edilen hastalarda, deksametazonun plazma konsantrasyonlar� y�kselebilir
(Bkz. B�l�m 4.4).
CYP3A4-inhibit�rleri (ritonavir ve kobisistat dahil) deksametazon klirensini azaltabilir; bu da etkinin artmas�na ve adrenal bez supresyonuna/Cushing sendromuna yol a�abilir. Fayda, sistemik kortikosteroidlerin istenmeyen etkilerine dair risk art���ndan a��r basmad�k�a, bu maddelerin kombinasyonundan ka��n�lmal�d�r. B�yle bir durumda hastalar sistemik kortikosteroidlerin etkileri a��s�ndan izlenmelidir.
Yatk�nl��� olan hastalarda, deksametazonun atropin ya da ba�ka antikolinerjikler i�eren g�z damlalar� ile e� zamanl� kullan�lmas� durumunda intraok�ler bas�n�ta ilave bir art�� olas�l�k d��� b�rak�lamaz.
Birden fazla oftalmik ila� �r�n� kullan�l�yorsa, ila�lar en az 5 dakika ara ile uygulanmal�d�r. G�z merhemleri en son uygulanmal�d�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
Pediyatrik pop�lasyon:
Pediyatrik pop�lasyona ili�kin herhangi bir etkile�im �al��mas� yap�lmam��t�r.
4.6. Gebelik ve laktasyon
Gebelik kategorisi: C�ocuk do�urma potansiyeli bulunan kad�nlar / Do�um kontrol� (Kontrasepsiyon)
�ocuk do�urma potansiyeli bulunan kad�nlarda kullan�m�na ili�kin yeterli veri mevcut de�ildir. �ocuk do�urma potansiyeli olan kad�nlar tedavi s�resince etkili do�um kontrol� uygulamak zorundad�r.
Gebelik d�nemi
Deksametazonun gebe kad�nlarda kullan�m�na ili�kin yeterli veri mevcut de�ildir.
Hayvanlar �zerinde yap�lan �al��malar, gebelik ve/veya embriyonel/fetal geli�im ve/veya do�um ve/veya do�um sonras� geli�im �zerindeki etkiler bak�m�ndan yetersizdir (bkz. B�l�m 5.3). �nsanlara y�nelik potansiyel risk bilinmemektedir.
Gebe kad�nlarda deksametazon kullan�m� ile ilgili yeterli �al��ma yap�lmam��t�r veya �al��malar �ok k�s�tl�d�r. Gebelik s�ras�nda glukokortikoidlerin uzun s�reli veya tekrarl� sistemik kullan�m�, rahim i�i b�y�me gerili�i ve d���k fetal do�um a��rl��� riskinde art�� ve yeti�kinlikte y�ksek tansiyon, vask�ler hastal�k ve ins�lin direnci riskinde y�kselme ile ili�kilendirilmi�tir. Gebeli�in sonunda y�ksek sistemik glukokortikoid dozlar�n�n uygulanmas� da fetal adrenal kortekste atrofi riskini artt�rmaktad�r.
Hayvanlarda yap�lan deneysel �al��malar, oral yar�k olu�umu dahil olmak �zere �reme toksisitesine i�aret etmi�tir (bkz. B�l�m 5.3).
Sistemik maruz kalma, g�zde kullan�m�ndan sonra bile g�z ard� edilemedi�inden, DEXA-S�NE SE'nin gebelikte kullan�lmas� �nerilmez.
Laktasyon d�nemi
Sistemik olarak uygulanan glukokortikoidler anne s�t�ne ge�er ve b�y�me ve endojenik glukokortikoid �retimini bask�layabilir ya da ba�ka advers etkileri olabilir. DEXA-S�NE SE'nin anlaml� miktarlarda olmak �zere anne s�t�ne ge�ip ge�medi�i bilinmemektedir.
Emzirilen bebekler a��s�ndan risk olas�l�k d��� b�rak�lamaz. Emzirmenin �ocuk a��s�ndan faydas� ve tedavinin kad�n a��s�ndan faydas� g�z �n�ne al�narak emzirmeyi b�rakma ya da tedaviyi b�rakma/tedaviden ka��nma karar� verilmelidir.
�reme yetene�i /Fertilite
Sistemik olarak uygulanan glukokortikoidler, hipotalamus ve hipofizdeki hormon salg�s�n�, testisler ve overlerdeki gametogenezi ve dolay�s�yla fertiliteyi etkileyebilir. Bununla birlikte oftalmolojik kullan�mdan sonra deksametazonun fertiliteyi etkileyip etkilemedi�i bilinmemektedir.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
DEXA-S�NE SE'nin ara� ve makine kullan�m� �zerinde bir etkisi yoktur ya da etki ihmal edilebilir d�zeydedir. Di�er herhangi bir g�z damlas�yla oldu�u gibi, ge�ici olarak g�rme bulan�kl��� ya da di�er g�rsel bozukluklar araba ya da makine kullan�m�n� etkileyebilir. �la� kullan�m� s�ras�nda g�rme bulan�kl��� olu�ursa hasta arabay� ya da makineyi kullanmadan �nce g�r�nt� netle�ene kadar beklemelidir.
4.8. �stenmeyen etkiler
G�venlilik profilinin �zeti
Klinik �al��malarda, en yayg�n advers reaksiyon g�zde rahats�zl�kt�r.
DEXA-S�NE SE ile yap�lan klinik �al��malarda a�a��daki advers reaksiyonlar bildirilmi�tir ve bunlar takip eden s�n�fland�rmaya g�re s�n�fland�r�lm��t�r:�ok yayg�n (≥ 1/10); yayg�n (≥ 1/100 ila < 1/10); yayg�n olmayan (≥ 1/1,000 ila < 1/100); seyrek (≥1/10,000 ila < 1/1,000); �ok seyrek (< 1/10,000) ya da bilinmiyor (eldeki verilerden tahmin edilemiyor). Her bir s�kl�k gruplamas� i�inde, advers reaksiyonlar azalan ciddiyete g�re s�ralanmaktad�r.
Sistem Organ S�n�fland�rmas� | Advers etki |
Sinir sistemi hastal�klar� | Yayg�n olmayan: disguzi |
G�z hastal�klar� | Yayg�n: ok�ler rahats�zl�k
Yayg�n olmayan: keratit, konjunktivit, g�z kurumas�, kornea vital boya lekelenmesi mevcut, fotofobi, bulan�k g�rme (bkz. B�l�m 4.4), g�zde ka��nt�, g�zde yabanc� cisim hissi, lakrimasyonda art��, g�zde anormal duyum, g�z kapa�� s�n�r�nda kabuklanma, g�zde tahri�, ok�ler hiperemi |
�ok nadir durumlarda, fosfat g�z damlas� kullan�m�na ba�l� ciddi kornea hasar� olan baz� hastalarda kornea kire�lenmesi vakalar� bildirilmi�tir.
Pazarlama sonras� g�zetimde belirlenmi� ilave advers reaksiyonlar a�a��dakileri kapsamaktad�r. Mevcut verilerden s�kl�k hesaplanamaz.
Sistem Organ S�n�fland�rmas� | MedDRA Tercih Edilen Terim (v.12.1) |
Ba����kl�k sistemi hastal�klar� | Bilinmiyor: a��r� duyarl�l�k |
Endokrin bozukluklar | Bilinmiyor: adrenal yetmezlik, Cushing sendromu, adrenal supresyon (bkz. B�l�m 4.4) |
Sinir sistemi hastal�klar� | Bilinmiyor: ba� d�nmesi, ba� a�r�s� |
G�z hastal�klar� | Bilinmiyor: glokom, �lseratif keratit, intraok�ler bas�n� art���, g�rme keskinli�inde azalma, kornea erozyonu, g�z kapaklar�nda ptoz, g�z a�r�s�, midriazis, katarakt |
Se�ilmi� advers olaylar�n a��klamas�
Topikal oftalmik kortikosteroidlerin uzun s�reli kullan�m�; optik sinir hasar�, g�rme keskinli�inde azalma ve g�rme alan� kusurlar� ve posterior subkaps�ler katarakt olu�umu ile birlikte intraok�ler bas�n�ta art��a neden olabilir (bkz. B�l�m 4.4).
Kortikosteroid bile�eni nedeniyle, kornea veya sklerada incelmeye yol a�an hastal�klarda,
�zellikle uzun tedavilerden sonra perforasyon riski daha y�ksektir (bkz. B�l�m 4.4).
Kortikosteroidler enfeksiyonlara direnci azaltabilir ve bu tip enfeksiyonlar�n olu�umuna yard�mc� olabilir (bkz. B�l�m 4.4).
Nedene y�nelik e�zamanl� tedavi olmaks�z�n, DEXA-S�NE SE ile tedavi s�ras�nda var olan kornea enfeksiyonunda bozulma olabilir ve fungal (Candida albicans) ya da viral enfeksiyon (Herpes simplex keratitis) riskinde art�� olmaktad�r.
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e-posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz a��m� ve tedavisi
Fizyolojik ko�ullar (konjunktiva kesesinin tutma kapasitesi) uygulamada doz a��m�n� engellemektedir. Bu preparat�n �zellikleri nedeniyle, bu �r�nle akut ok�ler doz a��m� durumunda ya da tek bir doz kab�n�n i�eri�inin kazara yutulmas� durumunda ilave toksik etkiler beklenmemektedir.
DEXA-S�NE SE ile topikal doz a��m� durumunda, ila� g�z(ler)den �l�k su ile y�kanarak uzakla�t�r�labilir.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Oftalmolojikler, antiinflamatuvar ila�lar, kortikosteroidler ATC kodu: S01B A01
Deksametazon, DEXA-S�NE SE'de fosfat esteri olarak kullan�lan bir 9-α-floro-11-hidroksi-16- metil-glukokortikoiddir.
Deksametazon sodyum fosfat�n terap�tik kullan�m�, kortizolden 25-30 kat daha kuvvetli olan g��l� anti-enflamatuar etkisine dayanmaktad�r; bununla birlikte sodyum ve su tutulumu, potasyum kayb� ve glukoz metabolizmas�ndaki bozulmalar gibi sistemik yan etkiler, kortizolle kar��la�t�r�ld���nda minimaldir.
Sentetik steroidlerin etki mekanizmas� kortizol�nkine benzer. Spesifik h�cre i�i resept�r proteinlerine ba�lan�rlar. Enflamatuar ve alerjik reaksiyonlar�n bask�lanmas�na yol a�an spesifik
etki mekanizmas� tam olarak bilinmemektedir. Kemotoksik ve imm�nolojik reaksiyonlar i�in �nemli olan spesifik proteinlerin sentezinin inhibe olmas�n�n ve l�kosit ve makrofajlar�n fonksiyonlar�ndaki di�er de�i�ikliklerin bir rol oynad��� g�r�lmektedir. G�z�n topikal steroid tedavisinin, g�z�n �n b�l�mlerindeki, korneadaki ve konjunktivadaki enflamatuar ve alerjik rahats�zl�klar�n tedavisinde etkili oldu�u kan�tlanm��t�r. Deksametazon ve di�er steroidler ameliyat sonras� profilaksi ve enflamasyonun kontrol�nde kullan�lmaktad�r. Bununla birlikte, posterior g�z rahats�zl�klar�n�n tedavisi i�in sistemik steroid uygulamas� gereklidir.
5.2. Farmakokinetik �zellikler
Genel �zellikler
Deksametazon, suda pratik olarak ��z�nmez, susuz etil alkolde k�smen ��z�n�r, metilen klor�r i�inde hafif ��z�n�r. pH de�eri 7-7,5 aras�ndad�r. Deksametazonun suda ��z�n�r anorganik bir esteri olan deksametazon sodyum fosfat 25°C'de suda hidrokortizondan yakla��k �� bin kat fazla ��z�n�r.
Emilim:
Kortikosteroidler g�z�n ak�z humoruna, korneas�na, irisine, siliyer cismine ve retinas�na emilir. Belirli bir miktar� sistemik olarak emilmesine ra�men, y�ksek dozlarda ya da �ocuklarda uzun s�reli kullan�lmas� d���nda sistemik dola��ma kar��an miktarlar� �nemli de�ildir.
Da��l�m:
Y�ksek dozlarda ya da �ocuklarda uzun s�reli kullan�lmas� d���nda sistemik dola��ma kar��an miktarlar� �nemli de�ildir.
Biyotransformasyon:
Kortikosteroidler sistemik olarak emildi�i takdirde v�cutta esas olarak karaci�erde metabolize edilir. Ancak b�breklerde de metabolizasyon s�z konusudur. Bunun yan�nda deney hayvanlar�nda ger�ekle�tirilen �al��malardan g�zde lokal bir degradasyonun ger�ekle�ti�i de bilinmektedir.
Eliminasyon:
�drarla at�l�r.
Di�er steroidlerde oldu�u gibi, deksametazon da oral uygulamadan sonra h�zl� bir �ekilde emilir ve yakla��k 190 dakika sonra biyolojik yar� �mr�ne ula��r. Kortikosteroidlerin metabolizasyonu esasen karaci�erde ve belirli bir oranda b�breklerde ger�ekle�ir; idrarla at�l�rlar.
Tav�an g�z� ile ilgili ara�t�rmalar, deksametazon fosfat�n topikal olarak uygulanmas�ndan sonra etkili lokal doku konsantrasyonlar�na ula��ld���n� g�stermektedir. Di�er yandan permeasyon, uygulama b�lgesindeki doku ko�ullar�ndan etkilenebilir ve enflamasyonlu g�zde ya da abrasyondan sonra belirgin �ekilde artmaktad�r.
Topikal ok�ler instilasyondan sonra deksametazonun ok�ler yararlan�m�, katarakt cerrahisi yap�lan hastalarda de�erlendirilmi�tir. Ak�z humorda maksimum d�zeylere 2 saat sonra ula��lm��t�r. Bu d�zeylerden takip eden azalma i�in yar� �m�r 3 saattir.
Plasenta bariyeri arac�l���yla penetrasyon
T�m kortikoidlerde oldu�u gibi, deksametazon da plasenta bariyerini ge�ebilir. Bu, premat�re do�um riski durumunda pulmoner mat�rasyonun te�vik edilmesi i�in gebe kad�nlarda profilaktik kortikoid uygulamas�n�n temelini olu�turmaktad�r.
Anne s�t�ne ge�i�
Deksametazon i�in veri mevcut de�ildir. K���k miktarlarda glukokortikoid anne s�t�ne ge�mektedir. Normal olarak bebe�in maruziyeti, emziren annede sistemik olarak mevcut miktar�n 1/100'inden d���kt�r. Yine de daha y�ksek dozajlar�n uygulanmas� s�ras�nda ya da uzun s�reli tedavide ablaktasyon �nerilmektedir.
5.3. Klinik �ncesi g�venlilik verileri
Deksametazonun akut toksik potansiyeli ile ilgili konvansiyonel �al��malara dayal� olarak, DEXA-S�NE SE'nin insanlara y�nelik olarak spesifik riskleri belirlenmemi�tir. Tekrarl� deksametazon uygulamas� ile toksisite testleri, tipik glukokortikoid doz a��m� semptomlar�na i�aret etmektedir (�rn., kan serumunda glukoz ve kolesterol d�zeylerinde art��, periferik kanda lenfosit azalmas�, miyelosupresyon, dalak, timus ve adrenal bezde atrofik de�i�iklikler ve ayr�ca kilo kazan�m�nda azalma). Glukokortikoidlerle yap�lan �al��malardan elde edilen sonu�lar, klinik a��dan anlaml� genotoksik �zelliklere dair kan�t sa�lamamaktad�r. T�m�rojenik potansiyelle ilgili uzun s�reli �al��malar mevcut de�ildir.
Fareler, s��anlar, hamsterler, tav�anlar ve k�pekler �zerinde yap�lan �reme toksisitesi �al��malar�nda, deksametazon, yar�k dama�a ve daha d���k bir d�zeyde olmak �zere ba�ka deformitelere yol a�m��t�r. �nsanlarda d���k vaka say�s� nedeniyle, klinik uygulama s�ras�nda olu�abilecek bir risk olas�l�k d��� b�rak�lamaz.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Disodyum edetat
Sodyum klor�r
Sodyum monohidrojen fosfat Sodyum dihidrojen fosfat Saf su.
6.2. Ge�imsizlikler
Bilinen bir ge�imsizli�i yoktur.
6.3. Raf �mr�
36 ay.
Her bir tek dozluk �nite tek kullan�ml�kt�r. G�z damlalar�, kap a��ld�ktan hemen sonra kullan�lmal�d�r. Kulland�ktan sonra arta kalan ��zelti at�lmal�d�r.
6.4. Saklamaya y�nelik �zel tedbirler
25C alt�ndaki oda s�cakl�klar�nda, ���ktan koruyarak ve ambalaj�nda saklay�n�z. Dondurmay�n�z.
6.5. Ambalaj�n niteli�i ve i�eri�i
Bir kutuda; 0,5 ml'lik transparan LDPE flakon, PET/Aluminyum/LDPE folyo ile paketlenmi� 5'er flakon i�eren toplam 10 adet flakon bulunmaktad�r.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi at�klar�n kontrol� y�netmeli�i” ve “Ambalaj At�klar�n�n Konrol� Y�netmelikleri”ne uygun olarak imha edilmelidir.
 Parkinson Hastal���
Hastal�k ilk kez 1817 de �ngiliz doktor James Parkinson taraf�ndan tan�mlanm�� ve Dr. Parkinson hastal��� “sallay�c� fel�” olarak kaleme alm��.
Parkinson Hastal���
Hastal�k ilk kez 1817 de �ngiliz doktor James Parkinson taraf�ndan tan�mlanm�� ve Dr. Parkinson hastal��� “sallay�c� fel�” olarak kaleme alm��. |
 �izofrenlik
�izofrenli�in psikiatrik te�hisi hakk�nda �ok fazla anla�mazl�k vard�r. Bu
sayfadaki bilgiler, �izofrenli�in te�hisi, nedenleri ve tedavisi hakk�ndaki fakl� teoriler
hakk�nda bilgi verecektir.
�izofrenlik
�izofrenli�in psikiatrik te�hisi hakk�nda �ok fazla anla�mazl�k vard�r. Bu
sayfadaki bilgiler, �izofrenli�in te�hisi, nedenleri ve tedavisi hakk�ndaki fakl� teoriler
hakk�nda bilgi verecektir. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| DEKORT | 8699525010186 | 59.10TL |
| DEKSALON | 8699550010151 | |
| DEKSAMET | 8699788570014 | |
| DEKSAMETAZON-PF | 8699606756873 | 26.42TL |
| DEKSINJECT | 8681176314133 | 28.17TL |
| Di�er E�de�er �la�lar |
 |
HIV ve Aids HIV, Human Immunodeficiency Virus’d�r (�nsanlarda Ba����kl�k Sistemini Bozan Vir�sd�r). Bu vir�s AIDS hastal���na sebep olur. |
 |
Artrit Artrit, olduk�a yayg�n bir hastal�kt�r ancak iyi anla��lamam��t�r. Asl�nda �artrit� tek bir hastal���n ad� de�ildir; eklem a�r�s� veya eklem hastal�klar�n� adland�rman�n gayri resmi yoludur. |
 |
Mesane Kanseri Mesane kanseri her zaman mukozada ba�lar. Erken safhalarda bu tabakada s�n�rl� kal�r ve h�cre i�indeki karsinom olarak nitelendirilir. |
�LA� GENEL B�LG�LER�
Keymen �la� San. Ve T�c. Ltd. �ti.
| Sat�� Fiyat� | 113.62 TL [ 1 Dec 2025 ] |
| �nceki Sat�� Fiyat� | 113.62 TL [ 24 Nov 2025 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699839611444 |
| Etkin Madde | Deksametazon |
| �thal ( ref. �lke : Almanya ) ve Be�eri bir ila�d�r. |