DIANEFROL 4 %1.36 gl�koz i�eren PERITON diyaliz ��zeltisi(2500ml CIFT torba MINI KAPAK ILE) K�sa �r�n Bilgisi
{ Peritonal Diyaliz Sol�syonu }
1. BE�ER� TIBB� �R�N�N ADI
D�ANEFROL 4 % 3.86 glukoz i�eren periton diyaliz ��zeltisi Steril
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Glukoz anhidroz 38,6 g/L (42,5 g/L Glukoz monohidrat) Sodyum klor�r 5,38 g/L
Sodyum laktat 4,48 g/L Kalsiyum klor�r, 2H2O 0,184 g/L Magnezyum klor�r, 6H2O 0,051 g/L
Elektrolit bile�imi:
Sodyum: 132 mmol/litre (132 mEq/litre)
Kalsiyum: 1,25 mmol/litre (2,5 mEq/litre)
Magnezyum: 0,25 mmol/litre (0,5 mEq/litre)
Laktat: 40 mmol/litre (40 mEq/litre)
Klor�r: 95 mmol/litre (95 mEq/litre)
Ozmolarite: 483 mOsm/litre 25°C s�cakl�ktaki pH: 5,5
Yard�mc� maddeler
Yard�mc� maddeler i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Renksiz, berrak periton diyalizi ��zeltisi.
Mini kapa�� ambalaj�ndan al�n�z.
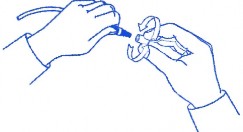
Ara setin u� k�sm�n� a�a��ya do�ru pozisyonda tutunuz. Mini kapa�� dikkatlice kavray�p elinizle saat y�n�nde s�karakiyicesabitlenene kadar ara seti �zerine (�ekle
bak�n�z) derhal yerle�tiriniz. Not: Mini kapa�� �ok s�kmay�n�z.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
D�ANEFROL 4 periton diyalizinin gerekli oldu�u �u durumlarda endikedir:
Akut ve kronik b�brek yetmezli�i;
4.2. Pozoloji ve uygulama �ekli
Pozoloji / Uygulama s�kl��� ve s�resi:Tedavi �ekli, s�kl���, kullan�lacak ��zeltinin hacmi, kar�n bo�lu�unda kalaca�� s�re ve toplam diyaliz s�resi hastan�n doktoru taraf�ndan kararla�t�r�l�r.
18 ya� alt� hastalarda her bir de�i�imde 800-1400 ml/m² (maksimum 2000 ml) dolum hacmi �nerilir. 2 ya� alt� hastalarda her bir de�i�imde 500-1000 ml/m² dolum hacmi �nerilir.
Hastan�n v�cut a��rl��� ideal kuru a��rl��a yakla�t�k�a, d���k konsantrasyonlardaki
D�ANEFROL 4'lerin tercih edilmesi �nerilir.
�iddetli dehidratasyon ve hipovolemi tehlikesiyle kar��la�mamak ve protein kayb�n� olabildi�ince azaltmak amac�yla, her bir de�i�imde kullan�lacak diyaliz s�v�s�n�n ozmolaritesinin, hastan�n gereksinimine yan�t veren en d���k ozmolariteye sahip olacak �ekilde se�ilmesi �nerilebilir.
Uygulama �ekli:
�lac� kullanma ve uygulama �ncesi al�nmas� gereken �nlemler
D�ANEFROL 4 yaln�zca periton i�ine uygulama i�indir; intraven�z yoldan kullan�lmaz.
4.3. Kontrendikasyonlar
D�ANEFROL 4, �r�n i�eri�indeki etkin maddelere ya da 6.1 b�l�m�nde listelenen
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Periton diyalizi �u durumlarda dikkatle uygulanmal�d�r:
�yile�me tamamlanana kadar cerrahi giri�imler, konjenital anomaliler ya da travma sonucu periton membran� ve diyafram�n b�t�nl���n�n bozulmas�, abdominal t�m�r, kar�n duvar�n�n enfeksiyonu, herniler, fekal fist�l, kolostomi veya ileostomi, s�k divertik�l iltihab� episodlar�, iflamatuvar ya da iskemik barsak hastal���, b�y�k polikistik b�breklerin olmas� ya da kar�n duvar�, kar�n y�zeyi ya da kar�n bo�lu�unun b�t�nl���n� bozan bir ba�ka rahats�zl���n bulundu�u abdominal durumlar.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
D�ANEFROL 4 ile di�er t�bbi �r�nlerin etkile�imini ara�t�ran bir �al��ma bulunmamaktad�r. Diyaliz i�lemi s�ras�nda, diyalizle uzakla�t�r�lan di�er ila�lar�n kan konsantrasyonlar� azalabilir.
Kardiyak glikozitleri kullanan hastalarda plazmadaki potasyum, kalsiyum ve magnezyum seviyeleri dijital intoksikasyonu riskine kar�� dikkatle izlenmelidir.
4.6. Gebelik ve laktasyon
:Gebelik Kategorisi: C
�ocuk do�urma potansiyeli bulunan kad�nlar / Do�um kontrol� (kontrasepsiyon) D�ANEFROL 4'�n �ocuk do�urma potansiyeli bulunan kad�nlarda kullan�m� ve do�um kontrol� �zerindeki etkilerine ili�kin veri yoktur. D�ANEFROL 4 kullan�l�rken herhangi bir do�um kontrol y�nteminin kullan�lmas�n�n gerekli olup olmad���na ili�kin bir �al��ma yap�lmam��t�r.
Gebelik d�nemi
D�ANEFROL 4'�n gebe kad�nlarda kullan�m�na ili�kin yeterli veri mevcut de�ildir.
Hayvanlar �zerinde yap�lan �al��malar, gebelik/ve-veya/embriyonal/fetal geli�im/ve- veya/do�um/ve-veya/do�um sonras� geli�im �zerindeki etkiler bak�m�ndan yetersizdir (bkz. k�s�m 5.3). �nsanlara y�nelik potansiyel risk bilinmemektedir. Hastan�n ba�ka bir diyaliz y�ntemi ile tedavi edilemedi�i durumlar d���nda gebelerde kullan�lmamal�d�r.
D�ANEFROL 4 doktor taraf�ndan gerekli g�r�lmedi�i s�rece gebe kad�nlarda kullan�lmamal�d�r. Gebe kad�nlara verilirken tedbirli olunmal�d�r.
Gebelik d�neminde periton diyalizi y�ntemi tercih edilecekse, elde edilecek faydalar, olas� komplikasyonlarla bir arada de�erlendirildikten sonra tedaviye karar verilmelidir.
Laktasyon d�nemi
Emziren kad�nlarda D�ANEFROL 4 kullan�m� ile ilgili deneyimler yeterli de�ildir. D�ANEFROL 4 re�etelemeden �nce emzirmenin durdurulup durdurulmayaca��na tedaviyi d�zenleyen hekim taraf�ndan karar verilmelidir.
�reme yetene�i / fertilite
D�ANEFROL 4'�n �reme yetene�i / fertilite �zerindeki etkisini ara�t�ran bir �al��ma bulunmamaktad�r.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
Periton diyalizi tedavisi g�ren Son D�nem B�brek Yetmezlikli (SDBY) hastalarda, ara� ve makine kullan�m�n� etkileyebilecek istenmeyen etkiler g�r�lebilir (halsizlik, hipovolemi gibi).
4.8. �stenmeyen etkiler
Bu b�l�mdeki advers etkiler, D�ANEFROL 4 ile veya periton diyalizi prosed�r�n�n uygulanmas�yla ba�lant�l� olarak sunulmaktad�r.
Klinik �al��malar ve pazarlama sonras� deneyim s�ras�nda hastalarda bildirilen advers etkiler a�a��da s�ralanm��t�r. Bildirilen advers ila� reaksiyonlar�n�n s�kl�k s�n�fland�rmas� �u �ekildedir: �ok yayg�n (≥1/10); yayg�n (≥1/100 ila <1/10); yayg�n olmayan (≥1/1.000 ila <1/100); seyrek (≥1/10.000 ila <1/1.000), �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Metabolizma ve beslenme hastal�klar�
Bilinmiyor: Hipokalemi, s�v� retansiyonu, hipervolemi, hipovolemi, hiponatremi, dehidratasyon, hipokloremi.
Vask�ler hastal�klar
Bilinmiyor: Hipertansiyon, hipotansiyon.
Solunum, g���s bozukluklar� ve mediastinal hastal�klar
Bilinmiyor: Dispne.
Gastrointestinal hastal�klar
Bilinmiyor: Enkaps�lan periton sklerozu (EPS), peritonit, peritoneal s�v�da bulan�kl�k, kusma, diyare, bulant�, kab�zl�k, kar�na�r �s�,kar�ndadistansiyon,kar�nda rahats�zl�k hissi.
Deri ve deri alt� doku hastal�klar�
Bilinmiyor: Stevens-Johnson sendromu, �rtiker, d�k�nt� (ka��nt�l�, eritemat�z ve yayg�n d�k�nt� dahil), ka��nt�.
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar�
Bilinmiyor: Miyalji, kas spazmlar�, kas-iskelet a�r�lar�.
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar
Bilinmiyor: Yayg�n �dem, ate�, halsizlik, inf�zyon b�lgesi a�r�s�.
Periton diyalizi s�ras�nda g�r�len di�er prosed�rel istenmeyen reaksiyonlar: Fungal peritonitler, bakteriyel peritonitler, kateterle ili�kili enfeksiyonlar, kateterle ili�kili komplikasyonlar.
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr; e-posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99)
4.9. Doz a��m� ve tedavisi
Doz a��m�n�n potansiyel sonu�lar� aras�nda hipervolemi, hipovolemi, elektrolit bozukluklar� ya da hiperglisemi (diyabetik hastalarda) yer al�r.
Doz a��m�n�n tedavisi:
Hipervolemi durumu hipertonik periton diyalizi ��zeltilerinin kullan�m� ve s�v� k�s�tlamas� ile tedavi edilir.
Hipovolemi durumu dehidratasyonun derecesine g�re oral veya intraven�z s�v� replasman�yla tedavi edilir.
Elektrolit dengesindeki bozulmalar, azalan ya da artan elektrolit kan testleriyle belirlendikten sonra spesifik olarak bozuklu�a y�nelik olarak d�zeltilmelidir. En olas� bozukluk olan hipokalemi durumu potasyumun oral olarak uygulanmas�yla ya da diyaliz ��zeltisine hekim �nerisiyle potasyum klor�r eklenmesiyle tedavi edilir.
Hiperglisemi (diyabetik hastalarda), ins�lin ya da di�er oral olarak kullan�lan ila�lar�n dozunun hekim taraf�ndan d�zenlenen ins�lin �emas�na g�re ayarlanmas�yla tedavi edilebilir.
Ara setin u� k�sm�n� a�a��ya do�ru pozisyonda tutunuz. Mini kapa�� dikkatlice kavray�p elinizle saat y�n�nde s�karakiyicesabitlenene kadar ara seti �zerine (�ekle
bak�n�z) derhal yerle�tiriniz. Not: Mini kapa�� �ok s�kmay�n�z.

5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grubu: Periton diyalizi ��zeltileri ATC kodu: B05D
Periton diyalizi, b�brek yetmezli�i olan hastalarda azot metabolizmas� sonucu olu�arak normalde b�brekler yoluyla at�lan toksik maddelerin v�cuttan uzakla�t�r�lmas�n� sa�layan ve bozulmu� olan asit-baz dengesi yan�nda s�v� ve elektrolit dengesizliklerinin d�zeltilmesine de yard�mc� olan bir y�ntemdir.
membran� boyunca ger�ekle�ir. Bir ka� saatlik bekleme s�resinden sonra, ��zelti toksik maddeler a��s�ndan doygun duruma gelir ve de�i�tirilmesi gerekir. Diyaliz s�v�s�n�n elektrolit yo�unluklar�, bikarbonat �n-maddesi olarak eklenmi� laktat hari�, plazman�n elektrolit konsantrasyonunu normalle�tirmek amac�yla form�le edilmi�tir. Kanda y�ksek konsantrasyonda bulunan azotlu at�k maddeler, periton membran�ndan diyaliz s�v�s�na do�ru ge�erler.
��zeltideki glukoz, ��zeltinin plazmaya g�re hiperozmolar olmas�n� sa�lar ve b�ylece ozmotik bir fark yaratarak, kronik b�brek yetmezlikli hastalarda g�r�len a��r� hidrasyon durumunu d�zeltmek i�in gerekli olan plazmadan, diyaliz ��zeltisine do�ru s�v� �ekilmesi i�lemini kolayla�t�r�r.
5.2. Farmakokinetik �zellikler
Genel �zelliklerPeriton membran� �zerindeki etkisini g�sterebilmesi i�in ��zelti periton bo�lu�una uygulan�r ve hekimin belirledi�i bir bekleme s�resinden sonra geri al�n�r.
Emilim:
��zeltinin bile�imine, hiperozmolar yapmak amac�yla kat�lan glukoz, v�cutta do�al olarak bulunan bir maddedir. Periton diyalizi uygulamas� s�ras�nda glukoz periton membran�ndan absorbe olabilir.
Benzer �ekilde ��zelti i�indeki sodyum, klor�r, laktat, kalsiyum ve magnezyum iyonlar� da v�cutta do�al olarak bulunan maddelerdir ve periton diyalizi uygulamas� s�ras�nda periton membran�ndan absorbe olabilirler.
Da��l�m:
Absorbe olan glukoz, normal beslenmede t�ketilen karbonhidratlar�n ya da ya��n metabolizasyonuyla v�cutta olu�an glukozla ayn� �ekilde da��l�ma u�rar.
Benzer �ekilde ��zelti i�indeki sodyum, klor�r, laktat, kalsiyum ve magnezyum iyonlar� da v�cutta do�al olarak bulunan maddelerdir ve absorbe olduklar�nda v�cutta normalde bulunan bu iyonlar�n fizyolojik da��l�m�na benzer bir da��l�m sergilerler.
Biyotransformasyon:
Absorbe olan glukoz, normal beslenmede t�ketilen karbonhidratlar�n ya da ya��n metabolizasyonuyla v�cutta olu�an glukozla ayn� �ekilde biyotransformasyona u�rar.
Laktat, bikarbonat�n biyolojik prek�rs�r�d�r; v�cutta bikarbonata d�n���r. Di�er elektrolitler olan sodyum, klor�r, kalsiyum ve magnezyum iyonlar� ise herhangi bir biyotransformasyona u�ramazlar.
Eliminasyon:
B�brek yetmezli�i durumunda b�breklerin eliminasyon yetene�i kayboldu�undan, v�cutta biyotransformasyona u�ram�� glukoz periton diyalizi ile uzakla�t�r�l�r.
V�cutta bikarbonata d�n��en laktat ile di�er elektrolitler olan sodyum, klor�r, kalsiyum ve magnezyum iyonlar� b�breklerin eliminasyon yetene�i kayboldu�undan periton diyaliziyle ve di�er b�brek d��� fizyolojik eliminasyon mekanizmalar�yla uzakla�t�r�l�r.
Do�rusall�k / do�rusal olmayan durum:
D�ANEFROL 4'�n bile�imindeki glukoz ve elektrolitlerin periton membran�ndan emilimi, ��zeltinin periton bo�lu�unda kal�� s�resi, hastan�n periton membran�n�n ge�irgenlik �zelli�i, hastan�n kan elektrolit ve glukoz konsantrasyonu gibi bir�ok parametre taraf�ndan belirlendi�inden, do�rudan uygulanan dozla do�rusal bir ili�kiden bahsedilemez.
5.3. Klinik �ncesi g�venlilik verileri
Bu konuda yap�lan herhangi bir �al��ma bulunmamaktad�r.
De�i�im s�ras�nda, Mini kapa�� saat y�n�n�n tersine �evirerek ara seti ba�lant�s�ndan ��kar�n�z.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Sodyum hidroksit ve/veya hidroklorik asit (pH ayarlay�c� olarak) Enjeksiyonluk su
6.2. Ge�imsizlikler
Katk� maddeleri kullan�ld���nda, ge�imsizlikler kontrol edilmelidir.
Potasyumun Eklenmesi
D�ANEFROL 4'de potasyum kullan�lmamaktad�r ��nk� diyaliz tedavisi hiperkalemiyi d�zeltmek i�in kullan�lmaktad�r. Normal serum d�zeyi ya da hipokalemi varsa, potasyum klor�r eklenmesi (4mEq/L konsantrasyona kadar) �iddetli hipokalemiyi �nlemede kullan�l�r. Potasyum klor�r eklenmesi karar�, serum potasyum d�zeylerinin dikkatli de�erlendirilmesi sonucunda doktor taraf�ndan verilmelidir.
6.3. Raf �mr�
24 ay.
D�� ambalaj�ndan ��kar�lan �r�n hemen kullan�lmal�d�r.
6.4. Saklamaya y�nelik �zel tedbirler
25°C'nin alt�ndaki oda s�cakl���nda korunarak saklanmal�d�r.
6.5. Ambalaj�n niteli�i ve i�eri�i
��zelti PVC torba i�inde sunulmaktad�r. Torba, ya uygun bir uygulama setine ba�lanabilecek �ekilde ili�tirilmi� bir port ile ya da dahili bir uygulama seti ve bo� drenaj torbas�na ba�l� olarak sunulmu�tur. Torbada ayr�ca, uygun oldu�u durumlarda ��zeltinin i�ine ila� ekleyebilmek amac�yla ili�tirilmi� lateksten bir enjeksiyon portu da bulunmaktad�r.
Daha sonra torba lineer y�ksek yo�unluklu polietilen koruyucu torba ile kaplanm��t�r.
Tek torbal� olan formlar� 1, 2, 2,5, 5 ve 6 litre, �ift torbal� olan formlar� ise 1, 2 ve 2.5 litre ��zelti i�ermektedir. Tek torbal� 6 litrelik olan form aletli periton diyaliz cihaz seti ile birlikte ve �ift torbal� olan formlar, mini kapakla birlikte kullan�ma sunulmu�tur
Ayr�ca tek ve �ift torbal� ambalajlarda sunulan % 1.36 ve % 2.27 Glukozlu formlar� da bulunmaktad�r.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Uygulamayla ilgili ayr�nt�lar i�in b�l�m 4.2'ye bak�n�z.
S�rekli Ayaktan Periton Diyalizi (SAPD) s�ras�nda torba de�i�im prosed�rleri hastalara �zel e�itimlerle ve Kullan�m Talimat�arac�l���ylaverilmektedir.
��zeltinin kullan�lmayan b�l�m� at�lmal�d�r.
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i“ ve “Ambalaj ve Ambalaj At�klar�n�n Kontrol� Y�netmeli�i” ne uygun olarak imha edilmelidir.
Mini Kapak (Povidon �yotlu):
Tan�m
Bu �r�n periton diyalizi tedavisinde kullan�lan plastik bir kapakt�r ve ara setini
kontaminasyondan korumak �zere povidon-iyot i�erir.
4.3. Kontrendikasyonlar
�yoda kar�� bilinen alerjik reaksiyon �yk�s� varsa bu �r�n� kullanmay�n�z. Daha fazla bilgi i�in
doktorunuza ba�vurunuz.
Uyar�lar
Aseptik teknik kullan�n�z. S�v� yolunun herhangi bir k�sm�nda kontaminasyon olmas� peritonit ile sonu�lanabilir.
Ambalaj� daha �nceden a��lm��, hasar g�rm�� veya lekelenmi�se ya da i� k�s�mda bulunan povidon-iyotlu s�nger kuruysa kullanmay�n�z. �r�n kullan�lm��sa at�n�z.
Oda s�cakl���nda saklay�n�z. A��r� �s�dan koruyunuz.
Bu �r�n tek kullan�ml�kt�r. Tek kullan�ml�k bir �r�n�n yeniden kullan�lmas� veya yeniden i�lemden ge�irilmesi, kontaminasyona ve �r�n�n i�levinin veya yap�sal b�t�nl���n�n zarar g�rmesine neden olabilir.
�ocuklar�n g�remeyece�i, eri�emeyece�i yerlerde ve ambalaj�nda saklay�n�z. Kazara yutulmas� halinde, derhal doktorunuza dan���n�z.
K���k peritoneal diyalizat dolum hacmi olan hastalarda, �zellikle bebek ve �ocuklarda, tiroid fonksiyonunun izlenmesi tavsiye edilmektedir. �yot maruziyetini minimuma indirmek i�in, klinik olarak m�mk�n oldu�unda, bir sonraki dolum d�ng�s�n� ba�latmadan �nce periton bo�lu�undaki s�v� drenaj torbas�na bo�alt�lmal�d�r.
Di�er �reticilerden temin edilebilen pek �ok diyaliz �r�n�, Polifarma periton diyaliz ekipman� veya tek kullan�ml�k �r�nleriyle birlikte kullan�lmas� durumunda bu �r�nlerdeki de�i�kenlik, toleranslar, mekanik kuvvet veya zaman zaman yap�labilecek de�i�iklikler Polifarma'n�n kontrol� d���ndad�r. Bundan dolay� Polifarma, ba�ka �reticilerin diyaliz �r�nlerinin, kendi �r�nleri ile kullan�ld���nda tatmin edici ve g�venli bir �ekilde i�leyece�ini garanti edemez.
Kullan�m Talimat�
Dikkat: Aseptik teknik kullan�n�z.
Doktorunuz taraf�ndan verilen talimatlara uyunuz. Bir y�z maskesi tak�n�z. Ellerinizi dezenfektan �zelli�i olan sabun ile y�kay�p tamamen kurutunuz. Ellerinize antiseptik uygulay�n�z.
Yerel at�k imha k�lavuzlar� do�rultusunda at�n�z.
 Deri Kanseri
Deri kanseri �ok rastlanan bir hastal�kt�r. �� ana t�r� bulunur ;genelde kemirici �lser olarak bilinen bazal h�creli karsinom, yass� h�creli karsinom ve k�t� huylu t�m�r.
Deri Kanseri
Deri kanseri �ok rastlanan bir hastal�kt�r. �� ana t�r� bulunur ;genelde kemirici �lser olarak bilinen bazal h�creli karsinom, yass� h�creli karsinom ve k�t� huylu t�m�r. |
 Mide Kanseri
Mide kanseri genellikle mideyi t�m�yle kaplayan ve mukus �retmekle g�revli h�crelerde ba�lar. Bu kanser tipine adenokarsinom denir.
Mide Kanseri
Mide kanseri genellikle mideyi t�m�yle kaplayan ve mukus �retmekle g�revli h�crelerde ba�lar. Bu kanser tipine adenokarsinom denir. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| BALANCE | 8699684675202 | 537.22TL |
| BIOPERITONAL | 8699788673029 | |
| BIOPERITONEAL | 8699788676013 | |
| CAPD | 8699684671723 | 706.00TL |
| DIA. | 8699556675132 | |
| Di�er E�de�er �la�lar |
 |
Do�um Sonras� Depresyonu Do�um sonras� depresyonu, do�umdan sonra her on kad�ndan biri taraf�ndan tecr�be edilen stresli bir durumdur. |
 |
Ast�m Ast�ml� ki�ilerin akci�erlerindeki hava borular� (bron�lar) hassast�r. Bu ki�iler belirli tetikleyici fakt�rlere maruz kald�klar�nda, hava borular� nefes almalar�n� g��le�tirecek �ekilde daral�r. |
 |
Artrit Artrit, olduk�a yayg�n bir hastal�kt�r ancak iyi anla��lamam��t�r. Asl�nda �artrit� tek bir hastal���n ad� de�ildir; eklem a�r�s� veya eklem hastal�klar�n� adland�rman�n gayri resmi yoludur. |
�LA� GENEL B�LG�LER�
Polifarma �la� San.ve Tic. A.�.
| Geri �deme Kodu | A17048 |
| Sat�� Fiyat� | 512.25 TL [ 1 Dec 2025 ] |
| �nceki Sat�� Fiyat� | 512.25 TL [ 24 Nov 2025 ] |
| Original / Jenerik | Jenerik �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699606675839 |
| Etkin Madde | Peritonal Diyaliz Sol�syonu |
| Yerli ve Be�eri bir ila�d�r. |