DROSMIN 3 mg/20 mg film kaplı tablet Kısa Ürün Bilgisi
{ Drospirenon + Ethinyl Estradiol }
1. BEŞERİ TIBBİ ÜRÜNÜN ADI
DROSMİN 3mg/20 mcg film kaplı tablet
2. KALİTATİF VE KANTİTATİF BİLEŞİM
Etkin madde
Her biri 3 mg drospirenon ve 20 mcg etinilestradiol içeren 24 adet hormon içeren film kaplı tablet ve bunları takip eden 4 adet hormon içermeyen beyaz film kaplı tablet.
Yardımcı maddeler
Hormon içeren tabletler 43,380 mg laktoz monohidrat (sığır kaynaklı) içermektedir. Hormon içermeyen tabletler ise 46,400 mg laktoz monohidrat (sığır kaynaklı) içermektedir.Yardımcı maddeler için 6.1'e bakınız.
3. FARMASÖTİK FORMU
Film kaplı tablet.
Hormon içeren tabletler; Açık pembe renkli, yuvarlak, bikonveks, bir yüzü D2 baskılı film kaplı tabletler. Hormon içermeyen tabletler; Beyaz renkli, yuvarlak, bikonveks, bir yüzü P baskılı film kaplı tabletler.
4. KLİNİK ÖZELLİKLER
4.1. Terapötik endikasyonlar
Gebeliği önleyici etkisinin yanı sıra antimineralokortikoid ve antiandrojenik etkileri sayesinde, hormona bağlı su tutulması ve buna bağlı belirtiler gösteren kadınlarda,
4.2. Pozoloji ve uygulama şekli
Tabletler paketin üstünde gösterildiği sırayla, her gün yaklaşık aynı zamanda bir miktar su ile alınmalıdır. Tablet alımı süreklidir. Birbirini izleyen 28 gün boyunca her gün bir tablet alınır. Bir sonraki pakete önceki kutudaki son tablet alımının ertesi günü başlanır. Çekilme kanaması genellikle hormon içermeyen beyaz film kaplı tablet alımına başlanmasından 2-3 gün sonra başlar ve bir sonraki pakete başlandığında devam ediyor
olabilir.
Kombine oral kontraseptiflerin (KOK) doğru şekilde alındıklarında yılda yaklaşık % 1 kadar başarısızlık oranı mevcuttur. Başarısızlık oranı tablet alımı unutulduğunda veya doğru alınmadığında artabilir.
Uygulama şekli:
Oral kullanım
DROSMİN'e başlangıç:
Bir önceki ay hormonal kontraseptif kullanımı yoksa:
Tabletler normal siklusun ilk günü (kanamanın ilk günü) alınmaya başlanmalıdır. Tablete 2. ile 5. günler arasında başlanması da kabul edilebilir, ancak bu durumda tablet alınmaya başlanmasından itibaren yedi gün boyunca ilave olarak bir bariyer kontrasepsiyon yöntemi kullanılmalıdır.
Diğer bir kombine hormonal kontraseptiften (KOK, vajinal halkadan veya transdermal flaster) geçiş:
Kullanıcı tercihen, bir önceki KOK'un son tabletini (hormon içeren son tablet) aldığı günü izleyen günde DROSMİN'e başlamalıdır. En geç, önceki KOK'un tabletsiz döneminin veya hormon içermeyen tablet döneminin ertesi gününde başlayabilir. Vajinal halka veya transdermal flaster kullanılıyorsa DROSMİN alımına döngü paketindeki son halkanın ya da flasterin çıkartıldığı gün veya en geç yeni uygulamanın yapılması gereken gün başlanmalıdır.
Yalnız progesteron içeren bir yöntemden (minipil, enjeksiyon, implant) ya da progesteron salımlı rahim içi sistemden (RİS) geçiş:
Minipilden herhangi bir günde, (implant veya RİS'in çıkarıldığı gün, enjeksiyonda ise bir sonraki enjeksiyonun yapılması gereken gün) geçiş yapılabilir. Ancak tüm bu koşullarda tablet alımının ilk 7 günü ek bir bariyer yönteminin kullanılması önerilir.
İlk trimester düşüğünden sonra:
Hemen başlanabilir. Bu durumda ek kontraseptif yöntemlere ihtiyaç duyulmaz
Doğumdan ya da ikinci trimester düşüğünden sonra: (Emziren kadınlar için bkz. bölüm 4.6 Gebelik ve Laktasyon)
Emzirmeyen kadınlar, tablet almaya doğumu veya ikinci trimester düşüğünü takip eden 21.-28. günleri arasında başlaması konusunda uyarılmalıdır. Eğer daha geç başlanacaksa tablet kullanımının ilk yedi gününde ek bir bariyer yöntemi önerilir. Ancak daha önce bir cinsel birleşme olduysa, oral kontraseptife başlamadan önce gebelik ekarte edilmeli ya da kullanıcı bir sonraki kanama dönemini beklemelidir.
Tablet alımı unutulduğunda:
Hormon içermeyen beyaz film kaplı tablet alımı unutulduğunda ek tedbire gerek yoktur, ancak hormon içermeyen beyaz film kaplı tablet alımının istem dışı uzamaması için unutulan tablet atılmalıdır. Aşağıdaki öneriler sadece hormon içeren açık pembe renkli film kaplı tabletlerin alınması unutulduğunda uygulanmalıdır:
Eğer kullanıcı aktif tabletini almakta 24 saatten daha az geç kalmışsa, kontraseptif koruyuculuk azalmaz. Hatırlanır hatırlanmaz tablet alınmalı ve bir sonraki tabletler de her zamanki gibi alınmaya devam edilmelidir. Eğer aktif tablet alımında 24 saatten daha fazla gecikme olmuşsa kontraseptif koruyuculuk azalmış olabilir. Bu durumda 2 basit kural uygulanır:
Aktif tablet alımına hiçbir zaman 7 günden fazla ara verilmez (önerilen hormon içermeyen tablet dönemi süresinin 4 gün olduğunu dikkate alınız).
4.3. Kontrendikasyonlar
KOK'lar aşağıdaki koşulların varlığında kullanılmamalıdır ve ilk kez KOK kullanımı sırasında bunlardan herhangi biri ortaya çıkacak olursa, tedavi hemen kesilmelidir.
VTE varlığı veya riski
Venöz tromboembolizm-mevcut VTE (antikoagülanlarla tedavide) veya öyküsü (örn. derin ven trombozu [DVT] veya pulmoner embolizm [PE])
4.4. Özel kullanım uyarıları ve önlemleri
)Uyarılar
Dolaşım bozuklukları ile ilgili advers etkilerin ortaya çıkma riski özellikle 35 yaş üzeri ve sigara içen kadınlarda yüksektir.
Epidemiyolojik çalışmalar, drospirenon içeren kombine oral kontraseptifler (KOK) için VTE riskinin, levonorgesterol içeren KOK'lardan (ikinci jenerasyon olarak bilinen preparatlar) daha fazla olduğunu ve bu riskin desogestrel/gestoden içeren KOK'lar (üçüncü jenerasyon olarak bilinen preparatlar) ile benzer olabileceğini göstermiştir.
Aşağıda belirtilen durum veya risk faktörlerinden herhangi biri varsa, DROSMİN'in uygun olup olmadığı kadın ile tartışılmalıdır.
Bu durumlardan veya risk faktörlerinden herhangi birinin şiddetlenmesi veya ilk defa ortaya çıkması halinde, kadının DROSMİN kullanımının sonlandırılmasının gerekli olup olmadığının belirlenmesi için doktoru ile iletişime geçmesi tavsiye edilmelidir.
Şüpheli veya onaylanmış VTE veya ATE durumunda, KHK kullanımı kesilmelidir. Antikoagülan tedaviye başlandığında, antikoagülan tedavinin (kumarin) teratojenisitesi nedeniyle, yeterli alternatif kontrasepsiyon başlatılmalıdır.
Dolaşım bozuklukları
VTE riski
KHK kullanan kadınlarda VTE riski kullanmayanlara göre artar. Levonorgestrel, norgestimat veya noretisteron içeren ürünler en düşük VTE riski ile ilişkilendirilmiştir. DROSMİN gibi diğer ürünlerde ise bu risk iki katına kadar çıkabilir. En düşük VTE riskine sahip olduğu bilinenlerden farklı bir ürünün kullanılması kararı, ancak kadının , mevcut risk faktörlerinin bu riski nasıl etkilediğini ve VTE riskinin bu ilacın kullanımının ilk yılında KHK'lerle ilişkili VTE riskinin en yüksek olduğunu anladığından emin olduktan sonra alınmalıdır. Ayrıca KHK kullanımına 4 hafta veya daha uzun süre ara verildikten sonra tekrar başlandığında riskin arttığını gösteren bazı kanıtlar vardır.
KHK kullanmayan ve gebe olmayan kadınlarda, 10.000 kişiden yaklaşık 2'si bir yıllık süre içinde VTE geliştirir. Bununla birlikte, herhangi bir kadında altta yatan risk faktörlerine bağlı olarak söz konusu risk çok daha yüksek olabilir (aşağı bakınız).
Drospirenon içeren KHK kullanan 10.000 kadından 9 ila 12'sinin bir yıl içinde VTE geliştireceği tahmin edilmektedir; bu oran levonorgestrel içeren KHK kullanan kadınlarda 6 civarındadır.
Düşük dozlu KHK'ler ile bir yıldaki VTE sayısı, gebelikte veya postpartum dönemde kadınlarda beklenen VTE sayısından düşüktür.
VTE, bu vakaların %1-2'sinde ölümcül olabilir.
Bir yıl içinde her 10.000 kadında görülen VTE vakası sayısı
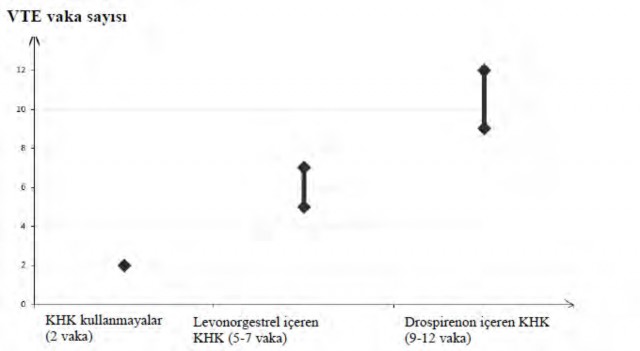
konstraseptifler için göreceli riske bağlı olarak yılda 10.000 kadından 5'i ila 7'si aralığının orta noktası
Son derece nadir olarak, KHK kullanıcılarında diğer kan damarlarında (örn. hepatik, mesenterik, böbrek veya retinal toplardamarlar ve atardamarlar) tromboz meydana geldiği rapor edilmiştir.
VTE risk faktörleri
Venöz tromboembolik komplikasyon riski KHK kullanıcılarında özellikle çoklu risk faktörleri olduğunda, ilave risk faktörleri olan kadınlarda ciddi ölçüde artabilir (bkz. Tablo: VTE Risk faktörleri).
Yüksek venöz tromboz riski oluşturan çoklu risk faktörleri mevcut olan kadında DROSMİN kullanımı kontrendikedir (bkz. bölüm Kontrendikasyonlar). Bir kadın birden fazla risk faktörüne sahipse risk artışı tüm faktörlerin ayrı ayrı toplamından fazla olabilir ve bu durumda toplam VTE riski dikkate alınmalıdır. Fayda ve risk dengesinin negatif olduğu düşünülüyorsa KHK reçete edilmemelidir (bkz. bölüm Kontrendikasyonlar).
Tablo: VTE Risk faktörleri
Risk faktörü: | Açıklama |
Obezite (vücut kitle indeksi 30 kg/m'nin üstündeyse) | Vücut kitle indeksi yükseldiğinde risk ciddi ölçüde artar. Diğer risk faktörleri mevcutsa özellikle dikkate alınmalıdır. |
Uzun süreli hareketsizlik, majör cerrahi müdahale, bacaklara ve pelvise cerrahi müdahale, nörocerrahi, veya majör travma Not: 4 saatten fazla hava yolu seyahati dahil geçici hareketsizlik de özellikle diğer risk faktörleri olan kadınlarda VTE için bir risk faktörü olabilir. | Bu durumlarda ilacı kesmek (cerrahi müdahale durumunda en az 4 hafta) ve tamamen iyileştikten iki hafta sonrasına kadar devam etmemek önerilir. İstenmeyen gebeliği önlemek için başka bir kontrasepsiyon yöntemi kullanılmalıdır. Önceden DROSMİN kesilmemişse, antitrombotik tedavi düşünülmelidir. |
Pozitif aile geçmişi (ebeveynlerden birinde ya da kardeşte erken yaşlarda (örn. 50 yaşından genç) VTE görülmüşse) | Kalıtımsal bir eğilimden şüpheleniliyorsa, KHK kullanımından önce mutlaka bir uzmandan tavsiye alınmalıdır. |
VTE ile ilişkili diğer tıbbi durumlar | Kanser, sistemik lupus eritematoz, hemolitik üremik sendrom ve kronik inflamatuar bağırsak hastalıkları (Crohn hastalığı veya ülseratif kolit) ve orak hücre hastalığı. |
İlerleyen yaş | Özellikle 35 yaş üstü |
Variköz venlerin ve yüzeysel tromboflebitin venöz tromboembolideki olası rolü
konusunda görüş birliği yoktur.
Gebelikte ve özellikle 6 haftalık puerperium periyodunda tromboemboli riskindeki artış dikkate alınmalıdır (bkz. bölüm Gebelik ve laktasyon).
VTE semptomları (DVT ve PE)
Semptomlar olması halinde, kadınlara acil tıbbi yardım almaları ve sağlık çalışanlarını KHK aldıkları konusunda bilgilendirmeleri tavsiye edilmelidir.
DVT semptomları aşağıdakileri kapsayabilir:
− bacakta/ayakta tek taraflı ya da bacaktaki bir damar boyunca şişme;
− bacakta yalnızca ayakta dururken ya da yürürken hissedilebilen ağrı ya da hassasiyet,
− etkilenen bacakta sıcaklık artışı; bacakta ciltte kırmızılık ya da renk değişmesi.
Pulmoner embolizm (PE) semptomları aşağıdakileri kapsayabilir:
− aniden ortaya çıkan, açıklanamayan nefes darlığı ya da hızlı soluma;
− kanın söz konusu olabileceği ani öksürük;
− keskin göğüs ağrısı;
− şiddetli dengesizlik ya da baş dönmesi;
− hızlı veya düzensiz kalp atışı.
Bu semptomlardan bazıları (ör, "nefes darlığı", "öksürük") özgün değildir ve daha yaygın ya da daha az şiddetli olaylar (ör, solunum yolu enfeksiyonları) şeklinde yanlış yorumlanabilir. Vasküler oklüzyona ilişkin diğer belirtiler; bir ekstremitedeki ani ağrı, şişme ya da mavi tonda hafif renk değişikliği olabilir.
Gözde oklüzyon meydana geldiği takdirde, semptomlar ağrısız bulanık görme ile başlayıp görme kaybına kadar ilerleyebilir. Bazen, görme kaybı aniden meydana gelebilir.
ATE riski
Epidemiyolojik çalışmalarda, KHK kullanımı ATE (miyokard enfarktüsü) veya serebrovasküler olay (ör. geçici iskemik atak, inme) riskinde artışla ilişkilendirilmiştir.
ATE ölümcül olabilir.
ATE risk faktörleri
Arteriyel tromboembolik komplikasyon veya serebrovaksüler olay riski, risk faktörleri olan KHK kullanıcılarında artar (bkz. Tablo: ATE Risk faktörleri).
Yüksek arteriyel tromboz riskine maruz bırakan ciddi ya da çoklu ATE risk faktörleri mevcut olan kadında DROSMİN kullanımı kontrendikedir (bkz. bölüm Kontrendikasyonlar). Bir kadında birden fazla risk faktörü varsa, riskteki artışın ayrı ayrı faktörlerin toplamından daha yüksek olması olasılığı vardır. Bu durumda VTE toplam riski dikkate alınmalıdır. Fayda ve risk dengesinin negatif olduğu düşünülüyorsa, KHK reçete edilmemelidir (bkz. bölüm Kontrendikasyonlar).
Tablo: ATE risk faktörleri
Risk faktörü: | Açıklama |
İlerleyen yaş | Özellikle 35 yaş üstü |
Sigara | Kadınlar KHK kullanıyorsa sigara içmemeleri tavsiye edilmelidir. 35 yaşın üzerindeki sigara içmeye devam eden kadınlarda farklı bir kontrasepsiyon yönteminin kullanılması şiddetle tavsiye edilmelidir. |
Hipertansiyon |
|
Obezite (vücut kitle indeksi 30 kg/m'nin üstündeyse) | Vücut kitle indeksi arttığında risk ciddi ölçüde artar Diğer risk faktörleri mevcutsa özellikle dikkate alınmalıdır |
Pozitif aile geçmişi (ebeveynlerden birinde ya da kardeşte erken yaşlarda (örn. 50 yaşından genç) ATE görülmüşse.) | Kalıtımsal bir eğilimden şüpheleniliyorsa, KHK kullanımından önce mutlaka bir uzmandan tavsiye alınmalıdır. |
Migren | KHK kullanımı sırasında migrenin şiddetinde veya sıklığında bir artış (serebrovasküler olay için bir ön belirti olabilir) ilacın hemen kesilmesi için bir neden olabilir. |
Advers vasküler olaylarla ilişkili diğer tıbbi durumlar | Diabetes mellitus, hiperhomosisteinemi, kalp kapak hastalığı ve atriyal fibrilasyon, dislipoproteinemia ve sistemik lupus eritematoz. |
ATE semptomları
Semptomlar görüldüğünde, en kısa sürede tıbbi yardıma başvurmaları ve KHK kullandıklarını sağlık uzmanına bildirmek konusunda kadınlar bilgilendirilmelidir.
Serebrovasküler bir olaya ilişkin semptomlar şunlardır:
− yüzde, bacak veya kolda, özellikle vücudun bir tarafında ani hissizlik ya da
güçsüzlük;
− ani yürümede güçlük, baş dönmesi, denge ya da koordinasyon kaybı;
− ani konfüzyon, konuşma ya da kavramada güçlük;
− bir ya da her iki gözde ani görme güçlüğü; ani yürüme güçlüğü,
− bilinen nedeni olmayan ani, şiddetli veya uzun süren baş ağrısı;
− bilinç kaybı ya da nöbetin eşlik ettiği ya da tek başına bayılma. Geçici belirtiler olayın geçici iskemik atak olduğunu göstermektedir.
Miyokard enfarktüsü (MI) semptomları şunları kapsayabilir:
− göğüs, kol ya da göğüs kemiği altında ağrı, rahatsızlık, basınç, ağırlık,
sıkışma ya da dolgunluk hissi;
− sırt, çene, boğaz, kol ve mideye yayılan rahatsızlık;
− tokluk hissi, hazımsızlık ya da sıkıştırma hissi;
− terleme, bulantı, kusma ya da baş dönmesi;
− aşırı güçsüzlük, anksiyete, nefes darlığı;
− hızlı veya düzensiz kalp atışı.
Tümörler
Servikal kanser için en önemli risk faktörü süregelen human papilloma virüs (HPV) enfeksiyonudur. Bazı epidemiyolojik çalışmalarda uzun süre KOK kullanımının servikal kanser riskinde artışa neden olabileceği bildirilmiştir, ancak bu bulguların KOK kullanımının hangi etkilerine bağlı olabileceği (servikal inceleme, hormonal olmayan kontraseptif kullanımı dahil olmak üzere seksüel davranış) halen tartışılmaktadır.
54 epidemiyolojik çalışmayı kapsayan bir meta-analiz sonucuna göre halen KOK kullanan kadınlarda meme kanseri teşhis edilmesi bağıl riskinde (bağıl risk = 1,24) hafif bir artış olduğu bildirilmiştir. Bu risk artışı KOK kullanımının kesilmesiyle birlikte 10 yıl içinde göreceli olarak ortadan kalkar. Meme kanseri 40 yaşın altındaki kadınlarda seyrek görüldüğünden, meme kanserinin halen KOK kullanan veya geçmişte kullanmış kadınlarda artmış olan tanısı genel meme kanseri riskine göre düşüktür. Bu çalışmalar nedensellik için kanıt sağlamazlar. Bu artmış risk tablosu, KOK kullanıcılarında meme kanserine erken tanı konması ya da KOK'ların biyolojik etkileri sonucu ortaya çıkabileceği gibi, ikisinin birleşimi ile de oluşabilir. Kullanıcılarda saptanan meme kanserleri klinik olarak, hiç kullanmamışlarda görülenden daha az ilerlemiş bulunur.
KOK kullanıcılarında nadir olarak iyi huylu, çok nadiren de habis karaciğer tümörleri gözlemlenmiştir. Çok sınırlı olguda bu tümörler yaşamı tehdit eden batın içi kanamalara yol açmışlardır. KOK kullanan kadınlarda, şiddetli üst batın ağrısı, karaciğerde büyüme ya da batın içi kanama bulguları ortaya çıkması durumunda ayırıcı tanıda bir karaciğer tümörü göz önüne alınmalıdır.
Daha yüksek dozda uygulanan KOK'ların (50 μg etinilestradiol) kullanımı ile endometriyal ve yumurtalık kanseri riski azalır.
Diğer uyarılar
DROSMİN'DEKİ progestin bileşeni, potasyum tutucu özellikleri olan bir aldosteron antagonistidir. Çoğu durumda, potasyum düzeylerinde artış beklenmez. Bununla birlikte, klinik bir çalışmada, hafif veya orta şiddette böbrek yetmezliği olan ve eş zamanlı olarak potasyum tutucu tıbbi ürünleri kullanan bazı hastalarda, serum potasyum seviyeleri drospirenon alımı sırasında anlamlı olmayan hafif bir artış göstermiştir. Bu nedenle, ilk tedavi döngüsünde renal yetmezliği ve önceden tedavi edilmiş üst referans aralığında serum potasyumu olan hastalarda ve özellikle potasyum tutucu ilaçların eş zamanlı kullanımı sırasında serum potasyum düzeyinin kontrol edilmesi önerilmektedir.
Ayrıca bkz. bölüm Diğer tıbbi ürünler ile etkileşimler Hipertrigliseridemisi olan ya da bu şekilde bir aile öyküsüne sahip bulunan kadınlarda,
KOK kullanımıyla pankreatit gelişimi riskinde artış ortaya çıkabilir.
KOK alan kadınların çoğunda kan basıncında hafif artış görüldüğü bildirilmesine rağmen, klinik olarak anlamlı artış enderdir. Drospirenon, antimineralokortikoid etkisinden dolayı diğer KOK'ları kullanan normal tansiyonlu kadınlarda etinilestradiole bağlı gelişen
tansiyon yükselmesini olumlu yönde etkileyebilir. Bununla beraber, KOK kullanımı sırasında ortaya çıkan klinik olarak belirgin bir hipertansiyon gelişiminde, hekimin KOK kullanımını kesmesi ve hipertansiyon tedavisine başlaması gerekir. Antihipertansif tedavi sırasında normal tansiyon değerlerinin elde edilmesi durumunda, KOK kullanımı tekrar gözden geçirilebilir.
Kolestaza bağlı sarılık ve/veya kaşıntı, safra taşı oluşumu, porfiri, sistemik lupus eritematozus, hemolitik üremik sendrom, Sydenham koresi, herpes gestationis, otoskleroza bağlı işitme kaybı gibi durumların gebelik ve KOK kullanımı sırasında ortaya çıktığı ya da kötüleştiği bildirilmişse de, bunların KOK'larla olan ilişkisi kesinlik kazanmamıştır.
Ailesel anjiyoödemi olan kadınlarda eksojen östrojenler anjiyoödem belirtilerinin ortaya çıkmasına veya alevlenmesine yol açabilirler.
Karaciğer fonksiyonlarında görülen akut ve kronik değişiklikler, KOK kullanımının fonksiyon testi değerleri normale dönene dek kesilmesini gerektirebilir. Gebelik sırasında ilk kez ortaya çıkan ya da daha önce seks steroidlerinin kullanıldığı sırada görülmüş olan kolestatik sarılığın nüks etmesi KOK kullanımının kesilmesini gerektirir.
KOK'lar periferik insülin direnci ve glukoz toleransı üzerinde etkili olabiliyorsa da, düşük dozlu (<0,05 mg etinilestradiol) KOK kullanan bir diyabetik hastada tedavi rejiminde değişiklikler yapma gerekliliğini gösteren bir kanıt yoktur. Ancak, KOK kullanan diyabetik kadınlar dikkatle izlenmelidir.
Crohn hastalığı, ülseratif kolit, epilepsi ve endojen depresyonunun kötüleşmesi KOK kullanımı ile ilişkilendirilmiştir.
Depresif ruh hali ve depresyon, hormonal kontraseptif kullanımının iyi bilinen istenmeyen etkileridir (bkz. bölüm İstenmeyen etkiler).
Depresyon ciddi olabilir ve bu durum intihar davranışı ve intihar için iyi bilinen bir risk faktörüdür. Kadınların, duygudurum değişiklikleri ve tedaviye başladıktan kısa bir süre sonra da dahil olmak üzere depresif belirtiler görülmesi durumunda doktorlarına başvurmaları önerilir.
Özellikle kloazma gravidarum öyküsü olan kadınlarda daha belirgin olmak üzere kloazma ortaya çıkabilir. Kloazma eğilimi olan kadınlar KOK kullanımı esnasında güneşe çıkmaktan ya da ultraviyole ışınlarına maruz kalmaktan kaçınmalıdır.
ALT yükselmeleri
Hepatit C virüsü enfeksiyonları (HCV) için tedavi gören hastalarda, ribavirinli veya ribavirinsiz, ombitasvir/paritaprevir/ritonavir ve dasabuvir içeren tıbbi ürünlerle yapılan klinik çalışmalar sırasında, normalin üst sınırının (ULN) 5 katından fazla transaminaz (ALT) yükselmeleri, kombine hormonal kontraseptifler (KHK'lar) gibi etinilestradiol içeren
ilaçlar kullanan kadınlarda önemli ölçüde daha sık meydana gelmiştir (bkz. bölüm Kontrendikasyonlar ve bölüm Diğer tıbbi ürünler ile etkileşimler).
Tıbbi muayene/konsültasyon:
Hastanın oral kontraseptif kullanmaya başlamadan önce ve sonrasında düzenli aralıklarla tıbbi öyküsü (aile öyküsünü de içerecek şekilde) değerlendirilmelidir ve gebelik ekarte edilmelidir. Kan basıncı ölçülmeli ve fiziksel muayene kontrendikasyonlar (bkz. bölüm Kontrendikasyonlar) ile uyarılar (bkz. bölüm Özel kullanım uyarıları ve önlemleri) doğrultusunda gerçekleştirilmelidir. VTE ve ATE semptomları, bilinen risk faktörleri ve şüpheli tromboz durumunda ne yapılacağı, DROSMİN'in diğer KHK'lara kıyasla riski de dahil olmak üzere venöz ve arteriyel tromboz bilgilerine kadının dikkatini çekmek önemlidir.
Ayrıca kadın, kullanma talimatını dikkatle okuması ve yapılan tavsiyelere uyması gerektiği konusunda bilgilendirilmelidir. Bu değerlendirmelerin içeriği ve sıklığı ilgili kılavuzlar doğrultusunda olmalı ve kadına özgü şekilde uyarlanmalıdır.
Kullanıcılar oral kontraseptiflerin HIV enfeksiyonları (AIDS) ve diğer cinsel yolla bulaşan hastalıklara karşı koruyucu olmadığı konusunda bilgilendirilmelidir.
Azalmış etkinlik:
Kombine oral kontraseptiflerin etkinliği hormon içeren açık pembe film kaplı tablet alımı unutulduğunda (bkz. Tablet alımı unutulduğunda), hormon içeren açık pembe film kaplı tablet alımı sırasında mide-bağırsak bozuklukları olması halinde (bkz. Mide-bağırsak bozuklukları durumunda), ya da eş zamanlı ilaç tedavilerinde (bkz. Diğer tıbbi ürünler ile etkileşimler) azalabilir.
Azalmış siklus kontrolü:
Tüm KOK'larda, özellikle kullanımın ilk aylarında düzensiz kanamalar (lekelenme veya ara kanama) gelişebilir. Bu nedenle herhangi bir düzensiz kanamanın araştırılması yaklaşık 3 siklusluk bir adaptasyon süresinden sonra anlamlıdır.
Eğer kanama düzensizliği devam eder veya kanamalar düzenliyken ortaya çıkarsa hormonal olmayan etkenler göz önüne alınmalı ve malignite veya gebeliğin ekarte edilmesi için kürtajın da dahil olabileceği uygun tanısal girişimlerde bulunulmalıdır.
Bazı kadınlarda hormon içermeyen beyaz film kaplı tablet alım döneminde çekilme kanaması oluşmayabilir. Eğer KOK, “Pozoloji ve uygulama şekli†bölümünde belirtilen şekilde kullanıldıysa kadının gebe olması beklenmemektedir. Ancak KOK, ilk gerçekleşmeyen çekilme kanamasından önce kullanım kurallarına uygun kullanılmadıysa ya da çekilme kanaması iki kez gerçekleşmediyse KOK kullanımına devam etmeden önce gebelik ekarte edilmelidir.
Laktoz:
DROSMİN açık pembe renkli film kaplı tabletler, tablet başına 43,380 mg, beyaz film kaplı
tabletler ise tablet başına 46,400 mg laktoz monohidrat içermektedir.
Nadir kalıtımsal galaktoz intoleransı, Lapp laktoz yetmezliği ya da glukoz galaktoz malabsorpsiyon problemi olan hastaların bu ilacı kullanmaması gerekir.
4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri
Not: Olası etkileşmeleri belirlemek amacıyla eşzamanlı kullanılacak ilacın prospektüsüne kullanma talimatına bakılmalıdır.
Diğer tıbbi ürünlerin DROSMİN ile etkileşimleri:
Mikrozomal enzimleri indükleyen ilaçlar ile arasındaki etkileşimler seks hormonu klirensinde artışa neden olabilir, bu durum da ara kanamalara ve/veya kontraseptif başarısızlığa yol açabilirler. Birkaç günlük tedavinin ardından enzim indüksiyonu gözlemlenebilir. En fazla enzim indüksiyonu genellikle birkaç hafta içinde görülür. Enzim indüksiyonu, ilaç tedavisinin kesilmesinin ardından 4 hafta kadar sürebilir.
Bu ilaçlardan herhangi biri ile kısa süreli tedavi edilmekte olan kadınlar, KOK dışında geçici olarak bir bariyer yöntemi kullanmalı ya da başka bir kontrasepsiyon yöntemi seçmelidirler. İlaçlar ile birlikte kullanımları süresince ve tedavinin kesilmesini takiben 28 gün boyunca bariyer yöntemi kullanmalıdırlar. Bu eş zamanlı tedavi uygulanan ve bariyer yönteminin kullanıldığı dönem KOK kutusundaki hormon içeren açı k pembe film kaplı tabletlerin bitiminden sonra da devam ediyorsa, bir sonraki DROSMİN kutusuna hormon içermeyen beyaz film kaplı tabletleri almadan başlanmalıdır.
Karaciğer enzimini indükleyici etkin maddeler ile uzun süreli tedavi gören kadınlarda, başka bir güvenilir, hormonal olmayan kontrasepsiyon yöntemi önerilmektedir.
Literatürde aşağıdaki etkileşimler bildirilmiştir.
KOK klirensini artıran maddeler (enzimlerin uyarılmasıyla KOK etkililiğinin azalması), örn.: Fenitoin, bosentan, ritonavir, nevirapine, efavirenz, barbitüratlar, primidon, karbamazepin, rifampisin ve muhtemelen oksakarbazepin, topiramat, felbamat, griseofulvin ve sarı kantaron (St John's wort) içeren ürünler.
KOK klirensi üzerine değişken etkilere sahip maddeler;
KOK ile birlikte uygulandığında HCV inhibitörleri ile olan kombinasyonlar dahil, birçok HIV proteaz inhibitörü ve nükleozid olmayan ters transkriptaz inhibitörleri kombinasyonu plazma östrojen veya progesteron konsantrasyonlarını azaltabilmekte ya da artırabilmektedir. Bu değişiklikler bazı olgularda klinik açıdan anlamlı olabilir.
Bu nedenle, HIV/HCV ilaç tedavisi ile eş zamanlı kullanım içinpotansiyel etkileşimleri tanımlamak ve bu konuya ilişkin herhangi bir tavsiye edinmek amacıyla kullanma talimatına bakılmalıdır. Herhangi bir süphe olması durumunda, proteaz inhibitörü ya da nükleozid olmayan ters transkriptaz inhibitörleri tedavisi durumunda kadın tarafından ilave bir önleyici kontraseptif metot kullanılmalıdır.
KOK klirensini azaltan maddeler (enzim inhibitörleri)
Enzim inhibitörleri ile potansiyel etkileşimlerin klinik anlamlılığı hala bilinmemektedir.
Kuvvetli düzeyde CYP3A4 inhibitörleri ile eş zamanlı kullanım östrojen veya progesteron veya her ikisinin de plazma konsantrasyonunu artırabilir.
Drospirenon (3 mg/gün)/etinilestradiol (0,02 mg/gün) kombinasyonunun güçlü CYP3A4 inhibitörü ketakonazol ile 10 gün boyunca birlikte alımında drospirenonun ve etinilestradiolün EAA'sı (0-24 saat) sırasıyla 2,7 ve 1,4 kat artmıştır.
60-120 mg/gün etorikoksib dozlarının 0,035 mg etinilestradiol içeren KHK ile eş zamanlı olarak alındığı takdirde etinilestradiolün plazma konsantrasyonlarını sırasıyla 1,4-1,6 kat arttırdığı görülmüştür.
DROSMİN'in diğer tıbbi ürünler üzerine etkisi:
KOK'lar diğer etkin maddelerin metabolizmaları ile etkileşebilmektedir. Buna bağlı olarak plazma ve doku konsantrasyonları artabilir (örn. siklosporin) veya azalabilir (örn. lamotrigin).
Omeprazol, simvastatin veya midazolam kullanan gönüllü kadınlarda yürütülen in vivo etkileşim çalışmasında elde edilen sonuçlara göre, drospirenonun 3 mg'lık dozlarda diğer ilaçların sitokrom P450 enzim aracılı metabolizmalarıyla klinik açıdan anlamlı bir etkileşim sergileme olasılığı bulunmamaktadır.
Klinik çalışmalar etinilestradiolun CYP1A2 substratlarının klirensini azalttığını ve plazma konsantrasyonlarının hafif (ör. teofilin) veya orta düzeyde (ör. tizanidin) artmasına neden olduğunu göstermektedir
Farmakodinamik etkileşimler
Ribavirin ile veya ribavirin olmadan, ombitasvir/paritaprevir/ritonavir ve dasabuvir içeren tıbbi ürünlerle eş zamanlı kullanım ALT yükselme riskini artırabilir (bkz. bölüm Kontrendikasyonlar ve Özel kullanım uyarıları ve önlemleri).
Bu nedenle, DROSMİN kullanıcıları, bu kombinasyon ilaç rejimiyle tedaviye başlamadan önce alternatif bir kontrasepsiyon yöntemine (örneğin, sadece progestajenle kontrasepsiyon veya hormonal olmayan yöntemler) geçmelidir. DROSMİN, bu kombinasyon ilaç rejimi ile tedaviyi tamamladıktan 2 hafta sonra yeniden başlatılabilir.
Böbrek yetmezliği olmayan hastalarda, drospirenon ve ACE inhibitörlerinin ya da NSAID'lerin eş zamanlı kullanımında serum potasyumu üzerinde önemli bir etki görülmemiştir. Ancak, aldesteron antagonistleri ya da potasyum tutucu diüretikler ile DROSMİN'in eş zamanlı kullanımı çalışılmamıştır. Bu durumda, ilk tedavi döngüsü sırasında serum potasyumu test edilmelidir (bkz. bölüm Özel kullanım uyarıları ve önlemleri).
Diğer etkileşmeler:
Laboratuvar testleri:
Kontraseptif steroidlerin kullanılması karaciğer, tiroid, adrenal ve renal fonksiyonların biyokimyasal parametreleri, kortikosteroid bağlayıcı globulin gibi (taşıyıcı) proteinlerin plazma düzeyleri ve lipid/lipoprotein fraksiyonları, karbonhidrat metabolizması, koagülasyon ve fibrinoliz parametreleri gibi bazı laboratuvar testlerinin sonuçlarını etkileyebilir.
Değişiklikler genellikle normal laboratuvar düzeyleri içinde kalmaktadır. Drospirenon hafif derecedeki antimineralokortikoid etkinliğine bağlı olarak, plazma renin etkinliğinde ve plazma aldosteronunda bir artışa neden olur.
Özel popülasyonlara ilişkin ek bilgiler:
Pediyatrik popülasyon: DROSMİN yalnızca menarştan sonra endikedir. Pediyatrik popülasyonda yapılmış etkileşim çalışması bulunmamaktadır.
4.6. Gebelik ve laktasyon
:Gebelik kategorisi X'dir.
Çocuk doğurma potansiyeli bulunan kadınlar / Doğum kontrolü (Kontrasepsiyon):
DROSMİN bir oral kontraseptiftir.
Gebelik dönemi:
DROSMİN film kaplı tabletlerin gebelikte kullanımı kontrendikedir. DROSMİN kullanımı sırasında gebelik meydana gelmesi durumunda kullanım durdurulmalıdır. Ancak, yaygın epidemiyolojik çalışmalar ne gebeliğinden önce KOK kullanmış olan kadınların çocuklarında doğumsal kusur riskinde herhangi bir artışı ne de erken gebeliği süresince yanlışlıkla KOK kullanıldığında oluşan bir teratojenik etkiyi göstermemiştir.
Hayvanlar üzerinde yapılan çalışmalar, gebelik ve emzirme döneminde istenmeyen etkiler olduğunu göstermiştir (bkz. bölüm Klinik öncesi güvenlilik verileri). Bu hayvan verilerine dayanarak, aktif bileşiklerin hormonal etkisine bağlı istenmeyen etkiler göz ardı edilemez. Bununla birlikte, gebelik sırasında KOK‘larla genel deneyim, insanlarda fiili bir istenmeyen etkiye yönelik kanıt ortaya koymamıştır.
DROSMİN'in gebelikte kullanımına ilişkin veriler, DROSMİN'in gebelik, fötus ya da yenidoğanın sağlığı üzerindeki olumsuz etkileri hakkında sonuçlara varılmasına izin veremeyecek kadar kısıtlıdır. Konu hakkında epidemiyolojik veri henüz mevcut değildir.
DROSMİN kullanımına yeniden başlarken postpartum dönem sırasında artan VTE riski dikkate alınmalıdır (bkz. bölüm Pozoloji ve uygulama şekli ve bölüm Özel kullanım uyarıları ve önlemleri).
Laktasyon dönemi:
Laktasyon, anne sütünün miktarında azalmaya ve bileşiminde değişikliğe yol açabileceğinden, KOK'lar tarafından etkilenebilir. Bu yüzden emziren anne bebeğini sütten kesinceye kadar KOK kullanımı genellikle önerilmemelidir. Kontraseptif steroidler ve metabolitleri küçük miktarlarda anne sütüne geçebilir. Bu miktar bebeği etkileyebilir.
Üreme yeteneği / Fertilite:
DROSMİN, bir oral kontraseptiftir. Kullanıldığı sürece fertiliteyi engeller.
4.7. Araç ve makine kullanımı üzerindeki etkiler
Araç ve makine kullanma becerileri üzerinde etkisi ile ilgili herhangi bir çalışma yapılmamıştır. KOK kullanımının araç ve makine kullanma becerileri üzerinde herhangi bir etkisi gözlenmemiştir.
4.8. İstenmeyen etkiler
KOK kullanıcılarında görülen ciddi istenmeyen etkiler için ayrıca bkz. bölüm 4.4 Özel
kullanım uyarıları ve önlemleri.
DROSMİN kullanımı sırasında aşağıdaki advers reaksiyonlar bildirilmiştir:
Advers reaksiyonlar, aşağıda sistem-organ sınıfı (MedDRA) ve sıklık derecesine göre listelenmektedir. Sıklık dereceleri şu şekilde tanımlanmaktadır; çok yaygın (≥1/10), yaygın (≥1/100, <1/10), yaygın olmayan (≥1/1.000, <1/100), seyrek (≥1/10.000 ila <1/1.000), çok seyrek (<1/10.000), bilinmiyor (yalnızca pazarlama sonrası gözetimde tanınan ve sıklığın öngörülemediği ilave advers ilaç reaksiyonları).
Enfeksiyonlar ve enfestasyonlar
Seyrek: Kandidiyaz
Kan ve lenf sistemi hastalıkları
Seyrek: Anemi, trombositemi
Bağışıklık sistemi hastalıkları Seyrek: Alerjik reaksiyon Bilinmiyor: Aşırı duyarlılık
Endokrin hastalıkları
Seyrek: Endokrin bozukluk
Metabolizma ve beslenme hastalıkları
Seyrek: İştah artışı, anoreksi, hiperkalemi, hiponatremi
Psikiyatrik hastalıkları
Yaygın: Duygusal değişkenlik
Yaygın olmayan: Depresyon, gerginlik, somnolans Seyrek: Anorgazmi, uykusuzluk
Sinir sistemi hastalıkları
Yaygın: Baş ağrısı
Yaygın olmayan: Baş dönmesi, parestezi Seyrek: Vertigo, titreme
Göz hastalıkları
Seyrek: Konjuktivit, göz kuruluğu, göz bozukluğu
Kardiyak hastalıkları
Seyrek: Taşikardi
Vasküler hastalıkları
Yaygın olmayan: Migren, Varikoz ven, hipertansiyon
Seyrek: Flebit, vasküler bozukluk, venöz ve arteriyel tromboembolik olaylar, epistaksis, senkop
Gastrointestinal hastalıkları
Yaygın: Bulantı
Yaygın olmayan: Karın ağrısı, kusma, dispepsi, şişkinlik, gastrit, diyare
Seyrek: Abdomende genişleme, gastrointestinal bozukluk, gastrointestinal doluluk, hiatus hernisi, oral kandidiyaz, kabızlık, ağız kuruluğu
Hepato-bilier hastalıkları
Seyrek: Biliyer ağrı, kolesistit
Deri ve deri altı doku hastalıkları
Yaygın olmayan: Akne, pruritus (kaşıntı), döküntü
Seyrek: Kloazma, egzema, alopesi, dermatit akneiform, deride kuruluk, eritema nodozum, hipertrikoz, deri bozukluğu, deride çizgilenme, kontak dermatit, fotosensitif dermatit, deri nodülü
Bilinmiyor: Eritema multiforme
Kas-iskelet bozukluklar, bağ doku ve kemik hastalıkları
Yaygın olmayan: Sırt ağrısı, ekstremitelerde ağrı, kas krampları
Üreme sistemi ve meme bozuklukları
Yaygın: Memelerde ağrı, metroraji*, amenore
Yaygın olmayan: Vajinal kandidiyaz, pelvik ağrı, memelerde büyüme, fibrokistik meme, uterin/genital kanama*, genital akıntı, ateş basması, vajinit, menstrüel bozukluk, dismenore, hipomenore, vajinal kuruluk, şüpheli papanicolaou smear, libido azalması
Seyrek: Disparöni, vulvovajinit, postkoital kanama, geri çekilme kanaması, memede kist, meme hiperplazisi, memede neoplazma, servikal polip, endometrial atrofi, over kisti, uterusda büyüme
Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklar
Yaygın olmayan: Asteni, terlemede artış, ödem (jeneralize ödem, periferik ödem, yüzde ödem)
Seyrek: Halsizlik
Araştırmalar
Yaygın olmayan: Vücut ağırlığında artış Seyrek: Vücut ağırlığında azalma
*Kanama düzensizlikleri genellikle tedavinin sürdürülmesiyle ortadan kalkmaktadır.
Seçilmiş advers reaksiyonların tanımlanması
KOK kullanan kadınlarda Özel kullanım uyarıları ve önlemleri bölümünde daha ayrıntılı olarak ele alınan aşağıdaki ciddi advers olaylar bildirilmiştir:
Venöz tromboembolik bozukluklar;
4.9. Doz aşımı ve tedavisi
DROSMİN hormon içeren açık pembe film kaplı tabletlerin doz aşımı ile ilgili klinik deneyim yoktur. Preklinik çalışmalarda doz aşımına bağlı bildirilen ciddi yan etki yoktur. KOK'ların kullanımı sonucu elde edilen deneyimlere göre DROSMİN film kaplı tabletlerin aktif tabletlerinin aşırı dozda kullanımında görülebilecek belirtiler, bulantı, kusma ve çekilme kanamasıdır. Çekilme kanaması, ilacı yanlışlıkla almaları halinde kız çocuklarında menarştan önce bile görülebilir. Antidotu yoktur ve tedavisi semptomatik olmalıdır.
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Östrojenler ve progestajenler, fiks kombinasyonlar ATC kodu: G03AA12
Yöntem başarısızlığına ilişkin Pearl İndeksi: 0,41 (üst iki yönlü %95 güven limiti: 0,85). Genel Pearl İndeksi (yöntem başarısızlığı + hasta başarısızlığı): 0,80 (üst iki yönlü %95 güven limiti: 1,30).
Drospirenonun kontraseptif etkisi, çeşitli faktörlerin etkileşimine dayanır ve bunlardan en önemlisi ovülasyon inhibisyonu ve endometriyumda değişiklikler şeklinde görülür.
24 günlük bir rejim ve 21 günlük bir rejimde drospirenon 3 mg / etinilestradiol 0,02 mg'ın karşılaştırıldığı 3 sikluslu ovülasyon inhibisyonu çalışmasında, 24 günlük rejim foliküler gelişimin daha fazla bastırılması ile ilişkilendirilmiştir. Tedavinin 3. siklusta kasıtlı olarak uygulanan dozlama hatalarının ardından, 21 günlük rejimdeki kadınların daha büyük bir kısmı 24 günlük rejimi alan kadınlara kıyasla kaçış ovülasyonları da dahil olmak üzere over aktivitesi göstermiştir. 24 günlük rejimi alan kadınların %91,8'inde tedavi sonrası siklusta over aktivitesi, tedavi öncesi seviyelerine dönmüştür.
DROSMİN etinilestradiol ve progesteron drospirenon içeren kombine oral kontraseptiftir.
Terapötik dozajda, drospirenon, antiandrojenik ve hafif antimineralokortikoid özellikler de gösterir. Östrojen, glukokortikoid ve antiglukortikoid aktivitesi yoktur. Bu da drospirenona, doğal hormon progesterona tıpatıp benzeyen bir farmakolojik profil sağlar.
Drospirenon ve etinilestradiol kombinasyonu hafif antimineralokortikoid özelliklerinin hafif bir antimineralokortikoid etkiye yol açtığı yönünde klinik çalışmalardan endikasyonlar mevcuttur.
Drospirenon ve etinilestradiol kombinasyonunun orta derecede akne vulgarisli kadınlardaki etkililiği ve güvenliliğini değerlendirmek üzere iki çok merkezli, çift kör, randomize, plasebo kontrollü çalışma yapılmıştır.
Altı ay tedaviden sonra, plaseboya kıyasla, Drospirenon ve etinilestradiol kombinasyonu enflamatuvar lezyonlarda %15,6 (%33,7'ye karşı %49,3), enflamatuvar olmayan lezyonlarda
%18,5 (%22,1'e karşı %40,6) ve toplam lezyon sayılarında %16,5 (%28,1'e karşı %44,6) gibi istatistiksel olarak anlamlı derecede daha fazla azalma ortaya koymuştur. Buna ilaveten,
%11,8 gibi daha yüksek oranda gönüllü (%6,8'e karşı %18,6), Araştırmacının Statik Global Değerlendirme (ISGA) ölçeğinde ‘net' veya ‘hemen hemen net' bir derecelendirme ortaya koymuştur.
5.2. Farmakokinetik özellikler
DrospirenonGenel özellikler
Emilim:
Oral olarak alınan drospirenon hızla ve hemen hemen tamamen emilir. Tek alımını takiben yaklaşık 1-2 saat sonra yaklaşık 38 ng/ml olan en yüksek etkin madde düzeyine ulaşılır. Biyoyararlılığı yaklaşık % 76-85'dir. Midenin boş olması ile karşılaştırıldığında gıda alımının drospirenonun biyoyararlılığı üzerine etkisi yoktur.
Dağılım:
Oral olarak alındıktan sonra serum drospirenon düzeyleri 31 saatlik bir terminal yarılanma ömrü ile azalır. Drospirenon serum albuminine bağlanır, SHBG'e (seks hormonu bağlayıcı globulin) ya da CBG'ye (kortikoid bağlayıcı globulin) bağlanmaz.
Toplam serum konsantrasyonun yalnızca % 3-5'i bağlanmamış halde bulunur. SHBG'nin etinilestradiole bağlı artışı drospirenonun serum protein bağlanmasını etkilemez. Drospirenon'un ortalama dağılım hacmi 3,7 ± 1,2 l/kg'dır.
Biyotransformasyon:
Oral olarak alınan drospirenon tam olarak metabolizasyona uğrar. Plazmada bulunan ana metabolitler drospirenonun lakton halkasının açılmasıyla oluşan asit formu ve indirgenmenin ve bunu takiben sülfatasyonun oluşturduğu 4,5-dihidro-drospirenon-3- sülfattır. Drospirenon, aynı zamanda CYP3A4 tarafından oksidatif metabolizmaya tabidir.
İn vitro olarak, drospirenon P450 sitokrom enzimleri CYP1A1, CYP2C9, CYP2C19 ve CYP3A4'ü zayıf ila orta düzeyde inhibe edebilir.
Eliminasyon:
Plazmadan klerens hızı yaklaşık 1,5 ± 0,2 ml/dak/kg'dır. Drospirenonun sadece eser miktarı değişmemiş olarak atılır. Metabolitler feçes ve idrar ile 1,2:1,4 oranıyla atılır. Metabolitlerin idrar ve feçes ile atılım yarı ömürleri yaklaşık 40 saattir.
Doğrusallık/Doğrusal olmayan durum:
Drospirenon doğrusal farmakokinetik gösterir.
Kararlı durum koşulları:
Bir tedavi siklusu boyunca, yaklaşık 70 ng/ml'lik serumdaki drospirenonun maksimum kararlı durum konsantrasyonlarına yaklaşık 8 gün tedaviden sonra ulaşılır. Serum drospirenon seviyeleri, terminal yarılanma ömrü ve dozlama aralığı oranının sonucu olarak yaklaşık 3'lük bir faktör ile birikmiştir.
Hastalardaki karakteristik özellikler
Böbrek yetmezliği
Hafif düzeyde böbrek bozukluğu (kreatinin klerensi 50-80 ml/dak) olan kadınlar ile böbrek fonksiyonları normal olan (kreatinin klerensi>80 ml/dak) kadınların kararlı durum serum drospirenon düzeyleri karşılaştırılabilir sonuçlar vermiştir. Orta derecede böbrek bozukluğu (kreatinin klerensi 30-50 ml/dak) olan kadınların serum drospirenon düzeyleri böbrek fonksiyonu normal olan kadınlar ile karşılaştırıldığında %37 daha yüksek bulunmuştur. Drospirenon tedavisi tüm gruplar tarafından iyi tolere edilmiştir.
Drospirenon tedavisi serum
potasyum konsantrasyonu üzerine klinik olarak anlamlı bir etki göstermemiştir.
Karaciğer yetmezliği
Tek dozlu bir çalışmada, oral klirens (CL/F), karaciğer fonksiyonları normal olanlara kıyasla orta derecede karaciğer bozukluğu olan gönüllülerde yaklaşık %50 azalmıştır. Normal hepatik fonksiyona sahip gönüllülerle karşılaştırıldığında orta derecede hepatik bozukluğu olan gönüllülerde gözlenen drospirenon klerensindeki azalma her iki grupta serum potasyum konsantrasyonlarında belirgin bir farklılık yaratmamıştır. Diabet varlığı ve spironolakton tedavisi (hastanın hiperkalemi eğilimini artıran iki durum) de serum potasyum düzeylerini normal sınırın üzerine çıkarmamıştır. Sonuç olarak drospirenonun hafif ve orta derecede karaciğer bozukluğu olan hastalarda (Child-Pugh B) iyi tolere edildiği söylenebilir.
Etnik gruplar: Japon ve beyaz kadınlar arasındaki etnik farklılıkların drospirenon ve etinilestradiolün farmakokinetikleri üzerine klinik olarak anlamlı etkisi olmadığı görülmüştür.
Etinilestradiol Genel özellikler Emilim:
Oral olarak alınan etinilestradiol hızla ve tamamen emilir. En yüksek serum konsantrasyonu olan yaklaşık 33 pg/ml'ye tek oral alımdan sonra 1-2 saat içerisinde ulaşılır. Karaciğerden ilk geçiş etkisi ve presistemik konjugasyon sonucu mutlak biyoyararlılığı yaklaşık %60 kadardır. Etinilestradiol'ün gıda ile birlikte alınmasının incelendiği bireylerin %25 kadarında biyoyararlanımının azaldığı gözlenmiştir.
Dağılım:
Etinilestradiol serumdan iki fazla yaklaşık 24 saatlik bir yarılanma ömrü ile elimine olur. Etinilestradiol serum albuminine yüksek oranda fakat non-spesifik olarak (yaklaşık %98,5) bağlanır ve SHBG ve CBG'nin serum konsantrasyonlarındaki artışı inhibe eder. Dağılım hacmi yaklaşık 5 l/kg olarak bildirilmiştir.
Biyotransformasyon:
Etinilestradiol önemli bağırsak ve hepatik ilk geçiş metabolizmasına tabidir ve esas olarak aromatik hidroksilasyon ile metabolize olur. Etinilestradiol ve oksidatif metabolitler öncelikle glukronid veya sülfat ile konjuge olurlar. Etinilestradiolün metabolik klirens oranı yaklaşık 5 ml/dak/kg'dır.
İn vitro etinilestradiol hem CYP2C19, CYP1A1 ve CYP1A2'nin geri döndürülebilir inhibitörü, hem de CYP3A4/5, CYP2C8, ve CYP2J2'nin mekanizma temelli inhibitörüdür.
Eliminasyon:
Etinilestradiol değişmemiş olarak atılmaz. Yaklaşık 1 günlük yarılanma ömrü olan metabolitler halinde böbrek ve safradan 4:6 oranında atılır. Metabolit atılım yarılanma ömrü yaklaşık 1 gündür.
Doğrusallık/Doğrusal olmayan durum:
Etinilestradiol doğrusal farmakokinetik gösterir.
Kararlı durum koşulları:
Kararlı durum koşullarına tedavi siklusunun ikinci yarısında ulaşılır ve serum etinilestradiol seviyeleri yaklaşık 2,0 – 2,3 gibi bir faktörle çoğalır.
5.3. Klinik öncesi güvenlilik verileri
Laboratuvar hayvanlarında, drospirenon ve etinilestradiolün etkileri bilinen farmakolojik etkiyle ilişkili olanlarla sınırlıdır. Özellikle üreme toksisitesi çalışmaları, hayvanlarda türe özgü olarak değerlendirilen embriyotoksik ve fetotoksik etkiler ortaya çıkarmıştır. Drospirenon ve etinilestradiol kombinasyonu kullanıcılarındaki maruziyetlerin üzerindeki maruziyetlerde, cinsi farklılaşma üzerindeki etkiler sıçan fetüslerinde gözlemlenirken, maymunlarda gözlemlenmemiştir. Çevresel risk değerlendirme çalışmaları, etinilestradiol ve drospirenonun su ortamı için risk teşkil etme potansiyeli olduğunu göstermiştir (bkz. bölüm
6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
).
6. FARMASÖTİK ÖZELLİKLER
6.1. Yardımcı maddelerin listesi
Etkin madde
Her biri 3 mg drospirenon ve 20 mcg etinilestradiol içeren 24 adet hormon içeren film kaplı tablet ve bunları takip eden 4 adet hormon içermeyen beyaz film kaplı tablet.Laktoz monohidrat (sığır kaynaklı) Mısır nişastası
Prejelatinize Nişasta Povidone K-25 Kroskarmelloz sodyum Magnezyum stearat Hipromelloz, Titanyum dioksit, Polietilen glikol, Kırmızı demir oksit
Etkin madde
Her biri 3 mg drospirenon ve 20 mcg etinilestradiol içeren 24 adet hormon içeren film kaplı tablet ve bunları takip eden 4 adet hormon içermeyen beyaz film kaplı tablet.Laktoz monohidrat (sığır kaynaklı) Mısır nişastası
Prejelatinize Nişasta Povidone K-25 Kroskarmelloz sodyum Magnezyum stearat Titanyum dioksit Polietilen glikol
Hidroksipropil metil selüloz E-6
6.2. Geçimsizlikler
Yoktur.
6.3. Raf ömrü
24 ay.
6.4. Saklamaya yönelik özel tedbirler
25°C altındaki oda sıcaklığında saklayınız.
6.5. Ambalajın niteliği ve içeriği
PVC/Aluminyum blister'de etkin madde içeren 24 adet ve etkin madde içermeyen 4 adet film kaplı tablet.
6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
).Kullanılmamış olan ürünler ya da atık materyaller, “Tıbbi Atıkların Kontrolü Yönetmeliği†ve “Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliğiâ€ne uygun olarak
imha edilmelidir.
 Deri Kanseri
Deri kanseri çok rastlanan bir hastalıktır. Üç ana türü bulunur ;genelde kemirici ülser olarak bilinen bazal hücreli karsinom, yassı hücreli karsinom ve kötü huylu tümör.
Deri Kanseri
Deri kanseri çok rastlanan bir hastalıktır. Üç ana türü bulunur ;genelde kemirici ülser olarak bilinen bazal hücreli karsinom, yassı hücreli karsinom ve kötü huylu tümör. |
 HIV ve Aids
HIV, Human Immunodeficiency Virus’dür (İnsanlarda Bağışıklık Sistemini Bozan
Virüsdür). Bu virüs AIDS hastalığına sebep olur.
HIV ve Aids
HIV, Human Immunodeficiency Virus’dür (İnsanlarda Bağışıklık Sistemini Bozan
Virüsdür). Bu virüs AIDS hastalığına sebep olur. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| DROSMAX | 8699828091394 | |
| DROSMIN | 8699828091356 | |
| DROSPERA | 8681026050297 | 364.81TL |
| JERASSI | 8699578092016 | 413.58TL |
| MINAYA | 8681026050051 | |
| Diğer Eşdeğer İlaçlar |
 |
Astım Astımlı kişilerin akciğerlerindeki hava boruları (bronşlar) hassastır. Bu kişiler belirli tetikleyici faktörlere maruz kaldıklarında, hava boruları nefes almalarını güçleştirecek şekilde daralır. |
 |
Doğum Sonrası Depresyonu Doğum sonrası depresyonu, doğumdan sonra her on kadından biri tarafından tecrübe edilen stresli bir durumdur. |
 |
Belsoğukluğu, Chlamydia ve Frengi Belsoğukluğu, bakterilerin sebep olduğu bir enfeksiyondur. Cinsel ilişki yoluyla bulaşır ve dölyatağı boynunda, idrar yollarında, anüste, makatta ve boğazda enfeksyona sebep olabilir. |
İLAÇ GENEL BİLGİLERİ
Koçak Farma İlaç ve Kimya Sanayi A.Ş.
| Satış Fiyatı | 302.06 TL [ 22 Sep 2023 ] |
| Önceki Satış Fiyatı | 302.06 TL [ 15 Sep 2023 ] |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8699828091349 |
| Etkin Madde | Drospirenon + Ethinyl Estradiol |
| Yerli ve Beşeri bir ilaçdır. |