ELIGARD 45 mg enj. ��z. i�in S.C. toz i�eren ��r�nga ve ��z. i�eren ��r�nga K�sa �r�n Bilgisi
{ Loprolid Asetat }
1. BE�ER� TIBB� �R�N�N ADI
ELIGARD45 mg enjeksiyonluk ��zelti i�in s.c. toz i�eren ��r�nga ve ��z�c� i�eren ��r�nga
Steril
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Kullan�ma haz�r her ��r�nga 41,7 mg leuprorelin'e e�de�er miktarda 45 mg leuprorelin asetat
i�erir.
��r�nga A: ELIGARD 45 mg'�n rekonstit�syonu i�in 434 mg steril ��z�c� i�erir. ��r�nga B: 59.2 mg leuprorelin asetat i�erir.
434 mg ��z�c� ile kar��t�r�ld�ktan sonra 45 mg/birim elde edilir.
Yard�mc� maddeler
Yard�mc� maddeler i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Enjeksiyonluk ��zelti i�in s.c. toz i�eren ��r�nga ve ��z�c� i�eren ��r�nga Toz (��r�nga B):
Beyaz ila kirli beyaz renkli toz i�eren kullan�ma haz�r ��r�nga.
��z�c� (��r�nga A):
Berrak, renksiz ila a��k sar� renkli ��z�c� i�eren kullan�ma haz�r ��r�nga.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
ELIGARD,
Hormonal m�dahaleye uygun ilerlemi� prostat kanseri tedavisinde
4.2. Pozoloji ve uygulama �ekli
Eri�kin erkek:
ELIGARD, 6 ayda bir kez derialt� enjeksiyon �eklinde uygulan�r. Enjekte edilen sol�syon, alt� ayl�k bir d�nem boyunca s�rekli leuprorelin asetat sal�m� sa�layan kat� bir depo olu�turur.
Kural olarak, ilerlemi� prostat kanserinin ELIGARD ile tedavisi uzun d�nemli tedaviyi gerektirmektedir ve remisyon ya da d�zelme g�r�ld���nde bu tedavi kesilmemelidir.
ELIGARD, tedaviye verilen yan�t� izlemede uygun deneyime sahip bir sa�l�k uzman�n�n g�zetiminde uygulanmal�d�r.
ELIGARD y�ksek riskli lokalize ve lokal ileri evre prostat kanserinin radyoterapi ile birlikte kombine tedavisinde neoadjuvan veya adjuvan terapi olarak kullan�labilir.
ELIGARD'a verilen yan�t, klinik parametreler yoluyla ve prostat spesifik antijen (PSA) serum d�zeyleri �l��lerek izlenmelidir. Klinik ara�t�rmalarda, testosteron d�zeylerinin or�iektomi uygulanmam�� hastalar�n b�y�k bir b�l�m�nde tedavinin ilk 3 g�n� boyunca artt��� ve daha sonra 3-4 hafta i�inde t�bbi kastrasyon d�zeylerinin alt�na d��t��� g�sterilmi�tir. Eri�ilen kastrasyon d�zeyleri, t�bbi �r�n tedavisinin s�rd�r�ld��� d�nem boyunca korunmu�tur (kastrasyon d�zeyi (50 ng/dl) �zerindeki testosteron y�kselmeleri %1). Hasta yan�t�n�n suboptimal olmas� durumunda, serum testosteron d�zeylerinin kastrasyon d�zeylerine ula�t��� ya da bu d�zeylerde kald��� do�rulanmal�d�r. Etkililik eksikli�inin sebebi hatal� haz�rlama, suland�rma veya uygulama olabilece�i i�in, ��pheli veya bilinen uygulama hatalar� durumunda testosteron seviyeleri incelenmelidir. (Bkz. B�l�m 4.4)
Androjen biyosentez inhibit�rleri veya androjen resept�r inhibit�rleri ile tedaviye uygun, cerrahi kastrasyon yap�lmam��, leuprorelin gibi bir GnRH agonisti alan metastatik kastrasyona diren�li prostat kanseri hastalar�nda GnRH agonisti ile tedaviye devam edilebilir.
Uygulama �ekli:
ELIGARD, sadece bu prosed�rlere a�ina olan sa�l�k profesyonelleri taraf�ndan haz�rlanmal�, suland�r�lmal� ve uygulanmal�d�r (Uygulamadan �nce t�bbi �r�n�n suland�r�lmas�na dair talimatlar i�in Bkz. B�l�m 6.6). E�er �r�n d�zg�n haz�rlanmad�ysa, uygulanmamal�d�r.
Kullan�ma haz�r olarak sunulan iki steril ��r�ngan�n i�eri�i, ELIGARD'�n derialt� enjeksiyon yoluyla uygulanmas�ndan hemen �nce kar��t�r�lmal�d�r.
Deney hayvan� �al��malar�ndan elde edilen verilere g�re intraarteryel ya da intraven�z enjeksiyondan kesinlikle ka��n�lmal�d�r.
Derialt� enjeksiyon yoluyla uygulanan di�er t�bbi �r�nlerde oldu�u gibi, enjeksiyon yeri periyodik olarak de�i�tirilmelidir.
�zel pop�lasyonlara ili�kin ek bilgiler:
B�brek / Karaci�er yetmezli�i:
B�brek veya karaci�er fonksiyon bozuklu�u olan hastalarda klinik ara�t�rma yap�lmam��t�r. Bu nedenle �zel bir uyar� bulunmamaktad�r.
Pediyatrik pop�lasyon:
0-18 ya� aras� �ocuklarda ELIGARD'�n g�venlili�i ve etkilili�i ortaya konmam��t�r (Bkz. B�l�m 4.3). �ocuklara uygulanmamaktad�r. ELIGARD pediatrik hastalarda kontrendikedir. (Bkz. B�l�m 4.3).
Geriyatrik pop�lasyon:
�zel bir uyar� bulunmamaktad�r.
4.3. Kontrendikasyonlar
ELIGARD a�a��da belirtilen durumlarda kontrendikedir:
Leuprorelin asetat'a, di�er GnRH agonistlerine ya da yard�mc� maddelerden herhangi birine kar�� a��r� duyarl�l�k halinde
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Do�ru suland�rma: �r�n�n hatal� suland�r�lmas�na ba�l� olarak klinik etkinlikte eksiklik g�zlenebilir. Haz�rlama ve uygulama i�in talimatlar ve ��pheli veya bilinen uygulama hatalar� durumunda testosteron seviyelerinin incelenmesi i�in bak�n�z (Bkz. B�l�m 4.2 ve B�l�m 6.6)
Androjen deprivasyon tedavisi QT aral���n� uzatabilir.
QT uzamas� ge�mi�i veya risk fakt�r� te�kil eden hastalarda ve QT aral���n� uzatma ihtimali olan t�bbi �r�nleri e�zamanl� kullanan hastalarda (Bkz. B�l�m 4.5) hekimler, ELIGARD 45 mg uygulamas�n� ba�latmadan �nce Torsade de pointes potansiyeli dahil olmak �zere fayda risk oran�n� de�erlendirmelidir.
Kardiyovask�ler hastal�klar: GnRH agonistleri kullan�lan erkeklerde, miyokart enfarkt�s�, ani kardiyak �l�m ve fel� bildirilmi�tir. Bildirilen olas�l�k oranlar� baz al�nd���nda, risk d���k g�r�nmektedir ve prostat kanserli hastalarda tedavi belirlenirken kardiyovask�ler risk fakt�rleri ile birlikte dikkatle de�erlendirilmelidir. GnRH agonistleri alan hastalarda, kardiyovask�ler hastal�k geli�mesini d���nd�ren semptomlar ve i�aretler izlenmelidir ve mevcut klinik tedaviye g�re y�netilmelidir.
Ge�ici testosteron art���: Leuprorelin asetat, di�er GnRH agonistleri gibi, tedavinin ilk haftas� boyunca testosteron, dihidrotestosteron ve asit fosfataz�n serum konsantrasyonlar�nda ge�ici bir art��a neden olmaktad�r. Hastalarda kemik a�r�s�, n�ropati, hemat�ri ya da �reter veya mesane ��k���nda obstr�ksiyonu i�eren yeni semptomlar g�r�lebilir ya da mevcut semptomlarda k�t�le�me ortaya ��kabilir (Bkz. B�l�m 4.8). Tedavi s�rd�r�ld���nde bu semptomlar�n genellikle azald��� g�r�lmektedir.
Leuprorelin tedavisinden 3 g�n �nce ba�lat�lan ve tedavinin ilk iki-�� haftas� boyunca s�rd�r�len uygun bir antiandrojenin ilave olarak uygulanmas� d���n�lmelidir. Bu uygulaman�n, ba�lang��ta serum testosteron d�zeyinde ortaya ��kan art��tan kaynaklanan sekelleri �nledi�i bildirilmi�tir.
Cerrahi kastrasyonu takiben, ELIGARD erkek hastalar�n serum testosteron d�zeylerinde daha fazla d����e yol a�maz.
Kemik dansitesi: T�bbi literat�rde, or�iektomi uygulanan ya da GnRH agonistleri ile tedavi edilen erkek hastalarda kemik dansitesinin azald��� bildirilmi�tir (Bkz. B�l�m 4.8).
Antiandrojen tedavisi, osteoporozdan kaynaklanan k�r�klar�n riskini anlaml� �l��de art�rmaktad�r. Bu konu hakk�nda yaln�zca s�n�rl� veriler mevcuttur. 22 ayl�k farmakolojik
androjen bask�lama tedavisini takiben hastalar�n %5'inde, 5 ila 10 y�ll�k tedaviden sonra hastalar�n %4'�nde osteoporozdan kaynaklanan k�r�klar g�zlenmi�tir. Osteoporozdan kaynaklanan k�r�k riski, genellikle patolojik k�r�klara k�yasla daha y�ksektir.
Uzun s�reli testosteron eksikli�i d���nda, ileri ya�, sigara i�me ve alkoll� i�ki t�ketimi, obezite ve yetersiz egzersiz de osteoporoz geli�imini etkileyebilir.
Pit�iter apopleksi: Pazarlama sonras� izlemlerde, GnRH agonistlerinin uygulanmas�ndan sonra, �o�unlu�u birinci dozdan sonraki 2 hafta i�inde, baz�lar� da birinci saat i�inde meydana gelen seyrek hipofizer apopleksi (hipofiz bezi enfarkt�s�ne sekonder klinik sendrom) olgular� bildirilmi�tir. Bu olgularda, hipofizer apopleksi ani ba� a�r�s�, kusma, g�rmede de�i�imler, oftalmopleji, de�i�en mental durum ve bazen kardiyovask�ler kollaps �eklinde ortaya ��km��t�r. Acil t�bbi m�dahale gerekmektedir.
Hiperglisemi ve diyabet: GnRH analoglar� ile tedavi edilen erkeklerde, hiperglisemi ve diyabet geli�imi riskinde art�� bildirilmi�tir. Hiperglisemi, diabetes mellitus geli�mesine veya diyabetli hastalarda glisemik kontrol�n k�t�le�mesine sebep olabilir. Bir GnRH agonisti ile tedavi edilen hastalarda, kan glukoz de�eri ve/veya glikozile hemoglobin (HbA1c) periyodik olarak izlenmeli ve hiperglisemi veya diyabet i�in hali haz�rda uygulanan tedavi ile birlikte kontrol edilmelidir.
Konv�lsiyonlar: Pazarlama sonras� raporlarda, predispozan fakt�r �yk�s� olan ya da olmayan leuprorelin asetat tedavisi g�ren hastalarda konv�lsiyon oldu�u g�zlenmi�tir. Konv�lsiyonlar g�ncel klinik prati�e g�re y�netilmelidir.
Di�er Durumlar: Fatal komplikasyonlar ile veya fatal komplikasyonlar olmaks�z�n paralizde pay� olan, �reter obstr�ksiyonu ve omurilik kompresyonu vakalar�, GnRH agonistleri ile bildirilmi�tir. Omurilik kompresyonu ya da b�brek fonksiyon bozuklu�u geli�mesi durumunda, bu komplikasyonlar i�in standart tedaviye ba�lanmal�d�r.
�riner sistem obstr�ksiyonu bulunan hastalar�n yan� s�ra, vertebra ve/veya beyin metastazlar� olan hastalar, tedavinin ilk birka� haftas� boyunca yak�ndan izlenmelidir.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
ELIGARD ile farmakokinetik ila�-ila� etkile�imi ara�t�rmalar� yap�lmam��t�r. Leuprorelin asetat ile di�er t�bbi �r�nler aras�nda herhangi bir etkile�ime ili�kin bildirim mevcut de�ildir. Androjen deprivasyon tedavisi QT aral���n� uzatabilece�i i�in, QT aral���n� uzatt��� bilinen t�bbi �r�nler veya Torsade de pointes'i ind�kleyici s�n�f IA (�rn. kinidin, dizopiramid) veya s�n�f III (�rn. amiodaron, sotalol, dofetilid, ibutilid) antiaritmik t�bbi �r�nleri, metadon, moksifloksasin, antipsikotikler, vb. ila�lar ile ELIGARD 45 mg'�n e�zamanl� kullan�m� dikkatlice de�erlendirilmelidir (Bkz. B�l�m 4.4).
�zel pop�lasyonlara ili�kin ek bilgiler:
Herhangi bir etkile�im �al��mas� bulunmamaktad�r.
Pediyatrik pop�lasyon:
Herhangi bir etkile�im �al��mas� bulunmamaktad�r.
4.6. Gebelik ve laktasyon
Genel tavsiye
Gebelik kategorisi: X
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (kontrasepsiyon)
ELIGARD kad�nlarda kontrendike oldu�undan uygulanamaz.
Gebelik d�nemi
ELIGARD kad�nlarda kontrendike oldu�undan uygulanamaz. ELIGARD gebelik d�neminde kontrendikedir.
Risk �zeti
Hayvan �al��malar�ndaki bulgulara ve etki mekanizmas�na dayanarak, ELIGARD gebe bir kad�na uyguland���nda fetal zarara neden olabilir. Gebe kad�nlarda, ila�la ili�kili risk hakk�nda bilgi sa�layacak bir veri mevcut de�ildir. ELIGARD tedavisi ile ortaya ��kan, beklenen hormonal de�i�iklikler gebelik kayb� riskini artt�rmaktad�r. Hayvan geli�im ve �reme �al��malar�nda, s��anlarda gestasyon boyunca leuprorelin asetat uygulanmas�ndan sonra maj�r fetal anomallikler g�zlenmi�tir. Gebe hastalara ve �reme potansiyeli olan kad�nlara fet�s �zerindeki potansiyel risk anlat�lmal�d�r.
Hayvan verileri
Hayvan geli�im ve �reme �al��malar�nda, gestasyon boyunca leuprorelin asetat uygulanmas�ndan sonra maj�r fetal anomallikler g�zlenmi�tir. S��anlarda ve tav�anlarda artan fetal mortalite ve azalan fetal a��rl�k g�zlenmi�tir. Fetal mortalitenin etkileri, bu ilac�n yol a�t��� hormonal seviyedeki de�i�ikliklerin beklenen sonu�lar�d�r.
Laktasyon d�nemi
ELIGARD kad�nlarda kontrendike oldu�undan uygulanamaz.
ELIGARD'�n g�venlili�i ve etkilili�i kad�nlarda tespit edilmemi�tir. ELIGARD'�n anne s�t�nde bulunmas�, emzirilen �ocuk �zerindeki etkileri veya s�t �retimi �zerindeki etkileri hakk�nda bilgi bulunmamaktad�r. Bir�ok ila� anne s�t�ne ge�ti�i i�in ve emzirilen �ocukta ELIGARD'�n ciddi advers reaksiyon potansiyeli sebebiyle, ilac�n anne i�in �nemi g�z �n�nde bulundurarak, emzirmeyi b�rakma veya ilac� b�rakma karar� al�nmal�d�r.
�reme yetene�i/Fertilite
Leuprorelin asetat, do�al olarak ortaya ��kan gonadotropin salg�lat�c� hormon (GnRH)'un sentetik bir nonapeptid agonistidir ve s�rekli olarak uyguland���nda hipofizer gonadotropin sekresyonunu inhibe eder ve erkeklerde testik�ler steroidogenezi bask�lar. Sonu� olarak �reme yetene�i geri d�n��l� olarak etkilenir.
Etki mekanizmas� sebebiyle, ELIGARD �retme potansiyeli olan erkeklerde fertiliteyi olumsuz etkileyebilir.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
ELIGARD'�n ara� ve makine kullanma yetene�i �zerindeki etkilerine ili�kin ara�t�rmalar yap�lmam��t�r.
Tedavinin olas� yan etkileri olan ya da altta yatan hastal�ktan kaynaklanan bitkinlik, ba� d�nmesi ve g�rme bozukluklar�, ara� ve makine kullanma yetene�inin bozulmas�na neden olabilir. Bu nedenle hastalar ara� ve makine kullan�rken dikkatli olmalar� konusunda uyar�lmal�d�r.
4.8. �stenmeyen etkiler
ELIGARD ile g�r�len advers reaksiyonlar, yani baz� hormon d�zeylerindeki art�� ve d����ler, temel olarak leuprorelin asetat�n spesifik farmakolojik etkisine ba�l�d�r. En s�k bildirilen advers reaksiyonlar s�cak basmas�, bulant�, bitkinlik ve yorgunluk ile enjeksiyon yerindeki ge�ici lokal iritasyondur. Hafif veya orta s�cak basmalar� hastalar�n yakla��k %58'inde ortaya ��kmaktad�r.
�lerlemi� prostat karsinomu olan hastalarda ELIGARD ile y�r�t�len klinik �al��malar s�ras�nda a�a��daki advers reaksiyonlar bildirilmi�tir.
A�a��daki advers reaksiyonlar MedDRA sistem-organ s�n�f� ve s�kl���na g�re �u yakla��mla rapor edilmi�tir:
�ok yayg�n (≥1/10); yayg�n (≥1/100 ila <1/10); yayg�n olmayan (≥1/1.000 ila <1/100); seyrek (≥1/10.000 ila <1/1.000); �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor)
ELIGARD ile yap�lan klinik ara�t�rmalarda bildirilen advers reaksiyonlar:
Enfeksiyonlar ve enfestasyonlar
Yayg�n : Nazofarenjit
Yayg�n olmayan : �drar yolu enfeksiyonu, lokal deri enfeksiyonu
Kan ve lenf sistemi hastal�klar�
Yayg�n : Hematolojik de�i�iklikler (k�rm�z� kan h�cresi say�s� ve hematokritte azalma), anemi (hemoglobinde azalma)
Metabolizma ve beslenme hastal�klar�
Yayg�n olmayan : Diabetes mellitusta k�t�le�me
Psikiyatrik hastal�klar
Yayg�n olmayan : Anormal r�yalar, depresyon, azalm�� libido
Sinir sistemi hastal�klar�
Yayg�n olmayan : Sersemlik hali, ba� a�r�s�, hipoestezi, insomnia, tat alma bozuklu�u, koku alma bozuklu�u, vertigo
Seyrek : Anormal istemsiz hareketler
Kardiyak hastal�klar�
Bilinmiyor : QT uzamas� (Bkz. B�l�m 4.4)
Vask�ler hastal�klar
�ok yayg�n : S�cak basmas�
Yayg�n olmayan : Hipertansiyon, hipotansiyon
Seyrek : Senkop, kollaps
Solunum, g���s bozukluklar� ve mediastinal hastal�klar
Yayg�n olmayan : Rinore, dispne
Bilinmiyor : �nterstisyel akci�er hastal���
Gastrointestinal hastal�klar
Yayg�n : Bulant�, diyare, gastroenterit /kolit
Yayg�n olmayan : Konstipasyon, a��z kurulu�u, dispepsi, kusma
Seyrek : �i�kinlik, ge�irme
Deri ve deri alt� doku hastal�klar�
�ok yayg�n : Ekimozlar, eritem
Yayg�n : Pruritus, gece terlemeleri Yayg�n olmayan : Ciltte �slakl�k, terlemede art�� Seyrek : Alopesi, deri d�k�nt�s�
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar�
Yayg�n : Artralji, ekstremite a�r�s�, miyalji, rigor, zay�fl�k Yayg�n olmayan : S�rt a�r�s�, kas kramplar�
B�brek ve idrar yolu hastal�klar�
Yayg�n : Seyrek idrara ��kma, idrar yapmada g��l�k, diz�ri, nokt�ri, olig�ri Yayg�n olmayan : Mesane spazm�, hemat�ri, idrara ��kma s�kl���nda art��, �riner
retansiyon
�reme sistemi ve meme hastal�klar�
Yayg�n : Meme hassasiyeti, testik�ler atrofi, testis a�r�s�, infertilite, meme, hipertrofisi, ereksiyon bozuklu�u, penis boyutunda azalma
Yayg�n olmayan : Jinekomasti, impotans, testik�ler bozukluk
Seyrek : Meme a�r�s�
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar�
�ok yayg�n : Yorgunluk, enjeksiyon yerinde yanma, enjeksiyon yerinde parestezi Yayg�n : Bitkinlik, enjeksiyon yerinde a�r�, enjeksiyon yerinde morarma,
enjeksiyon yerinde i�ne batmalar�,
Yayg�n olmayan : Enjeksiyon yerinde ka��nt�, enjeksiyon yerinde end�rasyon, letarji, a�r�, ate�
Seyrek : Enjeksiyon yerinde �lserasyon
�ok seyrek : Enjeksiyon yerinde nekroz
Ara�t�rmalar
Yayg�n : Kan kreatinin fosfokinaz art���, uzam�� koag�lasyon zaman�
Yayg�n olmayan : Alanin aminotransferazda art��, kan trigliseridlerinde art��, uzam�� protrombin zaman�, kilo art���
Leuprorelin asetat tedavisi ile genellikle ortaya ��kt��� bildirilmi� olan di�er advers reaksiyonlar �unlard�r: periferik �dem, pulmoner embolizm, palpitasyonlar, miyalji, kas zay�fl���, derihasasiyetinde de�i�iklik, titreme, d�k�nt�, amnezi ve g�rme bozukluklar�. Bu s�n�ftaki �r�nlerin uzun s�reli kullan�m� ile kas atrofisi g�zlenmi�tir.
�nceden mevcut hipofiz apopleksisinde infarkt hem k�sa, hem uzun etkili GnRH agonistleri ile tedavi sonras�nda seyrek olarak raporlanm��t�r. Trombositopeni ve l�kopeni de seyrek olarak raporlanan advers reaksiyonlar aras�ndad�r. Glukoz tolerans�nda de�i�iklikler bildirilmi�tir.
GnRH agonist analo�unun uygulanmas�ndan sonra konv�lsiyonlar bildirilmi�tir. (B�l�m 4.4.)
ELIGARD enjeksiyonundan sonra bildirilen lokal advers olaylar, derialt� enjeksiyon yoluyla uygulanan benzer �r�nlerle ili�kili olarak s�kl�kla bildirilen tipik olaylard�r.
Genel olarak, derialt� enjeksiyonu takiben ortaya ��kan bu lokalize advers olaylar hafiftir ve k�sa s�reli olarak tan�mlanm��t�r.
GnRH agonist analo�unun uygulanmas�ndan sonra nadiren anaflaktik/anaflaktoid reaksiyonlar bildirilmi�tir.
Kemik yo�unlu�undaki de�i�iklikler
T�bbi literat�rde, or�iektomi uygulanan ya da GnRH analogu ile tedavi edilen erkek hastalarda kemik dansitesinin azald��� bildirilmi�tir. Leuprorelin ile uzun d�nemli tedavide, osteoporoz belirtilerinde art�� g�zlenebilmesi beklenebilecek bir durumdur. Osteoporoza ba�l� k�r�k riskindeki art�� konusunda (Bkz. B�l�m 4.4)
Hastal���n belirti ve semptomlar�n�n alevlenmesi
Leuprorelin asetat ile tedavi, ilk birka� hafta boyunca hastal���n bulgu ve belirtilerinin alevlenmesine neden olabilmektedir. Vertebra metastazlar� ve/veya �riner obstr�ksiyon ya da hemat�ri gibi sorunlar�n �iddetlenmesi durumunda, zay�fl�k ve/veya alt ekstremitelerde parestezi gibi n�rolojik sorunlar ya da �riner semptomlarda k�t�ye gidi� ortaya ��kabilir.
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e-posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz a��m� ve tedavisi
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grubu: Gonadotropin sal�c� hormon analoglar� ATC kodu: L02AE02.
Leuprorelin asetat, do�al olarak �retilen gonadotropin salg�lat�c� hormon (GnRH)'un sentetik bir nonapeptid agonistidir. S�rekli olarak uyguland���nda hipofizer gonadotropin sekresyonunu inhibe eder ve erkeklerde testik�ler steroidogenezi bask�lar. Bu etki, t�bbi �r�n tedavisinin b�rak�lmas�ndan sonra geri d�n��l�d�r. Ancak bu agonist, do�al hormona k�yasla daha b�y�k bir potense sahiptir ve testosteron d�zeylerinin d�zelmesine kadar ge�en s�re hastadan hastaya de�i�kenlik g�sterebilir.
Leuprorelin asetat�n uygulanmas� ilk olarak dola��mdaki luteinle�tirici hormon (LH) ve folik�l stim�le edici hormon (FSH) d�zeylerinde bir art��la sonu�lan�r ve bu da erkeklerdeki gonadal steroidler, testosteron ve dihidrotestosteron d�zeylerinde ge�ici bir art��a yol a�ar. Leuprorelin asetat�n s�rekli olarak uygulanmas�, LH ve FSH d�zeylerinde bir d����e neden olur. Erkeklerde testosteron kastrasyon e�i�inden (50 ng/dL) daha d���k bir d�zeye inmektedir. Bu d����ler, tedavinin ba�lang�c�ndan sonra �� ila d�rt hafta i�inde ortaya ��kmaktad�r. Alt�nc� aydaki ortalama testosteron d�zeyleri 10,4 ( 0,53) ng/dL olarak saptanm��t�r ve bu, bilateral or�iektomiyi takiben elde edilen d�zeylerle kar��la�t�r�labilir bulunmu�tur. Pivotal klinik ara�t�rmada 45 mg'l�k tam doz leuprorelin uygulanan bir hasta d���nda t�m hastalarda 4 haftada kastrasyon d�zeylerine ula��lm��t�r. Hastalar�n b�y�k bir �o�unlu�unda g�zlenen testosteron d�zeyleri 20 ng/dL'nin alt�nda kalm��t�r, ancak bu d���k d�zeylerin tam yarar� hen�z saptanmam��t�r. PSA d�zeyleri alt� ayda %97 oran�nda d���� g�stermi�tir.
Uzun d�nemli ara�t�rmalar, tedavinin s�rd�r�lmesinin, yedi y�la varan bir d�nem boyunca ve tahminen s�resiz olarak kastrasyon d�zeyinin alt�nda testosteron sa�lad���n� g�stermi�tir.
Klinik �al��ma program� s�ras�nda t�m�r boyutu direkt olarak �l��lmemi�tir, ancak ELIGARD i�in ortalama PSA'da elde edilen %97'lik bir azalma ile dolayl� olarak yararl� bir t�m�r yan�t�n�n var oldu�u saptanm��t�r.
Lokal ileri evre prostat kanseri olan 970 hasta (a��rl�kl� olarak T2c-T4 ve biraz da T1c-T2b patolojik b�lgesel nodal hastal��� olanlar) �zerine yap�lm�� bir faz 3 randomize klinik �al��mada, hastalar�n 483'� radyoterapi ile birlikte k�sa d�nem (6 ay) ve 487'si uzun d�nem (3 y�l) androjen supresyon tedavisi alm��t�r. K�sa d�nem ve uzun d�nem supresyon tedavisi alan hastalar aras�nda GnRH agonisti (triptorelin veya goserelin) ile birlikte e� zamanl� ve adjuvan tedavi sonu�lar� non-inferiorite a��s�ndan kar��la�t�r�lm��t�r. 5-y�ll�k genel mortalite k�sa d�nem ve uzun d�nem hastalar�nda s�ras�yla %19 ve %15,2 olarak saptanm��t�r. �st seviye %95,71 g�ven aral��� (GA) 1,79 veya �ift y�nl� %95,71 GA 1,09-1,85 (non-inferiorite i�in P=0,65) olan Tehlike Oran�=1,42 de�erinde, radyoterapi art� 3 y�ll�k androjen deprivasyonu sa�layan tedavi alanlara k�yasla radyoterapi ile birlikte 6 ayl�k androjen deprivasyonu sa�layan tedaviyi alanlarda daha d���k sa�kal�m sa�lad��� g�sterilmi�tir. Uzun d�nem ve k�sa d�nem tedavi alanlar�n 5-y�ll�k genel sa�kal�m� de�erleri s�ras�yla %84,8 ve %81 olarak saptanm��t�r. QLQ- C30 ile �l��len genel ya�am kalitesi de�erlerinde ise iki grup aras�nda anlaml� fark saptanm��t�r (P=0,37). Sonu�larda lokal ileri evre t�m�rleri olan hastalar a��rl�ktad�r.
Y�ksek riskli lokalize prostat kanserindeki endikasyon kan�tlar� leuprorelin asetat�n da dahil oldu�u GnRH analoglar� ile birlikte radyoterapi yap�lm�� olan �al��malar�n sonu�lar�na dayanmaktad�r. Yay�nlanm�� olan 5 �al��man�n klinik verileri analiz edilmi�tir (EORTC 22863, RTOG 85-31, RTOG 92-02, RTOG 8610, ve D'Amico ve ark.'�., JAMA, 2004). Bu
�al��malar�n hepsinde GnRH analoglar� ile birlikte radyoterapi verilmesinin yarar� g�sterilmi�tir. Yay�nlanm�� olan �al��malarda lokal ileri evre prostat kanserli ve y�ksek riskli lokalize prostat kanserli hastalar i�in endikasyonlarda net ay�rt edici noktalar tespit edilememi�tir.
Klinik veriler, radyoterapiyi takiben 3 y�ll�k androjen deprivasyonu sa�layan tedavinin radyoterapi sonras� 6 ayl�k androjen deprivasyonu sa�layan tedaviye k�yasla daha tercih edilebilir oldu�unu g�stermektedir.
Androjen deprivasyonu sa�layan tedavi �nerilen s�resi t�bbi k�lavuzlarda radyoterapi alan T3- T4 hastalar i�in 2-3 y�l'd�r.
5.2. Farmakokinetik �zellikler
Genel �zelliklerEmilim
�lerlemi� prostat karsinomu hastalar�nda, ilk enjeksiyonu takiben ortalama serum leuprorelin konsantrasyonlar�, enjeksiyondan 4,4 saat sonra 82 ng/mL'ye (C) ula�maktad�r. Her bir enjeksiyonu takiben ortaya ��kan ilk art��tan sonra (her bir dozdan sonraki 3-168 g�nler aras�nda plato faz�), serum konsantrasyonlar� nispeten sabit kalmaktad�r (0,2-2 ng/mL). Tekrarlanan doz uygulamalar�nda birikim oldu�una dair herhangi bir kan�ta saptanmam��t�r.
Da��l�m
Sa�l�kl� erkek g�n�ll�lere uygulanan intraven�z bolus enjeksiyonu takiben leuprorelinin ortalama kararl� durum da��l�m hacmi 27 litre olarak saptanm��t�r. �n vitro olarak insan plazma proteinlerine ba�lanma oran� %43 ila %49 aras�nda de�i�mektedir.
Biyotransformasyon
ELIGARD ile hi�bir ila� metabolizmas� �al��mas� yap�lmam��t�r.
Eliminasyon
Sa�l�kl� erkek g�n�ll�lerde, intraven�z yolla bolus �eklinde uygulanan 1 mg'l�k leuprorelin asetat dozunun ortalama sistemik klerensinin 8,34 L/saat ve �ift kompartmanl� bir model temel al�narak terminal eliminasyon yar�lanma �mr�n�n ise yakla��k 3 saat oldu�u g�sterilmi�tir.
ELIGARD ile eliminasyon ara�t�rmalar� yap�lmam��t�r. Do�rusall�k /do�rusal olmayan durum
Enjekte edilen ELIGARD �r�n�n�n etkin maddesi leuprorelin'in farmakokinetik sal�m profili yava� sal�ml� bir polimer form�lasyonu �zellikleri nedeniyle zaman i�inde do�rusal de�ildir. Her bir ELIGARD dozaj form�lasyonu do�rusal olmayan bir sal�m karakteristi�ine sahiptir.
5.3. Klinik �ncesi g�venlilik verileri
Leuprorelin asetat ile yap�lan klinik �ncesi ara�t�rmalarda, bilinen farmakolojik �zelliklerine dayanarak, her iki cinsiyette de �reme sistemi �zerinde beklenen etkiler elde edilmi�tir. Bu etkilerin tedavinin kesilmesinden ve uygun bir rejenerasyon d�neminden sonra normale d�nd��� g�sterilmi�tir. Leuprorelin asetat teratojenisite g�stermemi�tir. Tav�anlarda, leuprorelin asetat�n �reme sistemi �zerindeki farmakolojik etkileriyle tutarl� olarak, embriyotoksisite/letalite g�zlenmi�tir.
Karsinojenisite ara�t�rmalar� 24 ay s�resince s��anlar ve fareler �zerinde yap�lm��t�r. S��anlarda, 0,6 ila 4 mg/kg/g�n �eklindeki dozlar�n derialt� yoluyla uygulanmas�ndan sonra, hipofiz apopleksisinde dozla ba�lant�l� bir art�� g�zlenmi�tir. Farelerde bu tip bir etki g�zlenmemi�tir.
Leuprorelin asetat ve ilgili alt� ayl�k �r�n ELIGARD, in vitro ve in vivo olarak y�r�t�len bir dizi analizde mutajenik bulunmam��t�r.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
��z�c� (��r�nga A) : 85:15 Poli (DL-laktik-ko-glikolit)
N-metil-2-pirolidon Toz (��r�nga B) : Bulunmamaktad�r
6.2. Ge�imsizlikler
��r�nga B'de bulunan leuprorelin, yaln�zca ��r�nga A'daki ��z�c� ile kar��t�r�lmal� ve di�er t�bbi �r�nlerle kar��t�r�lmamal�d�r.
6.3. Raf �mr�
A��lmam�� ambalaj: 24 ay
�r�n buzdolab�ndan ��kar�ld�ktan sonra orijinal ambalaj�nda, oda s�cakl���nda (25C'nin alt�nda), d�rt haftaya kadar saklanabilir.
Tablalardan birinin a��lmas�n� takiben, toz ve ��z�c� hemen kullan�ma haz�rlanmal� ve hastaya verilmelidir.
Steril ��z�c� ile kullan�ma haz�rlanan �r�n, mikrobiyolojik a��dan ve ��zeltinin viskozitesinin
zamanla artmas� sebebiyle derhal uygulanmal�d�r. Sadece tek kullan�ml�kt�r.
6.4. Saklamaya y�nelik �zel tedbirler
Buzdolab�nda (2C-8C aras�ndaki s�cakl�klarda) ve nemden korumak amac�yla orijinal ambalaj�nda saklay�n�z.
Bu �r�n, enjeksiyondan �nce oda s�cakl���nda olmal�d�r. Kullan�lmadan yakla��k 30 dakika �nce buzdolab�ndan ��kar�lmal�d�r. Buzdolab�ndan ��kar�ld�ktan sonra bu �r�n, orijinal ambalaj�nda oda s�cakl���nda (25ºC'nin alt�nda) d�rt haftaya kadar saklanabilir.
Dondurmay�n�z. Donmu� �r�nleri ��z�p kullanmay�n�z.
6.5. Ambalaj�n niteli�i ve i�eri�i
�ki kullan�ma haz�r ��r�nga vard�r; biri toz i�eren siklik olefin kopolimer ��r�nga (��r�nga B) ve di�eri ��z�c� i�eren polipropilen ��r�nga (��r�nga A). �ki ��r�nga birlikte bir kar���m sistemi meydana getirir.
��r�nga A termoplastik kau�uk pistona sahiptir ve polietilen veya polipropilen Luer-Lock kapakla kapat�lm��t�r. ��r�nga B'nin enjekt�r ucu kab� bromob�til kau�uktan olu�maktad�r ve iki piston ucu klorobutil kau�uktan imal edilmi�tir.
Bir kit, karton kutu i�inde iki adet �s�yla �ekillendirilmi� tabladan olu�maktad�r. Bir tabla, kullan�ma haz�r polipropilen ��r�nga A, b�y�k piston ve nem tutucu po�et i�erir. Di�er tabla,
kullan�ma haz�r siklik olefin kopolimer ��r�nga B, bir adet steril i�ne ve bir adet silikon nem tutucu po�et i�erir.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj ve Ambalaj At�klar�n�n Kontrol� Y�netmelik”lerine uygun olarak imha edilmelidir.
Kullan�ma haz�rlama:
�r�n�, kullan�m�ndan yakla��k 30 dakika �nce buzdolab�ndan ��kararak oda s�cakl���na gelmesini bekleyiniz.
L�tfen ilk olarak hastay� enjeksiyon i�in haz�rlay�n�z, ard�ndan a�a��daki talimatlar� uygulayarak �r�n�n haz�rl���n� yap�n�z. E�er �r�n uygun teknik kullan�larak haz�rlanmad�ysa, �r�n�n hatal� suland�r�lmas� sonucunda do�acak klinik etkinlik eksikli�inden �t�r� �r�n hastaya uygulanmamal�d�r.
Di�er benzer ajanlar gibi, kar��t�rma ve uygulama s�recince eldiven kullan�m� �nerilmektedir.
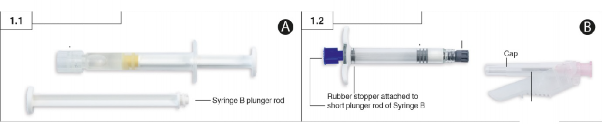
Ad�m 1: Her iki tablay� a��n (folyoyu, k���k bir baloncuk ile belirginle�tirilmi� k��eden y�rt�n) ve i�indekileri (��r�nga A (�ekil 1.1) ve ��r�nga B'yi (�ekil1.2) i�eren iki tabla) temiz bir alana bo�alt�n Nem �ekici torbalar� at�n.
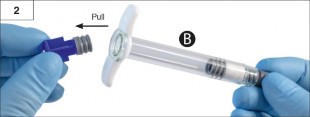
Ad�m 2: ��r�nga B'de (�ekil 2) mavi renkli k�sa piston �ubu�unu, tak�l� gri renkli t�pa ile birlikte �ekin. �ki t�pay� �evirerek a�maya �al��may�n. �ki t�pa da tak�l� iken �r�n� kar��t�rmaya �al��may�n!
Ad�m 3: ��r�nga B beyaz piston �ubu�unu, ��r�nga B'de kalan gri t�paya nazik�e s�k�n (�ekil 3).

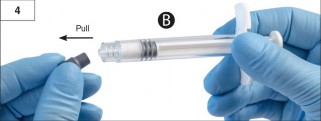
Ad�m 4: ��r�nga B'de gri renkli kau�uk kapa�� ��kar�n ve enjekt�r� b�rak�n (�ekil 4).
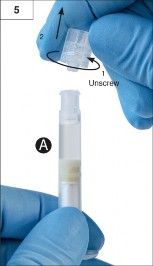
Ad�m 5: S�v� s�zmamas� i�in ��r�nga A'y� dikey konumda tutun ve ��r�nga A'dan �effaf kapa�� �evirerek ��kar�n (�ekil 5).
Ad�m 6: �ki enjekt�r� i�eri do�ru bast�rarak ve sabitlenene kadar ��r�nga B'yi ��r�nga A �zerine s�karak birle�tirin (�ekil 6a ve 6b). A��r� s�kmay�n.
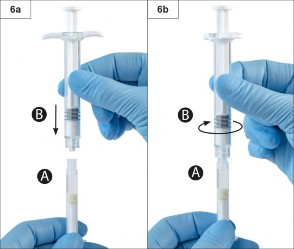
Ad�m 7: Ba�lanan �niteyi ters �evirin ve ��r�nga A'n�n s�v� i�eri�ini tozu (leuprorelin asetat) i�eren ��r�nga B'ye enjekte ederken ��r�nga B altta olacak �ekilde enjekt�rleri dikey �ekilde tutmaya devam edin (�ekil 7).
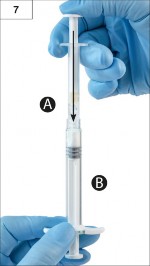
Ad�m 8: Her iki enjekt�r�n i�eriklerini, homojen ve viskoz bir ��zelti elde etmek i�in yatay konumda ileri ve geri y�nde nazik�e iterek (toplam 60 defa, yakla��k 60 saniye s�rer) �r�n� tamamen kar��t�r�n (�ekil 8). Enjekt�r sistemini b�kmeyin (enjekt�rleri k�smen a�abilece�iniz i�in bu durum s�z�nt�ya neden olabilir).
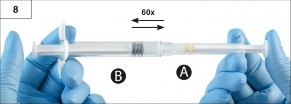
Tamamen kar��t�r�ld���nda viskoz ��zelti renksiz ila beyaz ile a��k sar� (beyaz ila a��k sar�n�n tonlar� dahil) renkte g�r�necektir.
�nemli: �r�n zaman ge�tik�e daha viskoz hale geldi�inden, kar��t�rd�ktan sonra hemen bir sonraki ad�ma ge�iniz. Kar��t�r�lm�� �r�n� so�utucuya koymay�n.
L�tfen dikkat: �r�n, anlat�ld��� �ekilde kar��t�r�lmal�d�r; �alkalama i�lemi �r�n�n yeterince kar��mas�n� SA�LAMAZ.
Ad�m 9: ��r�nga B altta olacak �ekilde enjekt�rleri dikey konumda tutun. Enjekt�rler g�venli �ekilde birle�mi� kalmal�d�r. ��r�nga A pistonuna bast�rarak ve ��r�nga B pistonunu hafif�e �ekerek, kar��t�r�lm�� �r�n�n tamam�n� ��r�nga B'ye (geni� enjekt�r) �ekin (�ekil 9).
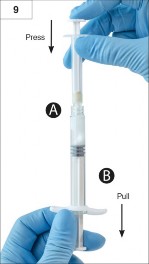
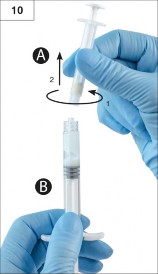
Ad�m 10: ��r�nga A pistonunu bast�rmaya devam ederken ��r�nga A'y� �evirerek ��kar�n (�ekil 10). �r�n�n s�zmad���ndan emin olun; aksi halde i�ne, tak�ld���nda tam olarak sabitlenmez.
L�tfen dikkat: Form�lasyonda bir tane b�y�k veya birka� tane k���k hava kabarc��� kalabilir, bu kabul edilebilir bir durumdur. �r�n kaybolaca��ndan l�tfen bu a�amada ��r�nga B'deki hava kabarc�klar�n� p�sk�rtmeyin!
Ad�m 11:
��r�nga B'yi dik konumda tutun ve �r�n kayb�n� engellemek i�in beyaz pistonu arkadan destekleyin.
 �izofrenlik
�izofrenli�in psikiatrik te�hisi hakk�nda �ok fazla anla�mazl�k vard�r. Bu
sayfadaki bilgiler, �izofrenli�in te�hisi, nedenleri ve tedavisi hakk�ndaki fakl� teoriler
hakk�nda bilgi verecektir.
�izofrenlik
�izofrenli�in psikiatrik te�hisi hakk�nda �ok fazla anla�mazl�k vard�r. Bu
sayfadaki bilgiler, �izofrenli�in te�hisi, nedenleri ve tedavisi hakk�ndaki fakl� teoriler
hakk�nda bilgi verecektir. |
 Mesane Kanseri
Mesane kanseri her zaman mukozada ba�lar. Erken safhalarda bu tabakada s�n�rl� kal�r ve
h�cre i�indeki karsinom olarak nitelendirilir.
Mesane Kanseri
Mesane kanseri her zaman mukozada ba�lar. Erken safhalarda bu tabakada s�n�rl� kal�r ve
h�cre i�indeki karsinom olarak nitelendirilir. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| LUCRIN | 8680656080117 | 4,887.91TL |
| PROSALID | 8699525776426 | |
| Di�er E�de�er �la�lar |
 |
Belso�uklu�u, Chlamydia ve Frengi Belso�uklu�u, bakterilerin sebep oldu�u bir enfeksiyondur. Cinsel ili�ki yoluyla bula��r ve d�lyata�� boynunda, idrar yollar�nda, an�ste, makatta ve bo�azda enfeksyona sebep olabilir. |
 |
Tiroid Kanseri En s�k g�r�len tiroid kanseri t�r� olan papiller tiroid kanseri, t�m tiroid kanserlerinin yakla��k %70'ini olu�turur. |
 |
S�rt A�r�s� S�rt a�r�s� birden bire ortaya ��k�p �iddetli (akut) olabilir veya zamanla geli�ip daha uzun s�reli sorunlara (kronik) neden olabilir. |
�LA� GENEL B�LG�LER�
Astellas Pharma �la� Ticaret Ve Sanayi A.�
| Geri �deme Kodu | A16251 |
| Sat�� Fiyat� | 6099.4 TL [ 10 Jul 2023 ] |
| �nceki Sat�� Fiyat� | 5988.5 TL [ 3 Jul 2023 ] |
| Original / Jenerik | Jenerik �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699043890291 |
| Etkin Madde | Loprolid Asetat |
| �thal ( ref. �lke : Hollanda ) ve Be�eri bir ila�d�r. |