ERLEADA 60 mg film kaplı tablet (120 tablet) Farmakolojik Özellikler
{ Apalutamit }
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Endokrin tedavi, anti-androjenler
ATC kodu: L02BB05
Etki mekanizması
Apalutamit, doğrudan Androjen Reseptörünün (AR) ligand bağlanma bölgesine bağlanan, oral yoldan uygulanan seçici bir AR inhibitörüdür. Apalutamit AR nükleer translokasyonunu önler, DNA bağlanmasını inhibe eder, AR aracılı transkripsiyonu engeller ve androjen reseptör agonist aktivitesinden yoksundur. Apalutamit tedavisi tümör hücrelerinin çoğalmasını azaltıp apoptozu artırarak, güçlü antitümör aktiviteye yol açar. Majör bir metaboliti olan N-desmetil apalutamit, apalutamidin in vitro aktivitesinin üçte birini sergiler.
Kardiyak elektrofizyoloji
Günde 1 kez alınan 240 mg apalutamidin QTc aralığına etkisi, KDPK'li 45 hastada açık etiketli, kontrolsüz, çok merkezli, tek kollu özel QT çalışmasında değerlendirildi. Kararlı durumda, başlangıçtan itibaren maksimum ortalama QTcF değişikliği 12,4 ms idi (2 taraflı % 90 üst GA: 16,0 ms). Bir maruz kalma-QT analizi, apalutamit ve aktif metaboliti için konsantrasyona bağlı QTcF artışı gösterdi.
Klinik etkililik ve güvenlilik
Apalutamidin etkililik ve güvenliliği, randomize, plasebo kontrollü iki Faz 3 çalışmada belirlenmiştir [ARN-509-003 (nmKDPK) ve 56021927PCR3002([mHDPK)].
SPARTAN: Metastatik Olmayan Kastrasyona Dirençli Prostat Kanseri (nmKDPK)
Çok merkezli, çift kör klinik çalışmada (ARN-509-003 Çalışması) toplam 1207 NM-KDPK hastası, androjen deprivasyon tedavisi (ADT) (tıbbi kastrasyon veya geçirilmiş cerrahi kastrasyon) ile kombine olarak günde bir kez 240 mg oral apalutamit veya ADT ile kombine olarak plasebo alacak şekilde 2:1 oranında randomize edildi. Kayıtlanan hastalarda Prostat Spesifik Antijen (PSA) İkiye Katlanma Zamanı (PSADT) ≤10 ay olup bu hastalar olası metastatik hastalık ve prostat kanserine bağlı ölüm için yüksek risk altında kabul edilmekteydi. Cerrahi kastrasyon geçirmemiş tüm hastalara çalışma boyunca sürekli olarak ADT verildi. PSA sonuçları körleştirildi ve tedavinin sonlandırılması için kullanılmadı. İki koldan birine randomize edilen hastalar, körleştirilmiş merkezi görüntüleme incelemesi (BICR) tarafından tanımlanan hastalık progresyonuna, yeni tedavi başlangıcına, kabul edilemez toksisiteye veya çalışmadan çıkmaya kadar tedaviye devam edecekti.
Aşağıdaki hasta demografik ve başlangıç hastalık özellikleri tedavi kolları arasında dengelendi. Medyan yaş 74 yıldı (aralık: 48-97) ve hastaların % 26'sı 80 yaş ve üzeriydi. Irk dağılımı % 66 beyaz, % 5,6 siyah, % 12 asyalı ve % 0,2 diğer şeklindeydi. Her iki tedavi kolundaki hastaların
% 77'si daha önce prostat cerrahisi geçirmiş veya prostat radyoterapisi almıştı. Hastaların çoğunluğunun Gleason skoru 7 veya daha yüksekti (% 81). Hastaların % 15'inde çalışmaya girişte <2 cm pelvik lenf nodları mevcuttu. Hastaların % 73'ü daha önce birinci jenerasyon anti- androjen ile tedavi; % 69'u bikalutamid ve % 10'u flutamid almıştı. Kayıtlanan tüm hastaların körleştirilmiş merkezi görüntüleme incelemesiyle metastatik olmadığı doğrulanmış olup çalışma girişinde Doğu Ortak Onkoloji Grubu Performans Durumu (ECOG PS) skoru 0 veya 1'di.
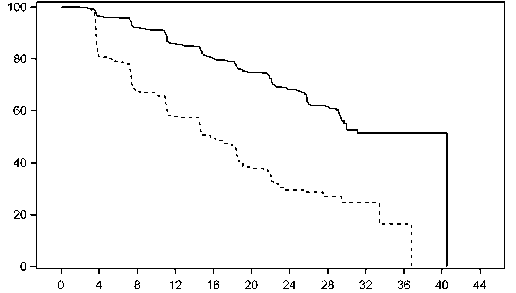
Metastazsız sağkalım (MFS); randomizasyondan, BICR ile doğrulanan kemik veya yumuşak doku uzak metastazının ilk belirtisinin görüldüğü zamana veya herhangi bir nedene bağlı ölüm olayına (hangisi önce meydana gelirse) kadar geçen süre olarak tanımlanan primer sonlanım noktasıydı. ERLEADA tedavisiyle MFS'de anlamlı düzelme sağlandı. ERLEADA, uzak metastaz veya ölüm için bağıl riski plaseboya kıyasla % 70 oranında azalttı (HR_0,30; % 95 GA: 0,24, 0,36; p 0,0001). ERLEADA için medyan MFS 41 ay iken plasebo için 16 aydı (bkz. Şekil
1. ERLEADA ile MFS'de tutarlı iyileşme, yaş, ırk, dünyanın farklı coğrafyaları, nodal durum,
önceki hormonal tedavi sayısı, bazal PSA, PSA iki katına çıkma süresi, bazal ECOG durumu ve kemik koruyucu ajanların kullanımı dahil, önceden belirlenmiş tüm alt gruplar için gözlendi.).
Şekil 1: ARN-509-003 Çalışmasında Kaplan-Meier metastazsız sağkalım (MFS) eğrisi
Metastaz veya Ölüm olayı yaşamayan Hasta Yüzdesi |
|
| Randomizasyondan itibaren geçen Aylar |
Risk altındaki hastalar | ||||||||||||
Plasebo | ||||||||||||
Apalutamit | ||||||||||||
|
|
| Plasebo |
| Apalutamit |
|
|
|
| |||
ERLEADA ve ADT ile tedavi edilen hastalar, tek başına ADT ile tedavi edilen hastalara kıyasla aşağıdaki sekonder sonlanım noktaları için anlamlı düzelme göstermiştir (HR=0,28; % 95 GA: 0,23, 0,34; p<0,0001), progresyonsuz sağkalım (PFS) (HR=0,30; % 95 GA: 0,25, 0,36; p<0,0001); semptomatik progresyona kadar geçen süre (HR=0,57; % 95 GA: 0,44, 0,73; p<0,0001) ve genel sağkalım eğilimi (OS) (HR=0,78; % 95 GA: 0,64, 0,96; p=0,0161) ve sitotoksik kemoterapinin başlatılmasına kadar geçen süre (HR=0,63; % 95 GA: 0,49, 0,81; p=0,0002).
Semptomatik ilerlemeye kadar geçen süre, randomizasyondan iskeletle ilişkili bir olayın gelişmesine, yeni bir sistemik anti-kanser tedavisinin başlatılmasını gerektiren ağrı/semptomlar veya radyasyon/cerrahi gerektiren lokal-bölgesel tümör ilerlemesine kadar geçen süre olarak tanımlandı. Toplam olay sayısı az iken, iki kol arasındaki fark istatistiksel olarak anlamlı olacak şekilde yeterince fazlaydı.
ERLEADA ile tedavi, semptomatik ilerleme riskini plasebo ile karşılaştırıldığında % 43 oranında azalttı (HR=0,567; % 95 GA: 0,443, 0,725; p < 0,0001). Her iki tedavi grubunda da semptomatik ilerlemeye kadar geçen medyan süreye ulaşılamadı.
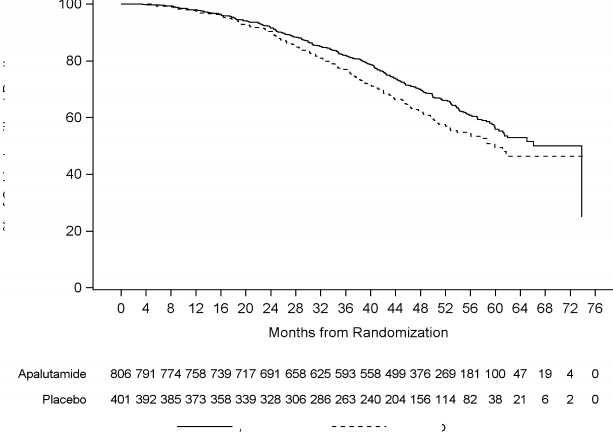
52 aylık medyan takip süresi ile sonuçlar, ERLEADA ile tedavinin plaseboya kıyasla ölüm riskini % 22 azalttığını önemli ölçüde göstermiştir. (HR = 0,784; % 95 GA: 0,643, 0,956; 2 taraflı p = 0,0161). Medyan OS, ERLEADA kolu için 73,9 ay ve plasebo kolu için 59,9 aydı.
Önceden belirlenmiş alfa sınırı (p ≤ 0,046) geçildi ve istatistiksel anlamlılık başarıldı. Bu iyileşme, plasebo kolundaki hastaların % 19'unun sonraki tedavi olarak ERLEADA almasına rağmen gösterilmiştir.
Ölüm olayı yaşamayan
Hasta Yüzdesi
Şekil 2: ARN-509-003 Çalışmasında Kaplan-Meier genel sağkalım (OS) eğrisi final analizi
Risk altındaki
hastalar
Plasebo
Apalutamit
Plasebo
Apalutamit
Randomizasyondan İtibaren Geçen Ay
ERLEADA ile tedavi, sitotoksik kemoterapiye başlama riskini plasebo ile karşılaştırıldığında (HR = 0,629; % 95 GA: 0,489, 0,808; p = 0,0002) % 37 oranında önemli ölçüde azalttı, plaseboya karşı ERLEADA için istatistiksel olarak önemli bir gelişme gösterdi. Her iki tedavi kolu için de sitotoksik kemoterapi başlangıcına kadar geçen medyan süreye ulaşılamadı.
PSA, radyografik veya semptomatik olarak ölüme veya hastalığın ilerlemesine kadar geçen süre olarak tanımlanan PFS-2, ERLEADA ile tedavi edilen hastalarda plasebo ile tedavi edilenlere göre sonraki ilk tedavide veya sonrasında daha uzundu. Sonuçlar, PFS-2 riskinde plaseboya karşı
% 44'lük bir azalma olduğunu göstermiştir. (HR = 0,565, % 95 CI: 0,471, 0,677; p < 0,0001).
ERLEADA'nın ADT'ye eklenmesiyle genel sağlıkla ilgili yaşam kalitesi üzerinde hiçbir zararlı etki görülmemiştir. Kanser Tedavisinin Fonksiyonel Değerlendirmesi-Prostat (FACT-P) toplam puanı ve alt ölçeklerinin analizinde başlangıca göre ERLEADA lehine değişimde küçük ama klinik olarak anlamlı olmayan bir fark gözlemlendi.
Pediyatrik popülasyon
Pediyatrik popülasyonda prostat kanseri görülmediğinden ERLEADA'nın pediyatrik hastalarda kullanımı bulunmamaktadır. ERLEADA'ya ait pediatrik popülasyonda klinik etkililik ve güvenlilik verisi yoktur (bkz. Bölüm 4.2).
5.2. Farmakokinetik özellikler
Günde tek doz ile tekrarlayan kullanımı takiben apalutamit maruziyeti (Cve konsantrasyon eğrisi altındaki alan [EAA]) 30 ila 480 mg doz aralığında dozla orantılı bir şekilde artmıştır. Günde bir kez 240 mg doz uygulandıktan sonra, apalutamit kararlı durumuna 4 hafta sonra ulaşılmış ve ortalama birikim oranı tek dozun yaklaşık 5 katı olmuştur. Kararlı durumda, apalutamit için ortalama (% CV) Cdeğeri 6 µg/mL (% 28) ve EAA değeri 100 µg.sa/mL (% 32) olmuştur. Apalutamit plazma konsantrasyonlarındaki günlük dalgalanmalar düşük olup ortalama vadi-tepe noktası oranı 1,63'tür. Tekrarlı dozlama ile olasılıkla apalutamidin kendi metabolizmasını indüklemesi sebebiyle görünür klirenste (CL/F) artış gözlenmiştir.
Kararlı durumda, majör aktif metabolit olan N-desmetil apalutamit için ortalama (% CV) Cdeğeri 5,9 µg/mL (% 18) ve EAA değeri 124 µg.sa/mL (% 19) olmuştur. N-desmetil apalutamit, ortalama 1,27'lik vadi-tepe noktası oranıyla kararlı durumda düz bir konsantrasyon-zaman profili ile karakterize edilmiştir. Tekrarlı doz uygulamasından sonra N-desmetil apalutamit için ortalama (% CV) EAA metabolit/ana ilaç oranı yaklaşık 1,3'tü (% 21). Sistemik maruziyet, bağıl potens ve farmakokinetik özellikler temel alındığında, N-desmetil apalutamidin, apalutamidin klinik aktivitesine katkıda bulunmuş olması olasıdır.
Emilim:
Oral uygulamadan sonra pik plazma konsantrasyonuna ulaşmak için geçen medyan süre (t) 2 saatti (aralık: 1 ila 5 saat). Ortalama mutlak oral biyoyararlanım yaklaşık % 100 olup apalutamidin oral uygulamadan sonra tamamen emildiği gösterilmiştir.
Apalutamit açlık koşullarında ve yüksek yağ içerikli bir öğünden sonra sağlıklı gönüllülere uygulandığında, Cve EAA değerlerinde klinik olarak anlamlı değişiklikler meydana gelmemiştir. T'a ulaşmak için geçen medyan süre yemekle birlikte yaklaşık 2 saat gecikmiştir (bkz. Bölüm 4.2).
Apalutamit ilgili fizyolojik pH koşulunda iyonlaşamaz, bu nedenle asit düşürücü ajanların (örn., proton pompası inhibitörü, H-reseptör antagonisti, antasit gibi) apalutamidin çözünürlüğünü ve biyoyararlanımını etkilemesi beklenmemektedir.
Apalutamit ve N-desmetil metaboliti in vitro P-gp substratlarıdır. Apalutamit oral uygulamayı takiben tamamen emildiğinden, P-gp apalutamidin emilimini sınırlamamakta ve bu nedenle P-gp inhibisyonu veya indüksiyonunun apalutamidin biyoyararlanımını etkilemesi beklenmemektedir.
Dağılım:
Apalutamidin kararlı durumda ortalama görünür dağılım hacmi yaklaşık 276 L'dir. Apalutamidin dağılım hacmi toplam vücut suyu hacminden daha büyük olup, kapsamlı ekstravasküler dağılım olduğuna işaret eder.
Apalutamit ve N-desmetil apalutamit, konsantrasyondan bağımsız olarak başta serum albümin
olmak üzere plazma proteinlerine sırasıyla % 96 ve % 95 oranında bağlanır.
Biyotransformasyon:
Apalutamidin başlıca eliminasyon yolu metabolizmadır. Esas olarak CYP2C8 ve CYP3A4 tarafından metabolize edilerek N-desmetil apalutamidi oluşturur. Apalutamit ve N-desmetil apalutamit, karboksilesteraz tarafından daha fazla metabolize edilerek inaktif karboksilik asit metaboliti oluşturulur. CYP2C8 ve CYP3A4'ün apalutamit metabolizmasına katkısının tek dozdan sonra sırasıyla % 58 ve % 13 olduğu, fakat kararlı durumda apalutamidin tekrarlayan dozlarında CYP3A4 indüksiyonuna bağlı olarak değiştiği tahmin edilmektedir.
Eliminasyon:
Genel olarak metabolit formundaki apalutamit esas olarak idrarla atılır. Radyoaktif işaretli apalutamidin tek oral uygulaması sonrasında, radyoaktivitenin % 89'u dozdan 70 gün sonrasına kadar: % 65'i idrarda (dozun % 1,2'si değişmemiş apalutamit ve % 2,7'si N-desmetil apalutamit olarak) ve % 24'ü feçeste (dozun % 1,5'i değişmemiş apalutamit ve % 2'si N-desmetil apalutamit olarak) bulunmuştur.
Tek dozlamadan sonra apalutamidin görünür oral klirensi (CL/F) 1,3 L/sa olup, günde bir kez dozlamadan sonra kararlı durumda 2,0 L/sa'e yükselmiştir. Apalutamidin hastalarda ortalama etkili yarılanma ömrü kararlı durumda yaklaşık 3 gündür.
İn vitro veriler, apalutamit ve N-desmetil metabolitinin BCRP, OATP1B1 veya OATP1B3 substratları olmadığını göstermiştir.
Hastalardaki karakteristik özellikler
Özel popülasyonlar:
Böbrek yetmezliği, karaciğer yetmezliği, yaş, ırk ve diğer dış faktörlerin apalutamidin farmakokinetiği üzerindeki etkileri aşağıda özetlenmiştir.
Böbrek yetmezliği
Apalutamit için özel bir böbrek yetmezliği çalışması yürütülmemiştir. Kastrasyona dirençli prostat kanseri (KDPK) olan hastalar ve sağlıklı gönüllülerde yapılan klinik çalışmaların verileri kullanılarak gerçekleştirilen popülasyon farmakokinetik analizine göre, önceden var olan hafif ila orta dereceli böbrek yetmezliği (tahmini glomerüler filtrasyon hızı [eGFR] 30 ila 89 mL/dak/1,73 m; N=585) olan hastalarda, başlangıçta normal böbrek fonksiyonuna (eGFR ≥ 90 mL/dak/1,73 m; N=372) sahip gönüllülere kıyasla sistemik apalutamit maruziyetinde anlamlı bir fark gözlenmemiştir. Şiddetli böbrek yetmezliği veya son evre böbrek hastalığının (eGFR
≤29 mL/dak/1,73 m) potansiyel etkisi, yeterli veri olmaması sebebiyle belirlenmemiştir.
Karaciğer yetmezliği
Özel bir karaciğer yetmezliği çalışmasında, normal karaciğer fonksiyonuna sahip sağlıklı kontrollere (N=8) kıyasla başlangıçta hafif karaciğer yetmezliği (N=8, Child-Pugh Sınıf A, ortalama skor = 5,3) veya orta şiddetli karaciğer yetmezliği (N=8, Child-Pugh Sınıf B, ortalama skor = 7,6) olan hastalarda, apalutamit ve N-desmetil apalutamidin sistemik maruziyeti karşılaştırılmıştır. Tek oral 240 mg apalutamit dozu uygulandıktan sonra, hafif yetmezliği olan hastalarda apalutamit için EAA ve Cdeğerlerinin geometrik ortalama oranı (GMR) sırasıyla
% 95 ve % 102 olup orta derecede yetmezliği olan hastalarda apalutamidin EAA ve Cdeğerleri için GMR sırasıyla % 113 ve % 104 olarak bulunmuştur. Şiddetli karaciğer yetmezliği (Child-Pugh Sınıf C) olan hastalar için apalutamit ile ilgili klinik ve farmakokinetik veriler mevcut değildir.
Etnik köken ve ırk
Popülasyon farmakokinetik analizine göre, Beyaz (Kafkas, Hispanik veya Latin; N=761), Siyah (Afrika kökenli veya Afrikalı Amerikalı; N=71), Asya (Japon olmayan; N=58) ve Japon (N=58) ırkları arasında apalutamit farmakokinetiği bakımından klinik olarak anlamlı farklılıklar görülmemiştir.
Yaş
Popülasyon farmakokinetik analizleri yaşın (aralık: 18 ila 94 yaş) apalutamit farmakokinetiği
üzerinde klinik olarak anlamlı bir etkisi olmadığını göstermiştir.
5.3. Klinik öncesi güvenlilik verileri
Apalutamit, standart bir in vitro ve in vivo test bataryasında genotoksisite sergilememiştir. Apalutamit, erkek transgenik (Tg.rasH2) farede günde 30 mg/kg'a kadar sırasıyla apalutamit ve N-desmetil için 1,2 ve 0,5 katı dozlarda yapılan 6 aylık bir çalışmada kanserojen değildir.
Önerilen klinik dozda klinik maruziyet (EAA) 240 mg/gün'dür.
Erkek Sprague-Dawley sıçanlarında yapılan 2 yıllık bir karsinojenisite çalışmasında, apalutamit oral gavaj yoluyla 5, 15 ve 50 mg/kg/gün dozlarında (hastalarda sırasıyla EAA'nın 0,2, 0,7 ve 2,5 katı (önerilen dozlarda insan maruziyeti 240 mg doz)) uygulanmıştır. 5 mg/kg/gün veya daha yüksek dozlarda testiküler Leydig hücre adenomu ve karsinomu, 15 mg/kg/gün veya 50 mg/kg/gün dozlarında meme adenokarsinomu ve fibroadenomu ve 50 mg/kg/gün'de tiroid foliküler hücre adenomu insidansı dahil olmak üzere neoplastik bulgular kaydedildi. Bu bulguların sıçana özgü olduğu ve bu nedenle insanlarla sınırlı ilgisi olduğu kabul edildi.
Apalutamidin farmakolojik aktivitesiyle tutarlı olan tekrarlı doz toksikoloji çalışmalarının bulgularına göre erkek fertilitesinin apalutamit tedavisinden etkilenme olasılığı bulunmaktadır. Erkek sıçanlar ve köpeklerde yapılan tekrarlı doz toksisite çalışmalarında, EEA değerine göre insan maruziyetine yaklaşık olarak eşit olan maruziyetlere karşılık gelen dozlarda üreme sisteminde atrofi, aspermi/hipospermi, dejenerasyon ve/veya hiperplazi ya da hipertrofi gözlenmiştir.
Erkek sıçanlarda yapılan bir fertilite çalışmasında, EEA değerine göre insan maruziyetine yaklaşık olarak eşit olan maruziyetlere karşılık gelen dozlarda 4 hafta dozlama sonrasında ikincil eşey bezleri ve epididim ağırlıklarında meydana gelen azalmayla birlikte sperm konsantrasyonu ve motilitesi, çiftleşme ve fertilite oranlarında azalma (tedavi edilmemiş dişilerle çiftleşme sonrasında) gözlenmiştir. Erkek sıçanlar üzerindeki etkiler, son apalutamit uygulamasından 8 hafta sonra düzelmiştir.
Sıçanlarda yapılan bir ön embriyofetal gelişimsel toksisite çalışmasında, apalutamit organogenez (gebelik günleri 6-20) periyodu boyunca 25, 50 veya 100 mg/kg/gün oral dozlarda uygulandığında gelişimsel toksisite sorunlarına neden olmuştur. Bu dozlar, insanlardaki 240 mg/gün dozundaki maruziyetin EAA bazında sırasıyla yaklaşık 2, 4 ve 6 katı sistemik maruziyetle sonuçlanmıştır. Bulgular hamile olmayan dişilerde 100 mg/kg/gün dozunda ve ≥50 mg/kg/gün dozlarında embriyofetal ölüm (rezorpsiyonlar), azalmış fetal anogenital mesafeyi ve
≥25 mg/kg/gün dozunda şekilsiz bir hipofiz bezini (daha yuvarlak şekil) içermiştir. ≥25 mg/kg/gün dozlarda, ortalama fetal ağırlık üzerinde bir etkiye yol açmadan, iskelet varyasyonları da (kemikleşmemiş falankslar, aşırı kısa torakolomber kaburga(lar) ve/veya hyoid anormallikleri) kaydedilmiştir.
 Kolon, Rektum yada Bağırsak Kanseri
Bağırsak kanseri kolon veya rektumda
(arka geçit) herhangi bir bölgede ortaya çıkabilir.Kolorektal kanser erken safhalarda teşhis edilmesi halinde daha kolay ve daha başarılı bir
şekilde tedavi edilir.
Kolon, Rektum yada Bağırsak Kanseri
Bağırsak kanseri kolon veya rektumda
(arka geçit) herhangi bir bölgede ortaya çıkabilir.Kolorektal kanser erken safhalarda teşhis edilmesi halinde daha kolay ve daha başarılı bir
şekilde tedavi edilir. |
 HIV ve Aids
HIV, Human Immunodeficiency Virus’dür (İnsanlarda Bağışıklık Sistemini Bozan
Virüsdür). Bu virüs AIDS hastalığına sebep olur.
HIV ve Aids
HIV, Human Immunodeficiency Virus’dür (İnsanlarda Bağışıklık Sistemini Bozan
Virüsdür). Bu virüs AIDS hastalığına sebep olur. |
İLAÇ GENEL BİLGİLERİ
Johnson & Jonhson Sıhhi Malzeme San. ve Tic.Ltd.Şti.
| Satış Fiyatı | 55145.32 TL [ 3 Jan 2025 ] |
| Önceki Satış Fiyatı | |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Kısıtlanmış Beyaz Reçeteli bir ilaçdır. |
| Barkodu | 8699593095436 |
| Etkin Madde | Apalutamit |
| ATC Kodu | L02BB05 |
| Birim Miktar | 60 |
| Birim Cinsi | MG |
| Ambalaj Miktarı | 120 |
| Antineoplastik ve İmmünomodülatör Ajanlar > Hormon Antagonistleri |
| İthal ( ref. ülke : Fransa ) ve Beşeri bir ilaçdır. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| Eşdeğer bir ilaç bulunamadı |
 |
Deri Kanseri Deri kanseri çok rastlanan bir hastalıktır. Üç ana türü bulunur ;genelde kemirici ülser olarak bilinen bazal hücreli karsinom, yassı hücreli karsinom ve kötü huylu tümör. |
 |
Grip, Soğuk Algınlığı ve Öksürük Grip ve soğuk algınlığı (nezle) semptomları arasındaki farkı bilmek önemlidir. Soğuk algınlığı gripten daha hafif belirtiler gösteren bir solunum yolu hastalığıdır. |
 |
En Yaygın Alerji Türleri Bağışıklık sistemi, polen, arı zehiri veya evcil hayvan gibi yabancı bir maddeye veya çoğu insanda reaksiyona neden olmayan bir yiyeceğe tepki gösterdiğinde alerjiler meydana gelir. |