GAZYVA 1000 mg IV konsantre inf�zyon ��z. i�eren flakon K�sa �r�n Bilgisi
{ Obinutuzumab }
1. BE�ER� TIBB� �R�N�N ADI
GAZYVA 1000 mg/40 ml IV inf�zyonluk konsantre ��zelti Steril
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Her bir 40 mL konsantre flakon, seyreltilmeden �nce 25 mg/mL olan konsantrasyona kar��l�k gelen 1000 mg obinutuzumab i�erir.
Obinutuzumab, parenteral B-Ly1 fare antikorunun h�manizasyonu yoluyla elde edilen ve �in Hamsteri Over h�cre hatt�nda rekombinant DNA teknolojisiyle �retilen, IgG1 alt s�n�f�n�n Tip II h�manize anti-CD20 monoklonal antikorudur.
Yard�mc� maddeler
Yard�mc� maddeler i�in b�l�m 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
�nf�zyonluk konsantre ��zelti i�eren flakon Berrak, renksiz ile hafif kahverengimsi s�v�
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Kronik Lenfositik L�semi (KLL):
GAZYVA, Kronik Lenfositik L�semi (KLL) endikasyonunun;
70 ya� ve �zerinde olup CIRS > 6 olan ve/veya kreatinin klerensi 30-69 ml/dk olan hastalarda klorambusil ile kombine olarak ilk seri tedavisinde endikedir.
4.2. Pozoloji ve uygulama �ekli
GAZYVA, uzman bir hekimin yak�n g�zetimi alt�nda ve t�m res�sitasyon ara�lar�n�n haz�r bulundu�u bir ortamda uygulanmal�d�r.
Pozoloji/Uygulama s�kl��� ve s�resi:
T�m�r Lizis Sendromu (TLS) i�in profilaksi ve premedikasyon
T�m�r y�k� y�ksek ve/veya dola��mda lenfosit say�s� y�ksek (>25 x 10/L) olan ve/veya renal yetmezli�i (KrKl <70 mL/dk) bulunan hastalar, TLS riski alt�nda kabul edilir ve profilaksi almal�d�r. Profilaksi, standart uygulama do�rultusunda GAZYVA inf�zyonuna ba�lamadan (bkz. B�l�m 4.4) 12-24 saat �nce, yeterli hidrasyon ve �rikostatikler (�rn. allopurinol) ya da �rat oksidaz (�rn. rasburikaz) gibi alternatif uygun bir tedaviyi i�ermelidir. Hastalar, gerekli g�r�ld���nde bir sonraki her inf�zyondan �nce yeniden profilaksi almaya devam etmelidirler.
�nf�zyonla �li�kili Reaksiyonlar (IRR'ler) i�in profilaksi ve premedikasyon
�nf�zyonla ili�kili reaksiyonlar� azaltmaya y�nelik premedikasyon, Tablo 1'de a��klanm��t�r (ayr�ca bkz. B�l�m 4.4). Kortikosteroid premedikasyonu, KLL hastalar� i�in birinci d�ng� s�ras�nda zorunludur, FL hastalar� i�in de tavsiye edilir (bkz. Tablo 1). Sonraki inf�zyonlar i�in premedikasyon ve di�er premedikasyon, a�a��da a��kland��� �ekilde verilmelidir.
�ntraven�z GAZYVA inf�zyonlar� s�ras�nda bir IRR belirtisi olan hipotansiyon meydana gelebilir. Bu nedenle, her GAZYVA inf�zyonundan 12 saat �nce, inf�zyon s�resince ve uygulamay� takiben bir saat s�reyle antihipertansif tedavilere ara verilmesi d���n�lmelidir (bkz. B�l�m 4.4).
Tablo 1. KLL ve FL hastalar�nda inf�zyonla ili�kili reaksiyonlar�n riskini azaltmak i�in GAZYVA inf�zyonundan �nce uygulanmas� gereken premedikasyon (bkz. B�l�m 4.4)
Tedavi D�ng�s� G�n� | Premedikasyon gereken hastalar | Premedikasyon | Uygulama |
D�ng� 1: KLL ve FL i�in 1. G�n |
T�m hastalar | �ntraven�z kortikosteroid (KLL i�in zorunludur, FL i�in tavsiye edilmektedir) | GAZYVA inf�zyonundan en az 1 saat �nce tamamlanmal� |
Oral analjezik/antipiretik | GAZYVA inf�zyonundan en az 30 dakika �nce | ||
Antihistaminik | |||
D�ng� 1: |
T�m hastalar | �ntraven�z kortikosteroid (zorunludur) | GAZYVA inf�zyonundan en az 1 saat �nce tamamlanmal� |
Oral analjezik/antipiretik |
|
Yaln�zca KLL hastalar� i�in 2. G�n |
| Antihistaminik | GAZYVA inf�zyonundan en az 30 dakika �nce |
KLL ve FL i�in takip eden t�m inf�zyonlar | �nceki inf�zyon s�ras�nda inf�zyon reaksiyonu olmayan hastalar | Oral analjezik/antipiretik | GAZYVA inf�zyonundan en az 30 dakika �nce |
�nceki inf�zyonla inf�zyon reaksiyonu (Evre 1 veya 2) olan hastalar | Oral analjezik/antipiretik Antihistaminik | ||
�nceki inf�zyonda Evre 3 inf�zyon reaksiyonu olan hastalar VEYA Bir sonraki tedaviden �nce lenfosit say�s� >25 x10 /L olan hastalar |
�ntraven�z kortikosteroid | GAZYVA inf�zyonundan en az 1 saat �nce tamamlanmal� | |
Oral analjezik/antipiretik Antihistaminik | GAZYVA inf�zyonundan en az 30 dakika �nce |
Doz
Kronik lenfositik l�semi (KLL, klorambusil ile kombinasyon �eklinde)
KLL hastalar� i�in klorambusil ile kombinasyon �eklinde �nerilen GAZYVA dozu Tablo 2'de g�sterilmektedir.
D�ng� 1
Klorambusil ile kombinasyon �eklinde �nerilen GAZYVA dozu, 28 g�nl�k ilk tedavi d�ng�s�n�n 1. ile 2. g�nlerinde (veya 1. g�n�n devam�nda), 8. g�n�nde ve 15. g�n�nde
uygulanan 1000 mg'd�r.
1 ve 2. g�nlerdeki inf�zyonlar i�in iki inf�zyon torbas� (1. g�n i�in 100 mg ve 2. g�n i�in 900 mg) haz�rlanacakt�r. �lk torba inf�zyon h�z�nda de�i�iklik veya hi�bir kesinti olmaks�z�n tamamland��� takdirde, inf�zyon s�resince uygun zaman, ko�ullar ve t�bbi g�zetim sa�land��� s�rece ikinci torba ayn� g�n uygulanabilir (dozun geciktirilmesine ve tekrar premedikasyona gerek yoktur). �lk 100 mg s�ras�nda inf�zyon h�z�nda herhangi bir de�i�iklik veya kesinti meydana gelmesi halinde ikinci torba ertesi g�n verilmelidir.
D�ng� 2 - 6
Klorambusil ile kombinasyon �eklinde �nerilen GAZYVA dozu, her bir d�ng�n�n 1. g�n�nde uygulanan 1000 mg'd�r.
Tablo 2. KLL hastalar�nda her biri 28 g�n s�ren 6 tedavi d�ng�s� boyunca uygulanmas� gereken GAZYVA dozu
Siklus | Tedavi g�n� | GAZYVA Dozu |
D�ng� 1 | 1. G�n | 100 mg |
2. G�n (veya 1. g�n�n devam�nda) | 900 mg | |
8. G�n | 1000 mg | |
15. G�n | 1000 mg | |
D�ng� 2-6 | 1. G�n | 1000 mg |
Uygulama s�kl��� ve s�resi
Her biri 28 g�n s�ren alt� tedavi d�ng�s�.
Geciktirilen veya atlanan dozlar
GAZYVA'n�n planlanm�� bir dozu atlan�rsa, m�mk�n olan en k�sa s�rede uygulanmal�d�r; planlanm�� olan bir sonraki doza kadar beklemeyiniz. GAZYVA i�in planlanm�� tedavi aral��� dozlar aras�nda korunmal�d�r.
Folik�ler lenfoma (FL)
GAZYVA'n�n FL hastalar� i�in �nerilen kemoterapi ile kombinasyon �eklinde �nerilen dozu Tablo 3'te g�sterilmi�tir.
Daha �nce tedavi edilmemi� folik�ler lenfoma hastalar� �nd�ksiyon (kemoterapi ile kombinasyon �eklinde)
GAZYVA kemoterapi ile a�a��daki �ekilde uygulanmal�d�r:
Bendamustin ile kombinasyon �eklinde 28 g�nl�k 6 d�ng� ya da,
Siklofosfamid, doksorubisin, vinkristin, prednizolon (CHOP) ile kombinasyon halinde 21 g�nl�k 6 d�ng�, ard�ndan yaln�zca GAZYVA ile 2 ilave d�ng� ya da,
Siklofosfamid, vinkristin ve prednizon / prednizolon / metilprednizolon (CVP) ile
kombinasyon halinde 21 g�nl�k 8 d�ng�.
�dame
Kemoterapi (CHOP veya CVP veya bendamustin) ile kombinasyon halinde GAZYVA ind�ksiyon tedavisinde tam ya da k�smi ba�ar� sa�layan hastalar, idame tedavisi olarak 1000 mg GAZYVA'y� 2 y�l s�reyle her 2 ayda bir veya hastal�k progresyonuna kadar (hangisi daha �nce ger�ekle�irse) tek ajan (monoterapi) �eklinde almaya devam etmelidirler.
Rituximab ile birlikte kemoterapi uygulanm�� folik�ler lenfoma olgular�nda yan�ts�zl�k veya 6 ay i�erisinde n�ks geli�mesi durumunda
�nd�ksiyon (bendamustin ile kombinasyon �eklinde)
GAZYVA, bendamustin ile kombinasyon �eklinde 28 g�nl�k 6 d�ng� �eklinde uygulanmal�d�r.
�dame
Bendamustin ile kombinasyon �eklindeki GAZYVA ile ind�ksiyon tedavisine (�rn. ilk 6 tedavi d�ng�s�) tam veya k�smi yan�t veren veya hastal�klar� stabil olan hastalar, tek ajan olarak GAZYVA'y� 1000 mg'l�k dozda iki y�l s�reyle her 2 ayda bir veya hastal�k progresyonuna kadar (hangisi daha �nce ger�ekle�irse) idame tedavisi olarak almaya devam etmelidir.
Tablo 3. Folik�ler Lenfoma: �nd�ksiyon tedavisi s�ras�nda uygulanacak GAZYVA dozu
Siklus | Tedavi G�n� | GAZYVA Dozu |
D�ng�1 | 1. G�n | 1000 mg |
8. G�n | 1000 mg | |
15. G�n | 1000 mg | |
D�ng�2 – 6 yada 2-8 | 1. G�n | 1000 mg |
�dame | 2 y�l s�reyle her 2 ayda bir veya hastal�k progresyonuna kadar (hangisi daha �nce ger�ekle�irse) | 1000 mg |
Tedavinin s�resi
Yakla��k 6 ay s�ren ind�ksiyon tedavisi (bendamustin ile kombine edildi�inde her biri 28 g�n s�ren 6 GAZYVA tedavi d�ng�s� ya da CHOP veya CVP ile kombine edildi�inde her biri 21 g�n s�ren 8 GAZYVA tedavi d�ng�s�) ve iki y�l s�reyle her iki ayda bir veya hastal�k progresyonuna kadar (hangisi daha �nce ger�ekle�irse) uygulanacak idame tedavisini i�ermektedir.
Geciktirilen veya atlanan dozlar
Planlanan GAZYVA dozu atland��� takdirde m�mk�n olan en k�sa s�rede verilmelidir; doz atlanmamal�d�r ya da planlanan bir sonraki doza kadar beklenmemelidir. E�er D�ng�1, 8. g�n ya da D�ng�1, 15. g�nden �nce toksisite meydana gelirse, bu dozlar toksisite sorunu ��z�ld�kten sonra verilmelidir. Bu t�r �rneklerde, sonraki ziyaretlerin t�m� ve D�ng�2'nin ba�lang�c�, D�ng�1'deki gecikmeye uyumlu olmak i�in de�i�tirilecektir.
�dame s�ras�nda, takip eden dozlara ait orijinal dozlama plan� s�rd�r�lmelidir.
Tedavi s�ras�ndaki doz de�i�iklikleri (t�m endikasyonlar)
GAZYVA dozunun azalt�lmas� �nerilmemektedir.
Semptomatik advers olaylar�n (inf�zyon reaksiyonlar� dahil) y�netimi i�in a�a��daki paragrafa bak�n�z (�nf�zyonla �li�kili Reaksiyonlar�n Y�netimi veya B�l�m 4.4).
Uygulama �ekli
GAZYVA intraven�z kullan�m i�indir. Seyreltildikten sonra �zel bir yolla intraven�z inf�zyon �eklinde uygulanmal�d�r (bkz. B�l�m 6.6). GAZYVA inf�zyonlar�, IV pu�e veya bolus �eklinde uygulanmamal�d�r.
Uygulamadan �nce GAZYVA'n�n seyreltilmesine ili�kin talimatlar i�in bkz. B�l�m 6.6. �nf�zyon h�z�na ili�kin talimatlar Tablo 4-6'da g�sterilmektedir.
Kronik lenfositik l�semi (KLL)
Tablo 4. Kronik Lenfositik L�semi: �nf�zyon reaksiyonlar�/a��r� duyarl�l�k olmad��� durumda standart inf�zyon h�z� ve �nceki inf�zyonla meydana gelmi� bir IRR olmas� durumunda tavsiyeler
Siklus |
Tedavi G�n� | �nf�zyon h�z� Hastan�n tolere etti�i durumda, inf�zyon h�z� artt�r�labilir. �nf�zyon s�ras�nda meydana gelen IRR'lerin y�netimi i�in “IRR'lerin Y�netimi” k�sm�na bak�n�z. |
| 1. G�n (100 mg) | 4 saat boyunca 25 mg/saat h�z�nda uygulay�n�z. �nf�zyon h�z�n� artt�rmay�n�z. |
D�ng�1 |
2. G�n (veya 1. g�n�n devam�) (900 mg) | �nceki inf�zyon s�ras�nda IRR meydana gelmemi�se 50 mg/saat h�z�nda uygulay�n�z. �nf�zyon h�z�, maksimum h�z 400 mg/saat olacak �ekilde 30 dakikada bir 50 mg/saat art��lar�yla y�kseltilebilir. E�er bir hasta bir �nceki inf�zyonda bir IRR deneyimlemi�se, 25 mg / saat h�zda uygulamaya ba�lay�n�z. �nf�zyon h�z�, maksimum h�z 400 mg/saat olacak �ekilde 30 dakikada bir 50 mg/saat art��lar�yla y�kseltilebilir. |
| 8. G�n (1000 mg) | Son inf�zyon h�z�n�n 100 mg/saat veya �zerinde oldu�u �nceki inf�zyon s�ras�nda IRR meydana gelmemi�se, inf�zyonlar 100 mg/saat h�z�nda ba�lat�labilir ve maksimum 400 mg/saat olacak �ekilde 30 dakikada bir 100 mg/saat art��lar�yla y�kseltilebilir. |
15. G�n (1000 mg) | ||
D�ng�2-6 | 1. G�n (1000 mg) | |
|
| E�er bir hasta 50 mg/saat h�z�ndaki �nceki inf�zyonunda bir IRR deneyimlemi�se, inf�zyon h�z�, maksimum h�z 400 mg/saat olacak �ekilde 30 dakikada bir 50 mg/saat art��lar�yla y�kseltilebilir. |
Folik�ler Lenfoma (FL)
GAZYVA 1. D�ng�de standart inf�zyon h�z�nda uygulanmal�d�r (bkz. Tablo 5). 1. D�ng� s�ras�nda Derece ≥3 inf�zyonla ili�kili reaksiyonlar (IRR'ler) ya�amayan hastalarda, GAZYVA 2. D�ng�den itibaren k�sa (yakla��k 90 dakika) s�reli inf�zyon (SDI) olarak uygulanabilir (bkz. Tablo 6).
Tablo 5. Folik�ler Lenfoma: Standart inf�zyon h�z� ve �nceki inf�zyonla meydana gelmi� bir IRR olmas� durumunda tavsiyeler
Siklus |
Tedavi G�n� | �nf�zyon h�z� Hastan�n tolere etti�i durumda, inf�zyon h�z� artt�r�labilir. �nf�zyon s�ras�nda meydana gelen IRR'lerin y�netimi i�in “IRR'lerin Y�netimi” k�sm�na bak�n�z. |
D�ng�1 |
1. G�n (1000 mg) | Saatte 50 mg olarak uygulay�n�z. �nf�zyon h�z�, maksimum h�z 400 mg/saat olacak �ekilde 30 dakikada bir 50 mg/saat art��larla kademeli olarak y�kseltilebilir. |
8. G�n (1000 mg) | Son inf�zyon h�z�n�n 100 mg/saat veya �zerinde oldu�u �nceki inf�zyon s�ras�nda inf�zyonla ili�kili reaksiyon meydana gelmemi�se veya daha �nceki inf�zyonda Evre 1 IRR g�r�lm��se, inf�zyonlar 100 mg/saat h�z�nda ba�lat�labilir ve maksimum 400 mg/saat olacak �ekilde 30 dakikada bir 100 mg/saat art��larla y�kseltilebilir.
E�er hasta �nceki inf�zyonda Evre 2 veya daha y�ksek bir IRR deneyimlemi�se, 50 mg/saat h�z�nda uygulay�n�z. �nf�zyon h�z�, maksimum h�z 400 mg/saat olacak �ekilde 30 dakikada bir 50 mg/saat art��larla kademeli olarak y�kseltilebilir. | |
15. G�n (1000 mg) | ||
D�ng�2–6 ya da 2-8 |
1. G�n (1000 mg) | |
�dame | 2 y�l s�reyle her 2 ayda bir veya hastal�k progresyonuna kadar (hangisi daha �nce ger�ekle�irse) |
Tablo 6. Folik�ler lenfoma: K�sa s�reli inf�zyon h�z� ve �nceki inf�zyonda IRR olu�mas� durumunda �neriler
Siklus | Tedavi G�n� | �nf�zyon h�z� �nf�zyon s�ras�nda meydana gelen IRR'lerin y�netimi i�in “IRR'lerin Y�netimi” k�sm�na bak�n�z. |
D�ng�2–6 ya da 2-8 | 1. G�n (1000 mg) | D�ng� 1 s�ras�nda Derece ≥3 IRR olu�mad�ysa: 30 dakika boyunca 100 mg/saat, ard�ndan yakla��k 60 dakika boyunca 900 mg/saat.
Devam eden semptomlarla Derece 1-2 IRR veya �nceki SDI inf�zyonu s�ras�nda Derece 3 IRR meydana geldiyse, bir sonraki obinutuzumab inf�zyonunu standart h�zda uygulay�n (bkz. Tablo 5). |
�dame | 2 y�l s�reyle her 2 ayda bir veya hastal�k progresyonuna kadar (hangisi daha �nce ger�ekle�irse) |
�nf�zyonla �li�kili Reaksiyonlar�n Y�netimi (t�m endikasyonlar)
�nf�zyon reaksiyonlar�n�n y�netimi; a�a��da belirtildi�i gibi GAZYVA tedavisinin ge�ici olarak kesilmesini, inf�zyon h�z�n�n azalt�lmas�n� veya tedavinin sonland�r�lmas�n� gerektirebilir (ayr�ca bkz. B�l�m 4.4).
Evre 4 (ya�amsal tehlike): �nf�zyon durdurulmal� ve tedavi kal�c� olarak sonland�r�lmal�d�r.
Evre 3 (�iddetli): �nf�zyon ge�ici olarak durdurulmal� ve semptomlar tedavi edilmelidir. Semptomlar kaybolduktan sonra, �nceki h�z�n (inf�zyonla ili�kili reaksiyon olu�tu�u s�rada kullan�lan h�z�n) en fazla yar�s� h�z�nda inf�zyon yeniden ba�lat�labilir ve hastada IRR semptomlar� olu�muyorsa, tedavi dozu i�in uygun art��larda ve aral�klardaki inf�zyon h�z� art���na devam edilebilir (bkz. Tablo 4 ve 5). Dozu 2 g�nde uygulanan KLL hastalar� i�in, 1. g�nde (D�ng�1) inf�zyon h�z�, 1 saat sonra yeniden 25 mg/sa olarak y�kseltilebilir, ancak daha fazla art�r�lamaz. Hastada ikinci defa Evre 3 IRR meydana geldi�i takdirde inf�zyon durdurulmal� ve tedavi kal�c� olarak kesilmelidir.
Evre 1-2 (hafif ile orta): �nf�zyon h�z� azalt�lmal� ve semptomlar tedavi edilmelidir. Semptomlar kaybolduktan sonra, inf�zyona devam edilebilir ve hastada IRR semptomlar� olu�muyorsa, inf�zyon h�z�n�n art��� tedavi dozu i�in uygun art��larla ve aral�klarla s�rd�r�lebilir (bkz. Tablo 4 ve 5). Dozu 2 g�ne b�l�nerek uygulanan KLL hastalar� i�in,
1. g�n (D�ng�1) inf�zyon h�z�, 1 saat sonra yeniden 25 mg/sa olarak y�kseltilebilir, ancak daha fazla art�r�lamaz.
SDI s�ras�nda meydana gelen �nf�zyonla �li�kili Reaksiyonlar�n Y�netimi
Derece 4 (hayat� tehdit eden): �nf�zyon durdurulmal� ve tedavi kal�c� olarak kesilmelidir.
Derece 3 (�iddetli): �nf�zyon ge�ici olarak durdurulmal� ve semptomlar tedavi edilmelidir. Semptomlar d�zeldikten sonra, inf�zyon �nceki h�z�n yar�s�ndan (IRR'nin meydana geldi�i s�rada kullan�lan h�z) ve 400 mg/saat'ten fazla olmayacak �ekilde yeniden ba�lat�labilir.
�nf�zyona devam edildikten sonra hasta ikinci bir Derece 3 IRR ya�arsa, inf�zyon durdurulmal� ve tedavi kal�c� olarak kesilmelidir. Hasta inf�zyonu ba�ka Derece 3 IRR olmadan tamamlayabiliyorsa, bir sonraki inf�zyon standart h�zdan daha y�ksek olmayan bir h�zda verilmelidir.
Derece 1-2 (hafif ila orta): �nf�zyon h�z� azalt�lmal� ve semptomlar tedavi edilmelidir. Semptomlar d�zeldikten sonra inf�zyona devam edilebilir ve hasta herhangi bir IRR semptomu ya�amazsa, inf�zyon h�z� art��� tedavi dozuna uygun art��larla ve aral�klarla devam edebilir (bkz. Tablo 5-6).
�zel pop�lasyonlara ili�kin ek bilgiler B�brek yetmezli�i
Hafif ile orta �iddette b�brek yetmezli�i (kreatinin klerensi [KrKl] >30-89 mL/dakika) olan hastalarda doz ayarlamas� gerekli de�ildir (bkz. B�l�m 5.2). �iddetli b�brek yetmezli�i (kreatinin klerensi < 30 mL/dakika) olan hastalarda GAZYVA'n�n g�venlili�i ve etkilili�i belirlenmemi�tir.
Karaci�er yetmezli�i
Karaci�er fonksiyonu bozulmu� hastalarda GAZYVA'n�n g�venlili�i ve etkilili�i belirlenmemi�tir. Spesifik doz �nerileri yap�lamamaktad�r.
Pediyatrik pop�lasyon
�ocuklarda ve 18 ya��n alt�ndaki adolesanlarda GAZYVA'n�n g�venlili�i ve etkilili�i belirlenmemi�tir. Veri bulunmamaktad�r. G�venlilik ve etkilili�e ili�kin very eksikli�i nedeniyle �ocuklarda ve 18 ya��n alt�ndaki adolesanlarda GAZYVA'n�n kullan�lmas� tavsiye edilmemektedir.
Geriyatrik pop�lasyon
Ya�l� hastalarda doz ayarlamas� gerekli de�ildir (bkz. B�l�m 5.2).
4.3. Kontrendikasyonlar
Etkin madde
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Daha �nce tedavi uygulanm�� folik�ler lenfomal� hastalarda bir alt grup analizine dayanarak, FLIPI d���k riskli (0-1) hastalardaki etkililik verileri �u anda yetersizdir (bkz. B�l�m 5.1). Bu hastalar i�in bir tedavi belirlerken, GAZYVA ile birlikte kemoterapi uygulamas�n�n genel g�venlilik profili ve hastaya �zg� durumu dikkatle de�erlendirilmelidir.

UYARILAR
�nf�zyonla ili�kili reaksiyonlar (IRR)
GAZYVA alan hastalarda en s�k g�zlenen advers ila� reaksiyonlar� (A�R'ler), a��rl�kl� olarak ilk 1000 mg'nin inf�zyonu s�ras�nda meydana gelen IRR'ler olmu�tur. Hastalar�n b�y�k b�l�m�nde IRR'ler, hafif ile orta �iddette olmu� ve ilk inf�zyonun yava�lat�lmas�yla veya ge�ici olarak durdurulmas�yla kontrol alt�na al�nabilmi�tir ancak semptomatik tedavi gerektiren �iddetli ve ya�amsal tehlike te�kil eden IRR'ler de bildirilmi�tir.
Evre 4 inf�zyon reaksiyonu i�in inf�zyon durdurulmal� ve s�resiz olarak sonland�r�lmal�d�r. Evre 3 inf�zyon ili�kili reaksiyonlar i�in inf�zyon ge�ici olarak kesilmeli ve semptomlar�n tedavisi i�in uygun ila� uygulanmal�d�r.
A�a��daki durumlarda, hastalara ba�ka GAZYVA inf�zyonu verilmemelidir:
Akut hayat� tehdit eden solunum semptomlar�,
Evre 4 (hayat� tehdit eden) inf�zyon reaksiyonlar� veya
Evre 3 (uzun s�reli/tekrarlayan) inf�zyon reaksiyonlar�n�n ikinci kez olu�mas� (ilk inf�zyonun s�rd�r�lmesinin ard�ndan veya takip eden inf�zyon s�ras�nda).
T�m�r Lizis Sendromu (TLS)
GAZYVA ile TLS bildirilmi�tir. Risk alt�nda oldu�u d���n�len t�m hastalar, tedavinin ilk g�nlerinde, �zellikle b�brek fonksiyonlar�, potasyum ve �rik asit d�zeyleri a��s�ndan dikkatle izlenmelidir. Standart uygulamaya y�nelik t�m ek k�lavuzlar takip edilmelidir. TLS'nin tedavisi i�in elektrolit anormallikleri d�zeltilmeli, b�brek fonksiyonu ve s�v� dengesi izlenmeli ve gerekti�inde diyaliz dahil, destekleyici bak�m uygulanmal�d�r.
Progresif Multifokal L�koensefalopati (PML)
GAZYVA ile tedavi uygulanan hastalarda PML vakalar� bildirilmi�tir (bkz. B�l�m 4.4 & B�l�m 4.8).
Hepatit B Vir�s (HBV) Reaktivasyonu
GAZYVA da dahil olmak �zere Anti-CD20 antikorlar�yla tedavi edilen hastalarda baz� durumlarda fulminan hepatit, hepatik yetmezlik ve �l�mle sonu�lanan HBV reaktivasyonu meydana gelebilir (bkz. B�l�m 4.8). GAZYVA ile tedaviye ba�lanmadan �nce t�m hastalarda Hepatit B vir�s taramas� yap�lmal�d�r. Aktif hepatit B hastal��� olan hastalar GAZYVA ile tedavi edilmemelidir.
�nf�zyonla ili�kili reaksiyonlar (IRR)
GAZYVA alan hastalarda en s�k g�zlenen advers ila� reaksiyonlar� (A�R'ler), a��rl�kl� olarak ilk 1000 mg'nin inf�zyonu s�ras�nda meydana gelen IRR'ler olmu�tur. �nf�zyonla ili�kili reaksiyonlar, ayn� zamanda GAZYVA ile tedavi edilen hastalarda da bildirilen sitokin sal�verilmesi sendromuyla da ili�kili olabilir. IRR'lerin �nlenmesi i�in B�l�m 4.2'de a��klanan �nlemlerin (yeterli kortikosteroid, oral analjezik/anti-histaminik, ilk inf�zyon sabah�nda antihipertansif ilac�n atlanmas� ve 2 g�n s�reyle verilen 1. D�ng�1. g�n dozu) birlikte uyguland��� KLL hastalar�nda t�m Evre'lerdeki IRR'lerde azalma g�zlenmi�tir. Evre 3-4 IRR oranlar� (g�rece az say�da hastay� temel alan), hafifletici �nlemler al�nmadan �nce ve al�nd�ktan sonra benzerdir. IRR'lerin azalt�lmas�na y�nelik hafifletici �nlemler izlenmelidir (bkz. B�l�m 4.2). �nf�zyona ba�l� semptomlar�n insidans� ve �iddeti, ilk 1000 mg'nin inf�zyonunu takiben �nemli �l��de azalm�� ve hastalar�n bir�o�unda, takip eden GAZYVA inf�zyonlar� s�ras�nda IRR meydana gelmemi�tir (bkz. B�l�m 4.8).
Hastalar�n b�y�k b�l�m�nde IRR'ler, endikasyondan ba��ms�z olarak hafif ile orta �iddette olmu� ve ilk inf�zyonun yava�lat�lmas�yla veya ge�ici olarak durdurulmas�yla kontrol alt�na al�nabilmi�tir ancak semptomatik tedavi gerektiren �iddetli ve ya�amsal tehlike te�kil eden IRR'ler de bildirilmi�tir. IRR'ler imm�noglob�lin E (IgE) arac�l� alerjik reaksiyonlardan (�rn. anafilaksi) klinik olarak ay�rt edilemeyebilir. T�m�r y�k� y�ksek ve/veya KLL'de dola��mdaki lenfosit say�s� y�ksek (>25 x 10/L) olan hastalar �iddetli IRR'ler a��s�ndan y�ksek risk alt�nda olabilir. Renal yetmezli�i bulunan hastalar (KrKl <50 mL/dk) ve hem K�m�latif Hastal�k Derecelendirme �l�e�i (CIRS) >6 hem de KrKl <70 mL/dk olan hastalar, �iddetli IRR'ler de dahil olmak �zere daha y�ksek IRR riski alt�ndad�r (bkz. B�l�m 4.8). IRR'lerin y�netimi i�in “Pozoloji ve uygulama �ekli” k�sm�na bak�n�z.
A�a��daki durumlarda, hastalara ba�ka GAZYVA inf�zyonu verilmemelidir:
Akut hayat� tehdit eden solunum semptomlar�,
Evre 4 (hayat� tehdit eden) inf�zyon reaksiyonlar� veya
Evre 3 (uzun s�reli/tekrarlayan) inf�zyon reaksiyonlar�n�n ikinci kez olu�mas� (ilk inf�zyonun s�rd�r�lmesinin ard�ndan veya takip eden inf�zyon s�ras�nda).
�nceden kardiyak veya pulmoner hastal�klar� bulunan hastalar, inf�zyon boyunca ve inf�zyon sonras� d�nemde dikkatle izlenmelidir. GAZYVA intraven�z inf�zyonlar� s�ras�nda hipotansiyon olu�abilir. Bu nedenle, her GAZYVA inf�zyonundan �nce 12 saat boyunca ve inf�zyon s�ras�nda ve uygulaman�n ard�ndan ilk saat boyunca antihipertansif tedavilerin durdurulmas� d���n�lmelidir. Hipertansif kriz a��s�ndan akut risk alt�ndaki hastalar,
antihipertansif ila�lar�n�n durdurulmas�na ili�kin yararlar ve riskler a��s�ndan de�erlendirilmelidir.
Anafilaksi dahil a��r� duyarl�l�k reaksiyonlar�
GAZYVA ile tedavi uygulanan hastalarda ani (�rn. anafilaksi) ve gecikmeli (�rn. serum bulant�s�) a��r� duyarl�l�k reaksiyonlar� bildirilmi�tir. A��r� duyarl�l���n IRR'lerden ay�rt edilmesi g�� olabilir. A��r� duyarl�l�k belirtileri �nceki maruziyetten sonra ve �ok nadiren ilk inf�zyonla ortaya ��kabilir. �nf�zyon s�ras�nda veya sonras�nda a��r� duyarl�l�k reaksiyonundan ��pheleniliyorsa, inf�zyon durdurulmal� ve tedavi s�resiz olarak sonland�r�lmal�d�r. Obinutuzumaba kar�� bilinen a��r� duyarl�l��� olan hastalara tedavi uygulanmamal�d�r (bkz. B�l�m 4.3).
T�m�r lizis sendromu (TLS)
GAZYVA ile TLS bildirilmi�tir. TLS a��s�ndan risk alt�nda oldu�u d���n�len hastalara (�rn. t�m�r y�k� y�ksek olan ve/veya dola��mdaki lenfosit say�s� y�ksek olan [>25 x 10/L] ve/veya b�brek yetmezli�i [KrKl <70 mL/dk] olan hastalara), profilaksi uygulanmal�d�r. Profilakside, standart uygulama do�rultusunda GAZYVA inf�zyonundan 12-24 saat �nce ba�lat�lmak �zere yeterli hidrasyon sa�lanarak ve �rikostatiklerin (�rn. allopurinol) veya �rat oksidat (�rn. rasburikaz) gibi uygun bir alternatif tedavi uygulanmal�d�r (bkz. B�l�m 4.2). Risk alt�nda oldu�u d���n�len t�m hastalar, tedavinin ilk g�nlerinde, �zellikle b�brek fonksiyonlar�, potasyum ve �rik asit d�zeyleri a��s�ndan dikkatle izlenmelidir. Standart uygulamaya y�nelik t�m ek k�lavuzlar takip edilmelidir. TLS'nin tedavisi i�in elektrolit anormallikleri d�zeltilmeli, b�brek fonksiyonu ve s�v� dengesi izlenmeli ve gerekti�inde diyaliz dahil, destekleyici bak�m uygulanmal�d�r.
N�tropeni
GAZYVA tedavisi s�ras�nda febril n�tropeni dahil �iddetli ve ya�am� tehdit eden n�tropeni bildirilmi�tir. N�tropeni olu�an hastalar, bu durum ortadan kalkana kadar d�zenli laboratuvar testleriyle yak�ndan izlenmelidir. Tedavi gerekti�inde, yerel k�lavuzlara uygun �ekilde uygulanmal� ve gran�losit koloni uyar�c� fakt�rlerin (G-CSF) uygulanmas� d���n�lmelidir. E� zamanl� enfeksiyon belirtileri, uygun �ekilde tedavi edilmelidir. �iddetli veya ya�am� tehdit eden n�tropeni vakalar�nda dozun geciktirilmesi d���n�lmelidir. �iddetli ve 1 haftadan uzun s�ren n�tropenisi olan hastalara Evre 1 veya 2 d�zelme sa�lan�ncaya kadar tedavi s�resince antimikrobiyal profilaksi verilmesi �iddetle �nerilir. Antiviral ve antifungal profilaksi de d���n�lmelidir (bkz. B�l�m 4.2). Ge� ba�lang��l� n�tropeni (tedavinin sonlanmas�ndan 28 g�n sonra olu�an) veya uzun s�reli n�tropeni de (tedavinin tamamland�ktan/sonland�r�ld�ktan sonra 28 g�nden fazla s�ren) bildirilmi�tir. Renal yetmezli�i (KrKl < 50 mL/dk) olan hastalar, daha y�ksek n�tropeni riski alt�ndad�r (bkz. B�l�m 4.8).
Trombositopeni
GAZYVA tedavisi s�ras�nda akut trombositopeni (inf�zyondan sonra 24 saat i�inde olu�an) dahil, �iddetli ve ya�am� tehdit eden trombositopeni g�zlenmi�tir. Renal yetmezli�i (KrKl < 50 mL/dk) olan hastalar daha y�ksek trombositopeni riski alt�ndad�r (bkz. B�l�m 4.8). GAZYVA ile tedavi edilen hastalarda D�ng�1'de �l�mle sonu�lanan hemoraji vakalar� da bildirilmi�tir. Trombositopeni ve hemoraji vakalar� aras�nda kesin bir ili�ki kurulmam��t�r.
Hastalar, �zellikle de birinci d�ng� s�ras�nda trombositopeni i�in yak�ndan izlenmeli, durum ortadan kalk�ncaya kadar laboratuvar testleri yap�lmal� ve �iddetli, ya�am� tehdit eden
trombositopeni durumunda dozun geciktirilmesi d���n�lmelidir. Kurumsal uygulamaya g�re kan �r�nlerinin transf�zyonu (yani trombosit transf�zyonu), tedavi uygulayan hekimin karar�na ba�l�d�r. �zellikle birinci d�ng� s�ras�nda platelet inhibit�rleri ve antikoag�lanlar gibi trombositopeni ile ili�kili olaylar� k�t�le�tirme olas�l��� bulunan herhangi bir e�zamanl� terapinin kullan�m� da g�z �n�nde bulundurulmal�d�r.
Dissemine intravask�ler koag�lasyon (yayg�n damar i�i p�ht�la�ma) dahil p�ht�la�ma bozukluklar�
�l�mc�l olaylar� i�eren dissemine intravask�ler koag�lasyon (D�K), klinik �al��malarda ve GAZYVA alan hastalarda pazarlama sonras� g�zetimde rapor edilmi�tir. Vakalar�n �o�u, trombositlerde ve laboratuvar p�ht�la�ma parametrelerinde subklinik (asemptomatik) de�i�iklikler ile ilk inf�zyondan sonraki 1-2 g�n i�inde meydana gelen ve genellikle bir ila iki hafta i�inde ortaya ��kan spontan iyile�me ile ilac�n kesilmesini veya �zel m�dahale gerektirmeyen, belirgin olmayan D�K i�ermi�tir. Baz� vakalarda, olaylar IRR'ler ve/veya TLS ile ili�kilendirilmi�tir. D�K i�in hi�bir spesifik temel risk fakt�r� tan�mlanmam��t�r. Belirgin olmayan D�K oldu�undan ��phelenilen hastalar, trombositler ve belirgin D�K belirti ve semptomlar� i�in klinik g�zlem dahil olmak �zere p�ht�la�ma parametreleri ile yak�ndan izlenmelidir. Belirgin D�K ��phesinin ilk ba�lang�c�nda GAZYVA kesilmeli ve uygun tedavi ba�lat�lmal�d�r.
�nceden var olan kalp hastal�klar�n�n k�t�le�mesi
Altta yatan kalp hastal��� olan hastalarda, GAZYVA tedavisi uyguland���nda atriyal fibrilasyon ve ta�iaritmi gibi aritmiler, angina pektoris, akut koroner sendrom, miyokard infarkt�s� ve kalp yetmezli�i olu�mu�tur (bkz. B�l�m 4.8). Bu olaylar inf�zyonla ili�kili reaksiyonun bir par�as� olabilir ve �l�me yol a�abilir. Bu nedenle kalp hastal��� �yk�s� olan hastalar yak�ndan izlenmelidir. Ayr�ca bu hastalar, potansiyel a��r� s�v� y�klenmesini �nlemek i�in dikkatli �ekilde hidrate edilmelidir.
Enfeksiyonlar
GAZYVA, aktif enfeksiyon varl���nda uygulanmamal�d�r ve tekrarlayan veya kronik enfeksiyon �yk�s� olan hastalarda GAZYVA kullan�lmas� d���n�l�yorsa dikkatli olunmal�d�r. GAZYVA tedavisi s�ras�nda ve tedavinin tamamlanmas� ard�ndan ciddi bakteriyel, fungal ve yeni veya reaktif viral enfeksiyonlar olu�abilir. �l�mle sonu�lanan enfeksiyonlar bildirilmi�tir.
CIRS >6 ve KrKl <70 mL/dk olan hastalar, �iddetli enfeksiyonlar da dahil olmak �zere daha y�ksek enfeksiyon riski alt�ndad�r (bkz. B�l�m 4.8). Takip dahil, folik�ler lenfoma �al��malar�n�n her faz�nda y�ksek enfeksiyon insidans� g�r�lm��t�r. Takip faz� s�ras�nda ind�ksiyon faz�nda GAZYVA ile birlikte bendamustin tedavisi alan hastalarda Evre 3-5 enfeksiyonlar� daha fazla g�r�lm��t�r.
Hepatit B vir�s (HBV) reaktivasyonu
GAZYVA da dahil olmak �zere Anti-CD20 antikorlar�yla tedavi edilen hastalarda baz� durumlarda fulminan hepatit, hepatik yetmezlik ve �l�mle sonu�lanan HBV reaktivasyonu meydana gelebilir (bkz. B�l�m 4.8). GAZYVA ile tedaviye ba�lanmadan �nce t�m hastalarda Hepatit B vir�s taramas� yap�lmal�d�r.
Tarama, en az�ndan hepatit B y�zey antijen (HBsAg) durumu ve hepatit B �ekirdek antikor (HBcAb) durumunu i�ermelidir. Bunlar, yerel k�lavuzlara uygun olarak di�er uygun
belirte�lerle tamamlanabilir. Aktif hepatit B hastal��� olan hastalar GAZYVA ile tedavi edilmemelidir. Pozitif hepatit B serolojisi olan hastalar, tedaviye ba�lanmadan �nce bir karaci�er hastal�klar� uzman�yla g�r��meli ve hepatit reaktivasyonunu �nlemek amac�yla yerel t�bbi standartlara uyularak izlenmeli ve kontrol alt�nda tutulmal�d�r.
Progresif multifokal l�koensefalopati (PML)
GAZYVA ile tedavi uygulanan hastalarda PML vakalar� bildirilmi�tir (bkz. B�l�m 4.8). Yeni ba�lam�� veya �nceden var olan n�rolojik belirtiler g�r�len hastalarda PML tan�s� dikkate al�nmal�d�r. PML semptomlar� spesifik de�ildir ve beynin etkilenen b�lgesine g�re farkl�l�k g�sterebilir. Kortikospinal kanal bulgular� olan motor semptomlar (�rn. kas zay�fl���, paraliz ve duyusal bozukluklar), duyusal anormallikler, serebellar semptomlar ve g�rme alan� defektleri yayg�nd�r. “Kortikal” kabul edilen baz� belirtiler/semptomlar (�rn. afazi veya g�rsel-uzaysal disoryantasyon) olu�abilir. PML'nin de�erlendirilmesi bir n�rolog ile kons�ltasyonu, beyin manyetik rezonans g�r�nt�lemeyi (MRG) ve lomber ponksiyonu (John Cunningham viral DNA i�in beyin omurilik s�v�s� testi) i�erir fakat bunlarla s�n�rl� de�ildir. GAZYVA tedavisi, olas� PML incelemesi s�ras�nda durdurulmal�d�r ve PML'nin do�rulanmas� halinde s�resiz olarak sonland�r�lmal�d�r. Ayr�ca e� zamanl� kemoterapinin veya imm�nosupresif tedavinin sonland�r�lmas� veya azalt�lmas� dikkate al�nmal�d�r. Hasta, PML'nin de�erlendirilmesi ve tedavisi i�in bir n�rologa sevk edilmelidir.
�mm�nizasyon
GAZYVA tedavisi ard�ndan canl� veya aten�e viral a��larla imm�nizasyonun g�venlili�i incelenmemi�tir ve tedavi s�ras�nda ve B-h�cre geri kazan�m� sa�lanana kadar canl� vir�s a��lar�yla a��lama �nerilmemektedir.
Anne karn�nda obinutuzumab maruziyeti ve bebeklerin canl� vir�s a��lar�yla a��lanmas�
Gebelik s�ras�nda GAZYVA'ya maruz kalan annelerin bebeklerinde B h�cre deplesyonu meydana gelme potansiyelinden dolay� bebekler B h�cre deplesyonu a��s�ndan izlenmeli ve canl� vir�s a��lar�yla a��lamalar, bebe�in B h�cre say�s�n�n geri kazan�m� sa�lanana kadar ertelenmelidir (bkz. B�l�m 4.6). A��n�n g�venlili�i ve zamanlamas� i�in bebe�in hekimiyle g�r���lmelidir (bkz. B�l�m 4.6).
Biyolojik t�bbi �r�nlerin izlenebilirli�ini artt�rmak i�in uygulanan �r�n�n ticari ad� ve seri numaras� hastan�n dosyas�na a��k �ekilde kaydedilmelidir (veya belirtilmelidir).
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Bendamustin, CHOP (siklofosfamit, doksorubisin, vinkristin ve prednizolon), FC (fludarabin, siklofosfamit) ve klorambusil ile birlikte GAZYVA kullan�m� i�in s�n�rl� say�da ila� etkile�im alt �al��mas� yap�lmas�na kar��n, resmi ila� etkile�im �al��malar� ger�ekle�tirilmemi�tir.
Di�er e�zamanl� kullan�lan t�bbi �r�nlerle etkile�im riski g�z ard� edilemez. Farmakokinetik etkile�imler
Obinutuzumab, sitokrom P450 (CYP450), �ridin difosfat glukuroniltransferaz (UGT) enzimleri ve P-glikoprotein gibi ta��y�c�lar�n substrat�, inhibit�r� veya ind�kleyicisi de�ildir. Bu nedenle, bu enzim sistemleri taraf�ndan metabolize edildi�i bilinen t�bbi �r�nlerle farmakokinetik etkile�im beklenmemektedir.
GAZYVA'n�n bendamustin, FC, klorambusil veya CHOP'nin tekli bile�enleriyle e�zamanl� kullan�m�, bu ila�lar�n farmakokineti�i �zerinde hi�bir etki g�stermemi�tir. Ayr�ca bendamustin, FC, klorambusil veya CHOP'un, GAZYVA'n�n farmakokineti�i �zerine belirgin bir etkisi olmam��t�r.
Farmakodinamik etkile�imler:
Obinutuzumab�n immunosupresif etkisinden dolay�, tedavi s�ras�nda ve B h�cresi geri kazan�m�na kadar canl� vir�s a��lar� ile a��lanma tavsiye edilmemektedir (bkz. B�l�m 4.4).
Obinutuzumab�n klorambusil veya bendamustin ile kombinasyonu, n�tropeniyi artt�rabilir (bkz. B�l�m 4.4).
�zel pop�lasyonlara ili�kin ek bilgiler Herhangi bir etkile�im �al��mas� yap�lmam��t�r. Pediyatrik pop�lasyon
Herhangi bir etkile�im �al��mas� yap�lmam��t�r.
4.6. Gebelik ve laktasyon
Gebelik kategorisi: C
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
�ocuk do�urma potansiyeli bulunan kad�nlar, GAZYVA tedavisi s�ras�nda ve tedavi bitiminden sonraki 18 ay boyunca etkili bir do�um kontrol y�ntemi kullanmal�d�r.
Gebelik d�nemi
Hayvanlar �zerinde yap�lan �al��malar, gebelik ve – veya embriyonal / fetal geli�im ve – veya do�um ve – veya do�um sonras� geli�im �zerindeki etkiler bak�m�ndan yetersizdir (bkz. B�l�m 5.3). �nsanlara y�nelik potansiyel risk bilinmemektedir. GAZYVA gerekli olmad�k�a; olas� yarar�, potansiyel riski a�mad��� s�rece, gebelik d�neminde kullan�lmamal�d�r.
Sinomolgus maymunlarda yap�lan bir �reme �al��mas�, embriyofetal toksisite veya teratojenik etkilere ili�kin kan�t g�stermemi�, ancak yavrularda B lenfositlerin tam deplesyonuyla sonu�lanm��t�r.
B-h�cre say�lar� yavrularda normal d�zeylere d�nm�� ve imm�nolojik fonksiyon do�umdan sonra 6 ay i�inde geri kazan�lm��t�r. Yavrulardaki serum obinutuzumab konsantrasyonlar�, annelerde do�umdan sonra 28. g�ndeki konsantrasyonlarla ayn�d�r. Ayn� g�n i�erisinde s�tte bulunan konsantrasyonlar �ok d���k olup, obinutuzumab�n plasentaya ge�ti�ine i�aret etmektedir (bkz. B�l�m 5.3). Gebe kad�nlarda obinutuzumab kullan�m�na ili�kin veri yoktur.
Gebelik s�ras�nda maruz kalma durumunda bebeklerde �r�n�n farmakolojik �zelliklerinden �t�r� B h�cre deplesyonu beklenebilir. Gebelik s�ras�nda GAZYVA'ya maruz kalan annelerin
bebeklerinde canl� a��larla a��laman�n, bebe�in B h�cre d�zeyleri normal aral��a ula��ncaya kadar ertelenmesi d���n�lmelidir (bkz. B�l�m 4.4).
Laktasyon d�nemi
Hayvanlar �zerinde yap�lan �al��malar, obinutuzumab�n anne s�t�ne ge�ti�ini g�stermi�tir (bkz. B�l�m 5.3).
�nsan immunoglob�lin G'nin (IgG) anne s�t�ne ge�mesi ve emilim potansiyelinin ve bebe�e zarar�n�n bilinmemesi nedeniyle, kad�nlara GAZYVA tedavisi s�ras�nda ve son GAZYVA dozundan sonra 18 ay boyunca emzirmemeleri �nerilmelidir.
�reme yetene�i / Fertilite
Hayvanlarda GAZYVA'n�n fertilite �zerindeki etkisini de�erlendirmek i�in spesifik �al��malar yap�lmam��t�r. Sinomolgus maymunlar�nda yap�lan tekrarl� doz toksisite �al��malar�nda erkek ve di�i �reme organlar� �zerinde advers etki g�zlenmemi�tir (bkz. B�l�m 5.3).
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
GAZYVA'n�n, ara� ve makine kullan�m� �zerinde etkisi yoktur veya g�z ard� edilebilir. �lk GAZYVA inf�zyonunda IRR'ler �ok yayg�nd�r ve inf�zyona ba�l� semptomlarla kar��la�an hastalara, semptomlar ortadan kalkana kadar ara� veya makine kullanmamalar� �nerilmelidir.
4.8. �stenmeyen etkiler
G�venlilik Profilinin �zeti
Bu b�l�mde a��klanan advers ila� reaksiyonlar� (A�R'ler) �� pivotal klinik �al��mada FL dahil indolent Hodgkin d��� lenfomaya (iNHL) y�nelik ind�ksiyon, idame ve takip esnas�nda ve KLL'ye y�nelik tedavi ve takip esnas�nda tespit edilmi�tir:
BO21004/CLL11 (N=781): Daha �nce tedavi edilmemi� KLL'si olan hastalar
BO21223/GALLIUM (N=1390): Daha �nce tedavi edilmemi� iNHL'si olan hastalar (hastalar�n %86's�nda FL oldu�u g�r�lm��t�r)
GAO4753g/GADOLIN (N=409): Rituximab veya rituximab i�eren bir rejimle tedavi esnas�nda veya tedaviden sonraki 6 ayda yan�t vermeyen veya progresyon g�steren iNHL'li hastalar (�al��madaki hastalar�n %81'i FL hastas�yd�).
Bu �al��malarda GAZYVA KLL i�in klorambusil ile kombinasyon halinde ve iNHL i�in bendamustin, CHOP veya CVP ile kombinasyon halinde ve ard�ndan uygulanan GAZYVA idame tedavisi olarak incelenmi�tir. BO21223/GALLIUM and GAO4753g/GADOLIN �al��malar�na FL dahil iNHL'si olan hastalar al�nm��t�r. Dolay�s�yla, en kapsaml� g�venlilik bilgisini sa�lamak �zere b�t�n �al��ma pop�lasyonu (iNHL pop�lasyonu) �zerinde a�a��da belirtilen A�R'lere y�nelik analiz ger�ekle�tirilmi�tir.
Tablo 7'de pivotal �al��malarda (BO21004/CLL11, BO21223/GALLIUM, GAO4753g/GADOLIN) a�a��dakiler �zerinde yap�lan en az bir pivotal �al��madaki ilgili kar��la�t�rma kollar�na k�yasla daha y�ksek insidansta (≥%2 oran�nda fark) ger�ekle�en A�R'ler �zetlenmi�tir:
Tek ba��na klorambusil veya rituximab + klorambusil alanlara k�yasla GAZYVA + klorambusil alan KLL'li hastalar (�al��ma BO21004/CLL11)
Daha �nce tedavi uygulanmam�� iNHL hastalar�nda GAZYVA + kemoterapi (bendamustin, CHOP, CVP) uygulanmas�n� takiben yan�t al�nan hastalarda GAZYVA idamesinin uygulanmas�na kar�� rituximab + kemoterapi ve sonras�nda yan�t al�nan hastalarda rituximab idamesinin uygulanmas� (�al��ma BO21223/GALLIUM)
Tek ba��na bendamustine k�yasla GAZYVA + bendamustin ve ard�ndan baz� hastalara olmak �zere GAZYVA idame tedavisi uygulanan, rituximab veya rituximab i�eren bir rejimle tedavi esnas�nda veya tedaviden sonraki 6 ayda yan�t vermeyen veya progresyon g�steren iNHL hastalar� (�al��ma GAO4753g/GADOLIN)
Tablo 7'de sunulan s�kl�klar (b�t�n dereceler ve 3-5. Derece) �� �al��man�n herhangi birinde ilgili A�R i�in bildirilen en y�ksek s�kl�klard�r.
S�kl�klar ��yle tan�mlanm��t�r; �ok yayg�n (≥1/10), yayg�n (≥1/100 ila <1/10), yayg�n olmayan (≥1/1.000 ila <1/100), seyrek (≥1/10.000 ila <1/1.000) ve �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). Her s�kl�k gruplamas� aras�ndaki advers reaksiyonlar, azalan ciddiyet s�ras�na g�re sunulmu�tur.
Tablo 7. GAZYVA + kemoterapi* alan hastalarda y�ksek insidansla ( kar��la�t�rma koluna kar��n ≥%2 fark) bildirilen A�R'lerin �zeti *
S�kl�k | T�m Evreler GAZYVA + kemoterapi* (KLL, iNHL)'yi takiben GAZYVA idamesi (iNHL) | Evre 3-5† GAZYVA + kemoterapi* (KLL, iNHL)'yi takiben GAZYVA idamesi (iNHL) |
Enfeksiyonlar ve enfestasyonlar | ||
�ok yayg�n | �st solunum yolu enfeksiyonu, sin�zit, idrar yolu enfeksiyonu, pn�moni, herpes zoster, nazofarenjit |
|
Yayg�n | Oral herpes, rinit, farenjit, akci�er enfeksiyonu, grip, | �drar yolu enfeksiyonu, pn�moni, akci�er enfeksiyonu, �st solunum yolu enfeksiyonu, sin�zit, herpes zoster |
Yayg�n olmayan |
| Nazofarenjit, rinit, grip, oral herpes |
(Kist ve polipler de dahil olmak �zere) iyi huylu ve k�t� huylu neoplazmalar | ||
Yayg�n | Yass� h�creli cilt kanseri, Bazal h�creli kanser | Yass� h�creli cilt kanseri, bazal h�creli kanser |
Kan ve lenf sistemi hastal�klar� | ||
�ok yayg�n | N�tropeni, trombositopeni, anemi, l�kopeni | N�tropeni, trombositopeni |
Yayg�n | Febril n�rtopeni | Anemi, l�kopeni, Febril n�tropeni |
Yayg�n olmayan | Dissemine intravask�ler koag�lasyon |
|
Metabolizma ve beslenme hastal�klar� | ||
Yayg�n | T�m�r lizis sendromu, hiper�risemi, hipokalemi | T�m�r lizis sendromu, hipokalemi |
Yayg�n olmayan |
| Hiper�risemi |
Psikiyatrik hastal�klar | ||
�ok yayg�n | Uykusuzluk |
|
Yayg�n | Depresyon, anksiyete |
|
Yayg�n olmayan |
| Uykusuzluk, depresyon, anksiyete |
Sinir sistemi hastal�klar� | ||
�ok yayg�n | Ba� a�r�s� |
|
Yayg�n olmayan |
| Ba� a�r�s� |
Kardiyak hastal�klar� | ||
Yayg�n | Atriyal fibrilasyon | Atriyal fibrilasyon |
|
|
|
Vask�ler hastal�klar� | ||
Yayg�n | Hipertansiyon | Hipertansiyon |
Solunum, g���s bozukluklar� ve mediastinal hastal�klar | ||
�ok yayg�n | �ks�r�k |
|
Yayg�n | Burun t�kan�kl���, rinore, orofarenjial a�r� |
|
Yayg�n olmayan |
| �ks�r�k, orofarenjial a�r� |
Gastrointestinal hastal�klar� | ||
�ok yayg�n | Diyare, jonstipasyon |
|
Yayg�n | Haz�ms�zl�k, hemoroid | Diyare |
Yayg�n olmayan |
| Konstipasyon, hemoroid |
Deri ve deri alt� doku hastal�klar� | ||
�ok yayg�n | Alopesi, ka��nt� |
|
Yayg�n | Egzema |
|
Yayg�n olmayan |
| Ka��nt� |
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar� | ||
�ok yayg�n | Artralji, s�rt a�r�s�, ekstremitelerde a�r� |
|
Yayg�n | Kas-iskelet g���s a�r�s�, kemik a�r�s� | Ekstremitelerde a�r� |
Yayg�n olmayan |
| Artralji, s�rt a�r�s�, kas-iskelet g���s a�r�s�, kemik a�r�s� |
B�brek ve idrar yolu hastal�klar� | ||
Yayg�n | Dis�ri, idrar tutamama |
|
Yayg�n olmayan |
| Dis�ri, idrar tutamama |
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar� | ||
�ok yayg�n | Pireksi, asteni, yorgunluk |
|
Yayg�n | G���s a�r�s� | Pireksi, asteni, yorgunluk |
Yayg�n olmayan |
| G���s a�r�s� |
Ara�t�rmalar | ||
Yayg�n | Beyaz kan h�cre say�s�nda azalma, n�trofil say�s�nda azalma, kilo art��� | Beyaz kan h�cre say�s�nda azalma, n�trofil say�s�nda azalma |
Yaralanma ve zehirlenme | ||
�ok yayg�n | �nf�zyonla ili�kili reaksiyonlar | �nf�zyonla ili�kili reaksiyonlar |
# Daha y�ksek insidansl� (tedavi kollar� aras�nda ≥%2'lik fark). Sadece �al��malarda en �ok g�r�len s�kl�klar rapor edilmi�tir (BO21004/daha �nce tedavi edilmemi� KLL, BO21223/daha �nce tedavi edilmemi� ilerlemi� iNHL ve GAO4753g/rituximab refrakter iNHL)
## GAZYVA alan hastalarda klinik �al��malarda ve pazarlama sonras� g�zetimde �l�mc�l olaylar dahil dissemine intravask�ler koag�lasyon (D�K) bildirilmi�tir (bkz. B�l�m 4.4).
† Tedavi kollar� aras�nda ≥%2'lik farkla Evre 5 advers reaksiyonlar� g�r�lmemi�tir.
*Kemoterapi: KLL'de Klorambusil; bendamustin, CHOP, FL dahil iNHL'de CVP
§ GAZYVA kolunda (BO21223) en az %2'den daha y�ksek insidansla idame tedavisinde de g�r�lm��t�r.
�al��ma GAO4753g/GADOLIN'de bendamustin kolundaki hastalara sadece 6 ayl�k ind�ksiyon tedavisi uygulan�rken, ind�ksiyon periyodunun ard�ndan GAZYVA ile birlikte bendamustin kolundaki hastalar GAZYVA idame tedavisine devam etmi�tir.
�al��ma GAO4753g/GADOLIN'de idame periyodunda meydana gelen en yayg�n advers reaksiyonlar �ks�r�k (%20), n�tropeni (%13) �st solunum yolu enfeksiyonlar� (%12), sin�zit (%10), diyare (%10), bron�it (%10), bulant� (%9), yorgunluk(%9), IRR'ler (%8), , idrar yolu
enfeksiyonlar� (%7), nazofarenjit (%7), pireksi (%7), artralji (%6), kusma (%6), d�k�nt�
(%6), pn�moni (%5), dispne (%5) ve ekstremitelerde a�r�d�r(%5). En yayg�n 3-5. Derece advers reaksiyonlar n�tropeni (%10), febril n�tropeni (%2), anemi, trombositopeni, pn�moni, sepsis, �st solunum yolu enfeksiyonu ve idrar yolu enfeksiyonudur (t�m� %1 oran�nda).
FL hastalar�ndaki advers reaksiyon profili, her iki �al��madaki genel iNHL pop�lasyonu ile tutarl� olmu�tur.
Se�ilmi� advers reaksiyonlar�n tan�m�
A�a��daki b�l�mlerde a��klanan insidanslardan iNHL ile ilgili olanlar, her 2 pivot �al��mada (BO21223/GALLIUM, GAO4753g/GADOLIN) raporlanan en y�ksek insidansl� A�R'lerdir.
MO40597 �al��mas�, daha �nce tedavi g�rmemi� FL hastalar�nda D�ng� 2'den itibaren k�sa s�reli inf�zyonlar�n (yakla��k 90 dakika) g�venlik profilini karakterize etmek i�in tasarlanm��t�r.
�nf�zyonla ili�kili reaksiyonlar (IRR'ler)
�nf�zyonla ili�kili reaksiyonla ili�kilendirilen ve en s�k bildirilen (≥%5) semptomlar, bulant�, halsizlik, titreme, hipotansiyon, pireksi, kusma, dispne, g���s a�r�s�, k�zarma, hipertansiyon, ba� a�r�s�, ta�ikardi, ba� d�nmesi ve diyaredir. Bronkospazm, larinks ve bo�az iritasyonu, h�r�lt�, larinks �demi ve atriyal fibrilasyon gibi solunum ve kardiyak semptomlar da bildirilmi�tir (bkz. B�l�m 4.4).
Kronik Lenfositik L�semi
IRR'lerin insidans�, rituximab + klorambusil koluna k�yasla GAZYVA + klorambusil kolunda daha y�ksek olmu�tur. �lk 1000 mg GAZYVA inf�zyonuyla birlikte %66 IRR insidans� meydana gelmi�tir (hastalar�n %20'sinde Evre 3-4 IRR meydana gelmi�). Genel olarak hastalar�n %7'si, GAZYVA'n�n kesilmesiyle sonu�lanan bir IRR ile kar��la�m��t�r. Sonraki inf�zyonlarda kar��la��lan IRR insidans�, ikinci 1000 mg dozda %3, ard�ndan ise %1'dir. 1. D�ng�n�n ilk 1000 mg inf�zyonlar�ndan sonra Evre 3-5 IRR bildirilmemi�tir.
B�l�m 4.2'de a��klanan �ekilde inf�zyonla ili�kili reaksiyonlar�n engellenmesi i�in kombine �ekilde �nlemlerin al�nd��� hastalarda t�m Evrelerdeki inf�zyonla ili�kili reaksiyonlarda azalma g�zlenmi�tir. Evre 3-4 IRR'lerin (g�rece daha az say�da hastada meydana gelen) oranlar�, azalt�c� �nlemler uygulanmadan �nce ve uyguland�ktan sonra benzer olmu�tur.
Folik�ler Lenfoma dahil Indolent Non-Hodgkin Lenfoma
Hastalar�n %12'sinde Evre 3-4 A�R'ler g�r�lm��t�r. 1. D�ng�de A�R'lerin genel insidans�, kar��la�t�rma koluna k�yasla GAZYVA + kemoterapi alan hastalarda daha y�ksek olmu�tur. GAZYVA + kemoterapi alan hastalarda 1. G�nde A�R insidans� en y�ksek olmu� ve izleyen inf�zyonlarda kademeli olarak azalm��t�r. Bu azalma trendi tek ba��na GAZYVA ile idame s�ras�nda devam etmi�tir. 1. D�ng� d���nda izleyen inf�zyonlarda A�R'lerin insidans� GAZYVA ve ilgili kar��la�t�rma kollar� aras�nda kar��la�t�r�labilir olmu�tur. Genel olarak, hastalar�n %4'�nde GAZYVA tedavisinin kesilmesini gerektiren inf�zyonla ili�kili reaksiyonlar g�r�lm��t�r.
Folik�ler Lenfomal� Hastalarda K�sa S�reli �nf�zyon
SDI'nin g�venli�ini de�erlendiren MO40597 �al��mas�nda, BO21223 �al��mas�ndaki D�ng� 2'de standart inf�zyondan sonra IRR ya�ayan oran ile kar��la�t�r�ld���nda hastalar�n daha b�y�k bir k�sm� D�ng� 2'de herhangi bir derece IRR ya�am��t�r (s�ras�yla 10/99 [%10,1] ve 23/529 [%4,3]; ara�t�rmac� taraf�ndan �al��ma tedavisinin herhangi bir bile�enine atfedilen IRR'ler). MO40597'de D�ng� 2'de SDI'den sonra hi�bir hastada Derece 3 IRR ya�amam��t�r; 3/529 (%0,6), BO21223 �al��mas�nda 2. D�ng�de Derece 3 IRR ya�anm��t�r. Her iki �al��mada da IRR semptomlar� ve bulgular� benzerdir.
MO40597/GAZELLE �al��mas�nda g�zlemlenen inf�zyonla ilgili reaksiyonlar Tablo 8'de �zetlenmi�tir.
Tablo 8, �al��ma MO40597/GAZELLE K�sa S�reli �nf�zyon: D�ng�ye G�re �nf�zyonla �lgili Reaksiyonlar (G�venlik De�erlendirilebilir Pop�lasyon)
| ||||||||||||
|
|
|
|
|
| |||||||
|
|
|
|
|
|
|
|
|
|
| ||
C=d�ng�; CTCAE = Olumsuz Olaylar i�in Ortak Terminoloji Kriterleri; IRR=inf�zyonla ilgili reaksiyon �nf�zyonla ilgili reaksiyon, ara�t�rmac� taraf�ndan tedavinin herhangi bir bile�eniyle ilgili oldu�una karar verilen, �al��ma tedavisi inf�zyonunun bitiminden sonraki 24 saat i�inde veya s�ras�nda meydana gelen herhangi bir olay olarak tan�mlan�r.
N�tropeni ve enfeksiyonlar
4.9. Doz a��m� ve tedavisi
�nsan klinik �al��malar�nda doz a��m� ile ilgili deneyim bulunmamaktad�r. GAZYVA ile yap�lan klinik �al��malarda, inf�zyon ba��na 50 mg'den 2.000 mg'ye (dahil) kadar dozlar uygulanm��t�r. Bu �al��malarda bildirilen advers reaksiyonlar�n insidans� ve yo�unlu�u doza ba��ml� g�r�nmemektedir.
Doz a��m� olu�an hastalarda inf�zyon derhal kesilmeli veya azalt�lmal� ve yak�n g�zetim uygulanmal�d�r. Hastalarda B-h�cre deplesyonu s�ras�nda kan h�cre say�s�n�n d�zenli izlenmesi gerekti�ine ve enfeksiyon riskinde art�� oldu�una dikkat edilmelidir.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Antineoplastik ajanlar, monoklonal antikorlar ATC kodu: L01FA03
Etki mekanizmas�
Obinutuzumab, IgG1 izotipinin rekombinant monoklonal h�manize ve gliko i�lenmi� Tip II anti-CD20 antikorudur. Hematopoietik k�k h�crelerin, pro-B h�crelerin, normal plazma h�crelerinin veya di�er normal dokular�n de�il fakat spesifik olarak, malign olmayan ve malign pre-B ve olgun B lenfositlerin y�zeyindeki CD20 transmembran antijenin ekstrasel�ler
kulpunu hedef al�r. Obinutuzumab�n Fc k�sm�n�n gliko i�lenmesi, gliko i�lenmemi� antikorlara k�yasla do�al katil (NK) h�creler, makrofajlar ve monositler gibi imm�n efekt�r h�creler �zerindeki FcγRIII resept�rler i�in daha y�ksek afinite sa�lar.
Klinik d��� �al��malarda obinutuzumab do�rudan h�cre �l�m�ne yol a�makta ve FcγRIII pozitif imm�n efekt�r h�crelerin kat�lmas� yoluyla antikora ba��ml� h�cresel sitotoksisiteyi (ADCC) ve antikora ba��ml� h�cresel fagositozu (ADCP) d�zenlemektedir. Buna ek olarak, obinutuzumab d���k derecede kompleman ba��ml� sitotoksisiteyi (CDC) d�zenlemektedir. Hayvan modellerinde obinutuzumab, potent B h�cre deplesyonunu ve antit�m�r etkilili�i d�zenler. Tip I antikorlara k�yasla, Tip II antikor olan obinutuzumab, e�de�er dozda CDC'de e� zamanl� bir azalmayla birlikte do�rudan h�cre �l�m�n�n ind�klenmesinde art��la karakterize edilir. Gliko i�lenmemi� antikorlara k�yasla, gliko i�lenmi� bir antikor olarak obinutuzumab, e�de�er bir dozda y�ksek antikora ba��ml� h�cresel sitotoksisite (ADCC) ve fagositoz (ADCP) ile karakterize edilir. Obinutuzumab hayvan modellerinde potent B-h�cre deplesyonu ve antit�m�r etkilili�e arac�l�k eder.
KLL'li hastalarda yap�lan pivotal klinik �al��mada (BO21004/CLL11), GAZYVA uygulanmas�yla de�erlendirilebilen hastalar�n %91'inde (40/44) tedavi d�nemi sonunda B h�cre deplesyonu (CD19+ B h�cre say�s�n�n <0,07 x 10/L olmas� �eklinde tan�mlanm��t�r) olmu� ve deplesyon, ilk 6 ayl�k takip boyunca devam etmi�tir. B h�crelerin geri kazan�m�, progresif hastal�k olmaks�z�n hastalar�n %35'inde (14/40) ve progresif hastal�k varl���nda hastalar�n %13'�nde (5/40) takip d�neminin 12-18 ay�nda g�zlenmi�tir.
iNHL'li hastalarda yap�lan pivotal klinik �al��mada (GAO4753/GADOLIN), GAZYVA uygulamas� ile de�erlendirilebilen hastalar�n %97'sinde (171/176) tedavi d�nemi sonunda B h�cre deplesyonu olmu� ve %97'sinde (61/63) son dozu takiben 6 aydan fazla deplesyon devam etmi�tir. B h�crelerinin geri kazan�m�, tedaviye tepkileri �l��lebilir hastalar�n %11'inde (5/46) takip d�neminin 12-18 ay�nda g�zlenmi�tir.
Klinik etkililik ve g�venlilik
- Kronik Lenfositik L�semi
Komorbiditeleri bulunan daha �nce tedavi uygulanmam�� kronik lenfositik l�semili hastalarda rituximab + klorambusil (RClb) veya tek ba��na klorambusile (Clb) kar�� GAZYVA + klorambusilin (GClb) etkilili�ini ve g�venlili�ini inceleyen uluslararas�, �ok merkezli, a��k etiketli, randomize, iki a�amal�, �� kollu bir Faz III klinik �al��ma ger�ekle�tirilmi�tir.
Kat�l�mdan �nce hastalarda CD20+ KLL ve e� zamanl� mevcut t�bbi durumlara ili�kin a�a��daki �l��tlerden birinin veya ikisinin bulundu�unun belgelenmesi gerekmi�tir; 6'dan y�ksek komorbidite skoru (CIRS) veya b�brek fonksiyonunda azalma (KrKl <70 mL/dakika). Karaci�er fonksiyonu (Ulusal Kanser Enstit�s� – Evre 3 karaci�er fonksiyon testleri i�in Ortak Terminoloji Kriterleri (>2 haftal�k AST, ALT > 5 x N�S; bilirubin > 3 x N�S) ve renal fonksiyonu (KrKl < 30 mL/dk) yetersiz olan hastalar �al��ma d��� b�rak�lm��t�r. CIRS tan�m�na g�re g�z, kulak, burun, bo�az ve larenks organ sistemi d���nda bir veya daha fazla bireysel organ/sistem yetmezlik skoru 4 olarak de�erlendirilen hastalar, �al��ma d��� b�rak�lm��t�r.
Toplam 781 hasta, GAZYVA + klorambusil, rituximab + klorambusil veya tek ba��na klorambusil almak �zere 2:2:1 oran�nda randomize edilmi�tir. Evre 1a'da 356 hasta �zerinde GAZYVA + klorambusil ile tek ba��na klorambusil, Evre 2'de ise 663 hasta �zerinde GAZYVA
+ klorambusil ile rituximab + klorambusil kar��la�t�r�lm��t�r.
Hastalar�n b�y�k b�l�m�nde GAZYVA, ilk tedavi d�ng�s�n�n 1. g�n�, 8. g�n� ve 15. g�n� uygulanan 1.000 mg ba�lang�� dozu �eklinde intraven�z yolla verilmi�tir. Hastalarda inf�zyonla ili�kili reaksiyonlar�n oran�n� azaltmak i�in bir d�zenleme yap�lm�� ve 140 hasta, ilk GAZYVA dozunu 1. g�n [100 mg] ve 2. g�n [900 mg] b�l�nm�� olarak alm��t�r (bkz. b�l�m 4.2 ve 4.4). Sonraki her tedavi d�ng�s�nde (D�ng�2 ile 6), hastalar GAZYVA 1.000 mg dozunu yaln�zca 1. g�nde alm��t�r. Klorambusil, t�m tedavi d�ng�lerinin (1 ile 6) 1. g�n� ve 15. g�n� oral yolla 0,5 mg/kg v�cut a��rl��� �eklinde verilmi�tir.
Demografik veriler ve ba�lang�� �zellikleri, tedavi gruplar� aras�nda iyi dengelenmi�tir. Hastalar�n b�y�k b�l�m� beyaz (%95) ve erkektir (%61). Hastalar�n %44'� 75 ya� veya �zeri olmak �zere, medyan ya� 73't�r. Ba�lang��ta hastalar�n %22'sinde Binet Evre A, %42'sinde Binet Evre B ve %36's�nda Binet Evre C mevcuttur.
Medyan komorbidite skoru 8'dir ve kat�lan hastalar�n %76's�nda komorbidite skoru 6'dan y�ksek olmu�tur. Medyan tahmini KrKl 62 mL/dakika olmu� ve t�m hastalar�n %66's�nda KrKl <70 mL/dakika bulunmu�tur. Kat�lan hastalar�n y�zde k�rk ikisinde hem <70 mL/dakika KrKl, hem de >6 komorbidite skoru belirlenmi�tir. Hastalar�n y�zde otuz d�rd� yaln�zca komorbidite skoru �zerine �al��maya kat�l�rken, hastalar�n %23'� yaln�zca bozulmu� b�brek fonksiyonuyla kat�lm��t�r.
En s�k bildirilen e� zamanl� t�bbi hastal�klar (%30 veya daha y�ksek kesim de�eri kullan�larak), MedDRA v�cut sistemlerinde: Vask�ler hastal�klar (%73), kardiyak hastal�klar (%46), gastrointestinal hastal�klar (%38), metabolizma ve beslenme hastal�klar� (%40), b�brek ve idrar hastal�klar� (%38), kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar� (%33) olmu�tur.
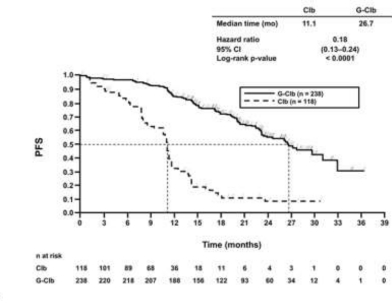
Daha �nce tedavi edilmemi� KLL hastalar�ndaki etkililik verileri Tablo 9'da �zetlenmektedir. Progresyonsuz sa�kal�m (PFS) ve Genel sa�kal�m (OS) i�in Kaplan-Meier e�rileri �ekil 1- 4'te verilmektedir.
Tablo 9. BO21004/CLL11 �al��mas�ndan etkililik �zeti
| Evre 1a | Evre 2 | ||
| klorambusil N=118 | GAZYVA + klorambusil N= 238 | Rituximab + klorambusil N= 330 | GAZYVA + klorambusil N= 333 |
| 22,8 ayl�k medyan g�zlem s�resi | 18,7 ayl�k medyan g�zlem s�resi | ||
Birincil sonlan�m noktas� | ||||
Ara�t�rmac� taraf�ndan de�erlendirilen PFS (PFS-IRC)a |
|
| ||
Olay meydana gelen hasta say�s� (%) | 96 (%81,4) | 93 (%39,1) | 199 (%60,3) | 104 (%31,2) |
Medyan PFS s�resi (ay) | 11,1 | 26,7 | 15,2 | 26,7 |
Tehlike oran� (%95 GA) | 0,18 [0,13; 0,24] | 0,39 [0,31; 0,49] | ||
p-de�eri(Log-s�ra testi, tabakaland�r�lm�� ) | <0,0001 | <0,0001 | ||
Kilit ikincil sonlan�m noktalar� | ||||
IRC-taraf�ndan de�erlendirilen PFS (PFS-IRC)a |
|
| ||
Olay meydana gelen hasta say�s� (%) | 90 (%76,3) | 89 (%37,4) | 183 (%55,5) | 103 (%30,9) |
Medyan PFS s�resi (ay) | 11,2 | 27,2 | 14,9 | 26,7 |
Tehlike oran� (%95 GA) | 0,19 [0,14; 0,27] | 0,42 [0,33; 0,54] | ||
p-de�eri(Log-s�ra testi, tabakaland�r�lm�� ) | <0,0001 | <0,0001 | ||
Tedavi bitimindeki yan�t oran� |
|
| ||
Analize dahil edilen hasta say�s� | 118 | 238 | 329 | 333 |
Yan�t verenler (%) | 37 (%31,4) | 184 (%77,3) | 214 (%65,0) | 261 (%78,4) |
Yan�t vermeyenler (%) | 81 (%68,6) | 54 (%22,7) | 115 (%35,0) | 72 (%21,6) |
Yan�t oran�ndaki fark,(%95 GA) | 45,95 [35,6; 56,3] | 13,33 [6,4; 20,3] | ||
p-de�eri (Ki-kare Testi) | <0,0001 | 0,0001 | ||
Tam yan�t verenlerin say�s� (%) | 0 (%0,0) | 53 (%22,3) | 23 (%7,0) | 69 (%20,7) |
Tedavi bitiminde molek�ler remisyon |
|
| ||
Analize dahil edilen hasta say�s� | 90 | 168 | 244 | 239 |
MRD negatif (%) | 0 (%0) | 45 (%26,8) | 6 (%2,5) | 61 (%25,5) |
MRD pozitiff (%) | 90 (%100) | 123 (%73,2) | 238 (%97,5) | 178 (%74,5) |
MRD oran�ndaki farklar, (%95 GA) | 26,79 [19,5; 34,1] | 23,06 [17,0; 29,1] | ||
Olays�z Sa�kal�m |
|
| ||
Olay meydana gelen hasta say�s� (%) | 103 (%87,3) | 104 (%43,7) | 208 (%63,0) | 118 (%35,4) |
Olaya kadar ge�en medyan s�re (ay) | 10,8 | 26,1 | 14,3 | 26,1 |
Tehlike oran� (%95 GA) | 0,19 [0,14; 0,25] | 0,43 [0,34; 0,54] | ||
p-de�eri (Log-s�ra testi, tabakaland�r�lm��) | <0,0001 | <0,0001 | ||
Yeni anti l�semi tedavisine kadar ge�en s�re |
|
| ||
Olay meydana gelen hasta say�s� (%) | 65 (%55,1) | 51 (%21,4) | 86(%26,1) | 55(%16,5) |
Olaya kadar ge�en medyan s�re (ay) | 14,8 | NR | 30,8 | NR |
Tehlike oran� (%95 GA) | 0,24 [0,16; 0,35] | 0,59 [0,42;0,82] | ||
p-de�eri(Log-s�ra testi,tabakaland�r�lm��) | <0.0001 | <0,0018 | ||
Genel sa�kal�m |
|
| ||
Olay meydana gelen hasta say�s� (%) | 57 (%48,3) | 93 (%39,1) | 147 (%44,5) | 121 (%36,3) |
Olaya kadar ge�en medyan s�re (ay) | 66,7 | NR | 73,1 | NR |
Tehlike oran� (%95 GA) | 0,68 [0,49; 0,94] | 0,76 [0,60; 0,97] | ||
p-de�eri(Log-s�ra testi, tabakaland�r�lm��) | 0,0196 | 0,0245 | ||
Alt grup analizleri
PFS alt grup analizinin bulgular� (yani cinsiyet, ya�, Binet evresi, KrKl, CIRS skoru, beta2- mikroglob�lin, IGVH durumu, kromozom anormallikleri, ba�lang��taki lenfosit say�s�), genel tedavi ama�l� pop�lasyonda g�r�len bulgularla tutarl� olmu�tur. Hastal�k progresyonu veya �l�m riski, 17p delesyonlu hasta alt grubu d���ndaki t�m hastalarda RClb kolu ve Clb koluna k�yasla GClb kolunda azalm��t�r. 17p delesyonlu k���k hasta alt grubunda Clb'ye (HR=0,42, p=0,0892) k�yasla yaln�zca bir pozitif trend g�zlenmi�, RClb'ye k�yasla yarar g�zlenmemi�tir. Alt gruplar i�in hastal�k progresyon veya �l�m riskindeki azalma GClb'ye kar�� Clb i�in %92 ile %58, GClb'ye kar�� RClb i�in ise %72 ile %29 aras�ndad�r.
Risk alt�ndaki hasta say�s�
Zaman (ay)
�ekil 1. KLL'li hastalarda ara�t�rmac� taraf�ndan de�erlendirilen Evre 1a progresyonsuz sa�kal�m�n Kaplan-Meier e�risi (BO21004/CLL11 �al��mas�)
�ekil 2. KLL'li hastalarda Evre 1a'ya ait genel sa�kal�m�n Kaplan-Meier e�risi (BO21004/CLL11 �al��mas�)
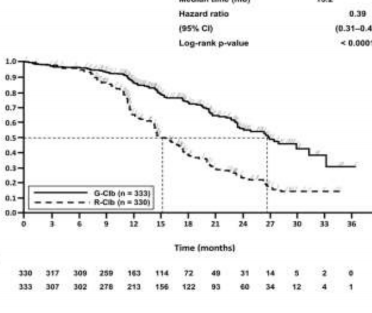
Zaman (ay)
Risk alt�ndaki hasta say�s�
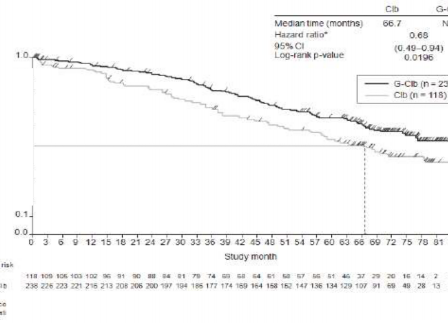
Risk alt�ndaki hasta say�s�
�ekil 3. KLL'li hastalarda ara�t�rmac� taraf�ndan de�erlendirilen Evre 2 progresyonsuz sa�kal�m�n Kaplan-Meier e�risi (BO21004/CLL11 �al��mas�)
�ekil 4. KLL'li hastalarda Evre 1a'ya ait genel sa�kal�m�n Kaplan-Meier e�risi (BO21004/CLL11 �al��mas�)
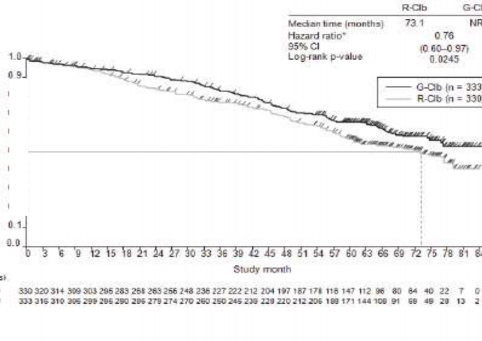
Risk alt�ndaki hasta say�s�
Zaman (ay)
Ya�am kalitesi
Tedavi d�nemi s�ras�nda yap�lan QLQC30 ve QLQ-CLL-16 anketlerinde, alt �l�eklerden herhangi birinde anlaml� bir farkl�l�k g�zlenmemi�tir. Takip s�ras�nda veriler, �zellikle tek ba��na klorambusil kolu i�in s�n�rl�d�r. Bununla birlikte, bug�ne kadar takip s�ras�nda ya�am kalitesi a��s�ndan belirgin bir farkl�l�k saptanmam��t�r.
Sa�l�kla ili�kili ya�am kalitesi de�erlendirmeleri, tedavi d�nemi boyunca �zellikle yorgunluk a��s�ndan istatistiksel olarak anlaml� bir fark g�stermemektedir; bu durum klorambusil rejimine GAZYVA eklenmesinin hastalarda yorgunlu�u artt�rmad���n� �ne s�rmektedir.
- Folik�ler Lenfoma
Daha �nce tedavi edilmemi� folik�ler lenfoma (BO21223/GALLIUM):
Faz III, a��k etiketli, �ok merkezli, randomize bir klinik �al��mada (BO21223/GALLIUM), daha �nce tedavi g�rmemi� Derece 1-3a ilerlemi� (evre II bulky hastal�k, evre III/IV) FL olan 1202 hasta de�erlendirilmi�tir. FL Derece 3b olan hastalar �al��ma d��� b�rak�lm��t�r. Hastalar, kemoterapi (bendamustin, CHOP veya CVP) ile kombinasyon halinde GAZYVA (n=601 hasta) veya rituximab (n=601 hasta) ve ard�ndan tam veya k�smi yan�t elde edilen hastalarda GAZYVA veya rituksimab idamesi almak �zere 1:1 olacak �ekilde randomize edilmi�tir.
GAZYVA, 1. D�ng�n�n ve takip eden d�ng�lerin 1., 8. ve 15. g�nlerinde 1.000 mg'l�k doz olarak intraven�z inf�zyon yoluyla verilmi�tir. Toplamda, alt� d�ng� GAZYVA (her 28 g�nde bir), alt� d�ng� bendamustin ile kombinasyon halinde ve alt� d�ng� CHOP veya sekiz d�ng� CVP ile birlikte toplam sekiz d�ng� GAZYVA (her 21 g�nde bir) verilmi�tir. GAZYVA kemoterapiden �nce uygulanm��t�r. Bendamustin, GAZYVA ile kombinasyon halinde verildi�inde 90 mg/m/g�n'de t�m tedavi d�ng�leri i�in (D�ng�1-6) 1. ve 2. G�nlerde intraven�z olarak verilmi�tir. Standart CHOP ve CVP dozu verilmi�tir. D�ng�6-8'i takiben, kemoterapi ile kombinasyon halinde, yan�t veren hastalar, hastal�k progresyonuna kadar veya 2 y�la kadar her 2 ayda bir GAZYVA idame tedavisi alm��t�r.
Hasta pop�lasyonunun demografik verileri ve temel �zellikleri, tedavi kollar� aras�nda iyi dengelenmi�tir; medyan ya� 59, %81 beyaz, %53 kad�n, %79 FLIPI skoru ≥2 ve %7 Evre II (bulky), %35 Evre III ve %57 Evre IV hastal�k, %44 bulky hastal��� (>7 cm), %34'�n�n ba�lang��ta en az bir B semptomu vard� ve %97'sinin ba�lang��ta ECOG performans durumu 0-1 idi. Hastalar�n %57'si bendamustin, %33'� CHOP ve %10'u CVP kemoterapisi alm��t�r.
�nceden tedavi edilmemi� FL hastalar�na y�nelik etkinlik sonu�lar� Tablo 10'da �zetlenmi�tir. Progresyonsuz sa�kal�m (PFS) i�in Kaplan-Meier e�rileri �ekil 5'te g�sterilmi�tir.
Tablo 10: BO21223/GALLIUM �al��mas�ndan daha �nce tedavi edilmemi� FL hastalar�na ait etkilili�in �zeti
| Rituximab idame | Gazyva idame tedavisinin |
tedavisinin takip etti�i | takip etti�i | |
Rituximab + Kemoterapi | Gazyva + Kemoterapi | |
N=601 | N=601 | |
| Medyan g�zlem s�resi: 34 ay | Medyan g�zlem s�resi: 35 ay |
Birincil sonlan�m noktas� |
| |
IRC taraf�ndan de�erlendirilen PFS (PFS-IRC) |
| |
Olayla kar��la�an hasta say�s� (%) | 144 (24%) | 101 (16.8%) |
HR (%95 GA) | 0.66 [0.51, 0.85] | |
p-de�eri (Log-Rank tabakaland�r�lm��*) | testi, |
0.0012 |
3 y�ll�k PFS tahmini | 73.3 | 80 |
[%95 GA] | [68.8, 77.2] | [75.9, 83.6] |
Kilit sonlan�m noktas� |
| |
IRC taraf�ndan de�erlendirilen PFS (PFS-IRC) |
| |
Olayla kar��la�an hasta say�s� (%) | 125 (20.8%) | 93 (15.5%) |
HR (%95 GA) | 0.71 [0.54, 0.93] | |
p-de�eri (Log-Rank tabakaland�r�lm��*) | testi, |
0.0138 |
Bir sonraki anti-lenfoma tedavisine kadar ge�en s�re |
| |
Olayla kar��la�an hasta say�s� (%) | 111 (18.5%) | 80 (13.3%) |
HR (%95 GA) | 0.68 [0.51, 0.91] | |
p-de�eri (Log-Rank tabakaland�r�lm��*) | testi, |
0.0094 |
Genel sa�kal�m |
| |
Olayla kar��la�an hasta say�s� (%) | 46 (7.7%) | 35 (5.8%) |
HR (%95 GA) | 0.75 [0.49, 1.17] | |
p-de�eri (Log-Rank tabakaland�r�lm��*) | testi, |
0.21 |
�nd�ksiyon Sonundaki Genel Yan�t Oran�** IR taraf�ndan de�erlemdirilen, CT) |
| |
Yan�t verenler (%) (TY, KY) | 522 (86.9%) | 532 (88.5%) |
Yan�t oran�ndaki fark (%) [%95 GA] |
1.7% [-2.1%, 5.5%] | |
p de�eri Haenszel testi) | (Cochran-Mantel- |
0.33 |
Tam Yan�t (TY) | 143 (23.8%) | 117 (19.5%) |
K�smi Yan�t (KY) | 379 (63.1%) | 415 (69.1%) |
IRC: Ba��ms�z �nceleme Komitesi; PFS: progresyonsuz sa�kal�m; HR: Tehlike Oran�; GA: G�ven Aral���
* Tabakaland�rma fakt�rleri kemoterapi rejimi, folik�ler lenfoma i�in FLIPI risk grubu, co�rafi b�lge idi.
§ Bu etkinlik ara analizindeki �nem d�zeyi: 0.012
¶ Veriler Hen�z Olgun De�il. Analiz s�ras�nda medyana ula��lamad�
# �okluk i�in ayarlanmad�
**De�i�tirilmi� Cheson 2007 kriterlerine g�re de�erlendirilmi�tir
‡ �nd�ksiyonun Sonu = ind�ksiyon faz�n�n sonu, monoterapi idamesini i�ermez
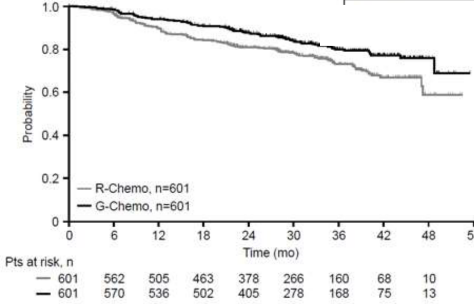
HR, 0.66; %95 GA, 0.51
0.85; p=0.0012
�ekil 5 Daha �nce tedavi edilmemi� FL hastalar�nda IRC taraf�ndan de�erlendirilen progresyonsuz sa�kal�m Kaplan-Meier e�risi (�al��ma BO21223/GALLIUM)
Alt grup analizlerinin sonu�lar�
Alt grup analizlerinin sonu�lar� (�okluk i�in ayarlanmam��) genel olarak FL pop�lasyonunda g�r�len sonu�larla tutarl�d�r ve genel sonucun sa�laml���n� desteklemektedir. De�erlendirilen alt gruplar, ba�lang��ta IPI, FLIPI, Bulky Hastal���, B Semptomlar�, Ann Arbor A�amas� ve ba�lang��ta ECOG'u i�ermekteydi. FLIPI skoru 0-1 (d���k risk) olan hastalarda, GAZYVA + kemoterapi ve rituximab + kemoterapi aras�nda fark g�zlenmemektedir (IRC-de�erli PFS HR
1.17 (%95CI 0.63;2.19, 40 PFS olay�). Bu alt grup %21'den (253/1202) olu�maktad�r ve PFS olaylar�n�n %16.3'�n� (40/245) ya�am��t�r. Ek olarak, kemoterapi rejimleri (bendamustin, CHOP ve CVP) genelinde PFS'nin ke�if ama�l� alt grup analizleri, GAZYVA art� kemoterapi pop�lasyonunda g�r�len sonu�larla tutarl�yd�. Kemoterapi alt grubuna g�re g�zlemlenen HR'ler a�a��daki gibidir; CHOP (n = 398): HR 0,77 (%95 GA: 0,50, 1,20), CVP (n = 118):
HR 0,63 (%95 GA: 0,32, 1,21) ve bendamustin (n = 686): HR 0,61 (95) %CI: 0.43, 0.86).
Hasta Bildirimli Sonlan�mlar
Tedavi ve takip a�amalar� s�ras�nda toplanan FACT-Lym anketine dayanarak, her iki tedavi kolundaki hastalar, Lenfoma alt �l�e�inde ba�lang�ca g�re 3 puanl�k bir art��, 6 puanl�k bir art�� ile tan�mlanan lenfoma ile ilgili semptomlarda klinik olarak anlaml� iyile�meler ya�anm��t�r. FACT Lym TOI'deki ba�lang�ca g�re ve FACT Lym Total skorunda ba�lang�ca g�re 7 puanl�k bir art��. EQ-5D fayda puanlar� ba�lang��ta, tedavi ve takip s�ras�nda benzerdi. HRQOL veya sa�l�k durumu �l��mlerinde kollar aras�nda anlaml� bir fark g�r�lmemi�tir.
A��k etiket tasar�m� nedeniyle, hasta taraf�ndan bildirilen sonu�lar dikkatle yorumlanmal�d�r.
Rituximab veya rituximab i�eren tedavi rejimi alan folik�ler lenfoma hastalar�nda tedavi s�ras�nda veya 6 ay sonras�na kadar yan�ts�zl�k veya n�ks geli�mesi durumunda (GAO4753g/GADOLIN):
Faz III, a��k etiketli, �ok merkezli, randomize bir klinik �al��mada (GAO4753g (GADOLIN)), tedavi s�ras�nda yan�t vermeyen veya (ind�ksiyon veya idame tedavisinin bir par�as� olarak rituximab monoterapisi de dahil olmak �zere) son rituximab ya da rituximab i�eren bir rejimin son dozunu takiben hastal��� ilerleyen 396 iNHL hastas� de�erlendirilmi�tir. Hastalar, her biri 28 g�n s�reli 6 d�ng� �eklinde tek ba��na bendamustin (B) (n = 202) veya bendamustin ile kombinasyon olarak GAZYVA (G+B) (n = 194= almak �zere 1:1 randomize edilmi�tir. Hastal��� ilerlemeyen G+B kolundaki hastalar (yani, ind�ksiyon bitiminde tam yan�t (CR), k�smi yan�t (PR) veren veya hastal��� stabil seyreden (SD)) hastalar, iki y�l s�reyle her iki ayda bir veya (hangisi daha �nce ise) hastal�k progresyonuna kadar GAZYVA ile idame tedavisi almaya devam etmi�tir. Hastalar, b�lge, iNHL alttipi (folik�ler versus non-folik�ler), rituximab-refrakter tip (rituximab monoterapisinden veya kemoterapiyle kombinasyon �eklinde rituximab tedavisinden �nce olmak �zere) ve �nceki tedavilerin say�s� (≤2'ye kar��
>2) do�rultusunda tabakaland�r�lm��t�r.
Demografik veriler ve ba�lang�� karakteristikleri iyi dengelenmi�tir (medyan ya� 63 y�ld�r; �o�unluk beyaz �rka mensuptur [%88] ve erkektir [%58]). Hastalar�n �o�unlu�unda folik�ler lenfoma (%81) vard�r. �lk tan�dan bu yana ge�en medyan s�re 3 y�ld�r ve �nceki tedavilerin medyan say�s� 2'dir (aral�k: 1 ila 10); hastalar�n %44'� daha �nce 1 kez, %34'� ise 2 tedavi alm��t�r.
GAZYVA, D�ng�1'in 1, 8 ve 15. ve D�ng�2-6'n�n 1. G�n�nde ve hastal�k progresyonu meydana gelmeyen hastalara, iki y�l s�reyle her iki ayda bir (ya da hangisi daha �nce ise) hastal�k progresyonuna kadar 1.000 mg kesin dozda intraven�z inf�zyon olarak verilmi�tir. Bendamustin, t�m tedavi d�ng�lerinin (D�ng�1-6) 1 ve 2. G�nlerinde, GAZYVA ile kombinasyon �eklinde 90 mg/m/g�n, tek ba��na verildi�inde ise 120 mg/m/g�n olarak intraven�z yolla verilmi�tir. B kolundaki hastalar�n %66,7'sine kar��l�k G+ B ile tedavi edilen hastalar�n %79,4'� alt� tedavi d�ng�s�n�n tamam�n� alm��t�r.
Ba��ms�z �nceleme Komitesine (IRC) dayal� primer analiz de�erlendirmesi, tek ba��na bendamustin alan hastalarla kar��la�t�r�ld���nda G+B ve onu takiben GAZYVA idame tedavisi alan iNHL hastalar�nda hastal�k progresyon (PD) veya �l�m riskinde, %45 oran�nda istatistiksel olarak �nemli ve klinik olarak anlaml� bir azalmay� g�stermi�tir. iNHL pop�lasyonunda g�r�len hastal�k progresyonu veya �l�m riskindeki azalma folik�ler lenfoma hastalar�n�n alt grubundan etkilenmi�tir.
GAO4753g �al��mas�nda yer alan hastalar�n �o�unlu�unda (%81,1) FL mevcuttur. FL pop�lasyonundaki primer analiz etkililik sonu�lar� Tablo 11 ve �ekil 6 ve 8'de g�sterilmektedir. Hastalar�n %11,6's�nda marjinal zon lenfoma (MZL) ve %7,1'inde k���k lenfositik lenfoma (SLL) mevcuttu. FL olmayan pop�lasyonda IRC ile de�erlendirilen PFS i�in HR 0,94 (% 95 GA: 0,49, 1,90)' d�r. MZL ve SLL alt pop�lasyonlar�ndaki etkilili�i konusunda kesin bir sonu� ��kar�lamam��t�r.
Final analizde, B kolundaki FL hastalar� i�in ortalama g�zlem s�resi 45,9 ay (aral�k: 0-100,9 ay) ve G + B kolundaki hastalar i�in 57,3 ay (aral�k: 0,4-97,6 ay) idi, bu da birincil analizden bu yana s�ras�yla B ve G + B kollar�nda ek 25,6 ay ve 35,2 ay ortalama takibi temsil etmektedir. IRC de�erlendirmeleri devam etmedi�i i�in nihai analizde sadece Ara�t�rmac� (IRC) taraf�ndan de�erlendirilen sonlan�m noktalar� rapor edilmi�tir. Genel olarak, ara�t�rmac� taraf�ndan de�erlendirilen etkililik sonu�lar�, birincil analizde g�zlemlenenlerle tutarl�d�r.
FL'li hastalarda genel sa�kal�m (OS) daha uzun takip do�rultusunda istikrarl�d�r (bkz. �ekil 7); �l�m riski i�in HR 0,71 (% 95 GA: 0,51, 0,98)'dir.
Tablo 11: GAO4753g/GADOLIN �al��mas�ndan FL hastalar�na ait primer etkililik analizi �zeti
| Bendamustin N=166 | Gazyva idame tedavisinin takip etti�i Gazyva + Bendamustin N= 155 |
| Medyan g�zlem s�resi: 20 ay | Medyan g�zlem s�resi: 22 ay |
FL pop�lasyonundaki birincil sonlan�m noktas� |
| |
IRC taraf�ndan de�erlendirilen PFS (PFS-IRC) |
| |
Olayla kar��la�an hasta say�s� (%) | 90 (54,2%) | 54 (34,8%) |
Medyan PFS s�resi (ay) (%95 GA) | 13,8 (11,4, 16,2) | NR (22,5,-) |
HR (%95 GA) | 0,48 (0,34, 0,68) | |
p-de�eri (Log-Rank testi, tabakaland�r�lm��*) | <0,0001 | |
�kincil Sonlan�m Noktalar� |
| |
Ara�t�rmac� taraf�ndan de�erlendirilen PFS (PFS-IRC) |
| |
Olayla kar��la�an hasta say�s� (%) | 102 (61,4%) | 62 (40,0%) |
Medyan PFS s�resi (ay) (%95 GA) | 13,7 (11,0, 15,5) | 29,2 (17,5,-) |
HR (%95 GA) | 0,48 (0,35, 0,67) | |
p-de�eri (Log-Rank testi, tabakaland�r�lm��*) | <0,0001 | |
En �yi Genel Yan�t (BOR) (IRC-taraf�ndan de�erlendirilen) |
| |
Analize dahil edilen hasta say�s� | 161 | 153 |
Yan�t verenler (%) (CR/PR) | 124 (77,0%) | 122 (79,7%) |
Yan�t oran� fark� (%95 GA) | 2,72 (-6,74, 12,18) | |
p-de�eri (Cochran-Mantel-Haenszel test,) | 0,6142 | |
Tam Yan�t Verenler (%) | 31 (19,3%) | 24 (15,7%) |
K�smi Yan�t Verenler (%) | 93 (57,8%) | 98 (64,1%) |
Stabil Hastal�k (%) | 18 (11,2%) | 13 (8,5%) |
Yan�t s�resi (IRC taraf�ndan de�erlendirilen) |
| |
Analize dahil edilen hasta say�s� | 127 | 122 |
Olayl� hasta say�s� (%) | 74 (58,3%) | 36 (29,5%) |
Medyan DOR s�resi (ay) (%95 GA) | 11,9 (8,8, 13,6) | NR (25,4,-) |
HR (%95 GA) | 0,36 (0,24, 0,54) | |
Genel sa�kal�m (hen�z olgunla�mam��) |
| |
Olayl� hasta say�s� (%) | 36 (21,7%) | 25 (16.1%) |
Olaya kadar ge�en medyan s�re (ay) | NR | NR |
HR (%95 GA) | 0,71 (0,43, 1,19) | |
p-de�eri (Log-Rank testi, tabakaland�r�lm��*) | 0,1976 | |
IRC: Ba��ms�z �nceleme Komitesi; PFS: progresyonsuz sa�kal�m; HR: Hazard Oran�; GA: G�ven Aral���, NR
= Ula��lamad�
*Analize y�nelik tabakaland�rma fakt�rleri refrakter tip (rituximab monoterapisi vs. rituximab + kemoterapi) ve �nceki tedaviler idi (≤ 2 vs ≥2). Folik�ler versus non-folik�ler de �al��maya y�nelik bit tabakaland�rma fakt�r� olmas�na kar��n, folik�ler lenfoma hastalar�n�n altgrup analizi i�in ge�erli de�ildir.
§ Tedavi ba�lang�c�ndan itibaren 12 ay i�erisindeki en iyi yan�t
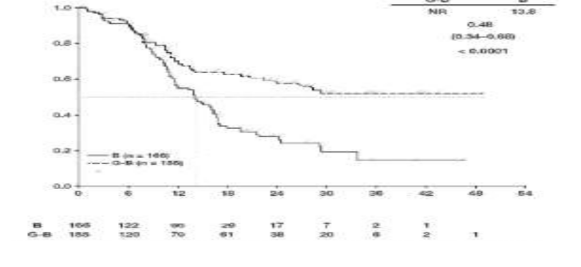
95% GA
�ekil 6: Folik�ler lenfoma hastalar�nda IRC ile de�erlendirilen progresyonsuz sa�kal�ma ait Kaplan-Meier e�risi (GAO4753g/GADOLIN �al��mas�)
�ekil 7: Folik�ler lenfoma hastalar�nda genel sa�kal�ma ait final analizinin Kaplan- Meier e�risi (GAO4753g/GADOLIN �al��mas�)
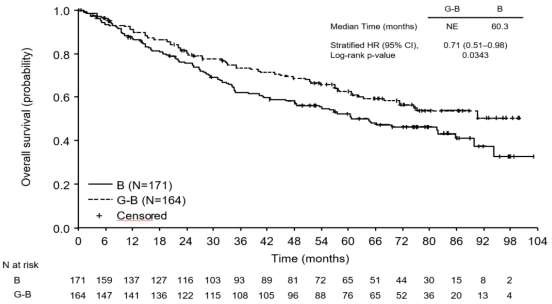
Alt grup analizlerinin sonu�lar�
Altgrup analizlerinin sonu�lar� genel olarak FL pop�lasyonunda g�r�len sonu�larla uyumludur ve genel sonucun sa�laml���n� desteklemektedir.
�ekil 8: Folik�ler lenfomada hasta altgrubuna g�re IRC taraf�ndan de�erlendirilen PFS* (GAO4753g/GADOLIN �al��mas�)
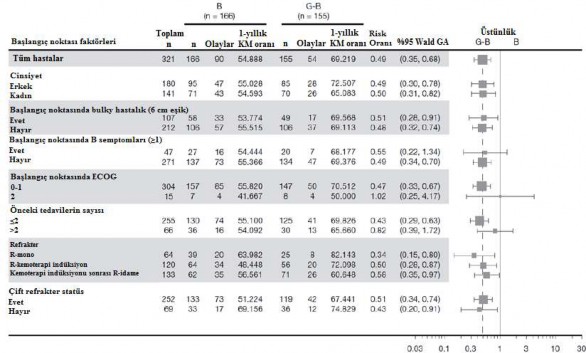
K�sa S�reli �nf�zyon �al��mas� MO40597 (GAZELLE)
CHOP, CVP veya bendamustin kemoterapisi ile kombinasyon halinde uygulanan obinutuzumab'�n k�sa (yakla��k 90 dakika) s�reli inf�zyonunun (SDI) g�venli�i, daha �nce tedavi edilmemi� ilerlemi� folik�ler lenfomas� olan 113 hastada �ok merkezli, a��k etiketli, tek kollu bir �al��mada de�erlendirilmi�tir (�al��ma MO40597/GAZELLE).
Hastalar, ilk obinutuzumab k�r�n�, D�ng� 1'in 1, 8 ve 15'inci g�nlerinde standart inf�zyon h�z�nda alm��t�r. �lk d�ng� s�ras�nda herhangi bir Derece ≥3 IRR ya�amayan hastalar, D�ng� 2'den itibaren SDI alm��t�r.
�al��man�n birincil sonlan�m noktas�, 2. D�ng� s�ras�nda SDI ile ili�kili Derece ≥3 IRR ya�ayan ve Derece ≥3 IRR ya�amadan 1. D�ng� s�ras�nda standart inf�zyon h�z�nda daha �nce 3 obinutuzumab uygulamas� alm�� olan hastalar�n oran�d�r.
2. D�ng�de SDI alan hastalar aras�nda Derece ≥3 IRR g�zlenmemi�tir. 2. D�ng�den sonra sadece bir hastada 3. A�ama IRR ya�anm��t�r (5. D�ng�de hipertansiyon) (bkz. B�l�m 4.8 �stenmeyen Etkiler).
Hasta Bildirimli Sonlan�mlar
Tedavi s�ras�nda ve takip d�nemlerinde yap�lan FACT-Lym anketi ve EQ-5D indeks �l�e�ine g�re, sa�l�kla ilgili ya�am kalitesi pivot �al��ma s�ras�nda genel olarak s�rd�r�lm�� olup, kollar aras�nda anlaml� fark bulunmam��t�r. Bununla birlikte, FL hastalar�nda bendamustine GAZYVA eklenmesi, xFACT-Lym TOI skoru ile �l��len sa�l�kla ilgili ya�am kalitesinde d����e kadar ge�en s�reyi 2,2 ay uzatm��t�r (benda ve G+B i�in s�ras�yla medyan 5,6'ya kar�� 7,8 ay HR= 0,83; %95 GA: 0,60, 1,13).
�mm�nojenisite
�mm�nojenisite tayin bulgular�; tayin duyarl�l��� ve �zg�ll���, tayin metodolojisi, tayinin dola��mdaki GAZYVA/antikor miktarlar� a��s�ndan g�c�, numunelerin kullan�m�, numune toplama zaman�, e� zamanl� ila�lar ve altta yatan hastal�klar dahil bir�ok fakt�re y�ksek d�zeyde ba��ml�d�r. Bu nedenlerle, GAZYVA'ya kar�� antikorlar�n insidans�n�n di�er �r�nlere kar�� antikorlar�n insidans�yla kar��la�t�r�lmas� yan�lt�c� olabilir.
BO21004/CLL11 pivot �al��mas�nda yer alan hastalar, GAZYVA'ya y�nelik anti-terap�tik antikorlar (ATA) i�in birden fazla zaman noktas�nda test edilmi�tir. GAZYVA ile tedavi edilen hastalar aras�ndan randomize fazdaki 140 hastadan 8'i ile ba�lang�� faz�ndaki 6 hastadan 2'sinin 12 ayl�k takip s�ras�ndaki ATA testleri pozitif olarak sonu�lanm��t�r. Bu hastalardan hi�biri, ATA ile ili�kili oldu�u d���n�len anafilaktik veya a��r� duyarl�l�k reaksiyonlar�yla kar��la�mad��� gibi, klinik yan�t da etkilenmemi�tir.
GAO4753g/GADOLIN �al��mas�nda tedavi g�ren iNHL hastalar�nda ba�lang�� referans� sonras�nda HAHA (�nsan Anti-�nsan Antikoru) g�zlenmemi�tir. HAHA'n�n klinik anlaml�l��� bilinmiyor olmas�na ra�men HAHA ve klinik s�re� aras�ndaki potansiyel ba�lant� g�zard� edilmemelidir.
Pediyatrik pop�lasyon
Pediyatrik kullan�m ile ilgili bilgiler i�in bkz. B�l�m 4.2.
5.2. Farmakokinetik �zellikler
Genel �zellikler
Faz I, Faz II ve Faz III �al��malarda obinutuzumab� tek ba��na ya da kemoterapiyle kombinasyon halinde alan 469 iNHL, 342 KLL ve 130 DBBHL (Diff�z B�y�k B H�creli Lenfoma) hastas�nda farmakokinetik verileri analiz etmek i�in bir pop�lasyon farmakokinetik (PK) modeli geli�tirilmi�tir.
Emilim:
Obinutuzumab intraven�z uygulan�r, bu nedenle emilim ge�erli de�ildir. Di�er uygulama �ekilleriyle �al��ma yap�lmam��t�r. Pop�lasyon PK modeline g�re; D�ng�6, 1. g�n inf�zyonunun ard�ndan KLL hastalar�nda tahmini medyan C de�eri 465,7 mcg/mL ve EAA(τ) de�eri 8961 mcg.g�n/mL, iNHL hastalar�nda tahmini medyan Cde�eri 539,3 mcg/mL ve EAA(τ) de�eri 10956 mcg.g�n/mL olmu�tur.
Da��l�m:
�ntraven�z uygulama ard�ndan santral kompart�man�n da��l�m hacmi (KLL hastalar�nda 2,98 L, iNHL hastalar�nda 2,97 L) serum hacmine yakla��r ve bu da, da��l�m�n b�y�k oranda plazma ve interstisiyel s�v� ile s�n�rl� oldu�unu g�stermektedir.
Biyotransformasyon:
Obinutuzumab�n metabolizmas� do�rudan incelenmemi�tir. Antikorlar b�y�k oranda katabolizmayla temizlenmektedir.
Eliminasyon:
Obinutuzumab klerensi, KLL hastalar�nda yakla��k 0,11 L/g�n ve iNHL hastalar�nda yakla��k 0,08 L/g�n olup, medyan eliminasyon tde�eri KLL hastalar�nda 26,4 g�n ve iNHL hastalar�nda 36,8 g�n olmu�tur. Obinutuzumab eliminasyonu, biri do�rusal klerens yola�� ve biri zaman�n fonksiyonu olarak de�i�en do�rusal olmayan klerens yola�� �eklinde klerensi tan�mlayan iki paralel yolak i�erir. Tedavi ba�lang�c�nda do�rusal olmayan zamanla de�i�en klerens yola�� bask�nd�r ve bu nedenle maj�r klerens yola��n� olu�turur. Tedavi devam ettik�e, bu yola��n etkisi azal�r ve do�rusal klerens yola�� belirginle�ir. Bu durum hedef arac�l� ila� da��l�m�n� (TMDD) g�sterir; CD20 h�crelerinin ba�lang��ta bol miktarda bulunmas� obinutuzumab�n dola��mdan h�zla ��kar�lmas�na neden olur. Bununla birlikte, CD20 h�crelerin b�y�k b�l�m� obinutuzumaba ba�land���nda hedef arac�l� ila� da��l�m�n�n farmakokinetik �zerindeki etkisi en aza indirgenir.
Farmakokinetik/farmakodinamik ili�ki(ler)
Pop�lasyon farmakokinetik analizinde, cinsiyetin hastalar aras�ndaki de�i�kenli�in bir k�sm�n� a��klayan bir kovaryat oldu�u belirlenmi�, erkeklerde kararl� durum klerensi (CLss) %22 daha y�ksek ve da��l�m hacmi (Vd) %19 daha fazla bulunmu�tur. Bununla birlikte, pop�lasyon analizinin bulgular� maruziyetteki farkl�l�klar�n anlaml� olmad���n� ortaya koymu� (6. D�ng�de KLL hastalar�nda tahmini medyan EAA ve C s�ras�yla, kad�nlarda 11282 mcg.g�n/mL ve 578,9 mcg/mL ve erkeklerde 8451 mcg.g�n/mL ve 432,5 mcg/mL'dir; iNHL hastalar�nda ise tahmini medyan EAA ve C s�ras�yla, kad�nlarda 13172 mcg.g�n/mL ve 635,7 mcg/mL ve erkeklerde 9769 mcg.g�n/mL ve 481,3 mcg/mL'dir), ve bu durum cinsiyet temelinde doz ayarlamas�n�n gerekli olmad���n� g�stermi�tir.
Hastalardaki karakteristik �zellikler
Geriyatrik pop�lasyon
Obinutuzumab�n pop�lasyon farmakokinetik analizi, ya��n obinutuzumab farmakokineti�ini etkilemedi�ini g�stermi�tir. <65 ya��ndaki (n=375), 65-75 ya�lar�ndaki (n=265) ve >75 ya��ndaki (n=171) hastalar aras�nda obinutuzumab�n farmakokinetik �zelliklerinde anlaml� farkl�l�k g�zlenmemi�tir.
Pediyatrik pop�lasyon
Pediyatrik hastalarda obinutuzumab�n farmakokineti�ini inceleyen �al��malar yap�lmam��t�r. B�brek yetmezli�i
Obinutuzumab�n pop�lasyon farmakokinetik analizi, kreatinin klerensinin obinutuzumab farmakokineti�ini etkilemedi�ini g�stermi�tir.
Hafif (kreatinin klerensi KrKl 50-89 mL/dakika, n=464) veya orta d�zeyde (KrKl 30-49 mL/dakika, n=106) b�brek bozuklu�u olan hastalarda obinutuzumab�n farmakokinetik �zellikleri, b�brek fonksiyonu normal (KrKl ≥90 mL/dakika, n=383) hastalardakine benzer bulunmu�tur. �iddetli b�brek bozuklu�u olan (KrKl 15-29 mL/dakika) hastalarda farmakokinetik veriler s�n�rl�d�r (n=8), bu nedenle doz �nerisi yap�lamamaktad�r.
Karaci�er yetmezli�i
Karaci�er bozuklu�u olan hastalarda formal farmakokinetik �al��ma yap�lmam��t�r.
5.3. Klinik �ncesi g�venlilik verileri
Obinutuzumab�n karsinojenik potansiyelini belirlemek �zere �al��ma yap�lmam��t�r.
Obinutuzumab�n fertilite �zerindeki etkisini de�erlendirmek i�in hayvanlarda spesifik �al��malar yap�lmam��t�r. Sinomolgus maymunlarda yap�lan tekrarl� doz toksisitesi �al��malar�nda obinutuzumab erkek ve di�i �reme organlar� �zerinde advers etki g�stermemi�tir.
Gebe sinomolgus maymunlarda geli�tirilmi� pre ve postnatal geli�im (ePPND) toksisitesi �al��mas�nda teratojenik etkilere dair kan�t bulunmam��t�r. Bununla birlikte, �iftle�me sonras�
20. g�nden do�uma kadar 25 ve 50 mg/kg dozlarda (C ve EAA temelinde klinik maruziyetin 2-5 kat�) uygulanan haftal�k intraven�z obinutuzumab dozlar�, bebek maymunlarda tam B h�cre deplesyonuna yol a�m��t�r. Do�umdan sonra 28. g�nde yavrular�n ilaca maruziyeti, obinutuzumab�n kan plasenta bariyerini ge�ebildi�ini g�stermektedir. Do�um sonras� 28. g�nde yavru serumundaki konsantrasyonlar, maternal serumdaki konsantrasyon aral���nda olurken, ayn� g�nde s�tteki konsantrasyonlar daha d���k bulunmu�tur (kar��l�k gelen maternal serum d�zeylerinin %0,5'inden daha d���k); bu durum yavrularda ilaca maruziyetin rahim i�inde olu�tu�unu g�stermektedir. Do�umdan sonra 6 ay i�inde B h�cre say�lar� normal d�zeylere d�nm�� ve imm�nolojik fonksiyon geri kazan�lm��t�r.
Sinomolgus maymunlarda yap�lan, haftal�k 5, 25 ve 50 mg/kg dozlarda obinutuzumab�n (kararl� durumda Cve EAA'ya dayal� olarak klinik maruziyetin 0,7-6 kat�) uyguland��� 26 haftal�k bir �al��mada, a��r� duyarl�l�k reaksiyonlar� kaydedilmi�tir ve bu reaksiyonlar sinomolgus maymunlarda h�manize antikorun yabanc� kabul edilmesine ba�lanm��t�r. Bulgular, akut anafilaktik ve anafilaktoid reaksiyonlar� ve arterit/periarterit, glomer�lonefrit ve serozal/adventisiyal inflamasyon gibi imm�n kompleks arac�l� a��r� duyarl�l�k reaksiyonlar� ile tutarl� �ekilde sistemik inflamasyonun ve infiltratlar�n prevalans�nda bir art��� i�ermektedir. Bu reaksiyonlar, doz uygulama ve iyile�me fazlar� s�ras�nda obinutuzumab ile tedavi edilen 36 hayvan�n 6's�nda tedavinin planl� olmaks�z�n sonland�r�lmas�na yol a�m��t�r; bu de�i�imler k�smen geri d�nd�r�lebilir olmu�tur. �nsanlarda obinutuzumab ile nedensel ili�kili renal toksisite g�zlenmemi�tir.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
L-histidin
L-histidin hidroklor�r monohidrat Trehaloz dihidrat
Poloksamer 188 Enjeksiyonluk Su
6.2. Ge�imsizlikler
Bu t�bbi �r�n, b�l�m 6.6'da belirtilenlerin d���nda hi�bir t�bbi �r�nle kar��t�r�lmamal�d�r.
6.3. Raf �mr�
A��lmam�� flakon
36 ay Seyreltildikten sonra
Seyreltildikten sonra, % 0,9'luk (9 mg/mL) sodyum klor�r enjeksiyonluk ��zeltisinde 0,4 mg/mL ile 20 mg/mL aras�ndaki konsantrasyonda 2°C - 8°C aras�ndaki s�cakl�kta 24 saat boyunca ve bunu takiben 30°C'nin alt�ndaki s�cakl�kta (inf�zyon s�resi de dahil olmak �zere) 48 saat boyunca kimyasal ve fiziksel stabilite kan�tlanm��t�r.
Mikrobiyolojik a��dan bak�ld���nda, haz�rlanan inf�zyon ��zeltisi derhal kullan�lmal�d�r. Derhal kullan�lmad��� takdirde kullan�m s�ras�ndaki saklama s�releri ve kullan�m �ncesindeki ko�ullar kullan�c�n�n sorumlulu�undad�r ve normalde, seyreltme i�lemi kontroll� ve valide edilmi� aseptik �artlarda yap�lmad�k�a, saklama s�resi 2°C-8°C'de 24 saati ge�memelidir.
GAZYVA antimikrobiyal koruyucular i�ermemektedir. Bu nedenle, inf�zyonluk ��zeltinin haz�rlanmas� s�ras�nda mikrobiyolojik a��dan tehlikeye girmemesi i�in dikkatli olunmal�d�r.
6.4. Saklamaya y�nelik �zel tedbirler
Flakonlar 2°C-8°C'de buzdolab�nda saklanmal�d�r. Dondurulmamal�d�r. Flakon, ���ktan korunmak i�in kutusunda saklanmal�d�r.
T�bbi �r�n�n seyreltildikten sonraki saklama ko�ullar� i�in bkz. B�l�m 6.3.
6.5. Ambalaj�n niteli�i ve i�eri�i
T�pal� (b�til kau�uk) 50 mL (berrak Tip I cam) flakon i�erisinde 40 mL konsantre. Ambalaj boyutu 1 flakondur.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Seyreltme i�in talimatlar
GAZYVA, bir sa�l�k mesle�i mensubu taraf�ndan aseptik teknik kullan�larak haz�rlanmal�d�r. Flakonun �alkalanmamas� gerekir. GAZYVA'y� haz�rlamak i�in steril bir i�ne ve ��r�nga kullan�lmal�d�r.
KLL D�ng� 2 – 6 i�in:
Flakondan 40 mL konsantreyi �ekin ve 9 mg/mL (%0,9) sodyum klor�r enjeksiyon ��zeltisi i�eren polivinil klor�r (PVC) veya PVC olmayan poliolefin inf�zyon torbalar�nda seyreltin.
Sadece KLL – D�ng� 1
�ki inf�zyon torbas� aras�nda 1.000 mg ba�lang�� dozu i�in ayr�m yapabilmek a��s�ndan, D�ng�1, 1. g�ne ait 100 mg doz ve D�ng�1, 1. g�ne ya da 2. g�ne ait 900 mg dozun (devam dozu) ay�rt edilmesi i�in farkl� boyda torbalar�n kullan�lmas� �nerilmektedir. 2 inf�zyon torbas� haz�rlamak i�in flakondan 40 mL konsantreyi �ekiniz ve 4 mL'yi 9 mg/mL (%0,9) sodyum klor�r enjeksiyon ��zeltisi i�eren 100 mL'lik PVC veya PVC olmayan poliolefin inf�zyon torbas�nda, kalan 36 mL'yi ise 9 mg/mL (%0,9) sodyum klor�r enjeksiyon ��zeltisi i�eren 250 mL'lik PVC veya PVC olmayan poliolefin torba i�erisinde seyreltiniz. Her inf�zyon torbas�n� a��k�a etiketleyiniz.
�nf�zyon torbalar�n�n saklama ko�ullar� i�in bkz. B�l�m 6.3.
Uygulanacak GAZYVA Dozu | Gerekli GAZYVA Konsantresi Miktar� | PVC veya PVC olmayan poliolefin inf�zyon torbas�n�n boyutu |
100 mg | 4 mL | 100 mL |
900 mg | 36 mL | 250 mL |
1000 mg | 40 mL | 250 mL |
Glikoz (%5) ��zeltisi gibi di�er seyrelticiler kullan�lmamal�d�r (bkz. B�l�m 6.2).
Torba, ��zeltiyi kar��t�rmak �zere, a��r� k�p�rmeyi �nlemek i�in hafif �ekilde alt�st edilmelidir. Seyreltilmi� �r�n �alkalanmamal� veya dondurulmamal�d�r.
Parenteral t�bbi �r�nler, uygulanmadan �nce partik�ller ve renk de�i�ikli�i a��s�ndan g�rsel olarak incelenmelidir.
GAZYVA'n�n sodyum klor�r 9 mg/mL (0,9%) enjeksiyonluk ��zeltiyle seyreltilmesini takiben 0,4 ile 20,0 mg/mL konsantrasyon aral�klar�nda GAZYVA ile;
PVC, polietilen (PE), polipropilen veya poliolefin torbalar
 S�rt A�r�s�
S�rt a�r�s� birden bire ortaya
��k�p �iddetli (akut) olabilir veya zamanla geli�ip daha uzun
s�reli sorunlara (kronik) neden olabilir.
S�rt A�r�s�
S�rt a�r�s� birden bire ortaya
��k�p �iddetli (akut) olabilir veya zamanla geli�ip daha uzun
s�reli sorunlara (kronik) neden olabilir. |
 Do�um Sonras� Depresyonu
Do�um sonras� depresyonu, do�umdan sonra her on kad�ndan biri taraf�ndan
tecr�be edilen stresli bir durumdur.
Do�um Sonras� Depresyonu
Do�um sonras� depresyonu, do�umdan sonra her on kad�ndan biri taraf�ndan
tecr�be edilen stresli bir durumdur. |
 |
Pankreas Kanseri Pankreas karn�n alt k�sm�nda yatay �ekilde bulunan bir organd�r. Sindirime yard�mc� olan enzimleri ve kan �ekerini y�netmeye yard�mc� olan hormonlar� v�cuda da��tmakla g�revlidir. |
 |
Mide Kanseri Mide kanseri genellikle mideyi t�m�yle kaplayan ve mukus �retmekle g�revli h�crelerde ba�lar. Bu kanser tipine adenokarsinom denir. |
 |
Kalp Krizi Kalbe giden kan ak��� durdu�unda kalp krizi meydana gelir. |
�LA� GENEL B�LG�LER�
Roche M�stahzarlar� Sanayi A.�.
| Geri �deme Kodu | A17126 |
| Sat�� Fiyat� | 58299.93 TL [ 1 Dec 2025 ] |
| �nceki Sat�� Fiyat� | 58299.93 TL [ 24 Nov 2025 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699505762630 |
| Etkin Madde | Obinutuzumab |
| �thal ( ref. �lke : Isvicre ) ve Be�eri bir ila�d�r. |