GLINIUM PLUS 85 MCG7 43 mcg inhilasyon tozu sert kaps�l K�sa �r�n Bilgisi
{ Indakaterol Maleat + Glikopironyum Bromur }
Kaps�llerin k���k par�a��klara ayr�lmas�n� nas�l �nlerim?
Cihaz�n yan�ndaki k�rm�z� kulak��kl�klara (d��melere) bast���n�zda (5.basamak), kaps�ller k�r�labilir ve nefes al�rken a�z�n�za ya da bo�az�n�za k���k par�alar ka�abilir. Bunu a�a��dakileri uygulayarak �nleyebilirsiniz:
K�rm�z� kulakc�klara (d��melere) yaln�zca bir kere basarak.
Kaps�lleri kullanmadan �nce orjinal ambalaj�nda tutarak.
Kaps�lleri 25 oC'nin alt�ndaki oda s�cakl���nda saklayarak.
Kaps�lleri nemden koruyarak.
Kaps�l par�ac�klar� zararl� m�d�r?
Hay�r. Kaps�l, zararl� olmayan yenilebilir nitelikte jelatinden yap�lm��t�r. A�z�n�za ya da bo�az�n�za ka�an jelatin par�ac�klar� yutulabilir.
Kaps�l b�lmesinde s�k��an kaps�l� nas�l ��kartaca��m? �nhalasyon cihaz�n� a��n, ba� a�a�� �evirin ve yava��a dibine vurun.
4.1. Terap�tik endikasyonlar
GL�N�UM PLUS, kronik obstr�ktif akci�er hastal��� (KOAH) olan yeti�kin hastalarda semptomlar� hafifletmek i�in bir idame bronkodilat�r tedavisi olarak endikedir.
4.2. Pozoloji ve uygulama �ekli
�nerilen doz, bir kaps�l i�eri�inin g�nde bir kez, GL�N�UM PLUS inhaler kullan�larak solunmas�d�r.
GL�N�UM PLUS'�n her g�n ayn� saatte uygulanmas� �nerilir. Bir doz ka��r�l�rsa, ayn� g�n m�mk�n olan en k�sa s�rede al�nmal�d�r. Hastalara g�nde birden fazla doz almamalar� konusunda bilgilendirilmelidir.
Uygulama �ekli:
Sadece inhalasyon yoluyla kullan�m i�indir. Kaps�ller yutulmamal�d�r.
Kaps�ller sadece GL�N�UM PLUS inhaleri kullan�larak uygulanmal�d�r (bkz. B�l�m 6.6). Her
yeni re�ete ile birlikte verilen inhaler kullan�lmal�d�r.
Hastalar be�erî t�bbi �r�n�n do�ru �ekilde nas�l uygulanaca�� konusunda bilgilendirilmelidir. Solunumda iyile�me ya�amam�� olan hastalara, be�erî t�bbi �r�n� solumak yerine yutup yutmad�klar� sorulmal�d�r.
Be�erî t�bbi �r�n� uygulamadan �nce, kullanma talimatlar� i�in b�l�m 6.6'ya bak�n�z.
�zel pop�lasyonlara ili�kin ek bilgiler:
B�brek yetmezli�i
GL�N�UM PLUS, hafif ila orta derecede b�brek yetmezli�i olan hastalarda �nerilen dozda kullan�labilir. �iddetli b�brek yetmezli�i veya diyaliz gerektiren son d�nem b�brek yetmezli�i olan hastalarda, yaln�zca beklenen fayda, potansiyel riskten daha �nemli ise kullan�lmal�d�r (bkz. B�l�m 4.4 ve 5.2).
Karaci�er yetmezli�i
GL�N�UM PLUS, hafif ve orta �iddette karaci�er yetmezli�i olan hastalarda �nerilen dozda kullan�labilir. �iddetli karaci�er yetmezli�i olan hastalarda GL�N�UM PLUS kullan�m�na ili�kin veri yoktur, bu nedenle bu hastalarda temkinli olunmal�d�r (bkz. B�l�m 5.2).
Pediyatrik pop�lasyon
GL�N�UM PLUS'�n pediatrik pop�lasyonda (18 ya� alt�) KOAH endikasyonuyla ilgili bir kullan�m� yoktur. GL�N�UM PLUS'�n �ocuklarda g�venli�i ve etkinli�i belirlenmemi�tir. Mevcut veri bulunmamaktad�r.
Geriyatrik pop�lasyon
GL�N�UM PLUS ya�l� hastalarda (75 ya� ve �st�) �nerilen dozda kullan�labilir.
4.3. Kontrendikasyonlar
�ndakaterol maleat, glikopironyum brom�r ve/veya �r�n i�eri�indeki yabanc� maddelerden herhangi maddelerden birine (bkz. B�l�m 6.1) kar�� bilinen a��r� duyarl�l�k halinde GL�N�UM PLUS kontrendikedir.
4.4. �zel kullan�m uyar�lar� ve �nlemleri
GL�N�UM PLUS, di�er uzun etkili beta-adrenerjik agonistler veya uzun etkili muskarinik antagonistler olan GL�N�UM PLUS bile�enlerinin ait oldu�u farmakoterap�tik gruplar� i�eren be�erî t�bbi �r�nlerle birlikte uygulanmamal�d�r (bkz. B�l�m 4.5).
Ast�m
GL�N�UM PLUS, bu endikasyonda veri olmamas� nedeniyle, ast�m tedavisinde kullan�lmamal�d�r. Uzun etkili beta2-adrenerjik agonistler, ast�m tedavisi i�in kullan�ld���nda ast�mla ili�kili�l�mler de dahil olmak �zere, ast�ma ba�l� ciddi advers olay riskini art�rabilir.
Akut kullan�m i�in de�ildir
GL�N�UM PLUS, akut bronkospazm ataklar�n�n tedavisi i�in endike de�ildir.
A��r� duyarl�l�k
GL�N�UM PLUS'�n aktif maddeleri olan indakaterol veya glikopironyum uygulamas�ndan
sonra aniden ortaya ��kan a��r� duyarl�l�k reaksiyonlar� bildirilmi�tir. Alerjik reaksiyonlar�
d���nd�ren belirtiler, �zellikle anjiyo�dem (nefes alma veya yutmada g��l�k, dil, dudak ve y�z�n �i�mesi) �rtiker veya deri d�k�nt�s� ortaya ��karsa, tedavi derhal kesilmeli ve alternatif tedavi ba�lat�lmal�d�r.
Paradoksal bronkospazm
GL�N�UM PLUS uygulamas� ya�am� tehdit edebilecek paradoksal bronkospazm ile sonu�lanabilir. B�yle bir durum olu�ursa, tedavi derhal kesilmeli ve alternatif tedavi uygulanmal�d�r.
![]()
![]()
Glikopironyum ile ilgili antikolinerjik etkiler
Dar a��l� glokom
Dar a��l� glokomu olan hastalara dair veri yoktur, bu nedenle bu hastalarda GL�N�UM PLUS dikkatli kullan�lmal�d�r.
Hastalar akut dar a��l� glokom belirtileri ve semptomlar� hakk�nda bilgilendirilmeli ve bu belirti veya semptomlardan herhangi biri geli�irse GL�N�UM PLUS kullanmay� b�rakmalar� konusunda bilgilendirilmelidir.
�riner retansiyon
�riner retansiyonu olan hastalara dair veri yoktur, bu nedenle bu hastalarda GL�N�UM PLUS dikkatli kullan�lmal�d�r.
�iddetli b�brek yetmezli�i olan hastalar
Hafif ve orta derecede b�brek yetmezli�i olan hastalarda, 1,4 kata kadar olan toplam sistem glikopironyum maruziyetinde (EAAson), �iddetli ve son d�nem b�brek yetmezli�i olan hastalarda 2,2 kata kadar olan toplam sistem glikopironyum maruziyetinde (EAAson) �l�ml� ortalama art�� g�r�lm��t�r. Diyaliz gerektiren son d�nem b�brek yetmezli�i olanlar da dahil olmak �zere, �iddetli b�brek yetmezli�i olan hastalarda (tahmini glomer�ler filtrasyon h�z� 30 ml/dak /1,73 m2'nin alt�nda), �ndakaterol/Glikopironyum, sadece beklenen fayda potansiyel riskten daha �nemli ise kullan�lmal�d�r (bkz. B�l�m 5.2). Bu hastalar potansiyel advers reaksiyonlar a��s�ndan yak�ndan izlenmelidir.
Kardiyovask�ler etkiler
GL�N�UM PLUS, kardiyovask�ler bozukluklar� (koroner arter hastal�k, akut miyokard enfarkt�s�, kardiyak aritmiler, hipertansiyon) olan hastalarda dikkatle kullan�lmal�d�r.
Beta-adrenerjik agonistler, baz� hastalarda nab�z, kan bas�nc� ve/veya semptomlardaki art��larla �l��len, klinik olarak anlaml� bir kardiyovask�ler etki �retebilir. Bu be�erî t�bbi �r�nle bu t�r etkilerin ortaya ��kmas� durumunda, tedavinin kesilmesi gerekebilir. Ek olarak, beta-adrenerjik agonistlerin, her ne kadar bu g�zlemlerin klinik �nemi bilinmese de, T dalgas�n�n d�zle�mesi, QT aral���n�n uzamas� ve ST segment depresyonu gibi elektrokardiyografik (EKG) de�i�iklikler �rettikleri bildirilmi�tir. Bu nedenle, QT aral���nda bilinen veya ��phelenilen uzamas� olan hastalarda veya QT aral���n� etkileyen be�erî t�bbi �r�nlerle tedavi edilen hastalarda uzun etkili beta2-adrenerjik agonistler, dikkatle kullan�lmal�d�r.
Stabil olmayan iskemik kalp hastal���, sol ventrik�l yetmezli�i, miyokard enfarkt�s� �yk�s�, aritmi (kronik stabil atriyal fibrilasyon hari�), uzun QT sendromu �yk�s� olan veya QTc
(Fridericia y�ntemi) uzam�� (> 450 ms) hastalar klinik �al��malarda �al��ma d��� b�rak�lm��t�r, dolay�s�yla bu hasta gruplar�nda deneyim yoktur. Bu hasta gruplar�nda GL�N�UM PLUS dikkatli kullan�lmal�d�r.
Hipokalemi
Beta-adrenerjik agonistler, baz� hastalarda olumsuz kardiyovask�ler etkilere sebep olma potansiyeline sahip, beligin hipokalemiye sebep olabilir. Serum potasyumundaki azalma genellikle ge�icidir, takviye gerektirmez. �iddetli KOAH hastalar�nda, hipokalemi hipoksi ve e�lik eden tedavi ile �iddetlenebilir, bu da kardiyak aritmilere duyarl�l��� art�rabilir (bkz. B�l�m 4.5).
GL�N�UM PLUS'�n �nerilen terap�tik dozunda yap�lan klinik �al��malar�nda, hipokaleminin klinik olarak anlaml� etkileri g�zlenmemi�tir (bkz. B�l�m 5.1).
![]()
Hiperglisemi
Y�ksek dozda beta-adrenerjik agonistlerin solunmas�, plazma glikozunda art��lara neden olabilir. Diyabetik hastalarda GL�N�UM PLUS ile tedaviye ba�land�ktan sonra plazma glikozu daha yak�ndan izlenmelidir.
Uzun s�reli klinik �al��malar s�ras�nda, �nerilen dozda GL�N�UM PLUS kullanan daha fazla hasta, plaseboya (%2,7) k�yasla, kan �ekerinde klinik olarak kayda de�er de�i�iklikler (%4,9) ya�am��t�r. GL�N�UM PLUS, diyabetes mellitus'un iyi kontrol edilmedi�i hastalarda ara�t�r�lmam��t�r, bu nedenle bu t�r hastalarda dikkatli ve uygun izleme �nerilmektedir.
Genel rahats�zl�klar
GL�N�UM PLUS, konvulsif rahats�zl�klar� veya tirotoksikozu olan hastalarda ve beta- adrenerjikagonistlere al���lmad�k derecede duyarl� olan hastalarda dikkatle kullan�lmal�d�r.
Yard�mc� maddeler
Bu be�erî t�bbi �r�n laktoz i�erir. Galaktoz intolerans�, toplam laktaz yetmezli�i veya glikoz- galaktoz malabsorpsiyonu gibi nadir kal�tsal problemleri olan hastalar bu be�erî t�bbi �r�n� kullanmamal�d�r.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Her ikisi de etkin madde olan ve kararl� durum �artlar� alt�nda oral yolla uygulanan inhale indakaterol ve glikopironyumun birlikte uygulanmas�, her iki etkin maddenin de farmakokineti�ini etkilememi�tir.
GL�N�UM PLUS ile spesifik bir etkile�im �al��mas� yap�lmam��t�r. Etkile�im potansiyeli hakk�nda bilgi, iki etkin maddenin her birinin potansiyeline dayanmaktad�r.
A�a��dakilerle birlikte kullan�m� �nerilmemektedir
Beta-adrenerjik blokerler
Beta-adrenerjik blokerler, beta-adrenerjik agonistlerin etkisini zay�flatabilir veya antagonize edebilir. Bu nedenle, GL�N�UM PLUS, kullan�mlar� i�in zorlay�c� nedenler olmad�k�a, beta- adrenerjik blokerlerle (g�z damlalar� dahil) birlikte verilmemelidir. Gerekti�inde, kardiyoselektif beta-adrenerjik blokerler tercih edilmeli, ancak dikkatle uygulanmal�d�r.
Antikolinerjikler
GL�N�UM PLUS'�n antikolinerjiki�erendi�erbe�erît�bbi�r�nlerle birlikte uygulanmas�
Sempatomimetikler
Di�er sempatomimetiklerin (tek ba��na veya kombinasyon terapisinin bir par�as� olarak) birlikte uygulanmas�, indakaterol�n advers etkilerini g��lendirebilir (bkz. B�l�m 4.4).
A�a��dakilerle birlikte kullan�mda dikkat edilmesi gerekmektedir
Hipokalemi tedavisi
E�lik eden ve metilksantin t�revleri, steroidler veya potasyum tutucu olmayan di�retiklerle yap�lan hipokalemik tedavi, beta-adrenerjik agonistlerin olas� hipokalemik etkisini g��lendirebilir, bu nedenle dikkatli kullan�lmal�d�r (bkz. B�l�m 4.4).
A�a��dakilerle birlikte kullan�m�nda dikkate al�nmas� gerekenler
Metabolik ve ta��y�c� tabanl� etkile�imler
�ndakaterol klerensi, CYP3A4 ve P-glikoproteinin (P-gp) �nemli katk� maddelerinin inhibisyonu, indakaterol�n sistemik maruziyetini iki kat�na kadar ��kar�r. Maruziyetin b�y�kl���ndeki etkile�imlere ba�l� art��, �nerilen maksimum indakaterol dozunun iki kat�na kadar olan dozlarda bir y�la kadar klinik �al��malarda indakaterol ile yap�lan g�venlilik deneyimi g�z �n�ne al�nd���nda, herhangi bir g�venlilik endi�esi yaratmaz.
Simetidin veya di�er organik katyon ta��y�c� inhibit�rler
Sa�l�kl� g�n�ll�lerde yap�lan bir klinik �al��mada, glikopironyumun renal at�l�m�na katk�da bulundu�u d���n�len organik katyon ta��nmas�n�n bir inhibit�r� olan simetidin, glikopironyuma toplam maruz kalmay� (EAA) %22 oran�nda artt�rm�� ve renal klerensi %23 oran�nda azaltm��t�r. Bu de�i�ikliklerin b�y�kl���ne ba�l� olarak, glikopironyum, simetidin veya organik katyon ta��y�c�n�n di�er inhibit�rleri ile birlikte uyguland���nda, klinik olarak anlaml� ila� etkile�imi beklenmez.
4.6. Gebelik ve laktasyon
Genel Tavsiye:Gebelik Kategorisi: C
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon):
�ocuk do�urma potansiyeli bulunan kad�nlarda ve do�um kontrol� (kontrasepsiyon) uygulayanlarda kullan�m�na ili�kin herhangi bir veri yoktur.
![]()
Gebelik d�nemi:
Hamile kad�nlarda GL�N�UM PLUS kullan�m�yla ilgili mevcut veri bulunmamaktad�r. Hayvan �al��malar�, klinik olarak anlaml� maruziyetlerde �reme toksisitesi ile ilgili do�rudan veya dolayl� zararl� etkiler oldu�unu g�stermemektedir (bkz. B�l�m 5.3).
�ndakaterol, uterus d�z kas�nda gev�etici bir etki nedeniyle do�umu engelleyebilir. Bu nedenle, GL�N�UM PLUS sadece hasta i�in beklenen fayda, fetusun potansiyel riski i�in gerek�e olu�turuyorsa, hamilelik s�ras�nda kullan�lmal�d�r.
Laktasyon d�nemi:
�ndakaterol, glikopironyum ve metabolitlerinin anne s�t�ne ge�ip ge�medi�i bilinmemektedir. Mevcut farmakokinetik/toksikolojik veriler, indakaterol, glikopironyum ve metabolitlerinin emziren s��anlar�n s�t�yle at�l�m�n� g�stermi�tir. GL�N�UM PLUS'�n emziren kad�nlar taraf�ndan kullan�lmas�, ancak anne i�in beklenen faydan�n, bebek i�in olas� herhangi bir riskten daha fazla olmas� durumundad���n�lmelidir(bkz.B�l�m5.3).
�reme yetene�i /Fertilite
�reme �al��malar� ve hayvanlardaki di�er veriler, hem erkeklerde hem de kad�nlarda do�urganl�kla ilgili bir endi�eye i�aret etmemektedir.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
GL�N�UM PLUS'�n ara� ve makine kullanma yetene�i �zerinde hi�bir etkisi yoktur. Bununla birlikte, ba� d�nmesini de i�eren sersemlik hali ortaya ��kmas�, ara� ve makine kullanma yetene�ini etkileyebilir (bkz.B�l�m 4.8).
4.8. �stenmeyen etkiler
G�venlilik profilinin sunumu, GL�N�UM PLUS ve etkin maddelerin her biriyle ilgili deneyime dayanmaktad�r.
G�venlilik profilinin �zeti
�ndakaterol / Glikopironyum ile g�venlilik deneyimi, 15 aya kadar �nerilen terap�tik dozda maruziyetten olu�maktayd�.
�ndakaterol / Glikopironyum, her bir bile�ene benzer advers reaksiyonlar g�stermi�tir. indakaterol ve glikopironyum i�erdi�inden, bu bile�enlerin her biriyle ili�kili advers reaksiyonlar�n t�r� ve �iddeti, kombinasyonda beklenebilir.
G�venlilik profili, kombinasyonun her bir bile�eni ile ili�kili tipik antikolinerjik ve beta- adrenerjik semptomlarla karakterizedir. Be�eri t�bbi �r�nle ilgili di�er en yayg�n advers reaksiyonlar (�ndakaterol / Glikopironyum i�in hastalar�n en az %3'� ve ayr�ca plasebodan daha b�y�k) �ks�r�k, nazofarenjit ve ba� a�r�s� idi.
Advers reaksiyonlar�n tablo halinde �zeti
Klinik �al��malar s�ras�nda ve pazarlama sonras� kaynaklardan tespit edilen advers reaksiyonlar MedDRA sistem organ s�n�f� taraf�ndan listelenmi�tir (Tablo 1). Advers reaksiyonlar, her sistem organ s�n�f� i�inde, en s�k g�r�len reaksiyonlar �nce olmak �zere, s�kl��a g�re s�ralan�r. Her bir s�kl�k grubunda, advers reaksiyonlar azalan ciddiyet s�ras�na g�re sunulmaktad�r. Ek olarak, her advers reaksiyon i�in kar��l�k gelen s�kl�k s�n�fland�rmas� a�a��daki d�zene dayanmaktad�r: �ok yayg�n (≥1/10); yayg�n (≥1/100 ila <1/10); yayg�n olmayan (≥1/1.000 ila <1/100); seyrek (≥1/10.000, <1/1.000); �ok seyrek (<1/10.000); bilinmiyor (eldeki verilerden hareketle belirlenemiyor).
Tablo 1 Advers reaksiyonlar
Advers reaksiyonlar | S�kl�k s�n�fland�rmas� |
Enfeksiyonlar ve enfestasyonlar | |
�st solunum yolu enfeksiyonu | �ok yayg�n |
Nazofarenjit | Yayg�n |
�drar yolu enfeksiyonu | Yayg�n |
Sin�zit | Yayg�n |
Rinit | Yayg�n |
Ba����kl�k sistemi hastal�klar� | |
A��r� duyarl�l�k | Yayg�n |
Anjio�dem | Yayg�n olmayan |
Metabolizma ve beslenme hastal�klar� | |
Hiperglisemi ve diabetes mellitus | Yayg�n |
Psikolojik hastal�klar | |
�nsomnia | Yayg�n olmayan |
Sinir sistemi hastal�klar� | |
Ba� d�nmesini de i�eren sersemlik hali | Yayg�n |
Ba� a�r�s� | Yayg�n |
Parastezi | Seyrek |
G�z hastal�klar� | |
Glokom | Yayg�n olmayan |
Kardiyak hastal�klar | |
�skemik kalp hastal��� | Yayg�n olmayan |
Atriyal fibrilasyon | Yayg�n olmayan |
Ta�ikardi | Yayg�n olmayan |
�arp�nt� | Yayg�n olmayan |
Solunum, g���s hastal�klar� ve mediyastinal hastal�klar | |
�ks�r�k | Yayg�n |
Bo�az tahri�i dahil olmak �zere orofaringeal a�r� | Yayg�n |
Paradoksal bronkospazm | Yayg�n olmayan |
Disfoni | Yayg�n olmayan |
Epistaksis | Yayg�nolmayan |
Gastrointestinal hastal�klar |
|
Dispepsi | Yayg�n |
Di� ��r��� | Yayg�n |
Gastroenterit | Yayg�n olmayan |
A��z kurulu�u | Yayg�n olmayan |
Deri ve deri alt� doku hastal�klar� |
|
Ka��nt�/d�k�nt� | Yayg�n olmayan |
Kas-iskelet sistemi hastal�klar�, ba� dokusu ve kemik hastal�klar� |
|
Kas-iskelet sistemi a�r�s� | Yayg�n olmayan |
Kas spazm� | Yayg�n olmayan |
Miyalji | Yayg�n olmayan |
Ekstremitede a�r� | Yayg�n olmayan |
B�brek ve idrar yolu hastal�klar� |
|
Mesane t�kan�kl��� ve �riner retansiyon | Yayg�n |
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar |
|
Y�ksek ate� | Yayg�n |
G���s a�r�s� | Yayg�n |
Periferik �dem | Yayg�n olmayan |
Yorgunluk | Yayg�n olmayan |
Se�ilen advers reaksiyonlar�n tan�m�
�ks�r�k yayg�n, ancak genellikle hafif �iddette.
![]()
��pheli advers reaksiyonlar�nraporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem
ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar / risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr; eposta;tufam@titck.gov.tr;tel:0 800 314 00 08; faks:0 312 218 35 99)
4.9. Doz a��m� ve tedavisi
GL�N�UM PLUS ile klinik olarak anlaml� doz a��m� hakk�nda bilgi yoktur.
A��r� doz, ta�ikardi, titreme, �arp�nt�, ba� a�r�s�, bulant�, kusma, uyu�ukluk, ventrik�ler aritmiler, metabolik asidoz, hipokalemi ve hiperglisemi gibi beta-adrenerjik uyar�c�lar�n tipik etkilerinin abart�l� olarak ortaya ��kmas�na yol a�abilir veya artm�� intraok�ler bas�n� (a�r�, g�rme bozukluklar� veya g�z�n k�zarmas�na neden olur), obstipasyon veya i�eme zorluklar� gibi antikoinerjik etkileri ind�kleyebilir. Destekleyici ve semptomatik tedavi endikedir. Ciddi vakalarda hastalar hastaneye yat�r�lmal�d�r. Beta-adrenerjik etkilerin tedavisi i�in kardiyoselektif beta blokerlerin kullan�m� d���n�lebilir, ancak beta-adrenerjik blokerlerin kullan�m� bronkospazm� provoke edebilece�inden, yaln�zca doktor g�zetimi alt�nda, �ok dikkatli �ekilde kullan�lmal�d�r.
E�er k�rm�z� kulak��klar (d��meler) s�k���rsa ne yapmal�y�m?
Kulak��klar� (d��meleri) yava��a kanat��klar�n yard�m�yla ilk konumuna geri �ekin.
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Obstr�ktif havayolu hastal�klar� i�in ila�lar, antikolinerjiklerle kombinasyon halinde adrenerjikler,
ATC kodu: R03AL04
Etki mekanizmas�
�ndakaterol/Glikopironyum
�ndakaterol ve glikopironyum birlikte uyguland���nda, d�z kas gev�emesini sa�lamak i�in farkl� resept�rleri ve yollar� hedefleyen farkl� etki bi�imleri nedeniyle, ek etkililik sa�larlar. Merkeziye kar�� periferik hava yollar�ndaki beta-adrenosept�rlerin ve M3-resept�rlerinin diferansiyel yo�unlu�u nedeniyle, beta-agonistleri periferik hava yollar�n�n gev�etilmesinde daha etkili olmal�d�r, ancak bir antikolinerjik bile�ik merkezi hava yollar�nda daha etkili olabilir. Bu nedenle, insan akci�erinin hem periferik hem de merkezi solunum yollar�nda bronkodilasyon i�in beta-adrenerjik agonist ve muskarinik antagonistin bir kombinasyonu faydal� olabilir.
Indakaterol
�ndakaterol, g�nde bir kez uygulama i�in uzun etkili bir beta-adrenerjik agonisttir. �ndakaterol de dahil olmak �zere beta-adrenosept�r agonistlerinin farmakolojik etkileri, en az�ndan k�smen, adenosin trifosfat�n (ATP) siklik-3 ', 5'-adenosin monofosfata (siklik AMP) d�n���m�n� katalize eden enzim olan intrasel�ler adenil siklaz�n stim�lasyonuna dayand�r�labilir. Artm�� siklik AMP seviyeleri bron�iyal d�z kas�n gev�emesine neden olur. In vitro �al��malar, indakaterol�n beta-resept�rlerinde betave beta-resept�rlerine k�yasla kat kat daha fazla agonist aktiviteye sahip oldu�unu g�stermi�tir.
Solundu�unda, indakaterol lokal olarak akci�erde bronkodilat�r olarak hareket eder. �ndakaterol, nanomolar potansiyeliolaninsanbeta2-adrenerjik resept�r�nde k�smi bir
agonisttir.
Her ne kadar beta-adrenerjik resept�rler bron�iyal d�z kasta ve beta-adrenerjik resept�rler insan kalbinde bask�n resept�rler olsa da, kalpte toplam adrenerjik resept�rlerin %10 ila
%50'sini olu�turan beta-adrenerjik resept�rler de vard�r. Kalpteki varl���, olduk�a se�ici beta- adrenerjik agonistlerin bile kardiyak etkilere sahip olma olas�l���n� art�r�r.
Glikopironyum
Glikopirronyum, KOAH'�n g�nde bir kez idame bronkodilat�r tedavisi i�in inhale uzun etkili muskarinik resept�r antagonistidir (antikolinerjik). Parasempatik sinirler, solunum yollar�ndaki ana bronkokonstriktif sinir yoludur ve kolinerjik ton, KOAH'ta hava ak��� t�kan�kl���n�n �nemli geri d�n���ml� bile�enidir. Glikopironyum, asetilkolinin hava yolu d�z kas h�creleri �zerindeki bronkokonstrikt�r etkisini bloke eder, b�ylece hava yollar�n� geni�letir.
Glikopironyum brom�r, y�ksek duyarl�l�kl� bir muskarinik resept�r antagonistidir. �nsan M2 resept�r�nden fazla M3 resept�rleri i�in 4 kattan fazla se�icilik, radyoligand ba�lanma �al��malar� kullan�larak g�sterilmi�tir.
Farmakodinamik etkiler
�ndakaterol ve glikopironyum kombinasyonu, dozlamadan sonraki 5 dakika i�inde h�zl� bir etki ba�lang�c� g�stermi�tir. Etki, 24 saatlik doz aral��� boyunca sabit kal�r.
24 saatlik seri FEV�l��mlerinden elde edilen ortalama bronkodilat�r etki, 26 haftal�k tedaviden sonra 320 ml idi. Etki, tek ba��na indakaterol, glikopironyum veya tiotropiyum ile kar��la�t�r�ld���nda, �ndakaterol/Glikopironyum i�in anlaml� olarak daha y�ksekti (her kar��la�t�rma i�in 110 ml'lik fark).
Plasebo veya monoterapi bile�enleriyle kar��la�t�r�ld���nda, �ndakaterol/Glikopironyum etkisi ile ilgili zaman i�inde ta�ifilaksiye dair kan�t yoktu.
Kalp at�� h�z� �zerindeki etkiler
Sa�l�kl� g�n�ll�lerdeki kalp at�� h�z� etkileri, her biri �ndakaterol/Glikopironyum 'un �nerilen terap�tik dozundan 4 kat fazla olan dozlar�n birer saat aral�klarla d�rt sefer uygulanmas�n�n ard�ndan, plasebo, indakaterol, glikopironyum ve salmeterol�n etkileriyle k�yaslanarak ara�t�r�ld�.
Plaseboya k�yasla en b�y�k zaman uyumlu kalp at�� h�z� art��� +5,69 bpm (% 90 CI [2,71, 8,66]), en b�y�k azalma -2,51 bpm (% 90 CI [-5,48, 0,47]) idi. Genel olarak zaman i�indeki kalp at�� h�z� �zerindeki etkisi, �ndakaterol/Glikopironyum'un tutarl� bir farmakodinamik etkisini g�stermedi.
Supraoterap�tik doz d�zeylerinde KOAH hastalar�nda kalp at�� h�z� ara�t�r�ld�. �ndakaterol/Glikopironyum 'un 24 saat boyunca ortalama kalp at�� h�z� ve 30 dakika, 4 saat ve 24 saat sonra de�erlendirilen kalp at�� h�z� �zerinde hi�bir ilgili etkisi olmam��t�r.
QT aral���
�ndakaterol/Glikopironyum bile�enlerinin klinik doz seviyelerinde QT uzama potansiyeline sahip oldu�u bilinmemektedir. Y�ksek doz inhale indakaterol (�nerilen maksimum terap�tik dozun iki kat�na kadar) ile sa�l�kl� g�n�ll�lerde yap�lan bir kapsaml� QT (TQT) �al��mas�, QT aral��� �zerinde klinik olarak anlaml� bir etki g�stermemi�tir. Benzer �ekilde, yap�lan bir TQT
�al��mas�nda, glikopironyum i�in, �nerilen terap�tik dozun 8 kat�n�n solunmas�n�n ard�ndan QT uzamas� g�zlenmemi�tir.
�ndakaterol/Glikopironyum 'un QTc aral��� �zerindeki etkileri, sa�l�kl� g�n�ll�lerde, �ndakaterol/Glikopironyum 'un �nerilen terap�tik dozunun 4 kat� fazlas�n�n birer saat aral�klarla d�rt defada inhalasyonundan sonra ara�t�r�ld�. Plaseboya kar�� en b�y�k zaman uyumlu fark 4,62 ms (% 90 CI 0,40, 8,85 ms), en b�y�k zaman uyumlu azalma -2,71 ms (% 90 CI -6,97, 1,54 ms) idi ve bu da �ndakaterol/Glikopironyum 'un, QT aral��� �zerine, bile�enlerinin �zelliklerinden beklendi�i gibi, ilgili bir etkisinin olmad���n� g�sterdi.
KOAH hastalar�nda, 116 mikrogram/86 mikrogram ve 464 mikrogram/86 mikrogram aras�ndaki �ndakaterol/Glikopironyum supraoterap�tik dozlar�, QTcF'li hastalar�n ba�lang�� de�erine g�re 30 ms ve 60 ms aras�nda daha y�ksek bir oran g�sterdi (plasebo i�in %16,0 ila
%21,6 ve 1,9 aras�nda de�i�iyor), ancak ba�lang�� de�erden >60 ms QTcF art��� yoktu. Ayr�ca 464 mikrogram/86 mikrograml�k en y�ksek doz �ndakaterol/Glikopironyum seviyesi, daha y�ksek oranda mutlak QTcF de�erleri > 450 ms (plasebo i�in %12,2'ye kar�� % 5,7) g�sterdi.
Serum potasyum ve kan �ekeri
Sa�l�kl� g�n�ll�lerde, tavsiye edilen terap�tik �ndakaterol/Glikopironyum dozunun 4 kat�n�n uygulanmas�ndan sonra, serum potasyum �zerindeki etki �ok k���kt� (plaseboya k�yasla maksimum fark –0,14 mmol/l). Kan �ekeri �zerindeki maksimum etki 0,67 mmol/ l idi.
Klinik etkililik ve g�venlilik
�ndakaterol/Glikopironyum klinik Faz III geli�tirme program�, 8.000'den fazla hastan�n kaydoldu�u alt� �al��may� i�ermi�tir: 1) 26 haftal�k plasebo ve aktif kontroll� (g�nde bir kez indakaterol, g�nde bir kez glikopironyum, g�nde bir kez a��k etiketli tiotropiyum); 2) 26 haftal�k aktif kontroll� (flutikazon/salmeterol g�nde iki kez) �al��ma; 3) 64 haftal�k aktif kontroll� (g�nde bir kez glikopironyum, g�nde bir kez a��k etiketli tiotropiyum) �al��ma; 4) 52 haftal�k plasebo kontroll� bir �al��ma; 5) 3 haftal�k plasebo ve aktif kontroll� (g�nde bir kez tiotropiyum) egzersiz tolerans �al��mas�; ve 6) 52 haftal�k aktif kontroll� (g�nde iki kez flutikazon/salmeterol) �al��ma.
Bu �al��malar�n d�rd�nde, orta ila �iddetli KOAH klinik tan�s� olan hastalar �al��maya al�nd�. 64 haftal�k �al��maya, bir �nceki y�l ≥1 orta veya �iddetli KOAH alevlenmesi �yk�s� olan �iddetli ila �ok �iddetli KOAH tan�s� alm�� hastalar dahil edildi. 52 haftal�k aktif kontroll� �al��mada, bir �nceki y�lda ≥1 orta veya �iddetli KOAH alevlenmesi �yk�s� olan orta ila �ok �iddetli KOAH'l� hastalar �al��maya al�nd�.
Akci�er fonksiyonu �zerindeki etkiler
�ndakaterol/Glikopironyum, bir dizi klinik �al��mada akci�er fonksiyonunda (bir saniyede zorlanan ekspiratuar hacim ile �l��len �ekliyle, FEV) klinik olarak anlaml� iyile�meler g�sterdi. Faz III �al��malar�nda, ilk dozdan sonraki 5 dakika i�inde bronkodilat�r etkileri g�r�ld� ve bu etki ilk dozdan itibaren 24 saatlik dozlama aral��� boyunca korundu. Bronkodilat�r etkisinde zamanla zay�flama g�zlenmedi.
Etkinin b�y�kl���, referans de�erde hava ak��� s�n�rlamas�n�n geri �evrilebilirlik derecesine ba�l�yd� (k�sa etkili muskarinik antagonist bronkodilat�r ve k�sa etkili beta2-agonist
bronkodilat�r�n uygulanmas�yla test edilmi�tir): Ba�lang��ta en d���k d�zelebilirlik derecesine sahip hastalar (<%5), genellikle ba�lang��ta d�zelebilirlik derecesi daha y�ksek olan hastalardan (≥%5) daha d���k bronkodilat�r yan�t� g�stermi�tir. 26 haftada (primer sonlan�m noktas�) �ndakaterol/Glikopironyum, en d���k d�zelebilirlik dereceli (<%5) (p = 0,053) en d���k FEV'i 80 ml artt�rm��t�r (�ndakaterol/Glikopironyum n = 82; plasebo n = 42) ve ba�lang��ta d�zelebilirlik derecesi (≥%5) plaseboya k�yasla (p <0,001) daha y�ksek olan hastalarda 220 ml artt�rm��t�r (�ndakaterol/Glikopironyum n = 392, plasebo n = 190).
En d���k ve en y�ksek FEV1:
�ndakaterol/Glikopironyum, 26 haftal�k primer sonlan�m noktas�nda (p <0,001) plaseboya k�yasla doz sonras� en d���k FEV'i 200 ml artt�rd� ve her monoterapi bile�eni tedavi kolu (indakaterol ve glikopironyum) ile tiotropiyum tedavi koluna k�yasla, a�a��daki tabloda g�sterildi�i gibi, istatistiksel olarak anlaml� art��lar g�sterdi.
Doz sonras� en d���k FEV1 (en k���k ortalama kareler), 1. G�n ve 26. hafta (primer sonlan�m noktas�)
Tedavi fark� | 1. G�n | 26. Hafta |
�ndakaterol/Glikopironyum – plasebo | 190 ml (p<0,001) | 200 ml (p<0,001) |
�ndakaterol/Glikopironyum – indakaterol | 80 ml (p<0,001) | 70 ml (p<0,001) |
�ndakaterol/Glikopironyum – glikopironyum | 80 ml (p<0,001) | 90 ml (p<0,001) |
�ndakaterol/Glikopironyum – tiotropiyum | 80 ml (p<0,001) | 80 ml (p<0,001) |
Ortalama doz �ncesi FEV(�al��ma ilac� sabah dozundan 45 ve 15 dakika �nce al�nan de�erlerin ortalamas�), 26. haftada flutikazon/salmeterol (en k���k kareler [LS]ortalama tedavi fark� 100 ml, p <0,001) ile kar��la�t�r�ld���nda, 52. haftada plasebo (LS ortalama tedavi fark� 189 ml, p <0,001) ile kar��la�t�r�ld���nda ve 64. haftaya kadar yap�lan t�m vizitlerde glikopironyum (LS ortalama tedavi fark� 70-80 ml, p <0,001) ve tiotropiyum (LS ortalama tedavi fark� 60-80 ml, p <0,001) ile kar��la�t�r�ld���nda �ndakaterol/Glikopironyum lehine istatistiksel olarak anlaml�yd�. 52 haftal�k aktif kontroll� �al��mada, flutikazon/salmeterol (LS ortalama tedavi fark� 62-86 ml, p <0,001) ile kar��la�t�r�ld���nda, 52. haftaya kadar olan t�m vizitlerde ortalama doz �ncesi FEV, �ndakaterol/Glikopironyum lehine istatistiksel olarak anlaml�yd�. 26. haftada �ndakaterol/Glikopironyum, dozdan sonraki ilk 4 saatte plasebo ile kar��la�t�r�ld���nda, FEVen y�ksek de�erinde istatistiksel olarak anlaml� iyile�me g�sterdi (LS ortalama tedavi fark� 330 ml) (p <0,001).
FEV1 EAA:
�ndakaterol/Glikopironyum, 26 haftada flutikazon/salmeterol ile kar��la�t�r�ld���nda, doz sonras� FEVEAA'yi (primer sonlan�m noktas�) 140 ml artt�rd� (p <0,001).
Semptomatik sonu�lar
Nefes darl���:
�ndakaterol/Glikopironyum, Ge�i� Dispne �ndeksi (TDI) ile de�erlendirilen nefes darl���n� istatistiksel olarak �nemli �l��de azaltt�; plasebo (LS ortalama tedavi fark� 1,09, p <0,001),
tiotropiyum (LS ortalama tedavi fark� 0,51, p = 0,007) ve flutikazon/salmeterol (LS ortalama tedavi fark� 0,76, p = 0,003) ile kar��la�t�r�ld���nda 26. haftadaki TDI odak skorunda istatistiksel olarak anlaml� bir iyile�me g�sterdi. �ndakaterol ve glikopironyumdaki iyile�meler s�ras�yla 0,26 ve 0,21 idi.
�ndakaterol/Glikopironyum alan hastalar�n istatistiksel olarak anlaml� derecede y�ksek bir y�zdesi, 26. haftada TDI odak skorunda plaseboya k�yasla 1 puan veya daha fazla iyile�me ile yan�t verdi (s�ras�yla %68,1 ve %57,5, p = 0,004). Hastalar�n daha y�ksek bir oran�, 26. haftada �ndakaterol/Glikopironyum ile tiotropiyum (%68,1 �ndakaterol/Glikopironyum 'a kar�� %59,2 tiotropiyum, p = 0,016) ve flutikazon/salmeterol (%65,1 �ndakaterol/Glikopironyum 'a kar�� %55,5 flutikazon/salmeterol, p = 0,088) ile kar��la�t�r�ld���nda klinik olarak anlaml� yan�t sergilemi�tir.
Sa�l�kla ili�kili ya�am kalitesi:
�ndakaterol/Glikopironyum, ayr�ca plasebo (LS ortalama tedavi fark� -3,01, p = 0,002) ve tiotropiyum (LS ortalama tedavi fark� -2,13, p = 0,009) ile kar��la�t�r�ld���nda 26 haftada SGRQ toplam skorunda bir azalma ve indakaterol ve glikopironuma kar�� s�ras�yla -1,09 ve - 1,18 azalmalar ile belirtildi�i gibi, St. George Solunum Anketi (SGRQ) kullan�larak �l��len sa�l�kla ili�kili ya�am kalitesi �zerinde istatistiksel olarak anlaml� bir etki g�stermi�tir. 64. haftada, tiotropiyum ile kar��la�t�r�ld���nda azalma istatistiksel olarak anlaml�yd� (LS ortalama tedavi fark� -2,69, p <0,001). 52. haftada flutikazon/salmeterol ile kar��la�t�r�ld���nda azalma istatistiksel olarak anlaml�yd� (LS ortalama tedavi fark� -1,3, p = 0,003).
�ndakaterol/Glikopironyum alan hastalar�n daha y�ksek bir y�zdesi, 26. haftada plasebo (s�ras�yla %63,7 ve %56,6, p = 0,088) ve tiotropiyum ile kar��la�t�r�ld���nda (% 63,7 �ndakaterol/Glikopironyum kar�� %56,4 tiotropiyum, p = 0,047), 64. haftada glikopironyum ve tiotropiyum ile kar��la�t�r�ld���nda (s�ras�yla %57,8 �ndakaterol/Glikopironyum, %51,8 glikopironyum, p = 0,055; % 50,8 tiotropiyum, p = 0,051), 52. haftada flutikazon/salmeterol ile kar��la�t�r�ld���nda (% 49,2 �ndakaterol/Glikopironyum, % 43,7 flutikazon/salmeterol, olas�l�k oran�: 1,30, p <0,001) SGRQ skorunda (ba�lang��tan en az 4 birim azalma olarak tan�mlanm��t�r) klinik olarak anlaml� bir iyile�me ile cevap vermi�tir.
G�nl�k aktiviteler
�ndakaterol/Glikopironyum, 26 hafta boyunca "ola�an g�nl�k aktivitelerin ger�ekle�tirilebildi�i g�nler” y�zdesinde, tiotropiyum kar��s�nda istatistiksel olarak �st�n bir iyile�me g�sterdi (LS ortalama tedavi fark� %8,45, p <0,001). 64. haftada, �ndakaterol/Glikopironyum glikopironyum kar��s�nda say�sal iyile�me (LS ortalama tedavi fark� %1,95; p = 0,175) ve tiotropiyum kar��s�nda istatistiksel iyile�me (LS ortalama tedavi fark� %4,96; p = 0,001) g�sterdi.
KOAH alevlenmeleri
�ndakaterol/Glikopironyum (n=729), glikopironyum (n=739) ve tiotropiyumun (n=737) kar��la�t�r�ld��� 64 haftal�k �al��mada, �ndakaterol/Glikopironyum, orta veya �iddetli KOAH alevlenmelerinin y�ll�k oran�n� glikopironyum ile kar��la�t�r�ld���nda %12 oran�nda (p = 0,038) ve tiotropiyum ile kar��la�t�r�ld���nda %10 oran�nda (p = 0,096) d���rd�. Orta veya �iddetli KOAH alevlenmesi/hasta-y�l say�s�, �ndakaterol/Glikopironyum i�in 0,94 (812 vaka), glikopironyum i�in 1,07 (900 vaka) ve tiotropyum i�in 1,06 (898 vaka) idi �ndakaterol/Glikopironyum ayr�ca, t�m KOAH alevlenmelerinin (hafif, orta veya �iddetli) y�ll�k oran�n� glikopironyum (p = 0.001) ile kar��la�t�r�ld���nda %15 ve tiotropiyum ile
kar��la�t�r�ld���nda %14 oran�nda istatistiksel olarak anlaml� �l��de azaltm��t�r (p = 0,002). T�m KOAH alevlenmelerinin/hasta-y�l say�s� �ndakaterol/Glikopironyum i�in 3,34 (2.893 vaka), glikopironyum i�in 3,92 (3.294 vaka) ve tiotropyum i�in 3,89 (3.301 vaka) idi.
�ndakaterol/Glikopironyum (n = 1.675) ve flutikazon/salmeterolun (n = 1.679) kar��la�t�r�ld���
52 haftal�k �al��mada, �ndakaterol/Glikopironyum, e�it etkililik primer �al��ma hedefini, flutikazon/salmeterol ile kar��la�t�rd���nda, t�m KOAH alevlenmeleri (hafif, orta veya �iddetli) oran�nda kar��lam��t�r. T�m KOAH alevlenmelerinin/hasta-y�l say�s� �ndakaterol / Glikopironyum i�in 3,59 (4.531 vaka) ve flutikazon/salmeterol i�in 4,03 (4.969 vaka) idi. �ndakaterol/Glikopironyum ayr�ca alevlenmelerin y�ll�k oran�nda %11 azaltma sa�layarak, flutikazon/salmeterol'e kar�� �st�nl�k g�sterdi (p = 0,003).
Flutikazon/salmeterol ile kar��la�t�r�ld���nda, �ndakaterol/Glikopironyum hem orta hem de �iddetli alevlenmelerin y�ll�k oran�n� %17 (p <0,001) ve �iddetli alevlenmelerin y�ll�k oran�n� (hastaneye yatmay� gerektiren) %13 (istatistiksel olarak anlaml� de�il, p = 0,231) azaltt�. Orta veya �iddetli KOAH alevlenmesi/hasta-y�l say�s� �ndakaterol/Glikopironyum i�in 0,98 (1.265 vaka) ve flutikazon/salmeterol i�in 1,19 (1.452 vaka) idi. �ndakaterol/Glikopironyum, alevlenme riskinde %22 azalma (p <0,001) ile ilk orta �iddetli alevlenmeye kadar olan s�reyi uzatt� ve alevlenme riskinde %19 azalma ile ilk �iddetli alevlenmeye kadar olan s�reyi uzatt� (p = 0,046).
�ndakaterol/Glikopironyum kolunda pn�moni insidans� %3,2 idi ve bu oran flutikazon/salmeterol kolunda %4,8 idi (p = 0,017). �lk pn�moniye kadar ge�en s�re, flutikazon/salmeterol ile kar��la�t�r�ld���nda, �ndakaterol/Glikopironyum ile uzat�ld� (p = 0,013).
�ndakaterol/Glikopironyum (n = 258) ve flutikazon/salmeterol'� (n = 264) 26 hafta boyunca kar��la�t�ran ba�ka bir �al��mada, orta veya �iddetli KOAH alevlenmesi/hasta-y�l say�s� s�ras�yla 0,15'e kar�� 0,18 (22 vakaya kar�� 18 vaka) idi (p = 0,512) ve t�m KOAH alevlenmesi/hasta-y�l say�s� (hafif, orta veya �iddetli) s�ras�yla 0,72'ye kar�� 0,94 (86 vakaya kar�� 113 vaka) idi (p = 0,098).
Kurtarma ila� tedavisi kullan�m�
26 hafta boyunca, �ndakaterol/Glikopironyum, kurtarma ilac� (salbutamol) kullan�m�n� plaseboya k�yasla g�nde 0,96 puf (p <0,001), tiotropiyuma k�yasla g�nde 0,54 puf (p <0,001) ve flutikazon/salmeterola k�yasla g�nde 0,39 puf (p = 0,019) olarak, istatistiksel olarak anlaml� derecede azaltm��t�r. 64 hafta boyunca bu azalma, tiotropiyum ile kar��la�t�r�ld���nda g�nde 0,76 puf (p <0,001) idi. 52 hafta boyunca, �ndakaterol/Glikopironyum kurtarma ilac� kullan�m�n�, flutikazon/salmeterol ile kar��la�t�r�ld���nda g�nde 0,25 puf azaltt� (p <0,001).
Egzersiz tolerans�
Sabahlar� al�nan �ndakaterol/Glikopironyum, dinamik hiperinflasyonu azaltt� ve ilk dozdan itibaren s�rd�r�lebilen egzersiz s�resini iyile�tirdi. Tedavinin ilk g�n�nde, egzersiz alt�ndaki inspiratuar kapasite plaseboya k�yasla anlaml� derecede iyile�ti (LS ortalama tedavi fark� 250 ml, p <0,001). �� haftal�k tedaviden sonra, �ndakaterol/Glikopironyum ile inspiratuar kapasitedeki iyile�me plaseboya k�yasla daha da b�y�kt� (LS ortalama tedavi fark� 320 ml, p
<0,001) ve egzersiz dayan�kl�l��� s�resi plaseboya k�yasla artt� (LS ortalama tedavi fark� 59,5 saniye, p = 0,006).
Pediyatrik pop�lasyon
Avrupa �la� Ajans�, kronik obstr�ktif akci�er hastal���nda (KOAH) pediyatrik pop�lasyonun t�m alt k�melerinde �ndakaterol/Glikopironyum ile yap�lan �al��malar�n sonu�lar�n� g�nderme
zorunlulu�undan vazge�mi�tir (pediatrik kullan�m hakk�nda bilgi i�in b�l�m 4.2'ye bak�n�z).
5.2. Farmakokinetik �zellikler
Genel �zellikler:Emilim
�ndakaterol/Glikopironyum
�ndakaterol/Glikopironyum solunduktan sonra, indakaterol ve glikopironyumun pik plazma konsantrasyonlar�na ula�mak i�in ortalama s�re s�ras�yla yakla��k 15 dakika ve 5 dakikad�r.
In vitro performans verilerine dayanarak, akci�ere verilen indakaterol dozunun �ndakaterol/Glikopironyum ve indakaterol monoterapi �r�n� i�in benzer olmas� beklenir. �ndakaterol/Glikopironyum inhalasyonundan sonra indakaterole kararl� durum maruziyeti, indakaterol monoterapi �r�n� inhalasyonundan sonra sistemik maruziyete benzer veya biraz daha d���kt�.
�ndakaterol/Glikopironyum inhalasyonunun ard�ndan indakaterol�n mutlak biyoyararlan�m�n�n
, verilen dozun %61 ila 85'i aras�nda oldu�u ve glikopironyumun, verilen dozun yakla��k
%47'si aras�nda oldu�u hesaplanm��t�r.
�ndakaterol/Glikopironyum inhalasyonundan sonra glikopironuma kararl� durum maruziyeti, glikopironyum monoterapi �r�n� inhalasyonundan sonraki sistemik maruziyete benzerdi.
�ndakaterol
�ndakaterol�n kararl� durum konsantrasyonlar�na, g�nde bir kez uyguland�ktan sonraki 12 ila 15 g�n i�inde ula��lm��t�r. �ndakaterol, yani EAA'n�n 1. g�ne k�yasla 14. g�nde veya 15. g�nde 24 saatlik dozlama aral��� boyunca ortalama birikme oran�, 60 mikrogram ile 480 mikrogram (verilen doz) aral���ndaki g�nde bir kez solunan dozlar i�in 2,9 ila 3,8 aras�ndayd�.
Glikopironyum
KOAH'l� hastalarda, tedavinin ba�lamas�ndan sonraki bir hafta i�inde glikopironyum farmakokinetik kararl� durumuna ula��ld�. �nerilen g�nde-bir kez uygulanan dozlama rejiminde glikopironyumun kararl� durum ortalama en y�ksek ve en d���k plazma konsantrasyonlar� s�ras�yla 166 pikogram/ml ve 8 pikogram/ml idi. Glikopironyuma (24 saatlik dozlama aral��� boyunca EAA) kararl� durum maruziyeti, ilk dozdan sonra yakla��k 1,4 ila 1,7 kat daha y�ksekti.
Da��l�m
�ndakaterol
�ntraven�z inf�zyondan sonra terminal eliminasyon faz� s�ras�nda indakaterol�n da��l�m hacmi, geni� bir da��l�m� g�sterir �ekilde 2.557 litredir. In vitro insan serumu ve plazma proteinlerine ba�lanma yakla��k %95 idi.
Glikopironyum
�ntraven�z dozlamadan sonra, glikopironyumun kararl� durum da��l�m hacmi 83 litredir ve
terminal fazdaki da��l�m hacmi 376 litredir. �nhalasyondan sonra terminal fazdaki g�r�n�r da��l�m hacmi neredeyse 20 kat daha b�y�kt�, bu da inhalasyondan sonra daha yava� eliminasyonu yans�t�r. Glikopironyumun in vitro insan plazma proteinlerine ba�lanmas�, 1 ila 10 nanogram/ml konsantrasyonlarda %38 ila %41 idi.
Biyotransformasyon
�ndakaterol
Bir insan ADME (emilim, da��l�m, metabolizma, at�l�m) �al��mas�nda radyoaktif etiketli indakaterol�n oral uygulamas�ndan sonra, de�i�memi� indakaterol ana bile�endir ve 24 saat i�inde serumda toplam ila�la ilgili EAA'n�n yakla��k ��te birini olu�turur. Hidroksillenmi� bir t�rev, serumdaki en �nemli metabolittir. �ndakaterol ve hidroksile indakaterol�n fenolik O- glukuronidleri, daha da belirgin metabolitlerdir. Hidroksillenmi� t�revin bir diastereomeri, indakaterol�n N-glukuronidi ve C- ve N-dealkilatl� �r�nler, ayr�ca tan�mlanan metabolitlerdir.
In vitro UGT1A1 izoformu, indakaterol�n metabolik klerensine �nemli bir katk�da bulunur. Bununla birlikte, farkl� UGT1A1 genotiplerine sahip pop�lasyonlarda yap�lan bir klinik �al��mada g�sterildi�i gibi, indakaterole sistemik maruziyet UGT1A1-genotipinden �nemli �l��de etkilenmemektedir.
Rekombinant CYP1A1, CYP2D6 ve CYP3A4 ile ink�basyonlarda oksidatif metabolitler bulunmu�tur. CYP3A4'�n, indakaterol�n hidroksilasyonundan sorumlu bask�n izoenzim oldu�u sonucuna var�lm��t�r. In vitro ara�t�rmalar ayr�ca indakaterol�n, P-gp at�m pompas� i�in d���k afiniteli bir substrat oldu�unu g�stermi�tir.
Glikopironyum
In vitro metabolizma �al��malar�, hayvanlar ve insanlar aras�nda glikopironyum brom�r i�in tutarl� metabolik yollar g�stermi�tir. �e�itli mono- ve bis-hidroksillenmi� metabolitlerle sonu�lanan hidroksilasyon ve karboksilik asit t�revi (M9) olu�umuyla sonu�lanan direkt hidroliz g�r�lm��t�r. �nhale edilen glikopironyum brom�r�n yutulmu� dozu ile in vivo olarak M9 olu�mu�tur. Glikopironyumun glukuronid ve/veya s�lfat konjugatlar�, tekrarlanan inhalasyondan sonra insan idrar�nda bulunmu�tur ve verilen dozun yakla��k %3'�n� olu�turmaktad�r.
�oklu CYP izoenzimleri, glikopironyumun oksidatif biyotransformasyonuna katk�da bulunur. Glikopironyum metabolizmas�n�n inhibisyonu veya ind�klenmesi, etkin maddeye sistemik maruziyette ilgili bir de�i�ikli�e yol a�maz.
In vitro inhibisyon �al��malar�, glikopironyum brom�r�n CYP1A2, CYP2A6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 veya CYP3A4/5, MDR1, MRP2 veya MXR at�m
ta��y�c�lar�n� ve OCT1 veya OCT2 al�m ta��y�c�lar�n� inhibe etmek i�in uygun bir kapasiteye sahip olmad���n� g�stermi�tir. In vitro enzim ind�ksiyon �al��malar�, test edilen sitokrom P450 izoenzimlerinden herhangi biri veya UGT1A1 ve MDR1 ve MRP2 ta��y�c�lar� i�in glikopironyum brom�r ile klinik olarak anlaml� bir ind�ksiyon g�stermedi.
Eliminasyon
�ndakaterol
Klinik �al��malarda, idrar yoluyla de�i�meden at�lan indakaterol miktar� genellikle verilen
dozun %2,5'inden daha d���k olmu�tur. �ndakaterol�n renal klerensi ortalama olarak 0,46 ila
1,2 litre/saat aras�ndad�r. 23,3 litre/saat'lik indakaterol�n serum klerensiyle kar��la�t�r�ld���nda, renal klerensin sistemik olarak mevcut indakaterol�n ortadan kald�r�lmas�nda k���k bir rol oynad��� (sistemik klerensin yakla��k %2 ila 5'i) a��kt�r.
Bir insan ADME �al��mas�nda, oral yoldan verilen indakaterol, esas olarak de�i�memi� ana madde (dozun %54'�) ve daha az �l��de hidroksillenmi� indakaterol metabolitleri (dozun
%23'�) olarak insan d��k�s�yla at�lmaktad�r.
�ndakaterol serum konsantrasyonlar�, ortalama terminal yar� �mr� 45,5 ila 126 saat aras�nda de�i�en �ok fazl� bir �ekilde azalm��t�r. Tekrarlanan dozlamadan sonra indakaterol birikiminden hesaplanan etkili yar�lanma �mr�, yakla��k 12-15 g�nl�k g�zlemlenen zaman- kararl� durum ile tutarl� olarak 40 ila 52 saat aras�nda de�i�mi�tir.
Glikopironyum
[3H] etiketli glikopironyum brom�r�n intraven�z uygulamas�ndan sonra, 48 saat i�inde ortalama idrar yoluyla radyoaktivite at�l�m� dozun %85'ini olu�turmu�tur. Dozun %5'lik bir k�sm� da safrada bulunmu�tur.
Ana ilac�n renal eliminasyonu, sistemik olarak mevcut glikopironyumun toplam klerensinin yakla��k %60 ila 70'ini olu�tururken, b�brek d��� klerens yakla��k %30 ila 40't�r. Biliyer klerens renal olmayan klerense katk�da bulunur, ancak renal olmayan klerensin �o�unun metabolizmaya ba�l� oldu�u d���n�lmektedir.
�nhalasyonu takiben glikopironyumun ortalama renal klerensi 17,4 ila 24,4 litre/saat aral���ndayd�. Aktif t�b�ler sekresyon, glikopironyumun renal eliminasyonuna katk�da bulunur. Verilen dozun %23'�ne kadar� idrarda ana ila� olarak bulunmu�tur.
Glikopironyum plazma konsantrasyonlar� �ok fazl� bir �ekilde azald�. Ortalama terminal eliminasyon yar�lanma �mr�, inhalasyondan sonra (33-57 saat) intraven�z (6,2 saat) ve oral (2,8 saat) uygulamadan �ok daha uzundu. Eliminasyon paterni, inhalasyondan s�rekli akci�er emilimi ve/veya glikopironyumun sistemik dola��ma 24 saat sonra ve sonras�nda aktar�lmas�n� d���nd�rmektedir.
Do�rusall�k/ Do�rusal Olmayan Durum:
�ndakaterol
�ndakaterole sistemik maruziyet, dozla orant�l� bir �ekilde, artan (verilen) dozla (120 mikrogram ila 480 mikrogram) artm��t�r.
Glikopironyum
KOAH hastalar�nda, hem sistemik maruziyet hem de glikopironyumun farmakokinetik kararl� durumda toplam �riner at�l�m�, 44 ila 176 mikrogram (verilen) doz aral���nda dozla orant�l� olarak artm��t�r.
�zel pop�lasyonlar
�ndakaterol/Glikopironyum
KOAH'l� hastalarda �ndakaterol/Glikopironyumso lunduktan
sonra elde edilen verilerin
pop�lasyon farmakokinetik analizi, ya�, cinsiyet ve (ya�s�z v�cut) a��rl���n�n indakaterol ve
glikopironyumun sistemik maruziyeti �zerinde anlaml� bir etkisi olmad���n� g�stermi�tir. Ya�s�z v�cut a��rl��� (kilonun ve boyun bir fonksiyonudur) orta de�i�ken olarak tan�mlanm��t�r. Sistemik maruziyet ile ya�s�z v�cut a��rl��� (veya v�cut a��rl���) aras�nda negatif bir korelasyon g�zlenmi�tir; bununla birlikte, de�i�ikli�in b�y�kl��� veya ya�s�z v�cut a��rl���n�n tahmini hassasiyeti nedeniyle doz ayarlamas� �nerilmemi�tir.
Sigara i�me durumu ve ba�lang�� FEV'in, �ndakaterol/Glikopironyum inhalasyonundan sonra indakaterol ve glikopironyumun sistemik maruziyeti �zerinde belirgin bir etkisi olmam��t�r.
�ndakaterol
Bir pop�lasyon farmakokinetik analizi, ya��n (88 ya��na kadar yeti�kinler), cinsiyet, a��rl�k (32-168 kg) veya �rk�n indakaterol farmakokineti�i �zerinde klinik olarak anlaml� bir etkisi olmad���n� g�stermi�tir. Bu, pop�lasyondaki etnik alt gruplar aras�nda herhangi bir fark ortaya ��kmam��t�r.
Glikopironyum
KOAH'l� hastalardaki verilerin pop�lasyon farmakokinetik analizi, v�cut a��rl���n� ve ya��, sistemik maruziyette hastalar aras� de�i�kenli�e katk�da bulunan fakt�rler olarak tan�mlam��t�r. �nerilen dozda glikopironyum t�m ya� ve v�cut a��rl��� gruplar�nda g�venle kullan�labilir.
Cinsiyet, sigara i�me durumu ve ba�lang�� FEV'in sistemik maruziyet �zerinde belirgin bir etkisi olmam��t�r.
Karaci�er yetmezli�i olan hastalar �ndakaterol/Glikopironyum :
Monoterapi bile�enlerinin klinik farmakokinetik �zelliklerine dayanarak, �ndakaterol/Glikopironyum hafif ve orta �iddette karaci�er yetmezli�i olan hastalarda �nerilen dozda kullan�labilir. �iddetli karaci�er yetmezli�i olan hastalar i�in mevcut veri bulunmamaktad�r.
�ndakaterol:
Hafif ve orta �iddette karaci�er yetmezli�i olan hastalar, indakaterol�n Cveya EAA's�nda anlaml� bir de�i�iklik g�stermemi�tir veya protein ba�lanmas�, hafif ve orta �iddette karaci�er yetmezli�i olan denekler ile bunlar�n sa�l�kl� kontrolleri aras�nda farkl�l�k g�stermemi�tir. �iddetli karaci�er yetmezli�i olan ki�ilerde �al��ma yap�lmam��t�r.
Glikopironyum:
Karaci�er yetmezli�i olan hastalarda klinik �al��malar yap�lmam��t�r. Glikopironyum a��rl�kl� olarak renal at�l�m ile sistemik dola��mdan temizlenir. Glikopironyumun hepatik metabolizmas�n�n bozulmas�n�n, klinik olarak anlaml� bir sistemik maruziyet art��� ile sonu�land��� d���n�lmemektedir.
B�brek yetmezli�i olan hastalar �ndakaterol/Glikopironyum:
Monoterapi bile�enlerinin klinik farmakokinetik �zelliklerine dayanarak, �ndakaterol/Glikopironyum hafif ila orta derecede b�brek yetmezli�i olan hastalarda �nerilen dozda kullan�labilir. �iddetli b�brek yetmezli�i veya diyaliz gerektiren son d�nem b�brek yetmezli�i olan hastalarda,�ndakaterol/Glikopironyumsadece beklenen fayda potansiyel
riskten �nemli ise kullan�lmal�d�r.
�ndakaterol:
�drar yolunun indakaterol maleat�n toplam v�cut eliminasyonuna �ok d���k katk�s� nedeniyle, b�brek yetmezli�i olan hastalarda bir �al��ma yap�lmam��t�r.
Glikopironyum:
B�brek yetmezli�inin sistemik glikopironyum brom�r maruziyeti �zerinde etkisi vard�r. Hafif ve orta derecede b�brek yetmezli�i olanlarda toplam sistemik maruziyet (EAA) orta dereceli ortalama 1,4 kata kadar, �iddetli b�brek yetmezli�i ve son d�nem b�brek yetmezli�i olanlarda ise 2,2 kata kadar artm��t�r. Hafif ve orta derecede b�brek yetmezli�i olan KOAH hastalar�nda (tahmini glomer�ler filtrasyon h�z�, eGFR ≥30 ml/dak/1,73 m2) glikopironyum brom�r �nerilen dozda kullan�labilir.
Etnik k�ken
�ndakaterol/Glikopironyum:
Japon ve Kafkas denekler aras�nda her iki bile�ik i�in toplam sistemik maruziyette (EAA) �nemli bir fark yoktur. Di�er etnik k�kenler veya �rklar i�in mevcut farmakokinetik veriler yetersizdir.
�ndakaterol:
Etnik alt gruplar aras�nda fark tespit edilmemi�tir. Siyah pop�lasyon i�in s�n�rl� tedavi deneyimi mevcuttur.
Glikopironyum:
Japon ve Kafkas denekler aras�nda toplam sistemik maruziyet (EAA) aras�nda b�y�k fark yoktur. Di�er etnik k�kenler veya �rklar i�in mevcut farmakokinetik veriler yetersizdir.
5.3. Klinik �ncesi g�venlilik verileri
Dozu ger�ekten al�p almad���m� nas�l bilece�im?
�nhalasyon cihaz�n�z�n i�erisinden nefes ald���n�zda bir v�z�ldama sesi duyacaks�n�z.
A�z�n�zda laktozdan kaynaklanan '�eker tad�' hissedeceksiniz. Bo�az�n�z�n arka k�sm�nda toz hissedebilirsiniz. Bu normaldir.
Doz al�nd���nda kaps�l bo�alm�� olacakt�r.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Laktoz monohidrat (inek s�t� kaynakl�d�r)
6.2. Ge�imsizlikler
Ge�erli de�ildir.
6.3. Raf �mr�
24 ay
Her paketteki inhaler, bu paketteki t�m kaps�ller kullan�ld�ktan sonra at�lmal�d�r.
6.4. Saklamaya y�nelik �zel tedbirler
25 °Calt�nda oda s�cakl���nda saklay�n�z.
Kaps�ller, nemden korumak i�in daima orijinal ambalaj�nda saklanmal� ve sadece kullan�mdan hemen �nce ��kar�lmal�d�r.
6.5. Ambalaj�n niteli�i ve i�eri�i
Kutuda, GL�N�UM PLUS �nhalasyon Tozu Sert Kaps�l desikant kapakl� HDPE �i�e 30 kaps�l
+ 1 adet inhalasyon cihaz�.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller, “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj ve Ambalaj At�klar�n�n Kontrol� Y�netmeli�i” ne uygun olarak imha edilmelidir.
GL�N�UM PLUS uygulamas� esnas�nda a�a��daki talimatlara uyulmal�d�r:
Kaps�lleri yutmay�n�z. Kaps�ller yaln�zca kutunun i�erisinde yer alan inhalasyon cihaz� ile birlikte kullan�lmal�d�r. Bu cihaz, �zel olarak GL�N�UM PLUS kaps�lleri ile birlikte kullan�lmak �zere tasarlanm��t�r.
Kaps�llerin i�erisindeki toz yaln�zca teneff�s edilerek (nefes yoluyla) kullan�lacakt�r.
Kaps�lleri kullanmadan hemen �nce paketinden ��kar�n�z. kaps�llerin �slanmamas� i�in parmaklar�n�z�n kuru oldu�undan emin olunuz.
�lac�n�z� kulland�ktan sonra a�z�n�z� su ile iyice �alkalay�n�z ve �alkalad�ktan sonra a�z�n�zdaki suyu t�k�r�n�z. Bunu yapmak, a�z�n�zda mantar enfeksiyonu (pamuk�uk) geli�mesi riskini azalt�r.
Kaps�lleri inhalasyon cihaz� d���nda ba�ka bir cihaz ile kullanmay�n�z.
GL�N�UM PLUS'� her g�n ayn� saatlerde kullanman�z ilac�n�z� ne zaman kullanaca��n�z� hat�rlaman�za yard�mc� olacakt�r.
GL�N�UM PLUS'� doktorunuzun talimat�na g�re, d�zenli olarak kullanman�z �nemlidir. Ast�m belirtileriniz olmasa bile GL�N�UM PLUS'� kullanmaya devam etmelisiniz ��nk� bu ast�m n�betlerinin olu�mamas�na yard�mc� olur.
E�er ne kadar s�re GL�N�UM PLUS kullanaca��n�z hakk�nda sorular�n�z varsa, doktorunuza ya da eczac�n�za dan���n�z.
Hastalar�n jelatin kaps�l�n par�alanabilece�ini ve k���k jelatin par�alar�n�n inhalasyondan sonra a��z veya bo�az b�lgesine ula�abilece�ini bilmesi �nemlidir.
Hastaya jelatinin zarars�z oldu�u, a��zda yumu�ayaca�� ve yutulabildi�i s�ylenmelidir. Kaps�l� bir defadan fazla delmemek suretiyle par�alanma olas�l��� asgari d�zeye indirilebilir.
|
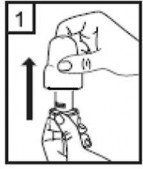
1-Kapa�� �ekip ��kar�n�z. |
|
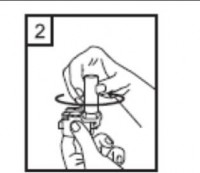
2-Kaps�l b�lmesini a��n�z.
�nhalerin taban�n� s�k�ca tutup, a�mak i�in a��zl��� �zerinde yer alan ok i�areti y�n�nde d�nd�r�n�z. |
|
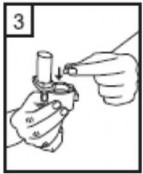
3-Parmaklar�n�z�n tamamen kuru oldu�undan emin olunuz. Ambalaj�ndan bir kaps�l ��kar�n�z ve bu kaps�l� cihaz�n taban�ndaki kaps�l b�lmesine yat�k olarak yerle�tiriniz. Kaps�lleri, kullan�mdan hemen �nce ambalaj�ndan ��karman�z �nemlidir.
�NEML�: Kaps�l� a��zl���n i�erisine yerle�tirmeyiniz! |
|
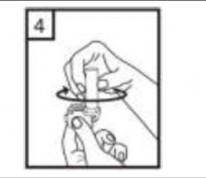
4-A��zl��� “klik” sesi duyana kadar geri �evirerek kapal� duruma getiriniz. |
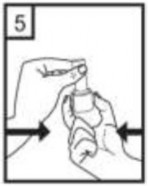
| 5-Tozu kaps�lden serbestlemek i�in: Not: Kaps�l bu a�amada par�alanabilir ve k���k jelatin par�ac�klar� a�z�n�za ya da bo�az�n�za gelebilir. Fakat jelatin yenebilir nitelikte oldu�u i�in zararl� de�ildir. |
|
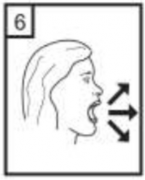
6-Nefesinizi olabildi�ince d��ar�ya veriniz. |
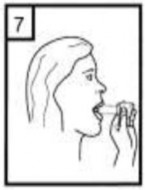
| 7-�lac� derin bir �ekilde hava yollar�n�za �ekmek i�in: Not: Kaps�l�n, kaps�l b�lmesinin �zerindeki alanda d�nmesine ba�l� olarak bir v�z�ldama sesi duymal�s�n�z. E�er bu v�z�ldama sesini duymazsan�z, kaps�l b�lmesini a��n�z ve kaps�l�n, kaps�l b�lmesinde s�k���p s�k��mad���n� kontrol ediniz. Daha sonra 7. basama�� tekrarlay�n�z. Kaps�l� s�k��t��� yerden kurtarmak i�in d��melere tekrar BASMAYINIZ. |
8- Cihaz�n i�erisinden nefes ald�ktan sonra, nefesinizi olabildi�ince tutunuz ve cihaz� a�z�n�zdan ��kar�n�z. Sonra burnunuzdan nefes veriniz. Kaps�l b�lmesini a��n�z ve kaps�lde toz kal�p kalmad���n� kontrol ediniz. E�er kalm�� ise 6, 7 ve 8 no' lu i�lemleri tekrarlay�n�z. | |
��kar�n�z. doktorunuzun �nerisi do�rultusunda ayn� i�lemleri di�er kaps�ller i�in de | |
Cihaz� a��zl�k yukar� do�ru bakacak �ekilde dik olarak tutunuz.
Kenarlardaki iki kulak���a (d��melere) ayn� anda ve sadece bir kez s�k�ca basarak kaps�l� deliniz.
A��zl��� a�z�n�za yerle�tiriniz ve ba��n�z� hafif�e geriye do�ru e�iniz.
Dudaklar�n�zla a��zl���n etraf�n� s�k�ca sar�n�z.
H�zl�, duraksamadan ve alabildi�iniz kadar derin bir nefes al�n�z.
10- ��eride kalan tozlar� temizlemek i�in kuru bir ka��t mendil ya da f�r�a kullan�n�z. Not: �nhalasyon cihaz�n� temizlemek i�in SU KULLANMAYINIZ.
�nce a��zl���, ard�ndan kapa�� kapat�n�z.
tekrarlay�n�z.
�lac�n�z� kulland�ktan sonra a�z�n�z� su ile iyice �alkalay�n�z ve �alkalad�ktan sonra a�z�n�zdaki suyu t�k�r�n�z. Bunu yapmak, a�z�n�zda mantar enfeksiyonu (pamuk�uk) geli�mesi riskini azalt�r.
Uygulamaya ili�kin sorular ve cevaplar�
Kaps�llerin k���k par�a��klara ayr�lmas�n� nas�l �nlerim?
Cihaz�n yan�ndaki k�rm�z� kulak��kl�klara (d��melere) bast���n�zda (5.basamak), kaps�ller k�r�labilir ve nefes al�rken a�z�n�za ya da bo�az�n�za k���k par�alar ka�abilir. Bunu a�a��dakileri uygulayarak �nleyebilirsiniz:
K�rm�z� kulakc�klara (d��melere) yaln�zca bir kere basarak.
Kaps�lleri kullanmadan �nce orjinal ambalaj�nda tutarak.
Kaps�lleri 25 oC'nin alt�ndaki oda s�cakl���nda saklayarak.
Kaps�lleri nemden koruyarak.
�nhalasyon cihaz�n�n i�erisindeki tozu nas�l temizlerim?
Kuru bir k�t mendil ya da yumu�ak bir f�r�a kullan�n�z.
�nhalasyon cihaz�n� asla y�kamaman�z gerekti�ini unutmamal�s�n�z.
 Y�ksek Tansiyon
Hipertansiyon s�rekli anormal derecede y�ksek olan kan bas�nc�d�r. Tansiyon
atardamarlar�n�zdaki kan�n bas�nc�d�r.
Y�ksek Tansiyon
Hipertansiyon s�rekli anormal derecede y�ksek olan kan bas�nc�d�r. Tansiyon
atardamarlar�n�zdaki kan�n bas�nc�d�r. |
 Omurilik zedelenmeleri
Omurilik zedelenmesini takip eden birka� g�n i�inde, hi�kimse hasarin ne kadar olacagini tahmin edemez. Buradaki sorun, omuriligin herhangi bir zedelenmesinden hemen sonra, bir omurilik sokunun olusmasidir.
Omurilik zedelenmeleri
Omurilik zedelenmesini takip eden birka� g�n i�inde, hi�kimse hasarin ne kadar olacagini tahmin edemez. Buradaki sorun, omuriligin herhangi bir zedelenmesinden hemen sonra, bir omurilik sokunun olusmasidir. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| COSEBLAR | 8699525558992 | 689.10TL |
| GLINIUM | 8681428551514 | 689.10TL |
| INKARANTO | 8681428551484 | |
| Di�er E�de�er �la�lar |
 |
S�rt A�r�s� S�rt a�r�s� birden bire ortaya ��k�p �iddetli (akut) olabilir veya zamanla geli�ip daha uzun s�reli sorunlara (kronik) neden olabilir. |
 |
�izofrenlik �izofrenli�in psikiatrik te�hisi hakk�nda �ok fazla anla�mazl�k vard�r. Bu sayfadaki bilgiler, �izofrenli�in te�hisi, nedenleri ve tedavisi hakk�ndaki fakl� teoriler hakk�nda bilgi verecektir. |
 |
Grip, So�uk Alg�nl��� ve �ks�r�k Grip ve so�uk alg�nl��� (nezle) semptomlar� aras�ndaki fark� bilmek �nemlidir. So�uk alg�nl��� gripten daha hafif belirtiler g�steren bir solunum yolu hastal���d�r. |
�LA� GENEL B�LG�LER�
Sandoz �la� San. ve Tic. A.�.
| Sat�� Fiyat� | 689.1 TL [ 17 Dec 2024 ] |
| �nceki Sat�� Fiyat� | 689.1 TL [ 2 Dec 2024 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8681428551514 |
| Etkin Madde | Indakaterol Maleat + Glikopironyum Bromur |
| ATC Kodu | R03AL04 |
| Birim Miktar | 85+43 |
| Birim Cinsi | MCG |
| Ambalaj Miktar� | 30 |
| Solunum Sistemi > Adrenerjikler (�nhalan) |
| Yerli ve Be�eri bir ila�d�r. |