HAEMATE-P FAKTOR VIII 500 IU 1 flakon Saklanması
{ Insan Koagulasyon Faktoru VIII }
Kan ve Kan Yapıcı Organlar > K Vitamini ve Diğer Hemostatikler > Anti hemofilik faktor viii Farma-Tek İlaç Sanayi ve Ticaret A.Ş. | Güncelleme : 30 December 18995.HAEMATE-P FAKTOR VIII'in saklanması
HAEMATE P' i çocukların göremeyeceği, erişemeyeceği yerlerde ve ambalajında saklayınız.
HAEMATE P'yi, 25 °C' nin altındaki oda sıcaklığında saklayınız. Dondurmayınız. Donmuş ürünü çözüp kullanmayınız.
Son kullanma tarihiyle uyumlu olarak kullanınız
Ambalajdaki son kullanma tarihinden sonra HAEMATE-P FAKTOR VIII'i kullanmayınız.
• Eğer üründe ve/ veya ambalajında bozukluklar fark ederseniz HAEMATE P' yi kullanmayınız.
• Sulandırıldıktan sonra derhal kullanılmalıdır. Sulandırılan çözelti, sterilitesi sağlandığı takdirde, 8 saat içinde uygulanabilir.
Çevreyi korumak amacıyla kullanmadığınız HAEMATE P' yi şehir suyuna veya çöpe atmayınız Bu konuda eczacınıza danışınız.
Ruhsat sahibi:
Farma-Tek İlaç San. ve Tic. Ltd. Şti. Şerifali Mah. Bayraktar Bulvarı. Beyan Sok. No:12 Ümraniye/İstanbul
Üretim yeri: CSL Behring GmbH Emil-von-Behring-StraPe 76, 35041 Marburg -Almanya
AŞAĞIDAKİ BİLGİLER BU İLACI UYGULAYACAK SAĞLIK PERSONELİ İÇİNDİR. Genel talimatlar:
Çözelti berrak veya hafif opak olmalıdır. Filtre edildikten/çekildikten sonra (aşağıya bakınız) hazırlanmış ürün uygulanma öncesi çökelti maddesi veya renk bozulmasına karşı göz ile incelenmelidir. Artık içeren (kalıntı/parçacık) veya berrak olmayan çözeltileri kullanmayınız. Mix2Vial setini içeren filtreler artık içeren kalıntı ya da parçacıkları tamamiyle söker. Filtrasyon dozaj hesaplarım etkilemez. Solüsyonu, filtrasyondan sonra da toz parçacıkları yada partiküller içeriyorsa kullanmayınız.
Hazırlanma ve enjektöre çekilme aseptik şartlarda gerçekleştirilmelidir.
Uygulama sonrası kullanılmayan ürün veya atık madde, yerel gerekliliklere uygun şekilde bertaraf edilmelidir.
Hazırlanması:
Çözücüyü oda sıcaklığına getiriniz. Toz ve çözücü flakonlarının kapaklarının çıkarıldığından ve stoperlerin aseptik bir solüsyonla silinerek Mix2Vial paketinin açılmasından önce kendiliğinden kuruduğundan emin olunuz.
1.Kapağı soyarak Mix2Vial paketini açınız. Mix2Vial' i blister paketinden çıkarmayınız,
l
2
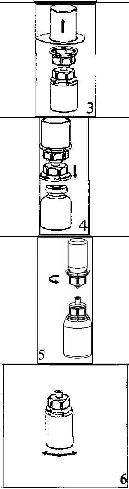
2. Çözücü flakonu düz ve temiz bir yüzey üzerine yerleştiriniz ve flakonu sıkıca tutunuz. Blister paketi ile birlikte aldığınız Mix2Vial setinin mavi adeptör ucunun tepe noktasını çözücü flakonun stoperinin üzerine doğru itiniz.
3. Kenarından tutarak ve dikey şekilde yukarıya doğru çekerek, blister paketini Mix2Vial setinden dikkatlice çıkarınız. Sadece blister paketini çekerek çıkardığınızdan ve Mix2Vial setini çıkarmadığınızdan emin olun.
4. Toz flakonunu düz ve sağlam bir zemin üzerine yerleştiriniz. Çözücü flakonunu takılı olan Mix2Vial setiyle birlikte ters çevirin ve saydam adaptör ucunun tepe noktasını, toz flakonun stoperinden aşağıya doğru bastırınız. Çözücü otomatik olarak toz flakonunun içine akacaktır.
5. Bir elinizle Mix2Vial setinin ürün tarafını, diğer elinizle de çözücü tarafını tutunuz ve ürünün çözülmesi sırasında aşırı köpük oluşmasını önlemek için seti dikkatli bir şekilde iki parçaya ayırınız. Çözücü flakonunu mavi Mix2Vial adaptörü takılı şekilde atınız.
6. Tozun tamamen çözündüğünden emin oluncaya kadar ürün flakonunu saydam adaptör takılı şekilde hafifçe sağa sola çeviriniz. Çalkalamayınız.
7. Boş, steril bir şırıngaya hava çekiniz. Ürün flakonu yukarıya doğru iken, şırıngayı Mix2Vial'ın Luer Lock bağlantı parçasına bağlayınız. Ürün flakonuna hava enjekte ediniz.
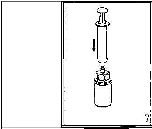
8. Şırınganın pistonunu basılı tutarak sistemi baş aşağı çeviriniz ve konsantreyi, pistonu yavaşça geriye çekerek şırıngaya alınız.
9. Çözelti şırıngaya aktarıldıktan sonra, şırınganın gövdesini sıkıca tutunuz (şırınganın sapını aşağıya bakacak şekilde tutarak) ve saydam Mix2Vial adaptörünü şırıngadan ayırınız.
Çözeltiyi hemen yavaş intravenöz enjeksiyonla veya infüzyonla uygulayınız Ve ürün dolu şırangaya kanın girmediğinden emin olunuz.
Uygulama şekli:
Ürünü hazırlandığında uygulamadan önceki sıcaklığı oda yada vücut sıcaklığında olmalıdır. Hastanın rahat edebileceği bir yerde intravenöz yolla yavaş bir şekilde uygulanır. Ürün şırınga içine çekilir çekilmez hemen kullanılmalıdır.
Büyük miktarda faktör uygulanması gerekli olan durumlarda bu uygulama infüzyon olarak yapılabilir. Bunun için kullanıma hazır ürün uygun bir infüzyon sisteme transfer edilir.
Enjeksiyon ya da infüzyon dakikada 4 mL'yi geçmemelidir. Ani değişmeler için hasta gözlenmelidir. Eğer HAEMATE P kullanımı ile ilgili herhangi bir değişiklik meydana gelirse infüzyon oranı düşürülebilir ya da uygulama kesilebilir ve hastanın klinik koşulları belirlenmelidir.(Ayrıca bakınız Bölüm 4.4.)
 Hastalık ilk kez 1817 de İngiliz doktor James Parkinson tarafından tanımlanmış ve Dr. Parkinson hastalığı “sallayıcı felç” olarak kaleme almış.
Hastalık ilk kez 1817 de İngiliz doktor James Parkinson tarafından tanımlanmış ve Dr. Parkinson hastalığı “sallayıcı felç” olarak kaleme almış.
 Diyabet, insülin hormonu ile ilgili problemlerden kaynaklanan bir hastalıktır.
Diyabet, insülin hormonu ile ilgili problemlerden kaynaklanan bir hastalıktır.
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| BERIATE-P | 8699738980467 | |
| ESPEROCT | 8699676791200 | 18,725.38TL |
| FACTOR | 8699743980025 | |
| FAKTOR | 8697507980144 | 5,466.74TL |
| HAEMATE-P | 8699738980207 | |
| IMMUNATE | 8699556980144 | 7,692.28TL |
| JIVI | 8699546790135 | 12,528.63TL |
| OCTANATE | 8699686980120 | 9,512.28TL |
| REFACTO | 8699572270113 | |
| Diğer Eşdeğer İlaçlar |
 Şizofrenliğin psikiatrik teşhisi hakkında çok fazla anlaşmazlık vardır. Bu
sayfadaki bilgiler, şizofrenliğin teşhisi, nedenleri ve tedavisi hakkındaki faklı teoriler
hakkında bilgi verecektir.
Şizofrenliğin psikiatrik teşhisi hakkında çok fazla anlaşmazlık vardır. Bu
sayfadaki bilgiler, şizofrenliğin teşhisi, nedenleri ve tedavisi hakkındaki faklı teoriler
hakkında bilgi verecektir.
 Kalbe giden kan akışı durduğunda kalp krizi meydana gelir.
Kalbe giden kan akışı durduğunda kalp krizi meydana gelir.
 HIV, Human Immunodeficiency Virus’dür (İnsanlarda Bağışıklık Sistemini Bozan
Virüsdür). Bu virüs AIDS hastalığına sebep olur.
HIV, Human Immunodeficiency Virus’dür (İnsanlarda Bağışıklık Sistemini Bozan
Virüsdür). Bu virüs AIDS hastalığına sebep olur.
İLAÇ GENEL BİLGİLERİ
Farma-Tek İlaç Sanayi ve Ticaret A.Ş.
| Geri Ödeme Kodu | A03511 |
| Satış Fiyatı | TL |
| Önceki Satış Fiyatı | |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Turuncu Reçeteli bir ilaçdır. |
| Barkodu | 8699738980153 |
| Etkin Madde | Insan Koagulasyon Faktoru VIII |
| ATC Kodu | B02BD06 |
| Birim Miktar | 500 |
| Birim Cinsi | IU |
| Ambalaj Miktarı | 1 |
| Kan ve Kan Yapıcı Organlar > K Vitamini ve Diğer Hemostatikler > Anti hemofilik faktor viii |
| İthal ( ref. ülke : Ispanya ) ve Beşeri bir ilaçdır. |