HIZENTRA 4 G/20 ml S.C. UYGULAMA için enjeksiyonluk çözelti (1 flakon) Kısa Ürün Bilgisi
{ Human Immunoglobulin }
1. BEŞERİ TIBBİ ÜRÜNÜN ADI
HİZENTRA 4 g/20 mL S.C. uygulama için enjeksiyonluk çözelti Steril
2. KALİTATİF VE KANTİTATİF BİLEŞİM
Etkin madde
Subkutan enjeksiyon için insan normal immünoglobulini (SCIg)
Her 1 mL çözelti: 200 mg insan normal immünoglobulini (en az % 98 saflıkta IgG)
IgG | % 69 |
IgG | % 26 |
IgG | % 3 |
IgG | % 2 |
Her 20 mL çözelti: 4 g insan normal immünoglobulini IgG alt sınıflarının yaklaşık dağılımı aşağıdaki gibidir:
Maksimum IgA içeriği 50 mikrogram/mL'dir. İnsan donörlerinin plazmasından üretilir.
Yardımcı maddeler
L-prolin Yaklaşık 250 mmol/L (aralık: 210 – 290)
Sodyum (pH ayarlama için) <10 mmol/L Yardımcı maddeler için bölüm 6.1'e bakınız.
3. FARMASÖTİK FORMU
Deri altına uygulama için enjeksiyonluk çözelti. Çözelti berrak ve açık sarı veya açık kahverengidir.
HİZENTRA yaklaşık 380 mOsmol/kg'lık bir osmolaliteye sahiptir.
4. KLİNİK ÖZELLİKLER
4.1. Terapötik endikasyonlar
Yetişkin, çocuklar ve adolesanlarda (0-18 yaş) replasman tedavisi: HİZENTRA aşağıdaki durumlarda endikedir:
Bozuk antikor üretimi olan primer immün yetmezlik sendromları (bkz. Bölüm 4.4.).
Şiddetli veya tekrarlayan enfeksiyonları, etkisiz antimikrobiyal tedavi ve kanıtlanmış spesifik antikor yetmezliği (PSAF)* veya < 4 g/L serum IgG seviyeleri olan hastalarda sekonder immün yetmezlikler (SID).
*PSAF = pnömokokal polisakkarit ve polipeptit antijen aşılarına karşı IgG antikor titresinde en az 2 kat artış sağlanamaması.
Yetişkinler, çocuklar ve adolesanlarda (0 – 18 yaş) immünomodülatör tedavisi:
HİZENTRA, kronik inflamatuvar demiyelinizan polinöropatisi (KİDP) olan hastalarda, intravenöz immünoglobulin (IVIg) ile stabilizasyondan sonra idame tedavisi olarak endikedir.
4.2. Pozoloji ve uygulama şekli
Doz ve doz rejimi endikasyona bağlıdır.
Tedavi, SCIg ile immün yetmezlik/KİDP tedavisinde tecrübeli bir hekim gözetiminde başlatılmalı ve takip edilmelidir.
Pozoloji/uygulama sıklığı ve süresi:
Yetişkinler ve çocuklar (0 – 18 yaş)
Replasman tedavisi
Tıbbi ürün subkutan yolla uygulanmalıdır.
Replasman tedavisinde; dozun, her bir hasta için klinik yanıt ve serum IgG dip seviyelerine bağlı olarak bireyselleştirilmesi gerekebilir. Aşağıdaki doz rejimleri rehber olarak verilmektedir:
Doz rejimi, en az 6 g/L veya popülasyon yaşı için normal referans aralığı dahilinde bir dip IgG seviyesine (bir sonraki infüzyondan önce ölçülür) ulaşmalıdır. En az 0,2-0,5 g/kg (1,0- 2,5 mL/kg) vücut ağırlığı yükleme dozu gerekebilir. Bu dozun birkaç güne bölünmesi gerekebilir. Kararlı hal IgG seviyelerine ulaşıldıktan sonra, idame dozları kümülatif aylık dozun 0,4-0,8 g/kg (2,0-4,0 mL/kg) vücut ağırlığına ulaşması için tekrarlı aralıklarla uygulanır. Her bir tekli dozun farklı anatomik bölgelere enjekte edilmesi gerekebilir.
Dip seviyeleri ölçülmeli ve hastanın klinik yanıtıyla bağlantılı olarak değerlendirilmelidir. Klinik yanıta bağlı olarak (örn. enfeksiyon hızı), daha yüksek dip seviyelerini elde etmek amacıyla doz ve/veya doz aralığının ayarlanması değerlendirilebilir.
KİDP hastalarında immünomodülatör tedavi
HİZENTRA ile tedavi en son IVIg infüzyonundan 1 hafta sonra başlatılır. Tavsiye edilen subkutan doz, haftada bir ardışık 1 veya 2 gün boyunca, 1 veya 2 seansta uygulanan 0,2 – 0,4 g/kg vücut ağırlığıdır. Başlangıç subkutan dozu, önceki IVIg dozundan (haftalık doz olarak hesaplanır) 1:1 oranında bir dönüşüm olabilir.
Örneğin üç haftada bir uygulanan 1 g/kg IVIg dozu haftalık 0,33 g/kg HİZENTRA dozuna dönüştürülebilir. Haftalık doz daha küçük dozlara bölünebilir ve her haftada istenilen sayıda uygulanabilir. İki haftada bir dozlama için, haftalık HİZENTRA dozu iki katına çıkarılır.
İstenilen klinik yanıtı elde etmek için dozun ayarlanması gerekebilir. Hastanın bireysel klinik yanıtı doz ayarlamasında primer değerlendirme olmalıdır. Klinik kötüleşme durumunda, doz tavsiye edilen maksimum haftalık doz olan 0,4 g/kg'a çıkarılabilir.
KİDP idame tedavisinde HİZENTRA 18 aydan daha uzun periyodlar için çalışılmamıştır. 18 aydan uzun herhangi bir tedavi süresi hastanın yanıtına göre ve devam tedavisi ihtiyacına göre bireyselleştirilir.
HİZENTRA'nın etkililiği intravenöz immünoglobulinlerden değiştirildikten sonra plaseboya karşı kanıtlanmıştır. HİZENTRA'nın IVIg 'ye karşı doğrudan karşılaştırma verisi mevcut değildir. Bölüm 5.1'e bakınız.
Uygulama şekli:
HİZENTRA yalnızca subkutan olarak uygulanmalıdır.
Evde tedavi:
Evde subkutan infüzyon tedavisi, evde tedavi için hastalara rehberlik konusunda tecrübeli bir sağlık uzmanı tarafından başlatılmalı ve takip edilmelidir. Sağlık uzmanı, hastanın bireysel tıbbi durumuna ve tercihlerine göre uygun infüzyon yöntemini (cihaz destekli veya manuel manuel yoldan iterek infüzyon) seçmelidir. İmmünglobulinlerin subkutan uygulaması için uygun infüzyon cihazları kullanılabilir. Hasta veya hasta bakıcısı infüzyon cihazlarının kullanımı, tedavi günlüğü tutulması ve şiddetli advers reaksiyonları tanıma ve böyle reaksiyonlar oluştuğunda alınacak önlemler konusunda bilgilendirilmeli ve eğitilmelidir.
HİZENTRA karın, uyluk, üst kol ve lateral kalça gibi bölgelere enjekte edilebilir.
Birden fazla infüzyon cihazı eş zamanlı kullanılabilir. Belirli bir bölgeye infüze edilen ürün miktarı değişebilir. Yenidoğanlarda ve çocuklarda infüzyon bölgesi her 5-15 mL'de değiştirilebilir. Yetişkinlerde doz 50 mL/bölgeye kadar uygulanabilir. İnfüzyon bölgesi sayısına ilişkin herhangi bir sınırlama yoktur. İnfüzyon bölgeleri en az 5 cm aralıklı olmalıdır.
İnfüzyon hızı
HİZENTRA infüzyonu aşağıdakiler kullanılarak yapılabilir:
İnfüzyon cihazı, veya
Enjektörle manuel yoldan iterek.
4.3. Kontrendikasyonlar
HİZENTRA;
Etkin madde
Hiperprolinemi tip I ve II'si olan hastalarda
kontrendikedir.
HİZENTRA intravasküler olarak uygulanmamalıdır.

4.4. Özel kullanım uyarıları ve önlemleri
Virüs güvenliğiHİZENTRA, insan plazmasından elde edilmektedir. İnsan plazmasından elde edilen ilaçlar, virüsler ve teorik olarak Varyant Creutzfeldt-Jacob (v-CJD) gibi, çeşitli hastalıklara yol açabilen enfeksiyon yapıcı ajanlar içerebilirler. HİZENTRA'da Varyant Creutzfeldt-Jacob hastalığının bulaşma riski teorik olarak minimumken, klasik Creutzfeldt-Jacob hastalığının bulaşma riski hiçbir kanıtla desteklenmez. Alınan önlemlere rağmen, bu tür ürünler halen potansiyel olarak hastalık bulaştırabilir.
Bu tip ürünlerin enfeksiyon yapıcı ajanları bulaştırma riski, plazma verenlerin belirli virüslere önceden maruz kalıp kalmadığının izlenmesi, belirli virüs enfeksiyonlarının halihazırda varlığının test edilmesi ve belirli virüslerin yok edilmesi ve/veya inaktivasyonu ile azaltılmıştır. Bütün bu önlemlere rağmen, bu ürünler hala potansiyel olarak hastalık bulaştırabilirler. Ayrıca, henüz bilinmeyen enfeksiyon yapıcı ajanların bu ürünlerin içerisinde bulunma ihtimali mevcuttur.
HIV, HBV, HCV gibi zarflı virüsler ve HAV gibi zarflı olmayan virüsler için etkili önlemlerin alınmasına dikkat edilmelidir. Parvovirüs B19 gibi zarflı olmayan virüslere karşı alınan tedbirler sınırlı sayıda olabilir. Parvovirüs B19 enfeksiyonu, gebelikte (fetal infeksiyon) ve immün yetmezlik ya da kırmızı kan hücre üretiminde artış olan hastalarda tehlikeli olabilir (hemolitik anemi gibi).
Doktor, bu ilacı hastaya reçete etmeden veya uygulamadan önce hastası ile risk ve yararlarını tartışmalıdır.
Ayrıca;
HİZENTRA kullanılması gerekiyorsa hekim tarafından, hastalık yapıcı etkenlerin hastaya bulaşmasını önlemek için uygun aşıların (Hepatit A, Hepatit B vb.) yaptırılması önerilebilir.
İzlenebilirlik
Biyolojik tıbbi ürünlerin izlenebilirliğini iyileştirmek için uygulanan ürünün adı ve seri
numarasının açıkça kaydedilmesi gerekir.
HİZENTRA yalnızca subkutan kullanım içindir. HİZENTRA intravasküler olarak verilmemelidir. HİZENTRA yanlışlıkla kan damarına uygulanırsa, hastada şok gelişebilir.
Bölüm 4.2 altında tavsiye edilen infüzyon hızına uyulmalıdır. Hastalar infüzyon periyodu boyunca herhangi bir advers olay açısından yakından takip edilmeli ve dikkatli gözlenmelidir.
Bazı advers reaksiyonlar ilk defa insan normal immünoglobulini alan hastalarda veya nadir durumlarda insan normal immünoglobulin ürünü değiştirildiğinde veya tedavi sekiz haftadan uzun süre durdurulduğunda daha sık meydana gelebilir.
Potansiyel komplikasyonlar aşağıdaki koşullara sahip hastaların sağlanması ile sıklıkla önlenebilir:
Başlangıçta yavaşça enjekte edilen insan normal immünoglobulini ürününe duyarlı olmayan hastalar (bkz. bölüm 4.2.).
4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri
Canlılığı azaltılmış virüs aşıları
İmmünoglobulin uygulaması kızamık, kızamıkçık, kabakulak ve suçiçeği gibi canlılığı azaltılmış virüs aşılarının etkililiğini en az 6 haftadan 3 aya kadar azaltabilir. Bu tıbbi ürünü uyguladıktan sonra, canlılığı azaltılmış virüs aşıları ile aşılamadan önce en az 3 aylık bir zaman geçmelidir. Kızamık durumunda, bu etkisizleşme 1 yıla kadar sürebilir. Bu nedenle, kızamık aşısı olan hastaların antikor durumu kontrol edilmelidir.
Özel popülasyonlara ilişkin ek bilgiler Pediyatrik popülasyon:
Pediyatrik popülasyonda aynı etkileşimler meydana gelebilir.
Geriyatrik popülasyon:
Geriyatrik popülasyonda aynı etkileşimler meydana gelebilir.
4.6. Gebelik ve laktasyon
Genel tavsiye
Gebelik kategorisi: C
Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon) HİZENTRA'da bulunan IgG molekülleri insan dolaşımındaki fizyolojik IgG'ye kıyasla değişmemiştir. IgG ile klinik deneyime dayanarak, çocuk doğurma potansiyeline (kadın doğurganlığına) zararlı etkiler beklenmemektedir.
Gebelik dönemi
İnsan normal immünoglobulinlerinin gebe kadınlarda kullanımına ilişkin prospektif klinik çalışmalardan elde edilen veriler sınırlıdır. Bu nedenle, HİZENTRA gebe kadınlara yalnızca dikkatli bir şekilde verilmelidir. İmmünoglobulinlerle klinik deneyim gebelik süreci veya fetüs veya yenidoğan üzerinde zararlı etki beklenmediğini öne sürmektedir.
Gebe kadınların tedavisine devam edilmesi yenidoğan için pasif bir bağışıklık sağlar.
Hayvanlar üzerinde yapılan çalışmalar, gebelik /ve-veya/ embriyonal/fetal gelişim /ve-veya/ doğum /ve-veya/ doğum sonrası gelişim üzerindeki etkiler bakımından yetersizdir (bkz. bölüm 5.3). İnsanlara yönelik potansiyel risk bilinmemektedir.
HİZENTRA, hastanın klinik durumu tedavi gerektirmediği sürece, gebelik döneminde kullanılmamalıdır.
Laktasyon dönemi
İnsan normal immünoglobulinlerinin emziren annelerdeki kullanımına ilişkin prospektif klinik çalışmalardan elde edilen veriler sınırlıdır. Bu nedenle; HİZENTRA emziren annelere yalnızca dikkatli bir şekilde verilmelidir. Ancak, immünoglobulinler ile klinik deneyim, yenidoğan üzerinde herhangi bir zararlı etki beklenmediğini öne sürmektedir. İmmünoglobulinler süte geçer ve koruyucu antikorların yenidoğana aktarılmasına katkıda bulunabilir.
Üreme yeteneği/Fertilite
İmmünoglobulinler ile klinik deneyim, fertilite üzerinde zararlı bir etki beklenmediğini öne
sürmektedir.
4.7. Araç ve makine kullanımı üzerindeki etkiler
HİZENTRA'nın araç ve makine kullanma yeteneği üzerinde minör etkisi vardır, örn. baş dönmesi (bkz. bölüm 4.8). Tedavi süresince advers reaksiyonlar yaşayan hastalar araç ve makine kullanmadan önce bu reaksiyonların ortadan kalkmasını beklemelidir.
4.8. İstenmeyen etkiler
Güvenlilik profilinin özeti
Titreme, baş ağrısı, ateş, kusma, alerjik reaksiyonlar, bulantı, artralji, düşük kan basıncı ve orta şiddette bel ağrısı gibi advers reaksiyonlar bazen oluşabilir.
Nadiren insan normal immünoglobulinleri kan basıncında ani bir düşüşe ve hatta hasta daha önceki uygulamada aşırı duyarlılık göstermemiş olsa bile izole vakalarda anafilaktik şoka neden olabilir.
İnfüzyon bölgelerindeki lokal reaksiyonlar: şişme, ağrı, kızarıklık, endürasyon, lokal ısınma, kaşınma, morarma ve döküntü.
Bulaşıcı ajanların güvenliliğine ilişkin bilgi için, bölüm 4.4'e bakınız. Advers reaksiyonların tablo halinde listesi
HİZENTRA klinik çalışmalarında advers reaksiyonlar (AR) primer immün yetmezliği olan hastalarla gerçekleştirilen 7 faz III çalışmasından (n= 231), PİD'i olan hastalarla gerçekleştirilen 2 faz IV çalışmasından (n=74), 1 faz III çalışmasından (n=115) ve KİDP'si olan hastalarla gerçekleştirilen 1 uzatma çalışmasından (n=82) toplanmıştır (toplam N=502 hasta: 26.646 infüzyon). Bu klinik çalışmalarda raporlanan ADR'ler aşağıdaki MedDRA Sistem Organ Sınıfına (SOC ve Tercih Edilen Terim seviyesi) ve görülme sıklığına göre özetlenmekte ve kategorize edilmektedir.
Her bir hasta için sıklık şu kriterler kullanılarak değerlendirilmiştir: çok yaygın (≥1/10), yaygın (≥1/100 ila <1/10), yaygın olmayan (≥1/1.000 ila <1/100) ve seyrek (≥1/10.000 ila <1/1.000), çok seyrek (≥1/100.000 ile <1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). Spontan pazarlama sonrası advers reaksiyonlar için raporlama sıklığı “bilinmiyor†olarak kategorize edilir.
Her bir sıklık grubu içinde, advers reaksiyonlar azalan sıklık sırasına göre sunulmuştur.
Klinik çalışmalardan ve pazarlama sonrası gözetiminden elde edilen HİZENTRA ile ilişkili Advers İlaç Reaksiyonlarının (ADR) Sıklığı, hasta başına veya infüzyon başına raporlanma oranı
Sistem Organ Sınıfı (SOC, MedDRA) | ADR (MedDRA Tercih Edilen Terim, PT) | Hasta başına ADR sıklık kategorisi | İnfüzyon başına ADR sıklık kategorisi |
Bağışıklık sistemi hastalıkları | Hipersensitivite | Yaygın olmayan | Seyrek |
Anafilaktik reaksiyonlar | Bilinmiyor | Bilinmiyor | |
Sinir sistemi hastalıkları | Baş ağrısı | Çok yaygın | Yaygın olmayan |
Baş dönmesi, migren | Yaygın | Seyrek | |
Tremor (psikomotor hiperaktivite dahil) | Yaygın olmayan | Seyrek | |
Aseptik menenjit | Yaygın olmayan | Çok seyrek | |
Yanma hissi | Bilinmiyor | Bilinmiyor | |
Kardiyak hastalıklar | Taşikardi | Yaygın olmayan | Çok seyrek |
Vasküler hastalıklar | Hipertansiyon | Yaygın | Seyrek |
Sıcak basması | Yaygın olmayan | Seyrek | |
Embolik ve trombotik olaylar | Bilinmiyor | Bilinmiyor | |
Gastrointestinal hastalıklar | Diyare, karın ağrısı, | Yaygın | Yaygın olmayan |
Bulantı, kusma | Yaygın | Seyrek | |
Deri ve deri altı dokusu hastalıkları | Döküntü | Çok yaygın | Yaygın olmayan |
Kaşıntı, ürtiker | Yaygın | Seyrek | |
Kas-iskelet bozuklukları bağ doku ve kemik hastalıkları | Kas-iskelet ağrısı, artralji | Yaygın | Yaygın olmayan |
Kas spazmları, kas zayıflığı | Yaygın olmayan | Seyrek | |
Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklar | İnfüzyon bölgesi reaksiyonları | Çok yaygın | Çok yaygın |
Yorgunluk (kırgınlık dahil), pireksi | Yaygın | Yaygın olmayan | |
Göğüs ağrısı, grip benzeri hastalık, ağrı | Yaygın | Seyrek | |
Titreme (hipotermi dahil) | Yaygın olmayan | Seyrek | |
İnfüzyon bölgesi ülseri | Bilinmiyor | Bilinmiyor | |
Araştırmalar | Kan kreatininde artış | Yaygın olmayan | Seyrek |
Pediyatrik popülasyon
HİZENTRA ile gerçekleştirilen klinik çalışmalar PİD'si olan pediyatrik ve yetişkin hastalarda benzer genel güvenlilik profili göstermiştir.
HİZENTRA klinik çalışmalarda KİDP'si olan 18 yaş altındaki pediyatrik hastalarda değerlendirilmemiştir.
Geriyatrik popülasyon
Geriyatrik popülasyonda aynı advers reaksiyonlar meydana gelebilir. Klinik çalışmalardan elde edilen mevcut bilgiler; 65 yaş ve üzeri hastaların güvenlilik profilinde daha genç hastaların güvenlilik profilinden herhangi bir farklılık olmadığını göstermiştir. 65 yaş ve üzeri hastalarda HİZENTRA ile pazarlama sonrası deneyim, bu yaş grubunda daha genç hastalarda olduğu gibi benzer bir genel güvenlilik profili göstermiştir.
Risk faktörleri ve takip tavsiyelerine ilişkin detaylar için bölüm 4.4.'e bakınız.
Şüpheli advers reaksiyonların raporlanması
Ruhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesine olanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu Türkiye Farmakovijilans Merkezi'ne (TÜFAM) bildirmeleri gerekmektedir (www.titck.gov.tr; e-mail: tufam@titck.gov.tr; telefon: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz aşımı ve tedavisi
Doz aşımı sonuçları bilinmemektedir.
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: İmmün serumlar ve immünoglobulinler: İmmünoglobulinler,
normal insan, ekstravasküler uygulama için
ATC kodu: J06BA01
İnsan normal immünoglobulini, başlıca enfeksiyöz ajanlara karşı geniş antikor spektrumuna sahip immünoglobulin G (IgG) içerir.
İnsan normal immünoglobulini normal popülasyonda bulunan IgG antikorların içerir. Genellikle 1000 donörden az olmamak üzere, havuzlanmış plazmadan hazırlanır. Doğal insan plazması ile yakın orantılı immünoglobulin G alt sınıfları dağılımına sahiptir.
Etki mekanizması
İmmün yetmezlikte, HİZENTRA'nın yeterli dozları anormal derecede düşük immünoglobulin G antikor seviyelerini normal aralığa getirebilir ve böylece enfeksiyonlara karşı yardımcı olur.
Replasman tedavisi dışındaki endikasyonlardaki etki mekanizması tam olarak açıklanmamıştır, ancak immünomodülatör etkileri içermektedir.
PID
Pivotal ileriye dönük açık etiketli, tek kollu ve çok merkezli bir Avrupa çalışmasında, yaşları 3 ve 60 arasında değişen ve primer immün yetmezlik sendromu olan toplam 51 gönüllü 41 haftaya kadar HİZENTRA ile tedavi edilmiştir. Her hafta uygulanan ortalama doz 0,12 g/kg vücut ağırlığıdır. 7,99 – 8,25 g/l ortalama konsantrasyon ile kesintisiz IgG dip düzeyleri tedavi dönemi boyunca sağlanmıştır. Gönüllüler toplam 1831 haftalık HİZENTRA infüzyonu almıştır.
İleriye dönük açık etiketli, tek kollu ve çok merkezli bir ABD çalışmasında, yaşları 5 ve 72 arasında değişen primer immün yetmezlik sendromu olan toplam 49 gönüllü 15 aya kadar HİZENTRA ile tedavi edilmiştir. Her hafta uygulanan ortalama doz 0,23 g/kg vücut ağırlığıdır. 12,53 g/L'lik ortalama konsantrasyon ile kesintisiz IgG dip düzeyleri tedavi dönemi boyunca sağlanmıştır. Gönüllüler toplam 2264 haftalık HİZENTRA infüzyonu almıştır. Klinik çalışmalar süresince HİZENTRA alan gönüllülerde etkililik periyodu boyunca herhangi bir ciddi bakteriyel enfeksiyon rapor edilmemiştir.
Manuel yoldan uygulama ve pompa destekli uygulama yoluyla uygulanan daha yüksek infüzyon hızlarının güvenliliği ve tolerabilitesini değerlendirmek amacıyla yaşları 2 ila 75
arasında değişen 49 PİD'li gönüllü; açık etiketli, çok merkezli, paralel kollu, randomize olmayan bir faz IV HILO (HİZENTRA Etiket Optimizasyonu) çalışmasına kaydedilmiştir ve en az 12 hafta boyunca HİZENTRA ile tedavi edilmiştir (2 ila 18 yaşın altındaki 11 pediyatrik hasta, 18 ila 65 yaşındaki 35 yetişkin hasta ve 65 yaş üzerindeki 3 geriyatrik hasta). Manuel itme tekniğiyle HİZENTRA alan ilk hasta grubunda (n=16), her hafta 30, 60 ve 120 ml/saat/bölge akış hızında her hafta 2 ila 7 infüzyon uygulanmıştır (bkz. Bölüm 4.2). Pompa destekli uygulama yoluyla HİZENTRA alan ikinci hasta grubunda (n=18), 25, 50, 75 ve 100 ml/saat/bölge akış hızında haftalık HİZENTRA infüzyonları uygulanmıştır. Üçüncü grupta, haftalık HİZENTRA dozlarının pompa destekli uygulamasıyla bölge başına 25, 40 ve 50 ml infüzyon hacimleri değerlendirilmiştir (n=15). Üç grubun tümünde, her bir infüzyon parametresi 4 hafta boyunca kullanılmış ve bu süre sonunda gereken minimum geçerli infüzyon sayısını başarıyla tamamlayan gönüllüler sıradaki daha yüksek infüzyon parametresine geçebilmiştir.
Primer sonlanım noktası, daha yüksek infüzyon parametresine yanıt veren gönüllülerin
yüzdesidir:
Grup İnfüzyon parametresi ve yanıt oranı (%)
1. Manuel itme akış hızları | 30 ml/sa/bölge | 60 ml/sa/bölge | 120 ml/sa/bölge | - |
%100 | %100 | %87,5 | - | |
2. Pompa destekli akış hızları | 25 ml/sa/bölge | 50 ml/sa/bölge | 75 ml/sa/bölge | 100 ml/sa/bölge |
%77,8 | %77,8 | %66,7 | %61,1 | |
3. Pompa destekli hacimler | 25 ml/bölge | 40 ml/bölge | 50 ml/bölge | - |
%86,7 | %73,3 | %73,3 | - |
Yanıt veren: Pompa destekli grupta, bir infüzyon parametresi için 4 infüzyonda 3 ve üzeri geçerli infüzyon yapılan bir gönüllü; manuel itme grubunda, bir infüzyon parametresi için %60 ve üzerinde geçerli infüzyonu olan bir gönüllü. 1 ve üzeri infüzyon bölgesi başına planlanan akış hızı/hacminin %95 ve üzerine ulaşıldıysa, infüzyon geçerli olarak kabul edilmektedir.
Genel olarak, şiddetli lokal reaksiyonlar olmayan infüzyonların sayısıyla toplam infüzyonların sayısının (tolerabilite) karşılaştırması tüm infüzyon parametreleri için tüm gruplarda 0,98 ve üzeridir. Tüm gönüllülerde 1. Günde başlangıçta ve çalışma sonunda serum IgG dip konsantrasyonları arasında klinik açıdan anlamlı hiçbir fark gözlemlenmemiştir.
KİDP
KİDP'si olan hastalarda HİZENTRA'nın güvenlilik, etkililik ve tolerabilitesi çok merkezli, çift kör, randomize, plasebo-kontrollü, paralel gruplu bir faz III PATH (Polinötropati ve HİZENTRA ile Tedavisi) çalışmasında değerlendirilmiştir. IVIg ile daha önceden tedavi edilen ve yanıt veren, kesin veya muhtemel KİDP'si olan 172 yetişkin haftalık 0,2 g/kg vücut ağırlığı HİZENTRA, haftalık 0,4 g/kg vücut ağırlığı HİZENTRA veya plasebo gruplarına randomize edilmiştir ve ardından 24 hafta süreyle takip edilmişlerdir. Ortalama maruziyet süresi 0,2 g/kg vücut ağırlığı HİZENTRA grubunda 118,9 gün ve 0,4 g/kg vücut ağırlığı HİZENTRA grubunda 129 gün olmuştur (her bir grupta maksimum maruziyet sırasıyla 167 gün ve 166 güne kadar). Gönüllüler genellikle paralel olarak 4 infüzyon bölgesi kullanmıştır (paralel olarak 8 bölgeye kadar). Toplamda, plasebo grubunda 57 gönüllüye 1514 infüzyon, 0,2 g/kg vücut ağırlığı HİZENTRA grubunda 57 gönüllüye 2007 infüzyon ve 0,4 g/kg vücut ağırlığı HİZENTRA grubunda 58 gönüllüye 2218 infüzyon uygulanmıştır (toplamda 5739 infüzyon).
Primer etkililik sonlanım noktası KİDP relapsına sahip gönüllülerin yüzdesi (başlangıç ile karşılaştırıldığında ayarlanan İnflamatuvar Nöropati Vakası ve Tedavisi ï›INCATï skorunda ≥
1 puan artışı olarak tanımlanmıştır) veya HİZENTRA tedavi periyodundan başka herhangi bir
nedenle geri çekilen hastaların yüzdesi olmuştur.
Her iki HİZENTRA dozu, primer sonlanım noktası açısından plaseboya karşı üstünlük göstermiştir. HİZENTRA ile tedavi edilen gönüllülerin istatistiksel olarak anlamlı daha az bir yüzdesi, 0,4 g/kg vücut ağırlığı için % 32,8 ve 0,2 g/kg vücut ağırlığı için % 38,6, plasebo ile tedavi edilen gönüllülerin % 63,2'si ile karşılaştırıldığında, KİDP relapsına sahiptir veya başka nedenlerle geri çekilmiştir (sırasıyla p<0,001 veya p= 0,007). Yalnızca relaps dikkate alındığında; KİDP relaps oranları, % 56,1'lik plasebo oranı ile karşılaştırıldığında, 0,4 g/kg vücut ağırlığı HİZENTRA için % 19,0 ve 0,2 g/kg vücut ağırlığı HİZENTRA için % 33,3 olmuştur (sırasıyla p<0,001 veya p= 0,012). Buna göre; 24 haftalık tedavi periyodu boyunca, HİZENTRA % 0,4 g/kg vücut ağırlığı ve 0,2 g/kg vücut ağırlığı gruplarında sırasıyla gönüllülerin % 81 ve % 67'sinde relapsı önlerken; plasebo grubunda gönüllülerin% 44'ünde relaps gözlenmemiştir.
KİDP relaps süresi (Şekil 1) değerlendirilmiş ve Kaplan-Meier tahminleri esas alınarak ilgili KİDP relaps olasılıkları plasebo için % 58,8, 0,2 g/kg vücut ağırlığı HİZENTRA için % 35,0 ve 0,4 g/kg vücut ağırlığı HİZENTRA için % 22,4 olmuştur. Plasebo ile karşılaştırıldığında düşük doz ve yüksek doz için tehlike oranı (% 95 güven aralığı) sırasıyla 0,48 (0,27, 0,85) ve 0,25 (0,12, 0,49) olmuştur. 0,2 g/kg vücut ağırlığı HİZENTRA ve 0,4 g/kg vücut ağırlığı HİZENTRA grupları arasında gözlemlenen fark istatistiksel anlamlılığa ulaşmamıştır.
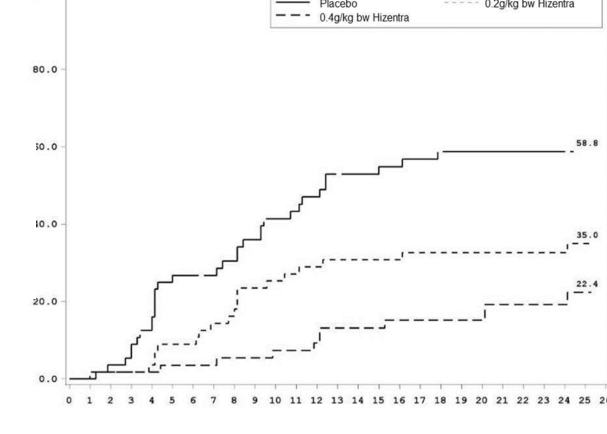
Hafta
------ Plasebo 0,2g/kg vücut ağırlığı HİZENTRA
- 0,4g/kg vücut ağırlığı HİZENTRA
Relaps olasılığı (%)
Şekil 1: KİDP Relapsı için Kaplan-Meier Zaman Grafiği
Etkililik skorlarında (INCAT skoru, ortalama kavrama gücü ve Medikal Araştırma Konseyi toplam skoru), plasebo grubundaki gönüllüler kötüleşirken, her iki HİZENTRA dozu
grubundaki gönüllüler stabil kalmıştır. Yüksek doz HİZENTRA grubundaki gönüllüler Rasch- yerleşik Genel Engellilik Ölçeği (R-ODS) Yüzde Birlik Skoru'nda stabil kalmıştır. Her iki HİZENTRA doz grubundaki gönüllüler elektrofizyoloji parametrelerinde stabil kalmıştır.
Bir faz III, çok merkezli, 48 haftalık açık etiketli genişletme çalışmasına, PATH çalışmasından KİDP'li 82 hasta dahil edilmiştir. Genişletme çalışması, iki haftalık 0,2 g/kg vücut ağırlığı ve 0,4 g/kg vücut ağırlığı dozlarında uygulanan HİZENTRA idame tedavisinin uzun dönem etkililik ve güvenliliğini araştırmıştır. Çalışma tasarımı nedeniyle, aynı gönüllüler çalışma sırasında her iki dozu da alabilir; etkililik değerlendirme periyodu boyunca 72 gönüllü 0,4 g/kg doz ve 73 gönüllü ise 0,2 g/kg doz almıştır. Ortalama etkililik değerlendirme periyodu 0,2 g/kg vücut ağırlığı grubunda 125,8 gün (aralık: 1-330) iken, ve 0,4 g/kg vücut ağırlığı grubunda ise 196,1 gündür (aralık: 1-330). 0,4 g/kg vücut ağırlığı dozunda herhangi bir relaps olmaksızın pivotal PATH çalışmasını tamamlayan ve genişletme çalışmasında başlangıçta bu dozu alan hastaların relaps oranı % 5,6 (1/18 hasta) olmuştur. PATH genişletme çalışmasında 0,4 g/kg vücut ağırlığı alan tüm hastaların % 9,7'sinde (7/72 hasta) relaps meydana gelmiştir. 0,2 g/kg vücut ağırlığı dozunda herhangi bir relaps olmaksızın PATH çalışmasını tamamlayan ve genişletme çalışmasında başlangıçta bu dozu alan hastaların relaps oranı % 50 (3/6 hasta) olmuştur. Genişletme çalışmasında 0,2 g/kg vücut ağırlığı alan tüm hastaların % 479'unda (35/73 hasta) relaps meydana gelmiştir. PATH çalışmasını tamamlayan ve genişletme çalışmasında 0,4 g/kg vücut ağırlığından 0,2 g/kg vücut ağırlığındaki düşük doza titre edilen hastaların % 67,9'unda (19/28 hasta) herhangi bir relaps meydana gelmemiş olup; relaps meydana gelen 9 hastalanın tamamı 0,4 g/kg vücut ağırlığı dozu ile tedavi sonrası 4 hafta içerisinde iyileşmiştir. Genişletme çalışmasında hiç relaps yaşamayan hastalar için; kavrama kuvveti, MRC toplam skoru ve R-ODS yüzde birlik skoru başlangıç değeri ile karşılaştırıldığında stabil kalmıştır.
Pediyatrik popülasyon
HİZENTRA'nın güvenliliği ve etkililiği yaşları 2 – 18 arasında değişen pediyatrik hastalarda kanıtlanmıştır. HİZENTRA yaşları 2 – <12 arasında değişen PID'li 68 pediyatrik hastada ve yaşları 12 – <18 arasında değişen 57 pediyatrik hastada değerlendirilmiştir. Yetişkin gönüllülerle karşılaştırıldığında; farmakokinetik, güvenlilik ve etkililik profilleri bakımından herhangi bir farklılık gözlenmemiştir. İstenen serum IgG seviyelerine ulaşmak için herhangi bir pediyatrik-spesifik doz ayarlamasına ihtiyaç duyulmamıştır. PID'li yetişkin ve pediyatrik çalışma hastaları arasında farmakodimamik özelliklerde herhangi bir fark gözlenmemiştir.
HİZENTRA klinik çalışmalarda KİDP'si olan ve 18 yaşın altındaki pediyatrik hastalarda değerlendirilmemiştir.
Geriyatrik popülasyon
65 yaşından büyük ve 18 – 65 yaş arası PID hastaları arasında güvenlilik veya etkililikte herhangi bir genel farklılık gözlenmemiştir. Klinik çalışmalarda, HİZENTRA 65 yaşından büyük ve PID'li 13 hastada değerlendirilmiştir.
65 yaşından büyük KİDP'li hastalar ve 18 – 65 yaş arasındaki KİDP'li hastalar arasında güvenlilik veya etkililik bakımından herhangi bir genel farklılık gözlenmemiştir. KİDP'li hastalarla gerçekleştirilen klinik çalışmalarda, 65 yaşından büyük 61 gönüllü HİZENTRA ile tedavi edilmiştir.
5.2. Farmakokinetik özellikler
Genel Özellikler
Emilim:
SCIg alımı, lokal bölgeden lenf sistemine, ardından vasküler boşluğa difüzyon aracılığı ile sağlanır.
Dağılım:
HİZENTRA'nın subkutan uygulamasını takiben; pik serum seviyelerine yaklaşık 2 gün sonra ulaşılır. Toplam serum IgG, IgG alt sınıfları ve spesifik IgG'lerin serum konsantrasyonları, doz aralığı boyunca stabildir.
Biyotransformasyon:
IgG ve IgG kompleksleri retiküloendotelyal sistemin hücrelerinde parçalanır.
Eliminasyon:
Yarılanma ömrü, özellikle primer immün yetmezlikte, hastadan hastaya değişkenlik gösterebilir.
PID
HİZENTRA ile gerçekleştirilen bir klinik faz III çalışmasında (n=46); gönüllüler haftalık 0,06 – 0,24 g/kg vücut ağırlığı medyan doz alırken, 29 haftalık bir periyod boyunca kesintisiz dip seviyelerine (medyan 8,1 g/L) ulaşmışlardır.
Ampirik Popülasyon Farmakokinetik modelleri ile gerçekleştirilen simülasyonlar; idame tedavisi boyunca HİZENTRA subkutan olarak her iki haftada bir haftada iki kez uygulanırsa, karşılaştırılabilir IgG maruziyet seviyelerinin (EAA, C) sağlanabildiğini öne sürmektedir.
Bu simülasyonlar aynı zamanda; HİZENTRA'nın haftalık idame dozu haftada birden daha sık orantılı miktarlarda uygulandığında (örn. haftada 2 kez, haftada 3 kez, haftada 5 kez veya günlük), karşılaştırılabilir serum IgG dip seviyelerine ulaşıldığını da öne sürmektedir.
Atlanılan 2-3 günlük doz simülasyonu, devamlı olarak alınan günlük dozla karşılaştırıldığında medyan serum IgG seviyelerinde ≤ % 4'lük bir azalma ile sonuçlanmıştır. Günlük dozlamaya yeniden başlandığında atlanılan dozları değiştirerek, medyan konsantrasyon profili 2-3 günde iyileşmiştir. Ancak; günlük dozlama tekrar başlandığında atlanılan dozlar değiştirilmezse, IgG dip seviyelerinin kararlı duruma dönmesi 5-6 hafta kadar sürmüştür.
KİDP:
PATH çalışmasında (n=172); gönüllüler haftalık sırasıyla 0,2 g/kg vücut ağırlığı ve 0,4 g/kg vücut ağırlığı doz alırken, 24 haftalık bir periyod boyunca kesintisiz dip seviyelerine ulaşmışlardır. 0,4 g/kg vücut ağırlığı grubunda HİZENTRA tedavisinden sonra ortalama (SD) IgG dip konsantrasyonu 20,4 (3,24) g/L ve 0,2 g/kg vücut ağırlığı grubunda ise 15,4 (3,06) g/l olmuştur. PATH çalışmasında popülasyon farmakokinetik modelleri ile gerçekleştirilen simülasyonlar; KİDP hastalarında iki haftada bir haftada iki defa HİZENTRA dozu uygulandığında, karşılaştırılabilir bir IgG maruziyetine (C, EAA, C) ulaşıldığını öne sürmektedir. Bu simülasyonlar aynı zamanda; KİDP hasta popülasyonunda HİZENTRA'nın haftalık idame dozu birkaç doza bölünerek daha sık uygulandığında (haftada
2 – 7 defa), buna uygun olarak karşılaştırılabilir bir IgG maruziyeti elde edildiğini da öne
sürmektedir.
Hastalardaki karakteristik özellikler
Pediyatrik popülasyon:
Yetişkin ve pediyatrik çalışma PID hastaları arasında farmakokinetik parametrelerde herhangi bir farklılık gözlenmemiştir.
HİZENTRA, KİDP'si olan 18 yaşından küçük hastalarda klinik çalışmalarda değerlendirilmemiştir.
Geriyatrik popülasyon:
65 yaşından büyük PİD hastaları ve 18 – 65 yaş arasındaki hastalar arasında farmakokinetik parametrelerde herhangi bir genel farklılık gözlenmemiştir.
65 yaşından büyük KİDP hastaları ve 18 – 65 yaş arasındaki hastalar arasında farmakokinetik parametrelerde herhangi bir genel farklılık gözlenmemiştir.
5.3. Klinik öncesi güvenlilik verileri
İmmünoglobulinler insan vücudunun normal bir bileşenidir. L-prolin, fizyolojik, esansiyel olmayan bir amino asittir.
HİZENTRA'nın güvenliliği, yardımcı madde L-proline özel referansla çeşitli klinik öncesi çalışmalarda değerlendirilmiştir. Klinik dışı veriler güvenlilik farmakolojisi ve toksisite çalışmaları temelinde insanlarda özel risk ortaya koymamıştır.
6. FARMASÖTİK ÖZELLİKLER
6.1. Yardımcı maddelerin listesi
L-prolin Polisorbat 80 Enjeksiyonluk su
Sodyum hidroksit (pH ayarlama için) Hidroklorik asit (pH ayarlama için)
6.2. Geçimsizlikler
6.2. Geçimsizlikler
6.3. Raf ömrü
30 ay.
Flakon açıldıktan sonra, çözelti derhal kullanılmalıdır.
6.4. Saklamaya yönelik özel tedbirler
25 °C altındaki oda sıcaklığında ve ışıktan korumak için orijinal ambalajında saklayınız. Dondurmayınız.
Çocukların göremeyeceği, erişemeyeceği yerlerde ve ambalajında saklayınız.
Tıbbi ürünün açıldıktan sonraki saklama koşulları için bölüm 6.3'e bakınız.
6.5. Ambalajın niteliği ve içeriği
Tıpalı (halobütil), kapaklı (alüminyum kırma) ve açma diskli (plastik) 20 mL (4 g) çözelti içeren Tip I cam flakon
Alkollü mendiller, iğneler ve diğer malzeme ve ekipmanlar ambalaj içinde yer almamaktadır.
6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
HİZENTRA tek kullanımlık flakonlarda kullanıma hazır çözelti olarak sunulur. Çözelti koruyucu içermediği için, HİZENTRA flakon açıldıktan sonra derhal kullanılmalıdır.
Tıbbi ürün kullanılmadan önce oda veya vücut sıcaklığına getirilmelidir. Çözelti berrak ve açık sarı veya açık kahverengi olmalıdır.
Bulanık ya da tortulu çözeltiler kullanılmamalıdır.
Kullanılmamış olan ürünler ya da atık materyaller ‘‘Tıbbi Atıkların Kontrolü Yönetmeliği'' ve ‘‘Ambalaj Atıklarının Kontrolü Yönetmeliği''ne uygun olarak imha edilmelidir.
 Şizofrenlik
Şizofrenliğin psikiatrik teşhisi hakkında çok fazla anlaşmazlık vardır. Bu
sayfadaki bilgiler, şizofrenliğin teşhisi, nedenleri ve tedavisi hakkındaki faklı teoriler
hakkında bilgi verecektir.
Şizofrenlik
Şizofrenliğin psikiatrik teşhisi hakkında çok fazla anlaşmazlık vardır. Bu
sayfadaki bilgiler, şizofrenliğin teşhisi, nedenleri ve tedavisi hakkındaki faklı teoriler
hakkında bilgi verecektir. |
 Tiroid Kanseri
En sık görülen tiroid kanseri türü olan papiller tiroid kanseri, tüm tiroid kanserlerinin yaklaşık %70'ini oluşturur.
Tiroid Kanseri
En sık görülen tiroid kanseri türü olan papiller tiroid kanseri, tüm tiroid kanserlerinin yaklaşık %70'ini oluşturur. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| HIZENTRA | 8681624980200 | 3,134.55TL |
| HYQVIA | 8681429550325 | 37,712.90TL |
| SUBCUVIA | 8699556981264 | |
| Diğer Eşdeğer İlaçlar |
 |
Artrit Artrit, oldukça yaygın bir hastalıktır ancak iyi anlaşılamamıştır. Aslında “artrit” tek bir hastalığın adı değildir; eklem ağrısı veya eklem hastalıklarını adlandırmanın gayri resmi yoludur. |
 |
Asperger Sendromu Asperger sendromu, otistik gurubun bir bölümü olan bir özürdür. Bu genelde, gurubun daha ”yüksek” tarafında yer aldığı düşünülen kişilere uygun bir tanıdır. |
 |
İnme İnme, beynin hasar görmesinin sonucudur. Bu hasar, beynin bir kısmındaki ya bir kanama ya da akut kan eksikliği nedeniyle o kısmın geçici ya da kalıcı olarak işlevini yapamamasına yol açar. |
İLAÇ GENEL BİLGİLERİ
Csl Behring Biyoterapi İlaç Dış Tic. A.Ş
| Satış Fiyatı | 12621.14 TL [ 14 Apr 2025 ] |
| Önceki Satış Fiyatı | 12621.14 TL [ 7 Apr 2025 ] |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Mor Reçeteli bir ilaçdır. |
| Barkodu | 8681624980224 |
| Etkin Madde | Human Immunoglobulin |
| ATC Kodu | J06BA01 |
| Birim Miktar | 4 |
| Birim Cinsi | G |
| Ambalaj Miktarı | 1 |
| Enfeksiyona Karşı Kullanılan (Antienfektif) İlaçlar > İmmünoglobülinler > Immunoglobulins, normal human, for extravascular administration |
| İthal ( ref. ülke : Isvicre ) ve Beşeri bir ilaçdır. |