IDEBEX 45 mg 30 film kaplı tablet Farmakolojik Özellikler
{ Idebenon }
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Diğer Psikostimülan ve Nootropikler ATC kodu: N06BX13
Etki mekanizması
Farklı bir etki mekanizmasına sahip olan idebenon, Alzheimer tedavisinde kullanılan potansiyel sitoprotektif bir ilaçtır. İdebenon gibi antioksidan ve serbest radikal etkili bileşikler, β-amiloid'e bağlı nörotoksisiteyi ve bilişsel fonksiyondaki bozulmaları düzeltebilir. Lipid peroksidasyonunu engelleme yeteneği nedeniyle idebenon, hücre membranlarını ve mitokondriyi oksidatif hasardan korur. Antioksidan özelliği ile merkezi sinir sistemini serebral iskemi ve sinir hasarına karşı korur. İdebenon aynı zamanda iskemi durumunda ATP formasyonunu koruyarak ETC (elektron transport zinciri) ile etkileşime girer. Bu bileşik aynı zamanda Alzheimer'da ve diğer nörodejeneratif hastalıkların tedavisinde önemli olan sinir gelişim faktörünü stimüle eder. Yapılan in vitro ve in vivo çalışmalar idebenonun iskemi nedeniyle oluşan sinir hücre hasarını azalttığını, nörotransimitter bozuklukları ve/veya serebral metabolizmayı düzelttiğini ve öğrenmeyi kolaylaştırdığını göstermektedir. Bunlara ek olarak, hafıza, dikkat toplanması ile oriyantasyon üzerine etkili olduğu ve hastalığın ilerlemesini yavaşlattığı gösterilmiştir.
Klinik etkililik ve güvenlilik
Prospektif, randomize, çift kör, plasebo kontrollü, çok merkezli bir çalışmada, hafif ila orta derecede Alzheimer tipi demansı (DAT) olan hastalarda idebenonun iki dozu ile çalışılmıştır. 300 hasta 6 ay boyunca plasebo (n=100), günde 3 kez 30 mg idebenon (n=100) veya günde 3 kez 90 mg idebenon (n=100) almak üzere randomize edilmiştir. 6 aylık tedaviden sonra günde 3 kez 90 mg idebenon alan grubun ADAS-total ve ADAS-Cog değişkenlerinde istatistiksel olarak anlamlı düzelmeler gözlenmiştir.
Tablo 1: Başlangıçtaki ADAS total skor değerine göre seçilen hastalar. Başlangıçtan 6. aya kadarki ADAS skorundaki ortalama değişim (parantez içindekiler plasebo düzeltilmiş değişimler); | ||||
ADAS Total'deki ciddiyet | Her bir gruptaki kişi sayısı (Pla/30/90) |
Plasebo |
30 mg |
90 mg |
ADAS-Cog | 40/43/43 | -5,3 | -5,8 (-0,5) | -7,8 (-2,5) |
≥20 | 30/27/25 | -5,7 | -6,6 (-0,9) | -9,1 (-3,5) |
≥30 | 20/19/77 | -6,8 | -8,0 (-1,3) | -10,7 (-4) |
≥40 | 13/10/9 | -7,9 | -11,9 (-4) | -14,8 (-6,9) |
≥50 |
|
|
|
|
ADAS-NonCog |
|
|
|
|
≥20 | 40/43/43 | -1,8 | -2,2 (-0,4) | -3,3 (-1,5) |
≥30 | 30/27/25 | -1,7 | -2,7 (-1) | -4,2 (-2,5) |
≥40 | 20/19/77 | -2,4 | -3,3 (-1) | -4,9 (-2,5) |
≥50 | 13/10/9 | -3,5 | -4,0 (-0,5) | -7,3 (-3,3) |
Plasebo-düzeltilmiş değişimler yuvarlanmayan değerlerden hesaplanmıştır. | ||||
CGI-Düzelmesi, ADAS-Cog ve ADAS-nonCog ölçümleri için yapılan analizde günde 3 kez
Tablo 2: 6 aylık tedaviden sonraki iyileşme oranları Tedaviye yanıt verenlerin toplam hasta sayısına oranı ve yanıt verenlerin yüzdesi | |||||||
Değişkenler | Plasebo |
| 30 mg |
| 90 mg |
| P değeri |
| Oran | % | Oran | % | Oran | % | |
Tüm hastalar |
|
|
|
|
|
|
|
ADAS-Cog | 34/83 | 41 | 35/79 | 44,3 | 47/85 | 55,3 | 0,031 |
ADAS-Noncog | 11/83 | 13,3 | 20/79 | 25,3 | 21/85 | 24,7 | 0,035 |
CGI-İyileşme | 56/83 | 67,5 | 57/79 | 72,2 | 71/87 | 81,6 | 0,018 |
ADAS-Total≥20 |
|
|
|
|
|
|
|
ADAS-Cog | 24/48 | 50 | 29/51 | 56,9 | 38/51 | 74,5 | 0,006 |
ADAS-Noncog | 9/48 | 18,8 | 16/51 | 31,4 | 20/51 | 39,2 | 0,014 |
CGI-İyileşme | 23/48 | 47,9 | 34/51 | 66,7 | 46/52 | 88,5 | 0 |
İlişkili iyileşme: ADAS-Cog; en az -6 puan; ADAS-nonCog: en az -4 puan; CGI-İyileşme: | |||||||
'az' ila “çok fazlaâ€. Tedaviler arasındaki P değerleri Mantel – Haenteszel x testten hesaplanmıştır. | |||||||
90 mg alınan idebenonun, plaseboya göre anlamlı oranda üstünlük sağladığı görülmüştür.
90 mg İdebenon ile tedaviye yanıt veren hastaların %'lik oranı plaseboya kıyasla daha üstün bulunmuştur.
Yapılan tüm değerlendirmelerde, güvenlilik ile ilgili olumsuz bir bulguya rastlanmamıştır. Bu çalışmanın sonuçları, DAT hastalarının tedavisinde idebenonun etkili ve güvenli olduğunu göstermiştir.
Hafif ila orta derecede Alzheimer tipi demansı (DAT) olan hastalarda, idebenonun etkililik ve güvenliliğinin değerlendirildiği 2 yıllık, prospektif, randomize, çift kör, çok merkezli ve 3 paralel gruptan oluşan bir çalışma gerçekleştirilmiştir. Toplam 450 hasta, 12 ay boyunca plasebo ve ardışık 12 ay boyunca da günde 3 kez 90 mg idebenon almak (n=153) veya 24 ay boyunca günde 3 kez 90 mg idebenon almak (n=148) veya 24 ay boyunca günde 3 kez 120 mg idebenon almak (n=149) üzere randomize edilmiştir. Plasebonun kullanıldığı kontrol periyodu boyunca (tedavinin ilk yılı) idebenon, birincil etkililik değişkeni ADAS-total ve tüm ikincil etkililik değişkenlerinde istatistiksel olarak anlamlı, doza bağımlı düzelmeler meydana getirmiştir. Tedavinin ikinci yılı boyunca etkililiğin kaybolduğuna dair bir bulgu
gözlenmemekle birlikte, 12. ayda yapılan vizitlere göre ikinci yılda çoğu etkililik değişkenlerinin daha da düzeldiği saptanmıştır. Ayrıca tedavinin ikinci yılı boyunca, açık bir şekilde doza bağlı olarak etkililiğin (plasebo/90 mg idebenon < 90 mg idebenon < 120 mg idebenon) arttığı gözlenmiştir.
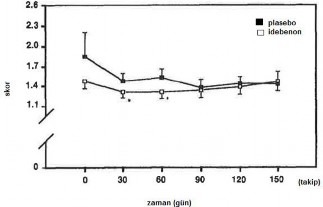
Hafif ila orta şiddetli vasküler kökenli mental bozukluğu olan 108 yaşlı hasta ile yapılan randomize, çift kör, plasebo kontrollü, çok merkezli bir çalışmada hastalar 120 gün boyunca, günde 2 kez 45 mg oral idebenon tedavisi almışlardır. 120 gün sonra ilaç tedavisi kesilmiş ve 30 gün boyunca hasta takip edilmiştir. Çalışmanın 90. gününde İdebenon grubunda hastanın modunda, davranışlarında, uykusunda ve hafızasında belirgin bir iyileşme gözlenirken, plasebo grubunda ise kötüleme gözlenmiştir. Çalışmanın sonunda (150. gün) İdebenon alan hastaların
%50'sinde global durumunda iyileşme gözlenirken, geri kalan %50'sinde ise herhangi bir gerileme gözlenmemiştir. Plasebo alan hastaların %66'sının durumu kötüleşmiş ya da aynı kalmıştır.
| Şekil 1 Demans için GBS derecelendirme skalası: emosyonel bozulma: veriler ortalama ± Standart Hata Ortalaması. *t0 vs t30 ve t0 vs t60 idebenon, P<0,006 |
Tedavi sonrası yapılan değerlendirmede, idebenonun multipl infarktlı demans tedavisinde etkili olduğu kanıtlanmıştır. Hafıza, dikkat ve bilişsel fonksiyonlardaki iyileşmeleri gösteren testlerde, plaseboya göre idebenon tedavisiyle, anlamlı oranda düzelmiş skorlar elde edilmiştir. İlacın iyi tolere edildiği ve multipl infarktlı demansı olan hastalarda etkili olduğu bildirilmiştir. Tedaviden önce veya sonra, hastaların laboratuar değerlerinde herhangi bir değişiklik gözlenmemiştir.
5.2. Farmakokinetik özellikler
Genel özelliklerEmilim:
İdebenon, oral uygulamanın ardından gastrointestinal sistemden hızlı bir şekilde emilir. İdebenon, sağlıklı gönüllülerde 30-180 mg tek doz uygulanmasının ardından 0,9-2,1 saat içerisinde 327-1.957 µg/L maksimum plazma konsantrasyonlarına (C) ulaşır. İdebenon dozu 30 ile 180 mg aralığında arttırıldığında, plazma konsantrasyonları da doğrusal olarak artar. Sağlıklı gönüllülerde idebenonun tekrarlı doz uygulamasının ardından (10 gün boyunca günde 2 kez 45 mg ya da 7 gün boyunca günde 3 kez 30-120 mg) ölçülen Cdeğerleri (369-1.896 µg /L aralığında) ile tek doz uygulanmasının ardından ölçülen değerler arasında anlamlı bir fark
yoktur. Bu da tekrarlı doz uygulaması boyunca kayda değer ilaç birikiminin olmadığını göstermektedir.
İdebenonun absorbsiyonu, tokluk durumunda açlık durumuna göre daha yüksektir. Kahvaltıdan önce ya da sonra tek doz 100 mg idebenon alan 3 sağlıklı gönüllüde Cdeğerleri açlık durumunda 439 µg /L ve tokluk durumunda 787 µg /L ve eğri altındaki alan (EAA) değerleri açlık durumunda 2.795 µg /L.s ve tokluk durumunda 4.158 µg/L.s olarak bulunmuştur.
Dağılım:
Deneysel veriler idebenonun kan-beyin bariyerini geçtiğini ve serebral dokuda önemli konsantrasyonlarda dağıldığını göstermiştir. Oral uygulamayı takiben, gözün aköz hümorunda farmakolojik olarak ilgili idebenon konsantrasyonları saptanabilir.
Uzun süreler boyunca kullanılması durumunda dahi idebenon birikme eğilimi göstermemektedir. Deneysel veriler idebenonun hematoensefalik bariyeri geçtiğini ve beyin dokusu seviyesinde anlamlı konsantrasyonlar halinde dağıldığını ortaya koymuştur.
Biyotransformasyon:
Metabolizma; yan zincirin oksidatif kısalması, kinon halkasının indirgenmesi ve glukuronidlere ve sülfatlara konjügasyon yoluyla meydana gelir. İdebenon, idebenon konjugatlarını (glukuronidler ve sülfatlar [IDE-C]) ve faz I metabolitleri QS10, QS6 ve QS4'ü ve bunların ilişkili faz II metabolitlerini (glukuronidler ve sülfatlar [QS10 + QS10-C, QS6 + QS6-C, QS4
+ QS4-C]) oluşturan yüksek bir ilk geçiş metabolizması gösterir. Plazmada ana metabolitler IDE-C ve QS4 + QS4-C'dir.
Eliminasyon:
İdebenonun renal klirensi güçlüdür. Sağlıklı gönüllülere radyoaktif olarak işaretlenmiş tek doz 90 mg idebenon uygulanmasının ardından 7 gün sonra, % 79,8'inin (ilk 8 saatte %60,2'si) idrarla; % 7,1'inin dışkı ile atıldığı gözlenmiştir.
Sağlıklı gönüllülerde tek doz idebenonun terminal plazma eliminasyon yarılanma ömrü (t), 2,6 ila 21,7 saat arasında değişmektedir. Bu çeşitliliğin, çalışmalar arasındaki metodoloji farlılıklardan kaynaklandığı düşünülmektedir. Tekrarlı uygulamalardan sonra idebenonun vücutta birikmediği görüldüğünden, bazı bireylerde bildirilen yüksek tdeğerleri muhtemelen klinik olarak anlamlı değildir.
Doğrusallık/doğrusal olmayan durum:
Sağlıklı erişkin erkek gönüllülerle yapılan bir çalışmada oral yolla 1.050 mg'a kadar tek doz ve
2.250 mg'a kadar tekrarlı dozlarda alınan idebenonun doğrusal farmakokinetik özellik gösterdiği gözlenmiştir.
5.3. Klinik öncesi güvenlilik verileri
Geleneksel güvenlilik farmakolojisi, tekrarlanan doz toksisitesi, genotoksisite, karsinojenik potansiyel, üreme ve gelişme toksisitesi çalışmalarına dayanan klinik öncesi çalışmalar idebenonun insanlara yönelik özel bir tehlike ortaya koymadığını göstermiştir.
 Ağız Kanseri
Ağız kanserinin en yaygın türleri, dudak, dil, dişetidir. Nadiren
yanak içi veya damak bölgelerini de içine alır.
Ağız Kanseri
Ağız kanserinin en yaygın türleri, dudak, dil, dişetidir. Nadiren
yanak içi veya damak bölgelerini de içine alır. |
 Parkinson Hastalığı
Hastalık ilk kez 1817 de İngiliz doktor James Parkinson tarafından tanımlanmış ve Dr. Parkinson hastalığı “sallayıcı felç” olarak kaleme almış.
Parkinson Hastalığı
Hastalık ilk kez 1817 de İngiliz doktor James Parkinson tarafından tanımlanmış ve Dr. Parkinson hastalığı “sallayıcı felç” olarak kaleme almış. |
İLAÇ GENEL BİLGİLERİ
Neutec İlaç San. Tic.A.Ş.
| Geri Ödeme Kodu | A14777 |
| Satış Fiyatı | 388.43 TL [ 24 Mar 2025 ] |
| Önceki Satış Fiyatı | 388.43 TL [ 17 Mar 2025 ] |
| Original / Jenerik | Jenerik İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8680881093579 |
| Etkin Madde | Idebenon |
| ATC Kodu | N06BX13 |
| Birim Miktar | 45 |
| Birim Cinsi | MG |
| Ambalaj Miktarı | 30 |
| Sinir Sistemi > Psikostimülan İlaçlar |
| Yerli ve Beşeri bir ilaçdır. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| Eşdeğer bir ilaç bulunamadı |
 |
Lösemi Kan Kanseri Lösemi, kan kanseridir ve vücudunun kan oluşturan dokularının hastalanması anlamına gelir. Birçok lösemi türü vardır; bazı lösemi türleri çocuklarda bazıları da yetişkinlerde sık görülür. |
 |
Diyabet Hastalığı Diyabet, insülin hormonu ile ilgili problemlerden kaynaklanan bir hastalıktır. |
 |
Mide Kanseri Mide kanseri genellikle mideyi tümüyle kaplayan ve mukus üretmekle görevli hücrelerde başlar. Bu kanser tipine adenokarsinom denir. |