JARDIANCE 25 mg film kapl� tablet K�sa �r�n Bilgisi
{ Empagliflozin }
1. BE�ER� TIBB� �R�N�N ADI
JARDIANCE 25 mg film kapl� tablet
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Her bir film kapl� tablet, 25 mg empagliflozin i�erir.
Yard�mc� maddeler
Her bir film kapl� tablette, 107,4 mg laktoz anhidre e�de�er laktoz monohidrat (inek s�t�nden elde edilir) bulunur.
Yard�mc� maddeler i�in B�l�m 6.1.'e bak�n�z.
3. FARMAS�T�K FORMU
Film kapl� tablet.
Oval, a��k sar� renkte, bikonveks, e�imli kenarl� film tablettir. Bir y�z�nde “S25” ve di�er y�z�nde Boehringer Ingelheim logosu bas�l�d�r (tablet uzunlu�u:11,1 mm, tablet geni�li�i: 5,6 mm).
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
JARDIANCE, eri�kinlerde, yeterli kontrol sa�lanamayan Tip-2 diyabetes mellitus tedavisinde, diyet ve egzersizle birlikte;
�ntolerans nedeniyle metformin kullan�m�n�n uygun bulunmad��� durumlarda monoterapi olarak
4.2. Pozoloji ve uygulama �ekli
Diyabet tedavisinde, monoterapi �eklinde veya di�er ila�larla kombinasyonu �eklinde ekleme tedavisi olarak �nerilen ba�lang�� dozu, g�nde bir kez 10 mg empagliflozindir. G�nde bir kez empagliflozin 10 mg dozu tolere eden eGFR de�erleri ≥60 mL/dk/1,73 m2 olan ve daha s�k� bir glisemik kontrole ihtiya� duyan hastalarda, doz, g�nde bir kez 25 mg'a y�kseltilebilir. Maksimum g�nl�k doz 25 mg'd�r (Bkz. A�a��daki bilgiler ve B�l�m 4.4).
Empagliflozin, bir s�lfonil�re veya ins�linle kombine �ekilde kullan�ld���nda, hipoglisemi riskini azaltmak i�in s�lfonil�re veya ins�lin dozunun d���r�lmesi d���n�lebilir (Bkz. B�l�m
4.5 ve B�l�m 4.8).
Uygulama �ekli:
Tabletler yiyeceklerle birlikte veya yiyeceklerden ayr� olarak al�nabilir. B�t�n olarak su ile yutulmal�d�r. E�er bir doz atlan�rsa hat�rlar hat�rlamaz al�nmal�d�r. Ayn� g�n i�inde iki doz al�nmamal�d�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
B�brek yetmezli�i:
Tip-2 diyabetes mellitus hastalar�nda, empagliflozinin glisemik etkilili�i renal fonksiyonlara ba�l�d�r. Standart tedaviye ek olarak kardiyovask�ler riskin azalt�lmas� i�in, eGFR 60 ml/dk/1,73 m2'nin alt�nda olan hastalarda g�nde bir kez 10 mg empagliflozin dozu kullan�lmal�d�r (Bkz. Tablo 1). Empagliflozinin glisemik d���r�c� etkilili�i, orta derecede b�brek yetmezli�i olan hastalarda azald��� ve ciddi b�brek yetmezli�i olan hastalarda muhtemelen bulunmad��� i�in, daha fazla glisemik kontrol gerekiyorsa, di�er anti- hiperglisemik ajanlar�n eklenmesi d���n�lmelidir. eGFR veya CrCl de�erlerine g�re doz ayarlama �nerileri i�in Tablo 1'e bak�n�z.
Tablo1: Doz ayarlama �nerileria
Endikasyon | eGFR [ml/dk/1,73 m²] veya CrCL [ml/dk] | Toplam g�nl�k doz |
Tip 2 diyabetes mellitus | ≥60 | 10 mg empagliflozin ile ba�lan�r
10 mg empagliflozini tolere eden ve ek glisemik kontrol gerektiren hastalarda, doz 25 mg empagliflozine art�r�labilir. |
45 ila <60 | 10 mg empagliflozin ile ba�lan�r
Halihaz�rda JARDIANCE kullanmakta olan hastalarda 10 mg empagliflozin ile devam edilir. | |
30 ila <45 | 10 mg empagliflozin ile ba�lan�r.
Halihaz�rda JARDIANCE kullanmakta olan hastalarda 10 mg empagliflozin ile devam edilir. | |
<30 | Empagliflozin �nerilmemektedir. |
a Bkz. B�l�m 4.4, 4.8, 5.1 ve 5.2
b Tip 2 diyabetes mellitus ve tan�mlanm�� kardiyovask�ler hastal��� olanlarda
Empagliflozin, son d�nem b�brek hastalar�nda (ESRD) veya diyalizdeki hastalarda kullan�lmamal�d�r. Bu hastalarda kullan�m� destekleyecek yeterli veri bulunmamaktad�r (Bkz. B�l�m 4.4, 5.1 ve 5.2).
Karaci�er yetmezli�i:
Hepatik yetmezli�i olan hastalarda doz ayarlamas� gerekli de�ildir. �iddetli hepatik yetmezli�i olan hastalarda empagliflozin maruziyeti artar. �iddetli karaci�er yetmezli�i olan hastalarda terap�tik deneyim s�n�rl�d�r, bu nedenle bu hastalarda kullan�m� �nerilmez (Bkz. B�l�m 5.2).
Pediyatrik pop�lasyon:
Empagliflozinin �ocuklarda ve ergenlerde etkilili�i ve g�venlili�i belirlenmemi�tir. Veri bulunmamaktad�r.
Geriyatrik pop�lasyon:
Ya� nedeniyle herhangi bir doz ayarlamas� gerekli de�ildir. 75 ya� ve �zerindeki hastalarda hacim azalmas� riskinin artt��� dikkate al�nmal�d�r (Bkz. B�l�m 4.4 ve 4.8).
4.3. Kontrendikasyonlar
Etkin madde
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Empagliflozin dahil, SGLT-2 inhibit�rleri ile tedavi edilen diabetes mellitus hastalar�nda, hayati tehlike olu�turan ve fatal vakalar� da i�eren ketoasidoz vakalar� seyrek olarak bildirilmi�tir. Baz� hastalarda ketoasidoz, kan glikoz de�erlerinde sadece orta d�zeyde (14 mmol/L'nin (250 mg/dL) alt�nda) bir y�kselme �eklinde ortaya ��kan atipik bir tablo �eklinde g�r�lm��t�r. Ketoasidoz vakalar�n�n ortaya ��kma olas�l���n�n, daha y�ksek empagliflozinin dozlar�yla art�p artmad��� bilinmemektedir.
Bulant�, kusma, anoreksi, abdominal a�r�, a��r� susama, nefes almakta g��l�k, konf�zyon, ola�and��� yorgunluk veya uyku hali gibi spesifik olmayan semptomlar�n g�r�lmesi halinde, ketoasidoz riski d���n�lmelidir. Bu semptomlar ortaya ��karsa, hasta, kan �ekeri d�zeyi ne olursa olsun, derhal ketoasidoz a��s�ndan de�erlendirilmelidir.
Ketoasidoz ��phesi bulunan veya ketoasidoz tan�s� konan hastalarda, empagliflozin tedavisi derhal sonland�r�lmal�d�r.
Maj�r cerrahi i�lemler veya akut ciddi hastal�klar nedeniyle hastaneye yat�r�lm�� hastalarda tedaviye ara verilmelidir. Bu hastalarda ketonlar�n izlenmesi �nerilmektedir. Kan keton d�zeylerinin �l��lmesi idrar �l��mlerine tercih edilmelidir. Keton d�zeyleri normale d�nd�kten ve hastan�n durumu stabilize edildikten sonra empagliflozin tedavisi yeniden ba�lat�labilir.
Empagliflozin tedavisine ba�lamadan �nce, hastan�n ge�mi�indeki ketoasidoza yatk�nl�k yaratan fakt�rler dikkate al�nmal�d�r.
Ketoasidoz riski daha y�ksek olan hastalar aras�nda, beta h�cre fonksiyonu rezervi d���k olan hastalar (�rne�in, C-peptid d�zeyi d���k tip-2 diyabet hastalar� veya eri�kinlerde latent otoimm�n diyabeti olanlar veya pankreatit �yk�s� olan hastalar), besin al�m�n�n k�s�tlanmas�na veya �iddetli dehidratasyona neden olan durumlara sahip hastalar, ins�lin dozlar� azalt�lm�� hastalar ve akut hastal�k, cerrahi veya alkol ba��ml�l���na ba�l� olarak ins�lin gereksinimleri artm�� hastalar bulunur. Bu hastalarda, SGLT-2 inhibit�rleri dikkatli bir �ekilde kullan�lmal�d�r.
Daha �nce SGLT-2 inhibit�r tedavisi uygulan�rken ketoasidoz g�r�len hastalarda, ba�ka bir tetikleyici fakt�r net olarak tan�mlan�p ��z�mlenmedik�e, SGLT-2 inhibit�r tedavisine yeniden ba�lanmas� �nerilmez.
JARDIANCE, Tip 1 diyabet hastalar�n�n tedavisi i�in kullan�lmamal�d�r. Klinik �al��malardan elde edilen veriler, ins�lin tedavisine ek olarak 10 mg ve 25 mg empagliflozin ile tedavi edilen Tip I diyabet hastalar�nda, plaseboya g�re DKA'n�n ortaya ��kma s�kl���n�n artt���n� g�stermi�tir.
Renal yetmezlik
Tip 2 diabetes mellitus endikasyonu i�in, eGFR<60 mL/dk/1,73 m2 veya CrCl<60 mL/dk olan hastalarda g�nl�k empagliflozin dozu 10 mg ile s�n�rl�d�r (Bkz. B�l�m 4.2). eGFR<30 mL/dk/1,73 m2 veya CrCl<30 mL/dk oldu�unda empagliflozin �nerilmemektedir.
Empagliflozin, son d�nem b�brek yetmezli�i hastalar�nda veya diyalizdeki hastalarda kullan�lmamal�d�r. Bu hastalarda kullan�m� destekleyecek yeterli veri bulunmamaktad�r (Bkz. B�l�m 4.2, 5.1 ve 5.2).
Renal fonksiyonlar�n a�a��daki �ekilde de�erlendirilmesi �nerilir:
Empagliflozin tedavisine ba�lamadan �nce ve tedavi s�ras�nda periyodik olarak, yani en az y�lda bir kez (Bkz. B�l�m 4.2, 5.1 ve 5.2).
Renal fonksiyonlar �zerinde negatif etkisi olabilecek ila�larla e� zamanl� herhangi bir
tedaviye ba�lamadan �nce.
Hacim azalmas� riski
SGLT-2 inhibit�rlerinin etki mekanizmas�na dayanarak, glikoz�riye e�lik eden osmotik di�rez, kan bas�nc�nda orta dereceli bir d����e yol a�abilir (Bkz. B�l�m 5.1). Bu nedenle, bilinen kardiyovask�ler hastal��� olan, ge�mi�inde hipotansiyon �yk�s� olup antihipertansif tedavi g�ren hastalar veya 75 ya� ve �zerindeki hastalar gibi, empagliflozine ba�l� kan bas�nc� d��mesinin risk olu�turabilece�i hastalarda dikkatli olunmal�d�r.
Empagliflozin tedavisi g�ren hastalarda, s�v� kayb�na yol a�an durumlar varsa (�rne�in, gastrointestinal hastal�klar), hacim durumunun (�rne�in, fiziksel muayene, kan bas�nc� �l��mleri, hematokrit dahil laboratuvar testleri) ve elektrolitlerin dikkatle izlenmesi gerekir. S�v� kayb� d�zeltilinceye kadar, empagliflozin tedavisinin ge�ici olarak durdurulmas� d���n�lmelidir.
Ya�l� hastalar
Empagliflozinin idrarda glikoz at�l�m� �zerindeki etkileri osmotik di�rez ile ili�kilidir, bu durum hidrasyon durumunu etkileyebilir. 75 ya� ve �zerindeki hastalar, hacim azalmas� a��s�ndan daha b�y�k risk alt�nda olabilirler. Hacim azalmas� ile ilgili advers etkiler, plasebo ile kar��la�t�r�ld���nda, empagliflozin ile tedavi edilen bu grup hastalarda daha fazla bildirilmi�tir (Bkz. B�l�m 4.8). Bu nedenle, s�v� azalmas�na yol a�abilecek ila�larla (�rne�in, di�retikler, ACE inhibit�rleri) birlikte kullan�lmas� halinde, bu hastalar�n s�v� al�mlar�na �zel bir dikkat g�sterilmelidir.
Komplike idrar yolu enfeksiyonlar�
Empagliflozin ile tedavi edilen hastalarda, piyelonefrit ve �rosepsis i�eren komplike idrar yolu enfeksiyonu vakalar� raporlanm��t�r (Bkz. B�l�m 4.8). Komplike idrar yolu enfeksiyonlar� olan hastalarda empagliflozin tedavisinin ge�ici olarak durdurulmas� d���n�lmelidir.
Perineumda nekrotizan fasiit (Fournier gangreni)
SGLT2 inhibit�r� kullanan diyabeti olan kad�n ve erkek hastalarda, perineumda nekrotizan
fasiit (Fournier gangreni olarak da bilinir) vakalar� bildirilmi�tir. Bu durum, seyrek ama ciddi ve potansiyel olarak hayat� tehdit eden bir olayd�r ve acil cerrahi giri�im ve antibiyotik tedavisini gerektirir.
Hastalar, genital veya perineal b�lgelerde a�r�, hassasiyet, eritem veya �i�lik ile birlikte ate� veya k�r�kl�k semptomlar�ndan baz�lar�n� birlikte hissetmeleri halinde doktora ba�vurmalar� konusunda uyar�lmal�d�r. �rogenital enfeksiyon veya perineal absenin, nekrotizan fasiitten �nce ortaya ��kabilece�i ak�lda tutulmal�d�r. E�er Fournier gangreninden ��phe edilirse, JARDIANCE tedavisi kesilmeli ve derhal tedavi (antibiyotikler ve cerrahi debridman dahil) ba�lanmal�d�r.
Alt ekstremite amputasyonlar�
Ba�ka bir SGLT2 inhibit�r� ile devam eden uzun d�nemli klinik �al��malarda alt ekstremite amputasyon (ba�l�ca, ayak parma��) vakalar�nda art�� g�zlenmi�tir. Bu durumun s�n�f etkisi olup olmad��� bilinmemektedir. T�m diyabet hastalar�nda oldu�u gibi, hastalar rutin olarak koruyucu ayak bak�m� �zerine kons�lte edilmelidir.
Hepatik hasar
Klinik �al��malarda empagliflozin ile hepatik hasar vakalar� bildirilmi�tir. Empagliflozin ile hepatik hasar aras�nda bir nedensellik ili�kisi tespit edilmemi�tir.
Hematokrit y�kselmesi
Empagliflozin tedavisi ile hematokritte y�kselme g�zlemlenmi�tir (Bkz. B�l�m 4.8).
Kronik b�brek hastal���
Alb�min�rinin e�lik etti�i veya etmedi�i kronik b�brek hastal��� (eGFR ≥30 mL/dk/1,73 m2) olan diyabet hastalar�nda diyabet tedavisi i�in empagliflozin ile deneyim mevcuttur. Alb�min�risi olan hastalar empagliflozin tedavisinden daha fazla yarar g�rebilir.
�nfiltratif hastal�k veya Takotsubo kardiyomiyopatisi
�nfiltratif hastal��� veya Takotsubo kardiyomiyopatisi olan hastalar �zel olarak �al���lmam��t�r. Bu nedenle, bu hastalarda etkinlik belirlenmemi�tir.
�drar laboratuvar de�erlendirmeleri
Etki mekanizmas�na ba�l� olarak, JARDIANCE alan hastalarda idrarda glikoz testi pozitif ��kacakt�r.
1,5-anhidroglusitol (1,5-AG) testi ile etkile�im
SGLT2 inhibit�rleri alan hastalarda glisemik kontrol�n de�erlendirilmesinde, 1,5-AG �l��mlerinin g�venilir olmamas� nedeniyle, glisemik kontrol�n 1,5-AG testi ile izlenmesi �nerilmez. Glisemik kontrol� izlemek i�in alternatif y�ntemlerin kullan�lmas� �nerilir.
Laktoz
Tabletler laktoz i�erir. Nadir kal�t�msal galaktoz intolerans�, Lapp laktaz yetmezli�i ya da glikoz- galaktoz malabsorbsiyon problemi olan hastalar�n bu ilac� kullanmamalar� gerekir.
Sodyum
JARDIANCE her “doz”unda 1 mmol (23 mg)'dan daha az sodyum i�erir; yani asl�nda “sodyum i�ermez”.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Di�retikler:
Empagliflozin, tiyazid ve loop di�retiklerin di�retik etkisine ek etki yapabilir, b�ylece dehidratasyon ve hipotansiyon riskini artt�rabilir (Bkz. B�l�m 4.4).
�ns�lin ve ins�lin salg�lat�c�lar:
�ns�lin ve s�lfonil�reler gibi ins�lin salg�lat�c�lar hipoglisemi riskini artt�rabilir. Bu nedenle, hipoglisemi riskini azaltmak i�in, empagliflozin ile kombine olarak kullan�ld���nda ins�lin veya ins�lin salg�lat�c�lar�n daha d���k dozda kullan�lmas� gerekebilir (Bkz. B�l�m 4.2, B�l�m 4.8).
Farmakokinetik etkile�imler:
In vitro veriler, insanlarda empagliflozinin primer metabolizma yolunun, �ridin 5´- difosfoglukuronoziltransferazlar olan UGT1A3, UGT1A8, UGT1A9 ve UGT2B7 arac�l��� ile glukuronidasyon oldu�unu d���nd�rmektedir. Empagliflozin bir insan uptake ta��y�c�s� olan OAT3, OATP1B1 ve OATP1B3 substrat�d�r, ancak OAT1 ve OCT2'nin substrat� de�ildir. Empagliflozin, P-glikoprotein (P-gp) ve meme kanseri diren� proteininin (BCRP) bir substrat�d�r.
Empagliflozinin, UGT enzimleri ve OAT3'�n bir inhibit�r� olan probenesid ile e� zamanl� uygulanmas�, empagliflozinin pik plazma konsantrasyonlar�nda (C) % 26 oran�nda art��la ve konsantrasyon zaman e�risi alt�nda kalan alanda (EAA) % 53 oran�nda y�kselmeyle sonu�lanm��t�r. Bu de�i�iklikler, klinik olarak anlaml� kabul edilmemi�tir.
UGT ind�ksiyonunun (�rne�in rifampisin veya fenitoin ile ind�ksiyon) empagliflozin �zerindeki etkisi �al���lmam��t�r. Etkililikte muhtemel bir azalma riski nedeniyle, UGT enzimlerinin bilinen ind�kleyicileriyle e� zamanl� uygulanmas� �nerilmez. Bu UGT enzimlerinin bir ind�kleyicisinin birlikte uygulanmas� gerekiyorsa, JARDIANCE'a yan�t� de�erlendirmek i�in glisemik kontrol�n izlenmesi uygundur.
Gemfibrozil (OAT3 ve OATP1B1/B3 ta��y�c�lar�n�n bir in vitro inhibit�r�) ile yap�lan bir etkile�im �al��mas�, e� zamanl� kullan�m� takiben, empagliflozin C de�erinin % 15 ve EAA de�erinin % 59 oran�nda artt���n� g�stermi�tir. Bu de�i�iklikler klinik olarak anlaml� kabul edilmemi�tir.
E� zamanl� rifampisin uygulanmas� ile OATP1B1/1B3 ta��y�c�lar�n�n inhibe edilmesi, empagliflozinin C de�erinde % 75 ve EAA de�erinde % 35 oran�nda art��la sonu�lanm��t�r. Bu de�i�iklikler klinik olarak anlaml� kabul edilmemi�tir.
Bir P-gp inhibit�r� olan verapamil ile birlikte veya verapamil olmaks�z�n uygulanmas� halinde, empagliflozin maruziyeti benzerdir. Bu durum, P-gp inhibisyonunun empagliflozin �zerinde klinik olarak anlaml� bir etkisinin olmad���n� g�stermi�tir.
Etkile�im �al��malar�, metformin, glimepirid, pioglitazon, sitagliptin, linagliptin, varfarin, verapamil, ramipril, simvastatin, torasemid ve hidroklorotiyazid ile e� zamanl� kullan�mlar�n�n, empagliflozinin farmakokineti�i �zerinde bir etkisinin olmad���n�
d���nd�rmektedir.
Empagliflozinin di�er ila�lar �zerindeki etkileri:
Empagliflozin renal lityum at�l�m�n� art�rabilir ve kan lityum seviyesi d��ebilir. Empagliflozin ba�lat�ld�ktan ve doz de�i�ikliklerinden sonra serum lityum konsantrasyonu daha s�k izlenmelidir. Lityum serum konsantrasyonunu izlemek i�in, hasta lityum re�ete eden doktora sevk edilmelidir.
In-vitro �al��malara dayanarak, empagliflozin, CYP450 izoformlar�n� inhibe etmez, inaktive etmez veya ind�klemez. Empagliflozin UGT1A1, UGT1A3, UGT1A8, UGT1A9 veya UGT2B7'yi inhibe etmez. Bu nedenle, maj�r CYP450 veya UGT izoformlar�n�n empagliflozin ile ve bu enzimlerin substratlar� ile e� zamanl� uygulanmas� sonucunda ila�–ila� etkile�mesi beklenmez.
Empagliflozin terap�tik dozlarda P-gp'yi inhibe etmez. In-vitro �al��malara dayanarak, empagliflozinin P-gp substratlar� ile etkile�mesi beklenmez. Bir P-gp substrat� olan digoksinin empagliflozin ile e� zamanl� kullan�lmas�, digoksinin Cde�erinde % 14 ve EAA de�erinde
% 6 oran�nda art��a yol a�m��t�r. Bu de�i�ikliklerin klinik olarak anlaml� olmad��� d���n�lm��t�r.
Empagliflozin, in vitro ko�ullarda, klinik olarak anlaml� plazma konsantrasyonlar�nda, OAT3, OATP1B1 ve OATP1B3 gibi insan uptake ta��y�c�lar�n� inhibe etmez ve bu uptake ta��y�c�lar�n�n substratlar� ile ila�-ila� etkile�mesi beklenmez.
Sa�l�kl� g�n�ll�lerde y�r�t�len etkile�im �al��malar�, empagliflozinin, metformin, glimepirid, pioglitazon, sitagliptin, linagliptin, simvastatin, varfarin, ramipril, digoksin, di�retikler ve oral kontraseptiflerin farmakokineti�i �zerinde klinik olarak anlaml� bir etkisi olmad���n� d���nd�rmektedir.
�zel pop�lasyonlara ili�kin ek bilgiler
�zel pop�lasyona ili�kin bir etkile�im �al��mas� yap�lmam��t�r.
Pediyatrik pop�lasyon:
Veri mevcut de�ildir.
4.6. Gebelik ve laktasyon
Gebelik kategorisi: C�ocuk do�urma potansiyeli bulunan kad�nlar / Do�um kontrol� (Kontrasepsiyon) JARDIANCE tedavisi s�ras�nda uygun bir do�um kontrol y�ntemi kullan�labilir. B�l�m 4.5'te a��kland��� gibi empagliflozinin, oral kontraseptiflerin farmakokineti�i �zerinde anlaml� bir klinik etkisi olmad��� d���n�lmektedir.
Gebelik d�nemi
JARDIANCE'�n gebe kad�nlarda kullan�m�na ili�kin yeterli veri yoktur. Hayvanlar �zerinde yap�lan �al��malar, gebelik / ve-veya / embriyonal / fetal geli�im / ve-veya / do�um / ve-veya
/ do�um sonras� geli�im �zerindeki etkiler bak�m�ndan yetersizdir.
Hayvan �al��malar� empagliflozinin ge� gestasyon d�neminde �ok s�n�rl� bir oranda plasentaya
ge�ti�ini g�stermektedir. Ancak bu �al��malar, erken embriyonik geli�im d�nemi a��s�ndan direkt veya indirekt zararl� bir etkiyi i�aret etmemektedir. Bununla birlikte, hayvan �al��malar�, postnatal geli�im �zerinde advers etkiler g�stermi�tir (Bkz. B�l�m 5.3). Bir �nlem olarak, gebelik d�neminde JARDIANCE kullan�m�ndan ka��n�lmal�d�r.
�nsanlara y�nelik potansiyel risk bilinmemektedir. JARDIANCE gerekli olmad�k�a gebelik d�neminde kullan�lmamal�d�r.
Laktasyon d�nemi
�nsanlarda empagliflozinin s�te ge�i�i ile ilgili bir veri bulunmamaktad�r. Hayvan �al��malar�ndan elde edilen mevcut toksikolojik veriler, empagliflozinin s�te ge�ti�ini g�stermi�tir. Yenido�an/infant a��s�ndan bir risk g�z ard� edilemez. JARDIANCE emzirme d�neminde kullan�lmamal�d�r.
�reme yetene�i/ Fertilite
JARDIANCE i�in insan fertilitesi ile ilgili bir �al��ma y�r�t�lmemi�tir. Hayvan �al��malar�, fertilite ile ilgili direkt veya indirekt zararl� bir etki g�stermemi�tir (Bkz. B�l�m 5.3).
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
JARDIANCE'�n ara� ve makine kullan�m� �zerindeki etkisi d���kt�r. Hastalar, ara� ve makine kullan�m� s�ras�nda, �zellikle JARDIANCE'� bir s�lfonil�re ve/veya ins�lin ile birlikte al�yorlarsa, ortaya ��kabilecek hipoglisemiden ka��nmak i�in gerekli �nlemleri almalar� konusunda uyar�lmal�d�rlar.
4.8. �stenmeyen etkiler
G�venlilik profili �zeti
Tip 2 diabetes mellitus
Empagliflozinin g�venlili�ini de�erlendirmek �zere tip-2 diyabeti olan toplam 15.582 hasta klinik �al��malara dahil edilmi�tir. Bu hastalardan 10.004 ki�i monoterapi olarak veya metformin, bir s�lfonil�re, pioglitazon, DPP-4 inhibit�rleri veya ins�lin ile birlikte empagliflozin alm��t�r.
18-24 hafta s�reli, 3.534 hastan�n dahil edildi�i 6 plasebo kontroll� �al��mada, 1.183 hasta plasebo ile, 2.351 hasta ise empagliflozin ile tedavi edilmi�tir. Empagliflozin ile tedavi edilen hastalardaki genel advers olay insidans� plasebo ile benzer bulunmu�tur. En s�k bildirilen advers reaksiyon, s�lfonil�re veya ins�lin ile birlikte kullan�ld���nda, hipoglisemidir (“se�ilmi� advers reaksiyonlar�n a��klamas�” b�l�m�ne bak�n�z).
![]()
Plasebo kontroll� �al��malarda empagliflozin alan hastalarda bildirilen ve sistem-organ s�n�f�na ve MedDRA tercih edilen terimlerine g�re s�n�fland�r�lan advers reaksiyonlar a�a��daki tabloda sunulmu�tur (Tablo 2).
![]()
Advers reaksiyonlar mutlak s�kl�k dikkate al�narak listelenmi�tir. S�kl�k dereceleri �u �ekilde tan�mlan�r: �ok yayg�n (≥1/10); yayg�n (≥1/100 ila <1/10); yayg�n olmayan (≥1/1.,000 ila
![]()
![]()
![]()
<1/100); seyrek (≥1/10.,000 ila <1/1.,000); �ok seyrek (<1/10.,000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Tablo 2: Plasebo kontroll� �al��malarda ve pazarlama sonras� deneyimde bildirilen advers reaksiyonlar�n �izelgeli listesi (MedDRA)
Sistem organ s�n�f� | �ok yayg�n | Yayg�n | Yayg�n olmayan | Seyrek | �ok seyrek |
Enfeksiyonlar ve |
| Vajinal |
| Perineumda |
|
enfestasyonlar | moniliazis, | nekrotizan | |||
| vulvovajinit, | fasiit | |||
| balanitis ve di�er | (Fournier | |||
| genital | gangreni) | |||
| enfeksiyonlar | ||||
| �drar yolu |
| |||
| enfeksiyonu |
| |||
| (piyelonefrit ve |
| |||
| �rosepsis dahil) |
| |||
Metabolizma ve | Hipoglisemi | Susama hissi | Diyabetik |
|
|
beslenme | (s�lfonil�re |
| ketoasidoz* | ||
hastal�klar� | veya ins�linle |
|
| ||
| birlikte |
|
| ||
| kullan�ld���nda) |
|
| ||
Vask�ler hastal�klar | Hacim azalmas� |
|
|
|
|
Gastrointestinal hastal�klar |
| Konstipasyon |
|
|
|
Deri ve deri alt� doku hastal�klar� |
| Pir�rit (jeneralize) D�k�nt� | �rtiker Anjiyo�dem |
|
|
B�brek ve idrar yolu hastal�klar� |
| �rinasyonda art�� | Diz�ri |
| T�b�lointerstis yel nefrit |
Ara�t�rmalar |
| Serum lipidlerinde y�kselme | Kan kreatinin d�zeyinde art��/ Glomer�ler Filtrasyon h�z�nda azalma Hematokrit de�erinde y�kselme |
|
|
*B�l�m 4.4'e bak�n�z
Se�ilmi� advers etkilerin a��klamas�
Hipoglisemi
Hipoglisemi s�kl���, ilgili �al��malardaki ge�mi� tedaviye ba�l�d�r ve empagliflozin ve plasebo i�in, monoterapi, metformine ekleme tedavisi, metformin ile birlikte veya birlikte olmayan pioglitazona ekleme tedavisi, linagliptin ve metformine ekleme tedavisi ve standart bak�m tedavisine ekleme tedavisinde benzer bulunmu�tur. Hipoglisemi s�kl���, daha �nce ila�la tedavi edilmemi� hastalarda, empagliflozinin metforminle kombinasyonu ile empagliflozin ve metformin bile�enlerinden her birinin ayr� ayr� uygulanmas� kar��la�t�r�ld���nda da benzer bulunmu�tur.
Metformin ve bir s�lfonil�re tedavisine ekleme tedavisi (empagliflozin 10 mg: % 16,1, empagliflozin 25 mg: % 11,5, plasebo: % 8,4), metformin ile birlikte veya birlikte olmayan ve bir s�lfonil�re ile birlikte veya birlikte olmayan bazal ins�lin tedavisine ekleme tedavisi (ins�linin ayarlanamad��� ilk 18 haftal�k tedavi d�neminde empagliflozin 10 mg: % 19,5, empagliflozin 25 mg: % 28,4, plasebo: % 20,6; 78 hafta s�reli �al��ma boyunca, empagliflozin 10 mg ve empagliflozin 25 mg: % 36,1, plasebo: % 35,3) ve metforminle birlikte veya birlikte olmayan MDI (�oklu doz enjeksiyon) ins�lin tedavisine ekleme tedavisi olarak kullan�ld���nda (ins�linin ayarlanamad��� ilk 18 haftal�k tedavi d�neminde empagliflozin 10 mg: % 39,8, empagliflozin 25 mg: % 41,3, plasebo: % 37,2; 52 hafta s�reli �al��ma boyunca, empagliflozin 10 mg: % 51,1, empagliflozin 25 mg: % 57,7, plasebo: % 58) s�kl�klarda art�� kaydedilmi�tir.
Plasebo ile kar��la�t�r�ld���nda, monoterapi, metformin tedavisine ekleme tedavisi, metformin ve bir s�lfonil�re tedavisine ekleme tedavisi ve metformin ile birlikte veya birlikte olmayan pioglitazon tedavisine ekleme tedavisi, linagliptin ve metfomin tedavisine ekleme tedavisi, standart bak�m tedavisine ilave olarak ve daha �nce ila�la tedavi edilmemi� hastalarda, metformin ile empagliflozin kombinasyonu tedavisi, empagliflozin ve metformin bile�enlerinden her birinin ayr� ayr� uygulanmas�yla yap�lan tedavi ile kar��la�t�r�ld���nda, maj�r hipoglisemide bir art�� g�zlenmemi�tir. Metforminle birlikte olan veya birlikte olmayan ve bir s�lfonil�re ile birlikte olan veya birlikte olmayan bazal ins�lin tedavisine ekleme tedavisi olarak kullan�ld���nda (ins�linin ayarlanamad��� ilk 18 haftal�k tedavi d�neminde, empagliflozin 10 mg: % 0, empagliflozin 25 mg: % 1,3, plasebo: % 0; 78 hafta s�reli �al��ma
boyunca, empagliflozin 10 mg: % 0, empagliflozin 25 mg: % 1,3, plasebo: % 0) ve metforminle birlikte veya birlikte olmayan MDI ins�line ekleme tedavisi olarak kullan�ld���nda (ins�linin ayarlanamad��� ilk 18 haftal�k tedavi d�neminde empagliflozin 10 mg: %0,5, empagliflozin 25 mg: %0,5, plasebo: %0,5 ve 52 hafta s�reli �al��ma boyunca
empagliflozin 10 mg: % 1,6, empagliflozin 25 mg: % 0,5, plasebo: % 1,6) s�kl�kta art�� kaydedilmi�tir.
Vajinal moniliazis, vulvovajinit, balanit ve di�er genital enfeksiyonlar, empagliflozin (empagliflozin 10 mg: % 4, empagliflozin 25 mg: % 3,9) ile tedavi edilen hastalarda plaseboya (% 1) g�re daha s�k bildirilmi�tir. Bu enfeksiyonlar, plasebo ile kar��la�t�r�ld���nda, empagliflozin ile tedavi edilen kad�nlarda daha s�k bildirilmi�tir. S�kl�ktaki farkl�l�klar erkeklerde daha az belirgindir. Genital sistem enfeksiyonlar� hafif veya orta �iddettedir.
�rinasyonda art��
�rinasyonda art�� (�nceden tan�mlanm�� terimler olan pollak�ri, poli�ri ve nokt�ri dahil), plaseboya (% 1,4) g�re, empagliflozin (empagliflozin 10 mg: % 3,5, empagliflozin 25 mg: %
3,3) ile tedavi edilen hastalarda daha y�ksek s�kl�kta g�zlenmi�tir. Artm�� �rinasyon genellikle hafif veya orta �iddettedir. Bildirilen nokt�ri s�kl���, empagliflozin ve plasebo i�in benzerdir (<% 1).
�drar yolu enfeksiyonu
Advers olay olarak bildirilen idrar yolu enfeksiyonunun genel s�kl���, empagliflozin 25 mg ve plasebo grubunda benzer (% 7 ve % 7,2) ve empagliflozin 10 mg grubunda daha y�ksek bulunmu�tur (% 8,8). Plaseboya benzer �ekilde, empagliflozin grubunda da idrar yolu enfeksiyonlar�, kronik veya tekrarlayan idrar yolu enfeksiyonu �yk�s� bulunan hastalarda daha s�k bildirilmi�tir. �drar yolu enfeksiyonlar�n�n �iddeti (hafif, orta, �iddetli), empagliflozin ve plasebo grubundaki hastalarda benzer olmu�tur. �drar yolu enfeksiyonlar� kad�nlarda, empagliflozin ile tedavi edilen grupta plaseboya g�re daha s�k bildirilirken, erkeklerde bir farkl�l�k g�zlenmemi�tir.
Hacim azalmas�
Hacim azalmas�n�n (�nceden tan�mlanm�� terimler olan kan bas�nc�nda (ambulatuvar) d��me, sistolik kan bas�nc�nda d��me, dehidratasyon, hipotansiyon, hipovolemi, ortostatik hipotansiyon ve senkop dahil) genel s�kl���, empagliflozin (empagliflozin 10 mg: % 0,6, empagliflozin 25 mg: % 0,4) ve plasebo (% 0,3) ile tedavi edilen hastalar aras�nda benzer bulunmu�tur. Hacim azalmas� olaylar�n�n s�kl���, empagliflozin 10 mg (% 2,3) veya 25 mg (% 4,3) ile tedavi edilen 75 ya� ve �zerindeki hastalarda, plasebo (% 2,1) ile tedavi edilenlere g�re artm��t�r.
Kan kreatinin d�zeyinde y�kselme/glomer�ler filtrasyon h�z�nda azalma
Kan kreatinin d�zeyinde y�kselme ve glomer�ler filtrasyon h�z�nda azalma olan hastalar�n genel s�kl���, empagliflozin ve plasebo ile tedavi edilen hastalar aras�nda benzer bulunmu�tur (kan kreatininde y�kselme: Empagliflozin 10 mg % 0,6, empagliflozin 25 mg % 0,1, plasebo
% 0,5; glomer�ler filtrasyon h�z�nda azalma: Empagliflozin 10 mg % 0,1, empagliflozin 25
mg % 0, plasebo % 0,3).
Empagliflozin ile tedavi edilen hastalarda, kreatinin d�zeyinde ba�lang��taki y�kselmeler ve tahmin edilen glomer�ler filtrasyon h�z�nda ba�lang��taki azalmalar, tedavinin devam� s�ras�nda genellikle ge�ici �zellikte veya ila� tedavisinin kesilmesinden sonra geri d�n��l� olmu�tur.
Bunlarla tutarl� olarak, EMPA-REG OUTCOME �al��mas�nda, empagliflozin ile tedavi edilen hastalarda ba�lang��ta eGFR d�zeyinde bir d���� (ortalama 3 mL/dk/1,73 m2 ) g�r�lm��t�r. Daha sonra, devam eden tedavi s�ras�nda eGFR korunmu�tur. Tedavinin kesilmesinden sonra ortalama eGFR ba�lang�� d�zeylerine d�nm��t�r, bu durum, akut hemodinamik de�i�ikliklerin bu b�brek fonksiyon de�i�ikliklerinde rol oynayabilece�ini d���nd�r�r.
Serum lipidlerinde art��
Plasebo kar��s�nda empagliflozin 10 mg ve 25 mg i�in ba�lang�ca g�re ortalama y�zde art��lar s�ras�yla �u �ekildedir: Total kolesterol, % 3,5'e kar�� % 4,9 ve % 5,7; HDL-kolesterol, % 0,4'e kar�� % 3,3 ve % 3,6; LDL-kolesterol, % 7,5'e kar�� % 9,5 ve % 10,0; trigliseritler, % 10,5'e kar�� % 9,2 ve % 9,9.
Hematokrit art���
Hematokritte ba�lang�ca g�re ortalama de�i�imler, plasebo i�in % 0,1 kar��s�nda empagliflozin
10 mg ve 25 mg i�in s�ras�yla % 3,4 ve % 3,6 olmu�tur. EMPA-REG OUTCOME
�al��mas�nda, tedavi kesildikten sonra 30 g�nl�k bir izleme d�nemini takiben hematokrit de�erleri ba�lang�� de�erlerine d�nm��t�r.
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e- posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz a��m� ve tedavisi
Semptomlar
Kontroll� klinik �al��malarda, sa�l�kl� g�n�ll�lerde empagliflozinin 800 mg'a kadar tek doz uygulamas� ve tip-2 diyabeti olan hastalarda g�nde 100 mg'a kadar �oklu doz uygulamas�, herhangi bir toksisiteye neden olmam��t�r. Empagliflozin, idrarla glikoz at�l�m�n� artt�rarak idrar hacminde art��a yol a�m��t�r. �drar hacminde g�zlenen art��, doza ba��ml� de�ildir ve klinik olarak anlaml� bulunmam��t�r. �nsanlarda 800 mg'�n �st�ndeki dozlarda bir deneyim yoktur.
Tedavi
Doz a��m� halinde, hastan�n klinik durumuna uygun bir tedavi ba�lanmal�d�r. Empagliflozinin hemodiyaliz ile uzakla�t�r�lmas� �al���lmam��t�r.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Sodyum-Glikoz Ko-Transporter 2 (SGLT2) �nhibit�rleri ATC kodu: A10BK03
Etki mekanizmas�:
Empagliflozin, geri d�n��l�, olduk�a potent (ICR1,3 nmol) ve se�ici yar��mal� bir sodyum- glikoz ko-transporter 2 (SGLT-2) inhibit�r�d�r. Empagliflozin, glikozun periferik dokulara ta��nmas� i�in �nemli olan di�er glikoz ta��y�c�lar�n� inhibe etmez ve ba��rsakta glikoz absorpsiyonundan sorumlu maj�r ta��y�c� olan SGLT-2 i�in SGLT-1'e g�re 5000 kat daha se�icidir. SGLT-2 b�brekte olduk�a fazla eksprese edilir, di�er dokulardaki ekspresyonu ise ya yoktur ya da �ok d���kt�r. As�l ta��y�c� olarak glikozun glomer�ler filtrattan, dola��ma reabsorbsiyonundan sorumludur. Tip-2 diyabeti ve hiperglisemisi olan hastalarda daha y�ksek miktarda glikoz filtre edilir ve geri emilir.
Empagliflozin, tip 2 diyabet hastalar�nda renal glikoz geri emilimini azaltarak glisemik kontrol� iyile�tirir. B�breklerden bu glik�retik mekanizma arac�l��� ile uzakla�t�r�lan glikoz miktar�, kan glikoz konsantrasyonuna ve GFR'ye ba��ml�d�r. Tip-2 diyabeti ve hiperglisemisi olan hastalarda SGLT-2 inhibisyonu, idrarda a��r� glikoz at�l�m�na yol a�ar. Ayr�ca, empagliflozin kullan�m�na ba�lanmas�, sodyum at�l�m�n� artt�r�r ve bu durum da osmotik di�rez ve intravask�ler hacmin azalmas� ile sonu�lan�r.
Tip-2 diyabeti olan hastalarda, empagliflozinin ilk dozundan hemen sonra idrarda glikoz at�l�m� artar ve 24 saat s�reli doz aral��� boyunca devam eder. 4 haftal�k tedavi d�neminin
sonunda, idrarda glikoz at�l�mda art�� sa�lanm��t�r ve bu miktar, ortalama yakla��k 78 g/g�n olmu�tur. Tip-2 diyabetli hastalarda idrarda glikoz at�l�m�n�n artmas�, plazma glikoz d�zeylerinin ani d��mesi ile sonu�lanm��t�r.
Empagliflozin hem a�l�k hem de tokluk plazma glikoz d�zeylerini iyile�tirir. Empagliflozinin etki mekanizmas� beta h�crelerinin fonksiyonundan ve ins�lin yola��ndan ba��ms�zd�r ve bu durum hipoglisemi riskinin d���k olmas�na katk�da bulunur. Homeostaz Model De�erlendirmesi- (HOMA-) dahil, beta h�cre fonksiyonunun yerini tutan g�stergelerde de iyile�me kaydedilmi�tir. Ayr�ca, idrar glikoz at�l�m�, v�cut ya� kayb� ve v�cut a��rl���n�n azalmas� ile ba�lant�l� olarak kalori kayb�n� tetikler. Empagliflozin ile g�zlenen glikoz�ri, di�rez ile seyreder, bu da kan bas�nc�n�n s�rekli bir �ekilde orta derecede d��mesine katk�da bulunabilir.
Empagliflozin ayr�ca sodyum geri emilimini azalt�r ve distal t�b�le ula�an sodyum miktar�n� art�r�r. Bu durum: t�b�loglomer�ler geri beslemesinin art�r�lmas� ve intraglomer�ler bas�nc�n azalt�lmas�, kalbin hem �n hem de ard y�k�n�n d���r�lmesi, sempatik aktivitenin azalt�lmas� ve d���k NT-proBNP de�erleri ve kardiyak yeniden modelleme , dolum bas�n�lar� ve diyastolik fonksiyon �zerindeki faydal� etkilerle kan�tland��� �zere sol ventrik�l duvar stresinin azalt�lmas� dahil ancak bunlarla s�n�rl� olmamak �zere birka� fizyolojik i�levi etkileyebilir.
Klinik etkililik ve g�venlilik Tip-2 diyabetes mellitus
Glisemik kontrol�n iyile�mesi ve kardiyovask�ler morbidite ve mortalitenin azalmas�, Tip 2 diyabet tedavisinin ayr�lmaz bir par�as�d�r.
12 �ift k�r, plasebo ve aktif kontroll� klinik �al��mada, Tip 2 diyabeti olan toplam 14.663 hastada glisemik etkililik ve kardiyovask�ler sonu�lar de�erlendirilmi�tir. Bu �al��malarda
9.295 hasta empagliflozin kullanm��t�r (empagliflozin 10 mg: 4.165 hasta, empagliflozin 25 mg: 5.130 hasta). 5 �al��man�n s�resi 24 haftad�r. Bu �al��malar�n uzatmalar�nda ve di�er �al��malarda hastalar, 102 haftaya kadar s�relerle empagliflozin kullanm��t�r.
Empagliflozinin monoterapi ve metformin, pioglitazon, bir s�lfonil�re, DPP-4 inhibit�rleri ve ins�lin ile kombine olarak kullan�lmas�, HbA1c, a�l�k plazma glikozu (APG), v�cut a��rl���, sistolik ve diyastolik kan bas�nc�nda klinik olarak anlaml� iyile�melere yol a�m��t�r. Empagliflozin 25 mg grubunda, empagliflozin 10 mg ve plasebo gruplar�na g�re, % 7'den daha d���k HbA1c d�zeyi hedefine ula�an hasta oran� daha y�ksektir ve daha az say�da hasta glisemik kurtarma tedavisine ihtiya� duymu�tur. Ba�lang�� HbA1c d�zeyinin daha y�ksek olmas� HbA1c d�zeyinde daha fazla d��me ile ili�kili bulunmu�tur. Ayr�ca, standart bak�m tedavisine ilave olarak uygulanan empagliflozin, Tip 2 diyabeti ve tan�mlanm�� kardiyovask�ler hastal��� olanlarda kardiyovask�ler mortaliteyi azaltm��t�r.
Empagliflozinin monoterapi olarak etkilili�i ve g�venlili�i, daha �nce tedavi edilmemi� hastalarda, �ift k�r, plasebo kontroll� ve aktif kontroll� 24 hafta s�reli bir �al��mada de�erlendirilmi�tir. Empagliflozin ile tedavi, plasebo ile kar��la�t�r�ld���nda, HbA1c d�zeyinde istatistiksel olarak anlaml� (p<0,0001) bir d����e (Tablo 3) ve APG de�erlerinde klinik olarak �nemli bir azalmaya yol a�m��t�r.
Ba�lang�� HbA1c de�eri ≥% 8,5 olan hastalar�n (N=201) �nceden tan�mlanm�� bir analizinde, HbA1c d�zeyinde ba�lang�ca g�re azalma oran�, empagliflozin 10 mg i�in % -1,44, 25 mg i�in
% -1,43, sitagliptin i�in % -1,04't�r ve plasebo grubunda % 0,01 oran�nda art�� olmu�tur.
Bu �al��man�n �ift k�r, plasebo kontroll� uzatmas�nda, HbA1c de�erinde azalma, kilo kayb� ve kan bas�nc�nda d��me 76 haftaya kadar devam etmi�tir.
Tablo 3: 24 hafta s�reli plasebo kontroll� empagliflozin monoterapisi �al��mas�n�n etkililik sonu�lar�a
| Plasebo | JARDIANCE | Sitagliptin | |
10 mg | 25 mg | 100 mg | ||
N | 228 | 224 | 224 | 223 |
HbA1c (%) | ||||
Ba�lang�� (ortalama) | 7,91 | 7,87 | 7,86 | 7,85 |
Ba�lang�ca g�re de�i�iklik | 0,08 | -0,66 | -0.78 | -0,66 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -0,74* (-0,9, -0,57) | -0,85* (-1,01, -0,69) | -0,73 (-0,88, -0,59) |
N | 208 | 204 | 202 | 200 |
Ba�lang�� HbA1c de�eri ≥% 7 olan hastalardan, HbA1c de�eri <% 7 hedefine ula�an hastalar�n y�zdesi |
12 |
35,3 |
43,6 |
37,5 |
N | 228 | 224 | 224 | 223 |
V�cut a��rl��� (kg) | ||||
Ba�lang�� (ortalama) | 78,23 | 78,35 | 77,8 | 79,31 |
Ba�lang�ca g�re de�i�iklik | -0,33 | -2,26 | -2,48 | 0,18 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -1,93* (-2,48, -1,38) | -2,15* (-2,7,-1,6) | 0,52 (-0,04, 1) |
N | 228 | 224 | 224 | 223 |
SBP (mmHg) | ||||
Ba�lang�� (ortalama) | 130,4 | 133 | 129,9 | 132,5 |
Ba�lang�ca g�re de�i�iklik | -0,3 | -2,9 | -3,7 | 0,5 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -2,6* (-5,2, -0) | -3,4* (-6, -0,9) | 0,8 (-1,4, 3,1) |
GA: G�ven Aral��� SBP: Sistolik Kan Bas�nc�
*p-de�eri<0,0001
Kombinasyon tedavisi
Metformin, s�lfonil�re, pioglitazon tedavisine ekleme tedavisi olarak empagliflozin Metformin, metformin ve bir s�lfonil�re veya metformin ile birlikte olan veya birlikte olmayan pioglitazon tedavisine ekleme tedavisi olarak empagliflozin kullan�lmas�, HbA1c d�zeylerinde ve v�cut a��rl���nda, plaseboya g�re, istatistiksel olarak anlaml� (p<0,0001) azalmalarla sonu�lanm��t�r (Tablo 4). Ayr�ca, APG de�erlerinde, sistolik ve diyastolik kan bas�nc�nda da, plaseboya g�re, klinik olarak anlaml� azalmalar g�r�lm��t�r.
Bu �al��malar�n �ift k�r, plasebo kontroll� uzatmalar�nda, HbA1c, v�cut a��rl��� ve kan
bas�nc�ndaki azalmalar 76. haftaya kadar devam etmi�tir.
Tablo 4: 24 hafta s�reli plasebo kontroll� �al��malar�n etkililik sonu�lar�a
Metformin tedavisine ekleme tedavisi | |||
| Plasebo | JARDIANCE | |
10 mg | 25 mg | ||
N | 207 | 217 | 213 |
HbA1c (%) | |||
Ba�lang�� (ortalama) | 7,9 | 7,94 | 7,86 |
Ba�lang�ca g�re de�i�iklik | -0,13 | -0,7 | -0,77 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -0,57* (-0,72, -0,42) | -0,64* (-0,79, -0,48) |
N | 184 | 199 | 191 |
Ba�lang�� HbA1c de�eri ≥% 7 olan hastalarda, HbA1c de�eri <% 7 hedefine ula�an hastalar�n y�zdesi |
12,5 |
37,7 |
38,7 |
N | 207 | 217 | 213 |
V�cut a��rl��� (kg) | |||
Ba�lang�� (ortalama) | 79,73 | 81,59 | 82,21 |
Ba�lang�ca g�re de�i�iklik | -0,45 | -2,08 | -2,46 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -1,63* (-2,17, -1,08) | -2,01* (-2,56, -1,46) |
N | 207 | 217 | 213 |
SBP (mmHg) | |||
Ba�lang�� (ortalama) | 128,6 | 129,6 | 130 |
Ba�lang�ca g�re de�i�iklik | -0,4 | -4,5 | -5,2 |
Plaseboya g�re farkl�l�k (% 95 GA) |
| -4,1* (-6,2, -2,1) | -4,8* (-6,9, -2,7) |
Metformin ve bir s�lfonil�re tedavisine ekleme tedavisi | |||
| Plasebo | JARDIANCE | |
10 mg | 25 mg | ||
N | 225 | 225 | 216 |
HbA1c (%) | |||
Ba�lang�� (ortalama) | 8,15 | 8,07 | 8,1 |
Ba�lang�ca g�re de�i�iklik | -0,17 | -0,82 | -0,77 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -0,64* (-0,79, -0,49) | -0,59* (-0,74, -0,44) |
N | 216 | 209 | 202 |
Ba�lang�� HbA1c de�eri ≥% 7 olan hastalarda, HbA1c de�eri <% 7 hedefine ula�an hastalar�n y�zdesi |
9,3 |
26,3 |
32,2 |
N | 225 | 225 | 216 |
V�cut a��rl���(kg) | |||
Ba�lang�� (ortalama) | 76,23 | 77,08 | 77,5 |
Ba�lang�ca g�re de�i�iklik | -0,39 | -2,16 | -2,39 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -1,76* (-2,25, -1,28) | -1,99* (-2,48, -1,5) |
N | 225 | 225 | 216 |
SBP (mmHg) | |||
Ba�lang�� (ortalama) | 128,8 | 128,7 | 129,3 |
Ba�lang�ca g�re de�i�iklik | -1,4 | -4,1 | -3,5 |
Plaseboya g�re farkl�l�k (% 95 GA) |
| -2,7 (-4,6, -0,8) | -2,1 (-4, -0,2) |
Pioglitazon +/- metformin tedavisine ekleme tedavisi | |||
| Plasebo | JARDIANCE | |
10 mg | 25 mg | ||
N | 165 | 165 | 168 |
HbA1c (%) | |||
Ba�lang�� (ortalama) | 8,16 | 8,07 | 8,06 |
Ba�lang�ca g�re de�i�iklik | -0,11 | -0,59 | -0,72 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -0,48* (-0,69, -0,27) | -0,61* (-0,82, -0,4) |
N | 155 | 151 | 160 |
Ba�lang�� HbA1c de�eri ≥% 7 olan hastalarda, HbA1c de�eri <% 7 hedefine ula�an hastalar�n y�zdesi |
7,7 |
24 |
30 |
N | 165 | 165 | 168 |
V�cut a��rl��� (kg) | |||
Ba�lang�� (ortalama) | 78,1 | 77,97 | 78,93 |
Ba�lang�ca g�re de�i�iklik | 0,34 | -1,62 | -1,47 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -1,95* (-2,64, -1,27) | -1,81* (-2,49, -1,13) |
N | 165 | 165 | 168 |
SBP (mmHg) | |||
Ba�lang�� (ortalama) | 125,7 | 126,5 | 126 |
Ba�lang�ca g�re de�i�iklik | 0,7 | -3,1 | -4 |
Plaseboya g�re farkl�l�k (% 95 GA) |
| -3,9 (-6,23, -1,5) | -4,7 (-7,08, -2,37) |
GA: G�ven Aral���
* p-de�eri <0,0001
Daha �nce ila� tedavisi almam�� hastalarda metformin ile kombinasyon
Daha �nce ila� tedavisi almam�� hastalarda empagliflozinin etkilili�ini ve g�venlili�ini de�erlendirmek i�in 24 hafta s�reli fakt�riyel tasar�ml� bir �al��ma y�r�t�lm��t�r. Metformin ile kombine empagliflozin tedavisi (g�nde iki kez verilen 5 mg ve 500 mg; 5 mg ve 1000 mg; 12,5 mg ve 500 mg, 12,5 mg ve 1000 mg), HbA1c de�erlerinde istatistiksel olarak anlaml� iyile�meler sa�lam�� (Tablo 54) ve APG de�erleri (bile�enlerin her biri ile tek tek kar��la�t�r�ld���nda) ve v�cut a��rl���nda (metforminle kar��la�t�r�ld���nda) daha fazla azalmaya neden olmu�tur.
Tablo 5: Metformin ve empagliflozin kombinasyonunu her bir bile�en ile kar��la�t�ran 24. haftadaki etkililik sonu�lar�a
| Empagliflozin 10 mg | Empagliflozin 25 mg | Metformin | |||||
| + Met 1000 mgc | + Met 2000 mgc | Met yok | + Met 1000 mgc | + Met 2000 mgc | Met yok | 1000 mg | 2000 mg |
N | 161 | 167 | 169 | 165 | 169 | 163 | 167 | 162 |
HbA1c (%) | ||||||||
Ba�lang�� (ortalama) | 8,68 | 8,65 | 8,62 | 8,84 | 8,66 | 8,86 | 8,69 | 8,55 |
Ba�lang�ca g�re de�i�iklik | -1,98 | -2,07 | -1,35 | -1,93 | -2,08 | -1,36 | -1,18 | -1,75 |
Kar��la�t�rmaya kar�� empa (% 95 GA) | -0,63* (-0,86, -0,4) | -0,72* (-0,96, -0,49) |
| -0,57* (-0,81, -0,34) | -0,72* (-0,95, -0,48) |
|
|
|
Kar��la�t�rmaya kar�� met (% 95 GA) | -0,79* (-1,03, -0,56) | -0,33* (-0,56, -0,09) |
| -0,75* (-0,98, -0,51) | -0,33* (-0,56, -0,1) |
|
|
|
Met = Metformin; empa = Empagliflozin
* HbA1c i�in p ≤0,0062
Metformin ve linagliptin tedavisi ile yeterli kontrol sa�lanamayan hastalarda empagliflozin Metformin ve 5 mg linagliptin tedavisi ile yeterli kontrol sa�lanamayan hastalarda, gerek empagliflozin 10 mg, gerekse empagliflozin 25 mg ile uygulanan tedavi, plaseboyla kar��la�t�r�ld���nda, HbA1c d�zeylerinde ve v�cut a��rl���nda istatistiksel olarak anlaml� (p<0,0001) azalmayla sonu�lanm��t�r (Tablo 6). Ek olarak, APG, sistolik ve diyastolik kan bas�nc�nda da, plaseboya g�re klinik olarak anlaml� d���� sa�lam��t�r.
Tablo 6: Metformin ve linagliptin 5 mg tedavisi ile yeterli kontrol sa�lanamayan hastalarda 24 hafta s�reli plasebo kontroll� bir �al��man�n etkililik sonu�lar�
Metformin ve linagliptin 5 mg tedavisine ekleme tedavisi | |||
| Plasebo | Empagliflozin | |
10 mg | 25 mg | ||
N | 106 | 109 | 110 |
HbA1c (%) | |||
Ba�lang�� (ortalama) | 7,96 | 7,97 | 7,97 |
Ba�lang�ca g�re de�i�iklik | 0,14 | -0,65 | -0,56 |
Plaseboya g�re farkl�l�k (% 95 GA) |
| -0,79* (-1,02, -0,55) | -0,7* (-0,93, -0,46) |
N | 100 | 100 | 107 |
Ba�lang�� HbA1c de�eri ≥% 7 olan hastalardan, HbA1c de�eri <% 7 hedefine ula�an hastalar�n y�zdesi |
17 |
37 |
32,7 |
N | 106 | 109 | 110 |
V�cut a��rl��� (kg) | |||
Ba�lang�� (ortalama) | 82,3 | 88,4 | 84,4 |
Ba�lang�ca g�re de�i�iklik | -0,3 | -3,1 | -2,5 |
Plaseboya g�re farkl�l�k (% 95 GA) |
| -2,8* (-3,5, -2,1) | -2,2* (-2,9, -1,5) |
N | 106 | 109 | 110 |
SBP (mmHg) | |||
Ba�lang�� (ortalama) | 130,1 | 130,4 | 131 |
Ba�lang�ca g�re de�i�iklik | -1,7 | -3 | -4,3 |
Plaseboya g�re farkl�l�k (% 95 GA) |
| -1,3 (-4,2, 1,7) | -2,6 (-5,5, 0,4) |
*p de�eri <0,0001
Ba�lang�� HbA1c de�eri % 8,5 veya daha y�ksek olan �nceden belirlenmi� bir hasta alt grubunda, HbA1c de�erinde 24. haftada ba�lang�ca g�re d��me oran�, plaseboya g�re, empagliflozin 10 mg ve empagliflozin 25 mg ile -% 1,3 olmu�tur (p<0,0001).
Metformine ekleme tedavisi olarak empagliflozin i�in 24 ayl�k veri - Glimepirid ile kar��la�t�rma
Tek ba��na metformin ile yeterli glisemik kontrol�n sa�lanamad��� hastalarda, empagliflozin 25 mg'�n etkililik ve g�venlili�ini glimepirid (g�nde 4 mg'a kadar) ile kar��la�t�ran bir �al��mada, g�nl�k empagliflozin tedavisi, glimeprid ile kar��la�t�r�ld���nda, HbA1c de�erinde ortalaman�n �zerinde bir azalma (Tablo 7) ve APG de�erinde klinik olarak anlaml� bir azalma ile sonu�lanm��t�r. G�nl�k empagliflozin tedavisi, glimepirid ile kar��la�t�r�ld���nda, v�cut a��rl���nda, sistolik ve diyastolik kan bas�nc�nda istatistiksel olarak anlaml� bir azalma sa�lam�� ve istatistiksel olarak anlaml� oranda daha az hastada hipoglisemik olaylar ortaya ��km��t�r (empagliflozin i�in % 2,5, glimepirid i�in % 24,2, p<0,0001).
Tablo 7: Metformine ekleme tedavisi olarak empagliflozin ile glimepiridi kar��la�t�ran bir aktif kontroll� �al��man�n 104. haftada etkililik sonu�lar�a
| Empagliflozin 25 mg | Glimepirid |
N | 765 | 780 |
HbA1c (%) | ||
Ba�lang�� (ortalama) | 7,92 | 7,92 |
Ba�lang�ca g�re de�i�iklik | -0,66 | -0,55 |
Glimepiride g�re farkl�l�k (% 97,5 GA) | -0,11* (-0,2, -0,01) |
|
N | 690 | 715 |
Ba�lang�� HbA1c ≥% 7 olan hastalardan, HbA1c <% 7 hedefine ula�an hastalar�n y�zdesi | 33,6 | 30,9 |
N | 765 | 780 |
V�cut a��rl���(kg) | ||
Ba�lang�� (ortalama) | 82,52 | 83,03 |
Ba�lang�ca g�re de�i�iklik | -3,12 | 1,34 |
Glimepiride g�re farkl�l�k (% 97,5 GA) | -4,46** (-4,87, -4,05) |
|
N | 765 | 780 |
SBP (mmHg) | ||
Ba�lang�� (ortalama) | 133,4 | 133,5 |
Ba�lang�ca g�re de�i�iklik | -3,1 | 2,5 |
Glimepiride g�re farkl�l�k (% 97,5 GA) | -5,6** (-7,-4,2) |
|
GA: G�ven Aral���
* Daha a�a�� olmad���n� (non-inferiority) kan�tlamak i�in p-de�eri<0,0001 ve ortalaman�n �zerinde i�in p-de�eri= 0,0153
** p-de�eri <0,0001
�ns�line ekleme tedavisi
�oklu g�nl�k dozda ins�lin tedavisine ekleme tedavisi olarak empagliflozin
Metformin tedavisi ile birlikte olan veya olmayan �oklu g�nl�k dozdaki ins�lin tedavisine ekleme tedavisi olarak kullan�lan empagliflozinin etkilili�i ve g�venlili�i, �ift k�r, plasebo kontroll�, 52 hafta s�reli bir �al��mada de�erlendirilmi�tir. �lk 18 hafta ve son 12 hafta boyunca, ins�lin dozu sabit tutulmu� ancak 19-40. haftalar aras�nda a�l�k glikoz d�zeyleri
<100 mg/dL'ye [5,5 mmol/L] ve tokluk glikoz d�zeyleri <140 mg/dL'ye [7,8 mmol/L] ula�mak �zere ayarlanm��t�r.
18. haftada empagliflozin, plaseboya g�re, HbA1c d�zeylerinde istatistiksel olarak anlaml� iyile�me sa�lam��t�r (Tablo 8).
52. haftada empagliflozin tedavisi, plaseboya g�re, HbA1c d�zeylerinde ve ins�lin kullan�m�nda anlaml� bir azalma sa�lam�� ve APG de�erinde d��me ve kilo kayb� ile sonu�lanm��t�r.
Tablo 8: Metformin ile birlikte veya birlikte olmayan �oklu g�nl�k dozlardaki ins�line ekleme tedavisi olarak kullan�lan empagliflozin i�in y�r�t�len plasebo kontroll� bir �al��mada 18. ve
52. haftadaki etkililik sonu�lar�
| Plasebo | JARDIANCE | |
10 mg | 25 mg | ||
N | 188 | 186 | 189 |
18. haftada HbA1c (%) | |||
Ba�lang�� (ortalama) | 8,33 | 8,39 | 8,29 |
Ba�lang�ca g�re de�i�iklik | -0,5 | -0,94 | -1,02 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -0,44* (-0,61, -0,27) | -0,52* (-0,69, -0,35) |
N | 115 | 119 | 118 |
52. haftada HbA1c (%) |
|
|
|
Ba�lang�� (ortalama) | 8,25 | 8,4 | 8,37 |
Ba�lang�ca g�re de�i�iklik | -0,81 | -1,18 | -1,27 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -0,38*** (-0,62, -0,13) | -0,46* (-0,7, -0,22) |
N | 113 | 118 | 118 |
52. haftada ba�lang�� HbA1c ≥% 7 olan hastalarda, HbA1c <% 7 hedefine ula�an hastalar�n y�zdesi |
26,5 |
39,8 |
45,8 |
N | 115 | 118 | 117 |
52. haftada insulin dozu (��/g�n) | |||
Ba�lang�� (ortalama) | 89,94 | 88,57 | 90,38 |
Ba�lang�ca g�re de�i�iklik | 10,16 | 1,33 | -1,06 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -8,83# (-15,69, -1,97) | -11,22** (-18,09, -4,36) |
N | 115 | 119 | 118 |
52. haftada v�cut a��rl��� (kg) | |||
Ba�lang�� (ortalama) | 96,34 | 96,47 | 95,37 |
Ba�lang�ca g�re de�i�iklik | 0,44 | -1,95 | -2,04 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -2,39* (-3,54, -1,24) | -2,48* (-3,63, -1,33) |
GA: G�ven Aral���
<140 mg/dl (7,8 mmol/l)) hedefine ula�mak i�in ins�lin dozu ayarlamas�na y�nelik hedefe y�nelik tedavi rejimi
* p-de�eri <0,0001
** p-de�eri= 0,0003
*** p-de�eri= 0,0005
# p-de�eri= 0,004
Bazal ins�lin tedavisine ekleme tedavisi olarak empagliflozin
Metformin ve/veya bir s�lfonil�re ile birlikte veya birlikte olmayan bazal ins�lin tedavisine ekleme tedavisi olarak empagliflozinin etkilili�i ve g�venlili�i, 78 hafta s�reli bir �ift k�r, plasebo kontroll� �al��mada de�erlendirilmi�tir. �lk 18 haftada ins�lin dozu sabit tutulmu�, ancak sonraki 60 hafta s�resince APG <110 mg/dL d�zeylerini sa�lamak �zere ayarlanm��t�r.
18. haftada empagliflozin, HbA1c d�zeylerini istatistiksel olarak anlaml� oranda iyile�tirmi�tir (Tablo 9).
78. haftada empagliflozin, plasebo ile kar��la�t�r�ld���nda, HbA1c de�erinde ve ins�lin kullan�m�nda istatistiksel olarak anlaml� bir azalma olu�turmu�tur. Ayr�ca empagliflozin, APG, v�cut a��rl��� ve kan bas�nc�nda da d���� sa�lam��t�r.
Tablo 9: Metformin veya bir s�lfonil�re ile birlikte veya birlikte olmayan bazal ins�lin tedavisine ekleme tedavisi olarak kullan�lan empagliflozin i�in y�r�t�len bir plasebo kontroll� �al��man�n 18. ve 78. haftalardaki etkililik sonu�lar�a
| Plasebo | Empagliflozin 10 mg | Empagliflozin 25 mg |
N | 125 | 132 | 117 |
18. haftada HbA1c (%) |
|
|
|
Ba�lang�� (ortalama) | 8,1 | 8,26 | 8,34 |
Ba�lang�ca g�re de�i�iklik | -0,01 | -0,57 | -0,71 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -0,56* (-0,78, -0,33) | -0,7* (-0,93, -0,47) |
N | 112 | 127 | 110 |
78. haftada HbA1c (%) |
|
|
|
Ba�lang�� (ortalama) | 8,09 | 8,27 | 8,29 |
Ba�lang�ca g�re de�i�iklik | -0,02 | -0,48 | -0,64 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -0,46* (-0,73, -0,19) | -0,62* (-0,9, -0,34) |
N | 112 | 127 | 110 |
78. haftada bazal ins�lin dozu (��/g�n) |
|
|
|
Ba�lang�� (ortalama) | 47,84 | 45,13 | 48,43 |
Ba�lang�ca g�re de�i�iklik | 5,45 | -1,21 | -0,47 |
Plaseboya g�re farkl�l�k (% 97,5 GA) |
| -6,66** (-11,56, -1,77) | -5,92** (-11, -0,85) |
GA: G�ven Aral���
* p-de�eri <0,0001
** p-de�eri <0,025
Renal yetmezli�i olan hastalar, 52 hafta s�reli plasebo kontroll� veriler
Renal yetmezli�i olan hastalarda antidiyabetik tedaviye ekleme tedavisi olarak empagliflozinin etkilili�i ve g�venlili�i, 52 hafta s�reli, �ift k�r plasebo kontroll� bir �al��mada de�erlendirilmi�tir. Empagliflozin tedavisi, plasebo ile kar��la�t�r�ld���nda, 24. haftada, HbA1c d�zeylerinde istatistiksel olarak anlaml� bir azalma (Tablo 10) ve APG de�erlerinde klinik olarak anlaml� bir iyile�me ile sonu�lanm��t�r. HbA1c, v�cut a��rl��� ve kan bas�nc�ndaki iyile�meler 52. haftaya kadar devam etmi�tir.
Tablo 10: Renal bozuklu�u olan tip-2 diyabet hastalar�nda plasebo kontroll� bir empagliflozin �al��mas�nda 24. hafta sonu�lar�a
| Plasebo | Empagliflozin 10 mg | Empagliflozin 25 mg | Plasebo | Empagliflozin 25 mg |
eGFR ≥60 - <90 mL/dk/1,73 m² | eGFR ≥ 30 - <60 mL/dk/1,73 m² | ||||
N | 95 | 98 | 97 | 187 | 187 |
HbA1c (%) | |||||
Ba�lang�� (ortalama) | 8,09 | 8,02 | 7,96 | 8,04 | 8,03 |
Ba�lang�ca g�re de�i�iklik | 0,06 | -0,46 | -0,63 | 0,05 | -0,37 |
Plaseboya g�re farkl�l�k (% 95 GA) |
| -0,52* (-0,72, -0,32) | -0,68* (-0,88, -0,49) |
| -0,42* (-0,56, -0,28) |
N | 89 | 94 | 91 | 178 | 175 |
Ba�lang�� HbA1c ≥% 7 olan hastalarda, HbA1c <% 7 hedefine ula�an hastalar�n y�zdesi | 6,7 | 17 | 24,2 | 7,9 | 12 |
N | 95 | 98 | 97 | 187 | 187 |
V�cut a��rl��� (kg) | |||||
Ba�lang�� (ortalama) | 86 | 92,05 | 88,06 | 82,49 | 83,22 |
Ba�lang�ca g�re de�i�iklik | -0,33 | -1,76 | -2,33 | -0,08 | -0,98 |
Plaseboya g�re farkl�l�k (% 95 GA) |
| -1,43 (-2,09, -0,77) | -2 (-2,66, -1,34) |
| -0,91 (-1,41, -0,41) |
N | 95 | 98 | 97 | 187 | 187 |
SBP (mmHg) | |||||
Ba�lang�� (ortalama) | 134,69 | 137,37 | 133,68 | 136,38 | 136,64 |
Ba�lang�ca g�re de�i�iklik | 0,65 | -2,92 | -4,47 | 0,4 | -3,88 |
Plaseboya g�re farkl�l�k (% 95 GA) |
| -3,57 (-6,86, -0,29) | -5,12 (-8,41, -1,82) |
| - 4,28 (-6,88, -1,68) |
GA: G�ven Aral���
* p <0,0001
Kardiyovask�ler sonu�lar
�ift k�r, plasebo kontroll� EMPA-REG OUTCOME �al��mas�, tip 2 diyabeti ve tan�mlanm�� kardiyovask�ler hastal��� olan hastalarda, standart bak�m tedavisine ek olarak uygulanan empagliflozin 10 mg ve empagliflozin 25 mg'�n havuzda toplanm�� dozlar�n� plasebo ile kar��la�t�rm��t�r. Toplam 7.020 hasta tedavi edilmi� (empagliflozin 10 mg: 2.345, empagliflozin 25 mg: 2.342, plasebo: 2.333) ve medyan 3,1 y�l s�reyle takip edilmi�tir. Ortalama ya� 63, ortalama HbA1c % 8,1'dir ve hastalar�n % 71,5'i erkektir. Ba�lang��ta hastalar�n % 74'� metformin, % 48'i ins�lin ve % 43'� bir s�lfonil�re ile tedavi edilmi�tir.
Hastalar�n yakla��k yar�s�n�n (% 52,2) eGFR de�eri 60-90 mL/dk/1,73 m2, % 17,8'nin 45-60 mL/dk/1,73 m2 ve % 7,7'sinin 30-45 mL/dk/1,73 m2 olarak belirlenmi�tir.
12. haftada HbA1c'de uyarlanm�� ortalamadaki (SE) iyile�me, plasebo grubu i�in ba�lang��taki % 0,11 (0,02) de�eri ile kar��la�t�r�ld���nda, empagliflozin 10 mg grubunda % 0,65 (0,02) ve empagliflozin 25 mg grubunda % 0,71 (0,02) olarak g�zlenmi�tir. �lk 12 haftadan sonra glisemik kontrol, ara�t�rmac� tedaviden ba��ms�z olarak optimize edilmi�tir. Bu nedenle etki 94. haftada azalt�lm��, HbA1c de�erindeki uyarlanm�� ortalama iyile�me, plasebo grubunda % 0,08 (0,02), empagliflozin 10 mg grubunda % 0,5 (0,02) ve empagliflozin 25 mg
grubunda % 0,55 (0,02) bulunmu�tur.
Empagliflozin, birincil kombine sonlan�m noktas� olan kardiyovask�ler �l�m, fatal olmayan miyokard enfarkt�s� veya fatal olmayan inmenin �nlenmesinde , plaseboya g�re �st�n bulunmu�tur. Tedavi etkisi, kardiyovask�ler �l�mde anlaml� bir azalma ile sa�lanm��, fatal olmayan miyokard enfarkt�s� veya fatal olmayan inmede anlaml� bir de�i�iklik olmam��t�r. Kardiyovask�ler �l�mdeki azalma, empagliflozin 10 mg ve empagliflozin 25 mg i�in kar��la�t�r�labilir bulunmu�tur (�ekil 1) ve genel ya�am s�resindeki iyile�me ile de do�rulanm��t�r (Tablo 11). EMPA-REG OUTCOME �al��mas�nda empagliflozinin kardiyovask�ler �l�m, fatal olmayan miyokard enfarkt�s� veya fatal olmayan inmede birincil birle�ik sonlan�m noktas� �zerindeki etkisi, glisemik kontrolden veya renal fonksiyonundan (eGFR) b�y�k �l��de ba��ms�z olmu�tur ve genel olarak 30 ml/dakika/1,73m2 eGFR de�erine kadar inen eGFR kategorileri aras�nda tutarl� olmu�tur.
Kardiyovask�ler mortaliteyi �nlemedeki etkilili�i, empagliflozin ile birlikte DPP-4 inhibit�r� kullanan hastalarda veya siyah �rktan olanlarda tam olarak belirlenmemi�tir, ��nk� bu gruplar�n EMPA-REG OUTCOME �al��mas�ndaki temsil edilme d�zeyleri s�n�rl�d�r.
Tablo 11: Birincil bile�ik sonlan�m noktas� i�in tedavi etkisi, bile�enleri ve mortalitea
| Plasebo | Empagliflozin |
N | 2.333 | 4.687 |
�lk KV �l�m, fatal olmayan MI veya fatal olmayan inme olay�na kadar ge�en s�re N (% ) | 282 (12,1) | 490 (10,5) |
Tehlike oran�, plaseboya kar�� (% 95,.02 GA)* |
| 0,86 (0,74, 0,99) |
�st�nl�k i�in p de�eri |
| 0,0382 |
KV �l�m N (% ) | 137 (5,9) | 172 (3,7) |
Tehlike oran�, plaseboya kar�� (% 95 GA) |
| 0,62 (0,49, 0,77) |
p de�eri |
| <0,0001 |
Fatal olmayan MI N (% ) | 121 (5,2) | 213 (4,5) |
Tehlike oran�, plaseboya kar�� (% 95 GA) |
| 0,87 (0,7, 1,09) |
p de�eri |
| 0,2189 |
Fatal olmayan inme N (% ) | 60 (2,6) | 150 (3,2) |
Tehlike oran�, plaseboya kar�� (% 95 GA) |
| 1,24 (0,92, 1,67) |
p de�eri |
| 0,1638 |
T�m nedenlere ba�l� mortalite N (% ) | 194 (8,3) | 269 (5,7) |
Tehlike oran�, plaseboya kar�� (% 95 GA) |
| 0,68 (0,57, 0,82) |
p de�eri |
| <0,0001 |
KV olmayan mortalite N (% ) | 57 (2,4) | 97 (2,1) |
Tehlike oran�, plaseboya kar�� (% 95 GA) |
| 0,84 (0,6, 1,16) |
KV: Kardiyovask�ler, MI: Miyokard enfarkt�s�
* �al��madan elde edilen veriler bir ara analize dahil edildi�i i�in, anlaml�l�k i�in 0,0498'den d���k bir p de�erine kar��l�k gelen bir iki yanl� % 95,02 g�ven aral��� uygulanm��t�r.
�ekil 1 - EMPA-REG OUTCOME �al��mas�nda kardiyovask�ler �l�me kadar ge�en
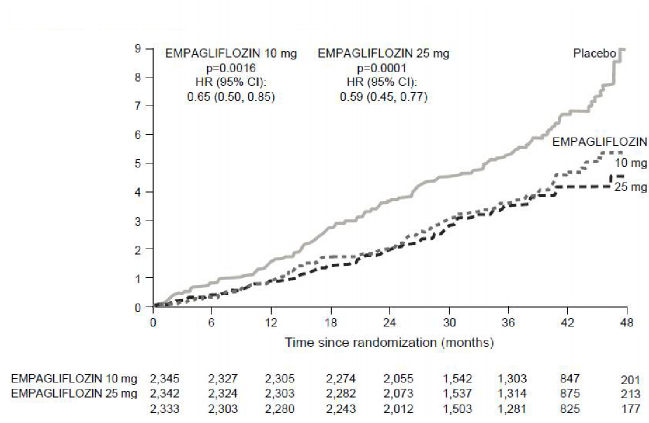
Her bir empagliflozin dozuna kar��l�k plasebo
Risk alt�nda olanlar�n say�s�
Plasebo
Randamizasyondan itibaren ge�en zaman (ay)
EMPAGLIFLOZIN 10 mg EMPAGLIFLOZIN 25 mg
p=0,0016 p=0,0001
TO (% 95 GA) TO (% 95 GA)
0,55 (0,50, 0,85) 0,59 (0,45, 0,77)
Plasebo
T�bbi durum ya�ayan hasta (%)
zaman
Hastaneye yat�� gerektiren kalp yetmezli�i
EMPA-REG OUTCOME �al��mas�nda, empagliflozin plasebo ile kar��la�t�r�ld���nda, hastaneye yat�� gerektiren kalp yetersizli�i riskini d���rm��t�r (empagliflozin % 2,7, plasebo
% 4,1; TO (Tehlike Oran�) 0,65, % 95 GA = 0,5, 0,85).
Nefropati
EMPA-REG OUTCOME �al��mas�nda, ilk nefropati olay�na kadar olan s�re boyunca, empagliflozine (% 12,7) k�yasla plasebo (18,8) i�in TO 0,61 (% 95 GA 0,53, 0,7) olmu�tur.
Ayr�ca, empagliflozin (% 49,7) plaseboya k�yasla (% 28,8), ba�lang��ta makroalbumin�risi olan hastalarda, daha y�ksek (TO 1,82, % 95 GA 1,40, 2,37) s�rekli normo- veya mikro- alb�min�ri olu�umu g�stermi�tir.
A�l�k plazma glikozu
4 adet plasebo kontroll� �al��mada, empagliflozin monoterapisi veya metformin, pioglitazon veya metformin + bir s�lfonil�re tedavisine ekleme tedavisi, APG de�erinde ba�lang�ca g�re, plasebo (7,4 mg/dL [0,41 mmol/L]) ile kar��la�t�r�ld���nda, empagliflozin 10 mg i�in -20,5
mg/dL [-1,14 mmol/L], empagliflozin 25 mg i�in -23,2 mg/dL [-1,29 mmol/L] ortalama de�i�iklikle sonu�lanm��t�r. Bu etki 24 haftadan sonra g�zlenmi�tir ve 76 hafta s�resince
devam etmi�tir.
2 saatlik tokluk glikozu
Metformin veya metformin + bir s�lfonil�re tedavisine ekleme olarak empagliflozin tedavisi,
24. haftada, 2 saatlik tokluk glikoz d�zeylerinde (yemek tolerans testi) klinik olarak anlaml� bir d��me sa�lam��t�r (metformine ekleme: Plasebo +5,9 mg/dL, empagliflozin 10 mg: -46 mg/dL, empagliflozin 25 mg: -44,6 mg/dL, metformin + bir s�lfonil�re tedavisine ekleme: Plasebo -2,3 mg/dL, empagliflozin 10 mg: -35,7 mg/dL, empagliflozin 25 mg: -36,6 mg/dL).
Ba�lang�� HbA1c>% 10 (y�ksek) olan hastalar
3 Faz III �al��mas�n�n �nceden tan�mlanan havuzda toplanm�� analizinde, �iddetli hiperglisemisi olan (N=184, ortalama ba�lang�� HbA1c % 11,15) hastalarda, a��k etiketli empagliflozin 25 mg tedavisi, 24. haftada, HbA1c de�erinde, ba�lang�ca g�re % 3,27 oran�ndaki klinik olarak anlaml� bir azalma ile sonu�lanm��t�r. Bu �al��malara plasebo veya empagliflozin 10 mg kollar� dahil edilmemi�tir.
V�cut a��rl���
Plasebo-kontrollu d�rt �al��man�n �nceden tan�mlanm��, havuzda toplanm�� analizinde, empagliflozin tedavisi, 24. haftada v�cut a��rl���nda azalma ile sonu�lanm�� (plasebo i�in - 0,24 kg, empagliflozin 10 mg i�in -2,04 kg ve empagliflozin 25 mg i�in -2,26 kg) ve 52. haftaya kadar (plasebo i�in -0,16 kg, empagliflozin 10 mg i�in -1,96 kg ve empagliflozin 25 mg i�in - 2,25 kg) devam etmi�tir.
Kan bas�nc�
Empagliflozinin etkilili�i ve g�venlili�i, �e�itli antidiyabetik tedavi alan ve en fazla 2 antihipertansif ilac� kullanan kan bas�nc� y�ksek tip-2 diyabetli hastalarda 12 hafta s�reyle y�r�t�len �ift k�r, plasebo kontroll� bir �al��mada de�erlendirilmi�tir. Empagliflozinin g�nde bir kez uygulanmas� ile yap�lan tedavi, HbA1c de�erinde ve ambulatuvar kan bas�nc� izlenmesi ile tespit edilen 24 saatlik ortalama sistolik ve diyastolik kan bas�nc�nda istatistiksel olarak anlaml� bir iyile�me ile sonu�lanm��t�r (Tablo 12). Empagliflozin tedavisi, otururken �l��len SBP (Sistolik Kan Bas�nc�) ve DBP (Diyastolik Kan Bas�nc�)'de azalmalar sa�lam��t�r.
Tablo 12: Kan bas�nc� kontrol alt�nda olmayan tip-2 diyabetli hastalarda, empagliflozinin plasebo kontroll� bir �al��mas�nda 12. haftadaki etkililik sonu�lar�a
| Plasebo | JARDIANCE | |
10 mg | 25 mg | ||
N | 271 | 276 | 276 |
12. haftada HbA1c (%) | |||
Ba�lang�� (ortalama) | 7,9 | 7,87 | 7,92 |
Ba�lang�ca g�re de�i�iklik | 0,03 | -0,59 | -0,62 |
Plaseboya g�re farkl�l�k (% 95 GA) |
| -0,62* (-0,72, -0,52) | -0,65*
(-0.,75, -0,55) |
12. haftada 24 saatlik SBP | |||
Ba�lang�� (ortalama) | 131,72 | 131,34 | 131,18 |
Ba�lang�ca g�re de�i�iklik | 0,48 | -2,95 | -3,68 |
Plaseboya g�re farkl�l�k (% 95 GA) |
| -3,44* (-4,78, -2,09) | -4,16* (-5,5, -2,83) |
12. haftada 24 saatlik DBP | |||
Ba�lang�� (ortalama) | 75,16 | 75,13 | 74,64 |
Ba�lang�ca g�re de�i�iklik | 0,32 | -1,04 | -1,4 |
Plaseboya g�re farkl�l�k5 (% 95 GA) |
| -1,36** (-2,15, -0,56) | -1,72* (-2,51, -0,93) |
GA: G�ven aral���
* p-de�eri <0,0001
** p-de�eri <0,001
Plasebo kontroll� 4 �al��man�n �nceden tan�mlanm�� havuzda toplanm�� analizinde, empagliflozin tedavisi, 24. haftada, plasebo (-0,5 mmHg) ile kar��la�t�r�ld���nda, sistolik kan bas�nc�nda (empagliflozin 10 mg: -3,9 mmHg; empagliflozin 25 mg: -4,3 mmHg) ve diyastolik
kan bas�nc�nda (plasebo: -0,5 mmHg; empagliflozin 10 mg: -1,8 mmHg; empagliflozin 25 mg:
-2 mmHg) azalma ile sonu�lanm�� ve bu etki 52. haftaya kadar devam ettirilmi�tir.
Pediyatrik pop�lasyon
Avrupa �la� Ajans� (European Medicine Agency-EMA), JARDIANCE ile tip-2 diyabeti olan pediyatrik pop�lasyonun bir veya daha fazla alt grubunda yap�lan �al��malar�n sonu�lar�n� sunma zorunlulu�unu ertelemi�tir (pediyatrik kullan�m ile ilgili bilgiler i�in bkz. B�l�m 4.2).
Avrupa �la� Ajans� (European Medicine Agency-EMA), JARDIANCE ile kalp yetmezli�i olan pediyatrik pop�lasyonun alt gruplar�nda yap�lan �al��malar�n sonu�lar�n� sunma zorunlulu�unu ertelemi�tir (pediyatrik kullan�m ile ilgili bilgiler i�in bkz. B�l�m 4.2).
5.2. Farmakokinetik �zellikler
Genel �zelliklerEmilim:
Empagliflozinin farmakokineti�i, sa�l�kl� g�n�ll�lerde ve tip-2 diyabetli hastalarda ayr�nt�l� olarak tan�mlanm��t�r. Oral uygulamadan sonra, empagliflozin, ortalama t1,5 saatte meydana gelen pik plazma konsantrasyonlar� ile h�zl� bir �ekilde emilir. Sonras�nda, plazma konsantrasyonlar� h�zl� bir da��l�m faz� ile bifazik tarzda azal�r ve terminal faz� g�receli olarak yava�t�r. Kararl� durum ortalama plazma EAA ve Cde�erleri, g�nde bir kez empagliflozin 10 mg i�in 1870 nmol.saat/L ve 259 nmol/L ve empagliflozin 25 mg i�in 4740 nmol.saat/L ve 687 nmol/L'dir. Empagliflozinin sistemik maruziyeti dozla orant�l� �ekilde artar. Empagliflozinin tek doz ve kararl� durum farmakokinetik parametreleri benzerdir, bu durum zamana g�re lineer farmakokineti�i d���nd�r�r. Sa�l�kl� g�n�ll�lerle tip-2 diyabetli hastalar aras�nda empagliflozin farmakokineti�i a��s�ndan klinik olarak anlaml� bir farkl�l�k yoktur.
Y�ksek oranda ya�l� ve y�ksek kalorili bir yemekten sonra empagliflozin 25 mg al�nmas�, hafif oranda daha d���k bir maruziyetle sonu�lanm��t�r. A�l�k ko�ullar� ile kar��la�t�r�ld���nda, EAA yakla��k % 16 oran�nda ve Cyakla��k % 37 oran�nda azalm��t�r. Yiyeceklerin empagliflozin farmakokineti�i �zerinde g�zlenen etkileri, klinik olarak anlaml� kabul edilmez,
empagliflozin yiyeceklerle birlikte veya ayr� olarak kullan�labilir.
Da��l�m:
G�r�n�r kararl� durum da��l�m hacmi, pop�lasyon farmakokinetik analizlerine dayanarak, 73,8 L olarak tahmin edilmi�tir. Sa�l�kl� g�n�ll�lere oral [14C]-empagliflozin ��zeltisi uygulanmas�n� takiben k�rm�z� kan h�cre par�alanmas� yakla��k % 37 ve plazma protein ba�lanmas� % 86 bulunmu�tur.
Biyotransformasyon:
Empagliflozinin insan plazmas�nda maj�r bir metaboliti belirlenmemi�tir ve en belirgin metabolitleri 3 glukuronid konjugat�d�r (2-,3- ve 6-O glukuronid). Her metabolitin sistemik maruziyeti, ilaca ba�l� toplam materyalin % 10'undan daha azd�r. In vitro �al��malar, empagliflozinin insanlardaki birincil metabolizma yolunun, �ridin 5-difosfo-glukuronosil transferazlar UGT2B7, UGT1A3, UGT1A8 ve UGT1A9 arac�l��� ile glukuronidasyon oldu�unu d���nd�rmektedir.
Eliminasyon:
Pop�lasyon farmakokinetik analizlere dayanarak, empagliflozinin g�r�n�r terminal yar�lanma �mr� 12,4 saat olarak tahmin edilmi�tir, g�r�n�r oral klerensi 10,6 L/saattir. Empagliflozin oral klerensi a��s�ndan ki�iler aras� ve rezid�el de�i�kenlikler s�ras� ile % 39,1 ve % 35,8'dir. G�nde bir kez verilen dozla, empagliflozinin kararl� durum plazma konsantrasyonlar�na 5. dozla ula��lm��t�r. Yar� �mr� ile uyumlu olarak, kararl� durumda, plazma EAA a��s�ndan % 22'ye kadar birikim g�zlenmi�tir. Oral [14C]-empagliflozin ��zeltisinin sa�l�kl� g�n�ll�lere uygulanmas�ndan sonra, ila�la ili�kili radyoaktivitenin yakla��k % 96's�, fe�es (% 41) veya idrarla (% 54) at�lm��t�r. Fe�este geri kazan�lan ila�la ili�kili radyoaktivitenin b�y�k bir k�sm� de�i�memi� ana ila� olmu�tur ve idrarla at�lan ila�la ili�kili radyoaktivitenin yakla��k yar�s� de�i�memi� ana ila� olmu�tur.
Hastalardaki karakteristik �zellikler
Renal yetmezlik
![]()
Hafif, orta ve �iddetli renal bozuklu�u olan hastalarda (eGFR<30 - <90 mL/dk/1,.73 m2) ve b�brek yetmezli�i /son d�nem b�brek yetmezli�i (ESRD) olan hastalarda, renal fonksiyonlar� normal olan hastalarla kar��la�t�r�ld���nda, empagliflozinin EAA de�erleri s�ras�yla, yakla��k olarak, % 18, % 20, % 66 ve % 48 oran�nda artm��t�r. Empagliflozinin pik plazma d�zeyleri, orta dereceli renal bozuklu�u ve b�brek yetmezli�i/ESRD hastalar� ile renal fonksiyonlar� normal olan hastalar aras�nda benzerdir. Empagliflozinin pik plazma d�zeyleri, hafif ve �iddetli renal bozuklu�u olan hastalarda, renal fonksiyonlar� normal olan hastalara g�re, kabaca % 20 oran�nda daha y�ksektir. Pop�lasyon farmakokinetik analizi, empagliflozinin g�r�n�r oral klerensinin, eGFR de�erindeki azalma ile azald���n�, bunun da ila� maruziyetinde y�kselmeye neden oldu�unu g�stermi�tir.
Hepatik yetmezlik
Child-Pugh s�n�fland�rmas�na g�re hafif, orta ve �iddetli hepatik bozuklu�u olan hastalarda empagliflozinin EAA de�eri, hepatik fonksiyonlar� normal olan hastalara g�re, s�ras�yla yakla��k % 23, % 47 ve % 75, Cde�eri ise yakla��k % 4, % 23 ve % 48 artm��t�r.
V�cut kitle indeksi
Pop�lasyon farmakokinetik analizlerine dayanarak, v�cut kitle indeksinin empagliflozin farmakokineti�i �zerine klinik olarak anlaml� bir etkisi olmam��t�r. Bu analizde EAA
de�erinin, BMI 25 kg/m2 olanlara g�re, BMI 30, 35, ve 45 kg/m2 olan ki�ilerde s�ras� ile %
5,82, % 10,4 ve % 17,3 daha d���k oldu�u tahmin edilmi�tir.
Cinsiyet
Pop�lasyon farmakokinetik analizlerine dayanarak, cinsiyetin empagliflozin farmakokineti�i �zerine klinik olarak anlaml� bir etkisi yoktur.
Irk
Pop�lasyon farmakokinetik analizlerinde, EAA de�erinin, BMI 25 kg/m2 olan Asyal�larda, ayn� BMI de�erine sahip Asyal� olmayanlarla kar��la�t���nda, % 13,5 oran�nda daha y�ksek oldu�u tahmin edilmi�tir.
Geriyatrik pop�lasyon
Pop�lasyon farmakokinetik analizlerine dayanarak, ya��n empagliflozinin farmakokineti�i �zerine klinik olarak anlaml� bir etkisi olmam��t�r.
Pediyatrik pop�lasyon
Bir pediyatrik Faz 1 �al��mas�, empagliflozinin (5 mg, 10 mg ve 25 mg) farmakokineti�ini ve farmakodinami�ini, Tip 2 diabetes mellitus hastas� �ocuklar ve ≥10 - <18 ya�lar�ndaki adolesanlarda ara�t�rm��t�r. G�zlenen farmakokinetik ve farmakodinamik yan�tlar, eri�kin g�n�ll�lerden elde edilen bilgilerle tutarl� bulunmu�tur.
5.3. Klinik �ncesi g�venlilik verileri
G�venlilik farmakolojisi, genotoksisite, fertilite ve erken embriyonik geli�imle ilgili klasik
�al��malardaki klinik d��� veriler insanlar i�in �zel bir tehlike g�stermemi�tir.
K�peklerde ve kemirgenlerde yap�lan uzun d�nem toksisite �al��malar�nda, empagliflozinin klinik dozunun 10 kat�na e�it veya daha y�ksek maruziyetlerinde toksisite belirtileri g�zlenmi�tir. Toksisitenin �o�u, v�cut a��rl��� ve v�cut ya� d�zeyinde azalma, yiyecek t�ketiminde art��, diyare, dehidratasyon, serum glikoz d�zeyinde azalmay� da kapsayan idrarda glikoz kayb� ve elektrolit dengesizlikleri, protein metabolizmas�ndaki ve glikoneogenezdeki art��la g�r�len di�er serum proteinlerinde y�kselme, poli�ri ve glikoz�ri gibi idrar de�i�iklikleri ve b�breklerle baz� yumu�ak ve vask�ler dokular�n mineralizasyonunu da i�eren mikroskobik de�i�iklikler ile ili�kili ikincil farmakoloji ile uyumludur. Baz� t�rlerde, empagliflozinin 25 mg ile ili�kili olarak, empagliflozinin klinik EAA maruziyetinin yakla��k
4 kat�nda, b�brekler �zerindeki, abart�l� farmakolojik etkilerin mikroskobik kan�tlar� g�zlenmi�tir. Bu kan�tlar aras�nda, t�b�ler dilatasyon ve t�b�ler ve pelvik mineralizasyon bulunur.
Empagliflozin genotoksik de�ildir.
2 y�l s�reli bir karsinojenite �al��mas�nda empagliflozin, di�i s��anlarda, maksimum klinik empagliflozin EAA maruziyetinin 72 kat fazlas�na kar��l�k gelen, 700 mg/kg/g�n d�zeyindeki en y�ksek doza kadar, t�m�r insidans�n� artt�rmam��t�r. Erkek s��anlarda, en y�ksek dozda, mezenterik lenf nodlar�nda, tedaviye ba�l� benign vask�ler proliferatif lezyonlar� (hemanjiyomlar) g�zlenmi�tir. Ancak empagliflozinin maksimum klinik maruziyetinin yakla��k 26 kat�na kar��l�k gelen 300 mg/kg/g�n dozda bu etki g�zlenmemi�tir. S��anlarda, 300 mg/kg/g�n ve �zerindeki dozlarda, testislerde interstisyel h�cre t�m�rleri daha y�ksek insidansta g�zlenmi�, empagliflozinin maksimum klinik maruziyetinin yakla��k 18 kat�na
kar��l�k gelen 100 mg/kg/g�n dozda ise g�zlenmemi�tir. Her iki t�m�r de s��anlarda yayg�nd�r ve insanlarla ili�kili olmas� beklenmez.
Empagliflozin, di�i farelerde, maksimum klinik maruziyetinin yakla��k 62 kat�na kar��l�k gelen 1000 mg/kg/g�n doza kadar t�m�r insidans�n� artt�rmam��t�r. Erkek farelerde 1000 mg/kg/g�n dozda renal t�m�rleri ind�klemi�tir, ancak empagliflozinin maksimum klinik maruziyetinin yakla��k 11 kat�na kar��l�k gelen 300 mg/kg/g�n dozda bu ind�kleme g�r�lmemi�tir. Bu t�m�rlerin etki mekanizmas�, erkek farelerin renal patolojiye do�al predispozisyonuna ve bir metabolik yola�a ba�l� olup, insanlarda kar��l��� yoktur. Erkek farelerdeki renal t�m�rler insanlarla ili�kili bulunmam��t�r.
�nsanlarda, terap�tik dozlardan sonraki maruziyetin yeterli derecedeki maruziyet miktarlar�nda, empagliflozinin fertilite veya erken embriyolojik geli�me �zerinde herhangi bir advers etkisi olmam��t�r. Organogenez d�nemi s�ras�nda verilen empagliflozinin teratojen etkisi saptanmam��t�r. Sadece maternal olarak toksik dozlarda verildi�inde empagliflozin, s��anlarda kaburga kemiklerinde e�rili�e ve tav�anlarda embriyofetal kay�plarda art��a neden olmu�tur.
S��anlarda yap�lan pre- ve postnatal toksisite �al��malar�nda, empagliflozine maksimum klinik maruziyetin yakla��k 4 kat�ndaki maternal maruziyetlerde, yavrular�n kilo al�m�nda azalma g�zlenmi�tir. Empagliflozine maksimum klinik maruziyete e�de�er bir sistemik maruziyette b�yle bir etki g�zlenmemi�tir. Bu bulgular�n insanlarla ili�kisi belirsizdir.
S��anlarda yap�lan bir juvenil toksisite �al��mas�nda, postnatal 21. g�nden postnatal 90. g�ne kadar empagliflozin uygulanmas� halinde, juvenil s��anlarda sadece maksimum klinik doz olan 25 mg'�n yakla��k 11 kat�na kar��l�k gelen 100 mg/kg/g�n dozlarda advers olmayan, minimal- hafif dereceli renal t�b�ler ve pelvik dilatasyon g�r�lm��t�r. �la�s�z 13 haftal�k bir d�nem sonras�nda bu bulgular ortadan kalkm��t�r.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Laktoz monohidrat (inek s�t�nden elde edilmi�tir) Mikrokristalin sel�loz
Hidroksipropil sel�loz Kroskarmelloz sodyum Kolloidal anhidr silika Magnezyum stearat
Hipromelloz
Titanyum dioksid (E171) Talk
Makrogol (400)
Demir oksit, sar� (E 172)
6.2. Ge�imsizlikler
Uygulanabilir de�ildir.
6.3. Raf �mr�
36 ay
6.4. Saklamaya y�nelik �zel tedbirler
25ºC'nin alt�nda oda s�cakl���nda saklan�r.
6.5. Ambalaj�n niteli�i ve i�eri�i
PVC/aluminyum perfore birim doz blisterler.
Piyasaya 30 film tabletlik ambalaj b�y�kl�kleri ile sunulur.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj At�klar�n�n Kontrol� Y�netmeli�i” ne uygun olarak imha edilmelidir.
 Mide Kanseri
Mide kanseri genellikle mideyi t�m�yle kaplayan ve mukus �retmekle g�revli h�crelerde ba�lar. Bu kanser tipine adenokarsinom denir.
Mide Kanseri
Mide kanseri genellikle mideyi t�m�yle kaplayan ve mukus �retmekle g�revli h�crelerde ba�lar. Bu kanser tipine adenokarsinom denir. |
 A��r� Alkol Kullan�m�, Alkolizm
Alkol ba��ml�l���, alkol kullan�m� ve alkol sorunlar� aras�ndaki fark� a��klamak g��t�r.
�rne�in, ge�mi�te alkol kullanm�� olan bir kimsenin mutlaka alkol ba��ml�s� olmas�
gerekmez.
A��r� Alkol Kullan�m�, Alkolizm
Alkol ba��ml�l���, alkol kullan�m� ve alkol sorunlar� aras�ndaki fark� a��klamak g��t�r.
�rne�in, ge�mi�te alkol kullanm�� olan bir kimsenin mutlaka alkol ba��ml�s� olmas�
gerekmez. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| EMPACROS | 8699514097846 | 581.24TL |
| EMPAFEL | 8699540030763 | 612.22TL |
| EMPALFO | 8680030190333 | 612.22TL |
| GLIFLOMED | 8680199007862 | 612.22TL |
| GLYZARDA | 8680080000415 | 612.22TL |
| Di�er E�de�er �la�lar |
 |
Tiroid Kanseri En s�k g�r�len tiroid kanseri t�r� olan papiller tiroid kanseri, t�m tiroid kanserlerinin yakla��k %70'ini olu�turur. |
 |
HIV ve Aids HIV, Human Immunodeficiency Virus’d�r (�nsanlarda Ba����kl�k Sistemini Bozan Vir�sd�r). Bu vir�s AIDS hastal���na sebep olur. |
 |
Ast�m Ast�ml� ki�ilerin akci�erlerindeki hava borular� (bron�lar) hassast�r. Bu ki�iler belirli tetikleyici fakt�rlere maruz kald�klar�nda, hava borular� nefes almalar�n� g��le�tirecek �ekilde daral�r. |
�LA� GENEL B�LG�LER�
Boehringer Ingelheim �la� Tic. A.�.
| Geri �deme Kodu | A16755 |
| Sat�� Fiyat� | 637.87 TL [ 1 Dec 2025 ] |
| �nceki Sat�� Fiyat� | 637.87 TL [ 24 Nov 2025 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699693090126 |
| Etkin Madde | Empagliflozin |
| �thal ( ref. �lke : Yunanistan ) ve Be�eri bir ila�d�r. |