KARDOES PREMIX 2500 mg/250 ml INFUXYONLUK ��zelti K�sa �r�n Bilgisi
{ Esmolol Hcl }
1. BE�ER� TIBB� �R�N�N ADI
KARDOES PREMIX 2500 mg/250 ml �nf�zyonluk ��zelti Steril
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Esmolol hidroklor�r: 10 mg/ml (Her bir 250 ml'lik torba 2500 mg esmolol hidroklor�r i�erir).
Yard�mc� maddeler
Bu t�bbi �r�n her bir torbas�nda yakla��k 30,45 mmol (ya da 700 mg) sodyum i�erir. Yard�mc� maddeler i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
�nf�zyon i�in ��zelti.
Berrak, renksiz ila a��k sar� renkte ��zelti.
��zeltinin pH's� 4,5 - 5,5 aras� ve ozmolaritesi yakla��k 300 mOsm/l'dir.
Beta blok�rler s�n�f reaksiyonu olarak baz� durumlarda ps�riyazise ya da ps�riyaziste k�t�le�meye neden olabilir.
Uygulama seti tak�l�r; setle birlikte verilen talimata uyularak uygulamaya ba�lan�r.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Supraventrik�ler ta�ikardi (preeksitasyon sendromlar� hari�) veya d�zeltilebilir nedenlere ba�l� olmayan sin�s ta�ikardisi
KARDOES perioperatif, postoperatif d�nemdeki atriyal fibrillasyon ve atriyal flutter'li hastalarda ventrik�l h�z�n�n s�ratli kontrol�nde ya da ventrik�l h�z�n�n k�sa etkili bir ajanla k�sa s�reli kontrol�n�n istendi�i di�er durumlarda endikedir.
KARDOES ayr�ca hekim taraf�ndan h�zlanm�� kalp h�z�n�n �zel bir giri�imle d�zeltilmesi karar� verilmi�se, kompanse olmam�� sin�s ta�ikardisi durumunda da endikedir.
Perioperatif d�nemde olu�an ta�ikardi ve hipertansiyon
KARDOES, trakeal ent�basyon ve anestezi ind�ksiyonu s�ras�nda, cerrahi prosed�r devam ederken, anesteziden ��karken ve postoperatif d�nemde g�r�len ta�ikardi ve hipertansiyonda hekim taraf�ndan b�yle �zel bir giri�imle d�zeltilmesi karar� verilmi�se endikedir.
KARDOES 18 ya��na kadar olan �ocuklarda kullan�m i�in endike de�ildir (Bkz. B�l�m 4.2). KARDOES kronik ayarlamalarda kullan�lmak i�in tasarlanmam��t�r.
4.2. Pozoloji ve uygulama �ekli
Pozoloji / uygulama s�kl��� ve s�resi
KARDOES PREMIX 2500 mg/250 mL inf�zyon ��zeltisi, intraven�z uygulama i�in �nerilen, kullan�ma haz�r 10 mg/mL izo-ozmotik bir ��zeltidir.
Supraventrik�ler ta�ikardi (preeksitasyon sendromlar� hari�) veya kompanse olmam�� sin�s ta�ikardisinin tedavisinde dozlama
KARDOES'in supraventrik�ler ta�iaritmilerdeki dozu a�a��daki ak�� �emas�nda g�sterildi�i gibi ayr� ayr� titre edilmelidir:
Tedavi Ba�lama ve �dame i�in Ak�� �emas�
![]()
1 dakika boyunca 500 mikrogram/kg/dakika y�kleme dozu inf�zyonunun ard�ndan 4 dakika boyunca 50 mikrogram/kg/dk idame inf�zyonu
![]() Yan�t
Yan�t
�nf�zyonun 50 mikrogram/kg/dakika olarak devam�
5 dakika i�inde yetersiz cevap
1 dakika boyunca 500 mikrogram/kg/dakika dozunun tekrarlanmas�
�dame inf�zyonunun 4 dakika boyunca 100 mikrogram/kg/dakikaya ��kar�lmas�
![]()
![]() Yan�t
Yan�t
�nf�zyonun 100 mikrogram/kg/dakika
olarak devam�
5 dakika i�inde yetersiz cevap
1 dakika boyunca 500 mikrogram/kg/dakika dozunun tekrarlanmas�
�dame inf�zyonunun 4 dakika boyunca 150 mikrogram/kg/dakikaya ��kar�lmas�
![]()
![]() Yan�t
Yan�t
�nf�zyonun 150 mikrogram/kg/dakika
olarak devam�
Yetersiz cevap
1 dakika boyunca 500 mikrogram/kg/dakika dozunun tekrarlanmas�
�dame inf�zyonunun 4 dakika boyunca 200 mikrogram/kg/dakikaya ��kar�lmas� ve bu dozla devam�
Y�kleme dozu
Hemodinamik cevaba (kalp at�m h�z�, kan bas�nc�) ba�l� olarak y�kleme dozu ayar� gerekebilir.
�dame dozu
Devaml� ve basamakl� dozlama i�in etkili idame dozu 50 ila 200 mikrogram/kg/dk'd�r. 25 mikrogram/kg/dakika doz kullan�labilir. �stenen hemodinamik cevaba ba�l� olarak idame dozu ayarlamas� gerekli olabilir. 200 mikrogram/kg/dk'dan y�ksek dozlar�n uygulanmas�, kalp at�� h�z�n�n d���r�lmesinde k���k bir ek etki sa�lamakta ve advers reaksiyonlar�n oran�n� artt�rmaktad�r.
KARDOES'in farkl� hasta a��rl�klar� i�in uygulanacak olan y�kleme dozu ve idame dozlar�, Tablo 1 ve Tablo 2'de s�ras�yla g�sterilmi�tir:
Tablo 1
500 mcg/kg/dakikal�k bir BA�LANGI� Y�KLEME DOZU i�in gerekli olan 10 mg/mL KARDOES hacmi
Hacim (mL) | Hasta a��rl��� (kg) | ||||||||
40 | 50 | 60 | 70 | 80 | 90 | 100 | 110 | 120 | |
2 | 2,5 | 3 | 3,5 | 4 | 4,5 | 5 | 5,5 | 6 | |
Tablo 2
12,5 ve 300 mcg/kg/dakika aras�ndaki inf�zyon h�zlar�nda �DAME DOZLARI sa�lamak i�in gerekli olan 10 mg/mL KARDOES hacmi
Hasta a��rl��� (kg) | �nf�zyon Doz H�z� | ||||||
12,5 mcg/kg/ dk | 25 mcg/kg/ dk | 50 mcg/kg/ dk | 100 mcg/kg/ dk | 150 mcg/kg/ dk | 200 mcg/kg/ dk | 300 mcg/kg/ dk | |
Doz h�z�na ula�mak i�in saatte uygulanacak miktar (mL/saat) | |||||||
40 | 3 mL/saat | 6 mL/saat | 12 mL/saat | 24 mL/saat | 36 mL/saat | 48 mL/saat | 72 mL/saat |
50 | 3,75 mL/saat | 7,5 mL/saat | 15 mL/saat | 30 mL/saat | 45 mL/saat | 60 mL/saat | 90 mL/saat |
60 | 4,5 mL/saat | 9 mL/saat | 18 mL/saat | 36 mL/saat | 54 mL/saat | 72 mL/saat | 108 mL/saat |
70 | 5,25 mL/saat | 10,5 mL/saat | 21 mL/saat | 42 mL/saat | 63 mL/saat | 84 mL/saat | 126 mL/saat |
80 | 6 mL/saat | 12 mL/saat | 24 mL/saat | 48 mL/saat | 72 mL/saat | 96 mL/saat | 144 mL/saat |
90 | 6,75 mL/saat | 13,5 mL/saat | 27 mL/saat | 54 mL/saat | 81 mL/saat | 108 mL/saat | 162 mL/saat |
100 | 7,5 mL/saat | 15 mL/saat | 30 mL/saat | 60 mL/saat | 90 mL/saat | 120 mL/saat | 180 mL/saat |
110 | 8,25 mL/saat | 16,5 mL/saat | 33 mL/saat | 66 mL/saat | 99 mL/saat | 132 mL/saat | 198 mL/saat |
120 | 9 mL/saat | 18 mL/saat | 36 mL/saat | 72 mL/saat | 108 mL/saat | 144 mL/saat | 216 mL/saat |
1 mL KARDOES, 10 mg esmolol'e e�ittir.
�stenen kalp at�� h�z� veya g�venlilik son noktas�na (�rne�in d���k kan bas�nc�) yakla��ld���nda, y�kleme dozu atlanmal� (uygulanmamal�) ve idame inf�zyonundaki artan doz 50 mikrogram/kg/dakika'dan 25 mikrogram/kg/dakika'ya veya daha d���k bir seviyeye d���r�lmelidir. Gerekirse, titrasyon ad�mlar� aras�ndaki aral�k 5 dakikadan 10 dakikaya artt�r�labilir.
Perioperatif ta�ikardi ve hipertansiyon
Perioperatif ta�ikardi ve hipertansiyon i�in dozaj rejimi a�a��daki gibi de�i�ebilir:
�ntraoperatif tedavi i�in – anestezi s�ras�nda acil kontrol gerekti�inde:
15 ila 30 saniyede verilen 80 mg'l�k bir bolus enjeksiyonu takiben 150 mikrogram/kg/dakikal�k inf�zyon verilir. �nf�zyon h�z� 300 mikrogram/kg/dakika'ya kadar gereken �ekilde titre edilir. Farkl� hasta a��rl�klar� i�in gereken inf�zyon hacmi Tablo 2'de verilmi�tir.
Anesteziden uyanma �zerine
4 dakika boyunca 500 mikrogram/kg/dakikal�k bir inf�zyonu takiben 300 mikrogram/kg/dakikal�k bir inf�zyon verilir. Farkl� hasta a��rl�klar� i�in gereken inf�zyon hacmi Tablo 2'de verilmi�tir.
Titrasyon uygun oldu�u zaman ameliyat sonras� durumlar i�in
H�zl� bir etki ba�lang�c� olu�turmak i�in her titrasyon ad�m�ndan 1 dakika �nce 500 mikrogram/kg/dakikal�k bir y�kleme dozu verilir. 4 dakikada verilen ve istenen terap�tik etki olu�unca durulan 50, 100, 150, 200, 250 ve 300 mikrogram/kg/dakikal�k titrasyon ad�mlar� kullan�l�r. Farkl� hasta a��rl�klar� i�in gereken inf�zyon hacmi Tablo 2'de verilmi�tir.
�nerilen maksimum doz
Kan bas�nc�n�n yeterli kontrol� i�in daha y�ksek dozlar (250-300 mcg/kg/dak) gerekebilir. 300 mcg/kg/dak'�n �zerindeki dozajlar�n g�venlili�i yeterince �al���lmam��t�r.
KARDOES ile dozajlama s�ras�nda dikkat edilecek potansiyel etkiler
Advers reaksiyon durumunda, KARDOES dozu azalt�labilir veya kesilebilir. Farmakolojik advers reaksiyonlar 30 dakika i�inde ��z�lmelidir.
Lokal inf�zyon b�lgesi reaksiyonu olu�ursa, alternatif bir inf�zyon b�lgesi kullan�lmal� ve ekstravazasyonu �nlemek i�in dikkatli olunmal�d�r.
KARDOES'in 24 saatten daha uzun bir s�re boyunca uygulanmas� tam olarak de�erlendirilmemi�tir. 24 saatten daha uzun inf�zyon s�relerinde dikkatli kullan�lmal�d�r.
Ribaund ta�ikardisi ve ribaund hipertansiyonu riski nedeniyle inf�zyonun kademeli olarak sonland�r�lmas� �nerilir. T�m beta blokerlerde oldu�u gibi, geri �ekilme etkileri g�z ard� edilemedi�inden, koroner arter hastal��� (KAH) hastalar�nda KARDOES uygulamas�n�n aniden kesilmesinde dikkatli olunmal�d�r.
KARDOES tedavisinden alternatif ila�lara ge�i�
Hastalarda kalp h�z�nda yeterli kontrol ve stabil bir klinik tablo sa�land�ktan sonra alternatif antiaritmik ila�lara ge�i� yap�labilir.
Doz azaltma:
KARDOES tedavisinden alternatif ila�lara ge�ilece�i zaman hekim se�ilen alternatif ilac�n kullanma talimatlar�n� dikkatli �ekilde incelemeli ve KARDOES dozunu a�a��daki �ekilde azaltmal�d�r:
Alternatif ilac�n ilk dozundan sonraki 1 saat i�erisinde KARDOES inf�zyon h�z� yar�ya (%50) d���r�l�r.
Alternatif ilac�n ikinci dozunun uygulanmas�ndan sonra hastan�n yan�t� izlenir ve ilk saatte yeterli kontrol sa�lan�rsa KARDOES inf�zyonu kesilir.
Ek dozaj bilgisi
�stenen terap�tik etkiye veya bir g�venlilik u� noktas�na (�rne�in d���r�lm�� kan bas�nc�na) yakla��ld���nda, y�kleme dozu atlanmal� ve art�ml� inf�zyon 12,5 ila 25 mikrogram/kg/dakika'ya d���r�lmelidir. Gerekirse, titrasyon ad�mlar� aras�ndaki aral�k, 5 dakikadan 10 dakikaya artt�r�labilir.
KARDOES, kalp at�� h�z� veya kan bas�nc� h�zla bir g�venlilik s�n�r�na yakla�t���nda veya bu s�n�r� a�t���nda kesilmeli ve kalp at�� h�z� veya kan bas�nc� kabul edilebilir bir seviyeye d�nd�kten sonra daha d���k bir dozda y�kleme inf�zyonu olmadan yeniden ba�lat�lmal�d�r.
Uygulama �ekli:
KARDOES kullan�ma haz�r bir ��zelti oldu�undan, seyreltilmeden intraven�z yoldan kullan�l�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
B�brek yetmezli�i:
B�brek yetmezli�i olan hastalarda KARDOES asit metaboliti b�brekler taraf�ndan de�i�memi� formda at�ld���ndan inf�zyonla KARDOES uyguland���nda dikkatli olunmas� gerekir. Asit metabolitin at�l�m� son evre b�brek hastal��� olan ki�ilerde anlaml� �ekilde azalmakta olup eliminasyon yar� �mr� normalin yakla��k on kat�na artm�� ve plazma d�zeyleri ciddi �ekilde y�kselmi�tir.
Karaci�er yetmezli�i:
K�rm�z� kan h�crelerindeki esterazlar KARDOES metabolizmas�nda temel bir rol oynad���ndan karaci�er yetmezli�i durumunda �zel �nlemler gerekli de�ildir.
Pediyatrik pop�lasyon:
KARDOES'in 18 ya� alt� �ocuklarda kullan�mdaki etkilili�i ya da g�venlili�i hen�z kan�tlanmam��t�r. Bu nedenle, KARDOES pediyatrik pop�lasyonda kullan�m i�in endike de�ildir (Bkz. B�l�m 4.1). Mevcut veriler b�l�m 5.1 ve 5.2'de tan�mlanmaktad�r ancak bu verilerden pozoloji hakk�nda bir �neri sunulamaz.
Geriyatrik pop�lasyon:
Ya�l�larda tedaviye d���k dozdan ba�lanarak, uygulama dikkatle yap�lmal�d�r.
Ya�l�larda �zel �al��malar y�r�t�lmemi�tir. Ancak 65 ya� �zeri 252 hastadan elde edilmi� verilerin analizi, olu�an farmakodinamik etkiler a��s�ndan 65 ya� alt�ndakilerle herhangi bir farkl�l�k olmad���n� g�stermektedir.
4.3. Kontrendikasyonlar
Etkin madde
A��r sin�s bradikardisi (dakikada 50 vurumdan az),
Hasta sin�s sendromu; a��r AV d���m� ileti bozukluklar� (pacemaker olmayan); ikinci veya ���nc� derece kalp bloklar�,
Kardiyojenik �ok,
Ciddi hipotansiyon,
Dekompanse kalp yetmezli�i,
E�zamanl� ya da yak�n zamanda intraven�z yoldan verapamil kullan�m�. KARDOES, verapamil kesilmesinden sonraki 48 saat i�inde uygulanmamal�d�r (Bkz.B�l�m 4.4),
Tedavi edilmemi� feokromositoma,
Pulmoner hipertansiyon,
Akut ast�m ata��,
Metabolik asidoz.
4.4. �zel kullan�m uyar�lar� ve �nlemleri
KARDOES tedavisi g�ren t�m hastalarda kan bas�nc� ve EKG'nin s�rekli olarak izlenmesi �nerilmektedir.
Hastada hemodinamik bozukluk bulundu�unda veya hasta a�a��daki parametrelerin birini veya t�m�n� azaltan di�er ila�lar� kullan�yorsa, supraventrik�ler aritmili hastalarda ventrik�l yan�t�n�n kontrol� i�in esmolol hidroklor�r kullan�m� s�ras�nda dikkatli olunmal�d�r: Periferik diren�, miyokardiyal dolum, miyokardiyal kontraktilite veya miyokardiyumda elektriksel impuls propagasyonu.Esmolol hidroklor�r etkilerinin h�zl� ba�lamas� ve sonlanmas�na kar��n bilin� kayb�, kardiyojenik �ok, kardiyak arrest gibi �iddetli reaksiyonlar geli�ebilir. Esmolol hidroklor�r�n ventrik�l h�z�n� kontrol etmek i�in kullan�ld���n�n varsay�ld��� kompleks klinik ko�ullarda birka� �l�m vakas� bildirilmi�tir.
En s�k g�r�len yan etki dozla ili�kili olan, ancak her dozda da g�r�lebilen hipotansiyondur. Hipotansiyon �iddetli olabilmektedir. Bir hipotansif epizod ya�anmas� durumunda inf�zyon h�z� d���r�lmeli veya gerekirse inf�zyon kesilmelidir. Hipotansiyon genellikle geriye d�n��ebilir niteliktedir (KARDOES uygulamas�na son verildikten sonraki 30 dakika i�inde). Baz� vakalarda kan bas�nc�n� normal de�erlerine y�kseltebilmek i�in ek giri�imlere gerek duyulabilir. Sistolik kan bas�nc� d���k hastalarda dozun ayarlanmas� ve idame inf�zyonu s�ras�nda �zel dikkat gerekir.
Esmolol hidroklor�r kullan�m� s�ras�nda a��r bradikardi dahil bradikardi ve kardiyak arrest meydana gelmi�tir. KARDOES, tedavi �ncesinde kalp h�z� d���k olanlarda �zel bir dikkatle ve ancak olas� yararlar�, riskine a��r bas�yorsa kullan�lmal�d�r.
�nceden a��r sin�s bradikardisi olan hastalarda KARDOES kullan�m� kontrendikedir (Bkz.B�l�m 4.3). Nabz�n istirahatteyken dakikada 50-55 vurunun alt�na d��t��� ve hastada bradikardiye ili�kin semptomlar g�r�l�rse dozaj azalt�lmal� ya da uygulamaya son verilmelidir.
Konjestif kalp yetmezli�inde dola��m fonksiyonunun desteklenmesi i�in sempatik aktivite gereklidir. Beta blokaj�n�n miyokard depresyonunu artt�rarak yetmezli�i daha da a��rla�t�rma riski bulunmaktad�r. Belirli bir s�reden uzun s�relerle beta blok�rlerle miyokard depresyonunun devam ettirilmesi, baz� vakalarda kalp yetmezli�ine yol a�abilir.
Kardiyak fonksiyonlar� bozulmu� hastalarda KARDOES kullan�l�rken dikkatli olunmas� gerekir. Kalp yetmezli�inin ilk belirti ve semptomlar� g�r�l�r g�r�lmez KARDOES tedavisine son
verilmelidir. Her ne kadar eliminasyon yar� �mr�n�n k�sa olmas� nedeniyle, KARDOES'in kesilmesi yeterli olsa da ayr�ca spesifik tedavi uygulanmas� da d���n�lebilir (Bkz.B�l�m 4.9). KARDOES dekompanse kalp yetmezli�i olan hastalarda kontrendikedir (Bkz.B�l�m 4.3).
Kalpteki ileti s�resi �zerindeki negatif etkileri nedeniyle beta blok�r ila�lar birinci derece kalp blo�u veya di�er kalp ileti bozuklu�u olan hastalarda ancak dikkatle verilmelidir (Bkz.B�l�m 4.3).
KARDOES feokromositomal� hastalarda ancak alfa-resept�r blok�rleriyle �n tedavi g�rm�� olmak kayd�yla ve dikkatle kullan�lmal�d�r (Bkz.B�l�m 4.3).
Hipotermiyle uyar�lm�� hipertansiyonun tedavisinde KARDOES kullan�m�nda dikkatli olunmas� gerekir.
Genel olarak bronkospastik hastal�klar� olanlar beta blok�r kullanmamal�d�r. Beta-1 resept�rlere nispeten selektif olmas� ve kullan�m s�ras�nda titre edilebilir olmas� nedeniyle KARDOES bu hastalarda dikkatle kullan�labilir. Ancak beta-1 selektifli�i mutlak olmad���ndan KARDOES, olas� etkili en d���k dozu elde etmek i�in dikkatle titre edilmelidir. Bronkospazm durumunda inf�zyon derhal durdurulmal� ve gerekti�inde beta-2 agonist bir preparat uygulanmal�d�r.
Hasta zaten bir beta-2-resept�r stim�lan ajan kullan�yorsa, bu ajan�n dozunun yeniden de�erlendirilmesi gerekebilir.
KARDOES h�r�lt�l� solunum ya da ast�m hikayesi olan hastalarda dikkatli kullan�lmal�d�r.
KARDOES diyabetik hastalarda ya da ��pheli ya da ger�ek hipoglisemisi olanlarda dikkatli uygulanmal�d�r. Beta blok�rler hipogliseminin ta�ikardi gibi prodromal semptomlar�n� maskeleyebilir. Ancak sersemlik hali ve terleme etkilenmeyebilir. Beta blok�rlerle antidiyabetik ajanlar�n e�zamanl� kullan�m� antidiyabetik ajanlar�n hipoglisemik (kan �ekeri d���r�c�) etkisinde art��a yol a�abilir (Bkz.B�l�m 4.5).
Esmolol hidroklor�r kullan�m�na ba�l� olarak inf�zyon b�lgesinde reaksiyonlar meydana gelmi�tir. Bu reaksiyonlar aras�nda iritasyon ve enflamasyon bulunabildi�i gibi �zellikle ekstravazasyon ile ili�kili trombofilebit, nekroz ve deride blisterlenme gibi daha ciddi reaksiyonlar da bulunur (Bkz.B�l�m 4.8). K���k venlerden veya kelebek kateterle yap�lacak uygulamalardan ka��n�lmal�d�r. Lokal bir inf�zyon yeri reaksiyonu olu�tu�unda, alternatif bir inf�zyon b�lgesi kullan�lmal�d�r.
Beta blok�rler, kar��lanmam�� alfa-resept�r k�kenli koroner arter vazokonstr�ksiyonuna ba�l� olarak Prinzmetal anjinas� olan hastalarda anjina ataklar�n�n s�kl�k ve s�resini artt�rabilir. Bu t�r hastalarda selektif olmayan beta blok�rler kullan�lmamal�; beta-1 selektif olan blok�rler ise yaln�zca son derece dikkatli �ekilde kullan�lmal�d�r.
KARDOES hipovolemik hastalarda refleks ta�ikardiyi zay�flatabilir ve dola��m kollaps� riskini artt�rabilir. Bu nedenle bu t�r hastalarda KARDOES dikkatli kullan�lmal�d�r.
Beta blok�rler periferik dola��m bozukluklar�n�n (Raynaud hastal��� veya sendromu, intermittan kladikasyon) bulundu�u hastalarda bozukluklar� �iddetlendirebilece�i i�in son derece dikkatli uygulanmal�d�r.
KARDOES dahil, �zellikle intraven�z olarak uygulanan baz� beta blok�rler, serum potasyum d�zeylerinde y�kselme ve hiperkalemi ile ili�kilendirilmi�tir. Bu risk b�brek yetmezli�i ve hemodiyaliz tedavisi g�rme gibi risk fakt�rlerinin bulundu�u hastalarda artar.
Beta blok�rler hem alerjenlere duyarl�l��� hem de anafilaktik reaksiyonlar�n �iddetini artt�r�r. Beta blok�r kullanan hastalar anafilaktik ya da anafilaktoid reaksiyonlar�n tedavisinde kullan�lan ola�an dozlarda epinefrine yan�t vermeyebilir (Bkz.B�l�m 4.5).
Beta blok�rlerin ps�riyazis ya da ps�riyazis benzeri d�k�nt�lere yol a�abilece�i ve mevcut bir ps�riyazis hastal���n� a��rla�t�rabilece�i bildirilmi�tir. �zge�mi� ya da soyge�mi�inde ps�riyazis bulunanlarda beta blok�rler ancak tedaviden beklenen fayda ile olas� riskleri dikkatle de�erlendirildikten sonra kullan�lmal�d�r.
Propranolol ve metoprolol gibi beta blok�rler hipertiroidinin belirli klinik i�aretlerini (ta�ikardi gibi) maskeleyebilir. Tirotoksikoz geli�im riski ya da ku�kusu olan hastalarda beta blok�rlerle devam etmekte olan tedavinin aniden kesilmesi tiroid krizini h�zland�rabilir ve bu t�r hastalar yak�ndan izlenmelidir.
Bu �r�n 250 ml'lik bir torbas�nda 30,45 mmol (700 mg) sodyum i�erir. Bu durum kontroll� sodyum diyetinde olan hastalar i�in g�z �n�nde bulundurulmal�d�r.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
KARDOES di�er antihipertansif ajanlar veya bradikardiye neden olabilen di�er ila�larla birlikte kullan�ld���nda daima dikkatli olunmal�d�r: KARDOES'in etkileri veya hipotansiyon veya bradikardi yan etkileri �iddetlenebilir.
Verapamil gibi kalsiyum antagonistleri ve daha d���k d�zeyde diltiazem kontraktilitede ve AV iletiminde negatif bir etkiye sahiptir. Bu kombinasyon iletim anomalileri olan hastalara uygulanmamal� ve KARDOES verapamil kesildikten sonraki 48 saatte verilmemelidir (Bkz B�l�m 4.3).
Dihidropiridin t�revi (�rn. nifedipin) kalsiyum antagonistleri hipotansiyon riskini artt�rabilir. Kalp yetmezli�i i�in kalsiyum antagonisti ile tedavi g�ren hastalara beta blok�r uygulanmas� kalp yetmezli�ine neden olabilir. KARDOES'in dikkatle titre edilerek uygun hemodinamik monitorizasyonu �nerilir.
KARDOES ve S�n�f I anti-aritmik ila�lar�n (�rn; dizopiramid, kinidin) ve amiodaronun e�zamanl� kullan�m� atriyal-iletim s�resinde g��lendirici etkiye sahip olabilir ve negatif inotropik etkiye neden olabilir.
KARDOES ve ins�lin veya oral antidiyabetik ila�lar�n e�zamanl� kullan�m� kan �ekeri d���r�c� etkiyi art�rabilir (�zellikle selektif olmayan beta-blok�rler). Beta- adrenerjik blokaj� hipoglisemi belirtilerinin (ta�ikardi) g�zlenmesini engelleyebilir ancak ba� d�nmesi/sersemlik ve terleme gibi di�er belirtiler maskelenmeyebilir.
Anestezi ila�lar�: Hastalar�n hacim durumunun belirsiz oldu�u veya e�zamanl� antihipertansif ila�lar�n kullan�ld��� durumlarda refleks ta�ikardide azalma veya hipotansiyon riskinde art�� g�r�lebilir. Beta-blokaja devam edilmesi ind�ksiyon ve ent�basyon s�ras�nda aritmi riskini
azalt�r. Hastaya KARDOES'e ek olarak bir beta-blok�r ajan verilirken anestezist bilgilendirilmelidir. �nhalasyon anestezi ajanlar�n�n hipotansif etkileri KARDOES varl���nda artabilir. Her bir ajan�n dozu istenen hemodinamik parametrelerin korunmas� i�in de�i�tirilebilir. KARDOES ile gangliyon bloke edici ila�lar�n kombinasyonu hipotansif etkiyi artt�rabilir.
Steroid olmayan anti-enflamatuvar ila�lar (NSA��) ile birlikte kullan�ld�klar�nda beta blok�rlerin hipotansif etkileri azal�r.
Beta-blok�rlerle e�zamanl� olarak floktafenin veya amisulprid kullan�l�rken �zellikle dikkatli olunmal�d�r.
Trisiklik antidepresanlar�n (imipramin ve amitriptilin gibi), barbit�ratlar�n ya da fenotiyazinler (klorpromazin gibi) yan�nda di�er antipsikotik ajanlar�n (klozapin gibi) birlikte uygulan��� kan bas�nc�n� azalt�c� etkiyi artt�rabilir. Beklenmeyen bir hipotansif durumdan ka��nmak i�in birlikte kullan�mda KARDOES dozu azalt�lmal�d�r.
Beta-blok�rler kullan�l�rken anafilaktik reaksiyon riski olan hastalarda alerjen maruziyetine (kazara, diagnostik veya terap�tik) reaksiyon g�zlenebilir. Beta blok�r kullanan hastalar, anafilaktik reaksiyonlar�n tedavisinde kullan�lan mutad epinefrin dozlar�na yan�t vermeyebilir (Bkz. B�l�m 4.4).
KARDOES'in etkileri e�zamanl� uyguland���nda beta-adrenerjik agonist aktiviteye sahip sempatomimetik ila�lara ba�l� olarak azalabilir. Her bir ajan�n dozunun hasta yan�t�na g�re ayarlanmas� veya alternatif terap�tik ajanlar�n kullan�m�n�n d���n�lmesi gerekebilir.
Katekolamin bo�almas�na yol a�an ila�lar (�rn; rezerpin) beta-blok�r ila�larla birlikte verildi�inde aditif bir etki g�sterebilirler. KARDOES ile e�zamanl� olarak katekolamin bo�almas�na yol a�an ila� tedavisi alan hastalar vertigo, senkop veya postrual hipotansiyon ile sonu�lanabilen hipotansiyon ve �nemli bradikardi belirtileri a��s�ndan yak�ndan izlenmelidir.
Beta blok�rlerin, moksonidin veya alfa-2-agonistleriyle (klonidin gibi) birarada kullan�m� �ekilmeye ba�l� rebound hipertansiyon riskini artt�r�r. Klonidin veya moksonidin bir beta blok�rle birlikte kullan�lacaksa ve daha sonra her iki ila� da kesilecekse, ilk olarak beta blok�r, klonidin veya moksonidin birka� g�n sonra kesilmelidir.
Beta blok�rlerin ergot t�revleriyle bir arada kullan�m� ciddi periferik vazokonstr�ksiyon ve hipertansiyonla sonu�lanabilir.
Esmolol hidroklor�r ile varfarin aras�nda bir etkile�im olup olmad���n� belirlemek i�in yap�lan bir �al��madaki veriler, esmolol hidroklor�r ve varfarinin birlikte uygulanmas�n�n, varfarinin plazma d�zeylerini de�i�tirmedi�ini g�stermi�tir. Buna ra�men varfarin ile birlikte uygulanan esmolol hidroklor�r�r konsantrasyonlar� daha y�ksek olarak bulunmu�tur.
Esmolol hidroklor�r ve digoksin sa�l�kl� g�n�ll�lerde intraven�z yoldan birlikte uyguland���nda, baz� zaman noktalar�nda digoksinin kandaki d�zeylerinde %10-20'lik bir y�kselme oldu�u bildirilmi�tir. Dijital glikozitleriyle esmolol hidroklor�r kombinasyonu AV ileti s�resini uzatabilir. Digoksin, esmolol hidroklor�r�n farmakokinetik �zelliklerini etkilememi�tir.
�ntraven�z morfin ve esmolol hidroklor�r sa�l�kl� g�n�ll�lere e�zamanl� olarak uyguland���nda morfinin kan d�zeylerinde herhangi bir de�i�iklik olmad��� g�r�lm��t�r. Morfin varl���nda
esmolol hidroklor�r�n kararl� durum kan d�zeylerinin %46 oran�nda artt��� ancak di�er farmakokinetik parametrelerden hi�birinin de�i�medi�i saptanm��t�r.
Esmolol hidroklor�r�n suksametonyum klor�r ve mivakuryum ile uyar�lan n�rom�sk�ler blokaj�n s�resi �zerine etkisi cerrahi giri�imde bulunulan hastalarda incelenmi�tir. Esmolol hidroklor�r, suksametonyum klor�r ile ind�klenen n�rom�sk�ler blokaj�n ba�lamas�n� etkilememektedir, ancak n�rom�sk�ler blokaj�n s�resi 5 dakikadan 8 dakikaya ��km��t�r. Esmolol hidroklor�r, mivakuryumun klinik s�resini (%18,6) ve geri kazan�m indeksini (%6,7) k�smen uzatm��t�r.
Varfarin, digoksin, morfin, suksametonyum klor�r veya mivakuryum ile yap�lan �al��malarda g�zlenen etkile�imler klinik a��dan �ok �nemli olmamakla birlikte KARDOES ile e�zamanl� olarak varfarin, digoksin, morfin, suksametonyum klor�r veya mivakuryum uygulanan hastalarda titrasyon dikkatli yap�lmal�d�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
Bilgi bulunmamaktad�r.
Pediyatrik pop�lasyon:
Bilgi bulunmamaktad�r.
4.6. Gebelik ve laktasyon
:Gebelik Kategorisi: C / D (2. ve 3. trimester)
�ocuk do�urma potansiyeli bulunan kad�nlar / Do�um kontrol� (Kontrasepsiyon)
�ocuk do�urma potansiyeli olan kad�nlar tedavi s�resince etkili do�um kontrol� uygulamak zorundad�rlar.
Gebelik d�nemi
Hayvanlar �zerinde yap�lan �al��malar, gebelik /ve-veya/ embriyonal/fetal geli�im /ve-veya/ do�um /ve-veya/ do�um sonras� geli�im �zerindeki etkiler bak�m�ndan yetersizdir. Hayvanlar �zerinde esmolol hidroklor�rle yap�lan �al��malarda �reme toksisitesi g�r�lm��t�r (Bkz. B�l�m 5.3). �nsanlara y�nelik potansiyel risk bilinmemektedir.
Esmolol hidroklor�r gebelik d�neminde kullan�lmamal�d�r.
Farmakolojik etkileri nedeniyle gebeli�in ge� d�neminde fetus ve yenido�an �zerindeki yan etkileri (�zellikle hipoglisemi, hipotansiyon ve bradikardi) dikkate al�nmal�d�r.
Gebelikte KARDOES tedavisi gerekli olursa, uteroplasental kan ak�m� ve f�tal b�y�me izlenmelidir. Yenido�an bebe�in yak�ndan izlenmesi gerekir.
Laktasyon d�nemi
Esmolol hidroklor�r emzirme d�neminde kullan�lmamal�d�r.
Emziren kad�nlarda esmolol hidroklor�r�n anne s�t�ne ge�ip ge�medi�i bilinmemektedir. Yenido�an bebeklere potansiyel bir riski g�zard� edilemez.
�reme yetene�i / Fertilite
Esmolol�n insanlarda �reme yetene�i/fertilite �zerindeki etkisini ara�t�ran bir �al��ma bulunmamaktad�r.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
Ara� ve makine kullan�m� s�ras�nda KARDOES'in kullan�m� m�mk�n olmad���ndan bu konudaki etkisi bilinmemektedir.
4.8. �stenmeyen etkiler
�stenmeyen etkilerin g�r�lmesi durumunda KARDOES'in dozu azalt�labilir ya da uygulamaya son verilebilir.
G�r�len advers etkilerin �o�u hafif ve ge�ici nitelikte olarak bildirilmi�tir. En �nemlisi hipotansiyondur.
Advers etkilerin g�r�lme s�kl���, a�a��daki kriterler kullan�larak de�erlendirilmi�tir:
�ok yayg�n (≥1/10)
Yayg�n (≥1/100 ila <1/10)
Yayg�n olmayan (≥1/1.000 ila <1/100) Seyrek (≥1/10.000 ila <1/1 .000)
�ok seyrek <1/10.000)
Bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Metabolizma ve beslenme hastal�klar�
Yayg�n: Anoreksi.
Bilinmiyor: Hiperkalemi, metabolik asidoz.
Psikiyatrik hastal�klar
Yayg�n: Depresyon, anksiyete. Yayg�n olmayan: Anormal d���nce.
Sinir sistemi hastal�klar�
Yayg�n: | Ba� d�nmesi/sersemlik hali, uykuya meyil, ba�a�r�s�, parestezi, dikka bozuklu�u, konf�zyonel durum, ajitasyon. |
Yayg�n olmayan:
G�z hastal�klar� | Senkop, konv�lsiyon, konu�ma bozuklu�u. |
Yayg�n olmayan: | G�rmede bozulma. |
Kardiyak hastal�klar
Yayg�n olmayan: Bradikardi, atriyoventrik�ler blok, pulmoner arteriyel bas�n�ta y�kselme, kalp yetmezli�i, ventrik�ler ekstrasistoller, nodal ritim, anjina pektoris.
�ok seyrek: | Sin�s durmas�, asistol. |
Bilinmiyor: | Akselere idiyoventrik�ler ritim, koroner arteriyospazm, kardiyak arrest. |
Vask�ler hastal�klar
�ok yayg�n: Hipotansiyon.
Yayg�n olmayan: Periferik iskemi, solukluk, y�z ve boyun b�lgesinde k�zarma. �ok seyrek: Trombofilebit
Solunum, g���s bozukluklar� ve mediastinal hastal�klar
Yayg�n olmayan: Dispne, pulmoner �dem, bronkospazm, h�r�lt�l� solunum, nazal konjesyon, akci�er seslerinde ronkus ve raller.
Gastrointestinal hastal�klar
Yayg�n: Bulant�, kusma.
Yayg�n olmayan: Disguzi, dispepsi, kab�zl�k, a��zda kuruma, kar�nda a�r�.
Deri ve deri alt� doku hastal�klar�
�ok yayg�n: | Diaforez. |
Yayg�n olmayan: | Ciltte renk kayb�, eritem. |
�ok seyrek: | Deri nekrozu (ekstravazasyona ba�l�). |
Bilinmiyor: | Psoriyazis, anjiyo�dem, �rtiker. |
Kas-iskelet bozukluklar�, ba� doku ve iskelet hastal�klar�
Yayg�n olmayan: Kas-iskelet a�r�s�.
B�brek ve idrar yolu hastal�klar�
Yayg�n olmayan: �riner retansiyon.
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar:
Yayg�n: | Asteni, halsizlik, enjeksiyon yeri reaksiyonu, inf�zyon b�lgesi reaksiyonu, inf�zyon b�lgesi inflamasyonu, inf�zyon b�lgesi end�rasyonu. |
Yayg�n olmayan: | Titremeler, ate� y�kselmesi, �dem, a�r�, inf�zyon b�lgesinde yanma, inf�zyon b�lgesinde ekimoz. |
Bilinmiyor: | �nf�zyon b�lgesinde filebit, inf�zyon b�lgesinde vezik�ller, inf�zyon b�lgesinde blisterlenme. |
Ba� d�nmesi/sersemlik hali ve diyaforez semptomatik hipotansiyonla birlikte g�r�lm��t�r.
Midskapular a�r� ve kostokondrit dahil.
4.9. Doz a��m� ve tedavisi
Konsantre esmolol hidroklor�r sol�syonlar� ile kazara b�y�k doz a��m� vakalar� meydana gelmi�tir. Bu doz a��mlar�n�n baz�lar� �l�me yol a�arken, di�erleri kal�c� i�lev kayb�na neden olmu�tur. Preparat�n 6,25 mg – 2,5 g aras�ndaki y�kleme dozlar� (12,5 - 50 mg/kg) �l�mle sonu�lanm��t�r.
Doz a��m�n�n semptomlar�
Doz a��m� durumunda a�a��daki belirtiler olu�abilir:
�iddetli hipotansiyon, sin�s bradikardisi, atriyoventrik�ler blok, kalp yetmezli�i, kardiyojenik �ok, kardiyak arrest, bronkospazm, solunum yetmezli�i, komaya kadar ilerleyebilen bilin� kayb�, konv�lsiyonlar, bulant�, kusma, hipoglisemi ve hiperkalemi.
Doz a��m�nda tedavi
K�sa eliminasyon yar� �mr� nedeniyle (yakla��k 9 dakika) toksisite tedavisinde ilk basamak KARDOES inf�zyonunun durdurulmas�d�r. Doz a��m� sonras�nda semptomlar�n kaybolmas� i�in gereken s�re uygulanan KARDOES miktar�na ba�l� olacakt�r. Bu s�re KARDOES'in terap�tik doz d�zeyinde ila� kesildikten sonra 30 dakikadan uzun s�rebilir. Suni solunum gerekebilir.
Daha sonra g�zlenen klinik etkilere g�re a�a��daki �nlemler d���n�lebilir:
Bradikardi: Atropin ya da di�er bir antikolinerjik ila� intraven�z yoldan uygulan�r. Bradikardinin yeterince tedavi edilemedi�i durumlarda pacemaker gerekli olabilir.
Bronkospazm: Neb�lize beta-2-sempatomimetikler uygulanmal�d�r. Bu yeterli olmazsa beta- 2-sempatomimetikler ya da aminofilinin intraven�z yoldan uygulanmas� d���n�lmelidir.
Semptomatik hipotansiyon: �ntraven�z yoldan s�v�lar ve/veya press�r ajanlar verilmelidir.
Kardiyovask�ler depresyon veya kardiyak �ok: Di�retik veya sempatomimetikler uygulanabilir. Uygulanacak sempatomimetiklerin (semptoma g�re dobutamin, dopamin, noradrenalin, isoprenalin) dozu terap�tik etkiye ba�l�d�r.
Daha ileri tedavi gerekti�inde, klinik duruma ve tedaviyi y�r�ten hekimin karar�na g�re a�a��daki ila�lar intraven�z yoldan verilebilir.
Atropin,
�notropik ajanlar,
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik Grubu: Selektif beta blok�r ila�lar ATC kodu: C07AB09
KARDOES bir beta selektif (kardiyoselektif) adrenerjik resept�r blokaj ajan�d�r. Terap�tik dozlarda anlaml� bir intrensek sempatomimetik aktivite (ISA) ya da membran stabilizan etkinli�i yoktur.
KARDOES'in etkin maddesi olan esmolol hidroklor�r kimyasal olarak beta blok�rlerin fenoksi propanolamin s�n�f�ndand�r.
5. FARMAKOLOJ�K �ZELL�KLER
Uygun y�kleme dozu kullan�ld���nda, kandaki kararl� durum d�zeylerine 5 dakikada ula��l�r. Ancak terap�tik etkiye stabil plazma konsantrasyonundan daha k�sa s�rede eri�ilir. Daha sonra istenen farmakolojik etkinin elde edilmesi i�in inf�zyon oran� ayarlanabilir.
KARDOES beta blok�rlerin bilinen hemodinamik ve elektrofizyolojik etkilerine sahiptir:
�stirahat halinde ve egzersiz s�ras�nda kalp h�z�nda azalma,
Izoprenalin azalmas� sonucunda kalp h�z�nda art��,
Sinoatriyal (SA) d���m�n recovery s�resinde uzama,
Atriyoventrik�ler (AV) iletide gecikme,
Atriyoventrik�ler (AV) aral���n�n normal sin�s ritmi ile ve His-Purkinje dokusunda gecikme olmadan atrium stim�lasyonu s�ras�nda uzama,
PQ s�resinde uzama, evre II atriyoventrik�ler blok ind�ksiyonu,
Atriyum ve ventrik�llerin fonksiyonel refrakt�r periyodunda uzama,
Azalm�� ejeksiyon fraksiyonu ile negatif inotropik etki,
Kan bas�nc�nda azalma.
Pediyatrik pop�lasyon
Supraventrik�ler ta�ikardisi olan ya�lar� 2 ile 16 aras�ndaki 26 pediyatrik hastada kontroll� bir farmakokinetik/etkinlik �al��mas� y�r�t�lm��t�r. 1000 mikrogram/kg'l�k bir esmolol hidroklor�r y�kleme dozu uyguland�ktan sonra devaml� inf�zyonla dakikada 300 mikrogram/kg'l�k dozla idame tedavisine ge�ilmi�tir. Esmolol ba�land�ktan sonraki 5 dakikada hastalar�n %65'inde supraventrik�ler ta�ikardi sonlanm��t�r.
Randomize olan ancak kontrols�z bir doz kar��la�t�rmas� �al��mas�nda, ya�lar� 1 haftal�k ile 7 ya� aras�ndaki 116 pediyatrik hastan�n aort koarktasyonu d�zeltildikten sonra geli�en hipertansiyonda etkinlik ara�t�r�lm��t�r. 125 mikrogram/kg'l�k, 250 mikrogram/kg'l�k veya 500 mikrogram/kg'l�k esmolol hidroklor�r ba�lang�� dozu uygulanan hastalarda daha sonra devaml� inf�zyonla s�ras�yla dakikada 125 mikrogram/kg, 250 mikrogram/kg veya 500 mikrogram/kg'l�k dozlarla idame tedavisine ge�ilmi�tir. Her �� dozaj grubunda hipotansif etki a��s�ndan anlaml� bir fark g�r�lmemi�tir. Hastalar�n toplamda %54'�nde yeterli kan bas�nc� kontrol� sa�lanmas� i�in esmolol hidroklor�r d���nda ba�ka bir ila� kullan�lmas� gerekmi�tir. De�i�ik doz gruplar�nda bu a��dan bir farkl�l�k g�r�lmemi�tir.
5.2. Farmakokinetik �zellikler
Emilim:
Esmolol kineti�i sa�l�kl� yeti�kinlerde do�rusald�r, plazma konsantrasyonu doza orant�l�d�r. E�er bir y�kleme dozu kullan�lmazsa, sabit durumdaki kan konsantrasyonlar�na, dakikada 50 ila 300 mikrogram/kg dozlar�yla 30 dakika i�inde ula��l�r.
Da��l�m:
Esmolol hidroklor�r�n da��l�m yar�lanma s�resi yakla��k 2 dakika gibi �ok k�sad�r. Da��l�m hacmi 3,4 L/kg'd�r.
Esmolol hidroklor�r�n insan plazma proteinlerine %55 oran�nda ba�land���, asit metabolitinin ise sadece %10 oran�nda ba�land��� g�sterilmi�tir.
Biyotransformasyon:
Esmolol hidroklor�r�n metabolizmas� dozu 50 ile 300 mikrogram/kg/dakika oldu�unda dozdan ba��ms�zd�r.
Esmolol hidroklor�r esterazlar taraf�ndan bir asit metaboliti (ASL-8123) ve metanole metabolize olur. Bu metabolizasyon, ester ba�lar�n�n eritrositlerin sitozollerindeki esterazlar taraf�ndan hidrolizi yoluyla ger�ekle�ir.
Eliminasyon:
�ntraven�z uygulama sonucu eliminasyon yar� �mr� yakla��k 9 dakikad�r.
Toplam klerensi 285 ml/kg/dakikad�r; toplam klerens karaci�er veya di�er organlar�n dola��m�ndan ba��ms�zd�r. Esmolol hidroklor�r b�breklerden k�smen de�i�meden (uygulanan miktar�n %2'sinden az�) k�smen de zay�f bir beta blok�r etkinli�e sahip asit metaboliti olarak (uygulanan miktar�n %0,1'inden az�) at�l�r. Asit metabolit idrarla at�l�r ve eliminasyon yar� �mr� yakla��k 3,7 saattir.
Hastalardaki karekteristik �zellikler
Pediyatrik pop�lasyon:
Ya�lar� 3 ile 16 aras�nda olan 22 pediyatrik hastada bir farmakokinetik �al��ma ger�ekle�tirilmi�tir. 1000 mikrogram/kg'l�k bir KARDOES y�kleme dozu uyguland�ktan sonra devaml� inf�zyonla dakikada 300 mikrogram/kg'l�k dozla idame tedavisi uygulanm��t�r. �al��mada �ocuklardaki KARDOES kineti�inin eri�kinlerdekinden farkl� olmad���na i�aret edecek �ekilde ortalama toplam v�cut klerensi 119 ml/kg/dakika, ortalama da��l�m hacmi 283 ml/kg ve ortalama terminal eliminasyon yar�lanma �mr� 6,9 dakika olarak g�zlenmi�tir. Ancak, �ocuklarda bireysel de�i�kenli�in fazla oldu�u g�zlenmi�tir.
5.3. Klinik �ncesi g�venlilik verileri
Hayvan �al��malar�nda teratojenik etki g�r�lmemi�tir. Tav�anlarda olas�l�kla esmolol hidroklor�r�n neden oldu�u embriyotoksik bir etki (f�tal rezorpsiyonda artma) g�zlenmi�tir. Bu etki terap�tik dozlar�n en az 10 kat� y�ksek dozlarda g�zlenmi�tir.
KARDOES'in fertilite �zerindeki etkileri ile perinatal ve postnatal etkilerini ara�t�ran bir �al��ma ger�ekle�tirilmemi�tir. Esmolol hidroklor�r�n birka� in vitro ve in vivo test sistemlerinde mutajenik olmad��� bulunmu�tur. Esmolol hidroklor�r�n g�venilirli�i uzun s�reli �al��malarla incelenmemi�tir.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Sodyum asetat trihidrat Glasiyel asetik asit
Sodyum klor�r
Sodyum hidroksit ve/veya hidroklorik asit (pH ayarlanmas� i�in) Enjeksiyonluk su
6.2. Ge�imsizlikler
Ge�imlilik �al��malar� bulunmad���ndan bu ila� di�er ila�larla veya sodyum bikarbonat ��zeltisi ile kar��t�r�lmamal�d�r.
Alkali maddelerle temas�ndan ka��n�n�z.
6.3. Raf �mr�
24 ay.
A��lan �r�n 2-8 C aras�nda sakland���nda 24 saat s�reyle fizikokimyasal olarak stabildir.
Mikrobiyolojik a��dan �r�n torbas� a��ld�ktan sonra hemen kullan�lmal�d�r. Hemen kullan�lamad��� durumlarda, kullan�lmaya ba�lamadan �nceki saklama s�re ve ko�ullar� kullan�c�n�n sorumlulu�undad�r. Bu s�re 2-8C aras�nda torban�n kontroll� ve valide edilmi� aseptik ko�ullarda a��lmad��� durumlarda normalde 24 saatten uzun olamaz.
6.4. Saklamaya y�nelik �zel tedbirler
25 C'nin alt�ndaki oda s�cakl���nda ambalaj�nda saklanmal�d�r. Buzdolab�nda saklanmamal� ya da dondurulmamal�d�r.
��zeltinin saklama ko�ullar� i�in b�l�m 6.3'e bak�n�z.
6.5. Ambalaj�n niteli�i ve i�eri�i
PE d�� torba i�inde �ift ��k��l� 250 ml'lik bir adet PVC-free torba.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i”ne ve “Ambalaj At�klar�n�n Kontrol� Y�netmeli�i”ne uygun olarak imha edilmelidir.
TORBA KULLANIM TAL�MATI
KARDOES PREMIX 2500 mg/250 ml inf�zyon i�in kullan�ma haz�r ��zelti, 250 ml'lik PVC- free torbalarda (biri torbaya ila� uygulama i�in, di�eri torbadaki ilac�n hastaya verilmesi i�in olan �ift ��k��l� torba) sunulmaktad�r.
KARDOES PREMIX 2500 mg/250 ml inf�zyon i�in kullan�ma haz�r ��zeltinin torbas�ndaki ila� uygulama ucu yaln�zca torbadan ilk bolus uygulanacak ilac�n �ekilmesi i�in kullan�lmal�d�r; tekrarlanan bolus uygulamas� i�in de�ildir. Bolus dozunu �ekerken aseptik teknik kullan�lmal�d�r. KARDOES PREMIX 2500 mg/250 ml inf�zyon i�in kullan�ma haz�r ��zeltiye hi�bir ilave ila� eklenmemelidir.
Her torba tek hastada kullan�m i�indir. �la� uygulama ��k���n�n m�h�r� k�r�ld�ktan ve torbadan ilac�n �ekilmesinden sonra torban�n 24 saat i�inde kullan�lmas� gerekir. ��zeltinin kullan�lmayan b�l�m� ve torbas� yerel uygulamalar do�rultusunda imha edilmelidir. K�smen kullan�lm�� torbalar� yeniden kullanmay�n�z.
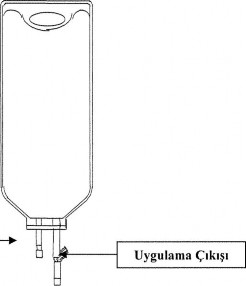
�ekil I. �ift-��k��l� torba
�la� ��k��� (Sadece ba�lang��taki bolus uygulama i�in ) |
|
D�KKAT
Plastik torbalar� seri ba�lamalar i�in kullanmay�n�z. Bu tip kullan�m ikinci kaptaki s�v�n�n uygulanmas� tamamlanmadan �nce birinci kaptan rezid�el havan�n �ekilmesine ba�l� emboliye neden olabilir.
A�MAK ���N
Kullan�mdan hemen �ncesine kadar d�� ambalaj�ndan (d�� torba) ��kar�lmamal�d�r. D�� torba daha �nceden a��lm��sa ya da hasar g�rm��se kullan�lmamal�d�r. D�� torba nemi �nleme amac�n� ta��r. �� torba ��zeltinin sterilitesini korur.
D�� torba �entikli yerinden a��larak premix torba ��kar�l�r. Bu a�amada plastik torba �zerinde g�r�lebilen opasiteler, sterilizasyon prosesi s�ras�ndaki nem absorbsiyonuna ba�l�d�r. Bu normaldir ve ��zeltinin kalitesini veya g�venilirli�ini etkilemez. Opakl�k giderek azalacakt�r.
�� torba s�k��t�r�larak k���k s�z�nt�lar olup olmad��� 1 dakika boyunca kontrol edilir. S�z�nt� varsa sterilizasyon etkilenmi� olaca��ndan ��zelti at�lmal�d�r. Uygulamadan �nce partik�ler madde ve renk de�i�ikli�i i�in sol�syon g�rsel olarak incelenir. Yaln�zca berrak ve renksiz veya a��k sar� renkli ��zeltiler kullan�lmal�d�r.
KARDOES PREMIX 2500 mg/250 ml'e ekstra hi�bir madde eklenmemelidir.
�NTRAVEN�Z UYGULAMA ���N HAZIRLIKLAR (aseptik teknik kullan�lmal�d�r)
Premix torba, asma yerinden bir ask�ya as�l�r.
 S�rt A�r�s�
S�rt a�r�s� birden bire ortaya
��k�p �iddetli (akut) olabilir veya zamanla geli�ip daha uzun
s�reli sorunlara (kronik) neden olabilir.
S�rt A�r�s�
S�rt a�r�s� birden bire ortaya
��k�p �iddetli (akut) olabilir veya zamanla geli�ip daha uzun
s�reli sorunlara (kronik) neden olabilir. |
 Diyabet Hastal���
Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r.
Diyabet Hastal���
Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| ESMOBLOC | 8699606524861 | 3,237.02TL |
| MULTIFLEX | 8680400770288 | |
| TURKTIPSAN | 8697637692023 | 2,322.01TL |
| Di�er E�de�er �la�lar |
 |
Do�um Sonras� Depresyonu Do�um sonras� depresyonu, do�umdan sonra her on kad�ndan biri taraf�ndan tecr�be edilen stresli bir durumdur. |
 |
Rahim Boyu ( Serviks ) Kanseri Rahim boynu (serviks) kanseri 35 ya� alt� kad�nlarda g�r�len vakalarda meme kanserinden sonra ikinci s�ray� al�r.Serviks kanserinin geli�mesi y�llarca s�rebilir. |
 |
Belso�uklu�u, Chlamydia ve Frengi Belso�uklu�u, bakterilerin sebep oldu�u bir enfeksiyondur. Cinsel ili�ki yoluyla bula��r ve d�lyata�� boynunda, idrar yollar�nda, an�ste, makatta ve bo�azda enfeksyona sebep olabilir. |
�LA� GENEL B�LG�LER�
T�m-Ekip �la� A.�.
| Geri �deme Kodu | A17364 |
| Sat�� Fiyat� | TL |
| �nceki Sat�� Fiyat� | |
| Original / Jenerik | Jenerik �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699614690099 |
| Etkin Madde | Esmolol Hcl |
| Yerli ve Be�eri bir ila�d�r. |