LUCENTIS 10 mg/ml enjeksiyonluk çözelti Saklanması
{ Ranibizumab }
Duyu Organları > Oküler Damar Bozukluğu Ajanları > Ranibizumab Novartis Sağlık,Gıda ve Tarım Ürünleri San. Tic. A.Ş. | Güncelleme : 3 August 20125.LUCENTIS'in saklanması
LUCENTIS'i çocukların göremeyeceği, erişemeyeceği yerlerde ve ambalajında saklayınız.
Ürünü 2-8°C arası sıcaklıklarda (buzdolabında) saklayınız. LUCENTIS kesinlikle dondurulmamalıdır. Ürün donmuş ise çözüp kullanılmamalıdır.
Flakonu ışıktan korumak için orijinal ambalajında saklayınız.
Son kullanma tarihiyle uyumlu olarak kullanınız
Ambalajdaki son kullanma tarihinden sonra LUCENTIS'i kullanmayınız.
Eğer üründe ve/veya ambalajında bozukluklar fark ederseniz LUCENTIS'i kullanmayınız.
Ruhsat sahibi: Novartis Ürünleri 34912 Kurtköy-İstanbul Tel: 0.216 560 10 00 Faks: 0 212 236 45 91
Üretim yeri: Novartis Pharma Stein AG Schaffhauserstrasse, CH-4332 Stein, İsviçre Tel: +41 62 868 6111 Faks: +41 62 868 6611
AŞAĞIDAKİ BİLGİLER BU İLACI UYGULAYACAK SAĞLIK PERSONELİ
İÇİNDİR
LUCENTIS'in hazırlanması ve uygulanması
Sadece intravitreal uygulama için tek kullanımlık flakon. Bir flakonun birden fazla uygulama için kullanılması kontaminasyona ve buna bağlı enfeksiyona yol açabilir.
LUCENTIS, bir "göz hastalıkları uzmanı" tarafından uygulanmalıdır.
LUCENTIS için önerilen doz, tek bir intravitreal enjeksiyon halinde uygulanacak olan 0.5 mg'dır. Bu doz 0.05 ml'lik bir enjeksiyon hacmine denk gelmektedir. İki uygulama arasında geçen süre 1 aydan kısa olmamalıdır.
Yaşa bağlı sarı nokta(makula) dejenerasyonu tedavisinde; LUCENTIS tedavisi birbirini takip eden 3 ay süreyle ayda bir enjeksiyonu içeren bir yükleme fazı ile başlatılmakta ve bunu hastaların aylık olarak görme keskinliğinin izlenmesi gereken bir idame fazı takip etmektedir. Eğer hastanın görme keskinliğinde > 5 harflik bir kayıp varsa (ETDRS ya da bir Snellen sırası eşdeğeri) tekrar LUCENTIS uygulanması gerekmektedir.
DME'den kaynaklanan görme bozukluğunda LUCENTIS tedavisi aylık olarak verilir ve görme keskinliği üç ardışık aylık değerlendirme boyunca (en az iki enjeksiyon anlamına gelir) stabil olana kadar devam edilir. Bu nedenle hastalar görme keskinliği açısından aylık olarak takip edilmelidir.
Takip sırasında DME nedeniyle görme keskinliği kaybı saptandığı durumlarda tedavi aylık olarak tekrar başlatılır ve yine üç ardışık aylık değerlendirme boyunca stabil görme keskinliği elde edilene kadar devam ettirilir.
DME'de Lucentis ve lazer fotokoagülasyon:
Lucentis, daha önce lazer fotokoagülasyon uygulanmış hastalarda ve lazer fotokoagülasyonla eşzamanlı olarak güvenli bir şekilde kullanılabilir. Aynı gün verilmesi durumunda Lucentis lazer fotokoagülasyondan en az 30 dakika sonra uygulanmalıdır.
RVO'ya bağlı maküler ödemden kaynaklanan görme bozukluğu
Tedavi aylık olarak verilir ve LUCENTIS tedavisi görürken yapılan 3 aylık ardışık aylık değerlendirmede stabil görme keskinliği ile doğrulanan maksimum görme keskinliği elde edilene kadar devam edilir. Ardından hastalar görme keskinliği için aylık olarak takip edilmelidir.
Takipte RVO'ya bağlı maküler ödemden kaynaklanan görme keskinliği kaybı görülürse tedaviye aylık enjeksiyonlarla tekrar başlanılır ve yine üç ardışık aylık değerlendirmede stabil görme keskinliği elde edilene kadar devam edilir.
Dal RVO'da (BRVO) Lucentis ve lazer fotokoagülasyon
Lucentis ve lazer fotokoagülasyonu eşzamanlı olarak güvenli bir şekilde uygulanabilir. Aynı gün verildiğinde, Lucentis lazer fotokoagülasyondan en az 30 dakika sonra uygulanmalıdır.
Parenteral kullanımlı bütün tıbbi ürünlerde olduğu gibi, uygulamadan önce LUCENTIS'in partiküllü madde ve renk değişimi açısından görsel olarak incelenmesi gerekmektedir.
Enjeksiyon prosedürü cerrahi el dezenfeksiyonu, steril eldiven, bir steril örtü ve bir steril göz kapağı spekulumu (ya da eşdeğeri) ve steril parasentez mevcudiyetini (gerektiğinde) içeren steril koşullar altında yürütülmelidir. İntravitreal prosedür uygulanmadan önce hastanın aşırı duyarlılık reaksiyonları açısından tıbbi geçmişi dikkatle değerlendirilmelidir. Perioküler cilt, göz kapağı ve oküler yüzey steril edilmelidir. Enjeksiyondan önce yeterli anestezi uygulanmalı ve steril ortam sağlanmalıdır.
Klinik çalışmalarda hastalara her bir enjeksiyondan önce ve sonra 3 gün boyunca günde 4 kere antimikrobiyal göz damlası uygulanmıştır. Ancak doktorun önerisi ile enjeksiyon öncesinde steril şartların sağlanması halinde antimikrobiyal damla enjeksiyon sonrasında uygulanabilir.
LUCENTIS'i intravitreal uygulamaya hazırlamak için aşağıdaki talimatları uygulayınız:
1. İlacı çekmeden önce flakonun lastik tıpasının dış kısmı dezenfekte edilmelidir.
2. 5 mikrometrelik filtreli iğneyi (verilmiştir) ile 1ml'lik şırıngaya (verilmiştir) aseptik teknikle takınız. Küt uçlu iğneyi flakon tıpasının ortasına sokarak flakonun tabanına dokununcaya kadar itiniz.
A.
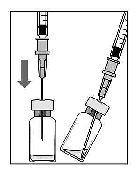
3. Flakondaki tüm sıvıyı flakonu dik pozisyonda tutarak çekiniz, sıvının tamamının çekilmesini kolaylaştırmak için flakonu hafifçe eğiniz.
B.
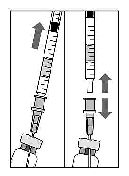
4. Flakonu boşaltırken iğne ucunun tamamen boşaltmak amacıyla piston çubuğun yeteri kadar geri çekildiğinden emin olun.
5. Küt uçlu filtreli iğneyi flakon içinde bırakınız ve küt uçlu filtreli iğneyi şırıngadan çıkarınız. Filtreli iğne flakon içeriğinin çekilmesinden sonra atılmalı ve intrevitreal enjeksiyon için kullanılmamalıdır.
6. Enjeksiyon iğnesini (verilmiştir) aseptik ve sıkı bir şekilde şırıngaya takınız.
7. Şırıngadan enjeksiyon iğnesini ayırmadan dikkatlice enjeksiyon iğnesinin başlığını çıkarınız.
Not: Başlığı çıkarırken enjeksiyon iğnesinin sarı göbek kısmından sıkıca tutunuz.
8. Şırıngadaki havayı dikkatle çıkarınız ve dozu şırınga üzerindeki 0.05 ml işaretine ayarlayınız. Şırınga enjeksiyon için hazırdır.
Not: Enjeksiyon iğnesini silmeyiniz. Pistonu geri çekmeyiniz.
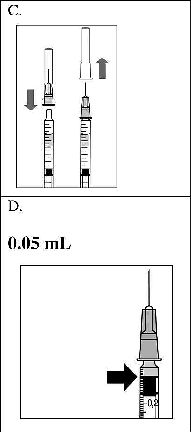
Enjeksiyon iğnesi yatay meridyenden kaçınılarak, gözün merkezi hedeflenerek ve gözün aksiyal uzunluğu göz önünde bulundurularak vitreus boşluğuna doğru limbusun 3.5-4.0 mm açığına batırılmalıdır. Sonra 0.05 ml'lik enjeksiyon hacmi verilmelidir.Daha sonraki enjeksiyonlar farklı sklera kadranına enjekte edilmelidir.
 Diyabet, insülin hormonu ile ilgili problemlerden kaynaklanan bir hastalıktır.
Diyabet, insülin hormonu ile ilgili problemlerden kaynaklanan bir hastalıktır.
 Diyabet, insülin hormonu ile ilgili problemlerden kaynaklanan bir hastalıktır.
Diyabet, insülin hormonu ile ilgili problemlerden kaynaklanan bir hastalıktır.
 Hipertansiyon sürekli anormal derecede yüksek olan kan basıncıdır. Tansiyon
atardamarlarınızdaki kanın basıncıdır.
Hipertansiyon sürekli anormal derecede yüksek olan kan basıncıdır. Tansiyon
atardamarlarınızdaki kanın basıncıdır.
 İnme, beynin hasar görmesinin sonucudur. Bu hasar, beynin bir kısmındaki ya bir kanama
ya da akut kan eksikliği nedeniyle o kısmın geçici ya da kalıcı olarak işlevini yapamamasına
yol açar.
İnme, beynin hasar görmesinin sonucudur. Bu hasar, beynin bir kısmındaki ya bir kanama
ya da akut kan eksikliği nedeniyle o kısmın geçici ya da kalıcı olarak işlevini yapamamasına
yol açar.
 Şizofrenliğin psikiatrik teşhisi hakkında çok fazla anlaşmazlık vardır. Bu
sayfadaki bilgiler, şizofrenliğin teşhisi, nedenleri ve tedavisi hakkındaki faklı teoriler
hakkında bilgi verecektir.
Şizofrenliğin psikiatrik teşhisi hakkında çok fazla anlaşmazlık vardır. Bu
sayfadaki bilgiler, şizofrenliğin teşhisi, nedenleri ve tedavisi hakkındaki faklı teoriler
hakkında bilgi verecektir.
İLAÇ GENEL BİLGİLERİ
Novartis Sağlık,Gıda ve Tarım Ürünleri San. Tic. A.Ş.
| Geri Ödeme Kodu | A10722 |
| Satış Fiyatı | 10592.36 TL [ 17 Dec 2024 ] |
| Önceki Satış Fiyatı | 10592.36 TL [ 2 Dec 2024 ] |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8699504770254 |
| Etkin Madde | Ranibizumab |
| ATC Kodu | S01LA04 |
| Birim Miktar | 10 |
| Birim Cinsi | MG/ML |
| Ambalaj Miktarı | 1 |
| Duyu Organları > Oküler Damar Bozukluğu Ajanları > Ranibizumab |
| İthal ( ref. ülke : Isvicre ) ve Beşeri bir ilaçdır. |
İLAÇ FİYATLARI
| Tarihi | İlaç Fiyatı |
|---|---|
| 17 Dec 2024 | 10,592.36 TL |
| 2 Dec 2024 | 10,592.36 TL |
| 19 Nov 2024 | 10,592.36 TL |
| 8 Nov 2024 | 10,592.36 TL |
| 1 Nov 2024 | 10,592.36 TL |
| 25 Oct 2024 | 10,592.36 TL |
| 18 Oct 2024 | 8,573.18 TL |
| 11 Oct 2024 | 8,573.18 TL |
| 2024 / 2008 İlaç Fiyatları |