LYNPARZA 100 mg film kapl� tablet (56 tablet) K�sa �r�n Bilgisi
{ Olaparib }
1. BE�ER� TIBB� �R�N�N ADI
LYNPARZATM 100 mg film kapl� tablet
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Olaparib 100 mg
Yard�mc� maddeler
Yard�mc� maddeler i�in B�l�m 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Film kapl� tablet.
Bir y�z�nde “OP100” bask�s� bulunan, di�er y�z� d�z, sar� ila koyu sar� renkli, oval, bikonveks tablet.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
LYNPARZA a�a��dakiler i�in endikedir:
Over kanseri Monoterapi olarak;
ilerlemi� (FIGO evre III ve IV) BRCA1/2-mutasyonlu (germ hatt� ve/veya somatik) y�ksek dereceli epitelyal over, fallop t�p� veya primer peritoneal kanser g�r�len ve birinci basamak platin bazl� kemoterapinin tamamlanmas�n� takiben tam ya da k�smi yan�t al�nan yeti�kin hastalara uygulanan idame tedavisinde,
daha �nce platin i�eren kemoterapi sonras� relaps geli�en platin duyarl� (Platin duyarl�l��� son tedavi dozundan en az 6 ay ve �zerinde relaps geli�en hastalard�r.) BRCA mutasyonu (BRCA1/2 mutasyonu, akreditasyon alm�� bir laboratuvarda �al���lm�� olmal�d�r.) pozitif olan y�ksek dereceli epitelyal over t�m�r�, fallop t�p� veya primer peritoneal kanserli hastalar�n platin i�eren ikinci basamak tedavisi sonras� idame tedavisinde endikedir.
Bevasizumabla kombinasyon halinde
ilerlemi� (FIGO evre III ve IV) y�ksek dereceli ser�z epitelyal over kanseri, fallop t�p� kanseri veya primer peritoneal kanser g�r�len ve birinci basamak platin bazl� kemoterapi ve bevasizumab kombinasyon tedavisinin tamamlanmas�n� takiben yan�t veren (tam veya k�smi) ve ECOG Performans durumu 0-1 olan yeti�kin hastalara bevasizumabla kombinasyon halinde uygulanan idame tedavisinde progresyona kadar veya en fazla 24 ay s�reyleendikedir.
Meme kanseri
LYNPARZA, germline BRCA 1 veya 2 mutasyonu olan triple negatif y�ksek riskli (Neoadjuvan tedavi sonras� patolojik rezid�el hastal��� olanlar veya primer cerrahisini olmu� ve patolojik olarak t�m�r �ap� 2 cm �st�nde yada lenf nodu pozitif olan adjuvan tedavisini alm�� hastalar) erken evre meme kanserinde lokal tedaviler ve antrasiklin ve/veya taksan i�eren adjuvan/neoadjuvan kemoterapi tamamland�ktan sonra monoterapi halinde maksimum 1 y�l s�reyle endikedir.
LYNPARZA, germ hatt� BRCA1 veya 2 mutasyonlar�na sahip olan, HER2 negatif metastatik meme kanseri olan yeti�kin hastalar�n�n tedavisinde monoterapi olarak endikedir. Hastalar, bu tedavi i�in uygun olmalar� durumunda, daha �nce (neo)adjuvan veya metastatik ortamda bir antrasiklin ve bir taksan ile tedavi g�rm�� olmal� ve (neo) adjuvan platin temelli bir tedavi alm��larsa son tedaviden itibaren 12 ay ge�mi� olmal�d�r (bkz. b�l�m 5.1).
Hormon resept�r� (HR) pozitif meme kanseri g�r�len hastalar ayn� zamanda �nceki endokrin tedavisi s�ras�nda veya sonras�nda progresyon g�stermi� olmal�d�r veya endokrin tedavisi i�in uygun olmad�klar� y�n�nde de�erlendirme yap�lm�� olmal�d�r.
Pankreas adenokarsinomu
LYNPARZA, birinci basamak platin bazl� kemoterapiyi en az 16 hafta kullan�p hastal��� progresyon g�stermeyen, germ hatt� BRCA1/2-mutasyonlu, metastatik pankreas adenokarsinomlu, ECOG Performans durumu 0-1 olan yeti�kin hastalar�n�n idame tedavisinde monoterapi olarak endikedir.
Prostat kanseri
LYNPARZA, metastatik kastrasyona diren�li prostat kanserinde �nceki enzalutamid veya abireteron tedavisine progresyon g�stermi� ve BRCA1,2 veya ATM mutasyonu olan yeti�kin hastalar�n tedavisinde monoterapi olarak endikedir.
4.2. Pozoloji ve uygulama �ekli
LYNPARZA ile tedavi, anti-kanser t�bbi �r�nlerin kullan�m�nda deneyimli bir hekim taraf�ndan ba�lat�lmal� ve takip edilmelidir.
Hasta Se�imi
BRCA mutasyonlu ileri over kanserinin birinci basamak idame tedavisi:
Y�ksek dereceli epitelyal over kanseri (EOK), fallop t�p� kanseri (FTK) veya primer peritoneal kanserin (PPK) birinci basamak idame tedavisi i�in LYNPARZA tedavisi ba�lat�lmadan �nce hastalar�n meme kanserine duyarl�l�k genleri (BRCA) 1 veya 2'de patojen veya olas� patojen germ hatt� ve/veya somatik mutasyonlara sahip oldu�u valide edilmi� bir test kullan�larak do�rulanmal�d�r.
Platine duyarl� relaps yapm�� over kanserinin idame tedavisi:
Platin bazl� tedaviye tam veya k�smi yan�t veren hastalarda, relaps yapm�� EOK, FTK veya PPK'nin idame tedavisinde monoterapi olarak LYNPARZA kullan�lmas�ndan �nce hastalar�n
meme kanserine duyarl�l�k genleri (BRCA) 1 veya 2'de patojen veya olas� patojen germ hatt� ve/veya somatik mutasyonlara sahip oldu�u valide edilmi� bir test kullan�larak do�rulanmal�d�r.
Bevasizumab ile kombinasyon halinde over kanserinin birinci basamak idame tedavisi:
Bevasizumabla birlikte birinci basamak platin bazl� kemoterapinin tamamlanmas�n� takiben yan�t veren (tam veya k�smi) hastalarda EOK, FTK veya PPK'nin birinci basamak tedavisinde bevasizumabla kombinasyon halinde LYNPARZA i�in meme kanserine duyarl�l�k genleri (BRCA1/2 ) testi yap�lmas�na gerek yoktur.
Germline BRCA-mutasyonlu y�ksek riskli erken meme kanserinin adjuvan tedavisi
Triple negatif, y�ksek riskli erken meme kanserinin adjuvan tedavisi i�in Lynparza ba�lanmadan �nce hastalarda ge�erli bir test ile zararl� veya zararl� oldu�undan ��phe edilen gBRCA1/2 mutasyonu do�rulanmal�d�r (bkz. B�l�m 5.1).
gBRCA1/2-mutasyonlu HER2-negatif metastatik meme kanseri:
Germline meme kanseri duyarl�l�k genleri (gBRCA1/2) mutasyona u�ram�� insan epidermal b�y�me fakt�r� resept�r� 2 (HER2)-negatif metastatik meme kanseri i�in, LYNPARZA tedavisine ba�lanmadan �nce hastalarda zararl� veya ��pheli zararl� bir gBRCA1/2 mutasyonu do�rulanmal�d�r. gBRCA1/2 mutasyon durumu, onaylanm�� bir test y�ntemi kullan�larak deneyimli bir laboratuvar taraf�ndan belirlenmelidir. Meme kanserinde t�m�r BRCA1/2 testlerinin klinik do�rulamas�n� g�steren veriler �u anda mevcut de�ildir.
BRCA mutasyonlu metastatik pankreas adenokarsinomunun birinci basamak idame tedavisi:
Germ hatt� gBRCA1/2 mutasyonlu metastatik pankreas adenokarsinomunun birinci basamak tedavisi i�in LYNPARZA tedavisi ba�lat�lmadan �nce hastalar�n patojenik veya olas� patojenik bulunan gBRCA1/2 mutasyonuna sahip oldu�u do�rulamal�d�r. gBRCA1/2 mutasyonu durumu deneyimli bir laboratuvar taraf�ndan valide edilmi� bir test y�ntemi kullan�larak belirlenmelidir.
BRCA1/2 ya da ATM genlerinde mutasyona u�ram�� metastatik kastrasyona diren�li prostat kanseri:
BRCA1,2 ya da ATM genlerinde mutasyonlu metastatik kastrasyona diren�li prostat kanserinde (mCRPC) LYNPARZA tedavisine ba�lanmadan �nce hastalar�n homolog rekombinasyon onar�m geni mutasyonu do�rulanmal�d�r (bir doku �rne�inden al�nan t�m�r DNA's� veya bir plazma �rne�inden al�nm�� ctDNA veya kan ya da ba�ka bir t�m�r d��� �rnekten elde edilmi� germ hatt� DNA's� kullan�larak). HRR genetik durumu, deneyimli bir laboratuvar taraf�ndan valide edilmi� bir test y�ntemi kullan�larak belirlenmelidir.
![]()
E�er uygulanabilir ise BRCA1/2 veya ATM genlerindeki mutasyonlar a��s�ndan test uygulanan hastalara y�nelik genetik dan��manl�k yerel d�zenlemelere uygun �ekilde verilmelidir.
Pozoloji/uygulama s�kl��� ve s�resi:
LYNPARZA, 100 mg ve 150 mg'l�k tabletler halinde mevcuttur.
LYNPARZA'n�n �nerilen dozu, 600 mg'l�k toplam g�nl�k doza kar��l�k gelecek �ekilde g�nde iki kez al�nan 300 mg'd�r (iki adet 150 mg tablet). 100 mg tablet, dozun azalt�lmas� i�in kullan�lmal�d�r.
LYNPARZA monoterapi:
Platin bazl� kemoterapiye (tam veya k�smi) yan�t veren platine duyarl� n�kseden (PSR) y�ksek dereceli epitelyal over, fallop t�p� veya primer periton kanseri olan hastalar, platin i�eren rejimin son dozu tamamland�ktan en ge� 8 hafta sonra LYNPARZA ile tedaviye ba�lamal�d�r.
Bevasizumabla kombinasyon halinde LYNPARZA
Bevasizumabla birlikte uygulanan birinci basamak platin bazl� tedavinin tamamlanmas�n� takiben y�ksek dereceli epitelyal over kanserine, fallop t�p� kanserine veya primer peritoneal kansere y�nelik birinci basamak idame tedavisinde LYNPARZA ile bevasizumab kombinasyonu uygulan�rken hastalar bevasizumabla kombinasyon halinde LYNPARZA tedavisine son kemoterapi dozlar�n�n tamamlanmas�ndan en az 3 hafta ve en fazla 9 hafta sonra ba�lamal�d�r. LYNPARZA bevasizumab ile kombinasyon halinde kullan�lacak oldu�unda �nerilen dozaj bilgisi i�in bevasizumaba ili�kin �r�n bilgisine ba�vurun (bkz. b�l�m 5.1).
Endokrin tedavi ile kombinasyonda LYNPARZA
�nerilen pozoloji i�in endokrin tedavi kombinasyonu bile�enlerinin (aromataz inhibit�r�/anti- �strojen ajan ve/veya LHRH) �r�n bilgisine ba�vurun.
gBRCA1/2 mutasyonlu metastatik pankreas adenokarsinomu g�r�len hastalar LYNPARZA tedavisine birinci basamak platin bazl� kemoterapilerinin son dozunun tamamlanmas�ndan en ge� 8 hafta sonra ba�lamal�d�r.
Tedavi s�resi
BRCA mutasyonlu ilerlemi� over kanserinin birinci basamak idame tedavisi:
Tedavi marker y�ksekli�i ve/veya radyolojik hastal�k progresyonu veya kabul edilemez toksisite geli�ene kadar verilebilir. Maksimum tedavi s�resi 2 y�ld�r.
BRCA mutasyonlu platine duyarl� relaps yapm�� over kanserinin idame tedavisi:
BRCA mutasyonlu platine duyarl� relaps yapm�� y�ksek dereceli epitelyal over, fallop t�p� veya primer peritoneal kanser g�r�len hastalarda tedavinin altta yatan hastal���n progresyonuna veya kabul edilemez toksisiteye kadar s�rd�r�lmesi �nerilmektedir.
BRCA mutasyonlu metastatik pankreas adenokarsinomunun birinci basamak idame tedavisi: Altta yatan hastal���n progresyonuna veya kabul edilemez toksisiteye kadar tedaviye devam edilmesi �nerilmektedir.
BRCA1/2 veya ATM -geni mutasyonlu metastatik kastrasyona diren�li prostat kanseri:
Altta yatan hastal���n progresyonuna veya kabul edilemez toksisiteye kadar tedaviye devam edilmesi �nerilmektedir. Cerrahi kastrasyon uygulanm�� olmayan hastalarda tedavi s�ras�nda l�teinizan hormon salg�lat�c� hormon (LHRH) analogu kullan�larak ila�la kastrasyona devam edilmelidir.
�lerlemi� over kanserinin bevasizumab ile kombinasyon halinde birinci basamak idame tedavisi:
Hastalar radyolojik hastal�k progresyonu, kabul edilemez toksisite veya 2 y�l tedaviden sonra radyolojik hastal�k kan�t� yoksa 2 y�la kadar tedaviye devam edebilir. Tedaviyi uygulayan doktorun g�r���ne g�re devam eden LYNPARZA tedavisinden ilave yarar elde edebilecek olan ve 2. y�lda hastal�k kan�t� sergileyen hastalara 2 y�ldan daha uzun s�re tedavi uygulanabilir. LYNPARZA bevasizumab ile kombinasyon halinde kullan�lacak oldu�unda �nerilen tedavi s�resi i�in bevasizumaba ili�kin �r�n bilgisine ba�vurun (bkz. b�l�m 5.1).
Over kanseri hastalar�nda ilk veya sonraki relaps� takiben LYNPARZA ile tekrar idame tedavisi uygulanmas� konusunda herhangi bir etkililik veya g�venlilik verisi yoktur (bkz. b�l�m 5.1).
Germline BRCA-mutasyonlu, y�ksek riskli meme kanserinin adjuvan tedavisi
Hastalar�n 1 y�la veya hastal�k n�ks�ne veya kabul edilemez toksisite geli�imine dek, hangisi �nce ger�ekle�irse, tedavi edilmesi �nerilir.
gBRCA1/2-mutasyonlu HER2-negatif metastatik meme kanseri:
Altta yatan hastal�k veya kabul edilemez toksisitenin ilerlemesine kadar tedaviye devam edilmesi �nerilir.
Dozun unutulmas�
E�er hastalar bir LYNPARZA dozunu almay� unuturlarsa, bir sonraki normal dozu planl� saatinde almal�d�r.
Advers reaksiyonlar i�in doz ayarlamalar�
Bulant�, kusma, diyare ve anemi gibi advers reaksiyonlar�n y�netimi i�in tedaviye ara verilebilir ve dozun azalt�lmas� d���n�lebilir (bkz. B�l�m 4.8).
�nerilen doz azalt�m� g�nde iki kez 250 mg'd�r (bir adet 150 mg tablet ve bir adet 100 mg tablet; 500 mg'l�k toplam g�nl�k doza e�de�er).
E�er dozun daha fazla azalt�lmas� gerekirse, g�nde iki kez 200 mg'a (iki adet 100 mg tablet; 400 mg'l�k toplam g�nl�k doza e�de�er) azalt�lmas� �nerilir.
CYP3A inhibit�rleri ile e�zamanl� uygulama i�in doz ayarlamalar�
LYNPARZA'n�n g��l� veya orta derecede g��l� CYP3A inhibit�rleri ile e�zamanl� uygulanmas� �nerilmemektedir ve alternatif ila�lar d���n�lmelidir. E�er g��l� bir CYP3A inhibit�r� ile e�zamanl� kullan�lmas� gerekiyorsa, LYNPARZA dozunun g�nde iki kez 100 mg'a (bir adet 100 mg tablet; 200 mg'l�k toplam g�nl�k doza e�de�er) azalt�lmas� �nerilir. E�er orta derece g��l� bir CYP3A inhibit�r� ile e�zamanl� kullan�lmas� gerekiyorsa, LYNPARZA dozunun g�nde iki kez 150 mg'a (bir adet 150 mg tablet; 300 mg'l�k toplam g�nl�k doza e�de�er) azalt�lmas� �nerilir (bkz. B�l�m 4.4 ve B�l�m 4.5).
Uygulama �ekli:
LYNPARZA oral kullan�m i�indir.
LYNPARZA tabletler b�t�n halde yutulmal� ve �i�nenmemeli, ezilmemeli, ��z�lmemeli ve b�l�nmemelidir. LYNPARZA tabletler a� veya tok karn�na al�nabilir.
�zel pop�lasyonlara ili�kin ek bilgiler:
B�brek yetmezli�i:
LYNPARZA'n�n �nerilen dozu g�nde iki kez 200 mg'd�r (iki adet 100 mg tablet; 400 mg'l�k toplam g�nl�k doza e�de�er) (bkz. B�l�m 5.2).
LYNPARZA, hafif derecede b�brek yetmezli�i (kreatinin klirensi 51 ila 80 mL/dk) olan hastalara herhangi bir doz ayarlamas� yap�lmadan uygulanabilir.
LYNPARZA'n�n a��r derecede b�brek yetmezli�i ya da son evre b�brek hastal��� (kreatinin klirensi ≤30 mL/dk) olan hastalarda kullan�m�, bu hastalardaki g�venlilik ve etkililik �al���lmam�� oldu�undan �nerilmemektedir. LYNPARZA a��r derecede b�brek yetmezli�i olan hastalarda ancak beklenen yarar, muhtemel risklere a��r bast��� takdirde kullan�labilir ve hasta b�brek fonksiyonlar� ve advers olaylar a��s�ndan dikkatle izlenmelidir.
Karaci�er yetmezli�i:
LYNPARZA, hafif ve orta derecede karaci�er yetmezli�i (Child-Pugh A veya B S�n�f�) olan hastalara herhangi bir doz ayarlamas� yap�lmadan uygulanabilir (bkz. B�l�m 5.2). LYNPARZA'n�n a��r derecede karaci�er yetmezli�i (Child-Pugh C S�n�f� olan hastalarda kullan�lmas�, bu hastalardaki g�venlili�i ve etkilili�i �al���lmam�� oldu�undan �nerilmemektedir.
Pediyatrik pop�lasyon:
LYNPARZA'n�n �ocuklarda ve adolesanlarda g�venlili�i ve etkilili�i belirlenmemi�tir. Veri mevcut de�ildir.
Geriyatrik pop�lasyon:
Ya�l�lar i�in ba�lang�� dozunda herhangi bir ayarlama gerekmemektedir.
Di�er:
Beyaz �rka mensup olmayan hastalar:
Beyaz �rka mensup olmayan hastalarda s�n�rl� klinik veri mevcuttur. Bununla birlikte etnik k�kene dayal� herhangi bir doz ayarlamas� gerekmemektedir (bkz. B�l�m 5.2).
4.3. Kontrendikasyonlar
Olaparibe veya B�l�m 6.1'de listelenen yard�mc� maddelerden herhangi birine kar�� a��r� duyarl�l�kta ya da,
Tedavi s�ras�nda ve son doz al�nd�ktan sonra 1 ay boyunca emzirmede (bkz. B�l�m 4.6).
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Hematolojik toksisite
LYNPARZA ile tedavi edilen hastalarda, genellikle hafif veya orta �iddetli (CTCAE derece 1 veya 2) anemi, n�tropeni, trombositopeni ve lenfopeninin klinik tan�lar�n� ve/veya laboratuvar bulgular�n� i�eren hematolojik toksisite bildirilmi�tir. �nceki anti-kanser tedavisinin neden oldu�u hematolojik toksisiteleri d�zelene kadar (hemoglobin, trombosit ve n�trofil d�zeyleri
≤ CTCAE derece 1 olmal�d�r) hastalar�n LYNPARZA ile tedaviye ba�lamamalar� gerekir. Tedavi s�ras�nda herhangi bir parametredeki klinik olarak anlaml� de�i�ikliklerin izlenebilmesi i�in tedavi �ncesi (ba�lang��) tam kan say�m�, bunu takiben tedavinin ilk 12 ay� s�resince ayl�k takip ve ard�ndan periyodik takip �nerilir (bkz. B�l�m 4.8).
LYNPARZA uygulamas�na ara verildikten 4 hafta sonra kan parametreleri halen klinik olarak anormal seyrediyorsa, kemik ili�i analizi ve/veya kan sitogenetik analizi �nerilir.
Miyelodisplastik Sendrom/Akut Miyeloid L�semi (MDS/AML)
LYNPARZA monoterapisi ile yap�lan klinik �al��malarda tedavi edilen hastalarda, uzun s�reli sa�kal�m takibi de dahil olmak �zere, miyelodisplastik sendrom/akut miyeloid l�seminin (MDS/AML) genel insidans� < %1,5 olup bu insidans, �nceden en az iki basamak platin kemoterapi alm�� ve 5 y�l boyunca takip edilmi� BRCAm platin duyarl� n�ks etmi� yumurtal�k kanseri hastalar�nda daha y�ksektir (bkz. b�l�m 4.8). Olaylar�n �o�u �l�mle sonu�lanm��t�r. MDS/AML geli�en hastalarda olaparib ile tedavi s�resi <6 ay ile >4 y�l aras�nda de�i�mi�tir.
MDS/AML'den ��pheleniliyorsa, hasta kemik ili�i analizi ve sitogenetik i�in kan numunesi al�nmas� dahil olmak �zere ileri ara�t�rmalar i�in bir hematolo�a sevk edilmelidir. Uzun s�reli hematolojik toksisite ara�t�rmas�n�n ard�ndan MDS/AML do�rulan�rsa, LYNPARZA kesilmeli ve hasta uygun �ekilde tedavi edilmelidir.
Ven�z Tromboembolik Olaylar
LYNPARZA ile tedavi edilen hastalarda a��rl�kl� olarak pulmoner emboli olaylar� olmak �zere ven�z tromboembolik olaylar meydana gelmi�tir ve tutarl� bir klinik paterni yoktur. Di�er onaylanm�� endikasyonlarla kar��la�t�r�ld���nda, ayn� zamanda androjen deprivasyon tedavisi alan metastatik kastrasyona diren�li prostat kanseri olan hastalarda daha y�ksek bir insidans g�zlenmi�tir (bkz. b�l�m 4.8). Hastalar ven�z tromboz ve pulmoner emboli klinik belirtileri ve semptomlar� a��s�ndan izlenmeli ve t�bbi a��dan uygun �ekilde tedavi edilmelidir. Daha �nce VTE �yk�s� olan hastalar daha fazla risk alt�nda olabilir ve uygun �ekilde izlenmelidir.
Pn�monit
�l�mle sonu�lanan olaylar� da i�eren pn�monit, klinik �al��malarda LYNPARZA ile tedavi edilen hastalar�n <%1,0'�nda bildirilmi�tir. Pn�monit bildirimlerinde tutarl� bir patern yoktur ve bir dizi yatk�nl�k olu�turucu fakt�r (akci�er kanseri ve/veya akci�erlere metastazlar, altta yatan pulmoner hastal�k, sigara �yk�s� ve/veya �nceden kemoterapi ve radyoterapi alm�� olmak) de�erlendirmeyi g��le�tirmi�tir. LYNPARZA klinik �al��malarda (g�venlik havuzundan de�erlendirilen) di�er tedaviler ile kombinasyon halinde kullan�ld���nda, �l�mc�l sonu�lar� olan olaylar g�r�lm��t�r. Hastalarda dispne, �ks�r�k ve ate� gibi yeni veya k�t�le�en respiratuvar semptomlar geli�irse ya da anormal g���s radyolojik bulgusu g�zlenirse, LYNPARZA tedavisine ara verilmeli ve derhal inceleme ba�lat�lmal�d�r. E�er pn�monit do�rulan�rsa, LYNPARZA tedavisi kesilmeli ve hastalar uygun �ekilde tedavi edilmelidir.
Embriyofetal toksisite
Etki mekanizmas�na (PARP inhibisyonu) dayan�larak, LYNPARZA, gebe kad�nlara uyguland���nda fetal zarara neden olabilir. S��anlar �zerinde y�r�t�len klinik d��� �al��malar olaparibin embriyofetal sa�kal�m �zerinde advers etkiler g�sterdi�ini ve g�nde iki kez 300 mg olarak �nerilen insan dozunda beklenenlerin alt�ndaki maruziyetlerde maj�r fetal malformasyonlar� tetikledi�ini g�stermi�tir.
Gebelik/Kontrasepsiyon
Lynparza gebelik s�ras�nda kullan�lmamal�d�r. �ocuk do�urma potansiyeli olan kad�nlar, Lynparza tedavisine ba�lamadan �nce, tedavi s�ras�nda ve son Lynparza dozunu ald�ktan sonra 1 ay boyunca iki adet g�venilir kontrasepsiyon y�ntemi kullanmal�d�r. �ki adet y�ksek etkili ve tamamlay�c� kontrasepsiyon y�ntemi �nerilmektedir. Erkek hastalar ve �ocuk do�urma potansiyeli olan kad�n partnerleri, tedavi s�ras�nda ve son Lynparza dozunu ald�ktan sonra 3 ay boyunca g�venilir bir kontrasepsiyon y�ntemi kullanmal�d�r (bkz. B�l�m 4.6).
Etkile�imler
LYNPARZA'n�n g��l� veya orta derecede g��l� CYP3A inhibit�rleri ile e�zamanl� uygulanmas� �nerilmemektedir (bkz. B�l�m 4.5). E�er g��l� veya orta derecede g��l� bir CYP3A inhibit�r� ile e�zamanl� uygulanmas� gerekiyorsa, LYNPARZA dozu azalt�lmal�d�r (bkz. B�l�m 4.2 ve B�l�m 4.5).
LYNPARZA'n�n g��l� veya orta derecede g��l� CYP3A ind�kleyicileri ile e�zamanl� uygulanmas� �nerilmemektedir. E�er halihaz�rda LYNPARZA almakta olan bir hastan�n, g��l� veya orta derecede g��l� bir CYP3A ind�kleyicisi ile tedavi edilmesi gerekiyorsa, hekim, LYNPARZA'n�n etkisinin �nemli �l��de azalaca��n� bilmelidir (bkz. B�l�m 4.5).
Bu t�bbi �r�n her tablette 1 mmol'den (23 mg) daha az sodyum i�erir, dolay�s�yla esas�nda “sodyum i�ermedi�i” kabul edilebilir.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Farmakodinamik etkile�imler
DNA'ya zarar veren ila�lar da dahil olmak �zere di�er anti-kanser ila�lar� ile kombinasyon halinde olaparibin incelendi�i klinik �al��malar, miyelosupresif toksisitenin artt���na ve s�resinin uzad���na i�aret etmektedir. �nerilen LYNPARZA monoterapi dozu, miyelosupresif anti-kanser t�bbi �r�nleri ile kombinasyon i�in uygun de�ildir.
Olaparibin a��lar veya immunosupresan ila�lar ile kombinasyonu �al���lmam��t�r. Bu nedenle, e�er bu ila�lar LYNPARZA ile e�zamanl� kullan�l�yorsa, dikkatli olunmal� ve hastalar yak�ndan takip edilmelidir.
Farmakokinetik etkile�imler
Di�er ila�lar�n olaparib �zerindeki etkisi
CYP3A4/5'ler, a��rl�kl� olarak olaparibin metabolik klirensinden sorumlu olan izoenzimlerdir.
kullan�lacaksa g�nde iki kez 150 mg'a (300 mg'l�k toplam g�nl�k doza e�de�er) azalt�lmas� �nerilir (bkz. B�l�m 4.2 ve B�l�m 4.4). Ayr�ca, LYNPARZA tedavisi s�ras�nda, bir CYP3A inhibit�r� oldu�undan greyfurt suyunun t�ketilmemesi �nerilir.
Bilinen bir CYP3A ind�kleyicisi olan rifampisinin etkisini de�erlendirmek i�in y�r�t�len bir klinik �al��mada, olaparib ile e�zamanl� uygulama durumunda ortalama olaparib Cde�erinin %71 (%90 GA: %76-67) ve ortalama EAA de�erinin %87 (%90 GA: %89-84) azald��� g�sterilmi�tir. Bu nedenle, bu enzimin bilinen g��l� ind�kleyicilerinin (�rn., fenitoin, rifampisin, rifapentin, karbamazepin, nevirapin, fenobarbital ve sar� kantaron) LYNPARZA ile kullan�lmas� �nerilmemektedir; ��nk� LYNPARZA'n�n etkilili�inin �nemli �l��de azalma ihtimali bulunmaktad�r. Orta ila g��l� ind�kleyicilerin (�rn., efavirenz, rifabutin) olaparib maruziyeti �zerindeki etkilerinin boyutu belirlenmemi�tir, dolay�s�yla LYNPARZA'n�n bu ila�larla birlikte uygulanmas� �nerilmemektedir (bkz. B�l�m 4.4).
Olaparibin di�er ila�lar �zerindeki etkileri
Olaparib in vitro olarak CYP3A4'� inhibe eder ve in vivo olarak hafif CYP3A inhibit�r� oldu�u tahmin edilmektedir. Bu nedenle, duyarl� CYP3A substratlar� veya dar terap�tik indekse sahip substratlar (�rn., simvastatin, sisaprid, siklosporin, ergot alkaloidleri, fentanil, pimozid, sirolimus, takrolimus ve ketiapin) LYNPARZA ile kombine edildi�inde dikkatli olunmal�d�r. Dar terap�tik indekse sahip CYP3A substratlar� ile e�zamanl� olarak LYNPARZA kullanan hastalar�n uygun klinik izlemi �nerilmektedir.
CYP1A2, 2B6 ve 3A4'�n ind�klenmesi in vitro olarak g�sterilmi�tir, klinik olarak anlaml� boyutta ind�klenmesi en muhtemel olan CYP2B6'd�r. Olaparibin CYP2C9, CYP2C19 ve P- gp'yi ind�kleme potansiyeli de g�z ard� edilemez. Bu nedenle, birlikte uyguland���nda olaparib, bu metabolik enzimlerin substratlar�na maruziyeti ve ta��y�c� proteinleri azaltabilir. Baz� hormonal kontraseptiflerin etkilili�i, olaparib ile birlikte uyguland���nda azalabilir (ayr�ca bkz. B�l�m 4.4 ve 4.6).
In vitro olarak, olaparib, efl�ks ta��y�c�s� P-gp'yi (IC50 = 76µM) inhibe eder, bu nedenle, olaparib'in P-gp substratlar� (�rn., Simvastatin, pravastatin, dabigatran, digoksin ve kol�isin) ile klinik olarak anlaml� ila� etkile�imlerine neden olabilece�i g�z ard� edilemez. E� zamanl� olarak bu tip t�bbi �r�nleri alan hastalar i�in uygun klinik izlem �nerilmektedir.
�n vitro olarak, olaparibin BCRP, OATP1B1, OCT1, OCT2, OAT3, MATE1 ve MATE2K'nin bir inhibit�r� oldu�u g�sterilmi�tir. Olaparibin BCRP (�rn. metotreksat, rosuvastatin), OATP1B1 (�rn. bosentan, glibenklamid, repaglinid, statinler ve valsartan), OCT1 (�rn. metformin), OCT2 (�rn. serum kreatinin), OAT3 (�rn. furosemid ve metotreksat), MATE1 (�rn. metformin) ve MATE2K (�rn. metformin) substratlar�na maruziyeti artt�rabilece�i g�z ard� edilemez. Olaparib, �zellikle bir statin ile kombinasyon halinde verildi�inde dikkatli olunmal�d�r.
Anastrozol, letrozol ve tamoksifen ile kombinasyon
Olaparib ile anastrozol, letrozol veya tamoksifen kombinasyonunu de�erlendirmek i�in klinik bir �al��ma yap�lm��t�r. Anastrozol veya letrozol ile anlaml� etkile�im g�zlenmezken, tamoksifen olaparibe maruziyeti % 27 oran�nda azaltm��t�r. Bu etkinin klinik anlaml�l��� bilinmemektedir. Olaparib, tamoksifenin farmakokineti�ini etkilemez.
4.6. Gebelik ve laktasyon
Genel tavsiye
Gebelik Kategorisi: D
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
�ocuk do�urma potansiyeli bulunan kad�nlar�n, LYNPARZA tedavisi g�rd�kleri s�re boyunca gebe kalmamalar� ve tedaviye ba�lad�klar�nda gebe olmamalar� gerekir. Tedavi �ncesinde �ocuk do�urma potansiyeli olan t�m kad�nlara hamilelik testi yap�lmal� ve tedavi s�resince d�zenli olarak testin yap�lmas� g�z �n�nde bulundurulmal�d�r.
�ocuk do�urma potansiyeli olan kad�nlar, Lynparza tedavisine ba�lamadan �nce, tedavi s�ras�nda ve son Lynparza dozunu ald�ktan sonra 1 ay boyunca, se�ilen kontrasepsiyon y�ntemi cinsel perhiz olmad�k�a, iki adet g�venilir kontrasepsiyon y�ntemi kullanmal�d�r (bkz. B�l�m 4.4). �ki adet y�ksek etkili ve tamamlay�c� kontrasepsiyon y�ntemi �nerilmektedir.
Olaparibin enzim ind�ksiyonu yoluyla CYP2C9 substratlar�na maruziyeti azaltabilece�i g�z ard� edilemeyece�inden, olaparib ile birlikte uyguland���nda baz� hormonal kontraseptiflerin etkinli�i azalabilir. Bu nedenle, tedavi s�ras�nda ek bir hormonal olmayan kontraseptif y�ntem uygulanmas� d���n�lmelidir (bkz. b�l�m 4.5). Hormona ba�l� kanseri olan kad�nlar i�in iki adet hormonal olmayan kontraseptif y�ntem d���n�lmelidir.
Erkeklerde kontrasepsiyon
Olaparib veya metabolitlerinin seminal s�v�ya ge�ip ge�medi�i bilinmemektedir. Erkek hastalar tedavi s�ras�nda ve son Lynparza dozunu almalar�n� takip eden 3 ay s�resince hamile veya �ocuk do�urma potansiyeline sahip olan bir kad�nla girilen cinsel ili�ki s�ras�nda prezervatif kullanmal�d�r. Ayn� zamanda erkek hastalar�n kad�n partnerleri de �ocuk do�urma potansiyeline sahip olmalar� durumunda y�ksek d�zeyde etkili bir do�um kontrol y�ntemi uygulamal�d�r (bkz. b�l�m 4.4). Erkek hastalar tedavi s�ras�nda ve son Lynparza dozunu almalar�n� takip eden 3 ay s�resince sperm ba���� yapmamal�d�r.
Gebelik d�nemi
Olaparibin gebelik ve/veya fetus/yeni do�an �zerinde zararl� farmakolojik etkileri bulunmaktad�r. Hayvanlar ile ger�ekle�tirilen �al��malarda, s��anlar �zerinde, insanlarda kullan�lan terap�tik dozlardan daha d���k maternal sistemik maruziyetlerde, ciddi teratojenik etkiler ve embriyofetal sa�kal�m �zerindeki etkileri i�eren �reme toksisitesi g�sterilmi�tir (bkz. B�l�m 5.3). Olaparibin gebe kad�nlarda kullan�m�na ili�kin veri bulunmamaktad�r; ancak olaparibin etki mekanizmas�na dayan�larak, LYNPARZA gebelik d�neminde ve �ocuk do�urma potansiyeli olup tedavi s�resince ve LYNPARZA'n�n son dozunu ald�ktan sonra bir ay s�reyle g�venilir bir do�um kontrol y�ntemi uygulamayan kad�nlarda kullan�lmamal�d�r (Do�um kontrol� ve gebelik testi hakk�nda daha fazla bilgi i�in yukar�daki “�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)” b�l�m�ne bak�n�z).
Laktasyon d�nemi
Olaparibin s�t ile at�ld���na ili�kin hayvan �al��mas� bulunmamaktad�r. Olaparibin veya metabolitlerinin insan s�t� ile at�l�p at�lmad��� bilinmemektedir. �r�n�n farmakolojik �zelli�i g�z �n�nde bulunduruldu�unda, emzirme s�resince ve son doz al�nd�ktan sonra bir ay boyunca LYNPARZA kontrendikedir (bkz. B�l�m 4.3).
�reme yetene�i/Fertilite
Fertilite hakk�nda klinik veri bulunmamaktad�r. Hayvanlar �zerinde ger�ekle�tirilen �al��malarda konsepsiyon �zerinde bir etki g�zlenmemi�tir; ancak embriyofetal sa�kal�m �zerinde advers etkiler s�z konusudur (bkz. B�l�m 5.3).
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
LYNPARZA'n�n ara� ve makine kullanma becerisi �zerinde orta derecede bir etkisi bulunmaktad�r. LYNPARZA ile tedavi s�ras�nda asteni, yorgunluk veya sersemlik hali bildirilmi�tir. Bu semptomlar� ya�ayan hastalar ara� veya makine kullan�rken dikkatli olmal�d�r.
4.8. �stenmeyen etkiler
G�venlilik profilinin �zeti
LYNPARZA monoterapisi genellikle hafif veya orta derece �iddetli olan (CTCAE derece 1 veya 2) ve genellikle tedavinin kesilmesini gerektirmeyen advers reaksiyonlar ile ili�kilendirilmi�tir. T�m klinik �al��malarda LYNPARZA monoterapisi (≥%10) alan hastalarda en s�k g�zlenen advers reaksiyonlar; bulant�, bitkinlik, anemi, kusma, diyare, i�tah azalmas�, ba� a�r�s�, disguzi, �ks�r�k, n�tropeni, dispne, ba� d�nmesi, dispepsi, l�kopeni ve trombositopeni olmu�tur.
Hastalar�n %2'sinde ortaya ��kan derece ≥3 advers reaksiyonlar anemi (%15), n�tropeni (%5), bitkinlik/asteni (%4), l�kopeni (%3) ve trombositopeni (%2) olmu�tur.
Monoterapide doza ara verilmesine ve/veya azalt�lmas�na en yayg�n �ekilde neden olan advers reaksiyonlar anemi (%16), kusma (%6), bulant� (%7), bitkinlik/asteni (%6) ile n�tropeni (%6) olmu�tur. �lac�n kal�c� �ekilde b�rak�lmas�na en yayg�n �ekilde neden olan advers reaksiyonlar anemi (%1,7), trombositopeni (%0,7), bitkinlik/asteni (%0,8),bulant� (%0,9), n�tropeni (%0.6) ve kusma (%0.5) olmu�tur.
Lynparza, bevasizumab ile kombinasyon halinde kullan�ld���nda, g�venlilik profili genellikle tedaviler tek ba��na uyguland���ndaki ile uyumludur.
Advers olaylar, bevasizumab ile birlikte kullan�ld���nda hastalar�n %57sinde doza ara verilmesine ve/veya azalt�lmas�na yol a�m�� ve hastalar�n %20'sinde olaparib/bevasizumab ve
%6's�nda plasebo/bevasizumab ile tedavinin kal�c� olarak kesilmesine yol a�m��t�r. Doza ara verilmesine ve/veya azalt�lmas�na en s�k neden olan advers reaksiyonlar anemi (%22), bulant� (%10) ve yorgunluk/asteni (%5) olmu�tur. �lac�n kal�c� olarak kesilmesine en s�k neden olan advers reaksiyonlar anemi (%3,6), bulant� (%3,4) ve yorgunluk/asteni (%1,5) olmu�tur.
Advers olaylar, abirateron ile birlikte kullan�ld���nda hastalar�n %46,9'unda olaparib dozunun kesilmesine veya azalt�lmas�na ve hastalar�n s�ras�yla %16,2 ve %8,1'inde olaparib/abirateron ve plasebo/abirateron tedavisinin kesilmesine neden olmu�tur. Dozun kesilmesine ve/veya azalt�lmas�na en yayg�n �ekilde neden olan advers reaksiyonlar anemi (%15,6), bulant� (%3), bitkinlik/asteni (%2,6) ve n�tropeni (%2,1) �eklindeydi. Kal�c� olarak kesilmesine neden olan en yayg�n advers reaksiyon anemi (%4,1) idi.
![]()
Advers reaksiyonlar�n listesi
G�venlilik profili, klinik �al��malardaterap�tikendikasyonda�nerilen dozda solid t�m�rlerle
LYNPARZA monoterapisi ile tedavi edilen 4098 hastaya ait veri havuzuna dayanmaktad�r.
Hasta maruziyetinin bilindi�i LYNPARZA monoterapisi alan hastalar�n incelendi�i klinik �al��malarda a�a��daki advers reaksiyonlar tan�mlanm��t�r. Advers ila� reaksiyonlar� MedDRA Sistem Organ S�n�f�na (SOC) ve ard�ndan MedDRA tercih edilen terime g�re listelenmektedir. Her bir SOC i�inde terimler azalan s�kl��a ve sonras�nda azalan ciddiyet derecesine g�re d�zenlenmi�tir. S�kl�klar �u �ekilde tan�mlanmaktad�r: �ok yayg�n (≥1/10); yayg�n (≥1/100 ila
<1/10); yayg�n olmayan (≥1/1.000 ila <1/100); seyrek (≥1/10,000 ila <1/1.000); �ok seyrek (<1/10,000); bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Tablo 1.LYNPARZA i�in bildirilen advers reaksiyonlar�n listesi
| Advers reaksiyonlar | |
MedDRA Sistem Organ S�n�f� | T�m CTCAE derecelerinin s�kl��� | CTCAE derece ≥3 s�kl��� |
Benign, malign ve | Yayg�n olmayan | Yayg�n olmayan |
tan�mlanmam�� (kist | Miyelodisplastik sendrom/ Akut | Miyelodisplastik sendrom/ Akut |
ve polipler dahil) | miyeloid l�semi | miyeloid l�semi |
neoplaziler |
|
|
Kan ve lenfatik | �ok yayg�n | �ok yayg�n |
sistem hastal�klar� | Anemi, N�tropeni, L�kopeni | Anemi |
| Yayg�n | Yayg�n |
| Lenfopeni Trombositopeni, | N�tropeni, Trombositopeni, L�kopeni |
|
| Lenfopeni |
�mm�n sistem hastal�klar� | Yayg�n olmayan A��r� duyarl�l�k, | Nadir A��r� duyarl�l�k |
| Nadir Anjiyo�dem |
|
Metabolizma ve beslenme bozukluklar� | �ok yayg�n ��tahs�zl�k | Yayg�n olmayan ��tahs�zl�k |
Sinir sistemi hastal�klar� | �ok yayg�n Ba� d�nmesi, Ba� a�r�s�, Tat alma duyusunda de�i�iklik | Yayg�n olmayan Ba� d�nmesi, Ba� a�r�s� |
Solunum, g���s | �ok yayg�n | Yayg�n |
bozukluklar� ve | �ks�r�k, Dispne | Dispne |
mediastinal |
| Yayg�n olmayan |
hastal�klar |
| �ks�r�k |
Gastrointestinal | �ok yayg�n | Yayg�n |
hastal�klar | Kusma, Diyare, Bulant�, Dispepsi | Kusma, Bulant� |
| Yayg�n | Yayg�n olmayan |
| Stomatit, �st abdominal a�r� | Stomatit, Diyare |
|
| Nadir |
|
| Dispepsi, �st abdominal a�r� |
Deri ve deri alt� dokusu bozukluklar� | Yayg�n D�k�nt� | Yayg�n olmayan D�k�nt� |
| Yayg�n olmayan Dermatit Nadir Eritema nodozum |
Nadir Dermatit |
Genel bozukluklar ve uygulama yerine ili�kin hastal�klar | �ok yayg�n Yorgunluk (asteni dahil) | Yayg�n Yorgunluk (asteni dahil) |
Tetkikler | Yayg�n Kan kreatinin d�zeyinde art��
Yayg�n olmayan Ortalama h�cre hacminde art�� | Nadir Kan kreatinin d�zeyinde art�� |
Ara�t�rmalar | Yayg�n Kanda kreatinin art��� Yayg�n olmayan Ortalama h�cre hacmi art��� | Seyrek Kanda kreatinin art��� |
Vask�ler bozukluklar | Yayg�n Ven�z tromboembolizm | Yayg�n Ven�z tromboembolizm |
a MDS/AML akut miyeloid l�semi, miyelodisplastik sendrom ve miyeloid l�seminin Tercih Edilen Terimlerini (PT) kapsar.
Anemi, anemi, makrositik anemi, eritropeni, hematokrit azalmas�, hemoglobin azalmas�, normokromik anemi, normokromik normositik anemi, normositik anemi ve k�rm�z� kan h�cresi say�m�nda azalma tercih edilen terimlerini (PT'lerini) i�erir; N�tropeni, agran�lositoz, ate�li n�tropeni, gran�losit say�s�nda azalma, gran�lositopeni, idiyopatik n�tropeni, n�tropeni, n�tropenik enfeksiyon, n�tropenik sepsis ve n�trofil say�s�nda azalma PT'lerini i�erir; Trombositopeni, trombosit say�s�nda azalma, trombosit �retiminde azalma, plateletkrit azalmas� ve trombositopeni PT'lerini i�erir; L�kopeni, l�kopeni ve beyaz kan h�cresi say�m�nda azalma PT'lerini i�erir; Lenfopeni, B-lenfosit say�s�nda azalma, lenfosit say�s�nda azalma, lenfopeni ve T-lenfosit say�s�nda azalma PT'lerini i�erir; �ks�r�k, �ks�r�k ve balgaml� �ks�r�k PT'lerini i�erir; A��r� duyarl�l�k, ila� a��r� duyarl�l��� ve a��r� duyarl�l�k PT'lerini i�erir; Dispne, dispne ve eforla dispne PT'lerini i�erir; Stomatit, aft�z �lser, a��z �lseri ve stomatit PT'lerini i�erir; D�k�nt�, eksfolyatif d�k�nt�, yayg�n eritem, d�k�nt�, eritemat�z d�k�nt�, yayg�n d�k�nt�, mak�ler d�k�nt�, mak�lo-pap�ler d�k�nt�, pap�ler d�k�nt� ve ka��nt�l� d�k�nt� PT'lerini i�erir; Dermatit, dermatit, alerjik dermatit ve eksfolyatif dermatit PT'lerini i�erir.
* Pazarlama sonras� ortamda g�zlemlendi�i gibi
Se�ili advers reaksiyonlar�n tan�m�
Hematolojik toksisite
Anemi ve di�er hematolojik toksisiteler genellikle d���k dereceli (CTCAE derece 1 veya 2) idi, ancak CTCAE derece 3 ve daha y�ksek olaylar bildirilmi�tir. Anemi ve di�er hematolojik toksisiteler genellikle d���k dereceli (CTCAE derece 1 veya 2) idi, ancak CTCAE derece 3 ve daha y�ksek olaylar bildirilmi�tir. Aneminin ilk ba�lang�c�na kadar ge�en medyan s�re yakla��k 4 hafta idi (CTCAE derece ≥ 3 olaylar i�in yakla��k 7 hafta). Anemi, doz kesintileri ve dozun azalt�lmas� ile (b�l�m 4.2'ye bak�n�z) ve uygun oldu�u durumlarda kan transf�zyonu ile kontrol alt�na al�nm��t�r. Tablet form�lasyonuyla ger�ekle�tirilen klinik �al��malarda anemi advers reaksiyonlar�n�n insidans� %35,2 olmu�tur (CTCAE derece ≥3 %14,8), anemi nedeniyle doza ara verme, doz azaltma ve kesme insidanslar� ise s�ras�yla %16,4, %11,1 ve %2,1 olmu�tur; olaparib ile tedavi edilen hastalar�n%15,6's�birveyadahafazla kan transf�zyonuna ihtiya�
duymu�tur. Olaparib ve hemoglobin d����leri aras�nda bir maruziyet-yan�t ili�kisi kan�tlanm��t�r. Lynparza ile yap�lan klinik �al��malarda, hemoglobinde ba�lang�ca g�re CTCAE derece ≥2 kaymalar�n (azalmalar) insidans� %21, mutlak n�trofillerde bu oran %17, trombositlerde %5, lenfositlerde %26 ve l�kositlerde %19 (hepsi yakla��k %) idi.
Ba�lang��ta d���k veya normal olan ortalama eritrosit hacminin ULN'nin �zerine ��kt��� vakalar�n insidans� yakla��k %51'di. Tedavi kesildikten sonra seviyelerin normale d�nd��� ve bu durumun herhangi bir klinik sonu� do�urmad��� g�r�lm��t�r.
Tedavi s�ras�nda herhangi bir parametrede klinik a��dan anlama sahip olan ve doza ara verilmesini, dozun azalt�lmas�n� ve/veya ilave tedavi uygulanmas�n� gerektirebilecek de�i�iklik ortaya ��k�p ��kmad���n�n takip edilmesi i�in ba�lang��ta test yap�lmas� ve tedavinin ilk 12 ay� boyunca her ay ve sonras�nda periyodik olarak tam kan say�m� takibi yap�lmas� �nerilir (bkz. b�l�m 4.2 ve 4.4).
Miyelodisplastik sendrom/Akut miyeloid l�semi
MDS/AML, monoterapi klinik �al��malar�nda t�m endikasyonlarda (%0,8) terap�tik dozda yayg�n olmayan �ekilde meydana gelen ciddi advers reaksiyonlard�r. �nsidans, uzun s�reli g�venlilik takibi s�ras�nda bildirilen olaylar dahil %0,5 olmu�tur (klinik �al��malarda en az bir doz oral olaparibe maruz kalan 17923hastal�k genel g�venlilik pop�lasyonuna g�re hesaplanm�� olan oran). T�m hastalar, daha �nce platin bazl� ajanlarla kemoterapi alm�� olup MDS/AML geli�imi i�in potansiyel katk�da bulunan fakt�rlere sahipti. Bir�o�u ayr�ca DNA'ya zarar veren ba�ka ajanlar ve radyoterapi alm��t�. Raporlar�n �o�unlu�u germ hatt� meme kanseri duyarl�l��� geni 1 veya 2 (gBRCA1/2) mutasyonunun ta��y�c�lar� ile ilgiliydi. MDS/AML olgular�n�n insidans� gBRCA1m ve gBRCA2m hastalar� aras�nda benzerdi (s�ras�yla %1,6 ve
%1,2). Hastalar�n baz�lar�nda kanser veya kemik ili�i displazisi �yk�s� vard�.
�nceden en az iki basamak platin kemoterapi g�rm�� ve hastal�k progresyonuna kadar �al��ma tedavisi alm�� (SOLO2 �al��mas�, hastalar�n %45'i ≥ 2 y�l olaparib tedavisi alm��t�r) BRCAm platin duyarl� n�ks etmi� yumurtal�k kanserli hastalarda MDS/AML insidans�, 5 y�ll�k takipte olaparib alan hastalarda %8 ve plasebo alan hastalarda %4 olmu�tur. Olaparib kolunda, 16 MDS/AML olgusundan 9'u, sa�kal�m takibi s�ras�nda olaparibin kesilmesinden sonra meydana gelmi�tir. MDS/AML insidans�, olaparib kolunda uzat�lm�� genel sa�kal�m ve ge� ba�lang��l� MDS/AML ba�lam�nda g�zlenmi�tir. MDS/AML riski, olaparib idame tedavisi 2 y�ll�k bir s�re boyunca bir basamak platin kemoterapisinden sonra verildi�inde birinci basamakta 5 y�ll�k takipte <%1,5 olarak kalmaktad�r (SOLO1 �al��mas�'nda %1,2 ve PAOLA-1 �al��mas�'nda
%0,7). Risk azaltma ve y�netimi i�in b�l�m 4.4'e bak�n.
Ven�z Tromboembolik Olaylar
mCRPC i�in birinci basamak tedavi olarak olaparib art� abirateron alan erkeklerde (PROpel �al��mas�), ven�z tromboembolik olaylar�n insidans�, olaparib art� abirateron kolunda %8 ve plasebo art� abirateron kolunda %3,3't�. Bu �al��mada ba�lang�ca kadar ge�en medyan s�re 170 g�nd� (aral�k: 12 ila 906 g�n). Hastalar�n b�y�k �o�unlu�u olaydan kurtulmu� ve standart t�bbi tedavi ile olaparibe devam edebilmi�tir.
�nemli kardiyovask�ler hastal��� olan hastalar �al��ma d��� b�rak�lm��t�r. Kardiyovask�ler hari� b�rakma kriterleri i�in l�tfen abirateron �r�n bilgilerine bak�n�z (b�l�m 4.4).
Di�er laboratuvar bulgular�
LYNPARZA ile yap�lan klinik �al��malarda, kandaki kreatinin seviyesinde ba�lang�ca g�re ortaya ��kan CTCAE derece ≥2 kaymalar�n (art��lar) insidans� yakla��k %11'di. �ift k�r plasebo kontroll� �al��madan elde edilen veriler, ba�lang�ca k�yasla %23'e varan medyan art�� ortaya koymu�tur ve bu art�� zaman i�inde tutarl�l�k sergilemi�, tedavi durdurulduktan sonra ise belirgin bir klinik sekel b�rakmadan ba�lang�� de�erine geri d�nm��t�r. Ba�lang�� noktas�nda hastalar�n %90'�n�n kreatinin de�erleri CTCAE derece 0 olup, ba�lang��ta CTCAE derece 1 olanlar�n oran�n�n ise %10 oldu�u g�r�lm��t�r.
Gastrointestinal toksisiteler
Bulant� genellikle �ok erken d�nemde bildirilmi� olup, ilk ba�lama zaman� hastalar�n �o�unlu�unda LYNPARZA tedavisinin ilk bir ay� i�erisindedir. Kusma da erken d�nemde bildirilmi� olup, ilk ba�lama zaman� hastalar�n �o�unlu�unda LYNPARZA tedavisinin ilk iki ay� i�erisindedir. Gerek bulant� gerekse kusman�n hastalar�n �o�unlu�unda aral�kl� oldu�u ve dozlara ara verme, dozun azalt�lmas� ve/veya antiemetik tedavi ile kontrol edilebildi�i bildirilmi�tir. Antiemetik profilaksi gerekmemektedir.
Birinci basamak over kanseri idame tedavisinde, hastalar bulant� olaylar� (olaparible %77, plaseboyla%38), kusma (olaparible %40, plaseboyla %15), ishal (olaparible %34, plaseboyla
%25) ve dispepsi (olaparible %17, plaseboyla %12) ya�am��t�r. Bulant� olaylar� olaparible tedavi uygulanan hastalar�n %2,3'�nde (CTCAE Derece 2) ve plasebo ile tedavi uygulanan hastalar�n %0,8'inde (CTCAE Derece 1) ilac�n kesilmesine neden olmu�tur; olaparible tedavi uygulanan hastalar�n %0,8'i ve %0,4'�, s�ras�yla d���k dereceli (CTCAE Derece 2) kusma ve dispepsi nedeniyle tedaviyi b�rakm��t�r.
Olaparib veya plasebo ile tedavi edilen hi�bir hasta, ishal nedeniyle tedaviyi b�rakmam��t�r. Plasebo ile tedavi edilen hi�bir hasta, kusma veya dispepsi nedeniyle tedaviyi b�rakmam��t�r. Bulant� olaylar�, olaparible tedavi edilen hastalar�n %14'�nde ve %4'�nde s�ras�yla doza ara verilmesine ve dozun azalt�lmas�na neden olmu�tur. Kusma olaylar� olaparible tedavi uygulanan hastalar�n %10'unda tedavinin duraklat�lmas�na neden olmu�tur; olaparible tedavi uygulanan hi�bir hasta dozun azalmas�na neden olan bir kusma olay� ya�amam��t�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
Pediyatrik pop�lasyon:
Pediatrik hastalarda �al��ma ger�ekle�tirilmemi�tir.
Geriyatrik pop�lasyon:
Ya�l�larda (≥ 75 ya�) s�n�rl� klinik veri mevcuttur.
Di�er:
Beyaz �rka mensup olmayan hastalar:
Beyaz �rka mensup olmayan hastalarda s�n�rl� klinik veri mevcuttur.
��pheli advers reaksiyonlar�n raporlanmas�
Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e-posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz a��m� ve tedavisi
Olaparible doz a��m� konusundaki deneyim s�n�rl�d�r. �ki g�nden fazla 900 mg'ye varan dozda olaparib tablet alan az say�da hastada hi�bir beklenmeyen advers reaksiyon bildirilmemi�tir. Doz a��m� belirtileri saptanmam��t�r ve LYNPARZA doz a��m� durumunda �zel bir tedavi yoktur. Doz a��m� s�z konusu oldu�unda, hekimler genel destekleyici �nlemleri takip etmeli ve hastay� semptomatik tedavi etmelidir.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Antineoplastikler ve immunomodulat�r ajanlar,antinoeplastik ajanlar,
Poli (ADP-riboz) polimeraz(PARP) inhibit�rleri
ATC kodu: L01XK01
Etki mekanizmas� ve Farmakodinamik etkiler:
Olaparib, insan poli (ADP-riboz) polimeraz enzimlerinin (PARP-1, PARP-2 ve PARP-3) potent bir inhibit�r�d�r ve ister tek ba��na tedavi olarak ister mevcut kemoterapiler ile kombinasyon halinde in vitro ko�ullarda se�ili t�m�r h�cre dizilerinin b�y�mesini ve in vivo ortamda t�m�r b�y�mesini inhibe etti�i g�sterilmi�tir.
PARP, DNA tek sarmal k�r�lmalar�n�n etkin onar�m� i�in gereklidir ve PARP kaynakl� onar�m�n �nemli bir �zelli�i i�in kromatin modifikasyonu sonras�nda PARP'nin kendi kendini modifiye etmesi ve DNA'dan ayr�larak baz eksizyon tamiri (BER) enzimlerinin eri�imini kolayla�t�rmas� gerekir. Olaparib, DNA ba�lant�l� PARP'�n aktif b�lgesine ba�land���nda PARP'�n ayr�lmas�n� �nler ve DNA'ya hapsederek onar�m� bloke eder. Replike olan h�crelerde bu durum ayr�ca replikasyon �atal�, PARP-DNA eklentileri ile kar��la�t���nda DNA �ift sarmal k�r�lmalar� (DSB'ler) olu�umuna da yol a�ar. Normal h�crelerde homolog rekombinasyon onar�m (HRR) yola��, bu DNA �ift sarmal k�r�lmalar�n� onarmada etkilidir. BRCA1 veya 2 gibi HRR fonksiyonel bile�enleri olmayan kanserlerde DNA DSB'ler do�ru veya etkili �ekilde tamir edilemez. Bunun yerine genomik instabilitede art��a yol a�an klasik homolog olmayan u� birle�mesi (NHEJ) mekanizmas� gibi, alternatif ve hataya e�ilimli mekanizmalar aktive edilir. Birka� replikasyon turunun ard�ndan genomik instabilite desteklenebilir olmayan d�zeylere ula�abilir ve kanser h�creleri normal h�crelere k�yasla halihaz�rda daha y�ksek bir DNA hasar� y�k�ne sahip oldu�undan, bu durum kanser h�cresinin �l�m� ile sonu�lanabilir. Neden olan bozukluk ve etkinlik tam olarak a��klanmam�� olmakla birlikte, BRCA1 veya BRCA2 mutasyonlar�n�n yoklu�unda HRR mekanizmas� ba�ka mekanizmalar taraf�ndan bozulabilir. Tam fonksiyonel HRR mekanizmas�n�n mevcut olmay��� overkanserlerinde ve di�er kanserlerde platin duyarl�l���n�n kilit roldeki belirleyicilerinden biridir.
BRCA1/2-eksikli�i bulunan in vivo modellerde platin tedavisinden sonra verilen olaparib, tek ba��na platin tedavisine k�yasla t�m�r progresyonunda bir gecikme ve genel sa�kal�mda bir art�� ortaya ��karm��t�r ve bunlar olaparib idame tedavisi periyodu ile korelasyon g�stermi�tir.
NHA'lar ile kombine anti-t�m�r etkisi
Prostat kanseri modellerinde yap�lan klinik �ncesi �al��malarda, PARP inhibit�rleri ve yeni nesil hormonal ajanlar birlikte uyguland���nda birle�ik bir anti-t�m�r etkisi bildirilmi�tir. PARP, androjen resept�r� (AR) sinyalinin pozitif ortak reg�lasyonunda yer al�r; bu, PARP/AR sinyali birlikte inhibe edildi�inde artan AR hedef gen supresyonuna yol a�ar. Di�er klinik �ncesi �al��malarda, NHA'larla yap�lan tedavinin baz� HRR genlerinin transkripsiyonunu inhibe etti�i dolay�s�yla HRR eksikli�ini ind�kledi�i ve genetik olmayan mekanizmalar yoluyla PARP inhibit�rlerine kar�� duyarl�l���n artt��� bildirilmi�tir.
BRCA1/2 mutasyonunun tespiti
Genetik testler, onaylanm�� bir test kullan�larak deneyimli bir laboratuvar taraf�ndan yap�lmal�d�r. Kan ve/veya t�m�r �rnekleri �zerinde BRCA1/2 mutasyonlar� a��s�ndan lokal veya merkezi olarak uygulanan testler farkl� �al��malarda kullan�lm��t�r. Kullan�lan teste ve uluslararas� s�n�fland�rma konsensusuna ba�l� olarak, BRCA1/2 mutasyonlar� zararl�/��pheli zararl� veya patojenik/olas� patojenik olarak s�n�fland�r�lm��t�r. Homolog rekombinasyon eksikli�i (HRD) pozitif durumu, zararl� / ��pheli zararl� veya patojenik / muhtemelen patojenik olarak s�n�fland�r�lan bir BRCA1 / 2 mutasyonunun saptanmas�yla tan�mlanabilir.
Bu mutasyonlar�n tespiti, HRD pozitif durumunu belirlemek i�in pozitif HRD skoru ile birle�tirilebilir.
Genomik instabilitenin tespiti
PAOLA-1'de ara�t�r�lan HR eksikli�i ile ili�kili genomik de�i�iklikler, �nceden tan�mlanm�� kriterleri ve puan� olan s�rekli �l��mler olan genom �ap�nda heterozigotluk kayb�, telomerik alelik dengesizlik ve b�y�k �l�ekli ge�i�i i�erir. Bile�ik genomik karars�zl�k skoru (GIS, HRD skoru olarak da adland�r�l�r), t�m�r h�crelerinde biriken spesifik genomik anormalliklerin kapsam�n� de�erlendirmek i�in birle�tirilmi� �l��mler ve ilgili skorlar kullan�larak belirlenir. Daha d���k puan, DNA'ya zarar veren ajanlara maruz kalmaya g�re numune alma s�ras�nda t�m�r h�crelerinin HR eksikli�i olas�l���n�n daha d���k oldu�unu tan�mlar ve daha y�ksek puan, t�m�r h�crelerinin HR eksikli�i olas�l���n�n daha y�ksek oldu�unu belirler. GIS pozitif durumunu belirlemek i�in valide edilmi� kesme noktalar� kullan�lmal�d�r.
HRD pozitif durumu, valide edilmi� bir test kullan�larak deneyimli bir laboratuvar taraf�ndan test edilen HR eksikli�i ile ili�kili genomik de�i�iklikler i�in birle�ik bir GIS puan� ile tan�mlanabilir.
Klinik etkililik ve g�venlilik
BRCA mutasyonlu ileri over kanserinin birinci basamak idame tedavisi: SOLO1 �al��mas�
Bir Faz III randomize, �ift k�r, plasebo kontroll� �ok merkezli �al��mada birinci basamak platin bazl� kemoterapinin tamamlanmas�n�n ard�ndan olaparibin idame tedavisi olarak g�venlili�i ve etkilili�i yeni tan� konmu� ilerlemi� (FIGO Evre III-IV) y�ksek dereceli ser�z veya endometroid BRCA1//2 mutasyonlu (mBRCA1//2) over kanseri hastalar�nda ara�t�r�lm��t�r. Bu �al��mada 391 hasta Lynparza (g�nde iki defa 300 mg [2 x 150 mg tablet]) veya plasebo almak �zere 2/1 oran�nda randomize edilmi�tir .Hastalarbirincibasam ak platin kemoterapisine verilen
hastal���n radyolojik progresyonuna, kabul edilemez toksisiteye veya 2 y�la kadar tedaviye devam edilmi�tir. Tam klinik yan�t durumunda kalan (yani, radyolojik hastal�k kan�t� olmayan) hastalar i�in maksimum tedavi s�resi 2 y�l olarak belirlenmi�tir; bununla birlikte, stabil kalan bir hastal�k kan�t� olan (yani, hastal�k progresyonuna dair kan�t bulunmayan) hastalar, 2 y�ldan uzun s�re Lynparza almaya devam edebilmi�tir.
Germ hatt� veya somatik BRCA1/2 mutasyonlar� g�r�len hastalar ya lokal bir test (n=208) veya merkezi bir test (n=181) yoluyla kanda germ hatt� testinden ya da lokal bir test kullan�larak bir t�m�r numunesinin test edilmesinden (n=2) prospektif �ekilde tespit edilmi�tir. Merkezi germ hatt� testinde, patojen veya olas� patojen mutasyonlar, hastalar�n s�ras�yla %95,3'�nde (365/383) ve %4,7'sinde (18/383) tespit edilmi�tir. Randomize edilen hastalar�n %5,5'inde (21/383) BRCA1/2 genlerinde b�y�k yeniden d�zenlenmeler tespit edilmi�tir. Yerel test yoluyla kaydedilen hastalar�n gBRCAm durumu merkezi testle retrospektif �ekilde do�rulanm��t�r. T�m�r �rnekleri mevcut olan hastalara uygulanan retrospektif testler merkezi test kullan�larak ger�ekle�tirilmi�tir ve %95'inde uygun bir mutasyon bulunan (bilinen [n = 47] veya muhtemel patojenik [n = 277]) 341 hastada ba�ar�l� sonu�lar elde edilmi�tir ve 2 gBRCAwt hastas�n�n sadece sBRCAm ta��d��� do�rulanm��t�r. SOLO1'de BRCA1/2m germ hatt� g�r�len 389 hasta tespit edilmi�tir ve bunlar�n 2'sinin somatik BRCA1/2m oldu�u g�r�lm��t�r.
Demografik �zellikler ve ba�lang�� �zellikleri olaparib ve plasebo tedavisi kollar� aras�nda genel olarak iyi bir denge sergilemi�tir. Medyan ya��n her iki kolda 53 oldu�u belirlenmi�tir. Over kanserinin hastalar�n %85'inde primer t�m�r oldu�u g�r�lm��t�r. En yayg�n histolojik tipin ser�z (%96) oldu�u g�r�lm��t�r, hastalar�n %2'sinde endometrioid histoloji bildirilmi�tir. �o�u hastan�n ECOG performans durumu 0 olarak belirlenmi�tir (%78), performans durumu 2 ila 4 olan hastalarda herhangi bir veri mevcut de�ildir. Hastalar�n y�zde altm�� ���ne (%63) �nceden t�m�r rezeksiyon cerrahisi uygulanm�� oldu�u belirlenmi�tir ve bunlar�n �o�unlu�unda (%75) makroskobik rezid�el hastal�k g�zlenmemi�tir. Hastalar�n %35'ine aral�kl� t�m�r rezeksiyon cerrahisi uygulanm��t�r ve bunlar�n %82'sinde makroskobik rezid�el hastal�k bildirilmemi�tir. T�m� evre IV olan yedi hastaya sitored�ktif cerrahi uygulanmam��t�r. T�m hastalar birinci basamak platin bazl� tedavi g�rm��t�r. �al��maya giri�te olaparib ve plasebo kollar�ndaki hastalar�n %73'�nde ve %77'sinde, ara�t�rmac� taraf�ndan s�ras�yla radyolojik hastal�k kan�t� bulunmamas� ve kanser antijeni 125'in (CA-125) normal aral�kta olmas� �eklinde tan�mland��� �zere, hastal�k kan�t� g�zlenmemi�tir (CR). Ba�lang��ta �l��lebilir veya �l��lemez lezyonlar�n varl��� veya y�ksek CA-125 �eklinde tan�mlanan PR, olaparib ve plasebo kollar�ndaki hastalar�n s�ras�yla %27'sinde ve %23'�nde bildirilmi�tir. Hastalar�n y�zde doksan ��� (%93) son platin bazl� kemoterapi dozunu takip eden 8 hafta i�inde randomize edilmi�tir. Bevasizumab ile tedavi uygulanan hastalar �al��ma d��� b�rak�lm��t�r, dolay�s�yla daha �nce bevasizumab alm�� olaparib hastalar�na ili�kin g�venlilik ve etkililik verisi bulunmamaktad�r. Somatik BRCA mutasyonu g�r�len hastalara ili�kin �ok s�n�rl� veri mevcuttur.
Primer sonlanma noktas� modifiye Solid T�m�rlerde Yan�t De�erlendirme Kriterleri (RECIST)
1.1 kullan�larak ara�t�rmac� de�erlendirmesi yoluyla belirlenen ve randomizasyondan progresyona kadar ge�en s�re �eklinde tan�mlanan progresyonsuz sa�kal�m (PFS) veya �l�md�r. Sekonder etkililik sonlanma noktalar� randomizasyondan ikinci progresyona veya �l�me kadar ge�en s�re (PFS2);O S(genelsa�kal�m),randomizasyondan tedavinin kesilmesine
ba�lang�c�na veya �l�me kadar ge�en s�re (TFST) ve sa�l�kla ili�kili ya�am kalitesini (HRQoL) i�ermi�tir. Hastalar ba�lang��ta ve 3 y�l boyunca her 12 haftada bir ve daha sonra randomizasyon tarihi baz al�narak objektif radyolojik hastal�k progresyonuna kadar her 24 haftada bir t�m�r de�erlendirmelerinden ge�irilmi�tir.
�al��ma ara�t�rmac� taraf�ndan de�erlendirilen PFS'de plaseboya k�yasla olaparib i�in klinik anlaml�l��a sahip olan ve istatistiksel a��dan anlaml� iyile�me ortaya koymu�tur. PFS konusunda ara�t�rmac� taraf�ndan yap�lan de�erlendirme, PFS �zerinde yap�lan bir k�rle�tirilmi� ba��ms�z merkezi radyolojik (BICR) inceleme ile desteklenmi�tir. PFS analizi s�ras�nda, ara OS verileri olgunla�mam��t� (% 21) ve HR 0,95'ti (%95 CI 0,60, 1,53; p de�eri=0,9). Etkililik sonu�lar� Tablo 2 ve �ekil 1 ve 2'de sunulmaktad�r.
Tablo 2 SOLO1'de BRCA1/2m ilerlemi� over kanseri g�r�len yeni tan� konmu� hastalara ait etkililik sonu�lar�
| G�nde iki defa olaparib 300 mg | Plasebo |
PFS (%51 olgunluk) |
|
|
Olay say�s�: Toplam hasta say�s� (%) | 102:260 (39) | 96:131 (73) |
Medyan s�re (ay) | NR | 13.8 |
HR (%95 CI) | 0.3 (0.23-0.41) |
|
P de�eri (2 yanl�) | p<0,0001 |
|
PFS2 (%31 olgunluk) |
|
|
Olay say�s�: Toplam hasta say�s� (%) | 69:260 (27) | 52:131 (40) |
Medyan s�re (ay) | NR | 41.9 |
HR (%95 CI) | 0.5 (0.35-0.72) |
|
P de�eri (2 yanl�) | p=0,0002 |
|
TFST (%49 olgunluk) |
|
|
Olay say�s�: Toplam hasta say�s� (%) | 99:260 (38) | 94:131 (72) |
Medyan s�re (ay) | 51.8 | 15.1 |
HR (%95 CI) | 0.3 (0.22-0.4) |
|
P de�eri* (2 yanl�) | p<0,0001 |
|
a Kaplan-Meier hesaplamalar�na g�re 24 ve 36. aylarda progresyon g�zlenmeyen hastalar�n oran� olaparib i�in %74 ve %60 plasebo i�inse %35 ve %27 olmu�tur; medyan takip s�resi hem olaparib hem de plasebo kollar�nda 41 ay olmu�tur.
b < 1 olan de�erler olaparib lehinedir. Analiz, �nceki platin kemoterapisine verilen yan�t� (CR veya PR) e� de�i�ken olarak i�eren bir Cox orant�l� tehlikeler modeli kullan�larak ger�ekle�tirilmi�tir.
c Plasebo kolunda takiben bir tedavi uygulanan 94 hastan�n 49'u (%52) bir PARP inhibit�r� alm��t�r.
* Multiplisite a��s�ndan kontrol edilmemi�tir.
bd: g�nde iki kez; NR Eri�ilmemi�tir; CI G�ven aral���; PFS progresyonsuz sa�kal�m; PFS2 �kinci progresyona veya �l�me kadar ge�en s�re; OS Genel sa�kal�m; TFST Randomizasyondan takip eden ilk anti-kanser tedaviye veya �l�me kadar ge�en s�re.
�ekil 1 SOLO1: Yeni tan� konmu� BRCA1/2m ilerlemi� over kanseri hastalar�nda Kaplan-Meier PFS grafi�i (%51 olgunluk - ara�t�rmac� de�erlendirmesi)
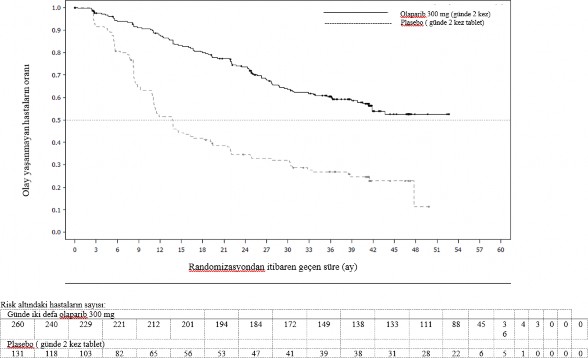
�ekil 2 SOLO1: Yeni tan� konmu� BRCA1/2m ilerlemi� over kanseri hastalar�nda Kaplan-Meier OS grafi�i (%21 olgunluk)
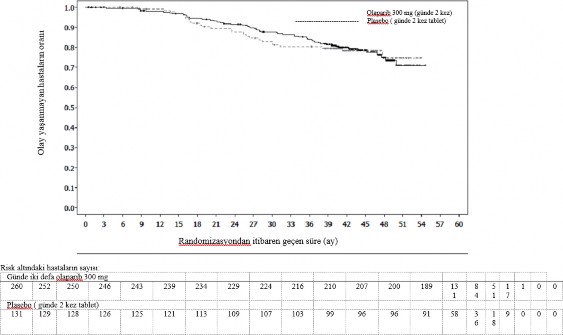
�al��maya giri�teki hastal�k kan�t�na g�re olu�turulmu� hasta alt gruplar�nda tutarl� sonu�lar g�zlenmi�tir. Ara�t�rmac� taraf�ndan tan�mlanan CR g�r�len hastalarda HR 0,34 (%95 CI 0,24- 0,47) olmu�tur; olaparibte medyan PFS'ye ula��lmam��t�r, plaseboda ise medyan PFS 15,3 ayd�.
24. ve 36. ayda, olaparib kolunda hastalar�n s�ras�yla %68'i ve %45'i, plasebo kolundaki hastalar�n ise %34'� ve%22'si CR durumunda kalm��t�r. �al��maya giri�te PR g�r�len hastalarda PFS HR 0,31 olarak tespit edilmi�tir (%95 CI 0,18, 0,52; ortalama PFS olaparible 30,9 ay, plaseboyla ise 8,4 ay). �al��maya giri�te PR g�r�len hastalar CR'ye ula�m�� (24. ayda olaparib kolunda %15 ve plasebo kolunda %4, 36. ayda CR durumunda kalm��t�r) veya daha fazla PR/stabil hastal�k sergilemi�tir (24. ayda olaparib kolunda %43 ve plasebo kolunda %15, 36. ayda olaparib kolunda %17 ve plasebo kolunda %15). Son platin bazl� kemoterapi dozunu takip eden 6 ay i�inde progresyon ya�ayan hastalar�n oran� olaparib ile %3,5, plaseboyla ise
%8,4 olmu�tur.
Platine duyarl� relaps yapm�� (PSR) over kanserinin idame tedavisi
SOLO2 �al��mas�
Olaparibin idame tedavisi olarak g�venlili�i ve etkilili�i germline BRCA1/2-mutasyonlu, platine duyarl�, relaps yapm�� (PSR) over, fallop t�p� veya primer peritoneal kanserli hastalarla ger�ekle�tirilen bir Faz III randomize, �ift k�r, plasebo kontroll� �al��mada de�erlendirilmi�tir. Bu �al��mada progresyona kadar al�nan LYNPARZA (g�nde iki defa 300 mg [2 x 150 mg tablet]) idame tedavisinin etkilili�i platin i�eren kemoterapinin tamamlanmas�n�n ard�ndan yan�t (CR veya PR) sergilemekte olan 295 y�ksek evre ser�z veya endometrioid PSR over kanseri hastas�nda plasebo tedavisiyle kar��la�t�r�lm��t�r (2/1 randomizasyon: 196 olaparib ve 99 plasebo).
�ki veya daha fazla platin i�eren rejim uygulanan ve hastal�klar� sondan �nceki platin bazl� kemoterapinin tamamlanmas�ndan > 6 ay sonra n�kseden hastalar kaydedilmi�tir. Hastalar�n daha �nce olaparib veya ba�ka bir PARP inhibit�r� tedavisi alm�� olmas�na izin verilmemi�tir. Hastalar�n, randomizasyondan hemen �nceki rejimde olmamak ko�uluyla, daha �nce bevasizumab alm�� olmas�na izin verilmi�tir.
T�m hastalarda ba�lang��ta gBRCA1/2m kan�t� tespit edilmi�tir. Hastalarda g�r�len BRCA1/2 mutasyonlar�ndan germline mutasyonu, ya lokal bir test ya da Myriad CLIA Integrated BRACAnalysis® testi yoluyla yahut da t�m�r dokusundan lokal bir test kullan�larak saptanm��t�r. Randomize edilen hastalar�n %4,7'sinde (14/295) BRCA1/2 genlerinde b�y�k rearanjmanlar tespit edilmi�tir.
Demografik �zellikler ve ba�lang�� �zellikleri olaparib ve plasebo kollar� aras�nda genel olarak iyi bir denge sergilemi�tir. Medyan ya��n her iki kolda 56 oldu�u belirlenmi�tir. Over kanserinin, hastalar�n > % 80'inde primer t�m�r oldu�u g�r�lm��t�r. En yayg�n histolojik tipin ser�z (> %90) oldu�u g�r�lm��t�r, hastalar�n %6's�nda endometrioid histoloji bildirilmi�tir. Olaparib kolunda hastalar�n %55'inin daha �nce yaln�zca 2 basamak tedavi g�rd��� belirlenmi�tir ve hastalar�n %45'i daha �nce 3 veya daha fazla basamak tedavi g�rm��t�r. Plasebo kolunda hastalar�n %61'inin daha �nce yaln�zca 2 basamak tedavi g�rd���, %39'unun ise daha �nce 3 veya daha fazla basamak tedavi g�rd��� belirlenmi�tir. �o�u hastan�n ECOG performans durumu 0 olarak belirlenmi�tir (%81). Platin uygulanmayan d�nem, hastalar�n
Primer sonlan�m noktas� RECIST 1.1 kullan�larak ara�t�rmac� de�erlendirmesiyle PFS'dir. Sekonder etkililik sonlanma noktalar�, PFS2; OS TDT, TFST, TSST ve HRQoL i�ermi�tir.
�al��ma primer amac�na ula�m��t�r ve ara�t�rmac� taraf�ndan de�erlendirilen PFS'de 0,30'luk HRplaseboya k�yasla olaparib lehine istatistiksel a��dan anlaml� bir iyile�me ortaya koymu�tur (%95 CI 0,22 - 0,41; p < 0,0001; olaparible medyan 19,1 aya kar��l�k plaseboyla medyan 5,5 ay). Ara�t�rmac� taraf�ndan de�erlendirilen PFS, k�rle�tirilmi� bir ba��ms�z merkezi radyolojik inceleme ile desteklenmi�tir (HR 0,25; %95 CI 0,18 – 0,35; p < 0,0001; olaparib i�in medyan 30,2 ay, plasebo i�in medyan 5,5 ay). Olaparibtedavisiuygulanan hastalar�n %43'� 2. y�lda progresyon sergilememeye devam etmi�tir, plasebo alan hastalarda ise bu oran yaln�zca %15'te kalm��t�r.
SOLO2'de gBRCA1/2m PSR over kanseri hastalar�nda primer sonlanma noktas� a��s�ndan elde edilen sonucun bir �zeti Tablo 3 ve �ekil 3'de verilmi�tir.
Tablo 3: SOLO2'de gBRCA1/2m PSR over kanseri hastalar�nda primer sonlan�m noktas� a��s�ndan elde edilen sonucun �zeti
| G�nde iki defa olaparib 300 mg tablet | Plasebo |
PFS (%63 olgunluk) | ||
Olay say�s�: Toplam hasta say�s� (%) | 107:196 (55) | 80:99 (81) |
Medyan s�re (ay) (%95 CI) | 19,1 (16,3 – 25,7) | 5,5 (5,2 – 5,8) |
HR (%95 CI) | 0,30 (0,22 – 0,41) |
|
P de�eri (2 yanl�) | P < 0,0001 |
|
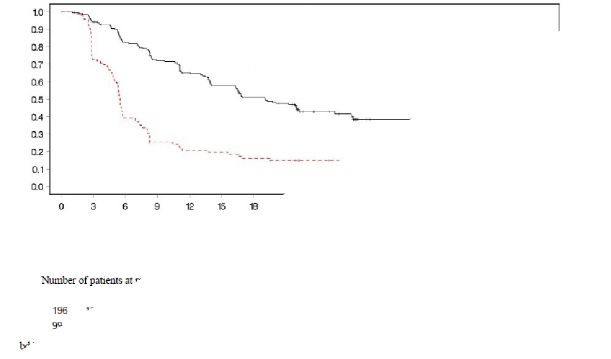
�ekil 3: SOLO2: gBRCA1/2m PSR over kanseri hastalar�nda Kaplan-Meier PFS grafi�i (%63 olgunluk - ara�t�rmac� de�erlendirmesi)
bd G�nde iki kez; PFS progresyonsuz sa�kal�m
OS'nin son analizinde (%61 olgunluk) HR 0.74 idi (%95 GA 0,54-1.00; p=0.0537; plasebo i�in medyan 51,7 ay ve plasebo i�in 38,8 ay) ve istatistiksel anlaml�l��a ula�mad�.
Sekonder sonlan�m noktalar� olan TFST ve PFS2, plaseboya k�yasla olaparib i�in kal�c� ve istatistiksel a��dan anlaml� iyile�me sergilemi�tir. OS, TFST ve PFS2 i�in sonu�lar Tablo 4 ve �ekil 4'te sunulmaktad�r.
Tablo 4: SOLO2'de gBRCA1/2m PSR yumurtal�k kanseri hastalar� i�in kilit sekonder objektif sonu�lar�n �zeti
| Olaparib 300 mg tablet, g�nde iki kez | Plasebo |
OS (%61 olgunluk) | ||
Olay say�s�: Toplam hasta say�s� (%) | 116:196 (59) | 65:99 (66) |
Medyan s�re (%95 GA), ay | 51,7 (41,5, 59,1) | 38,8 (31,4, 48,6) |
HR (%95 GA) | 0,74 (0,54 – 1,00) | |
P de�eri (2-tarafl�) | p=0,0537 | |
TFST (%71 olgunluk) | ||
Olay say�s�: Toplam hasta say�s� (%) | 139:196 (71) | 86:99(87) |
Medyan s�re (%95 GA), ay | 27,4 (22,6 – NR) | 7,2 (6,3 – 8,3) |
HR (%95 GA) | 0,37 (0,28 – 0,48) | |
P de�eri (2-tarafl�) | p < 0,0001 | |
PFS2 (%40 olgunluk) | ||
Olay say�s�: Toplam hasta say�s� (%) | 70:196 (36) | 49:99 (50) |
Medyan s�re (%95 GA), ay | NR (24,1 – NR) | 18,4 (15,4 – 22,8) |
HR (%95 GA) | 0,50 (0,34 – 0,72) | |
P de�eri (2-tarafl�) | p = 0,0002 | |
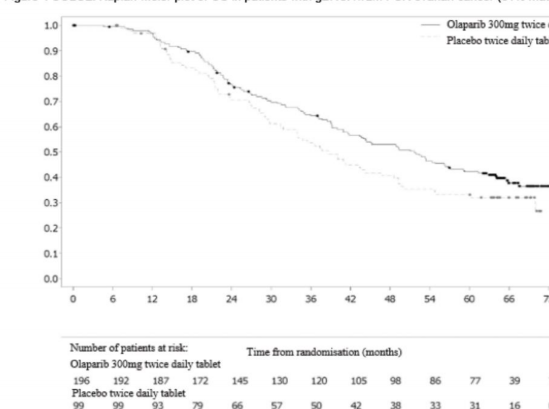
Hasta olaylar�n�n oran�
�ekil 4 SOLO2: gBRCA1/2m PSR yumurtal�k kanseri hastalar�nda Kaplan-Meier OS grafi�i (%61 olgunluk)
�al��maya �l��lebilir hastal�kla (ba�lang��ta hedef lezyonlar) kat�lan hastalar aras�nda Lynparza kolunda %41'lik bir objektif yan�t oran�na eri�ilmi�tir, plaseboda ise bu oran
%17'ydi. �al��maya hastal�k kan�t�yla (ba�lang��ta hedef veya hedef d��� lezyonlar) dahil edilen ve Lynparza ile tedavi uygulanan hastalar�n %15,0'� tam yan�t elde ederken plasebo alan hastalarda ise bu oran %9,1'di.
PFS analizi s�ras�nda medyan tedavi s�resi olaparib i�in 19,4 ay, plasebo i�inse 5,6 ay �eklindeydi. Hastalar�n �o�u g�nde iki kez 300 mg �eklindeki ba�lang�� dozunda kalm��t�r. Advers olay nedeniyle doz duraklatma, azaltma, kesme insidans� s�ras�yla %45,1,%25,1 ve
%10,8'di. Doz duraklatma en s�k olarak tedavinin ilk 3 ay� i�inde, doz azaltma ise 3-6 ay� i�inde
meydana gelmi�tir. Doz duraklatmaya veya doz azaltmaya neden olan en s�k g�r�len advers olaylar anemi, bulant� ve kusmayd�.
FACT-O'ya ait TOI'da ba�lang�ca g�re meydana gelen de�i�iklik ile de�erlendirildi�i �zere, hasta taraf�ndan bildirilen sonu� (PRO) verileri, plaseboya k�yasla olaparib ile tedavi edilen hastalar i�in herhangi bir farka i�aret etmemektedir.
�al��ma 19 (D0810C00019)
Olaparibin platin temelli iki veya daha fazla tedaviyi takiben fallop t�p� veya primer peritoneal kanseri de i�eren PSR over kanseri hastalar�nda idame tedavisi olarak g�venlili�i ve etkilili�i, b�y�k bir Faz II randomize, �ift k�r, plasebo kontroll� �al��mada (�al��ma 19) de�erlendirilmi�tir. Bu �al��mada progresyona kadar al�nan LYNPARZA kaps�l idame tedavisinin (g�nde iki defa 400 mg [8 x 50 mg kaps�l]) etkilili�i platin i�eren kemoterapinin tamamlanmas�n�n ard�ndan yan�t (CR veya PR) sergilemekte olan 265 (136 olaparib ve 129 plasebo) PSR y�ksek dereceli ser�z over kanseri hastas�nda plasebo tedavisiyle kar��la�t�r�lm��t�r. Primer sonlanma noktas� RECIST 1 kullan�larak ara�t�rmac� de�erlendirmesine g�re belirlenen PFS'dir. Sekonder etkililik sonlanma noktalar� OS'yi, CR/PR+ SD (stabil hastal�k) �eklinde tan�mlanan hastal�k kontrol oran�n� (DCR), HRQoL'yi ve hastal�kla ili�kili semptomlar� i�ermi�tir. Ayn� zamanda ara�t�rma ama�l� TFST ve TSST analizleri de ger�ekle�tirilmi�tir.
Hastal�klar� sondan �nceki platin bazl� kemoterapinin tamamlanmas�ndan > 6 ay sonra n�kseden hastalar kaydedilmi�tir. Kay�tta BRCA1/2 mutasyonu kan�t� �art� aranmam��t�r (baz� hastalar�n BRCA mutasyonu durumu retrospektif �ekilde belirlenmi�tir). Hastalar�n daha �nce olaparib veya ba�ka bir PARP inhibit�r� tedavisi alm�� olmas�na izin verilmemi�tir. Hastalar�n, randomizasyondan hemen �nceki rejimde olmamak ko�uluyla, daha �nce bevasizumab alm�� olmas�na izin verilmi�tir. Olaparib tedavisi s�ras�nda ortaya ��kan progresyonun ard�ndan olaparible yeniden tedaviye izin verilmemi�tir.
BRCA1/2 mutasyonlar� g�r�len hastalar ya lokal bir test ya da Myriad CLIA Integrated BRACAnalysis® testi yoluyla kandan germline mutasyon ya da Foundation Medicine taraf�ndan ger�ekle�tirilen bir test kullan�larak bir t�m�r dokusunsunda mutasyon saptanm��t�r. Randomize edilen hastalar�n %7,4'�nde (10/136) BRCA1/2 genlerinde b�y�k rearanjmanlar tespit edilmi�tir.
Demografik �zellikler ve ba�lang�� �zellikleri olaparib ve plasebo kollar� aras�nda genel olarak iyi bir denge sergilemi�tir. Medyan ya��n her iki kolda 59 oldu�u belirlenmi�tir. Over kanserinin hastalar�n %86's�nda primer t�m�r oldu�u g�r�lm��t�r. Olaparib kolunda hastalar�n %44'�n�n daha �nce yaln�zca 2 basamak tedavi g�rd��� belirlenmi�tir ve hastalar�n %56's� daha �nce 3 veya daha fazla basamak tedavi g�rm��t�r. Plasebo kolunda hastalar�n %49'unun daha �nce yaln�zca 2 basamak tedavi g�rd���, %51'inin ise daha �nce 3 veya daha fazla basamak tedavi g�rd��� belirlenmi�tir. �o�u hastan�n ECOG performans durumu 0 olarak belirlenmi�tir (%77). Platin uygulanmayan d�nem hastalar�n %60'�nda > 12 ay, %40'�nda ise > 6-12 ay olmu�tur. �nceki platin kemoterapisine yan�t hastalar�n %45'inde tam, %55'inde ise k�smi olmu�tur. Olaparib ve plasebo kollar�nda hastalar�n s�ras�yla %6's� ve %5'i daha �nce bevasizumab alm��t�r.
�al��ma primer amac�na ula�m��t�r ve genel pop�lasyonda PFS'de 0,35'lik HR ile plaseboya k�yasla olaparib lehine istatistiksela��dananlaml� biriyile�me ortaya koymu�tur (%95 CI 0,25
- 0,49; p < 0,00001; olaparible medyan 8,4 aya kar��l�k plaseboyla medyan 4,8 ay). Olgunluk d�zeyi %79 olan son OS analizinde (veri kesme tarihi [DCO] 9 May�s 2016), olaparib ile plasebo kar��la�t�r�ld���nda g�zlenen tehlike oran� 0,73 (%95 CI 0,55 – 0,95; p = 0,02138 [<0,0095'lik �nceden belirlenmi� anlaml�l�k d�zeyini kar��lamam��t�r]; olaparible medyan 29,8 aya kar��l�k plaseboyla medyan 27,8 ay) olmu�tur. Olaparible tedavi uygulanan grupta hastalar�n %23,5'i (n=32/136) tedaviye ≥ 2 y�l s�resince devam etmi�tir, plasebo alan hastalarda ise bu oran %3,9 (n=5/128) olmu�tur. Hasta say�lar� s�n�rl� olmakla birlikte olaparible tedavi uygulanan grupta hastalar�n %13,2'si (n=18/136) tedaviye ≥ 5 y�l s�resince devam etmi�tir, plasebo grubunda ise bu oran %0,8 (n=1/128) olmu�tur.
�nceden planlanm�� alt grup analizinde BRCA1/2-mutasyonlu over kanseri g�r�len hastalar�n (n=136, %51,3; somatik t�m�r BRCA1/2 mutasyonu tespit edilen 20 hasta dahil) olaparib idame monoterapisinden en fazla klinik fayda elde eden alt grup oldu�u tespit edilmi�tir. Ayn� zamanda BRCA1/2'nin yaban�l tipinin/anlam� belirsiz olan varyantlar�n�n (BRCA1/2 wt/VUS) g�r�ld��� hastalarda da daha d���k boyutlu olmakla birlikte bir fayda g�zlenmi�tir. Alt grup analizleri i�in uygulamaya konmu� herhangi bir �oklu test stratejisi mevcut de�ildir.
�al��ma 19'da BRCA1/2-mutasyonlu ve BRCA1/2 wt/VUS PSR over kanseri hastalar�nda primer sonlanma noktas� a��s�ndan elde edilen sonucun bir �zeti Tablo 5'te ve �al��ma 19'daki t�m hastalar i�in Tablo 5ve �ekil 5'de verilmi�tir.
Tablo 5: �al��ma 19'da t�m hastalar ve BRCA1/2-mutasyonlu ve BRCA1/2 wt/VUS PSR over kanseri hastalar�nda primer sonlan�m noktas� a��s�ndan elde edilen sonucun �zeti
| T�m hastalar | BRCA1/2- | BRCA1/2 wt/VUS | ||||
| mutasyonlu |
| |||||
G�nde iki | Plasebo | G�nde iki | Plasebo | G�nde | Plasebo | ||
defa |
| defa |
| iki defa |
| ||
olaparib |
| olaparib |
| olaparib |
| ||
400 mg |
| 400 mg |
| 400 mg |
| ||
kaps�l |
| kaps�l |
| kaps�l |
| ||
PFS – DCO 30 Haziran 2010 | |||||||
Olay | say�s�: | 60:136 (44) | 94:129 | 26:74 (35) | 46:62 | 32:57 | 44:61 |
Toplam | hasta |
| (73) |
| (74) | (56) | (72) |
say�s� (%) |
|
|
|
|
|
| |
Medyan s�re (ay) | 8,4 | 4,8 | 11,2 | 4,3 | 7,4 | 5,5 | |
(%95 CI) | (7,4 – 11,5) | (4,0 – 5,5) | (8,3 – NR) | (3,0 – | (5,5 – | (3,7 – | |
|
|
|
| 5,4) | 10,3) | 5,6) | |
HR (%95 CL) | 0,35 | 0,18 | 0,54 | ||||
(0,25 – 0,49) | (0,10 – 0,31) | (0,34 – 0,85) | |||||
P de�eri (2 yanl�) | p < 0,00001 | p < 0,00001 | p = 0,00745 | ||||
T�m hastalar �u alt gruplardan olu�maktad�r: BRCA1/2-mutasyonu, BRCA1/2 wt/VUS ve BRCA1/2 durumu bilinmeyen (durumu bilinmeyen 11 hasta tabloda ayr� bir alt grup olarak g�sterilmemektedir).
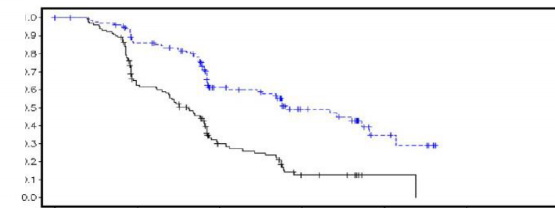
�ekil 5: �al��ma 19: DCO 30 Haziran 2010'da FAS'de (%58 olgunluk – ara�t�rmac� de�erlendirmesi) Kaplan-Meier PFS grafi�i
Randomizasyondan itibaren ge�en s�re (ay)
Olaparib 400 mg bd
---- - - - - - - -
![]()
![]()
---------- - - - - - - - -
Risk alt�ndaki hastalar�n say�s�:
136 | 106 | 53 | 24 | 7 | 0 | G�nde iki defa olaparib 400 mg |
129 | 72 | 24 | 7 | 1 | 0 | Plasebo |
bd g�nde iki defa; DCO veri kesme tarihi; FAS Tam analiz seti; PFS Progresyonsuz sa�kal�m
�al��ma 19'da BRCA1/2-mutasyonlu ve BRCA1/2 wt/VUS PSR over kanseri hastalar�nda kilit sekonder sonlanma noktalar� a��s�ndan elde edilen sonucun bir �zeti Tablo 4'te ve �al��ma 19'daki t�m hastalar i�in Tablo 6 ve �ekil 6'da verilmi�tir.
Tablo 6: �al��ma 19'da t�m hastalar ve BRCA1/2-mutasyonlu ve BRCA1/2 wt/VUS PSR over kanseri hastalar�nda kilit sekonder sonlanma noktalar� a��s�ndan elde edilen sonucun �zeti
| T�m hastalar | BRCA1/2- mutasyonlu | BRCA1/2 wt/VUS | |||
G�nde iki defa olapari b 400 mg kaps�l | Plasebo | G�nde iki defa olapari b 400 mg kaps�l | Plasebo | G�nde iki defa olapari b 400 mg kaps�l | Plasebo | |
OS – DCO 09 May�s 2016 | ||||||
Olay say�s�: Toplam hasta say�s� (%) | 98:136 (72) | 112:129 (87) | 49:74 (66) | 50:62 (81) | 45:57 (79) | 57:61 (93) |
Medyan s�re (ay) (%95 CI) | 29,8 | 27,8 | 34,9 | 30,2 | 24,5 | 26,6 |
| (26,9 – | (24,9 – | (29,2 – | (23,1 – | (19,8 – | (23,1 – |
| 35,7) | 33,7) | 54,6) | 40,7) | 35,0) | 32,5) |
HR (%95 CL) | 0,73 (0,55 – 0,95) | 0,62 (0,42 – 0,93) | 0,84 (0,57 – 1,25) | |||
p = 0,39749 | ||||||
TFST – DCO 09 May�s 2016 | ||||||
Olay say�s�: Toplam hasta say�s� (%) | 106:136 (78) | 124:128 (97) | 55:74 (74) | 59:62 (95) | 47:57 (83) | 60:61 (98) |
Medyan s�re (ay) (%95 CI) | 13,3 | 6,7 | 15,6 | 6,2 | 12,9 | 6,9 |
| (11,3 – | (5,7 – | (11,9 – | (5,3 – | (7,8 – | (5,7 – |
| 15,7) | 8,2) | 28,2) | 9,2) | 15,3) | 9,3) |
HR (%95 CL) | 0,39 (0,30 – 0,52) | 0,33 (0,22 – 0,49) | 0,45 (0,30 – 0,66) | |||
P de�eri (2 yanl�) | p < 0,00001 | p < 0,00001 | p = 0,00006 | |||
T�m hastalar �u alt gruplardan olu�maktad�r: BRCA1/2-mutasyonu, BRCA1/2 wt/VUS ve BRCA1/2 durumu bilinmeyen (durumu bilinmeyen 11 hasta tabloda ayr� bir alt grup olarak g�sterilmemektedir).
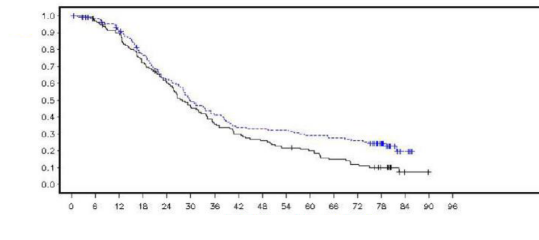
�ekil 6: �al��ma 19: DCO 09 May�s 2016'da FAS'de (%79 olgunluk) Kaplan-Meier OS grafi�i
bd g�nde iki defa; DCO veri kesme tarihi; FAS Tam analiz seti; OS Genel sa�kal�m
PFS analizi s�ras�nda medyan tedavi s�resi olaparib i�in 8 ay, plasebo i�inse 4 ay olarak belirlenmi�tir. Hastalar�n �o�u g�nde iki defa 400 mg �eklindeki ba�lang�� dozunda kalm��t�r. Advers olay nedeniyle doz duraklatma, azaltma, kesme insidans� s�ras�yla %34,6, %25,7 ve
%5,9 olmu�tur. Doz duraklatma ve azaltma en s�k olarak tedavinin ilk 3 ay� i�inde ortaya ��km��t�r. Dozun duraklat�lmas�naveyaazalt�lmas�naens�kneden olan advers olaylar bulant�,
anemi, kusma, n�tropeni ve bitkinlik olmu�tur. Anemi advers reaksiyonlar�n�n insidans�n�n
%22,8 (CTCAE derece ≥ 3 %7,4) oldu�u belirlenmi�tir.
TOI ve FACT-O toplam iyile�me ve k�t�le�me oranlar� ile de�erlendirildi�i �zere, hasta taraf�ndan bildirilen sonu� (PRO) verileri olaparib ile tedavi uygulanan hastalar ile plasebo aras�nda herhangi bir farka i�aret etmemektedir.
OPINION �al��mas�
Bir Faz IIIb tek kollu, �ok merkezli �al��ma olan OPINION'da olaparib, PSR yumurtal�k, fallop t�p� veya primer periton kanseri olan ve bilinen bir zararl� veya zararl� oldu�undan ��phelenilen gBRCA mutasyonu olmayan hastalarda, iki veya daha fazla basamak platin bazl� kemoterapiyi takiben idame tedavisi olarak ara�t�r�lm��t�r. Platin bazl� kemoterapinin tamamlanmas�n�n ard�ndan hastal��� yan�t veren (CR veya PR) hastalar �al��maya kaydedilmi�tir. Toplam 279 hasta kaydedilmi� olup bu hastalara, hastal�k progresyonuna veya kabul edilemez toksisiteye kadar olaparib tedavisi verilmi�tir. Merkezi teste g�re hastalar�n
%90,7'sinin durumu gBRCAm d��� olarak onaylanm��, ayr�ca %9,7'sinin durumu ise sBRCAm olarak tan�mlanm��t�r.
Primer sonlanma noktas�, de�i�tirilmi� RECIST v.1.1'e g�re ara�t�rmac� taraf�ndan de�erlendirilen PFS idi. Sekonder sonlanma noktalar� OS'i i�ermi�tir.
Olaparib, idame tedavisi olarak kullan�ld���nda, gBRCAm olmayan PSR yumurtal�k kanserli hastalarda klinik aktivite g�stermi�tir. Primer PFS analizi s�ras�nda, OS verileri %30 oran�nda mat�riteye sahipti.
OPINION'da gBRCAm olmayan PSR yumurtal�k kanserli hastalar i�in primer objektif sonucun bir �zeti Tablo 7' de sunulmu�tur.
Tablo 7: OPINION'da gBRCAm olmayan PSR yumurtal�k kanserli hastalar�n progresyonsuz sa�kal�m �zeti
| Olaparib tablet 300 mg bd |
PFS (%75 mat�rite) (DC2 2 Ekim 2020 | |
Olay say�s�: toplam hasta say�s� (%) | 210:279 (75.3) |
Medyan PFS (%95 CI), aya | 9.2 (7.6, 10.9) |
a Kaplan-Meier tekni�i kullan�larak hesaplanm��t�r.
Medyan PFS i�in g�ven aral�klar� Brookmeyer Crowley y�ntemine g�re t�retilmi�tir. bd: G�nde iki kez; PFD: Progresyonsuz sa�kal�m; DCO: Veri kesimi; CI: G�ven aral���.
HRD pozitif ileri evre yumurtal�k kanserinin birinci basamak idame tedavisi
PAOLA-1 �al��mas�
PAOLA-1, bevasizumab (her 3 haftada bir intraven�z inf�zyon olarak verilen 15 mg/kg) ile kombinasyon halinde verilen Lynparza'n�n (g�nde iki kez 300 mg [2 x 150 mg tablet]) etkililik ve g�venlili�ini birinci basamak platin bazl� kemoterapi ve bevasizumab� takiben ileri evre (FIGO Evre III-IV) y�ksek dereceli epitelyal over, fallop t�p� veya primer periton kanserinin idame tedavisi i�in plasebo ile kombine bevasizumab ile kar��la�t�ran bir Faz III randomize, �ift
k�r, plasebo kontroll�, �ok merkezli�al��mayd�.Bevasizumabtedavisi, kemoterapi ile birlikte
�al��mada 806 hasta (2:1 randomizasyon: 537 olaparib/bevasizumab: 269 plasebo/bevasizumab) randomize edilmi� olup bunlar tam cerrahi rezeksiyon nedeniyle hastal�k belirtisi olmayan (NED) ya da platin ve bevasizumab i�eren birinci basamak kemoterapinin tamamlanmas�ndan sonra tam yan�t (CR) ya da k�smi yan�t (PR) veren hastalard�. Hastalar minimum 4 ve maksimum 9 k�r� tamamlam�� olup �o�u (%63), minimum 2 k�r bevasizumab ile birlikte kemoterapinin son 3 k�r� dahil olmak �zere 6 k�r birinci basamak platin-taksan bazl� kemoterapi g�rm��t�r. Randomizasyon �ncesinde bevasizumab k�rlerinin medyan say�s� 5'ti.
Hastalar, birinci basamak tedavinin sonucuna (sitored�ktif cerrahinin zamanlamas� ve sonucu ile platin bazl� kemoterapiye yan�t) ve prospektif lokal testlerle belirlenen tBRCAm durumuna g�re katmanland�r�lm��t�r. Hastalar idame ortam�nda bevasizumaba devam etmi� ve son kemoterapi dozlar�n�n tamamlanmas�ndan minimum 3 hafta ve maksimum 9 hafta sonra Lynparza tedavisine ba�lam��t�r. Altta yatan hastal���n progresyonuna, kabul edilemez toksisiteye veya 2 y�la kadar Lynparza tedavisine devam edilmi�tir. Tedaviyi uygulayan doktorun d���ncesine g�re tedaviye devam edilmesinden daha da yarar sa�layabilece�i d���n�len hastalar 2 y�ldan daha uzun s�re tedavi edilebilir.
Demografik ve ba�lang�� �zellikleri, ITT pop�lasyonu ile tBRCAm (prospektif ve retrospektif olarak tan�mlanan), GIS ve HRD durumuna (bu �al��mada her iki biyobelirte�in kombinasyonu �eklinde tan�mlanan) g�re biyobelirte� tan�ml� alt gruplardaki her iki kolda dengeliydi. Hastalar�n medyan ya�� 61'di. Her iki koldaki �o�u hastan�n ECOG performans durumu 0'd� (%70). Yumurtal�k kanserinin hastalar�n %86's�nda primer t�m�r oldu�u g�r�lm��t�r. En yayg�n histolojik tipin ser�z (%96) oldu�u g�r�lm��t� ve hastalar�n %2'sinde endometrioid histoloji bildirilmi�tir. Hastalar�n �o�una FIGO evresi NIC'te tan� konmu�tu (%63). T�m hastalara birinci basamak platin bazl� tedavi ve bevasizumab verilmi�tir. Hastalar�n %63'�nde ilk veya aral�kl� t�m�r ��karma cerrahisinde tam sitored�ksiyon ve %37'sinde rezid�el makroskopik hastal�k olan hastalar cerrahi sonu�la s�n�rlanmam��t�r. Her iki koldaki hastalar�n y�zde otuzu (%30) taramada tBRCAm idi. Biyobelirte� alt gruplar�ndaki demografik ve ba�lang�� �zellikleri ITT pop�lasyonundakilerle tutarl�yd�. HRD-pozitif alt grubunda, hastalar�n %65'i tam sitored�ksiyon g�rm��t� ve hastalar�n %35'inde rezid�el makroskopik hastal�k vard�. Kaydolan genel hasta pop�lasyonunda, her iki koldaki hastalar�n %30'u lokal testlerle yap�lan taramada tBRCAm idi (y�k�c�/patojenik mutasyon) ve hastalar�n %4'� i�in BRCAm durumu bilinmiyordu. Mevcut klinik �rneklerin retrospektif analizi, tBRCAm durumunu do�rulamak ve yukar�da a��kland��� gibi genomik instabiliteyi ara�t�rmak �zere hastalar�n %97'si �zerinde ger�ekle�tirilmi�tir.
tBRCAm olmayan hastalar�n %29'unda (genel pop�lasyonun %19'u) bu �al��mada bile�ik skor
≥42 olarak �nceden tan�mlanm�� pozitif G�S vard�. tBRCAm durumu ve pozitif GIS birle�tirildi�inde, t�m�rleri HRD-pozitif, HRD-negatif ve HRD bilinmiyor durumunda olan hastalar genel hasta pop�lasyonunun %48'i, %34'� ve %18'ini temsil ediyordu.
Primer sonlanma noktas� modifiye Solid T�m�rlerde Yan�t De�erlendirme Kriterleri (RECIST)
progresyonuna kadar her 24 haftada bir (klinik veya CA 125 progresyonu ise 12 haftada CT/MRI) RECIST 1.1 t�m�r de�erlendirmeleri yap�lm��t�r.
�al��ma, plasebo/bevasizumab koluna k�yasla olaparib/bevasizumab kolu i�in ara�t�rmac� taraf�ndan de�erlendirilen PFS'de istatistiksel a��dan �nemli bir iyile�me sergileyen ITT pop�lasyonunda primer sonlanma noktas�n� kar��lam��t�r (plasebo/bevasizumab i�in medyan 16,6 ay kar��s�nda olaparib/bevasizumab i�in 22,1 ay ile HR 0,59, %95 GA 0,49-0,72, p<0,0001). Bu, PFS'nin BICR analizi ile tutarl�yd�. Bununla birlikte, biyobelirte� pozitif (tBRCAm ve/veya GIS pozitif olarak tan�mlanan tBRCAm, GIS, HRD durumu pozitif) olarak tan�mlanm�� hastalar en �ok fayday� g�rm��t�r.
Genel pop�lasyonda nihai PFS2 analizi (DCO 22 Mart 2020, %53 olgunluk) istatistiksel a��dan �nemliydi (HR 0,78, %95 GA, p=0,0125 plasebo/bevasizumab i�in 32,6 aya kar��l�k olaparib/bevasizumab i�in 36,5 ayl�k medyanla). Genel sa�kal�m verileri, genel pop�lasyon ve biyobelirte� alt gruplar�nda olgun de�ildi. Olaparib/bevasizumab kolundaki hastalar�n y�zde altm��� (%60) ile plasebo/bevasizumab kolundaki hastalar�n %74'� daha sonra tedavi g�rm��t�r ve olaparib/bevasizumab ve plasebo/bevasizumab kollar�ndaki bu hastalar�n s�ras�yla %20 ve
%47'si bir PARP inhibit�r� alm��t�r.
Randomize alt grup olarak tBRCAm'de (241/806 hasta) olaparib/bevasizumab kolu i�in medyan PFS 37,2 ay iken plasebo/bevasizumab kolu i�in 22,0 ayd� (HR = 0,34, %95 GA 0,23,0,51) ve OS (DCO 22 Mart 2020) HR 0,68 (%95 GA 0,40, 1,19) idi.
Retrospektif olarak analiz edilen t�m�r �rneklerine dayanan di�er biyobelirte� alt grup analizlerindeki etkililik sonu�lar� Tablo 8'de sunulmaktad�r.
Tablo 8 PAOLA-1'de ileri evre yumurtal�k kanseri hastalar�nda tBRCAm ve/veya GIS ile tan�mlanan homolog rekombinasyon eksikli�i (HRD) pozitif durumu olan hastalar i�in temel etkililik bulgular�n�n �zeti
| tBRCAm*, (n=235) | GIS pozitif *, (n=152) | HRD pozitif* (n=387) | |||
| Olaparib / bevasizumab | Plasebo / bevasizumab | Olaparib / bevasizumab | Plasebo / bevasizumab | Olaparib / bevasizumab | Plasebo / bevasizumab |
PFS, ara�t�rmac� de�erlendirmesi (%46 olgunluk) DCO 22 Mart 2019 | ||||||
Olay say�s�: Toplam hasta say�s� (%) |
44/158 (28) |
52/77 (68) |
43/97 (44) |
40/55 (73) |
87/255 (34) |
92/132 (70) |
Medyan s�re (ay) | 37,2 | 18,8 | 28,1 | 16,6 | 37,2 | 17,7 |
HR (%95) GA | 0,28 (0,19, 0,42) | 0,43 (0,28, 0,66) | 0,33 (0,25, 0,45) | |||
PFS2, ara�t�rmac� de�erlendirmesi (%40 olgunluk) DCO 22 Mart 2019 | ||||||
Olay say�s�: Toplam hasta say�s� (%) |
44/158 (28) |
37/77(48) |
41/97 (42) |
33/55 (60) |
85/255 (33) |
70/132 (53) |
Medyan s�re (ay) | NR | 42,2 | 50,3 | 30,1 | 50,3 | 35,4 |
HR (%95) GA | 0,53 (0,34, 0,82) | 0,60 (0,38, 0,96) | 0,56 (0,41, 0,77) //www.turkiye.gov.tr/saglik-titck-ebys | |||
Ara OS (%27 olgunluk) k) DCO 22 Mart 2020 | ||||||
Olay say�s�: Toplam hasta say�s� (%) |
31/158 (20) |
23/77 (30) |
30/97 (31) |
19/55 (35) |
61/255 (24) |
42/132 (32) |
Medyan s�re (ay) | NR | NR | NR | 45,8 | NR | NR |
HR (%95) GA | 0,61 (0,36, 1,06) | 0,84 (0,48, 1,52) | 0,70 (0,47, 1,04) | |||
* �nceden planlanan alt grup
%71 ve %29 kar��s�nda olaparib/bevasizumab i�in %89 ve %66 idi.
Myriad ile genomik instabilite skoru (GIS) ≥42 (�nceden belirlenmi� e�ik) GA G�ven aral���; HR Risk oran�; NR ula��lamad�.
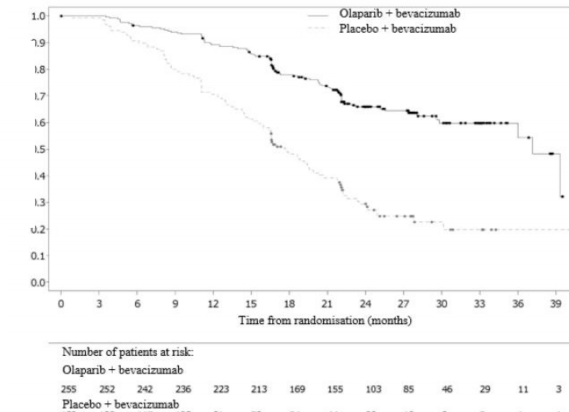
Olays�z hasta oran�
�ekil 7: PAOLA-1: PAOLA-1'de HRD pozitif olarak tan�mlanm�� ileri evre yumurtal�k kanseri olan hastalar i�in Kaplan Meier PFS grafi�i (%46 olgunluk - ara�t�rmac� de�erlendirmesi)
Germline BRCA mutasyonlu y�ksek riskli erken evre meme kanserinin adjuvan tedavisi
OlympiA
Definitif lokal tedaviyi ve neoadjuvan veya adjuvan kemoterapiyi tamamlam�� germline BRCA1/2 mutasyonlar� ve HER2-negatif y�ksek riskli erken meme kanseri olan hastalarda adjuvan tedavi olarak olaparibin g�venlili�i ve etkilili�i, bir Faz III randomize, �ift k�r, paralel grup, plasebo kontroll�, �ok merkezli �al��mada (OlympiA) incelenmi�tir. Hastalar�n antrasiklin, taksan veya her ikisini birden i�eren en az 6 k�r neoadjuvan veya adjuvan kemoterapisini tamamlamalar� gerekiyordu. �nceki kanser (�r. yumurtal�k) i�in veya meme kanserinde adjuvan veya neoadjuvan tedavi olarak daha �nce platine izin verilmi�tir. Y�ksek riskli erken meme kanseri hastalar� �u �ekilde tan�mlanm��t�r:
daha �nce neoadjuvan kemoterapisi alm�� hastalar: ��l� negatif meme kanseri (TNBC) veya hormon resept�r� pozitif meme kanseri olan hastalarda, cerrahi s�ras�nda memede ve/veya rezeke edilen lenf d���mlerinde (patolojik olmayan tam yan�t) rezid�el invazif kanser bulunmal�d�r. Ek olarak, hormon resept�r� pozitif meme kanseri olan hastalar�n, Tablo 9'da g�sterildi�i gibi tedavi �ncesi klinik ve tedavi sonras� patolojik evre (CPS), �strojen resept�r� (ER) durumu ve histolojik dereceye g�re ≥ 3 CPS&EG skoruna sahip olmas� gerekir.
Tablo 9: �al��maya Kay�t i�in Erken Evre Meme Kanseri, Resept�r Durumu ve Derece Puanlama Gereklilikleri
Evre / �zellik | Noktalar | |
Klinik evre (tedavi �ncesi) | I/IIA | 0 |
IIB/IIIA | 1 | |
IIIB/IIIC | 2 | |
Patolojik Evre (tedavi sonras�) | 0/I | 0 |
IIA/IIB/IIIA/IIIB | 1 | |
IIIC | 2 | |
Resept�r durumu | ER pozitif | 0 |
ER negatif | 1 | |
N�kleer derece | N�kleer derece 1-2 | 0 |
N�kleer derece 3 | 1 | |
* Hormon resept�r� pozitif meme kanseri olan hastalar i�in toplam skorun ≥ 3 olmas� gerekiyordu.
5.2. Farmakokinetik �zellikler
Genel �zelliklerOlaparibin 300 mg tablet dozundaki farmakokineti�i, ~7 L/saatlik g�r�n�r plazma klirensi,
~158 L'lik g�r�n�r da��l�m hacmi ve 15 saatlik terminal yar�lanma �mr� ile karakterizedir. �oklu dozlama ile 1.8'lik EAAbirikmeoran� g�zlenmi�tirve farmakokineti�in d���k bir
Emilim:
Olaparibin tablet form�lasyonu (2 x 150 mg) ile oral uygulanmas� sonras�nda emilim h�zl� olup, medyan doruk plazma konsantrasyonlar�na tipik olarak doz uygulamas�ndan 1.5 saat sonra ula��l�r.
Yiyecekler ile birlikte uygulama olaparib emiliminin h�z�n� azaltm�� (t2.5 saat gecikmi� ve Cyakla��k %21 azalm��t�r); fakat emilimin boyutunu anlaml� �l��de etkilememi�tir (EAA
%8 artm��t�r). Dolay�s�yla LYNPARZA, a� veya tok karn�na al�nabilir (bkz. B�l�m 4.2).
Da��l�m:
�n vitro plazma proteinlerine ba�lanmas�, klinik olarak anlaml� olan 10 µg/mL'lik konsantrasyonlarda yakla��k %82'dir.
�n vitro ko�ullarda olaparibin insan plazma proteinlerine ba�lanma oran� doza ba��ml�d�r; ba�lanan k�s�m 1 μg/mL'de yakla��k %91 iken, 10 μg/mL'de %82 ve 40 μg/mL'de %70'e d��m��t�r. Safla�t�r�lm�� protein ��zeltilerinde alb�mine ba�lanan olaparib fraksiyonu yakla��k
%56 olup, olaparib konsantrasyonlar�ndan ba��ms�zd�r. Ayn� analiz kullan�larak, alfa-1 asit glikoproteine ba�lanan fraksiyon 10 μg/mL'de %29 iken, daha y�ksek konsantrasyonlarda azalm�� ba�lanma e�ilimi g�zlenmi�tir.
Biyotransformasyon:
�n vitro ko�ullarda CYP3A4/5'lerin olaparibin metabolizmas�ndan esasen sorumlu izoenzimler oldu�u g�sterilmi�tir (bkz. B�l�m 4.5).
Kad�n hastalara 14C-olaparibin oral yolla verilmesinden sonra de�i�memi� olaparib plazmadaki radyoaktivitenin b�y�k k�sm�n� olu�turmu� (%70) ve gerek idrar gerekse fe�este bulunan ana bile�en olmu�tur (dozun s�ras�yla %15'i ve %6's�). Olaparibin metabolizasyonu yayg�nd�r. Metabolizman�n b�y�k k�sm� oksidasyon reaksiyonlar�na dayanmakta ve �retilen bile�enlerin bir k�sm� sonras�nda glukuronid veya s�lfat konj�gasyonuna u�ramaktad�r. Plazma, idrar ve fe�este s�ras�yla 20, 37 ve 20'ye kadar metabolit tespit edilmi�tir ve bunlar�n �o�u dozlanan materyalin <%1'ini temsil etmektedir. Bir a��k halkal� piperazin-3-ol k�sm� ve iki mono- oksijenli metabolit (her biri yakla��k %10) dola��mdaki ba�l�ca bile�enler olup, mono-oksijenli metabolitlerden birinin ayr�ca d��k�daki maj�r metabolit oldu�u belirlenmi�tir (idrar ve fe�esteki radyoaktivitenin s�ras�yla %6's� ve %5'i).
Olaparib, in vitro olarak UGT1A4, UGT1A9, UGT2B7 veya CYP 1A2, 2A6, 2B6, 2C8, 2C9, 2C19, 2D6 veya 2E1'i �ok az inhibe etmi�/hi� inhibe etmemi�tir ve bu CYP enzimlerinin herhangi birinin klinik olarak anlaml�, zamana ba�l� bir inhibit�r� olmas� beklenmez. Olaparib, UGT1A1'i in vitro olarak inhibe etmi�tir, ancak PBPK sim�lasyonlar� bunun klinik �nemi olmad���n� d���nd�rmektedir. Olaparib, in vitro olarak d�� ak�m ta��y�c�s� P-gp'nin bir substrat�d�r, ancak bunun klinik olarak anlaml� olmas� olas� de�ildir (bkz. b�l�m 4.5).
�n vitro ko�ullardan elde edilen veriler olaparibin OATP1B1, OATP1B3, OCT1, BCRP veya MRP2 substrat� olmad���n�, ve OATP1B3, OAT1 veya MRP2'nin inhibit�r� olmad���n� g�stermektedir.
Eliminasyon:
Tek bir 14C-olaparib dozundan sonra, radyoaktivitenin yakla��k %86's� 7 g�nl�k toplama s�resi i�inde tespit edilmi�tir. Bunun yakla��k %44'� idrar ile, yakla��k %42'si fe�es iledir. Materyalin �o�u metabolitler halinde at�lm��t�r.
Do�rusall�k/Do�rusal olmayan durum:
LYNPARZA isimli �r�n�m�z�n doz ve / veya zaman a��s�ndan etkin madde farmakokineti�inin do�rusall��� / do�rusal olmamas� durumu uygulanabilir de�ildir.
Hastalardaki karakteristik �zellikler
Pop�lasyon bazl� farmakokinetik analizlerde hasta ya��, v�cut a��rl��� veya �rk� (Beyaz ve Japon hastalar� i�erir) anlaml� e�de�i�kenler olmam��t�r.
B�brek yetmezli�i:
B�brek fonksiyonlar� normal olan hastalar ile kar��la�t�r�ld���nda hafif derecede b�brek yetmezli�i (kreatinin klirensi 51 ila 80 mL/dk) olan hastalarda EAA de�eri %24, Cde�eri
%15 artm��t�r. LYNPARZA hafif derecede b�brek yetmezli�i olan hastalara herhangi bir doz ayarlamas� yap�lmadan uygulanabilir.
B�brek fonksiyonlar� normal olan hastalar ile kar��la�t�r�ld���nda orta derecede b�brek yetmeli�i (kreatinin klirensi 31 ila 50 mL/dk) olan hastalarda EAA de�eri %44, Cde�eri
%26 artm��t�r. Orta derecede b�brek yetmezli�i olan hastalar i�in LYNPARZA dozunun ayarlanmas� �nerilir (bkz. B�l�m 4.2).
A��r derecede b�brek yetmezli�i veya son evre b�brek yetmezli�i (kreatinin klirensi < 30 mL/dk) olan hastalara ili�kin veri bulunmamaktad�r.
Karaci�er yetmezli�i:
Karaci�er fonksiyonu normal olan hastalarla kar��la�t�r�ld���nda hafif karaci�er yetmezli�i (Child Pugh s�n�fland�rmas� A) g�r�len hastalarda EAA %15, Cmaks ise %13 artarken, orta dereceli karaci�er yetmezli�i (Child Pugh s�n�fland�rmas� B) g�r�len hastalarda EAA %8, Cmaks ise %13 artm��t�r. Hafif veya orta dereceli karaci�er yetmezli�i bulunan hastalarda Lynparza dozunun ayarlanmas�na gerek yoktur (bkz. b�l�m 4.2). �iddetli karaci�er yetmezli�i (Child Pugh s�n�fland�rmas� C) olan hastalarla ilgili veri mevcut de�ildir.
Pediyatrik pop�lasyon:
Pediyatrik hastalarda olaparibin farmakokineti�ini incelemek �zere herhangi bir �al��ma ger�ekle�tirilmemi�tir.
5.3. Klinik �ncesi g�venlilik verileri
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Tablet �ekirde�iEkstrudat yard�mc� maddeleri
Kopovidon K28 Kolloidal silikon dioksit
Ekstr�zyon sonras� yard�mc� maddeler
Mannitol
Sodyum stearil fumarat Kolloidal silikon dioksit
Tablet kaplamas�
Hipromelloz 2910
Makrogol 400
Titanyum dioksit (E171) Sar� demir oksit (E172) Saf su
6.2. Ge�imsizlikler
Bilinen herhangi bir ge�imsizli�i bulunmamaktad�r.
6.3. Raf �mr�
48 ay
6.4. Saklamaya y�nelik �zel tedbirler
30°C'nin alt�ndaki oda s�cakl���nda saklay�n�z. Nemden korumak i�in orijinal ambalaj�nda saklay�n�z.
6.5. Ambalaj�n niteli�i ve i�eri�i
Alu/Alu perfore olmayan blister. Ambalaj b�y�kl���:56 film kapl� tablet (7 blister)
112 film kapl� tablet i�eren �oklu ambalaj (56 tabletlik iki paket)
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj At�klar�n�n Kontrol� Y�netmelik”lerine uygun olarak imha edilmelidir.
 A��r� Alkol Kullan�m�, Alkolizm
Alkol ba��ml�l���, alkol kullan�m� ve alkol sorunlar� aras�ndaki fark� a��klamak g��t�r.
�rne�in, ge�mi�te alkol kullanm�� olan bir kimsenin mutlaka alkol ba��ml�s� olmas�
gerekmez.
A��r� Alkol Kullan�m�, Alkolizm
Alkol ba��ml�l���, alkol kullan�m� ve alkol sorunlar� aras�ndaki fark� a��klamak g��t�r.
�rne�in, ge�mi�te alkol kullanm�� olan bir kimsenin mutlaka alkol ba��ml�s� olmas�
gerekmez. |
 Diyabet Hastal���
Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r.
Diyabet Hastal���
Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r. |
 |
Y�ksek Tansiyon Hipertansiyon s�rekli anormal derecede y�ksek olan kan bas�nc�d�r. Tansiyon atardamarlar�n�zdaki kan�n bas�nc�d�r. |
 |
Rahim Boyu ( Serviks ) Kanseri Rahim boynu (serviks) kanseri 35 ya� alt� kad�nlarda g�r�len vakalarda meme kanserinden sonra ikinci s�ray� al�r.Serviks kanserinin geli�mesi y�llarca s�rebilir. |
 |
Asperger Sendromu Asperger sendromu, otistik gurubun bir b�l�m� olan bir �z�rd�r. Bu genelde, gurubun daha ”y�ksek” taraf�nda yer ald��� d���n�len ki�ilere uygun bir tan�d�r. |
�LA� GENEL B�LG�LER�
AstraZeneca T�rkiye �la� Sanayi ve Ticaret Ltd.�ti.
| Sat�� Fiyat� | 50694.42 TL [ 17 Dec 2024 ] |
| �nceki Sat�� Fiyat� | 50694.42 TL [ 2 Dec 2024 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | K�s�tlanm�� Beyaz Re�eteli bir ila�d�r. |
| Barkodu | 8699786092907 |
| Etkin Madde | Olaparib |
| ATC Kodu | L01XK01 |
| Birim Miktar | 100 |
| Birim Cinsi | MG |
| Ambalaj Miktar� | 56 |
| Antineoplastik ve �mm�nomod�lat�r Ajanlar > Di�er Kanser �la�lar� |
| �thal ( ref. �lke : Yunanistan ) ve Be�eri bir ila�d�r. |