MACROL 250 mg/5 ml 100 ml SUSP Klinik Özellikler
{ Klaritromisin }
4. KLİNİK ÖZELLİKLER
4.1. Terapötik endikasyonlar
12 yaşından küçük pediyatrik hastalar
6 ay- 12 yaş arasındaki çocuklarda yürütülen klinik çalışmalar klaritromisin pediatrik süspansiyon ile yapılmıştır. Bu nedenle 12 yaşından küçük çocuklar klaritromisin pediatrik süspansiyon (oral süspansiyon için granül) kullanmalıdır.
MACROL aşağıdaki durumlarda, duyarlı organizmaların sebep olduğu enfeksiyonların tedavisinde endikedir:
Haemophilus influenzae, Moraxella catarrhalis, Streptococcus pneumoniae ve Streptococcus pyogenes'ten kaynaklanan farenjit, tonsillit ve akut maksiller sinüzit gibi üst solunum yolu enfeksiyonları.
Staphylococcus aureus, Streptococcus pyogenes'ten kaynaklanan impetigo, folikülit, selülit, erizipel, abseler gibi komplike olmayan deri ve yumuşak doku enfeksiyonları (abseler genellikle cerrahi drenaj gerektirir).
4.2. Pozoloji ve uygulama şekli
Pozoloji:MACROL Oral Süspansiyon (250 mg/5 ml) çocuklarda tavsiye edilen dozu günde iki defa 7,5 mg/kg olup mikobakteriyel olmayan enfeksiyonlar için maksimum doz günde iki defa 500 mg'dır. Dozajı belirlemek için aşağıdaki tablo yol gösterici olabilir:
ÇOCUKLARDA MACROL SÜSPANSİYON (250 mg/5 ml) DOZ TAYİNİ
Vücut Ağırlığına Göre KAŞIK DOZ TABLOSU
Vücut Ağırlığı* | Günde 2 kez uygulanan standart kaşık dozu | Doz |
8 - 11 kg | 1/4 kaşık | 62.5 mg |
12 - 19 kg | 1/2 kaşık | 125 mg |
20 - 29 kg | 3/4 kaşık** | 187.5 mg |
30 - 40 kg | 1 kaşık | 250 mg |
*Vücut ağırlığı (kg) esas alınarak hazırlanmıştır.
** Hastaya önce 1/2 (yarım) kaşık ve sonra 1/4 (çeyrek) kaşık verilerek 3/4 kaşık verilmesi sağlanmış olur.
Kilosu 8 kg'dan az çocuklara 0,15 ml/kg (7,5 mg/kg) dozda günde 2 kez verilmelidir.
Mikobakteriyel Enfeksiyonları Olan Hastalarda Dozaj
Yaygın veya lokalize mikobakteriyel enfeksiyonları olan çocuklarda (M. avium, M. intracellulare, M. chelonae, M. fortuitum, M. kansasii), önerilen doz, günde iki doza bölünmüş olarak 15 - 30 mg/kg klaritromisindir.
Klinik yarar gösterildiği sürece klaritromisin tedavisine devam edilmelidir. Başka antimikobakteriyel ajanların ilave edilmesi yararlı olabilir.
MİKOBAKTERİYEL ENFEKSİYONLARI OLAN PEDİYATRİK HASTALAR İÇİN DOZ TAYİNİ
Vücut Ağırlığına Göre KAŞIK DOZ TABLOSU
Ağırlık* | Günde 2 kez uygulanan standart kaşık dozu | |
15 mg/kg | 30 mg/kg | |
8 - 11 | ½ kaşık | 1 kaşık |
12 - 19 | 1 kaşık | 2 kaşık |
20 - 29 | 1½ kaşık | 3 kaşık |
30 - 40 | 2 kaşık | 4 kaşık |
*Ağırlığı ortalama <8 kg olan çocuklarda doz miktarı günde ortalama kg başına 15 - 30 mg olacak şekilde kg'a göre düzenlenmelidir.
Uygulama sıklığı ve süresi:
Normal tedavi süresi, ilgili patojene ve hastalığın şiddetine bağlı olarak 5 ila 10 gün arasındadır.
Uygulama şekli:
Sulandırılmış ilaç aç veya tok karnına verilebilir, ayrıca sütle de alınabilir.
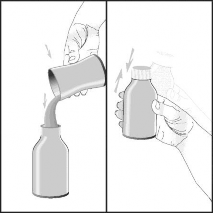
Süspansiyonun hazırlanması:
Açmadan önce şişeyi 2-3 kez çalkalayınız.
Şişeye, şişe üzerindeki işaret çizgisini geçmeyecek şekilde bir miktar kaynatılıp soğutulmuş su ilave edip, kuvvetlice çalkalayınız.
Birkaç dakika bekleyiniz. Sıvının düzeyi alçalacaktır. İşaret çizgisine kadar tekrar su ile tamamlayınız ve bu suretle elde edilen süspansiyonu yeniden çalkalayınız.
Her kullanımdan önce şişeyi iyice çalkalayınız. İlacın alınması:
İlacı kaşık ile çocuğunuza verebilirsiniz. Uygulama sırasında doktorunuzun önerdiği şekilde kaşık tablosunu esas alınız.
Özel popülasyonlara ilişkin ek bilgiler Böbrek/karaciğer yetmezliği:
Kreatinin klerensi 30 ml/dak'dan az olan çocuklarda klaritromisin dozu yarıya düşürülmelidir. Örneğin günde bir defa 250 mg'a kadar veya daha şiddetli vakalarda günde 2 defa 250 mg. Bu hastalarda tedavi süresi 14 günü geçmemelidir. Orta dereceden şiddetli dereceye kadar böbrek bozukluğu olan hastalarda da dikkatle uygulanmalıdır.
Karaciğer fonksiyonu bozuk olan hastalara klaritromisin uygulanırken dikkatli olunmalıdır. Bununla birlikte, şiddetli böbrek yetmezliği durumlarında, beraberinde karaciğer yetmezliği olsun veya olmasın, dozun azaltılması veya doz aralarının uzatılması uygun olabilir.
4.3. Kontrendikasyonlar
Klaritromisin, makrolid antibiyotiklere ya da içindeki herhangi bir maddeye karşı bilinen aşırı duyarlığı olan hastalarda kontrendikedir.
Klaritromisinin şu ilaçlardan biri ile beraber kullanılması QT uzaması ve ventriküler taşikardi, ventriküler fibrilasyon ve torsades de pointes gibi kardiyak aritmilere neden olabileceğinden kontrendikedir: Astemizol, sisaprid, pimozid ve terfenadin.
Klaritromisinin ergotamin ve dihidroergotamin ile beraber kullanılması ergot toksisitesine neden olabileceğinden kontrendikedir.
Klaritromisin, rabdomiyolizi de içeren miyopati artışı riski sebebiyle, CYP3A4 ile büyük ölçüde metabolize olan HMG-CoA redüktaz inhibitörleri (statinler; lovastatin veya simvastatin) ile eşzamanlı olarak kullanılmamalıdır.
Kolşisin P-glikoprotein ya da güçlü bir CYP3A4 inhibitörü kullanan renal ya da hepatik yetmezliği olan hastalarda kontrendikedir (bkz. Bölüm Özel kullanım uyarıları ve önlemleri ve Bölüm Diğer tıbbi ürünler ile etkileşimler).
Klaritromisin QT uzaması ya da Torsades de Pointes dahil ventriküler kardiyak aritmi öyküsü olan hastalara verilmemelidir (bkz. Bölüm Özel kullanım uyarıları ve önlemleri ve Bölüm Diğer tıbbi ürünler ile etkileşimler).
Hipokalemi (QT aralık uzaması riski) olan hastalara klaritromisin verilmemelidir.
Böbrek bozukluğu ile birlikte şiddetli karaciğer yetmezliği olan hastalarda klaritromisin kullanılmamalıdır.
4.4. Özel kullanım uyarıları ve önlemleri
MACROL oral süspansiyon ergenlik çağını aşan hastalarda kullanılacağında, eğer gebelik mevcut veya şüpheleniliyorsa, hekim tarafından yarar/risk faktörleri özenle tartılmalıdır.
Diğer antibiyotik kullanımlarında görüldüğü gibi uzun dönem kullanımı duyarlı olmayan bakteri ve mantarların sayısında artışa yol açar. Eğer süperinfeksiyon meydana gelirse, uygun tedaviye başlanmalıdır.
H. pylori infeksiyonunda ilaç direnci gelişmiş organizmalar için klaritromisin gibi herhangi bir antimikrobiyal tedavi seçilebilir.
Klaritromisin ile triazolam ve midazolam gibi triazolobenzodiazepinlerin eşzamanlı kullanımında dikkatli olunmalıdır (bkz. Bölüm 4.5. Diğer tibbi ürünler ile etkileşimler ve diğer etkileşim şekilleri).
QT uzaması riski nedeniyle, klaritromisin koroner arter hastalığı, şiddetli kalp yetmezliği, hipomagnezemi, bradikardi (<50 vuru/dk) durumunda ya da QT uzaması ile ilişkili diğer tıbbi ürünler ile eşzamanlı kullanımında dikkatli olunmalıdır (bkz. Diğer tıbbi ürünler ile etkileşimler).
Klaritromisin konjenital ya da belgelenmiş kazanılmış QT uzaması ya da ventriküler aritmi öyküsü olan hastalarda kullanılmamalıdır (bkz. bölüm 4.3 Kontrendikasyonlar).
Psödomembranöz kolit
Makrolidler dahil olmak üzere hemen hemen bütün antibakteriyel ajanlarla psödomembranöz kolit görülmüştür ve şiddeti hafiften hayatı tehdit eden dereceye kadar uzanabilir. Dolayısıyla, antibakteriyel ajanların uygulanmasından önce, diyaresi bulunan hastalarda bu teşhisin değerlendirmeye alınması önem taşır.
Clostridium difficile ile ilişkili diyare (CDAD) klaritromisin de dahil olmak üzere hemen hemen tüm antibakteriyel ajanların kullanımında bildirilmiştir ve diyarenin şiddeti hafiften
ölümcül kolite kadar değişmektedir. Antibakteriyel ajanların tedavisi C. difficile'nin çoğalmasına yol açabilecek olan kolonun normal florasında değişikliğe yol açar. CDAD antibiyotik kullanımını takiben gelişen diyare olan tüm hastalarda dikkate alınmalıdır. Antibakteriyel ajanların uygulanmasını takiben 2 aydan uzun süre sonra bile CDAD oluşumunun rapor edilmesi dikkatli bir medikal öykü alınmasını gerektirir.
Antibakteriyel ajanlarla tedavi, kalın barsağın normal florasını değiştirir ve klostridyumların aşırı üremesine sebep olabilir. Çalışmalar, Clostridium difficile'in ürettiği bir toksinin antibiyotiğe bağlı kolitin esas nedeni olduğunu göstermiştir.
Psödomembranöz kolit teşhisi konulduktan sonra tedaviye yönelik önlemler başlatılmalıdır. Hafif derecede psödomembranöz kolit vakaları genellikle sadece ilacın kesilmesine yanıt verirler. Orta ile şiddetli durumlarda sıvı, elektrolit tedavisi, protein desteği ve Clostridium difficile kolitine karşı etkili bir antibakteriyel ilaçla tedavi uygulanmalıdır.
Klaritromisin tedavisi alan hastalarda myastenia gravis belirtilerinin şiddetlendiği bildirilmiştir.
Böbrek ve karaciğer yetmezliği
Klaritromisin başlıca karaciğer tarafından atılır. Dolayısıyla bozuk karaciğer fonksiyonlu hastalara klaritromisin uygulanırken dikkatli olunmalıdır. Klaritromisin ile karaciğer enzimlerinde artış ve sarılık ile ya da tek başına hepatosellüler ve/veya kolestatik hepatiti de içeren hepatik disfonksiyon bildirilmiştir. Bu hepatik disfonksiyon şiddetli olabilir ve genellikle geri dönüşümlüdür. Bazı olgularda, ölümcül hepatik yetmezlik bildirilmiştir ve genellikle altta yatan şiddetli hastalık ve/veya eşzamanlı ilaç kullanımı ile ilişkilidir. Anoreksi, sarılık, koyu renkli idrar, kaşıntı ya da karında hassasiyet gibi hepatit belirti ve semptomları ortaya çıktığında klaritromisin hemen kesilmelidir.
Orta dereceden şiddetli dereceye kadar böbrek yetmezliği olan hastalarda dikkatli olunmalıdır. Bununla birlikte, şiddetli böbrek yetmezliği durumlarında, beraberinde karaciğer yetmezliği olsun veya olmasın, dozun azaltılması veya doz aralarının uzatılması uygun olabilir.
Kolşisin toksisitesi
Klaritromisin ve kolşisin birlikte kullanıldığında, özellikle yaşlılarda olmak üzere ve bazıları böbrek yetmezliği olan hastalarda ortaya çıkan kolşisin toksisitesi bildirimleri bulunmaktadır. Bu hastaların bazılarında ölümler bildirilmiştir (bkz. Bölüm Diğer tıbbi ürünler ile etkileşimler). Klaritromisin ve kolşisinin birlikte uygulanması gereken durumlarda hastalar kolşisin toksisitesi klinik belirtileri açısından gözlenmelidir. Kolşisin dozu, kolşisin ve klaritromisini birlikte alan tüm hastalarda azaltılmalıdır. Klaritromisin ve kolşisinin birlikte uygulanması, böbrek veya karaciğer yetmezliği olan hastalarda kontrendikedir (bkz. Bölüm 4.3).
Makrolid antibiyotikler
Klaritromisin ile linkomisin ve klindamisinde olduğu gibi diğer makrolid antibiyotiklerle çapraz rezistans olasılığı da düşünülmelidir.
Klaritromisin ile diğer ototoksik ilaçlar ve özellikle aminoglikozitlerin eşzamanlı kullanımında dikkatli olunmalıdır. Tedavi sırasında ve sonrasında vestibular ve işitme işlevleri izlenmelidir.
Oral hipoglisemik ajanlar/insülin
Klaritromisinin ve oral hipoglisemik ajanların ve/veya insülinin eşzamanlı kullanımı, önemli ölçüde hipoglisemiye neden olabilir. Nateglinid, pioglitazon, repaglinid ve rosiglitazon gibi belirli hipoglisemik ilaçlarla eşzamanlı olarak kullanıldığında, klaritromisin CYP3A enziminin inhibisyonuna ve sonuç olarak da hipoglisemiye neden olabilir. Bu gibi durumlarda glikoz seviyesinin dikkatle izlenmesi tavsiye edilir.
Oral antikoagülanlar
Klaritromisin varfarin ile birlikte uygulandığında, ciddi bir hemoraji riski ve INR, protrombin zamanında önemli artış riski vardır. Hastalar eşzamanlı olarak klaritromisin ve antikoagülan kullanırken, INR ve protrombin zamanları sık sık kontrol edilmelidir.
HMG-CoA redüktaz inhibitörleri (Statinler)
Klaritromisinin lovastatin ya da simvastatin ile eşzamanlı kullanımı, bu statinlerin büyük ölçüde CYP3A4 tarafından metabolize edilmesi ve klaritromisin ile eşzamanlı tedavinin plazma konsantrasyonlarını arttırarak rabdomiyaliz dahil miyopati riskini arttırması nedeniyle kontrendikedir (bkz. Bölüm 4.3 Kontrendikasyonlar). Bu statinler ile eşzamanlı olarak klaritromisin alan hastalarda rabdomiyoliz raporlanmıştır. Klaritromisin ile tedavi kaçınılmaz ise tedavi sırasında lovastatin veya simvastatin ile terapiye ara verilmelidir.
Klaritromisini statinler ile birlikte reçetelerken dikkatli olunmalıdır. Klaritromisinin statinler ile eşzamanlı kullanımının kaçınılmaz olduğu durumlarda, statinin kayıtlı olan en düşük dozunun yazılması önerilmektedir. CYP3A metabolizmasına bağımlı olmayan statinlerin (örn. fluvastatin) kullanımı değerlendirilebilir.
Klaritromisin, sitokrom CYP3A4 enzimini indükleyen ilaçlarla eşzamanlı kullanıldığında dikkatli olunmalıdır (bkz. Bölüm 4.5. Diğer tibbi ürünler ile etkileşimler ve diğer etkileşim şekilleri).
Pnömoni
Streptococcus pneumoni'nin makrolidlere karşı direnç geliştirmesi açısından, toplumda kazanılmış pnömoni için klaritromisin verilmeden önce duyarlılık testi yapılması önemlidir. Hastanede kazanılmış pnömonide klaritromisin uygun ek antibiyotiklerle kombinasyon halinde kullanılmalıdır.
Hafif ve orta şiddette deri ve yumuşak doku enfeksiyonları
Bu enfeksiyonlara sıklıkla makrolidlere direnç geliştirebilen Staphylococcus aureus ve Streptococcus pyogenes ya da her ikisi birlikte neden olur. Bu nedenle duyarlılık testinin yapılması önemlidir. Beta–laktam antibiyotiklerin kullanılamadığı (örn. allerji nedeniyle) olgularda, klindamisin gibi diğer antibiyotikler ilk seçenek ilaç olabilir. Güncel olarak makrolidlerin yalnızca Corynebacterium minutissimum (eritrazma) kaynaklı enfeksiyonlar, akne vulgaris ve erizipel gibi bazı deri ve yumuşak doku enfeksiyonlarda ve penisilin tedavisinin kullanılamadığı durumlarda rol oynadığı düşünülmektedir.
Anafilaksi, Stevens-Johnson Sendromu, toksik epidermal nekroliz, DRESS ve Henoch- Schonlein purpurası gibi şiddetli akut hipersensitivite reaksiyonları durumunda, hemen klaritromisin tedavisi kesilmeli ve uygun tedaviye başlanmalıdır.
Koroner arter hastalığı olan hastalarda klaritromisin ile tedavinin sonuçlarının değerlendirildiği bir klinik çalışmada, klaritromisin almak üzere randomize edilmiş hastalarda, tedavi bitiminden bir yıl ya da daha fazla süre sonra, tüm nedenlere bağlı ölüm riskinde artış gözlenmiştir. Klaritromisin koroner arter hastalığının tedavisinde endike değildir. Risk artışının nedeni belirlenememiştir. Bu riskin değerlendirildiği diğer epidemiyolojik çalışmalar değişken sonuçlara ulaşmıştır. Koroner arter hastalığı veya şüphesi olan hastalarda klaritromisin kullanmadan önce yarar-risk değerlendirmesi yapılmalıdır.
MACROL oral süspansiyon şeker içermektedir. Nadir kalıtımsal früktoz intoleransı, glikoz- galaktoz malabsorpsiyon veya sükraz-izomaltaz yetmezliği problemi olan hastaların bu ilacı kullanmamaları gerekir.
MACROL oral süspansiyon'nun içeriğinde bulunan hint yağı, mide bulantısı ve ishale sebep olabilir.
Bu tıbbi ürün her bir dozununda 20 mg potasyum ihtiva eder. Bu durum, böbrek fonksiyonlarında azalma olan hastalar ya da kontrollü potasyum diyetinde olan hastalar için göz önünde bulundurulmalıdır.
4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri
Aşağıda yer alan ilaçların kullanımı ciddi ilaç etkileşimleri dolayısıyla kontrendikedir.
Sisaprid, pimozid, astemizol ve terfenadin: Klaritromisin sisaprid ile birlikte uygulandığında, sisaprid seviyeleri yükselebilir. Bu durum özellikle kalp hastalarında QT aralığı genişlemesi ile ventriküler taşikardi, ventriküler fibrilasyon ve Torsades de Pointes dahil kardiyak aritmilerle sonuçlanabilir. Klaritromisin pimozid ile birlikte kullanıldığında da benzer etkiler ortaya çıkabilir (bkz. Bölüm Kontrendikasyonlar).
Makrolidler, terfenadin ile uygulandıklarında, terfenadin seviyeleri yükselebilir ve terfenadin metabolizması etkilenebilir. Bu etkilenme sonucu kalp hastalarında QT aralığı genişlemesi, ventriküler taşikardi, ventriküler fibrilasyon ve Torsades de Pointes dahil kardiyak aritmiler gelişebilir (bkz. Bölüm Kontrendikasyonlar). On dört sağlıklı gönüllüde yapılan bir çalışmada klaritromisin tablet ve terfenadinin birlikte uygulanması, terfenadinin asit metabolitinin serum düzeyinde 2-3 kat artışlarla ve QT aralığında klinik açıdan saptanabilir bir etkiye yol açmayan uzamayla sonuçlanmıştır. Astemizol ve diğer makrolidlerin birlikte uygulanmasıyla benzer etkiler görülmüştür.
Ergotamin/dihidroergotamin: Pazarlama sonrası raporlarda, klaritromisinin ergotamin veya dihidroergotaminin eş zamanlı uygulanmasının, kol ve bacaklarda ve merkezi sinir sistemi dahil diğer dokularda vazospazm ve iskemiyle karakterize akut ergot toksisitesiyle ilişkili olduğuna işaret edilmektedir. Klaritromisin ve bu tıbbi ürünlerin eş zamanlı verilmesi kontrendikedir (bkz. Bölüm 4.3.Kontrendikasyonlar).
Etravirin: Klaritromisin maruziyeti etravirin ile azalmıştır; bununla birlikte aktif metabolit 14- OH-klaritromisin konsantrasyonu artmıştır. 14-OH-klaritromisin Mycobacterium avium
kompleksine (MAC) karşı etkinliği azalttığından, bu patojene karşı toplam aktivite değişebilir; bu nedenle MAC tedavisi için klaritromisinin alternatifleri düşünülmelidir.
Diğer ilaçların klaritromisin üzerindeki etkileri
CYP3A indükleyici ilaçlar: CYP3A (örn. rifampisin, fenitoin, karbamazepin, fenobarbital, St John Bitkisi) indükleyicisi ilaçlar klaritromisin metabolizmasını artırabilir. Bu durum etkinliğinin azalmasına yol açan subterapötik klaritromisin düzeylerine neden olabilir. Ayrıca, CYP3A indükleyicisinin plazma düzeyinin de izlenmesi gerekebilir; klaritromisinin CYP3A inhibisyonuna bağlı olarak bu ilacın düzeyi artabilir (bkz. kullanılan CYP3A4 indükleyicisi ürün bilgisi). Rifabutin ve klaritromisinin eşzamanlı kullanımında, rifabutin serum düzeyi artarken klaritromisin serum düzeyi azalarak üveit riski artışına yol açar.
Aşağıdaki ilaçlar dolaşımdaki klaritromisin konsantrasyonları üzerinde bilinen veya şüpheli etki gösterir; klaritromisin doz ayarlaması veya alternatif tedaviye geçiş gerekli olabilir.
Efavirenz, nevirapin, rifampisin, rifabutin ve rifapentin:Sitokrom P450 metabolizma sisteminin kuvvetli uyaranları, örneğin efavirenz, nevirapin, rifampisin, rifabutin ve rifapentin klaritromisinin metabolizmasını hızlandırabilir ve böylece mikrobiyolojik olarak aktif olan 14(R)-hidroksi-klaritromisini (14-OH-klaritromisin) arttırarak klaritromisinin plazma seviyelerini düşürür. Klaritromisin ve 14-OH-klaritromisinin mikrobiyolojik aktiviteleri farklı bakteriler için farklılık gösterir. Klaritromisin ile birlikte enzim uyaranlarının verilmesiyle amaçlanan terapötik aktivite bozulabilir.
Flukonazol: 21 sağlıklı gönüllüye flukonazol 200 mg/gün ile birlikte klaritromisin 500 mg/ günde 2 kez verilmiştir. Klaritromisinin ortalama sabit durum minimum konsantrasyonu (C) ve eğri altındaki alan (AUC) sırası ile %33 ve %18 olarak ölçülmüştür. Flukonazol ile eş zamanlı verilmesinden aktif metabolit 14-OH-klaritromisinin sabit durum konsantrasyonları anlamlı derecede etkilenmemiştir. Klaritromisin için doz ayarlaması yapılmasına gerek yoktur.
Ritonavir: 8 saatte bir 200 mg ritonavir ile 12 saatte bir 500 mg klaritromisinin birlikte uygulandığı bir çalışma, klaritromisin metabolizmasında belirgin bir inhibisyonla sonuçlanmıştır. Ritonavir ile birlikte uygulanmasıyla klaritromisin C%31, C%182 ve AUC %77 artmıştır. 14-[R]-hidroksiklaritromisin oluşumunun tamamen inhibe olduğu görülmüştür. Klaritromisinin geniş terapötik aralığı nedeniyle böbrek fonksiyonu normal olan hastalarda dozun azaltılmasına gerek yoktur. Bununla birlikte, böbrek bozukluğu olan hastalarda şu doz ayarı yapılmalıdır: CL< 30-60 ml/dak. olan hastalarda klaritromisin dozu
%50 azaltılmalıdır. CL< 30 ml/dak. olan hastalarda doz %75 azaltılmalıdır. Günde 1 g'dan daha yüksek klaritromisin dozları ritonavir ile uygulanmamalıdır.
Renal işlevleri azalmış hastalarda farmakolojik bir artırıcı olarak ritonavir, atazanavir ve sakinavir gibi diğer HIV proteaz inhibitörleri ile birlikte kullanıldığında benzer doz ayarlamaları düşünülmelidir (bkz. bölüm Çift-yönlü İlaç Etkileşimleri).
Klaritromisinin diğer ilaçlar üzerindeki etkileri Antiaritmikler:
Klaritromisinin kinidin veya disopiramid ile birlikte kullanımıyla oluşan Torsades de Pointes bildiren pazarlama sonrası raporları vardır. Hastaların, bu ilaçlar ile birlikte klaritromisin
verilmesi sırasında QTc uzaması açısından elektrokardiyografi ile izlenmesi gereklidir. Bu ilaçların serum düzeyleri klaritromisin tedavisi sırasında izlenmelidir.
CYP3A-kaynaklı etkileşimler
CYP3A'yı inhibe ettiği bilinen klaritromisin ile öncelikli olarak CYP3A tarafından metabolize edilen bir ilacın birlikte verilmesi, bu ilaçların konsantrasyonlarında hem terapötik ve hem de advers etkilerin artışına veya uzamasına yol açabilecek artışlara neden olabilir. CYP3A enzim substratları olarak bilinen, özellikle eğer CYP3A substratı dar güvenlik sınırına sahipse (örneğin karbamezapin) ve/veya substrat bu enzim tarafından geniş çaplı olarak metabolize ediliyorsa, diğer ilaç tedavileri alan hastalarda dikkatli kullanılmalıdır. Eğer mümkünse, CYP3A tarafından öncelikli olarak metabolize edilen ilaçların serum konsantrasyonları klaritromisin alan hastalarda yakından izlenmeli ve doz ayarlaması düşünülmelidir.
Aşağıdaki ilaçların veya ilaç sınıflarının aynı CYP3A izozimi tarafından metabolize edildiği bilinmekte veya bundan kuşkulanılmaktadır:
Alfentanil, bromokriptin, alprazolam, astemizol, karbamazepin, silostazol, sisaprid, siklosporin, disopiramid, ergot alkaloidleri, lovastatin, metilprednizolon, midazolam, omeprazol, oral antikoagülanlar (örneğin varfarin), pimozid, kinidin, rifabutin, sildenafil, simvastatin, sirolimus, takrolimus, terfenadin, triazolam, vinblastin, fenitoin, heksobarbital, teofilin ve valproat.
Teofilin, karbamazepin: Klinik çalışmalar, teofilin ve karbamazepinin klaritromisinle birlikte uygulanması sonucunda, kanda bu ilaçların seviyelerinde orta derecede ama istatistiki olarak anlamlı (P ≤ 0.05) bir artış olduğunu göstermiştir. Dozun azaltılması gerekebilir.
Omeprazol: Sağlıklı erişkin kişilere klaritromisin (500 mg/8 saatte bir) omeprazol (40 mg/ gün) ile kombine edilerek verilmiştir. Omeprazolün sabit durum plazma konsantrasyonları (C, AUCve tsırası ile %30, %89 ve %34) klaritromisinin eş zamanlı verilmesi ile yükselmiştir. Omeprazolün tek başına verildiği durumda ortalama 24 saatlik gastrik pH 5,2 olarak bulunurken klaritromisin ile eş zamanlı verilmesinde ise 5,7 olarak tespit edilmiştir.
Ranitidin bizmut sitrat: Klinik olarak önemsiz olmakla birlikte, ranitidin bizmut sitrat ile klaritromisinin birlikte uygulanması ranitidin, bizmut ve 14-hidroksiklaritromisinin plazma konsantrasyonlarının artışı ile sonuçlanmıştır.
Sildenafil, tadalafil ve vardenafil: Fosfodiesteraz inhibitörlerin herbiri, en azından kısmi olarak, CYP3A ile metabolize edilmektedir ve CYP3A klaritromisinin eş zamanlı verilmesi ile inhibe edilebilir. Klaritromisinin sildenafil, tadalafil veya vardenafil ile birlikte verilmesi artmış fosfodiesteraz inhibitör maruziyetine yol açabilir. Sildenafil, tadalafil ve vardenafil ile birlikte klaritromisin verildiği zaman bu ilaçların dozlarının azaltılması düşünülmelidir.
Tolterodin: Tolterodin'in öncelikli metabolizma yolu sitokrom P450'nin 2D6 izoformu (CYP2D6) aracılığı iledir. Fakat, CYP2D6'si bulunmayan bir alt grup topluluk için tespit edilmiş olan metabolizma yolu CYP3A aracılığı iledir. Bu topluluk alt grubunda CYP3A'nın inhibisyonu anlamlı derecede yüksek serum tolterodin konsantrasyonlarına yol açar. Tolterodin dozajındaki bir düşüş CYP3A inhibitörleri, örneğin CYP2D6'yı zayıf metabolize eden toplulukta klaritromisin kullanımı, varlığında gerekli olabilir.
Triazolobenzodiazepinler (örneğin, alprazolam, midazolam, triazolam):
Midazolam, klaritromisin tablet (500 mg/günde 2 kez) ile birlikte verildiğinde, midazolamın AUC değeri intravenöz uygulamadan sonra 2,7 kat ve oral verilmesinden sonra ise 7 kat artmıştır. Oral midazolam ile klaritromisinin eş zamanlı olarak verilmesinden kaçınılmalıdır. Eğer klaritromisin ile birlikte intravenöz midazolam veriliyorsa, hasta doz ayarlaması için yakından izlenmelidir. Aynı önlemler CYP3A tarafından metabolize edilen diğer benzodiazepinler için de uygulanmalıdır. Eliminasyon için CYP3A'ya bağımlı olmayan benzodiazepinler (temazepam, nitrazepam, lorazepam) için klaritromisin ile klinik olarak önemli etkileşim söz konusu değildir. Pazarlama sonrası klaritromisin ve triazolamın eş zamanlı kullanımında ilaç etkileşimleri ve merkezi sinir sistemi (MSS) etkileri (örneğin uykululuk hali ve konfüzyon) bildirilmiştir. Hastaların artmış MSS farmakolojik etkileri açısından izlenmeleri önerilmektedir.
Diğer ilaç etkileşimleri
Kolşisin: Kolşisin hem CYP3A'nın hem de dışarıya akış taşıyıcısı olan P-glikoprotein'in (Pgp) bir substratıdır. Klaritromisin ve diğer makrolidlerin CYP3A ve Pgp'yi inhibe ettikleri bilinmektedir. Klaritromisin ve kolşisin birlikte uygulandıklarında Pgp ve/veya CYP3A'nın klaritromisin tarafından inhibisyonu, kolşisine maruziyette artışa öncülük edebilir. Hastalar kolşisin toksisitesinin klinik semptomları yönüyle izlenmelidir (bkz. Bölüm Özel kullanım uyarıları ve önlemleri).
Digoksin: Digoksinin dışarı akış taşıyıcısı (efflux transporter) olan P-glikoprotein (Pgp) için bir substrat olduğu düşünülmektedir. Klaritromisinin Pgp'yi inhibe ettiği bilinmektedir. Klaritromisin ile digoksin birlikte verildikleri zaman Pgp'nin klaritromisin tarafından inhibe edilmesi digoksin maruziyetinde artışa yol açar. Klaritromisin ile eş zamanlı olarak digoksin alan hastalarda artmış serum digoksin konsantrasyonları pazarlama sonrası gözlem çalışmalarında bildirilmiştir. Bazı hastalarda potansiyel ölümcül aritmileri de kapsayan digoksin toksisitesi ile uyumlu klinik bulgular gözlenmiştir. Hastalar digoksin ve klaritromisini birlikte kullanırlarken serum digoksin konsantrasyonları dikkatli izlenmelidir.
Zidovudin: HIV-enfeksiyonlu yetişkinlere sürekli olarak oral klaritromisin ve zidovudin uygulanması, zidovudinin kararlı durum seviyelerinde düşüşe sebep olabilir. Klaritromisin eşzamanlı uygulanan oral zidovudin emilimini engellediğinden, bu etkileşim klaritromisin ve zidovudin dozlarının 4 saatlik aralarla kullanılması sonucu önlenebilir. Bu etkileşim, klaritromisin süspansiyon ile birlikte zidovudin veya dideoksinozin alan pediyatrik HIV-enfekte hastalarda gözlenmemiştir. Bu etkileşim klaritromisin, intravenöz infüzyon ile uygulandığında muhtemel değildir.
Fenitoin ve valproat: Klaritromisin dahil olmak üzere CYP3A inhibitörleri ile CYP3A ile metabolize olduğu düşünülmeyen ilaçlar (örn. fenitoin ve valproat) arasındaki etkileşime ilişkin spontan ya da yayınlanmış bildirimler mevcuttur. Bu ilaçlar klaritromisin ile eşzamanlı kullanıldığında serum düzeylerinin saptanması önerilir. Serum düzeylerinin artışı bildirilmiştir. Klaritromisinin, aşağıdaki ilaçlarla etkileşimine dair in-vivo insan verisi bulunmamaktadır; aprepitant, eletriptan, halofantrine ve ziprasidon. Fakat, in-vitro verilerin bu ilaçların CYP3A sübstratları olduğunu önermesi sebebiyle klaritromisinin bu ilaçlarla birlikte uygulanmasında dikkatli olunmalıdır. Eletriptan, klaritromisin gibi CYP3A inhibitörleri ile birlikte uygulanmamalıdır.
Klaritromisin dahil CYP3A inhibitörleri ile siklosporin, takrolimus, metilprednisolon, vinblastin ve silostazol etkileşimlerine dair spontane veya yayınlanmış raporlar olmuştur.
Çift-yönlü ilaç etkileşimleri
Atazanavir: Klaritromisin ve atazanavirin her ikisi de CYP3A'nın substrat ve inhibitörleridir ve çift yönlü ilaç etkileşimine yol açtığı yönünde kanıt mevcuttur. Klaritromisinin (500 mg/günde 2 kez) atazanavir (400 mg/günde 1 kez) ile birlikte verilmesi klaritromisine maruziyette 2 kat artışa ve 14-OH-klaritromisin maruziyetinde %70 azalmaya ve atazanavirin AUC değerinde %28 artışa yol açar. Klaritromisinin geniş terapötik penceresi nedeni ile böbrek fonksiyonları normal olan hastalarda doz düşürülmesi gerekmez. Orta dereceli böbrek fonksiyonu olan hastalarda (kreatinin klerensi 30-60 mL/dak), klaritromisin dozu %50 azaltılmalıdır. Kreatinin klerensi <30 mL/dak olan hastalarda uygun klaritromisin formülasyonu kullanılarak klaritromisin dozu %75 azaltılmalıdır. 1000 mg'dan yüksek günlük dozlarda klaritromisin proteaz inhibitörleri ile birlikte verilmemelidir.
İtrakonazol: Klaritromisin ve itrakonazolün her ikisi de CYP3A'nın substrat ve inhibitörleridir ve çift yönlü ilaç etkileşimine yol açar. Klaritromisin itrakonazolün plazma seviyelerini yükseltebilirken itrakonazol klaritromisinin plazma seviyelerini yükseltebilir.
İtrakonazol ve klaritromisini eş zamanlı olarak alan hastalar artmış veya uzamış farmakolojik etki belirtileri açısından yakından izlenmelidir.
Sakuinavir: Klaritromisin ve sakuinavirin her ikisi de CYP3A'nın substrat ve inhibitörleridir ve çift yönlü ilaç etkileşimine yol açtıkları yönünde delil vardır.
Klaritromisin (500 mg/günde 2 kez) ve sakuinavir (yumuşak jel kapsüller, 1200 mg/günde 3 kez) eş zamanlı olarak 12 sağlıklı gönüllüye verilmiştir. Sakuinavirin ortalama sabit durum eğri altındaki alan (AUC) ve minimum konsantrasyonu (C) tek başına sakuinavir alımına göre
%177 ve % 187 olarak saptanmıştır. Klaritromisin AUC ve Cdeğerleri tek başına klaritromisin alımına göre yaklaşık %40 daha yüksek olarak bulunmuştur. Her iki ilacın çalışılmış olan dozlarda/formülasyonlarda sınırlı bir zaman için eş zamanlı olarak verilmesi halinde doz ayarlamasına gerek yoktur. Yumuşak jelatin kapsül formülasyonu kullanımında ilaç etkileşim çalışmalarının gözlemleri sakuinavir sert jelatin kapsül kullanımındaki etkileri temsil etmeyebilir. Tek başına sakuinavir tedavisi ilaç etkileşim çalışmalarındaki gözlemler sakuinavir/ritonavir tedavisindeki etkileri temsil etmeyebilir. Sakuinavir ritonavir ile birlikte eş zamanlı olarak verildiğinde, ritonavirin klaritromisin üzerindeki potansiyel etkileri düşünülmelidir (bkz. Önlemler, İlaç Etkileşimleri).
Didanosin: Klaritromisin, didanosin ile eş zamanlı olarak HIV ile enfekte yetişkinlere uygulandığında didanosinin farmakokinetiğinde istatistiksel olarak önemli bir değişiklik olmadığı kaydedilmiştir.
Verapamil:
Eşzamanlı olarak klaritromisin ve verapamil alan hastalarda hipotansiyon, bradiaritmi ve laktik asidoz gözlemlenmiştir.
4.6. Gebelik ve laktasyon
:Gebelik kategorisi C.
Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon):
Herhangi bir veri bulunmamaktadır.
Gebelik dönemi:
Klaritromisinin gebe kadınlarda kullanımına ilişkin yeterli veri mevcut olmadığından gebelik sırasında kullanımının güvenliliği saptanmamıştır. Bu nedenle, MACROL Oral Süspansiyonun dikkatli biçimde yarar risk değerlendirmesi yapılmadan kullanılması önerilmez.
Laktasyon dönemi:
Klaritromisinin emzirilen bebeklerdeki güvenliliği saptanmamıştır. Klaritromisin anne sütüne geçer.
Üreme yeteneği/Fertilite:
Fertilite ve üreme çalışmalarında, 150-160 mg/kg/günlük dozlar erkek ve dişi sıçanların, estrus siklusunda, fertilitede, doğumda ve yavruların sayı ve yaşamasında hiçbir advers etkiye sebep olmamıştır (bkz. Bölüm 5.3. Klinik öncesi güvenlilik çalışmaları).
4.7. Araç ve makine kullanımı üzerindeki etkiler
Klaritromisinin araç ve makine kullanımı üzerine etkisi hakkında veri bulunmamaktadır. İlaç ile baş dönmesi, vertigo, konfüzyon ve dezoryantasyon ortaya çıkma potansiyeli hastaların araç ya da makine kullanması öncesinde dikkate alınmalıdır.
4.8. İstenmeyen etkiler
Klaritromisin tedavisinin yetişkinlerde ve pediatrik popülasyonda en sık ve yaygın görülen advers reaksiyonları karın ağrısı, diyare, bulantı, kusma ve tat değişiklikleridir. Bu advers reaksiyonlar genellikle hafif şiddette olup makrolid antibiyotiklerinin bilinen güvenirlik profili ile uyumludur.
Klinik çalışmalarda saptanan bu gastrointestinal advers reaksiyonların insidansı açısından önceden mikobakteriyel enfeksiyon olan ve olmayan hasta popülasyonları arasında anlamlı fark bulunmamıştır.
Klaritromisin ile en azından ilişkisi olası bulunan reaksiyonlar sistem organ sınıfına ve aşağıdaki sıklığa göre gösterilmiştir: çok yaygın (≥1/10), yaygın (≥ 1/100 ile < 1/10), yaygın olmayan (≥1/1,000 ile < 1/100) ve bilinmeyen (pazarlama sonrası deneyime ilişkin advers reaksiyonlar; mevcut veri ile sıklığı hesaplanamayan). Her bir sıklık grubunda advers reaksiyonlar şiddet değerlendirmesine göre azalan şiddete göre sunulmuştur.
Klaritromisin ile Bildirilen Advers Reaksiyonlar
Sistem Organ Sınıfı | Çok yaygın (≥1/10) | Yaygın (≥ 1/100 ile<1/10) | Yaygın olmayan (≥1/1,000 ile < 1/100) | Bilinmeyen (mevcut veri ile sıklığı hesaplanamayan)* |
Enfeksiyonlar ve Enfestasyonlar |
|
| Kandidiazis, enfeksiyon, vajinal enfeksiyon | Psödomembranöz kolit, erizipel, eritrazma |
Kan ve lenf sistemi hastalıkları |
|
| Lökopeni, trombositemi | Agranulositoz, trombositopeni |
Bağışıklık sistemi hastalıkları |
|
| Hipersensitivite | Anafilaktik reaksiyon |
Sistem Organ Sınıfı | Çok yaygın (≥1/10) | Yaygın (≥ 1/100 ile<1/10) | Yaygın olmayan (≥1/1,000 ile < 1/100) | Bilinmeyen (mevcut veri ile sıklığı hesaplanamayan)* |
Metabolizma ve beslenme hastalıkları |
|
| Anoreksi, iştah azalması | Hipoglisemi |
Psikiyatrik hastalıklar |
| İnsomni | Anksiyete, sinirlilik, çığlık atma | Psikotik bozukluk, konfüzyon durumu, depersonalizasyon, depresyon, dezoryantasyon, halüsinasyon, anormal rüyalar |
Sinir sistemi hastalıkları |
| Disguzi, baş ağrısı, tat değişikliği | Baş dönmesi, tremor | Konvülsiyon, agözi, parosmi, anosmi, parestezi |
Kulak ve iç kulak hastalıkları |
|
| Vertigo, duyma bozukluğu, tinnitus | Sağırlık |
Kardiyak hastalıklar |
|
| Elektrokardiyogra mda uzamış QT, palpitasyonlar | Torsade de pointes, ventriküler taşikardi |
Vasküler Hastalıklar |
|
|
| Hemoraji |
Gastrointestinal hastalıklar |
| Diyare, kusma, dispepsi, bulantı, karın ağrısı | Gastrit, stomatit, glossit, konstipasyon, ağız kuruluğu, erüktasyon, flatulans | Akut pankreatit, dilde renk değişikliği, dişte renk değişikliği |
Hepato-bilier Hastalıkları |
| Anormal karaciğer fonksiyon testleri | Alanin aminotransferaz artışı, aspartat aminotransferaz artışı | Hepatik yetmezlik, hepatosellüler sarılık |
Deri ve derialtı doku hastalıkları |
| Döküntü, hiperhidroz | Pruritus, ürtiker, makulopapular döküntü | Stevens-Johnson sendromu, toksik epidermal nekroliz, eozinofili ve sistemik semptomlu ilaç döküntüsü (DRESS), akne, Henoch- Schonlein purpurası |
Kas iskelet bozukluklar, bağ doku ve kemik hastalıkları |
|
| Kas spazmları | Miyopati |
Sistem Organ Sınıfı | Çok yaygın (≥1/10) | Yaygın (≥ 1/100 ile<1/10) | Yaygın olmayan (≥1/1,000 ile < 1/100) | Bilinmeyen (mevcut veri ile sıklığı hesaplanamayan)* |
Böbrek ve idrar hastalıkları |
|
|
| Renal yetmezlik, interstisyal nefrit |
Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklar |
|
| Pireksi, asteni |
|
Araştırmalar |
|
|
| Uluslararası normalleştirilmiş oranı artışı, protrombin zamanında uzama, anormal renkte idrar |
*Bilinmeyen bir büyüklükteki popülasyonda gönüllü olarak bildirilen bu reaksiyonların sıklıklarının ya da ilaç ile nedensel ilişkisinin saptanması her zaman mümkün olmamaktadır. Klaritromisin için hasta kullanımı en az 1 milyar hasta tedavi günü olarak hesaplanmıştır. | ||||
Klaritromisin ve kolşisin birlikte kullanıldığında, özellikle yaşlılarda olmak üzere ve bazıları böbrek yetmezliği olan hastalarda ortaya çıkan kolşisin toksisitesi bildirimleri vardır. Bu hastaların bazılarında ölümler bildirilmiştir (bkz. İlaç etkileşimleri ve Uyarılar/Önlemler).
Bağışıklık sistemi bozulmuş pediyatrik hastalar:
Mikobakteriyel enfeksiyonlar için uzun süre klaritromisinin yüksek dozları ile tedavi edilen AIDS hastaları veya bağışıklık sistemi bozuk diğer hastalarda, olasılıkla klaritromisin uygulamasıyla alakalı advers etkileri altta yatan HIV hastalığının veya seyir eden hastalığın belirtilerinden ayırt etmek genellikle zordur.
1000 mg ve 2000 mg klaritromisin toplam günlük dozu ile tedavi edilen yetişkin hastalar tarafından en sık bildirilen advers reaksiyonlar: bulantı, kusma, tat değişiklikleri, karın ağrısı, diyare, döküntü, gaz, baş ağrısı, konstipasyon, duyma bozukluğu, SGOT ve SGPT yükselmesidir. Daha düşük sıklıkta dispne, insomni ve ağız kuruluğu bildirilmiştir. İnsidans açısından 1000 mg ve 2000 mg tedavisi arasında fark saptanmazken, günlük 4000 mg klaritromisin tedavisinde insidans 3-4 kat artmıştır.
Bağışıklık sistemi bozulmuş bu hastalarda testin en yüksek ya da en düşük düzeyi dışına çıkan laboratuvar değerleri analiz edilmiştir. Bu analize göre günlük toplam 1000 mg ya da 2000 mg klaritromisin kullanan hastaların yaklaşık %2-3'ünde SGOT ve SGPT düzeyleri yüksek ve beyaz kan hücresi ile trombosit sayısı normalden düşük bulunmuştur. Bu iki tedavi grubunda daha az oranda kan üre nitrojeninde yükselme saptanmıştır. Günlük 4000 mg doz grubunda beyaz kan hücresi dışındaki tüm paramatrelerde insidans biraz daha yüksek olmuştur.
Laboratuar bulgularında değişiklikler
Klinik açıdan önemli olabilecek laboratuar bulgularındaki değişimler şunlardır:
Karaciğer: Yükselmiş SGPT (ALT) < %1, SGOT (AST) < %1, GGT < %1, alkalen fosfataz < %1, LDH < %1 ve total bilirubin < %1.
Hematoloji: Azalmış lökosit sayısı < %1 ve yüksek protrombin zamanı %1.
Böbrek: Yüksek BUN %4 ve yüksek serum kreatinini < %1
Şüpheli advers reaksiyonların raporlanması:
Ruhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesine olanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu Türkiye Farmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e- posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz aşımı ve tedavisi
Aşırı miktarlarda klaritromisin alımının, gastrointestinal (mide-barsak ile ilgili) semptomları vermesi beklenebilir. Bipolar bozukluk öyküsü olan bir hasta 8 g klaritromisin almış ve mental durumda değişmeler, paranoid davranışlar, hipokalemi ve hipoksemi görülmüştür. Aşırı doza eşlik eden advers reaksiyonlar, absorbe edilmemiş ilacın uygun eliminasyonu ve destekleyici tedavi ile kontrol altına alınmalıdır. Diğer makrolidlerle olduğu gibi, klaritromisin serum seviyeleri hemodiyaliz veya peritoneal diyalizden etkilenmez.
 Grip, Soğuk Algınlığı ve Öksürük
Grip ve soğuk algınlığı (nezle) semptomları arasındaki farkı bilmek önemlidir. Soğuk algınlığı gripten daha hafif belirtiler gösteren bir solunum yolu hastalığıdır.
Grip, Soğuk Algınlığı ve Öksürük
Grip ve soğuk algınlığı (nezle) semptomları arasındaki farkı bilmek önemlidir. Soğuk algınlığı gripten daha hafif belirtiler gösteren bir solunum yolu hastalığıdır. |
 Asperger Sendromu
Asperger sendromu, otistik gurubun bir bölümü olan bir özürdür. Bu genelde,
gurubun daha ”yüksek” tarafında yer aldığı düşünülen kişilere uygun bir tanıdır.
Asperger Sendromu
Asperger sendromu, otistik gurubun bir bölümü olan bir özürdür. Bu genelde,
gurubun daha ”yüksek” tarafında yer aldığı düşünülen kişilere uygun bir tanıdır. |
İLAÇ GENEL BİLGİLERİ
Sanovel İlaç Sanayi ve Ticaret A.Ş.
| Geri Ödeme Kodu | A04806 |
| Satış Fiyatı | 327.18 TL [ 1 Dec 2025 ] |
| Önceki Satış Fiyatı | 327.18 TL [ 24 Nov 2025 ] |
| Original / Jenerik | Jenerik İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8699536280073 |
| Etkin Madde | Klaritromisin |
| Yerli ve Beşeri bir ilaçdır. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| Eşdeğer bir ilaç bulunamadı |
 |
Doğum Sonrası Depresyonu Doğum sonrası depresyonu, doğumdan sonra her on kadından biri tarafından tecrübe edilen stresli bir durumdur. |
 |
Rahim Boyu ( Serviks ) Kanseri Rahim boynu (serviks) kanseri 35 yaş altı kadınlarda görülen vakalarda meme kanserinden sonra ikinci sırayı alır.Serviks kanserinin gelişmesi yıllarca sürebilir. |
 |
Depresyonu Anlamak Depresyon farklı kişileri farklı biçimlerde etkiler. Duygusal veya fiziksel olmak üzere geniş alanda belirtilere sebep olabilir.Depresyona neler sebep olur? |