MAXIFLU %0.25 oral sprey. ��zelti (30 ml. 1 �i�e) K�sa �r�n Bilgisi
{ Flurbiprofen }
1. BE�ER� TIBB� �R�N�N ADI
MAX�FLU %0.25 oral sprey, ��zelti
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
30 ml oral sprey, ��zelti 0.075 g flurbiprofen (%0.25) i�erir.
Yard�mc� maddeler
Metil paraben 0.027 g
Propil paraben 0.006 g
Yard�mc� maddeler i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Oral sprey, ��zelti Mavi renkli ��zelti.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Orofarenjiyal alana da ba�l� (�rn. di�eti iltihaplar�, a��z iltihaplar�, yutak iltihaplar�) a�r�larda rahats�zl��� giderici, antiinflamatuar olarak semptomatik tedavide kullan�l�r. Di� tedavileri sonras�nda da koruyucu olarak kullan�l�r.
4.2. Pozoloji ve uygulama �ekli
G�nde 3 defa ilgili b�lgeye do�rudan 3 p�sk�rtme yap�larak uygulan�r. Her bir p�sk�rtme
0.13 ml olup, 0.325 mg flurbiprofen i�erir.
Uygulama �ekli:
MAX�FLU oral sprey, ��zelti a��zda ilgili b�lgeye p�sk�rt�lerek uygulan�r, yutulmamal�d�r. Uygulama s�ras�nda a�a��daki y�nlendirmeleri takip ediniz:
Maxiflu % 0.25 Oral Sprey, ��zelti �i�esini �ekil 1'de oldu�u gibi dik konumda tutunuz.
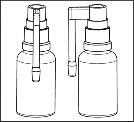
�ekil 1
4.3. Kontrendikasyonlar
Flurbiprofene veya �r�n�n form�l�nde bulunan yard�mc� maddelerden herhangi birine kar�� a��r� duyarl�l��� olanlarda,
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Haricen kullan�l�r.
MAX�FLU oral sprey, ��zelti a��zda ilgili b�lgeye p�sk�rt�lerek uygulan�r, yutulmamal�d�r. B�brek yetmezli�i, kalp yetmezli�i ya da karaci�er yetmezli�i olan hastalarda dikkatli kullan�lmal�d�r.
Metil paraben ve propil paraben i�erdi�inden alerjik reaksiyonlara (muhtemelen gecikmi�) sebebiyet verebilir.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Flurbiprofen, furosemidin di�retik faaliyetini nadiren azaltabilir. Ayr�ca, flurbiprofen nadiren antikoag�lan ila�larla etkile�ime girebilir. Bunun yan� s�ra flurbiprofenin digoksin, tolbutamid ve antiasit ile bir etkile�imi yoktur.
4.6. Gebelik ve laktasyon
Gebelik kategorisi C (3. trimesterde D)'dir.
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
�ocuk do�urma potansiyeli bulunan kad�nlarda flurbiprofen kullan�m�yla ilgili herhangi bir veri yoktur.
Gebelik d�nemi
Hayvanlar �zerinde yap�lan �al��malarda flurbiprofenin teratojenik etkisinin bulunmad��� g�sterilmi� olmas�na ra�men insanlar �zerindeki �al��malar�n yetersizli�inden dolay� flurbiprofen, hamilelerde olu�turaca�� yarar fet�s �zerinde yapabilece�i potansiyel zarardan fazla ise kullan�lmal�d�r.
Laktasyon d�nemi
Prostaglandin inhibit�r� ila�lar�n yeni do�anlar �zerindeki olas� yan etkileri nedeniyle flurbiprofenin laktasyonda kullan�lmas� tavsiye edilmez.
�reme yetene�i/Fertilite
�reme yetene�i �zerine bilinen bir etkisi yoktur.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
Flurbiprofenin araba ve makine kullanmaya etkisi konusunda �al���lmam��t�r, fakat farmakodinamik �zellikleri ve genel emniyet profiline dayan�larak bir etki olu�turmas� beklenmez.
4.8. �stenmeyen etkiler
�stenmeyen yan etkilerin s�n�fland�r�lmas�nda a�a��daki sistem kullan�lm��t�r:
�ok yayg�n (≥1/10), yayg�n (≥1/100 ila <1/10), yayg�n olmayan (≥1/1000 ila <1/100), seyrek (≥1/10000 ila <1/1000), �ok seyrek (<1/10000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar
Bilinmiyor:
Hassasiyet bulgular� Lokal irritasyonlar
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e-posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99)
4.9. Doz a��m� ve tedavisi
Etkin madde
Doz a��m�n�n semptomlar� mide bulant�s�, kusma, gastrointestinal rahats�zl�klar olabilir.
5. FARMAKOLOJ�K �ZELL�KLER
Genel �zellikler
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Bo�az preparatlar� ATC Kodu: R02AX01
MAX�FLU, antiinflamatuar, analjezik ve antipiretik etki g�steren nonsteroidal bir antienflamatuvar ila� olan flurbiprofen i�erir. Flurbiprofenin etki mekanizmas�, di�er nonsteriodal antiinflamatuar ila�larda oldu�u gibi tamamen anla��lamam�� olup, prostaglandin sentetaz inhibisyonuyla ilgili oldu�u d���n�lmektedir.
Di�er NSA� ila�larda oldu�u gibi; flurbiprofen, v�cut dokular�nda COX-1 ve COX-2 izoenzimleri dahil olmak �zere siklooksijenaz� (COX) inhibe ederek prostaglandin sentezini inhibe eder. Flurbiprofen, en g��l� prostaglandin inhibitor aktivite g�steren NSA� ila�lardan biridir.
5.2. Farmakokinetik �zellikler
Emilim
Flurbiprofen pasif dif�zyonal mekanizma yoluyla bukal olarak absorbe edilir. Bukal membran esas itibariyle bir lipid membrand�r ve flurbiprofen y�ksek lipid ��z�n�rl��� nedeniyle, bukal mukozadan kolayca ge�er. Flurbiprofen zay�f asittir ve bunun sonucu olarakta absorpsiyon oranlar� pH de�i�kenlidir.
Flurbiprofen, antiinflamatuar etkisinden dolay� periodontal hastal�klar�n tedavisinde ve �nlenmesinde kullan�l�r. Lokal olarak a�za uyguland���nda etkisi lokal olaca��ndan, y�ksek sistemik konsatrasyon gerekmemektedir. Bu endikasyon i�in bukal olarak zay�f absorpsiyon istenilir.
MAX�FLU oral sprey, ��zelti haricen kullan�lan lokal etkili bir ila�t�r. Bu nedenle tarife uygun kullan�m�nda yutulmamas� gerekir. MAX�FLU oral sprey, ��zelti kullan�m�nda anlaml� bir sistemik etki beklenmez. Bununla birlikte, flurbiprofenin oral yolla kullan�lan 50-100 mg'l�k tedavi dozlar�nda a�a��daki farmakokinetik �zellikler bulunur:
Da��l�m
Yakla��k 1,5-2 saat i�inde plazma doruk seviyelerine ula��r. Hem R- hem de S-flurbiprofenin g�r�nen da��l�m hacmi (Vz/F) yakla��k 0.12 L/Kg'd�r. Her iki flurbiprofen enantiomeri de
%99'un �zerinde bir oranla albumin ba�ta olmak �zere plazma proteinlerine ba�lan�r. Plazma proteinlerine ba�lanma, tavsiye edilen dozlarla elde edilen tipik ortalama kararl� durum konsantrasyonlar�nda (≤10 µg/ml) nispeten sabittir.
Biyotransformasyon
�nsan plazmas� ve idrar�nda �ok say�da flurbiprofen metaboliti saptanm��t�r. Bu metabolitler aras�nda, flurbiprofen'in 2 �nemli metaboliti [(2-(2-floro-4-hidroksi-4- bifenil)] ve [(2-(2- floro-3-hidroksi-4-metoksi-4-bifenil, ayr�ca 4'-hidroksi-flurbiprofen, 3',4'-dihidroksi- flurbiprofen, 3'-hidroksi-4'-metoksi- flurbiprofen, bunlar�n konjugatlar� ve konjuge flurbiprofen yer almaktad�r. Di�er arilpropiyonik asit t�revlerinin (�rne�in, ibuprofen) aksine, R-flurbiprofenin S-flurbiprofene metabolize olmas� minimal d�zeyde ger�ekle�mektedir. Yap�lan in vitro �al��malar, sitokrom P450 2C9'un flurbiprofenin ana metaboliti olan 4'- hidroksi-flurbiprofen'in metabolizmas�nda �nemli bir rol oynad���n� g�stermi�tir. 4'-hidroksi- flurbiprofen metaboliti, hayvan enflamasyon modellerinde �ok az antienflamatuvar aktivite g�stermi�tir. Flurbiprofen, metabolizmas�n� de�i�tiren enzimleri ind�klememektedir. Ba�lanmam�� durumdaki flurbiprofenin toplam plazma klirensi stereoselektif olmay�p, terap�tik aral�kta kullan�ld���nda flurbiprofenin klirensi dozdan ba��ms�zd�r.
Eliminasyon
Eliminasyon yar�lanma �mr� 3 ila 4 saat aras�nda de�i�ir.
�lac�n kullan�m� sonras�nda flurbiprofenin %3'ten az� de�i�meden idrarla at�l�r ve idrarda elimine olan dozun yakla��k %70'ini ana ila� ve metabolitleri olu�turur. %20'si serbest ve konjuge formda, yakla��k %50'si ise hidroksilenmi� metabolitleri halinde idrarla v�cuttan at�l�r. Renal eliminasyon flurbiprofen metabolitlerinin �nemli bir eliminasyon yolu oldu�u i�in, orta veya �iddetli b�brek yetmezli�i bulunan hastalarda, flurbiprofen metabolitlerinin birikimini �nlemek amac�yla doz ayarlamas� yapmak gerekebilir. R- ve S-flurbiprofenin ortalama terminal yar� �m�rleri (t½) s�ras�yla 4.7 ve 5.7 saat olup, birbirleriyle benzerdir. �oklu doz uygulamas� sonras�nda flurbiprofen birikimi �ok az olmu�tur.
Do�rusall�k / Do�rusal olmayan durum
Flurbiprofen'in farmakokineti�i do�rusald�r. Plazma d�zeyleri verilen doza ba�l� olarak art�� g�sterir.
5.3. Klinik �ncesi g�venlilik verileri
5.3. Klinik �ncesi g�venlilik verileri
insanlardaki yan�t� yans�tmayabilir. Gebe kad�nlarda ger�ekle�tirilmi� yeterli ve iyi kontroll� �al��malar mevcut de�ildir.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Sorbitol Sakkarin sodyum Gliserin
Polioksil 40 hidrojene hint ya�� Metil paraben
Propil paraben Etil alkol (%96)
Patent blue E131 (mavi) Mentol
Sodyum hidroksit Saf su
6.2. Ge�imsizlikler
Bug�ne kadar belirlenmi� herhangi bir ge�imsizli�i bulunmamaktad�r.
6.3. Raf �mr�
24 ay
6.4. Saklamaya y�nelik �zel tedbirler
25°C'nin alt�ndaki oda s�cakl���nda saklay�n�z.
6.5. Ambalaj�n niteli�i ve i�eri�i
P�sk�rtme ba�l�kl� dozaj pompal�, krimp kapamal�, 30 ml amber renkli cam flakon ve karton kutu ambalaj.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj ve Ambalaj At�klar�n�n Kontrol� Y�netmelik”lerine uygun olarak imha edilmelidir.
 Travma Sonras� Bunal�m�
Travmatik bir olay, g�nl�k ola�an olaylar�n d���nda olan ve ki�iyi derinden
rahats�z eden bir olayd�r.Bir�ok olay b�yle bir etki g�sterebilir.
Travma Sonras� Bunal�m�
Travmatik bir olay, g�nl�k ola�an olaylar�n d���nda olan ve ki�iyi derinden
rahats�z eden bir olayd�r.Bir�ok olay b�yle bir etki g�sterebilir. |
 Parkinson Hastal���
Hastal�k ilk kez 1817 de �ngiliz doktor James Parkinson taraf�ndan tan�mlanm�� ve Dr. Parkinson hastal��� “sallay�c� fel�” olarak kaleme alm��.
Parkinson Hastal���
Hastal�k ilk kez 1817 de �ngiliz doktor James Parkinson taraf�ndan tan�mlanm�� ve Dr. Parkinson hastal��� “sallay�c� fel�” olarak kaleme alm��. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| ANSAID | 8699532098597 | |
| ANSA�D | 8699532098078 | |
| FIERA | 8698747090150 | |
| FLUBI | 8699578171018 | |
| FLUBIMAK | 8680265090101 | |
| Di�er E�de�er �la�lar |
 |
HIV ve Aids HIV, Human Immunodeficiency Virus’d�r (�nsanlarda Ba����kl�k Sistemini Bozan Vir�sd�r). Bu vir�s AIDS hastal���na sebep olur. |
 |
Grip, So�uk Alg�nl��� ve �ks�r�k Grip ve so�uk alg�nl��� (nezle) semptomlar� aras�ndaki fark� bilmek �nemlidir. So�uk alg�nl��� gripten daha hafif belirtiler g�steren bir solunum yolu hastal���d�r. |
 |
Omurilik zedelenmeleri Omurilik zedelenmesini takip eden birka� g�n i�inde, hi�kimse hasarin ne kadar olacagini tahmin edemez. Buradaki sorun, omuriligin herhangi bir zedelenmesinden hemen sonra, bir omurilik sokunun olusmasidir. |
�LA� GENEL B�LG�LER�
Genveon �la� San. ve Tic. A.�.
| Geri �deme Kodu | A17519 |
| Sat�� Fiyat� | 171.19 TL [ 1 Dec 2025 ] |
| �nceki Sat�� Fiyat� | 171.19 TL [ 24 Nov 2025 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699293512776 |
| Etkin Madde | Flurbiprofen |
| Yerli ve Be�eri bir ila�d�r. |