MITOMYCIN-C KYOWA 20 mg 1 flakon Kısa Ürün Bilgisi
{ Mitomisin C }
1. BEŞERİ TIBBİ ÜRÜNÜN ADI
MİTOMYCİN-C Kyowa 20 mg Enjektabl Flakon Steril-apiroj en2. KALİTATİF VE KANTİTATİF BİLEŞİM
Etkin madde:
20 mg Mitomisin-C içerir.
Sodyum Klorür 480 mg
Yardımcı maddeler için 6.1.’e bakınız.
Yardımcı maddeler için 6.1.’e bakınız.
3. FARMASÖTİK FORMU
Kullanılmadan önce sulandırılan enjeksiyonluk çözelti Lastik tıpalı cam flakonda, mavi-mor toz
4. KLİNİK ÖZELLİKLER
4.1. Terapötik Endikasyonlar
Mesane kanserinde sistemik ve mesane içi uygulamalarda, meme kanseri, baş-boyun yassı hücreli kanserleri, mide ve pankreas kanserleri, prostat kanseri, serviks uterinin yassı hücreli kanseri.
4.2. Pozoloji ve Uygulama Şekli Pozoloji / uygulama sıklığı ve süresi:
İntravenöz uygulama
İntravenöz uygulama mümkün olduğunca yavaş ve ekstravazasyonu önlemek için çok dikkatli olarak yapılmalıdır.
Mutad doz aralığı 4-10 mg (0.06- 0.15 mg/kg) olup diğer ilaçlarla kombinasyon şeklinde ya da kemik iliği yenilenmesine bağlı olarak 1-6 haftalık intervalle uygulanır.
Kombinasyon tedavisinde genel doz şeması 10 mg /m vücut yüzey alanı şeklindedir ve doz ihtiyaç duyulduğunda tekrarlanır. Tek başına ya da kombinasyon tedavisinde dozun 40-80 mg (0.58- 1.2 mg/kg) olarak uygulanmasıyla yeterli cevap sağlanmıştır. Daha yüksek doz rejimi 2 mg/ kg olarak toplam kümülatif doz şeklinde tek başına ya da kombinasyon olarak da uygulanabilir.
Intraarteriyel uygulama
Spesifik dokular içine uygulamada, MİTOMYCİN-C intraarteriyel yolla doğrudan tümör içine verilebilir.
Doz azaltılması
Kümülatif miyelosüpresyondan dolayı hastalar her bir uygulamadan sonra gözetim altında tutulmalı ve toksik etkilerin ortaya çıkması durumunda doz azaltılmasına gidilmelidir. 0.6 mg/kg’dan yüksek dozların, miyelosüpresyona yol açma açısından düşük dozlardan daha etkili ve daha toksik olmadığı görülmüştür.
Hastalığın ilerlemesi
İki tedavi rejimi arasında hastalığın ilerlemesi durumunda, minimum cevap elde edilinceye kadar ilaç durdurulmalıdır.
Mesane tümörlü hastalarda kullanım
Yüzeyel mesane tümörünün tedavisinde mutad doz 20-40 mg (20-40 mİ çözelti şeklinde)’dır ve haftada bir ya da 3 haftada bir üretral kateter yardımıyla mesane içine instilasyon yoluyla uygulanır. Çözelti mesanede minimum 1 saat tutulmalıdır. İlacın tutulduğu süre boyunca hastanın konumu her 15 dakikada bir değiştirilerek MİTOMYCİN-C’nin tüm mesane epiteline temas etmesi sağlanmalıdır.
Mesanenin boşaltılması esnasında, kasık ya da genital bölgeden kaynaklanabilecek kontaminasyon açısından gerekli önlemler alınmalıdır.
Yüzeyel mesane tümörünün tekrarlanmasının önlenmesi amacıyla çeşitli dozlar uygulanabilir. Bu dozlar 20 mg (20 mİ çözelti şeklinde) her 2 haftada bir ve 40 mg (40 mİ çözelti şeklinde) ayda bir ya da 3 ayda bir şeklinde bir üreter kateter yardımıyla mesaneye instilasyon şeklindedir.
Tüm vakalarda doz, hastanm yaşı ve durumuna uygun şeklide ayarlanmalıdır.
Uygulama şekli:
İntravenöz olarak uygulanır. Gerektiği takdirde, intraarteriyel veya intravezikal yolla erişkinlerde uygulanabilir.
Özel popülasyonlara ilişkin ek veriler:
Böbrek/Karaciğer yetmezliği:
Advers reaksiyonlar artabileceğinden doz azaltılmalı veya uygun önlemler alınmalıdır. Peritonal diyaliz altındaki hastalarda gerekli dozun % 75’i uygulanmalıdır.
Pediyatrik popülasyon:
Prematüre bebeklerde, yeni doğanlarda, bebeklerde ve çocuklarda MİTOMYCİN-C’nin güvenliği kanıtlanmamıştır.
Geriyatrik popülasyon:
4.3. Kontrendikasyonlar
MİTOMYCİN-C’ye karşı geçmişlerinde aşırı duyarlılık bulunan hastalarda, platelet sayısının
3 3
4.4. Özel kullanım uyarıları ve önlemleri
MİTOMYCİN-C aşağıdaki hastalara çok dikkatli şekilde uygulanmalıdır:
• Karaciğer ya da böbrek bozukluklan olan hastalar (advers reaksiyonlar artabilir)
• Kemik iliği depresyonu bulunan hastalar (bu ürünün uygulaması kemik iliği depresyonunu şiddetlendirebilir)
• Enfeksiyon hastalıklan bulunan hastalar (bu ürünün uygulaması kemik iliği depresyonu sebebiyle enfeksiyonu ağırlaştırabilir)
• Varicella’lı hastalar (ölümcül sistemik bozukluklar meydana gelebilir)
MİTOMYCİN-C sitotoksik kanser kemoterapi sinde deneyimli bir hekim gözetiminde uygulanmalıdır.
Doku ekstravazasyonuyla lokal ülserasyon ve selülitis ortaya çıkabileceğinden intravenöz enjeksiyon ve uygulama süresince azami dikkat gösterilmelidir. Ekstravasazyon ortaya çıkması durumunda etkilenen bölgeye derhal % 8.4’lük sodyum bikarbonat çözeltisinin uygulanması ve ardından 4 mg deksametazon enjeksiyonu önerilmektedir. Sistemik olarak uygulanacak 200 mg Vitamin B6 enjeksiyonunun, meydana gelen tahribata karşı dokulann yenilenmesini desteklediği belirtilmiştir.
Hastalar, sık laboratuvar kontrolleriyle (hematolojik test, karaciğer fonksiyon testi ve böbrek fonksiyon testi vb. gibi) dikkatlice izlenmelidirler çünkü kemik iliği depresyonu gibi ciddi yan etkiler meydana gelebilir. Herhangi bir bozukluk görüldüğü takdirde, dozu azaltmak veya uygulamayı ertelemek gibi yeterli düzeyde önlemler alınmalıdır. Ek olarak, uzun süreli uygulama, yan etkilerin artmasına neden olabileceğinden dolayı büyük bir dikkat ile yapılmalıdır.
3 3
Lökosit sayısı 4000/mm , platelet sayısı 150000/ mm veya altında ise veya bu değerlerde progresif bir düşme gözlendiyse hematolojik düzelme oluşuncaya kadar ilaç kesilmelidir. Pulmoner toksisite geliştiyse ilaç kesilmelidir.
Enfeksiyon ve kanama eğiliminin belirginleşmesi veya ağırlaşması olasılığına karşı özel önlemler gerekir.
Sistemik MİTOMYCİN-C uygulanan hastalarda, öncelikle mikroanjiopatik hemolitik anemi, trombositopeni ve geri dönüşümsüz böbrek yetmezliğiyle ortaya çıkan ciddi komplikasyonlar gösteren ölümcül olabilen Hemolitik Üremik Sendrom (HUS) rapor edilmiştir. HUS, sistemik tedavinin herhangi bir zamanında, MİTOMYCİN-C’nin tek ajan ya da diğer ilaçlarla kombine şekilde kullanımıyla görülmesine rağmen, vakaların birçoğunda 60 mg’ın üzerindeki MİTOMYCİN-C dozlannın uygulanmasıyla ortaya çıkabilmektedir. Kan ürünü preparatlarının transfüzyonuyla bu semptomların şiddetlenebileceği ilişkilendirilmektedir. Sendromun insidansı belirtilmemiştir.
MİTOMYCİN-C ve diğer antikanser ajanlarını kombine kullanan hastalar akut lösemi veya myelodispastik sendrom (MDS) oluşma ihtimaline karşı uyarılmalıdır.
MİTOMYCİN-C’nin uygulanması sırasında yan etkilerin özellikle başlangıcına dikkat edilmeli ve enjeksiyon uygulaması çok dikkatli yapılmalıdır.
Yapılan hayvan çalışmalarında, subkutan uygulandığı farelerde ve intraperitonal ya da intravenöz uygulandığı sıçanlarda çeşitli tümör oluşumu rapor edilmiştir.
İntravenöz uygulama vasküler ağrı, flebit, tromboz, enjeksiyon yerinde sertleşme ve nekroza neden olabileceğinden MİTOMYCİN-C olabildiğince yavaş enjekte edilmeli, uygulama yeri ve yöntemine büyük dikkat gösterilmelidir.
İlacm damar dışına çıkması enjeksiyon yerinde ülserasyon, selülitis, sertleşme veya nekroza yol açabileceğinden ilacın damar dışına çıkmasından kaçınmak için ilaç, dikkatli bir şekilde enjekte edilmelidir.
İntraarteriyal uygulama, deri/kas nekroz öncülüğü olan bölgeyi içeren yerde ülser, sertleşme, ağrı, kırmızılık, eritem, kabarcık ve erozyon gibi deri bozukluklarına sebep olabilir. Semptomlardan herhangi biri geliştiğinde uygulama durdurulmalı ve uygun önlemler alınmalıdır. Özellikle parankimatöz karaciğer bozukluklan, bilioma, kolanjit (hatta sklerozan) ve safra kanalı nekrozlan ilacın hepatik arteriyal uygulanmasından sonra meydana gelebilir.
Hepatik artere uygulamada ilacın hedeflenen alandan diğer alanlara akmasından dolayı gastroduodenal ülser, hemoraji, perforasyon meydana gelebilir, kateter sonunun konumu ve ilacın dağıldığı bölge fotoğrafla ya da diğer ölçümlerle konfırme edilmeli, olası sapmaya veya kateterin değiştirilmesi ve infüzyon oranına dikkat edilmelidir. Semptomlardan herhangi biri geliştiğinde uygulama durdurulmalı ve uygun önlemler alınmalıdır.
Pazarlama sonrası verilerden intravezikal uygulama sonrasında mesane fıbrozu/kasılması, bazı seyrek vakalarda ise sistektomiye gerek duyulduğu rapor edilmiştir. Mesane nekrozu ya da penil nekroz da rapor edilmiştir (Bkz. bölüm 4.8 Advers Etkiler).
Hastalar, intravezikal uygulama sonrasındaki ürinasyonun ardından kontakt dermatitin engellenmesi açısından ellerin ve genital bölgenin yıkanması konusunda uyarılmalıdır.
Bu tıbbi ürün her bir flakonunda 240 mg sodyum klorür ihtiva eder. Bu durum kontrollü sodyum diyetinde olan hastalar için göz önünde bulundurulmalıdır.
4.5. Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim şekilleri
MİTOMYCİN-C enjeksiyonu aşağıda belirtilen ilaçlarla birlikte kullanıldığında dikkatli olunmalıdır.
ilaçlar | Belirti, semptom ve tedavi | Mekanizma ve risk faktörleri |
Diğer antineoplastik ajanlar Işınlama | Kemik iliği depresyonu gibi advers reaksiyonlar artabilir | Her bir ilacın advers reaksiyonlan artabilir. |
Vinka alkoloidleri Antikanser ajanlar Vindesin sülfat vb. | Nefes darlığı ve bronkospazm meydana gelebilir | Etki mekanizması bilinmiyor |
MİTOMYCİN-C tedavisi süresince ve tedaviden sonra en az 6 ay boyunca canlı aşılar (OPV, MMR, BCG, oral tifo, sarı humma, varicella) ile immünizasyon yapılmamalıdır.
Özel popülasyonlara ilişkin ek bilgiler:
4.6. Gebelik ve laktasyon
Genel tavsiye
Gebelik Kategorisi D’dir.
Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)
Gebe olduğundan şüphelenilen kadınlara uygulanması önerilmemektedir.
Gebelik dönemi
Mitomisin-C enjeksiyonu gebe hastalara uygulanması önerilmemektedir. Farelerle yapılan hayvan çalışmaları, bu ilacın gelişimle ilgili inhibisyon, yarık damak, kuyruğun tam gelişmemesi, çenelerin tam gelişmemesi, bir ya da birkaç parmağın doğuştan olmayışı (ektrodaktili) v.b. gibi bu ilacın teratojenitesini göstermiştir.
Laktasyon dönemi
Emziren anneler, tedavi süresince emzirmeyi durdurmalıdırlar MİTOMYCİN-C süte geçer ve emziren annelerde kullanımı kontrendikedir.
Üreme yeteneği/ Fertilite
Üreme yeteneğine sahip yaşlardaki hastalara bu ilacın uygulanması gerektiğinde ilacm üreme organları üzerindeki potansiyel etkisi göz önünde bulundurulmalıdır.
4.7. Araç ve makine kullanımına etkisi
4.8. İstenmeyen etkiler
Rapor edilen istenmeyen etkiler aşağıdaki sıklık derecesine göre listelenmiştir.
Çok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan (>1/1.000 ila <1/100); seyrek (>1/10.000 ila <1/1.000); çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Sistemik uygulama ile görülen advers etkiler
Enfeksiyon ve infestasyonlar
Bilinmiyor: Bakteriyel enfeksiyon, viral veya mantar enfeksiyonu, sepsis ve septik şok
Kan ve lenf sistemi hastalıkları
Çok yaygın: Lökopeni, trombositopeni, anemi, kanama eğilimi,
Yaygm: Pansitopeni, granülositopeni, febril nötropeni, eritropeni, trombotik trombositopenik purpura, miyelodisplastik sendrom, akut myeloid lösemi ve akut lösemi Seyrek: Hemolitik Üremik Sendrom (HUS)
Bağışıklık sistemi hastalıkları
Bilinmiyor: Hipersensitivite, anaflaktik reaksiyonlar, anaflaktik şok (Eozinofil sayısının artması, terleme, kan basıncının düşmesi, dispne)
Metabolizma ve beslenme hastalıkları
Çok yaygın: Kilo kaybı Yaygm: Anoreksiya
Sinir sistemi hastalıkları:
Yaygm: Konfüzyon
Göz hastalıkları
Yaygm: Bulanık görme
Kardiyak hastalıkları
Seyrek: Kardiyak bozukluk (özellikle bir önceki tedavisi antrasiklin ile yapılmış hastalarda) Bilinmiyor: Konjestif kalp yetmezliği (doz >30 mg/m üzerinde)
Vasküler hastalıkları
Yaygm: Tromboflebit Bilinmiyor: Flushing, hipertansiyon
Solunum, göğüs bozuklukları ve mediastinal hastalıkları
Yaygm olmayan: İnterstisyel pulmoner fıbrozis
Bilinmiyor: Solunum bozukluklan, bronkospazm, pnömoni ve öksürük
Gastrointestinal hastalıkları
Çok yaygın: Bulantı/kusma, iştahsızlık
Yaygm: Stomatit, diyare, konstipasyon, kann ağnsı
Hepatobiliyer hastalıklar
Bilinmiyor: Parankimatöz karaciğer bozukluğu, kolesistit, sarılık, safra kesesi iltihabı, safra kanalı nekrozu
Deri ve deri altı doku hastalıkları
Yaygm: Deri ve mukus membranlarda reaksiyonlar; Eritem, ülserasyonlar, stomatit, alopesi.
Böbrek ve idrar hastalıkları
Yaygm: Ağırlıklı olarak glomerüler tipte böbrek hasarı, serum kreatinin seviyelerinde yükselme
Bilinmiyor: Akut renal yetmezlik, renal bozukluk, albuminüri, ödem, sistit, hematüri, proteinüri, mesane atrofısi
Genel bozukluklar ve uygulama yeri hastalıkları
Çok yaygın: Halsizlik
Bilinmiyor: Yüksek ateş (ürperti), enjeksiyon yerinde iltihap, ülserasyon, selülitis, nekroz
İntravezikal uygulama
Deri ve deri altı doku hastalıkları
Yaygın: Ellerde ve genital bölgede dermatit ve prürit
Genito-üriner sistem bozukluklan
Yaygm: Genital bölgede ve üriner yolda iritasyon, disüri, sistit, noktüri, miksiyon sıklığında
4.9. Doz aşımı ve tedavisi
Doz aşımı, süresi uzamış kemik iliği fonksiyonlarının supresyonu gibi ciddi advers reaksiyonlarla sonuçlanabilir. Herhangi bir özel antidotun yokluğunda, B2, B6 ve C vitaminleri veya glutatyon’un büyük miktarlarda uygulanmasının, ilacın metabolik bozulmasının hızlanması ile ilacın deaktivasyonunda etkili olduğu bildirilmiştir.
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grubu: Antineoplastik ajanlar / diğer Sitotoksik antibiyotikler ATC Kodu: L01DC03
Mitomisin-C’nin alkilleyici ajan olarak, tümör hücrelerinde DNA’ya bağlandığı ve DNA çift sarmalının iki kolu arasında çapraz bağlar oluşturmak suretiyle DNA replikasyonunu önleyerek antitümöral etki gösterdiği sanılmaktadır. Faza özgü bir ajan olmasa da Mitomisin-C’ye duyarlılığın DNA’nın son Gı fazında, DNA sentezinin erken S fazı boyunca yüksek olduğu ispatlanmıştır.
5.2. Farmakokinetik özellikler
Genel özellikler
Emilim:
Mitomisin-C’nin kan seviyelerindeki değişiklikler, kanser hastalarında 2-30 mg’lik dozun bir defada intravenöz enjeksiyonundan sonra aşağıdaki gibidir:
ug/rrit
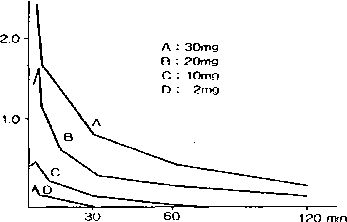
A,B,C,D= İntravenöz olarak uygulanan Mitomisin-C Dozu Farmakokinetik parametreler
^^^Parametre | Y arılanma | ömrü (dak) | AUCO~oo ((.ıg’inL.dak) |
Doz | TVıa | TVıfi | |
10 mg IV | 1.3 | 32.9 | 10.0 |
20 mg IV | 4.7 | 41.2 | 42.8 |
30 mg IV | 5.2 | 50.2 | 98.9 |
( Referans: US çalışma verisi)
^~’~’’-’-^J^araırı etre | n | CL | Vı | v2 |
Doz | (mL/dak/m2) | (L/m2) | (L/m2) | |
6 - 8 | 9 | 314.7 | 9.0 | 23.0 |
10 | 9 | 320.8 | 9.6 | 32.2 |
15-20 | 12 | 355.6 | 10.1 | 23.6 |
Dağılım:
Dokularda dağılım (farelerle yapılan deney verileri)
Mitomisin-C konsantrasyonu, kanserli sıçanlara 8 mg/kg Mitomisin-C intravenöz olarak uygulandıktan 5 dakika sonra en yüksek akciğer, takiben deri, böbrek, kas, kalp, ince bağırsak, dalak, tümör, mide ve sonra karaciğer bulunmuştur. Mitomisin-C, SSS’e büyük olasılıkla geçmemektedir.
Protein bağlama oranı (denge diyaliz ile)
Konsantrasyon (fj,g/mL) | 0.1 | 1.0 | 10.0 |
Bağlama oranı (%) | 12.8 | 9.4 | 8.4 |
Biyotransformasyon:
Mitomisin-C büyük ihtimalle karaciğerde sonradan aktive veya inaktive olan redüktant bir maddeye metabolize olur. (US in vitro çalışma verisi)
Eliminasyon:
İdrarda değişmemiş Mitomisin-C’ nin itrah oranı, kanser hastalarında 10-30 mg Mitomisin-C’nin bir defada enjekte edildikten sonraki 4 saat içinde dozun % 4,3-8,8’i olmuştur.
Doğrusallık/doğrusal olmayan durum:
Mevcut veri bulunmamaktadır.
5.3. Preklinik güvenlik bilgileri
Tek doz toksisite (LD 50 mg/kg):
Uygulama yolu Hayvan türleri ^ | I.V | i.p. | p.o. |
Fare (ICR türü farelerde) | 4.3 | 8.4 | 53.5 |
(ddy türü farelerde) | 8.2 | 8.4 | 26.8 |
Sıçan | 3.1 | 5.0 | 67.4 |
Tavşan | 3.4 | N/A | N/A |
Köpek | 0.72 | N/A | N/A |
Tekrar doz toksisitesi:
Sıçanlara, 6 ay için günlük 0,4; 1,2; 3,6; 11; 33 veya 100 |~ıg/kg’ lık doz intraperitonal olarak uygulandığında, 11 |LXg/kg ve daha yüksek doz grubundaki hayvanlarda kilo artışının önlendiği, 100 ng/kg grubunda ise istemli hareketlerde ve sklerotik gelişimde azalma ile 130 gün sonra ölümler kaydedilmiştir. Hematolojik ve biyokimyasal laboratuvar testlerinde (uygulamadan sonra 150. günde), erkekler ve 100 |_ıg/kg ‘lık dişi grubunda, WBC’de (lökosit sayısı) azalma eğilimi, K+yükselmesi, BUN ve NPN değerlerinde yükselme, 100 |Lxg/kg’lık erkek grubunda ise eritropeni, hematokrit miktannda azalma, hemoglobin konsantrasyonunda düşme, retikülositoz ve serum proteininde azalma ortaya çıkmıştır. Histopatolojik testlerde (uygulamadan sonra 150. günde), erkek ve dişilerde timus veya dalak atrofısi, erkeklerde testis, seminal vezikül ve prostat atrofısi ve 100 |_ıg/kg ‘lık dişi grubunda yumurtalık atrofısi olduğu ortaya çıkmıştır.
Teratojenite:
2.0-10.0 mg/kg tek intravenöz dozun, farelerde hamileliğin 10-14. günlerinde yaşayan fetusun büyümesini önemli ölçüde engellemiştir. 7.5 mg/kg doz grubunda, yarık damak, kuyruk kısalığı, çenenin normale oranla çok küçük oluşu ve oligodaktili ile teratojenite görülmüştür.
Karsinojenite:
Ürünün 0.2 |_ıg’ı, toplam olarak 35 defa haftada 2 kere farelere subkutan uygulandığında, uygulamanın 39-54. haftasında lokal olarak sarkom kaydedilmişir.
6. FARMASÖTİK ÖZELLİKLER
6.1. Yardımcı maddelerin listesi
6.2. Geçimsizlikler
Mitomisin-C potensi çözünme için düşük pH çözeltisi kullanıldığında azalabilir, çözündükten hemen sonra kullanılması tavsiye edilir. Ek olarak, düşük pH’lı enjeksiyonluk çözeltiler ile karıştırılmaktan kaçınılması önerilir. Mitomisin-C’ nin, düşük pH’lı Cefam antibiyotikleri, B1 vitamin ürünleri ve enjeksiyonluk cisplatin karışımı ile potensinin azaldığı bildirilmiştir. Bundan dolayı bu ürünlerle direkt karışımdan kaçınılmalıdır. Ayrıca, yüksek miktarlarda glukoz ya da laktoz içeren infüzyon solüsyonlarında Mitomisin-C stabil olmadığından, kullanım öncesinde, bu infüzyon solüsyonları ile birlikte hazırlanmasından kaçınılması tavsiye edilir.
6.3. Raf ömrü
6.4. Saklamaya yönelik özel tedbirler
25°C’de oda sıcaklığında ışıktan koruyarak saklayınız.
Dondurmayınız.
Orijinal ambalajında saklayınız.
Distile su ile rekonsititüe edilen MİTOMYCİN-C çözeltisi 5°C’de 24 saat (1 gün) stabildir. Rekonstitüe çözelti herhangi bir koruyucu içermediğinden mikrobiyolojik açıdan hazırlandıktan sonra mümkün olan en kısa sürede kullanılmalıdır. Eğer hemen kullanılmayacaksa buzdolabında (2-8°C’de) saklanmalı, 8 saat içinde kullanılmalıdır.
Oda sıcaklığında IV çözeltiler içindeki MİTOMYCİN-C stabilitesi:
% 5 Glukoz çözeltisi | Hemen kullanılmalıdır | ||||||||||||||||||||||||||||||||
% 0.9 Sodyum Klorür Çözeltisi | 8 saat içinde kullanılmalıdır. | ||||||||||||||||||||||||||||||||
Sodyum Laktat Çözeltisi | 6.5. Ambalajın niteliği ve içeriği6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerMİTOMYCİN-C sitotoksik kanser kemoterapi sinde deneyimli bir hekim gözetiminde uygulanmalıdır. Hazırlama Talimatları: İnfüzyonluk çözeltinin hazırlanması: MİTOMYCİN-C intravenöz uygulamadan önce steril distile su ile rekonstitiüe edilerek ön çözelti (konsantre çözelti) hazırlanmalıdır. Konsantre çözelti: MİTOMYCİN-C konsantre çözeltisi, steril enjeksiyonluk su kullanılarak 1 mg/2 mL (0,5 mg/1 mL) konsantrasyon oluşturacak şekilde hazırlanır. Bunun için; • 2 mg toz içeren flakona; 4 mİ steril enjeksiyonluk su, • 10 mg toz içeren flakona; 20 mİ steril enjeksiyonluk su, • 20 mg toz içeren flakona; 40 mİ steril enjeksiyonluk su eklenir. Çözünmesi için çalkalanır, çözünme hemen sağlanmazsa oda sıcaklığına gelene kadar bekletilebilir. İnfüzyonluk çözelti: Hesaplanan miktarda Mitomisin-C içeren konsantre çözelti 100 mL % 0,9 sodyum klorür çözeltisi içine enjekte edilir. İnfüzyonluk çözelti; % 5 glukoz çözeltisi ya da sodyum laktat çözeltisi kullanılarak da hazırlanabilir ancak bu çözeltiler intravezikal olarak uygulanmamalıdır. Uzun süreli uygulama için intravenöz infüzyonluk çözelti: • 500 mİ % 0,9’luk sodyum klorür çözeltisi, infüzyon için bir kanüle bağlanır ve infüzyon süresi 60 dakika olarak ayarlanır. MİTOMYCİN-C çözeltisi de bir kanül yardımıyla 30-40 dakika boyunca % 0,9’luk sodyum klorür çözeltisi ile eş zamanlı olarak uygulanır. • Arta kalan % 0,9’luk sodyum klorür çözeltisi (100-200 mL) 20 dakika boyunca verilir. İntravenöz uygulamada infüzyon boyunca enjektörün ven içinde olduğundan emin olunmalıdır. Ektravazasyon oluşması durumunda ciddi inflamatuvar reaksiyonlar meydana gelebilir. Böyle bir durumda intravenöz uygulamaya başka bir venden devam edilmelidir. İntravezikal uygulama çözeltisinin hazırlanması: Hesaplanan doz Mitomisin-C tozu, lmg/ml konsantrasyon oluşturacak şekilde steril enjeksiyonluk su ile çözülür. Bunun için; • 2 mg toz içeren flakona; 2 mİ steril enjeksiyonluk su, • 10 mg toz içeren flakona; 10 mİ steril enjeksiyonluk su, • 20 mg toz içeren flakona; 20 mİ steril enjeksiyonluk su eklenir. Rekonstitüe çözeltide çözünmeyen partiküller kalırsa, ılık su altmda 2 dakika boyunca şeffaf çözelti elde edilinceye kadar dikkatlice çalkalanmalıdır. Hazırlanan çözelti bir kateter yardımıyla mümkün olan en kısa sürede mesaneye uygulanmalıdır. MİTOMYCİN-C, cilt ile temas ettirilmemelidir. Temas halinde derhal bol miktarda sabunlu suyla yıkanmalıdır ve ardından etkilenen bölgeye % 8,4 sodyum bikarbonat çözeltisi uygulanmalıdır. Epidermal dokudan penetrasyonu arttırabileceğinden krem ya da nemlendirici kullanılmamalıdır. MİTOMYCİN-C’nin gözle teması halinde birkaç kez bol miktarda izotonik sodyum klorür (şalin) çözeltisi ile yıkanmalıdır. Komeal hasara karşı birkaç gün gözetim altmda tutulmalı, gerekirse medikal tedavi alınmalıdır. Kullanılmamış olan ürünler ya da atık materyaller "Tıbbi atıkların kontrolü yönetmeliği" ve "Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmelikleri” ne uygun olarak imha edilmelidir
İLAÇ EŞDEĞERLERİ
|
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| MITOMYCIN-C | 8699650271193 | |
| Diğer Eşdeğer İlaçlar |
 |
Belsoğukluğu, Chlamydia ve Frengi Belsoğukluğu, bakterilerin sebep olduğu bir enfeksiyondur. Cinsel ilişki yoluyla bulaşır ve dölyatağı boynunda, idrar yollarında, anüste, makatta ve boğazda enfeksyona sebep olabilir. |
 |
Kalp Krizi Kalbe giden kan akışı durduğunda kalp krizi meydana gelir. |
 |
Asperger Sendromu Asperger sendromu, otistik gurubun bir bölümü olan bir özürdür. Bu genelde, gurubun daha ”yüksek” tarafında yer aldığı düşünülen kişilere uygun bir tanıdır. |
İLAÇ GENEL BİLGİLERİ
Onko Koçsel İlaç San. Tic. A.ş
| Geri Ödeme Kodu | A09871 |
| Satış Fiyatı | 809.51 TL [ 1 Dec 2025 ] |
| Önceki Satış Fiyatı | 809.51 TL [ 24 Nov 2025 ] |
| Original / Jenerik | Jenerik İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8699650272046 |
| Etkin Madde | Mitomisin C |
| İthal ( ref. ülke : Ispanya ) ve Beşeri bir ilaçdır. |

