MULTIFLEX ERMOLOC PREMIKS 10 mg/ml I.V. infüzyon için 250 ml çözelti Kısa Ürün Bilgisi
{ Esmolol Hcl }
1. BEŞERİ TIBBİ ÜRÜNÜN ADI
Multiflex ERMOLOC Premiks 10 mg/mL I.V. infüzyon için çözelti Steril
2. KALİTATİF VE KANTİTATİF BİLEŞİM
Etkin madde
Esmolol hidroklorür: 10 mg/mL (Her bir 250 mL'lik torba 2500 mg esmolol hidroklorür içerir).
Yardımcı maddeler
Bu tıbbi ürün her bir torbasında yaklaşık 30.45 mmol (ya da 700 mg) sodyum içerir. Yardımcı maddeler için 6.1'e bakınız.
3. FARMASÖTİK FORMU
İnfüzyon için çözelti.
Berrak, renksiz ila açık sarı renkte çözelti.
Çözeltinin pH'sı 4.5 - 5.5 arası ve ozmolaritesi yaklaşık 300 mOsm/l'dir.
Beta blokörler sınıf reaksiyonu olarak bazı durumlarda psoriyazise ya da psoriyaziste kötüleşmeye neden olabilir.
Uygulama seti takılır; setle birlikte verilen talimata uyularak uygulamaya başlanır.
4. KLİNİK ÖZELLİKLER
4.1. Terapötik endikasyonlar
Supraventriküler taşikardi veya kompanse olmamış sinüs taşikardisi
ERMOLOC perioperatif, postoperatif ya da kısa sürede etkili bir preparatla ventrikül hızının hızlı kontrolünün istendiği diğer acil girişim gereken durumlarda ortaya çıkan atriyal fibrilasyon ya da atriyal flutter durumlarında endikedir.
ERMOLOC ayrıca hekim tarafından hızlanmış kalp hızının özel bir girişimle düzeltilmesi kararı verilmişse kompanse olmamış sinüs taşikardisi durumunda da endikedir.
ERMOLOC kısa süreli kullanıma yöneliktir.
İntraoperatif ve postoperatif taşikardi ve/veya hipertansiyon
ERMOLOC endotrakeal entübasyon, anestezi indüksiyonu, cerrahi prosedür devam ederken, anesteziden çıkarken ve postoperatif dönemde görülen taşikardi ve hipertansiyonda hekim tarafından böyle özel bir girişimle düzeltilmesi kararı verilmişse endikedir.
ERMOLOC'un, böyle durumların oluşmasını engellemek amacıyla kullanımı önerilmemektedir.
4.2. Pozoloji ve uygulama şekli
Pozoloji / uygulama sıklığı ve süresiSupraventriküler taşikardi veya kompanse olmamış sinüs taşikardisinin tedavisinde dozlama
ERMOLOC devamlı intravenöz infüzyonla yükleme dozu ile birlikte veya yükleme dozu olmaksızın uygulanır. İstenilen ventriküler yanıta göre ilave yükleme dozları ve/veya idame infüzyonun (basamaklı dozlama) titrasyonu gerekli olabilir.
Tablo 1-Basamaklı Dozlama
Adım | İşlem |
1 | Opsiyonel yükleme dozu (500 mcg/kg 1 dk içinde), sonra 4 dk süreyle 50 mcg/kg/dk |
2 | Gerekliyse opsiyonel yükleme dozu, 4 dk süreyle 100 mcg/kg/dk |
3 | Gerekliyse opsiyonel yükleme dozu, 4 dk süreyle 150 mcg/kg/dk |
4 | Gerekliyse, doz 200 mcg/kg/dk'ya çıkarılır |
Yükleme dozu uygulanmadığı durumlarda sabit konsantrasyonda uygulanan esmololün farmakokinetik ve farmakodinamik açıdan sabitlenmiş konsantrasyonlarına yaklaşık 30 dakikada ulaşılmaktadır.
Etkili idame dozu, devamlı ve basamaklı dozlama için 25 mikrogram/kg/dk kadar düşük dozların yeterli olmasına karşın 50 ila 200 mikrogram/kg/dk'dır. 200 mikrogram/kg/dk'dan yüksek dozlar, etkisini azaltarak kalp atış hızında küçük bir artışa sebep olmakta ve advers reaksiyonların oranını arttırmaktadır.
İdame infüzyon 48 saate kadar devam ettirilebilir.
İntraoperatif ve postoperatif taşikardi ve/veya hipertansiyon
Bu kullanımda terapötik etki için yavaşça titre edilmesi her zaman önerilmez. Bu yüzden iki dozlama seçeneği sunulmaktadır: Hemen kontrol ve basamaklı kontrol.
Hemen kontrol sağlamak için doz önerisi
Bolus doz olarak 30 saniye içerisinde 1 mg/kg ardından gerekliyse 150 mikrogram/kg/dk infüzyonla uygulanır.
4.3. Kontrendikasyonlar
Etkin madde
4.4. Özel kullanım uyarıları ve önlemleri
ERMOLOC tedavisi gören tüm hastalarda kan basıncı ve EKG'nin sürekli olarak izlenmesi önerilmektedir.
Hastada hemodinamik bozukluk bulunduğunda veya hasta aşağıda parametrelerin birini veya tümünü azaltan diğer ilaçları kullanıyorsa, supraventriküler aritmili hastalarda ventrikül yanıtının kontrolü için ERMOLOC kullanımı sırasında dikkatli olunmalıdır: periferik direnç, miyokardiyal dolum, miyokardiyal kontraktilite veya miyokardiyumda elektriksel impuls propagasyonu. ERMOLOC etkilerinin hızlı başlaması ve sonlanmasına karşın bilinç kaybı, kardiyojenik şok, kardiyak arrest gibi şiddetli reaksiyonlar gelişebilir. Esmolol'ün ventrikül hızını kontrol etmek için kullanıldığının varsayıldığı kompleks klinik koşullarda birkaç ölüm vakası bildirilmiştir.
En sık görülen yan etki dozla ilişkili olan, ancak her dozda da görülebilen hipotansiyondur. Hipotansiyon şiddetli olabilmektedir. Bir hipotansif epizod yaşanması durumunda infüzyon hızı düşürülmeli veya gerekirse infüzyon kesilmelidir. Hipotansiyon genellikle geriye dönüşebilir niteliktedir (ERMOLOC uygulamasına son verildikten sonraki 30 dakika içinde). Bazı vakalarda kan basıncını normal değerlerine yükseltebilmek için ek girişimlere gerek duyulabilir. Sistolik kan basıncı düşük hastalarda dozun ayarlanması ve idame infüzyonu sırasında özel dikkat gerekir.
ERMOLOC kullanımı sırasında ağır bradikardi dahil bradikardi ve kardiyak arrest meydana gelmiştir. ERMOLOC, tedavi öncesinde kalp hızı düşük olanlarda özel bir dikkatle ve ancak olası yararları, riskine ağır basıyorsa kullanılmalıdır.
Önceden ağır sinüs bradikardisi olan hastalarda ERMOLOC kullanımı kontrendikedir (bölüm 4.3'e bakınız). Nabzın istirahattayken dakikada 50-55 vurunun altına düştüğü ve hastada bradikardiye ilişkin semptomlar görülürse dozaj azaltılmalı ya da uygulamaya son verilmelidir.
Konjestif kalp yetmezliğinde dolaşım fonksiyonunun desteklenmesi için sempatik aktivite gereklidir. Beta blokajının miyokard depresyonunu arttırarak yetmezliği daha da ağırlaştırma riski bulunmaktadır. Belirli bir süreden uzun sürelerle beta blokörlerle miyokard depresyonunun devam ettirilmesi, bazı vakalarda kalp yetmezliğine yol açabilir.
Kardiyak fonksiyonları bozulmuş hastalarda ERMOLOC kullanılırken dikkatli olunması gerekir. Kalp yetmezliğinin ilk belirti ve semptomları görülür görülmez. ERMOLOC tedavisine son verilmelidir. Her ne kadar eliminasyon yarı ömrünün kısa olması nedeniyle, ERMOLOC'un kesilmesi yeterli olsa da ayrıca spesifik tedavi uygulanması da düşünülebilir (bölüm 4.9'a bakınız). ERMOLOC dekompanse kalp yetmezliği olan hastalarda kontrendikedir (bölüm 4.3'e bakınız).
Kalpteki ileti süresi üzerindeki negatif etkileri nedeniyle beta blokör ilaçlar birinci derece kalp bloğu veya diğer kalp ileti bozukluğu olan hastalarda ancak dikkatle verilmelidir (bölüm 4.3'e bakınız).
ERMOLOC feokromositomalı hastalarda ancak alfa-reseptör blokörleriyle ön tedavi görmüş olmak kaydıyla ve dikkatle kullanılmalıdır (bölüm 4.3'e bakınız).
Hipotermiyle uyarılmış hipertansiyonun tedavisinde ERMOLOC kullanımında dikkatli olunması gerekir.
Genel olarak bronkospastik hastalıkları olanlar beta blokör kullanmamalıdır. Beta- 1 reseptörlere nispeten selektif olması ve kullanım sırasında titre edilebilir olması nedeniyle ERMOLOC bu hastalarda dikkatle kullanılabilir. Ancak beta-1 selektifliği mutlak olmadığından ERMOLOC, olası etkili en düşük dozu elde etmek için dikkatle titre edilmelidir. Bronkospazm durumunda infüzyon derhal durdurulmalı ve gerektiğinde beta-2 agonist bir preparat uygulanmalıdır.
Hasta zaten bir beta-2-reseptör stimülan ajan kullanıyorsa, bu ajanın dozunun yeniden değerlendirilmesi gerekebilir.
ERMOLOC hırıltılı solunum ya da astım hikayesi olan hastalarda dikkatli kullanılmalıdır.
ERMOLOC diyabetik hastalarda ya da edinsel hipoglisemisi olduğundan kuşkulanılanlarda dikkatli uygulanmalıdır. Beta blokörler hipogliseminin taşikardi gibi prodromal semptomlarını maskeleyebilir. Ancak sersemlik hali ve terleme etkilenmeyebilir. Beta blokörlerle antidiyabetik ajanların eşzamanlı kullanımı antidiyabetik ajanların hipoglisemik etkisinde artışa yol açabilir (bölüm 4.5'e bakınız).
ERMOLOC kullanımına bağlı olarak infüzyon bölgesinde reaksiyonlar meydana gelmiştir. Bu reaksiyonlar arasında iritasyon ve enflamasyon bulunabildiği gibi özellikle ekstravazasyon ile ilişkili tromboflebit, nekroz ve deride blisterlenme gibi daha ciddi reaksiyonlar da bulunur (bölüm 4.8'e bakınız). Küçük venlerden veya kelebek kateterle yapılacak uygulamalardan kaçınılmalıdır. Lokal bir infüzyon yeri reaksiyonu oluştuğunda, alternatif bir infüzyon bölgesi kullanılmalıdır.
Beta blokörler, karşılanmamış alfa-reseptör kökenli koroner arter vazokonstriksiyonuna bağlı olarak Prinzmetal anjinası olan hastalarda anjina ataklarının sıklık ve süresini arttırabilir. Bu tür hastalarda selektif olmayan beta blokörler kullanılmamalı; beta-1 selektif olan blokörler ise yalnızca son derece dikkatli şekilde kullanılmalıdır.
ERMOLOC hipovolemik hastalarda refleks taşikardiyi zayıflatabilir ve dolaşım kollapsı riskini arttırabilir. Bu nedenle bu tür hastalarda ERMOLOC dikkatli kullanılmalıdır.
Beta blokörler periferik dolaşım bozukluklarının (Raynaud hastalığı veya sendromu, intermittan kladikasyon) bulunduğu hastalarda son derece dikkatli uygulanmalıdır.
ERMOLOC dahil, özellikle intravenöz olarak uygulanan bazı beta blokörler, serum potasyum düzeylerinde yükselme ve hiperkalemi ile ilişkilendirilmiştir. Bu risk böbrek yetmezliği ve hemodiyaliz tedavisi görme gibi risk faktörlerinin bulunduğu hastalarda artar.
Beta blokörler hem alerjenlere duyarlılığı, hem de anafilaktik reaksiyonların şiddetini arttırır. Beta blokör kullanan hastalar anafilaktik ya da anafilaktoid reaksiyonların tedavisinde kullanılan olağan dozlarda epinefrine yanıt vermeyebilir (bölüm 4.5'e bakınız).
Beta blokörlerin psöriyazis ya da psöriyazis benzeri döküntülere yol açabileceği ve mevcut bir psöriyazis hastalığını ağırlaştırabileceği bildirilmiştir. Özgeçmiş ya da soy
geçmişinde psöriyazis bulunanlarda beta blokörler ancak tedaviden beklenen fayda ile olası riskleri dikkatle değerlendirildikten sonra kullanılmalıdır.
Propranolol ve metoprolol gibi beta blokörler hipertiroidinin belirli klinik işaretlerini (taşikardi gibi) maskeleyebilir. Tirotoksikoz gelişim riski ya da kuşkusu olan hastalarda beta blokörlerle devam etmekte olan tedavinin aniden kesilmesi tiroid krizini hızlandırabilir ve bu tür hastalar yakından izlenmelidir.
Bu ürün 250 ml'lik bir torbasında 30.45 mmol (700 mg) sodyum içerir. Bu durum kontrollü sodyum diyetinde olan hastalar için göz önünde bulundurulmalıdır.
4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri
ERMOLOC diğer antihipertansif ajanlar veya bradikardiye neden olabilen diğer ilaçlarla birlikte kullanıldığında daima dikkatli olunmalıdır: ERMOLOC'un etkileri veya hipotansiyon veya bradikardi yan etkileri şiddetlenebilir.
Verapamil gibi kalsiyum antagonistleri ve daha düşük düzeyde diltiazem kontraktilitede ve AV iletiminde negatif bir etkiye sahiptir. Bu kombinasyon iletim anomalileri olan hastalara uygulanmamalı ve ERMOLOC verapamil kesildikten sonraki 48 saatte verilmemelidir (bkz bölüm 4.3).
Dihidropiridin türevi (örn. nifedipin) kalsiyum antagonistleri hipotansiyon riskini arttırabilir. Kalp yetmezliği için kalsiyum antagonist ile tedavi gören hastalara beta blokör uygulanması kalp yetmezliğine neden olabilir. ERMOLOC'un dikkatle titre edilerek uygun hemodinamik monitorizasyon önerilir.
ERMOLOC ve Sınıf I anti-aritmik ilaçların (örn, dizopiramid, kinidin) ve amiodaronun eşzamanlı kullanımı atriyal-iletim süresinde güçlendirici etkiye sahip olabilir ve negatif inotropik etkiye neden olabilir.
ERMOLOC ve insülin veya oral anti-diyabetik ilaçların eşzamanlı kullanımı kan şekeri düşürücü etkiyi artırabilir (özellikle selektif olmayan beta-blokörler). Beta- adrenerjik blokajı hipoglisemi belirtilerinin (taşikardi) gözlenmesini engelleyebilir ancak baş dönmesi / sersemlik ve terleme gibi diğer belirtiler maskelenmeyebilir.
Anestezi ilaçları: hastaların hacim durumunun belirsiz olduğu veya eşzamanlı antihipertansif ilaçların kullanıldığı durumlarda refleks taşikardide azalma veya hipotansiyon riskinde artış görülebilir. Beta-blokaja devam edilmesi indüksiyon ve entübasyon sırasında aritmi riskini azaltır. Hastaya ERMOLOC'a ek olarak bir beta-blokör ajan verilirken anestezist bilgilendirilmelidir. İnhalasyon anestezi ajanlarının hipotansif etkileri ERMOLOC varlığında artabilir. Her bir ajanın dozu istenen hemodinamik parametrelerin korunması için değiştirilebilir.
ERMOLOC ile gangliyon bloke edici ilaçların kombinasyonu hipotansif etkiyi arttırabilir.
Steroid olmayan anti-enflamatuvar ilaçlar (NSAİİ) ile birlikte kullanıldıklarında beta blokörlerin hipotansif etkileri azalabilir.
Beta-blokörlerle eşzamanlı olarak floktafenin veya amisulprid kullanılırken özellikle dikkatli olunmalıdır.
Trisiklik antidepresanların (imipramin ve amitriptilin gibi), barbitüratların ya da fenotiyazinler
(klorpromazin gibi) yanında diğer antipsikotik ajanların (klozapin gibi) birlikte uygulanması kan basıncını azaltıcı etkiyi arttırabilir. Beklenmeyen bir hipotansif durumdan kaçınmak için birlikte kullanımda ERMOLOC dozu azaltılmalıdır.
Beta-blokörler kullanılırken anafilaktik reaksiyon riski olan hastalarda alerjen maruziyetine (kazara, diagnostik veya terapötik) reaksiyon gözlenebilir. Beta blokör kullanan hastalar, anafilaktik reaksiyonların tedavisinde kullanılan mutad epinefrin dozlarına yanıt vermeyebilir (bkz bölüm 4.4).
ERMOLOC'un etkileri eşzamanlı uygulandığında beta-adrenerjik agonist aktiviteye sahip sempatomimetik ilaçlara bağlı olarak azalabilir. Her bir ajanın dozunun hasta yanıtına göre ayarlanması veya alternatif terapötik ajanların kullanımının düşünülmesi gerekebilir.
Katekolamin boşalmasına yol açan ilaçlar (örn., rezerpin) beta-blokör ilaçlarla birlikte verildiğinde aditif bir etki gösterebilirler. ERMOLOC ile eşzamanlı olarak katekolamin boşalmasına yol açan ilaç tedavisi alan hastalar vertigo, senkop veya postüral hipotansiyon ile sonuçlanabilen hipotansiyon ve önemli bradikardi belirtileri açısından yakından izlenmelidir.
Beta blokörlerin moksonidin veya alfa-2-agonistleriyle (klonidin gibi) birarada kullanımı çekilmeye bağlı rebound hipertansiyon riskini arttırır. Klonidin veya moksonidin bir beta blokörle birlikte kullanılacaksa ve daha sonra her iki ilaç da kesilecekse, ilk olarak beta blokör, klonidin veya moksonidin birkaç gün sonra kesilmelidir.
Beta blokörlerin ergo türevleriyle birarada kullanımı ciddi periferik vazokonstriksiyon ve hipertansiyonla sonuçlanabilir.
ERMOLOC ile varfarin arasındaki bir etkileşim olup olmadığını belirlemek için yapılan bir çalışmadaki veriler, ERMOLOC ve varfarinin birlikte uygulanmasının, varfarinin plazma düzeylerini değiştirmediğini göstermiştir. Buna rağmen varfarin ile birlikte uygulanan ERMOLOC'un konsantrasyonları daha yüksek olarak bulunmuştur.
ERMOLOC ve digoksin sağlıklı gönüllülerde intravenöz yoldan birlikte uygulandığında, bazı zaman noktalarında digoksinin kandaki düzeylerinde %10-20'lik bir yükselme olduğu bildirilmiştir. Dijital glikozitleriyle ERMOLOC kombinasyonu AV ileti süresini uzatabilir. Digoksin, ERMOLOC'un farmakokinetik özelliklerini etkilememiştir.
İntravenöz morfin ve ERMOLOC sağlıklı gönüllülere eşzamanlı olarak uygulandığında morfinin kan düzeylerinde herhangi bir değişiklik olmadığı görülmüştür. Morfin varlığında ERMOLOC'un kararlı durum kan düzeylerinin %46 oranında arttığı ancak diğer farmakokinetik parametrelerden hiçbirinin değişmediği saptanmıştır.
ERMOLOC'un suksametonyum klorür ve mivakuryum ile uyarılan nöromüsküler blokajın süresi üzerine etkisi cerrahi girişimde bulunulan hastalarda incelenmiştir. ERMOLOC,suksametonyum klorür ile indüklenen nöromüsküler blokaj in başlamasını etkilememektedir,ancak nöromüsküler blokajın süresi 5 dakikadan 8 dakikaya çıkmıştır. ERMOLOC, mivakuryumun klinik süresini (%18,6) ve geri kazanım indeksini (%6,7) kısmen uzatmıştır.
Varfarin, digoksin, morfin, suksametonyum klorür veya mivakuryum ile yapılan çalışmalarda özlenen etkileşimler klinik açıdan çok önemli olmamakla birlikte esmolol eşzamanlı olarak varfarin, digoksin, morfin, suksametonyum klorür veya mivakuryum uygulanan hastalarda titrasyon dikkatli yapılmalıdır.
Gebelik ve Iaktasyon Genel tavsiye:
Gebelik Kategorisi: C / D (2. ve 3. trimester)
Çocuk doğurma potansiyeli bulunan kadınlar / Doğum kontrolü (Kontrasepsiyon)
Çocuk doğurma potansiyeli olan kadınlar tedavi süresince etkili doğum kontrolü uygulamak zorundadırlar.
Gebelik dönemi
Hayvanlar üzerinde yapılan çalışmalar, gebelik /ve-veya/ embriyonal/fetal gelişim /ve- veya/ doğum /ve-veya/ doğum sonrası gelişim üzerindeki etkiler bakımından yetersizdir. Hayvanlar üzerinde ERMOLOC ile yapılan çalışmalarda üreme toksisitesi görülmüştür (bkz. kısım 5.3). İnsanlara yönelik potansiyel risk bilinmemektedir.
Esmolol hidroklorür gebelik döneminde önerilmez.
Farmakolojik etkileri nedeniyle gebeliğin geç döneminde fetus ve yenidoğan üzerindeki yan etkileri (özellikle hipoglisemi, hipotansiyon ve bradikardi) dikkate alınmalıdır.
Gebelikte ERMOLOC tedavisi gerekli olursa, ancak potansiyel yarar, fetus üzerindeki toksisiteden fazla ise kullanılmalıdır ve uteroplasental kan akımı ve fötal büyüme izlenmelidir. Yenidoğan bebeğin yakından izlenmesi gerekir.
Laktasyon dönemi
Esmolol hidroklorür emzirme döneminde kullanılmamalıdır.
Emziren kadınlarda esmolol hidroklorürün anne sütüne geçip geçmediği bilinmemektedir. Yenidoğan bebeklere/bebeklere potansiyel bir risk gözardı edilemez.
Üreme yeteneği / fertilite
Esmolol'ün insanlarda üreme yeteneği / fertilité üzerindeki etkisini araştıran bir çalışma bulunmamaktadır.
4.7. Araç ve makine kullanımı üzerindeki etkiler
Araç ve makine kullanımı sırasında ERMOLOC'un kullanımı mümkün olmadığından bu konudaki etkisi bilinmemektedir.
4.8. İstenmeyen etkiler
İstenmeyen etkilerin görülmesi durumunda ERMOLOC'un dozu azaltılabilir ya da uygulamaya son verilebilir.
Görülen advers etkilerin çoğu hafif ve geçici nitelikte olarak bildirilmiştir. En önemlisi hipotansiyondur.
Advers etkilerin görülme sıklığı, aşağıdaki kriterler kullanılarak değerlendirilmiştir: Çok yaygın (≥1/10); yaygın (≥1/100 ila <1/10); yaygın olmayan (≥1/1.000 ila <1/100); seyrek (≥1/10.000 ila <1/1.000); çok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle
tahmin edilemiyor).
Metabolizma ve beslenme hastalıkları
Yaygın: Anoreksi
Bilinmiyor: Hiperkalemi, metabolik asidoz
Psikiyatrik hastalıklar
Yaygın: Depresyon, anksiyete
Yaygın olmayan: Anormal düşünce
Sinir sistemi hastalıkları
Yaygın: Baş dönmesi / sersemlik hali, uykuya meyil, baş ağrısı, parestezi, dikkat bozukluğu, konfüzyonel durum, ajitasyon
Yaygın olmayan: Senkop, konvülsiyon, konuşma bozukluğu.
Göz hastalıkları
Yaygın olmayan: Görmede bozulma
Kardiyak hastalıklar
Yaygın olmayan: Bradikardi, atriyoventriküler blok, pulmoner arteriyel basınçta yükselme, kalp yetmezliği, ventriküler ekstrasistoller, nodal ritim, anjina pektoris Çok seyrek: Sinüs durması, asistol.
Bilinmiyor: Akselere idiyoventriküler ritim, koroner arteriyospazm, kardiyak arest.
Vasküler hastalıklar
Çok yaygın: Hipotansiyon
Yaygın olmayan: Periferik iskemi, solukluk, yüz ve boyun bölgesinde kızarma Çok seyrek: Trombofilebit
Solunum, göğüs bozuklukları ve mediastinal hastalıklar
Yaygın olmayan: Dispne, pulmoner ödem, bronkospazm, hırıltılı solunum,
nazal konjesyon, akciğer seslerinde ronkus ve raller
Gastrointestinal hastalıklar
Yaygın: Bulantı, kusma
Yaygın olmayan: Disguzi, dispepsi, kabızlık, ağızda kuruma, karında ağrı
Deri ve deri altı doku hastalıkları
Çok yaygın: Diaforez
Yaygın olmayan: Ciltte renk kaybı, eritem
Çok seyrek: Deri nekrozu (ekstravazasyona bağlı)
Bilinmiyor: Psoriyazis, anjiyoödem, ürtiker
Kas-iskelet bozuklukları, bağ doku ve iskelet hastalıkları
Yaygın olmayan: Kas-iskelet ağrısı
Böbrek ve idrar yolu hastalıkları
Yaygın olmayan: Üriner retansiyon
Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklar:
Yaygın: Asteni, halsizlik, enjeksiyon yeri reaksiyonu, infüzyon bölgesi reaksiyonu, infüzyon bölgesi inflamasyonu, infüzyon bölgesi endürasyonu
Yaygın olmayan: Titremeler, ateş yükselmesi, ödem, ağrı, infüzyon bölgesinde yanma, infüzyon bölgesinde ekimoz
Bilinmiyor: İnfüzyon bölgesinde filebit, infüzyon bölgesinde veziküller, infüzyon bölgesinde blisterlenme
Baş dönmesi / sersemlik hali ve diyaforez semptomatik hipotansiyonla birlikte görülmüştür.
Midskapular ağrı ve kostokondrit dahil.
4.9. Doz aşımı ve tedavisi
Konsantre ERMOLOC solüsyonları ile kazara büyük doz aşımı vakaları meydana gelmiştir. Bu doz aşımlarının bazıları ölüme yol açarken, diğerleri kalıcı işlev kaybına neden olmuştur. Preparatın 6.25 mg - 2.5 g arasındaki bolus dozları (12.5 - 50 mg/kg) ölümle sonuçlanmıştır.
Doz aşımının semptomları
Doz aşımı durumunda aşağıdaki belirtiler oluşabilir: şiddetli hipotansiyon, sinüs bradikardisi, atriyoventriküler blok, kalp yetmezliği, kardiyojenik şok, kardiyak arest, bronkospazm, solunum yetmezliği, komaya ilerleyebilen bilinç kaybı, havaleler, bulantı, kusma, hipoglisemi ve hiperkalemi.
Doz aşımında tedavi
Kısa eliminasyon yarı ömrü nedeniyle (yaklaşık 9 dakika) toksisite tedavisinde ilk basamak ERMOLOC infüzyonunun durdurulmasıdır. Doz aşımı sonrasında semptomların kaybolması için gereken süre uygulanan ERMOLOC miktarına bağlı olacaktır. Bu süre ERMOLOC'un terapötik doz düzeyinde ilaç kesildikten sonra 30 dakikadan uzun sürebilir. Suni solunum gerekebilir. Daha sonra gözlenen klinik etkilere göre aşağıdaki tedaviler uygulanabilir:
Bradikardi: Atropin ya da diğer bir antikolinerjik ilaç intravenöz yoldan uygulanır. Bradikardinin yeterince tedavi edilemediği durumlarda pacemaker gerekli olabilir.
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik Grubu: Selektif beta blokör ilaçlar ATC kodu: C07AB09
ERMOLOC bir beta selektif (kardiyoselektif) adrenerjik reseptör blokaj ajanıdır. Terapötik dozlarda anlamlı bir intrensek sempatomimetik aktivite (ISA) ya da membran stabilizan etkinliği yoktur.
ERMOLOC'un etkin maddesi olan esmolol hidroklorür kimyasal olarak beta blokörlerin fenoksi propanolamin sınıfındandır.
5. FARMAKOLOJİK ÖZELLİKLER
Uygun yükleme dozu kullanıldığında, kandaki kararlı durum düzeylerine 5 dakikada ulaşılır. Ancak terapötik etkiye stabil plazma konsantrasyonundan daha kısa sürede erişilir. Daha sonra istenen farmakolojik etkinin elde edilmesi için infüzyon oranı ayarlanabilir.
ERMOLOC beta blokörlerin bilinen hemodinamik ve elektro fizyolojik etkilerine sahiptir:
İstirahat halinde ve egzersiz sırasında kalp hızında azalma;
5.2. Farmakokinetik özellikler
Emilim:
İntravenöz uygulama sonrası maksimum plazma konsantrasyonuna süratle ulaşılır.
Dağılım:
Esmolol hidroklorürün dağılım yarılanma süresi yaklaşık 2 dakika gibi çok kısadır. Dağılım hacmi 3.4 L/kg'dır.
Bivotransformasvon:
Esmolol hidroklorür esterazlar tarafından bir asit metaboliti (ASL-8123) ve metanole metabolize olur. Bu metabolizasyon, ester bağlarının eritrositlerin sitozollerindeki esterazlar tarafından hidrolizi yoluyla gerçekleşir.
Esmolol hidroklorürün metabolizması dozunun 50 ile 300 mikrogram/kg/dakika olduğunda dozdan bağımsızdır.
Esmolol hidroklorürün insan plazma proteinlerine %55 oranında bağlandığı, asit metabolitinin ise sadece %10 oranında bağlandığı gösterilmiştir.
Eliminasyon:
İntravenöz uygulama sonucu eliminasyon yan ömrü yaklaşık 9 dakikadır.
Toplam klerensi 285 ml/kg/dakikadır; toplam klerens karaciğer veya diğer organların dolaşımından bağımsızdır. Esmolol hidroklorür böbreklerden kısmen değişmeden (uygulanan miktarın %2''sinden azı) kısmen de zayıf bir beta blokör etkinliğe sahip asit metaboliti olarak (uygulanan miktarın %0.1'inden azı) atılır. Asit metabolit idrarla atılır ve eliminasyon yarı ömrü yaklaşık 3.7 saattir.
Doğrusallık / doğrusal olmayan durum:
Sağlıklı erişkinlerde esmolol kinetiği doğrusaldır. Bir yükleme dozu uygulanmazsa 50-300 mikrogram/kg/dakikalık dozlarda uygulandığında, plazma sabitlenmiş düzeylerine ulaşım süresi dozla doğrusaldır.
Hastalardaki karakteristik özellikler
Pediyatrik popülasyon:
Yaşlan 3 ile 16 arasında olan 22 pediyatrik hastada bir farmakokinetik çalışma gerçekleştirilmiştir. 1000 mikrogram/kg'lık bir esmolol yükleme dozu uygulandıktan sonra
devamlı infüzyonla dakikada 300 mikrogram/kg'lık dozla idame tedavisi uygulanmıştır. Çalışmada çocuklardaki esmolol kinetiğinin erişkinlerdekinden farklı olmadığına işaret edecek şekilde ortalama toplam vücut klerensi 119 ml/kg/dakika, ortalama dağılım hacmi
283 ml/kg ve ortalama terminal eliminasyon yarılanma ömrü 6.9 dakika olarak gözlenmiştir. Ancak, çocuklarda bireysel değişkenliğin fazla olduğu gözlenmiştir.
5.3. Klinik öncesi güvenlilik verileri
Hayvan çalışmalarında teratojenik etki görülmemiştir. Tavşanlarda olasılıkla esmololün neden olduğu embriyotoksik bir etki (fötal rezorpsiyonda artma) gözlenmiştir. Bu etki terapötik dozların en az 10 katı yüksek dozlarda gözlenmiştir.
Esmolol'ün fertilite üzerindeki etkileri ile périnatal ve postnatal etkilerini araştıran bir çalışma gerçekleştirilmemiştir. Esmolol'ün birkaç in vitro ve in vivo test sistemlerinde mutajenik olmadığı bulunmuştur. Esmolol'ün güvenilirliği uzun süreli çalışmalarla incelenmemiştir.
6. FARMASÖTİK ÖZELLİKLER
6.1. Yardımcı maddelerin listesi
Sodyum asetat trihidrat Glasiyel asetik asit Sodyum klorür
Sodyum hidroksit ve/veya hidroklorik asit – pH ayarı için
Enjeksiyonluk su
6.2. Geçimsizlikler
Geçimlilik çalışmaları bulunmadığından bu ilaç diğer ilaçlarla veya sodyum bikarbonat çözeltisi ile karıştırılmamalıdır.
Alkali maddelerle temasından kaçınınız.
6.3. Raf ömrü
24 ay.
Açılan ürün 2-8°C arasında saklandığında 24 saat süreyle fizikokimyasal olarak stabildir
Mikrobiyolojik açıdan ürün torbası açıldıktan sonra hemen kullanılmalıdır. Hemen kullanılamadığı durumlarda, kullanılmaya başlamadan önceki saklama süre ve koşulları kullanıcının sorumluluğundadır. Bu süre 2-8°C arasında torbanın kontrollü ve valide edilmişaseptik koşullarda açılmadığı durumlarda normalde 24saatten uzun olamaz.
6.4. Saklamaya yönelik özel tedbirler
25°C altındaki oda sıcaklığında ambalajında saklanmalıdır. Buzdolabında saklanmamalı ya da dondurulmamalıdır. Çözeltinin saklama koşulları için bölüm 6.3'e bakınız.
6.5. Ambalajın niteliği ve içeriği
Alüminyum dış torba içinde iki çıkışlı 250 ml'lik non-pvc torba.
6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
Kullanılmamış olan ürünler ya da atık materyaller “Tıbbi Ürünlerin Kontrolü Yönetmeliği†ve “Ambalaj ve Ambalaj Atıklarının Kontrolü Yönetmeliğiâ€ne uygun olarak imha edilmelidir.
TORBA KULLANIM TALİMATI
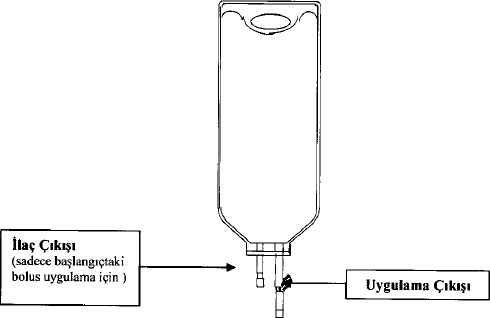
Multiflex ERMOLOC Premiks 10 mg/mL infüzyon için kullanıma hazır çözelti, 250 ml'lik polyolefinik torbalarda (biri torbaya ilaç uygulama için, diğeri torbadaki ilacın hastaya verilmesi için olan iki PVC çıkışlı non-lateks polyolefinik torba) sunulmaktadır.
Multiflex ERMOLOC Premiks 10 mg/mL infüzyon için kullanıma hazır çözeltinin torbasındaki ilaç uygulama ucu yalnızca torbadan ilk bolus uygulanacak ilacın çekilmesi için kullanılmalıdır; tekrarlanan bolus uygulaması için değildir. Bolus dozunu çekerken aseptik teknik kullanılmalıdır. Multiflex ERMOLOC Premiks 10 mg/mL infüzyon için kullanıma hazır çözelti'ye hiçbir ilave ilaç eklenmemelidir. Her torba tek hastada kullanım içindir. İlaç uygulama çıkışının mühürü kırıldıktan ve torbadan ilacın çekilmesinden sonra torbanın 24 saat içinde kullanılması gerekir. Çözeltinin kullanılmayan bölümü ve torbası yerel uygulamalar doğrultusunda imha edilmelidir. Kısmen kullanılmış torbaları yeniden kullanmayınız.
Şekil 1. Çift-çıkışlı Multiflex torba
DİKKAT
Plastik torbaları seri bağlamalar için kullanmayınız. Bu tip kullanım ikinci kaptaki sıvının uygulanması tamamlanmadan önce birinci kaptan rezidüel havanın çekilmesine bağlı emboliye neden olabilir.
AÇMAK İÇİN
Kullanımdan hemen öncesine kadar dış ambalajından (dış torba) çıkarılmamalıdır. Dış torba daha önceden açılmışsa ya da hasar görmüşse kullanılmamalıdır. Dış torba nemi önleme amacını taşır. İç torba çözeltinin sterilitesini korur.
Dış torba çentikli yerinden açılarak premiks torba çıkarılır. Bu aşamada plastik torba üzerinde görülebilen opasiteler, sterilizasyon prosesi sırasındaki nem absorbsiyonuna bağlıdır ve çözeltinin kalitesini veya güvenilirliğini etkilemez. Opaklık giderek azalacaktır.
İç torba sıkıştırılarak küçük sızıntılar olup olmadığı kontrol edilir. Sızıntı varsa sterilizasyon etkilenmiş olacağından çözelti atılmalıdır. Uygulamadan önce partiküler madde ve renk değişikliği için solüsyon görsel olarak incelenir. Yalnızca berrak ve renksiz veya açık sarı renkli çözeltiler kullanılmalıdır.
Multiflex ERMOLOC Premiks 10mg/mL'ye hiçbir ekstra maddeeklenmemelidir.
İNTRAVENÖZ UYGULAMA İÇİN HAZIRLIKLAR (aseptikteknik kullanılmalıdır)
Premiks torba, asma yerinden bir askıya asılır.
 Lösemi Kan Kanseri
Lösemi, kan kanseridir ve vücudunun kan oluşturan dokularının hastalanması anlamına gelir. Birçok lösemi türü vardır; bazı lösemi türleri çocuklarda bazıları da yetişkinlerde sık görülür.
Lösemi Kan Kanseri
Lösemi, kan kanseridir ve vücudunun kan oluşturan dokularının hastalanması anlamına gelir. Birçok lösemi türü vardır; bazı lösemi türleri çocuklarda bazıları da yetişkinlerde sık görülür. |
 Tiroid Kanseri
En sık görülen tiroid kanseri türü olan papiller tiroid kanseri, tüm tiroid kanserlerinin yaklaşık %70'ini oluşturur.
Tiroid Kanseri
En sık görülen tiroid kanseri türü olan papiller tiroid kanseri, tüm tiroid kanserlerinin yaklaşık %70'ini oluşturur. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| ESMOBLOC | 8699606524861 | 3,237.02TL |
| KARDOES | 8699614690099 | |
| MULTIFLEX | 8680400770288 | |
| TURKTIPSAN | 8697637692023 | 2,322.01TL |
| Diğer Eşdeğer İlaçlar |
 |
Grip, Soğuk Algınlığı ve Öksürük Grip ve soğuk algınlığı (nezle) semptomları arasındaki farkı bilmek önemlidir. Soğuk algınlığı gripten daha hafif belirtiler gösteren bir solunum yolu hastalığıdır. |
 |
En Yaygın Alerji Türleri Bağışıklık sistemi, polen, arı zehiri veya evcil hayvan gibi yabancı bir maddeye veya çoğu insanda reaksiyona neden olmayan bir yiyeceğe tepki gösterdiğinde alerjiler meydana gelir. |
 |
Asperger Sendromu Asperger sendromu, otistik gurubun bir bölümü olan bir özürdür. Bu genelde, gurubun daha ”yüksek” tarafında yer aldığı düşünülen kişilere uygun bir tanıdır. |
İLAÇ GENEL BİLGİLERİ
Haver Pharma İlaç A.Ş.
| Geri Ödeme Kodu | A15517 |
| Satış Fiyatı | 3355.75 TL [ 2 May 2025 ] |
| Önceki Satış Fiyatı | 3355.75 TL [ 25 Apr 2025 ] |
| Original / Jenerik | Jenerik İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8681153070021 |
| Etkin Madde | Esmolol Hcl |
| ATC Kodu | C07AB09 |
| Birim Miktar | 10 |
| Birim Cinsi | MG |
| Ambalaj Miktarı | 250 |
| Kalp Damar Sistemi > Beta Bloke Edici Ajanlar > Esmolol |
| Yerli ve Beşeri bir ilaçdır. |