NOVOMIX 30 PENFILL 3 ml 5 PENFILL Kısa Ürün Bilgisi
{ Insulin Aspart }
1. BEŞERİ TIBBİ ÜRÜNÜN ADI
NovoMix30 Penfill100 U/mL enjeksiyonluk süspansiyon içeren kartuş Steril
2. KALİTATİF VE KANTİTATİF BİLEŞİM
Etkin madde
Çözünür insülin aspart*/protamin-kristalize insülin aspart* (30/70 oranında, 100 ünite/mL)
*Saccharomyces cerevisiae'den rekombinant DNA teknolojisi ile üretilmiş bir proteindir. 1 ünite insülin aspart 6 nmol, 0,035 mg tuzsuz anhidr insülin asparta eşdeğerdir.
1 kartuş 300 üniteye eşdeğer 3 mL süspansiyon içerir.
Yardımcı maddeler
Sodyum klorür 0,877 mg/mL
Disodyum fosfat dihidrat… 1,25 mg/mL
Sodyum hidroksit (pH ayarı için) yaklaşık 2,2 mg/mL
Yardımcı maddeler için 6.1'e bakınız.
3. FARMASÖTİK FORMU
Enjeksiyon için süspansiyon.
NovoMix30 Penfillbulanık, beyaz renkli, sulu bir süspansiyondur.
4. KLİNİK ÖZELLİKLER
4.1. Terapötik endikasyonlar
Erişkinlerde, adolesanlarda ve 10 yaş ve üstü çocuklarda diyabetes mellitus hastalığının tedavisinde endikedir.
4.2. Pozoloji ve uygulama şekli
Pozoloji/uygulama sıklığı ve süresi:
İnsan insülini internasyonal ünite olarak ifade edilirken, insülin aspart dahil, insülin analoglarının etkinliği ünite olarak ifade edilir.
NovoMix30 Penfill'in dozu bireylere özgüdür ve hastanın ihtiyacına bağlı olarak belirlenmelidir. Optimal glisemik kontrolü sağlayabilmek için kan glukoz izlemesi ve insülin doz ayarlamaları önerilir.
Tip 2 diyabetli hastalarda, NovoMix30 Penfilltek başına verilebilir. NovoMix30 Penfilloral antidiyabetik ilaçlar ve/veya GLP-1 reseptör agonistleri ile kombinasyon halinde de
verilebilir. Tip 2 diyabetli hastalarda önerilen NovoMix30 Penfillbaşlangıç dozu kahvaltıda 6 ünite ve akşam yemeğinde 6 ünitedir. NovoMix 30 Penfill aynı zamanda günde bir kez akşam yemeğinde 12 ünite olarak da başlanabilir. NovoMix30 Penfillgünde bir kez kullanılırken, toplam doz 30 üniteye ulaştığında genellikle kahvaltı ve akşam yemeği dozu olmak üzere eşit iki doza bölünmesi önerilmektedir. Eğer günde 2 doz NovoMix30 Penfilltekrarlayan gün içi hipoglisemik ataklara neden olursa, sabah dozu, sabah ve öğle yemeği dozu olarak ikiye bölünebilir (günde 3 doz uygulaması).
Doz ayarlamaları için aşağıdaki titrasyon kılavuzu önerilmektedir:
Yemek öncesi kan şekeri düzeyi |
| |
< 4,4 mmol/l | < 80 mg/dl | - 2 ünite |
4,4-6,1 mmol/l | 80-110 mg/dl | 0 |
6,2-7,8 mmol/l | 111-140 mg/dl | + 2 ünite |
7,9-10 mmol/l | 141-180 mg/dl | + 4 ünite |
> 10 mmol/l | > 180 mg/dl | + 6 ünite |
Son üç günün en düşük yemek öncesi kan glukoz değerleri kullanılmalıdır. Bu günlerde eğer hipoglisemi olmuşsa doz artırılmamalıdır. Doz değişiklikleri HbAhedefine ulaşılana kadar haftada bir kez yapılabilir. Yemek öncesi kan şekeri değerleri yemekten bir önceki dozun yeterli olup olmadığına karar vermek için kullanılmalıdır.
Tip 2 diyabetli hastalarda, hipoglisemi riskini en aza indirmek için NovoMix30 Penfille bir GLP-1 reseptör agonisti eklendiğinde; HbA'nin % 8'den daha az olduğu hastalar için % 20'lik bir doz azaltılması önerilir. HbAnin % 8'den daha yüksek olduğu hastalar için, doz azaltımı değerlendirilmelidir. Daha sonra, dozaj bireysel olarak ayarlanmalıdır.
Tip 1 diyabetli hastalarda bireysel insülin gereksinimi genellikle 0,5 ve 1,0 ünite/kg/gün arasındadır. NovoMix30 Penfillbu gereksinimi tamamen veya kısmen karşılayabilir.
Hasta, fiziksel aktivitesini artırırsa, genel diyetini değiştirirse ya da başka hastalıklar da varsa, doz ayarlaması yapmak gerekebilir.
Diğer insülin tıbbi ürünlerinden geçiş
Bifazik insan insülini kullanan bir hastayı NovoMix30 Penfill'e transfer ederken aynı doz ve rejimle tedaviye başlayınız. Daha sonra kişisel gereksinimlere uygun biçimde titre ediniz (yukarıdaki tabloda yer alan titrasyon kılavuzuna bakınız). Geçiş ve geçişten sonraki ilk haftalarda sıkı glukoz gözetimi önerilmektedir (bkz. Bölüm 4.4).
Uygulama şekli:
NovoMix30 Penfill, insülin analogu olan insülin aspartın bifazik süspansiyonudur. Süspansiyon, 30/70 oranında hızlı etkili ve orta etkili insülin aspart içermektedir.
NovoMix30 Penfillsadece deri altı uygulama içindir.
NovoMix30 Penfillkarın duvarı veya uyluk bölgesine deri altına enjekte edilerek kullanılır. Eğer uygunsa kalça veya deltoid bölgeleri kullanılabilir. Lipodistrofi ve kutanöz amiloidoz riskini azaltmak için enjeksiyonlar, aynı bölge içinde olmak koşuluyla, farklı yerlere yapılmalıdır (bkz. Bölüm 4.4 ve 4.8). Değişik enjeksiyon bölgelerinin NovoMix30 Penfill'in emilimine etkisi araştırılmamıştır. Etki süresi doza, enjeksiyon bölgesine, kan akımına, ısı ve fiziksel aktivitenin derecesine bağlı olarak değişiklik gösterecektir.
NovoMix30 Penfill'in etki başlangıcı bifazik insan insülininden daha hızlıdır ve genellikle yemekten hemen önce verilmelidir. Gerekli olduğunda, NovoMix30 Penfillyemekten hemen sonra verilebilir.
Detaylı kullanıcı talimatları için, kullanma talimatına bakınız.
İnsülin enjeksiyon sistemi ile uygulama:
NovoMix30 Penfill, Novo Nordisk insülin enjeksiyon sistemleri ve NovoFineveya NovoTwistiğne uçları ile kullanılmak üzere tasarlanmıştır. NovoMix30 Penfilltekrar kullanılabilir kalem ile sadece subkütan enjeksiyon için uygundur. Eğer şırınga ile uygulama gerekli ise, bir flakon kullanılmalıdır.
Özel popülasyonlara ilişkin ek bilgiler:
Böbrek/Karaciğer yetmezliği:
Böbrek ve karaciğer yetmezlikleri hastanın insülin ihtiyacını azaltabilir.
Böbrek veya karaciğer yetmezliği olan hastalarda, glukoz gözetimi arttırılmalı ve insülin aspart dozu bireye özgü olarak ayarlanmalıdır.
Pediyatrik popülasyon:
NovoMix30 Penfillhazır karışım insülin tercih edildiğinde adolesanlarda ve 10 yaş ve üstü çocuklarda kullanılabilir. 6 ila 9 yaş arası çocuklarda NovoMix30 Penfillile klinik deneyim sınırlıdır (bkz. bölüm 5.1). 6 yaş altındaki çocuklarda NovoMix30 Penfilliçin hiçbir veri yoktur.
Geriyatrik popülasyon:
NovoMix30 Penfillyaşlı hastalarda kullanılabilir; ancak 75 yaş üstü hastalarda NovoMix30 Penfillile oral antidiyabetik ilaçların birlikte kullanımı ile ilgili deneyimler sınırlıdır. Yaşlı hastalarda glukoz gözetimi arttırılmalı ve insülin aspart dozu bireye özgü olarak ayarlanmalıdır.
4.3. Kontrendikasyonlar
İnsülin aspart veya yardımcı maddelerden herhangi birisine aşırı duyarlılık durumları (bkz. bölüm 6.1).
4.4. Özel kullanım uyarıları ve önlemleri
NovoMix30 Penfill, ciddi hipoglisemi ile sonuçlanabileceğinden damar içine uygulanmamalıdır. Kas içine uygulamadan kaçınılmalıdır. NovoMix30 Penfillinsülin infüzyon pompalarında kullanılmamalıdır.
Değişik zaman dilimleri arasında yolculuk, hastanın insülini ve öğünleri farklı zamanda almasını gerektirebileceğinden, seyahat öncesinde doktora danışılmalıdır.
Hiperglisemi
Yetersiz dozlarda kullanımı veya tedaviye ara verilmesi, özellikle tip I diyabette hiperglisemiye ve diyabetik ketoasidoza yol açabilir. Genellikle hipergliseminin ilk belirtileri saatler veya günler içinde giderek artar. Susuzluk, idrar yapma sıklığında artış, bulantı, kusma, baş dönmesi, kızarık-mor kuru deri, ağız kuruluğu, iştah kaybına ilaveten nefesin aseton kokmasını içerir. Tip I diyabette, tedavi edilmeyen hiperglisemik vakalar en sonunda diyabetik ketoasidoza yol açabilir, bu potansiyel olarak ölümcüldür.
Hipoglisemi
Bir ana öğünün atlanması veya plansız, ağır fiziksel egzersiz yapılması hipoglisemiye yol açabilir.
İnsülin dozu insülin ihtiyacına göre çok yüksekse hipoglisemi oluşabilir. Hipoglisemi durumunda veya hipoglisemiden şüphelenilirse, NovoMix30 Penfillenjekte edilmemelidir. Doz ayarlaması, hastanın kan şekeri sabitlendikten sonra düşünülmelidir (bkz. bölüm 4.2, 4.8 ve 4.9).
NovoMix30 Penfill, enjeksiyondan sonra 6 saate kadar uzayan ve bifazik insan insülinine göre daha güçlü glukoz düşürücü etkiye sahip olabilir. Bu durumun hastaya özel olarak insülin dozunun ayarlanması ve/veya yiyecek alımı ile kompanse edilmesi gerekebilir.
İntensif insülin tedavisi gibi tedavilerle kan glukoz kontrolü büyük ölçüde sağlanmış olan hastalarda alışılmış hipoglisemi uyarıcı semptomlarında değişiklik olabileceğinden hastalar bu konuda bilgilendirilmelidir. Uzun süredir diyabeti olan hastalarda genel uyarıcı semptomlar yok olabilir.
Glukoz düzeyinin sıkı kontrolü hipoglisemik olay olasılığını artırabilir ve bu yüzden bölüm
4.2'de açıklanan doz intensifikasyonu sırasında özellikle dikkatli olmak gereklidir.
NovoMix30 Penfill'in yemekler ile çok yakın zamanda uygulanması gerektiğinden, gıdaların emiliminde bir gecikme beklenebilecek başka hastalıkları olan veya başka ilaçlar kullanmakta olan hastalarda, preparatın etkisinin hızlıbaşlayabileceği dikkate alınmalıdır.
Eşlik eden başka hastalık; özellikle enfeksiyon hastalıkları ve ateş yapan durumlar genellikle hastanın insülin gereksinimini artırır. Böbrekteki, karaciğerdeki ya da böbreküstü, hipofiz veya tiroit bezlerini etkileyen hastalıklar insülin dozunda değişiklik gerektirebilir.
Hastalar değişik tipte insülinlere transfer edildiğinde, hipogliseminin erken uyarıcı semptomları önceki insülinle yaşadıklarından farklı olabilir veya daha az belirgin hale gelebilir.
Diğer insülin tıbbi ürünlerinden transfer
Hastaların yeni bir çeşit veya marka insüline transfer edilmesi sıkı bir tıbbi gözetim altında yapılmalıdır. Dozaj, marka (üretici), çeşit, orijin (hayvan insülini, insan insülini veya insülin analogu) ve/veya üretim metodundaki (hayvan kaynaklı insülin yerine rekombinant DNA) değişiklikler doz değişikliklerini gerektirebilir. NovoMix30 Penfill'e transfer edilen hastaların daha önce kullandıkları insüline göre günlük enjeksiyon sayısında artış veya dozunda değişiklik yapmaları gerekebilir. Doz ayarlaması gerektiğinde, bu bazen ilk dozda bazen de ilk birkaç hafta veya ay içinde yapılabilir.
Enjeksiyon yeri reaksiyonları
Herhangi bir insülin tedavisi sırasında ağrı, kızarıklık, ürtiker, enflamasyon, morarma, şişme ve kaşıntı gibi enjeksiyon bölgesi reaksiyonları oluşabilir. Belirli bir bölgede enjeksiyon yerinin devamlı değiştirilmesi bu reaksiyonların oluşma riskini azaltır. Reaksiyonlar genellikle birkaç gün ila birkaç haftada düzelir. Enjeksiyon yeri reaksiyonları nadiren NovoMix30 Penfill'in bırakılmasını gerektirebilir.
Deri ve deri altı doku hastalıkları
Hastalara, lipodistrofi ve kutanöz amiloidoz gelişme riskini azaltmak için enjeksiyon bölgesini sürekli rotasyona tabi tutmaları konusunda talimat verilmelidir. Bu reaksiyonların görüldüğü bölgelerde insülin enjeksiyonlarını takiben gecikmiş insülin emilimi ve kötüleşmiş glisemik kontrol riski vardır. Enjeksiyon yerinde ani değişiklik yapıp, ciltte etkilenmemiş bir bölgeye enjeksiyon yapmanın hipoglisemiye neden olduğu bildirilmiştir. Enjeksiyon yerinde etkilenen bir bölgeden etkilenmeyen bir bölgeye değişiklik yapıldıktan sonra kan şekerinin izlenmesi önerilir ve antidiyabetik ilaçların doz ayarlaması düşünülebilir.
![]()
NovoMix30 Penfillile pioglitazon kombinasyonu
Özellikle kalp yetmezliği gelişimi riski yüksek olan hastalarda, pioglitazon ile insülin kombine kullanıldığında kalp yetmezliği vakaları bildirilmiştir. Bu, pioglitazon ve NovoMix30 Penfill'in kombine tedavisi düşünüldüğünde akılda tutulmalıdır. Eğer bu kombinasyon kullanılırsa, hastalar kalp yetmezliği, kilo alımı ve ödemin semptom ve belirtileri için incelenmelidir. Pioglitazon, kardiyak semptomlarda herhangi bir kötüleşme olduğunda kesilmelidir.
Kazayla oluşan karışıklıkların/ tıbbi hataların engellenmesi
NovoMix30 Penfillile diğer insülin ürünlerinin yanlışlıkla karıştırılmasını önlemek üzere hastalara, her enjeksiyon öncesinde her zaman insülin etiketini kontrol etmeleri tavsiye edilmelidir.
İnsülin antikorları
İnsülin uygulaması insülin antikorlarının oluşmasına neden olabilir. Hiperglisemi ya da hipoglisemi eğilimini kontrol altına almak için, insülin antikorlarının varlığı nadir durumlarda insülin dozunun ayarlanmasını gerektirebilir.
Hipokalemi
İnsülin aspart dahil tüm insülin ilaçları, ekstraselülerden intraselüler boşluğa potasyum geçişine neden olarak hipokalemiye yol açar. Tedavi edilmeyen hipokalemi, solunum felcine, ventriküler aritmiye ve ölüme neden olabilir. Hipokalemi riski olan hastalarda (örn. potasyum düşürücü ilaçlar kullanan hastalar, serum potasyum konsantrasyonuna duyarlı ilaçlar alan hastalar) potasyum düzeyleri izlenmelidir.
Takip edilebilirlik
Biyoteknolojik ürünlerin takip edilebilirliğinin sağlanması için uygulanan ürünün ticari ismi ve
seri numarası mutlaka hasta dosyasına kaydedilmelidir.
Bu tıbbi ürün her “dozâ€unda 1 mmol (23 mg)'dan daha az sodyum ihtiva eder; yani aslında “sodyum içermezâ€.
4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri
Bazı ilaçların glukoz metabolizması ile etkileşime girdiği bilinmektedir. Aşağıdaki maddeler hastanın insülin ihtiyacını azaltabilir:Oral antidiyabetik ilaçlar, GLP-1 reseptör agonistleri, monoamin oksidaz inhibitörleri (MAOİ), beta blokerler, anjiyotensin dönüştürücü enzim (ADE) inhibitörleri, salisilatlar, anabolik steroidler ve sülfonamidler.
Aşağıdaki maddeler hastanın insülin ihtiyacını artırabilir:
Oral kontraseptifler, tiyazidler, glukokortikoidler, tiroit hormonları, sempatomimetikler, büyüme hormonu ve danazol.
Beta blokerler hipoglisemi semptomlarını maskeleyebilirler.
Oktreotid/ lanreotit insülin ihtiyacını hem arttırabilir hem de azaltabilir. Alkol, insülinin hipoglisemik etkisini yoğunlaştırabilir veya azaltabilir. Özel popülasyonlara ilişkin ek bilgiler
Özel popülasyonlarda etkileşimlere dair bir çalışma yürütülmemiştir.
Pediyatrik popülasyon:
Pediyatrik popülasyonda etkileşimlere dair bir çalışma yürütülmemiştir.
4.6. Gebelik ve laktasyon
Gebelik kategorisi: C
Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)
Herhangi bir bilgi bulunmamaktadır.
Gebelik dönemi
NovoMix30 Penfill'in gebe kadınlarda kullanımına ilişkin klinik çalışma sınırlıdır.
Hayvanlar üzerinde yapılan çalışmalar, gebelik /ve-veya/ embriyonal/fetal gelişim /ve-veya/ doğum /ve-veya/ doğum sonrası gelişim üzerindeki etkiler bakımından yetersizdir. İnsülin aspart ile ilgili konvansiyonel güvenlilik farmakolojisi, tekrarlayan doz toksisitesi, üreme üzerine genotoksisite ve toksisite çalışmalarına dayanan klinik olmayan veriler insanlar için hiçbir özel zarar göstermemektedir (bkz. Bölüm 5.3).
Genelde, diyabetli gebe kadınların gebelikleri süresince ve gebe kalmayı düşünenlerde kan glukozunun yoğun şekilde takip edilmesi ve kontrolü önerilmektedir. İnsülin gereksinimi genellikle gebeliğin ilk trimesterinde azalmakta ve ikinci ve üçüncü trimesterde giderek artmaktadır. Doğumdan sonra, insülin gereksinimi hızla gebelik öncesi düzeylere döner.
Laktasyon dönemi
Laktasyon döneminde NovoMix 30 Penfill tedavisi için herhangi bir kısıtlama yoktur. Emziren annelerin insülin kullanmasının bebek için hiçbir riski yoktur. Bununla birlikte NovoMix30 Penfilldozunun ayarlanması gerekebilir.
Üreme yeteneği/Fertilite
Hayvan üreme çalışmaları fertilite açısından insülin aspart ve insan insülini arasında herhangi bir fark ortaya çıkarmamıştır.
4.7. Araç ve makine kullanımı üzerindeki etkiler
Hastanın konsantre olma ve reaksiyon gösterme becerisi hipogliseminin bir sonucu olarak bozulabilir. Bu durum, bu becerilerin özel önem taşıdığı koşullarda risk oluşturabilir (örn. araba sürme veya makine kullanma).
Hastalara araba sürme veya makine kullanma esnasında hipoglisemiye girmemeleri için gerekli önlemleri almaları önerilmelidir. Bu durum özellikle hipogliseminin uyarıcı belirtilerini az olarak farkeden veya hiç farketmeyen kişiler için ya da sık sık hipoglisemi atağı geçiren hastalar için önemlidir. Bu gibi durumlarda araç veya makine kullanımının uygunluğu değerlendirilmelidir.
4.8. İstenmeyen etkiler
Güvenlilik Profilinin Özeti
NovoMix30 Penfillkullanımı sırasında hastalarda görülen advers ilaç reaksiyonları genellikle insülin aspartın farmakolojik etkilerinden dolayı görülür.
Tedavi sırasında en çok rapor edilen istenmeyen etki hipoglisemidir. Hipogliseminin sıklığı, hasta popülasyonuna, dozaja ve glisemik kontrolün seviyesine göre değişebilir, lütfen aşağıdaki “Seçilmiş istenmeyen etkilerin tanımı†bölümüne bakınız.
İnsülin tedavisinin başlangıcında kırılma anomalileri, ödem ve enjeksiyon yeri reaksiyonları (enjeksiyon yerinde ağrı, kızarıklık, ürtiker, inflamasyon, morarma, şişme ve kaşınma) oluşabilir. Bu reaksiyonlar genellikle geçici türdedir. Kan glukoz kontrolündeki hızlı iyileşme, genellikle geri dönüşümlü olan akut ağrılı nöropatiye neden olabilir. Uzun süreli gelişmiş glisemik kontrol diyabetik retinopatinin ilerleme riskini azaltırken, glisemik kontrolün ani gelişimi ile insülin terapisinin yoğunluğu, diyabetik retinopatinin geçici olarak kötüleşmesi ile bağlantılı olabilir.
Klinik çalışmalarda görülen ve insülin asparta bağlı olarak değerlendirilen advers ilaç reaksiyonlarının sıklığı aşağıda sıralanmıştır. Sıklıklar şu şekilde tanımlanmıştır:
Çok yaygın (≥1/10); yaygın (≥1/100 ila <1/10); yaygın olmayan (≥1/1.000 ila <1/100); seyrek (≥1/10.000 ila <1/1.000); çok seyrek (<1/10.000); bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Her bir sıklık gruplamasında, istenmeyen etkiler azalan ciddiyet sırasına göre sunulmaktadır.
Bağışıklık sistemi hastalıkları
Yaygın olmayan: Ürtiker, döküntü, erupsiyonlar Çok seyrek: Anafilaktik reaksiyonlar *
Metabolizma ve beslenme hastalıkları
Çok yaygın: Hipoglisemi*
Sinir sistemi hastalıkları
Seyrek: Periferal nöropati (ağrılı nöropati)
Göz hastalıkları
Yaygın olmayan: Kırılma bozuklukları, diyabetik retinopati
Deri ve deri altı doku hastalıkları Yaygın olmayan: Lipodistrofi* Bilinmiyor: Kutanöz amiloidoz*â€
Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklar
Yaygın olmayan: Ödem, enjeksiyon yeri reaksiyonları
*Bkz. bölüm “Seçilmiş istenmeyen etkilerin tanımıâ€.
†Pazarlama sonrası kaynaklardan elde edilen advers reaksiyon. Seçilmiş istenmeyen etkilerin tanımı
Anafilaktik reaksiyonlar:
Genel aşırı duyarlılık reaksiyonlarının (yaygın deri döküntüsü, kaşınma, terleme, gastrointestinal bozukluk, anjiyonoörotik ödem, nefes almada zorluk, çarpıntı ve düşük kan basıncını içeren) oluşumu çok seyrektir ancak potansiyel olarak hayatı tehdit edebilir.
Hipoglisemi:
En çok rapor edilen istenmeyen etki hipoglisemidir. Hipoglisemi, insülin dozu insülin ihtiyacına göre çok yüksekse oluşabilir. Ciddi hipoglisemi durumunda şuur kaybı ve/veya konvülziyon oluşabilir ve beyin fonksiyonlarında geçici veya kalıcı hasarla hatta ölümle sonuçlanabilir. Hipogliseminin semptomları genelde aniden belirir. Bunlar, soğuk terleme, soğuk soluk deri, yorgunluk, sinirlilik veya titreme, endişe hissi, anormal derecede yorgunluk veya bitkinlik, kafa karışıklığı, konsantrasyon güçlüğü, sersemlik, aşırı açlık hissi, görme değişiklikleri, baş ağrısı, bulantı ve çarpıntıdır.
Klinik çalışmalarda hipoglisemi sıklığı, hasta popülasyonu, dozaj ve glisemik kontrolün seviyesine göre değişmiştir. Klinik çalışmalar sırasında hipogliseminin görülme oranları, insan insülini ve insülin aspart arasında değişkenlik göstermemiştir.
Deri ve deri altı doku hastalıkları:
Lipodistrofi (lipohipertrofi, lipoatrofiyi içeren) ve kutanöz amiloidoz enjeksiyon bölgesinde oluşabilir ve lokal insülin absorpsiyonunu geciktirebilir. Belli bir alan içindeki enjeksiyon yerinin devamlı değiştirilmesi bu reaksiyonların oluşma riskini azaltabilir veya önleyebilir (bkz. Bölüm 4.4.).
Özel popülasyonlara ilişkin ek bilgiler:
Pediyatrik popülasyon:
Pazarlama sonrası kaynaklara ve klinik çalışmalara dayanarak, pediyatrik popülasyonda gözlemlenen istenmeyen etkilerin sıklığı, tipi ve ciddiyeti genel popülasyondaki kapsamlı deneyimlerden hiçbir farklılık göstermemiştir.
Diğer özel popülasyonlar:
Pazarlama sonrası kaynaklara ve klinik çalışmalara dayanarak, yaşlı hastalarda ve böbrek veya karaciğer yetmezliği olan hastalarda gözlemlenen istenmeyen etkilerin sıklığı, tipi ve ciddiyeti genel popülasyondaki kapsamlı deneyimlerden hiçbir farklılık göstermemiştir.
Şüpheli advers reaksiyonların raporlanması
Ruhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesine olanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu Türkiye Farmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr; e-posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99)
4.9. Doz aşımı ve tedavisi
İnsülin için spesifik olarak bir doz aşımı tanımlanamaz ancak hastanın ihtiyacına göre çok yüksek dozlarda verilirse birbirini takip eden evreler sonucunda hipoglisemi gelişebilir:
Hafif hipoglisemi atakları oral yoldan glukoz veya şekerli gıdalar alınarak tedavi edilebilir. Bu nedenle diyabetli hastaların beraberlerinde sürekli şekerli gıdalar bulundurmaları önerilmektedir.
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Diyabet tedavisinde kullanılan ilaçlar. Hızlı etkililer ile kombine orta ya da uzun etkili insülinler ve analogları, enjektabl.
ATC kodu: A10AD05.
NovoMix30 Penfill, % 30 çözünür insülin aspart (hızlı etkili insan insülini analogu) ve % 70 protamin- kristalize insülin aspartın (orta etkili insan insülini analogu) bifazik süspansiyonudur.
Etki mekanizması ve farmakodinamik etkiler
İnsülin aspartın kan şekerini düşürücü etkisi, insülinin kas ve yağ hücrelerindeki reseptörlere bağlanarak glukozun hücre içine girişini kolaylaştıracak molekülleri harekete geçirmesi ile ortaya çıkar ve eş zamanlı olarak karaciğerden glukoz açığa çıkmasını da inhibe eder.
NovoMix30 Penfill, %30 çözünür insülin aspart içeren bir bifazik insülindir. Çözünür insan insülinine göre etki başlangıcı hızlıdır, bu nedenle yemeğe yakın bir zamanda verilebilir (yemeğin ilk 0–10 dakikası içinde). Kristal fazı (%70) etki profili insan NPH insülinine benzeyen aktif profile sahip protamin-kristalize insülin aspart içermektedir.
NovoMix30 Penfill'in etkisi subkutan enjeksiyonunu takiben 10 ila 20 dakika içinde başlar. Maksimum etki, enjeksiyondan sonra 1-4 saat içinde elde edilir. Etki süresi 24 saat kadardır (Şekil 1).
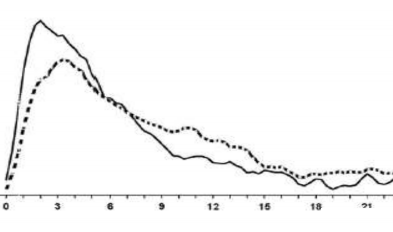
Saat
Glukoz infüzyon hızı
![]()
Şekil 1: Sağlıklı bireylerde NovoMix30 Penfill'in ( ) ve bifazik insan insülini 30'un ( )
aktivite profili
Klinik etkililik ve güvenlilik
Tip 1 ve tip 2 diyabetli hastalarda yapılan 3 aylık bir çalışmada NovoMix30 Penfillbifazik insan insülini 30 ile tedaviye kıyasla eşit glikolize hemoglobin kontrolü sağlamıştır. Molar bazda insülin aspart insan insülinine eşdeğer etkinliktedir. Bifazik insan insülini 30 ile kıyaslandığında, NovoMix30 Penfill'in kahvaltıdan ve akşam yemeğinden önce uygulanması, her iki yemekten (kahvaltı ve akşam yemeği) sonra da yemek sonrası (postprandiyal) kan şekerini düşürmüştür.
Tip 1 ve tip 2 diyabetli hastalarda gerçekleştirilen dokuz çalışmayı içeren bir meta-analizi açlık kan glukozunun NovoMix30 Penfillile tedavi edilen hastalarda bifazik insan insülini 30'a göre daha yüksek olduğunu göstermiştir.
Bir çalışmada tip 2 diyabetli 341 hasta tek başına ya da metforminle birlikte NovoMix30 Penfillya da metforminle birlikte sülfonilüre ile tedavi edilmek üzere randomize edilmiştir. 16 haftalık tedavi sonrasında birincil etkinlik değişkeni olan HbA'de metforminle kombine NovoMix30 Penfillkullanan hastalar ile metforminle kombine sülfonilüre kullananlar
arasında fark olmamıştır. Bu çalışmada hastaların %57'sinde başlangıçtaki HbA%9'un üstündeydi; bu hastalarda metforminle NovoMix 30 Penfill'in kombinasyon tedavisi metforminle sülfonilüre kombinasyonuna göre anlamlı oranda daha düşük HbAile sonuçlanmıştır.
Bir çalışmada tek başına oral hipoglisemik ajanlar ile kontrol altına alınamayan tip 2 diyabetli hastalar günde iki kez NovoMix30 Penfill(117 hasta) veya günde bir kez glarjin (116 hasta) ile tedavi edilmek üzere randomize edilmiştir. 28 haftalık tedavi sonrasında bölüm 4.2'deki doz rehberi izlendiğinde NovoMix 30 Penfill ile ortalama HbAdüşüşü %2,8 (başlangıçtaki ortalama HbA= %9,7) olmuştur. NovoMix 30 Penfill ile hastaların %66 ve %42'sinin HbA'si sırasıyla %7 ve %6,5'in altına inmiş ve ortalama APG (açlık plazma glukozu) yaklaşık 7 mmol/l azalmıştır (başlangıç düzeyi olan 14,0 mmol/l'den 7,1 mmol/l'e).
Tip 2 diyabetli hastalarda bir meta analizi, toplam noktürnal hipoglisemik ataklar ve majör hipoglisemi riskinin bifazik insan insülini 30'a göre NovoMix30 Penfillile daha düşük olduğunu göstermiştir. Günlük toplam hipoglisemik atak riski, NovoMix30 Penfillile tedavi edilen hastalarda artmıştır.
Pediyatrik popülasyon
10 ila 18 yaşları arasında 167 hastada yemek öncesi NovoMix30 Penfillile yemek öncesi insan insülini/bifazik insan insülini 30 ve gece yatarken uygulanan NPH insülinin postprandiyal glisemik kontrollerini karşılaştıran 16 haftalık bir klinik çalışma yapılmıştır. Her iki tedavi grubunda da tedavi boyunca ortalama HbAbaşlangıca göre benzer düzeyde kaldı ve NovoMix30 Penfillveya bifazik insan insülini 30 ile görülen hipoglisemi oranları arasında fark yoktu.
Daha küçük (54 hasta) ve daha genç yaştaki (yaş aralığı 6 ila 12) bir popülasyonda yapılan çift-kör, çaprazlamalı (her bir tedavi 12 hafta sürmek üzere) çalışmada NovoMix30 Penfillkullananlarda hipoglisemik atakların oranı ve postprandiyal glukoz yükselmelerinin oranı bifazik insan insülini 30 kullananlara kıyasla NovoMix30 Penfillile belirgin biçimde daha düşüktü. Bifazik insan insülini 30 alan grupta çalışma sonu HbA, NovoMix 30 Penfill alan gruba göre belirgin biçimde daha düşüktü.
5.2. Farmakokinetik özellikler
Genel özelliklerÇözünür insan insülini ile kıyaslandığı zaman, insülin aspartta B28 pozisyonundaki aspartik asit ile prolin amino asidinin yer değiştirmesi, hekzamer oluşum eğilimini azaltmaktadır.
Emilim:
NovoMix30 Penfill'in çözünür fazı olan insülin aspart, total insülinin %30'unu oluşturmaktadır. İnsülin aspart, deri altı dokusundan bifazik insan insülininin çözünür insülin komponentinden daha hızlı emilir. Geri kalan %70'lik kısmı kristal form olan protamin- kristalize insülin asparttan oluşur. İnsülin aspart protamin, insan NPH insülinine benzer uzamış emilim profiline sahiptir.
NovoMix30 Penfillile maksimum serum insülin konsantrasyonu bifazik insan insülini 30'a göre ortalamada %50 daha yüksektir. Maksimum konsantrasyona ulaşma süresi ortalamada bifazik insan insülini 30'un ortalama yarısıdır.
Dağılım:
Sağlıklı gönüllülerde 140±32 pmol/l'lik bir ortalama maksimum serum konsantrasyonuna 0,20 ünite/kg (vücut ağırlığı) subkütan doz uygulamasından dan yaklaşık 60 dakika sonra ulaşılır.
Biyotransformasyon:
İnsülin aspartın bozunması insan insülinine benzer, oluşan tüm metabolitleri inaktiftir.
Eliminasyon:
NovoMix30 Penfill'in protamine bağlı kısmının emilim hızını gösteren ortalama yarılanma ömrü yaklaşık 8-9 saattir. Subkutan dozdan 15-18 saat sonra serum insülin düzeyleri başlangıçtaki değerlerine döner. Tip 2 diyabetli hastalarda dozdan yaklaşık 95 dakika sonra maksimum konsantrasyona ulaşılır ve uygulanan dozdan en az 14 saat sonra sıfırın üstünde konsantrasyonlar ölçülmüştür.
Hastalardaki karakteristik özellikler
Pediyatrik popülasyon:
NovoMix30 Penfill'in farmakokinetiği çocuklarda veya adolesanlarda araştırılmamıştır. Ancak çözünür insülin aspartın farmakodinamik ve farmakokinetik özellikleri tip 1 diyabetli çocuklarda (6-12 yaş) ve adolesanlarda (13-17 yaş) araştırılmıştır. İnsülin aspart her iki yaş grubunda da erişkinlerdeki t'a benzer şekilde hızla emilmiştir. Ancak, Cinsülin aspartın bireysel titrasyonunun önemini işaret edecek şekilde yaş grupları arasında farklılıklar göstermiştir.
NovoMix30 Penfill'in farmakokinetiği yaşlılarda veya böbrek veya karaciğer fonksiyon bozukluğu olan hastalarda araştırılmamıştır.
5.3. Klinik öncesi güvenlilik verileri
İnsülin aspart ile ilgili konvansiyonel güvenlilik farmakolojisi, tekrarlayan doz toksisitesi, üreme üzerine genotoksisite ve toksisite çalışmalarına dayanan klinik olmayan veriler insanlar için hiçbir özel zarar göstermemektedir.
İnsülin ve IGF-1 reseptör bölgelerine bağlanma ve hücre büyümesi üzerine olan etkileri de dahil olmak üzere in vitro testlerde insülin aspartın insan insülinine benzer bir şekilde davranış gösterdiği belirlenmiştir. Çalışmalar aynı zamanda, insülin aspartın insülin reseptörüne bağlanmasındaki ayrılığın insan insülinine eşdeğer olduğunu göstermiştir.
6. FARMASÖTİK ÖZELLİKLER
6.1. Yardımcı maddelerin listesi
Gliserol Fenol Metakrezol Çinko klorür
Sodyum klorür Disodyum fosfat dihidrat
Protamin sülfat (somon balığından elde edilir) Sodyum hidroksit (pH ayarı için)
Hidroklorik asit (pH ayarı için) Enjeksiyonluk su
6.2. Geçimsizlikler
Geçimlilikle ilgili çalışmalar olmadığından, bu tıbbi ürün diğer tıbbi ürünlerle karıştırılmamalıdır.
6.3. Raf ömrü
Açılmadan önce: 24 ay.
Kullanım sırasında veya yedek olarak taşınırken: En fazla 4 hafta içinde tüketilmelidir.
6.4. Saklamaya yönelik özel tedbirler
Açılmadan önce: Buzdolabında dondurucu kısımdan uzakta (2°C - 8°C) saklanmalıdır. Dondurulmamalıdır.
Kullanım sırasında veya yedek olarak taşınırken: 30°C'nin altında saklanmalıdır. Buzdolabında saklanmamalıdır. Dondurulmamalıdır.
Işıktan korumak için kartuşlar kutusunda saklanmalıdır.
6.5. Ambalajın niteliği ve içeriği
Bir piston (bromobutil) ve bir lastik kapak (bromobutil/poliizopren) ile kapatılmış kartuş (Tip 1 cam) içinde 3 mL süspansiyon. Kartuşun içinde süspansiyonun karışmasını kolaylaştıran bir cam top bulunur.
Paketlerde 5 adet (3 mL) kartuş bulunur.
6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
Kullanılmamış olan ürünler ya da atık maddeler “Tıbbi Atıkların Kontrolü Yönetmeliği†ve “Ambalaj Atıklarının Kontrolü Yönetmeliği†gereklerine uygun olarak imha edilmelidir.
NovoMix30 Penfillbuzdolabından çıkarıldıktan sonra, insülin ilk kez kullanılacağı zaman tarif edildiği biçimde, karıştırılmadan önce NovoMix30 Penfill'in oda sıcaklığına ulaşması beklenmelidir.
Karıştırılan sıvının eşit oranda beyaz, bulanık ve sulu olmadığı fark edilirse bu tıbbi ürün kullanılmamalıdır.
Kullanmadan hemen önce NovoMix30 Penfillsüspansiyonunun iyice karıştırılmasının gerektiği hastalara özellikle vurgulanmalıdır.
Donmuş NovoMix30 Penfillkullanılmamalıdır.
Hastalar, her enjeksiyon sonrası iğne ucunu atmaları konusunda uyarılmalıdır.
NovoMix 30 Penfill ve iğne uçları yalnız bir kişinin kullanımı içindir. Kartuş yeniden doldurulmamalıdır.
 Diyabet Hastalığı
Diyabet, insülin hormonu ile ilgili problemlerden kaynaklanan bir hastalıktır.
Diyabet Hastalığı
Diyabet, insülin hormonu ile ilgili problemlerden kaynaklanan bir hastalıktır. |
 Artrit
Artrit, oldukça yaygın bir hastalıktır ancak iyi anlaşılamamıştır. Aslında “artrit” tek bir hastalığın adı değildir; eklem ağrısı veya eklem hastalıklarını adlandırmanın gayri resmi yoludur.
Artrit
Artrit, oldukça yaygın bir hastalıktır ancak iyi anlaşılamamıştır. Aslında “artrit” tek bir hastalığın adı değildir; eklem ağrısı veya eklem hastalıklarını adlandırmanın gayri resmi yoludur. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| HUMULIN-M | 8699673954172 | 808.60TL |
| MIXTARD | 8699676770472 | |
| NOVOMIX | 8699676950706 | 1,050.63TL |
| NOVORAPID | 8699676770656 | 464.17TL |
| Diğer Eşdeğer İlaçlar |
 |
Diyabet Hastalığı Diyabet, insülin hormonu ile ilgili problemlerden kaynaklanan bir hastalıktır. |
 |
Belsoğukluğu, Chlamydia ve Frengi Belsoğukluğu, bakterilerin sebep olduğu bir enfeksiyondur. Cinsel ilişki yoluyla bulaşır ve dölyatağı boynunda, idrar yollarında, anüste, makatta ve boğazda enfeksyona sebep olabilir. |
 |
Kalp Krizi Kalbe giden kan akışı durduğunda kalp krizi meydana gelir. |
İLAÇ GENEL BİLGİLERİ
Novo Nordisk Sağlık Ürünleri Tic. Ltd. Şti.
| Geri Ödeme Kodu | A05566 |
| Satış Fiyatı | 825.55 TL [ 25 Apr 2025 ] |
| Önceki Satış Fiyatı | 825.55 TL [ 18 Apr 2025 ] |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8699676950690 |
| Etkin Madde | Insulin Aspart |
| ATC Kodu | A10AD30 |
| Birim Miktar | 100 |
| Birim Cinsi | IU |
| Ambalaj Miktarı | 5 |
| Sindirim Sistemi ve Metabolizma > İnsülinler ve Analogları > Insulin aspart |
| İthal ( ref. ülke : Yunanistan ) ve Beşeri bir ilaçdır. |