ONEPTUS 97 mg/103 mg 56 film kaplı tablet Farmakolojik Özellikler
{ Sakubitril + Valsartan }
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Kardiyovasküler sistem
Farmakoterapötik grup: Renin-anjiyotensin sistemi üzerinde etki eden ajanlar; anjiyotensin II
reseptör blokerleri (ARB'ler) ve kombine formları, valsartan ve sakubitril
ATC kodu: C09DX04
Etki mekanizması
ONEPTUS, eşzamanlı olarak bir anjiyotensin reseptörü olan neprilisini (nötral endopeptidaz; NEP) ön ilaç sakubitrilin aktif metaboliti olan LBQ657 yoluyla inhibe etmek ve anjiyotensin II tip 1 (AT1) reseptörünü valsartan ile bloke etmek suretiyle anjiyotensin reseptörü neprilisin inhibitörü etki mekanizması sergiler. ONEPTUS'un kalp yetersizliği olan hastalardaki tamamlayıcı kardiyovasküler faydaları natriüretik peptidler (NP) gibi, neprilisin tarafından parçalanan peptidlerin LBQ657 tarafından korunmasına ve eşzamanlı olarak anjiyotensin II'nin zararlı etkilerinin valsartan tarafından inhibisyonuna bağlanmaktadır. NP'ler etkilerini membrana bağlanan guanilil siklaza bağlı reseptörü aktive ederek gösterir ve bunun
sonucunda ikincil mesajcı siklik guanozin monofosfat (cGMP) konsantrasyonlarını artırarak ve bu şekilde vazodilatasyonu, natriürezi ve diürezi, artmış glomerüler filtrasyon hızını ve renal kan akışını, renin ve aldosteron salımının inhibisyonunu, sempatik aktivitenin azalmasını ve anti-hipertrofik ve anti-fibrotik etkilerin azalmasını destekleyerek gösterir.
Valsartan, AT1 reseptörünü selektif olarak bloke ederek anjiyotensin II'nin zararlı kardiyovasküler ve renal etkilerini inhibe eder ve ayrıca anjiyotensin II'ye bağımlı aldosteron salımını da inhibe eder. Bu sayede vasokonstiksiyona, renal sodyum ve sıvı tutulumuna, hücre büyümesi ve proliferasyonunun aktivasyonuna ve buna bağlı maladaptif kardiyovasküler remodelling neden olacak renin-anjiyotensin-aldosteron sisteminin sürekli aktivasyonu önlenir.
Farmakodinamik etkiler:
ONEPTUS'un farmakodinamik etkileri sağlıklı gönüllülerde ve kalp yetersizliği olan hastalarda tek ve çoklu doz uygulamalarından sonra değerlendirilmiştir ve eşzamanlı neprilisin inhibisyonu ve RAAS blokajı ile uyumludur. Ejeksiyon fraksiyonu azalmış (DEF- KY: Düşük ejeksiyon fraksiyonlu kalp yetersizliği) hastalarda valsartan kontrollü 7 günlük bir çalışmada, valsartan ile karşılaştırıldığında ONEPTUS uygulaması, natriürezde anlamlı fakat sürekli olmayan artış, idrar cGMP değerinde artış ve plazma MR-proANP (orta bölge pro- atriyal natriüretik peptid) ve NT-proBNP (N terminal prohormon beyin natriüretik peptid) değerlerinde azalma ile sonuçlanmıştır. DEF-KY hastalarındaki 21 günlük bir çalışmada ONEPTUS, başlangıç değerlerine göre idrar ANP (atriyal natriüretik peptid) ve cGMP ile plazma cGMP değerini anlamlı düzeyde artırmış; plazma NT-proBNP, aldosteron ve endotelin-1 düzeylerini düşürmüştür. ONEPTUS ayrıca plazma renin aktivitesindeki ve plazma renin konsantrasyonlarındaki artıştan anlaşıldığı üzere AT1-reseptörünü bloke etmiştir. PARADIGM-HF çalışmasında, ONEPTUS, enalapril ile karşılaştırıldığında, plazma NT-proBNP değerini düşürmüş ve plazma BNP ve idrar cGMP değerlerini yükseltmiştir. BNP bir neprilisin substratı iken, NT-proBNP neprilisin substratı değildir. Bu nedenle, ONEPTUS ile tedavi edilen kalp yetersizliği hastalarının izleminde NT-proBNP uygun bir biyolojik belirteçtir (BNP değildir).
LVEF ≥ %45 olan kalp yetersizliği olan hastalarda günde iki kez 97/103 mg ONEPTUS (n=149) ile 160 mg valsartanı (n=152) karşılaştıran randomize, çift kör, 36 haftalık bir çalışma olan PARAMOUNT'ta 12. haftada ONEPTUS, NT-proBNP'yi %17 azaltırken valsartan, NT- proBNP'yi %8 artırmıştır (p = 0,005).
PARAGON-HF'de ONEPTUS NT-proBNP'yi %24 (16. Hafta) ve %19 (48. Hafta) oranında azaltırken bu değerler valsartan ile sırasıyla %6 ve %3 olmuştur.
QT Uzaması: Sağlıklı erkek gönüllülerde yürütülen detaylı bir QTc klinik çalışmasında tek doz olarak uygulanan 194 mg sakubitril / 206 mg valsartan ve 583 mg sakubitril / 617 mg valsartan ONEPTUS'un kardiyak repolarizasyon üzerinde herhangi bir etkisi olmamıştır.
Neprilisin, amiloid-β'nin (Aβ) beyin ve beyin-omurilik sıvısından (BOS) temizlenmesinde rolü olan çok sayıda enzimden biridir. Sağlıklı gönüllülere 2 hafta süreyle ONEPTUS'un günde bir kez 194 mg sakubitril / 206 mg valsartan dozunda uygulanması, plasebo ile karşılaştırıldığında BOS Aβ 1-38 değerinde artış ile ilişkilendirilmiştir; BOS Aβ 1-40 ve 1-42 konsantrasyonlarında herhangi bir değişiklik olmamıştır. Bu bulgunun klinik anlamı bilinmemektedir (bkz. bölüm 5.3).
Kan Basıncı: Hipertansiyonlu hastalarda kararlı durumda ONEPTUS'a 50 mg tek doz sildenafil eklenmesi (5 gün boyunca günde bir kez 194 mg sakubitril/206 mg valsartan), tek başına ONEPTUS uygulamasına kıyasla, ilave kan basıncı (KB) düşüşü (~5/4 mmHg, sistolik/diyastolik KB) ile ilişkilendirilmiştir.
ONEPTUS'un birlikte uygulanması, intravenöz nitrogliserinin BP etkisini önemli ölçüde değiştirmemiştir.
Klinik etkililik ve güvenlilik:
PARADIGM-HF (enalaprile karşı) ve PARAGON-HF (valsartana karşı) klinik çalışmalarında toplam 6.622 kalp yetersizliği hastası ONEPTUS ile tedavi edilmiştir. Bunlardan 5.085'inde maruziyet süresi en az 1 yıl olmuştur.
PARADIGM-HF
PARADIGM-HF, 8.442 hastayı içeren çok uluslu, randomize, çift kör bir çalışma olup NYHA sınıf II – IV kronik kalp yetersizliği ve sistolik disfonksiyonu (sol ventriküler ejeksiyon fraksiyonu ≤%40; daha sonra ≤%35 olarak düzeltilmiştir) olan hastalara, her ikisi de başka kalp yetersizliği tedavilerine ek olarak verilen ONEPTUS ile enalaprili karşılaştırmıştır. Birincil birleşik sonlanım noktası kardiyovasküler ölüm veya kalp yetersizliği sebebiyle hastaneye yatış olmuştur. SKB değeri <100 mmHg, şiddetli böbrek bozukluğu (eGFR <30 ml/dk/1,73 m2) ve şiddetli karaciğer bozukluğu olan hastalar tarama sırasında çalışmadan hariç tutulmuş dolayısıyla prospektif olarak incelenmemişlerdir.
Çalışmaya katılmadan önce hastalar, ADE inhibitörleri/ARB'leri (>%99), beta-blokerleri (%94), mineralokortikoid antagonistlerini (%58) ve diüretikleri (%82) içeren standart tedaviler ile iyi düzeyde tedavi edilmiştir. Medyan takip süresi 27 ay olup hastalar 4,3 yıla varan sürelerle tedavi edilmiştir.
Hastaların mevcut ADE inhibitörü veya ARB tedavilerini bırakmaları gerekmiştir ve hastalar,
günde iki kez 10 mg enalapril, daha sonra günde iki kez 100 mg ve ardından günde iki kez
200 mg'a artırılan ONEPTUS ile tedavi edildikleri ardışık, tek kör alıştırma fazına girmişlerdir (bu dönemde çalışmadan ayrılmalar için bkz. bölüm 4.8). Hastalar daha sonra günde iki kez ONEPTUS 200 mg (n=4.209) veya enalapril 10 mg (n=4.233) alacakları çift kör fazına randomize edilmiştir.
İncelenen popülasyonun ortalama yaşı 64 olup %19'u 75 yaş ve üzeridir. Randomize edildikleri tarihte hastaların %70'i NYHA Sınıf II ve %24'ü Sınıf II-I ve %0,7'si IV'tür Ortalama sol ventrikül ejeksiyon fraksiyonu %29 olup 963 (%11,4) hastanın sol ventrikül ejeksiyon fraksiyonu >%35 ve ≤%40'tır.
ONEPTUS grubunda hastaların %76'sı çalışmanın sonunda hedef doz olan günde iki kez 200 mg dozunda kalmıştır (ortalama günlük doz 375 mg). Enalapril grubunda hastaların %75'i çalışmanın sonunda hedef doz olan günde iki kez 10 mg dozunda kalmıştır (ortalama günlük doz 18,9 mg).
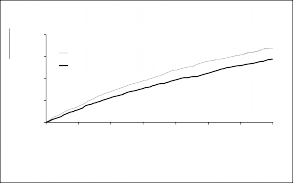
ONEPTUS, kardiyovasküler ölüm riskini veya kalp yetersizliğine bağlı hastaneye yatışları
%21,8'e indirmiş ve enalaprile göre üstün (enalapril için %26,5) bulunmuştur. Mutlak risk azalması birleşik KV ölüm veya kalp yetersizliğine bağlı hastaneye yatış sonlanımı için %4,7, tek başına KV ölüm için %3,1 ve tek başına kalp yetersizliğine bağlı hastaneye yatış için %2,8 olmuştur. Rölatif risk azalması enalapril karşısında %20 olmuştur (bkz. Tablo 1). Bu etki erken dönemde görülmüş ve çalışma boyunca devam etmiştir (bkz. Şekil 1). Her iki bileşen risk azalmasına katkıda bulunmuştur (bkz.Tablo 1).Ani ölüm, kardiyovasküler ölümlerin
%45'ini oluşturmuştur ve enalapril ile tedavi edilen hastalar ile karşılaştırıldığında ONEPTUS ile tedavi edilen hastalarda %20 oranında düşmüştür (HR 0,80, p= 0,0082). Pompa yetmezliği, kardiyovasküler ölümlerin %26'sından sorumlu olmuştur ve enalapril ile tedavi edilen hastalar ile karşılaştırıldığında ONEPTUS ile tedavi edilen hastalarda %21 oranında azaltılmıştır (HR 0,79, p = 0,0338).
Yaş, cinsiyet, ırk, coğrafi bölge, NYHA sınıfı (II/III), ejeksiyon fraksiyonu, böbrek fonksiyonu, diyabet veya hipertansiyon öyküsü, kalp yetersizliği öyküsü ve atriyal fibrilasyonu içeren farklı alt gruplarda riskte tutarlı azalma gözlenmiştir.
ONEPTUS, tüm nedenlere bağlı mortalitede %2,8'lik anlamlı azalma ile sağkalımı iyileştirmiştir (ONEPTUS %17, enalapril %19,8). ONEPTUS ayrıca enalaprile kıyasla tüm nedenlere bağlı mortaliteyi %16 oranında azaltmıştır.
Tablo 1 Birincil birleşik sonlanım noktası, bileşenleri ve tüm nedenlere bağlı
mortalite için tedavi etkisi
| ONEPTUS N = 4187 n (%) | Enalapril N = 4212 n (%) | Tehlike oranı (%95 GA) | Bağıl risk azalması | p değeri |
Kardiyovasküler ölüm ve kalp yetersizliğine bağlı hastaneye yatıştan oluşan birincil kompozit sonlanım noktası * | 914 (21,83) | 1117 (26,52) | 0,80 (0,73, 0,87) | %20 | 0,0000002 |
Birincil sonlanım noktasının ayrı bileşenleri | |||||
Kardiyovasküler | 558 (13,33) | 693 (16,45) | 0,80 (0,71, | %20 | 0,00004 |
ölüm ** |
|
| 0,89) |
|
|
Kalp yetersizliğine | 537 (12,83) | 658 (15,62) | 0,79 (0,71, | %21 | 0,00004 |
bağlı ilk hastaneye |
|
| 0,89) |
|
|
yatış |
|
|
|
|
|
İkincil sonlanım noktası | |||||
Tüm nedenlere | 711 (16,98) | 835 (19,82) | 0,84 (0,76, | %16 | 0,0005 |
bağlı mortalite |
|
| 0,93) |
|
|
*Birincil sonlanım noktası, ilk olaya kadar geçen süre olarak tanımlanmıştır.
** KV ölüm, önceden hastane yatıp yatmaması fark etmeksizin veri kesme tarihine kadar ölen tüm hastaları içerir
*** Tek yönlü p değeri
Şekil 1 Birincil birleşik sonlanım noktası ve kardiyovasküler ölüm bileşeni için Kaplan-Meier eğrileri

TITRATION
TITRATION, önceden ADE inhibitörü veya ARB tedavisi görmemiş ya da çeşitli dozlarda ADE inhibitörleri veya ARB'ler ile tedavi edilmiş, kronik kalp yetersizliği (NYHA sınıf II – IV) ve sistolik disfonksiyonu (sol ventriküler ejeksiyon fraksiyonu ≤%35) olan 538 hasta ile gerçekleştirilmiş olan 12 haftalık bir güvenlilik ve tolerabilite çalışmasıdır. Hastalara günde iki kez ONEPTUS 50 mg başlanmış, dozları günde iki kez 100 mg'a ve ardından hedef doz olan günde iki kez 200 mg'a yükseltilmiştir (3 veya 6 haftalık rejim ile).
Toplamda hastaların %76'sı ONEPTUS'un günde iki kez 200 mg'lık hedef dozuna ulaşmıştır ve 12 haftalık dönemde doza ara verilmeden veya dozda azaltma yapılmadan bu dozda kalmıştır. Önceden ADE inhibitörü veya ARB tedavisi görmemiş veya düşük dozla (<10 mg enalapril/güne eşdeğer) tedavi edilmiş hastalardan, 3 haftalık rejimle karşılaştırıldığında, 6 haftalık rejimle doz titrasyonu yapılanların daha büyük bölümü (sırasıyla %73,6 ve %84,8) ONEPTUS 200 mg dozuna ulaşabilmiş ve bu dozda kalabilmiştir.
PARAGON-HF
PARAGON-HF, sol ventrikül ejeksiyon fraksiyonu ≥ %45, semptomatik kalp yetersizliği ve yapısal kalp hastalığı [ya sol atriyal genişleme (LAE) ya da sol ventrikül hipertrofisi (LVH)] olan 4.796 erişkin hastada ONEPTUS ile valsartanı karşılaştıran çok merkezli, randomize, çift kör bir çalışmadır. Tarama sırasında sistolik kan basıncı <110 mmHg olan hastalar ve önceden herhangi bir ekokardiyografik LVEF'si <%40 olan hastalar çalışma dışı bırakılmıştır.
PARAGON-HF'nin birincil amacı, ONEPTUS'un toplam (ilk ve tekrarlayan) kalp yetersizliği (HF) nedenli hastaneye yatışları ve kardiyovasküler (CV) ölümden oluşan bileşik sonlanım noktası oranını azaltıp azaltmadığını belirlemek olmuştur.
Mevcut ADE inhibitörü veya ARB tedavisini bıraktıktan sonra hastalar, günde iki kez 80 mg valsartan ve ardından günde iki kez 100 mg ONEPTUS aldıkları sıralı tek kör alıştırma dönemlerine girmişlerdir. Önceden düşük dozlarda ADEi veya ARB alan hastalar, 1-2 hafta boyunca günde iki kez 40 mg valsartan alan alıştırma dönemine başlamıştır. Sıralı alıştırma dönemlerini başarıyla tamamlayan hastalar, günde iki kez ONEPTUS 200 mg (N = 2.419) veya günde iki kez 160 mg valsartan (N = 2.403) almak üzere randomize edilmiştir. Ortanca takip süresi 35 ay olup hastalar 4,7 yıla kadar tedavi edilmiştir.
Popülasyon %81 Kafkas, %13 Asyalı ve %2 Siyahtır; ortalama yaş 73 olup %52'si kadındır. Randomizasyonda, hastaların %77'si NYHA Sınıf II, %19'u NYHA Sınıf III ve %0,4'ü NYHA Sınıf IV'tür. Ortanca sol ventrikül ejeksiyon fraksiyonu %57'dir. Kalp yetersizliğinin altta yatan nedeni, hastaların %36'sında iskemik etiyolojidir. Ayrıca, %96'sında hipertansiyon öyküsü, %23'ünde miyokard enfarktüsü öyküsü, %46'sında eGFR <60 mL/dk/1,73 m2 ve
%43'ünde diyabet vardır. Hastaların çoğunun beta bloker (%80) ve diüretik (%95) almakta
olduğu belirlenmiştir.
PARAGON-HF, orantılı oranlar modelinin (oran oranı [RR] % 95 GA [0,75, 1,01], p = 0,06) kullanıldığı bir analize dayalı olarak, ONEPTUS'un toplam (ilk ve tekrarlayan) KY hastaneye yatışları ve KV ölüm bileşik son noktası oranında sayısal bir azalmaya sahip olduğunu göstermiştir (Tablo 2'ye bakınız). Tedavi etkisi öncelikle ONEPTUS'a randomize edilen hastalarda KY hastaneye yatışları (RR 0,85; %95 GA [0,72, 1,00]) toplam sayısında azalma eşlik etmiştir.
Tablo 2: PARAGON-HF'de Birincil Bileşik Sonlanım Noktası ve Bileşenleri için Tedavi
Etkisi
| ONEPTUS N = 2.407 | Valsartan N = 2.389 | Etki Boyutu (%95 GA) | ||
Etkililik Sonlanım Noktaları | N | Olay Oranı | N | Olay Oranı |
|
Toplam (ilk ve tekrarlayan) KY nedenli hastaneye yatışlar ve KV ölümlerin bileşimi | 894 | 12,8 | 1.009 | 14,6 | RR = 0,87 (0,75, 1,01) p- değeri 0,06 |
Toplam KY Nedenli Hastaneye Yatış Sayısı | 690 | 9,9 | 797 | 11,6 | RR = 0,85 (0,72, 1,00) |
KV Ölüm | 204 | 2,9 | 212 | 3,1 | HR = 0,95 (0,79, 1,16) |
Kısaltmalar: RR = oran oranı, HR = tehlike oranı.
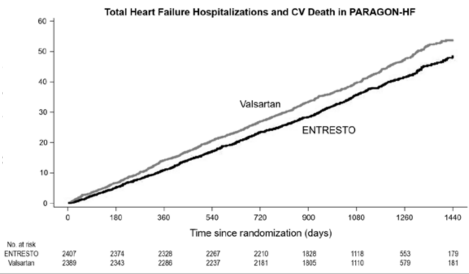
ONEPTUS
Şekil 2'de, zaman içinde toplam KY hastaneye yatışların ve KV ölümlerden oluşan bileşik sonlanım noktası olaylarının ortalama sayısı gösterilmektedir.
Bileşik Sonlanım Noktası için Zaman İçinde Ortalama Olay Sayısı
Çok çeşitli demografik özellikler, başlangıç hastalık özellikleri ve başlangıçtaki eşzamanlı ilaçlar, sonuçlar üzerindeki etkileri açısından incelenmiştir (Şekil 3).
Şekil 3: Toplam KV Nedenli Hastaneye Yatışlar ve KV Ölümlerden Oluşan Birincil Bileşik Sonlanım Noktası - Alt Grup Analizi (PARAGON-HF)
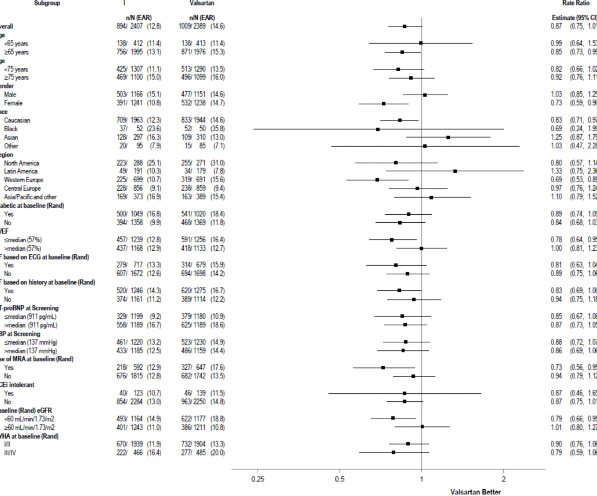
Not: Yukarıdaki şekil, tümü başlangıç karakteristikleri olan çeşitli alt gruplardaki etkileri göstermektedir. Gösterilen %95 güven sınırlarında, yapılan karşılaştırmaların sayısı hesaba katılmamaktadır ve diğer tüm faktörler için düzeltme yapıldıktan sonra belirli bir faktörün etkisini yansıtmayabilir
LVEF ile PARADIGM-HF ve PARAGON-HF'deki sonuç arasındaki ilişkinin bir analizinde, ONEPTUS ile tedavi edilen LVEF normalin altında olan hastalarda daha fazla risk azalması görülmüştür (Şekil 4).
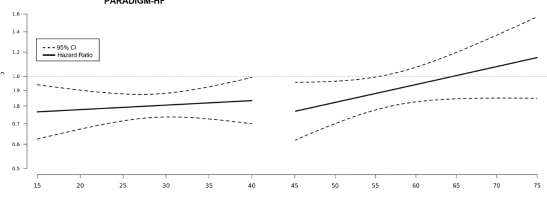
PARADIGM-HF
PARAGON-HF
Taramada sol ventriküler ejeksiyon fraksiyonu (%)
Şekil 4: PARADIGM-HF ve PARAGON-HF'de İlk KY Nedenli Yatış veya LVEF Nedenli KV Ölüme kadar geçen Sürenin Birincil Bileşik Sonlanım Noktası için Tedavi Etkisi
Laboratuvar Anormallikleri
Hemoglobin ve Hematokrit
PARADIGM-HF'de çift kör dönem sırasında hem ONEPTUS hem de enalapril ile tedavi edilen hastaların yaklaşık %5'inde hemoglobin/hematokritte > %20'lik düşüşler gözlenmiştir. PARAGON-HF'de çift kör dönem sırasında ONEPTUS ile tedavi edilen hastaların yaklaşık
%7'sinde ve valsartan ile tedavi edilen hastaların yaklaşık %9'unda hemoglobin/hematokritte
> %20'lik düşüşler gözlenmiştir.
Serum kreatinin
PARADIGM-HF'de çift kör dönem sırasında, hem ONEPTUS hem de enalapril ile tedavi edilen hastaların yaklaşık %16'sında serum kreatininde >%50'lik artışlar olmuştur. PARAGON-HF'de çift kör dönem sırasında, ONEPTUS ile tedavi edilen hastaların yaklaşık
%17'si ve valsartan ile tedavi edilen hastaların yaklaşık %21'inde serum kreatininde >
%50'lik artışlar olmuştur.
Serum Potasyum
PARADIGM-HF'nin çift kör dönemi sırasında, hem ONEPTUS hem de enalapril ile tedavi edilen hastaların yaklaşık %16'sında potasyum konsantrasyonları > 5,5 mEq/L olmuştur. PARAGON-HF'nin çift kör dönemi sırasında, ONEPTUS ile tedavi edilen hastaların yaklaşık
%18'inde ve valsartan ile tedavi edilen hastaların %20'sinde potasyum konsantrasyonları > 5,5 mEq/L olmuştur.
Pediyatrik popülasyon:
Avrupa İlaç Ajansı (EMA), kalp yetersizliği tedavisinde pediyatrik popülasyonun bir veya daha fazla alt kümesinde çalışmaların sonuçlarının sunulma gerekliliğini iptal etmiştir (pediyatrik kullanım ile ilgili bilgi için bkz. bölüm 4.2).
5.2. Farmakokinetik özellikler
Genel özelliklerONEPTUS formülasyonunda yer alan valsartanın biyoyararlanımı, piyasada bulunan diğer
tablet formülasyonlarına kıyasla daha fazladır; ONEPTUS içindeki 26 mg, 51 mg ve 103 mg valsartan, başka tablet formülasyonlarında sırasıyla 40 mg, 80 mg ve 160 mg'a eşdeğerdir.
Emilim:
Oral uygulama sonrasında, ONEPTUS, ön ilaç sakubitril ve valsartan şeklinde ayrışır. Sakubitril ve valsartanın oral mutlak biyoyararlanımı sırasıyla ≥%60 ve %23 şeklinde hesaplanmaktadır. Sakubitril aktif metaboliti LBQ657'ye metabolize olur. Bu metabolitler maksimum plazma konsantrasyonuna sırasıyla 2, 1 ve 2 saatte ulaşır.
ONEPTUS'un günde iki kez uygulanmasının ardından sakubitril, LBQ657 ve valsartanın kararlı durum düzeylerine 3 gün içinde ulaşılır. Kararlı durumda, sakubitril ve valsartan önemli düzeyde birikmezken LBQ657 1,6 kat birikme gösterir. ONEPTUS'un yiyecek ile birlikte uygulanmasının sakubitril, LBQ657 ve valsartanın sistemik maruziyetleri üzerinde klinik olarak anlamlı bir etkisi bulunmamaktadır. ONEPTUS aç veya tok karnına uygulanabilir.
Dağılım:
ONEPTUS, plazma proteinlerine yüksek oranda bağlanır (%94-%97). Plazma ve BOS maruziyetleri arasındaki karşılaştırmaya göre, LBQ657 kan beyin bariyerini sınırlı oranda (%0,28) geçer. Valsartan ve sakubitrilin ortalama görünür dağılım hacmi sırasıyla 75 L ila 103 L'dir.
Biyotransformasyon:
Sakubitril karboksilesteraz lb ve lc'ler tarafından LBQ657'ye kolaylıkla dönüştürülür; LBQ657 önemli düzeyde başka bir metabolizasyona uğramaz. Valsartan minimal düzeyde metabolize olur; dozun sadece %20'si metabolitler şeklinde tespit edilir. Plazmada düşük düzeylerde (<%10) bir hidroksil metaboliti tanımlanmıştır.
Sakubitril ve valsartanın CYP450 enziminin aracılık ettiği metabolizmaları minimal düzeyde olduğundan, CYP450 enzimlerini etkileyen ilaçlarla bir arada uygulamanın farmakokinetiği etkilemesi beklenmez.
İn vitro metabolizma çalışmaları, CYP450 bazlı ilaç etkileşimleri potansiyelinin düşük olduğuna işaret etmektedir zira ONEPTUS'un CYP450 enzimleri ile metabolizması sınırlıdır. ONEPTUS CYP450 enzimlerini indüklemez veya inhibe etmez.
Eliminasyon:
Oral uygulama sonrasında, sakubitrilin %52-68'i (temelde LBQ657 olarak), valsartan ve metabolitlerinin yaklaşık %13'ü idrara atılır; sakubitrilin %37-48'i (temelde LBQ657 şeklinde), valsartan ve metabolitlerinin %86'sı feçese atılır.
Sakubitril, LBQ657 ve valsartan plazmadan sırasıyla yaklaşık 1,43, 11,48 ve 9,90 saatlik
ortalama eliminasyon yarı ömrü (T) ile atılır.
Doğrusallık/doğrusal olmayan durum:
Sakubitril, LBQ657 ve valsartanın farmakokinetik özellikleri test edilen doz aralığında (ONEPTUS 24 mg / 26 mg'dan 97 mg / 103 mg'a) doğrusaldır.
Hastalardaki karakteristik özellikler
Yaşlı hastalar:
LBQ657 ve valsartanın maruziyetleri yaşlı hastalarda, daha gençler ile karşılaştırıldığında sırasıyla %42 ve %30 oranlarında daha yüksektir.
Pediyatrik hastalar (<18 yaş):
ONEPTUS pediyatrik hastalarda çalışılmamıştır.
Böbrek fonksiyonunda bozukluk:
Hafif ila şiddetli böbrek bozukluğu olan hastalarda böbrek fonksiyonu ile LBQ657'ye sistemik maruziyet arasında bir korelasyon gözlenmiştir. Orta dereceli böbrek bozukluğu (30 mL/dk/1,73 m2 ≤eGFR< 60 mL/dk/1,73 m2) ve şiddetli böbrek bozukluğu (15 mL/dk/1,73 m2
≤eGFR <30 mL/dk/1,73 m2) olan hastalarda LBQ657'ye maruziyet, hafif böbrek bozukluğu (60 mL/dk/1,73 m2 ≤eGFR< 90 mL/dk/1,73 m2) olan hastalar (PARADIGM-HF çalışmasına kaydedilen en büyük hasta grubu) ile karşılaştırıldığında 1,4 kat ve 2,2 kat daha yüksek olmuştur. Hafif veya orta dereceli böbrek bozukluğu olan hastalarda herhangi bir doz ayarlaması gerekmemektedir. Şiddetli böbrek bozukluğu, safra sirozu veya kolestazı olan hastalarda sınırlı veri mevcuttur; bu hastalara ONEPTUS uygulanması önerilmemektedir. Valsartana maruziyet, hafif böbrek bozukluğu olan hastalar ile karşılaştırıldığında orta dereceli ve şiddetli böbrek bozukluğu olan hastalarda benzer bulunmuştur. Diyalize giren hastalarda herhangi bir çalışma gerçekleştirilmemiştir. Bununla birlikte, LBQ657 ve valsartan yüksek oranda plazma proteinlerine bağlanmaktadır ve bu nedenle diyaliz ile etkin bir şekilde uzaklaştırılması olası değildir.
Karaciğer fonksiyonunda bozukluk:
Sağlıklı gönüllüler ile karşılaştırıldığında, hafif ila orta dereceli karaciğer bozukluğu olan hastalarda sakubitrile maruziyet sırasıyla 1,5 ve 3,4 kat, LBQ657'ye maruziyet 1,5 ve 1,9 kat ve valsartana maruziyet 1,2 ve 2,1 kat artmıştır. Diğer yandan, hafif ile orta dereceli karaciğer bozukluğu olan hastalarda serbest LBQ657 konsantrasyonlarına maruziyet, benzer özelliklere sahip sağlıklı gönüllüler ile karşılaştırıldığında sırasıyla 1,47 ve 3,08 kat artmış ve serbest valsartan konsantrasyonlarına maruziyet de sırasıyla 1,09 ve 2,20 kat yükselmiştir. ONEPTUS şiddetli karaciğer bozukluğu, biliyer sirozu veya kolestazı olan hastalarda çalışılmamıştır (bkz. bölüm 4.3 ve 4.4).
Cinsiyet etkisi:
ONEPTUS'un (sakubitril, LBQ657 ve valsartan) farmakokinetiği erkek ve kadın gönüllüler arasında benzerdir.
5.3. Klinik öncesi güvenlilik verileri
Güvenlilik farmakolojisi, tekrarlı doz toksisitesi, genotoksisite, karsinojenik potansiyel, fertilite açısından konvansiyonel çalışmalara dayalı klinik dışı veriler (sakubitril ve valsartan bileşenleri ve/veya ONEPTUS ile çalışmaları içerir) insanlar için özel bir tehlike ortaya koymamaktadır.
Fertilite, üreme ve gelişim:
Organogenez sırasında ONEPTUS tedavisi sıçanlarda ≥49 mg sakubitril / 51 mg valsartan/kg/gün dozlarda [valsartan ve LBQ657'nin EAA değeri bazında MRHD'nin ≤0,72 katı] ve tavşanda ≥4,9 mg sakubitril / 5,1 mg valsartan /kg/gün dozlarda [EAA bazında MRHD'nin sırasıyla 2 ve 0,03 katı] embriyo-fetal letalitede artış ile sonuçlanmıştır. Tavşanlarda ≥4,9 mg sakubitril / 5,1 mg valsartan/kg/gün ONEPTUS dozunda gözlenen, maternal toksik dozlarla ilişkili olan düşük insidanslı fetal hidrosefaliye dayalı olarak ONEPTUS teratojeniktir. Anne için toksik olmayan dozda (1,46 mg sakubitril/1,54 mg valsartan/kg/gün) tavşan fetüslerinde kardiyovasküler anomaliler (başlıca kalp büyümesi) gözlenmiştir. Tavşanlarda 4,9 mg sakubitril / 5,1 mg valsartan/kg/gün ONEPTUS dozunda fetal iskelet varyasyonlarında (deforme sternebra, sternebra bipartit osifikasyonu) hafif bir artış gözlenmiştir. ONEPTUS'un advers embriyo-fetal etkileri anjiyotensin reseptör antagonist aktivitesine bağlanmaktadır (bkz. bölüm Gebelik ve laktasyon).
Organogenez sırasında sakubitril tedavisi, tavşanda maternal toksisite ile ilişkili dozlarda (500 mg/kg/gün; LBQ657 EAA değeri bazında MRHD'nin 5,7 katı) embriyo-fetal letalite ve embriyo-fetal toksisite ile sonuçlanmıştır (fetal beden ağırlığında azalma ve iskelet malformasyonları). >50 mg/kg/gün dozlarında osifikasyonda genel ve hafif bir gecikme gözlenmiştir. Bu bulgu advers olarak değerlendirilmemiştir. Sakubitril ile tedavi edilen sıçanlarda herhangi bir embriyo-fetal toksisite ya da teratojenisite gözlenmemiştir. Sakubitril için embriyo-fetal advers etki gözlenmeyen düzey sıçanda en az 750 mg/kg/gün ve tavşanda ve 200 mg/kg/gün olmuştur (LBQ657 EAA değeri bazında MRHD'nin 2,2 katı).
750 mg/kg/gün [EAA bazında MRHD'nin 2,2 katı] dozuna kadar sakubitril ve 600 mg/kg/dün [EAA bazında MRHD'nin 0,86 katı] dozuna kadar valsartan ile sıçanlarda gerçekleştirilen prenatal ve postnatal gelişim çalışmaları organogenez, gestasyon ve laktasyon sırasında ONEPTUS ile tedavinin yavru gelişimini ve sağkalımını etkileyebileceğine işaret etmektedir.
Diğer klinik öncesi bulgular:
Sakubitril/valsartan
ONEPTUS'un beyin-omurilik sıvısındaki (BOS) ve beyin dokusundaki amiloid-β konsantrasyonları üzerindeki etkisi iki hafta süreyle ONEPTUS (24 mg sakubitril / 26 mg valsartan /kg/gün) ile tedavi edilen genç (2-4 yaş) sinomolgus maymunlarında değerlendirilmiştir. Bu çalışmada sinomolgus maymunlarında ONEPTUS'un BOS Aβ klerensi üzerinde farmakodinamik etkisi olmuş, BOS Aβ 1-40, 1-42 ve 1-38 düzeylerini yükseltmiştir; beyindeki Aβ düzeylerinde buna karşılık gelen bir artış olmamıştır. BOS Aβ 1-
40 ve 1-42 düzeylerindeki artışlar insandaki iki haftalık sağlıklı gönüllü çalışmasında gözlenmemiştir (bkz. bölüm Farmakodinamik özellikler). Ayrıca, 39 hafta süreyle 146 mg sakubitril/154 mg valsartan/kg/gün dozunda ONEPTUS ile tedavi edilen sinomolgus maymunları ile gerçekleştirilen bir çalışmada beyinde amiloid plakları görülmemiştir. Fakat bu çalışmada amiloid içeriği kantitatif olarak ölçülmemiştir.
Sakubitril
Sakubitril ile tedavi edilen juvenil sıçanlarda (postnatal 7-70 gün) yaşla ilişkili kemik kütlesi gelişiminde ve kemik uzamasında azalma olmuştur. Sıçanlardaki bir çalışma kemik mineral yoğunluğunda sadece minimal geçici bir inhibitör etki göstermiş; fakat aynı etki, kemik büyümesi ile ilişkili diğer parametrelerde görülmeyerek normal koşullar altında erişkin hasta popülasyonlarında sakubitrilin kemik üzerinde anlamlı bir etkisinin olmayacağını düşündürmüştür. Diğer yandan, erişkinlerde kırk iyileşmesinin erken fazında sakubitrilin geçici, hafif bir etkisi olasılık dışı bırakılamamaktadır.
Valsartan
Sakubitril ile tedavi edilen juvenil sıçanlarda (postnatal 7-70 gün) 1 mg/kg/gün kadar düşük dozlar tübüler nefropati (bazen tübüler epitelyum nekrozunun eşlik ettiği) ve pelvis dilatasyonunu içeren kalıcı, geri dönüşsüz böbrek değişikliklerine neden olmuştur. Bu böbrek değişiklikleri, anjiyotensin dönüştürücü enzim inhibitörlerinin ve anjiyotensin II tip I blokerlerinin beklenen abartılı farmakolojik etkisini yansıtmaktadır; bu tür etkiler, sıçanlar yaşamın ilk 13 gününde tedavi edildiğinde görülmektedir. Bu dönem, insanda gestasyonun 36 haftası ile örtüşmektedir ve insanda bu süre bazı durumlarda doğumdan sonraki 44 haftaya uzayabilmektedir.
 Belsoğukluğu, Chlamydia ve Frengi
Belsoğukluğu, bakterilerin sebep olduğu bir enfeksiyondur. Cinsel ilişki
yoluyla bulaşır ve dölyatağı boynunda, idrar yollarında, anüste, makatta ve
boğazda enfeksyona sebep olabilir.
Belsoğukluğu, Chlamydia ve Frengi
Belsoğukluğu, bakterilerin sebep olduğu bir enfeksiyondur. Cinsel ilişki
yoluyla bulaşır ve dölyatağı boynunda, idrar yollarında, anüste, makatta ve
boğazda enfeksyona sebep olabilir. |
 Doğum Sonrası Depresyonu
Doğum sonrası depresyonu, doğumdan sonra her on kadından biri tarafından
tecrübe edilen stresli bir durumdur.
Doğum Sonrası Depresyonu
Doğum sonrası depresyonu, doğumdan sonra her on kadından biri tarafından
tecrübe edilen stresli bir durumdur. |
İLAÇ GENEL BİLGİLERİ
Farmanova Sağlık Hizmetleri Ltd. Şti
| Satış Fiyatı | 3146.7 TL [ 24 Mar 2025 ] |
| Önceki Satış Fiyatı | 3146.7 TL [ 17 Mar 2025 ] |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8699074090554 |
| Etkin Madde | Sakubitril + Valsartan |
| ATC Kodu | C09DX04 |
| Birim Miktar | 97+103 |
| Birim Cinsi | MG |
| Ambalaj Miktarı | 56 |
| Kalp Damar Sistemi > Anjiyotesin II Antagonistleri Kombinasyonları |
| İthal ( ref. ülke : Isvicre ) ve Beşeri bir ilaçdır. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| Eşdeğer bir ilaç bulunamadı |
 |
Aşırı Alkol Kullanımı, Alkolizm Alkol bağımlılığı, alkol kullanımı ve alkol sorunları arasındaki farkı açıklamak güçtür. Örneğin, geçmişte alkol kullanmış olan bir kimsenin mutlaka alkol bağımlısı olması gerekmez. |
 |
Astım Astımlı kişilerin akciğerlerindeki hava boruları (bronşlar) hassastır. Bu kişiler belirli tetikleyici faktörlere maruz kaldıklarında, hava boruları nefes almalarını güçleştirecek şekilde daralır. |
 |
Travma Sonrası Bunalımı Travmatik bir olay, günlük olağan olayların dışında olan ve kişiyi derinden rahatsız eden bir olaydır.Birçok olay böyle bir etki gösterebilir. |