PHOSPHO-SODA oral LAKSATIF K�sa �r�n Bilgisi
{ Dibazik Sodyum Fosfat + Monobazik Sodyum Fosfat }
1. BE�ER� TIBB� �R�N�N ADI
PHOSPHO -SODA21.6 g+8.1 g/45 ml oral ��zelti
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
45 mL i�inde:
Monobazik sodyum fosfat 21,6 g Dibazik sodyum fosfat 8,1 g
Yard�mc� maddeler
45 mL i�inde:
Sodyum benzoat 15,5 mg
Sodyum sakarin 150 mg
Etanol her dozda 100 mg'dan daha az miktarda i�erir. Her 45 mL'lik �i�e 5 g sodyum i�erir.
Yard�mc� maddeler i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Oral ��zelti
Berrak, renksiz, zencefil-limon kokulu, ��kelti ve bulan�kl�k i�ermeyen ��zelti
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Ba��rsak temizleyicisi olarak, hastay� kolon cerrahisine, kolonu r�ntgen ya da endoskopik inceleme i�in haz�rlamak amac�yla kullan�l�r.
Ba��rsak temizleme ajanlar�, kab�zl���n tedavisi i�in kullan�ma y�nelik de�ildir. PHOSPHO -SODA yeti�kin hastalar�n kullan�m� i�in endikedir.
4.2. Pozoloji ve uygulama �ekli
Pozoloji/uygulama s�kl��� ve s�resi
Yeti�kinlere iki ayr� PHOSPHO -SODA dozu uygulan�r.
PHOSPHO -SODA uygulamas�na hastane randevusundan bir g�n �nce ba�lanmal�d�r.
��len 12 �ncesi hastane randevular� i�in sabah dozaj talimatlar�, ��leden sonraki randevular i�in de ��leden sonraki dozaj talimatlar�na uyulmal�d�r.
�nerilen kullan�m dozu a��lmamal�d�r.
Uygulama �ekli:
Randevudan �nceki g�n
SABAH RANDEVUSU
Sabah saat 7'de kahvalt� yerine, en az bir bardak su veya "kat� partik�l i�ermeyen s�v�" i�ilir. Arzu edildi�inde daha fazla i�ilebilir.
"Kat� partik�l i�ermeyen s�v�" su, kat� partik�l i�ermeyen �orba, posas�z meyve suyu, siyah �ay veya sade kahve, kat� partik�l i�ermeyen karbonatl� veya karbonats�z me�rubatlar� i�ermektedir.
Doz – 45 mL PHOSPHO-SODA'y� yar�m bardak (120 mL) so�uk suda kar��t�r�n�z ve hemen i�iniz. �zerine bir bardak (240 mL) so�uk su i�iniz. Arzu edildi�inde daha fazla i�ilebilir.
Ba��rsak hareketleri boyunca, kaybolan s�v�y� yerine koyabilmek i�in i�ebildi�iniz kadar ekstra s�v� i�iniz.
��len 13:00 - ��le yeme�i yerine en az 3 bardak dolusu (720 mL) "kat� partik�l i�ermeyen s�v�" veya su i�ilir. Arzu edildi�inde daha fazla i�ilebilir.
Ak�am 19:00 - Ak�am yeme�i yerine en az 1 bardak dolusu "kat� partik�l i�ermeyen s�v�" veya su i�ilir. Arzu edildi�inde daha fazla i�ilebilir.
4.3. Kontrendikasyonlar
A�a��daki hallerde kullan�lmamal�d�r:
18 ya��n alt�ndaki �ocuklarda,
Bulant�, kusma veya kar�n a�r�s� oldu�unda,
Etkin madde
B�brek yetmezli�inde
Assitte,
Bilinen veya ��phelenilen gastrointestinal obstr�ksiyonda,
Megakolonda (konjenital veya sonradan edinilen),
Gastrointestinal perforasyonda,
�leus (Ba��rsak t�kan�kl���nda)
Aktif inflamatuvar ba��rsak hastal���nda,
Hiperkalseminin e�lik etti�i primer hiperparatiroidizmde.
PHOSPHO-SODA di�er sodyum fosfat i�eren laksatif �r�nlerle birlikte kullan�lmamal�d�r.
4.4. �zel kullan�m uyar�lar� ve �nlemleri
PHOSPHO-SODA ya�l� hastalarda nadiren de olsa elektrolit kayb�ndan dolay� potansiyel ve ciddi �l�m vakalar�yla ili�kilendirilmi�tir. PHOSPHO-SODA'n�n riskli pop�lasyonda tedavi ba�lamadan �nce yarar-risk oran� dikkatlice de�erlendirilmelidir.
Riskli pop�lasyonlarda ve bilinen kontrendikasyonu olan hastalarda PHOSPHO-SODA re�etelenirken �zel olarak dikkat edilmelidir (bkz. B�l�m 4.2. ve 4.3). Yeterli hidrasyonun sa�lanmas�na �nem verilmelidir. Tedavi �ncesi ve sonras� elektrolit d�zeylerinin �l��lmesi �nemlidir.
Risk alt�ndaki hastalar
Altta yatan b�brek yetmezli�i i�in risk art��� olan hastalarda, �nceden mevcut olan elektrolit bozukluklar�nda, elektrolit bozukluklar� ile ilgili risk art��� olan hastalarda (�rn. dehidratasyon, gastrik retansiyon, kolit, oral yolla yeterli miktarda s�v� al�namayan durumlar, hipertansiyon veya hastalarda dehidratasyona neden olabilecek �r�nlerin kullan�ld��� di�er durumlar), klinik etkisi olan veya hipovolemiye ba�l� hipotansiyon, kalp hastal���, akut miyokard enfarkt�st�, stabil olmayan angina veya zay�f b�nyeli, d��k�n ya da ya�l� hastalarda dikkatle kullan�lmal�d�r. Bu risk alt�ndaki hastalarda sodyum, potasyum, kalsiyum, klor�r, bikarbonat, fosfat, kan �re azotu ve kreatinin de�erleri, klinik olarak belirtildi�i takdirde tedavi ba�lang�c�nda ve sonras�nda elde edilmelidir.
Dehidratasyon
Bu �r�n �o�unlukla 30 dakika ila 6 saat aras�nda etki g�sterir. PHOSPHO-SODA ald�ktan sonra 6 saat i�inde ba��rsak hareketi olmad��� takdirde hastaya, ilac�n kullan�m�n�n kesilmesi ve dehidratasyon olas�l��� nedeniyle derhal bir doktora ba�vurmas� talimat� verilmelidir.
Hastalar s�k ve sulu d��k�lama konusunda uyar�lmal�d�r. Dehidratasyonun �nlenmesine yard�mc� olmas� i�in hastalar m�mk�n oldu�unca �ok s�v� almaya te�vik edilmelidir. Etkili bir p�rgatif kullan�l�rken yeterli s�v� al�nmamas�, a��r� s�v� kayb�na neden olabilir. Bunun sonucunda da dehidratasyon ve hipovolemi olu�turabilir. P�rgatif kullan�m�na ba�l� dehidratasyon ve hipovolemi, oral yoldan yetersiz s�v� al�m�yla, bulant� ve kusma ile, i�tahs�zl�kla, antihipertansifler (�r. anjiyotensin d�n��t�r�c� enzim (ADE) inhibit�rleri, anjiyotensin resept�r blokerleri(ARB'ler),kalsiyumkanalblokerleri), di�retikler, nonsteroidal
yetmezli�i ile birlikte meydana gelebilir. Sodyum fosfatlar ve PEG-3350 de dahil olmak �zere p�rgatifler ile akut b�brek yetmezli�ine ili�kin nadir bildirimler olmu�tur.
Dehidratasyon yatk�nl��� olabilecek durumlar� bulunan ya da glomer�ler filtrasyon oran�n� azaltabilecek ila� kullanan hastalarda, p�rgatif preparatlar�n kullan�m�ndan �nce hidrasyon durumu de�erlendirilmeli ve bu durum uygun �ekilde ele al�nmal�d�r.
Akut fosfat nefropatisine sekonder geli�en nefrokalsinozis
Akut b�brek yetmezli�i ve renal t�b�llerde kalsiyum fosfat kristali birikimleri ile ili�kili olan nefrokalsinozis, ba��rsak temizli�i i�in sodyum fosfat kullanan hastalarda �ok nadir olarak rapor edilmi�tir. Nefrokalsinozis, kal�c� b�brek fonksiyon bozuklu�u ve uzun s�reli diyaliz gereksinimi ile sonu�lanabilecek ciddi bir advers olayd�r. Bu raporlar�n �o�u, hipertansiyon tedavisi i�in ila� kullanan ya da di�retikler veya NSAII'ler gibi di�er ila� �r�nlerini kullanan ya�l� kad�n hastalarda bildirilmi�tir ve dehidratasyon ile sonu�lanabilir.
PHOSPHO-SODA re�ete edilirken prosed�rden �nce, haz�rl�k s�ras�nda ve prosed�rden sonra yeterli hidrasyon sa�lanmas�na, �nerilen doz aral�klar�na uyulmas�na ve ilac�n bilinen kontrendikasyonlar�na �zellikle dikkat edilerek, �zen g�sterilmelidir.
Elektrolit bozukluklar�
Serum sodyum ve fosfat d�zeylerinde y�kselme; kalsiyum ve potasyum d�zeylerinde ise d���� riski vard�r ve bunlar�n sonucunda hipernatremi, hiperfosfatemi, hipokalsemi, hipokalemi ve asidoz olu�abilir.
Konf�zyon, koma veya konv�lsiyonlar gibi n�rolojik bozukluklarla komplike hiponatremi meydana gelebilir.
Hipokalsemi veya hipokalemi gibi elektrolit dengesizliklerinin bir sonucu olarak nadiren hafif QT aral��� uzamas� olu�abilir. Bu de�i�iklikler klinik a��dan anlaml� de�ildir.
Hipomotilite:
Hipomotilite bozuklu�u olan veya gastrointestinal operasyon ge�irmi� veya hipomotilite bozuklu�una yatk�n di�er t�bbi durumlara sahip hastalarda dikkatli kullan�lmal�d�r. Hastan�n kolostomisi veya ileostomisi varsa veya tuzsuz bir diyete uymas� gerekiyorsa bu durum elektrolit dengesinde bozulma, dehidrasyon veya asit dengesinde bozulmaya neden olabilece�inden ila� dikkatli kullan�lmal�d�r.
Lezyonlar
Endoskopide rektosigmoid b�lgede tek veya �ok say�da aftoid benzeri noktasal lezyonlar g�zlemlenmi�tir. Bunlar kolon preparat�nda lenfoid folik�ller veya farkl� inflamatuar infiltratlar ya da epitelyal konjesyonlar/de�i�iklikler olarak ortaya ��kar. Bu anormallikler klinik olarak anlaml� de�ildir ve tedavi edilmeden spontan olarak kaybolurlar.
Bu t�bbi �r�n her 45 mL'lik �i�ede 150 mg sodyum sakarin i�erir.
Bu t�bbi �r�n her 45 mL'lik �i�ede 5 g sodyum ihtiva eder. Bu durum, kontroll� sodyum diyetinde bulunan hastalar i�in g�z �n�nde bulundurulmal�d�r.
Bu t�bbi �r�n her 45 mL'lik �i�ede az miktarda, 100 mg dan az, etanol (alkol) i�erir.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Antihipertansif ila�lar (�r. kalsiyum kanal blokerleri, anjiyotensin d�n��t�r�c� enzim inhibit�rleri (ADE), anjiyotensin resept�r blokerleri (ARB)), di�retikler, lityum tedavisi veya elektrolit d�zeylerini hiperfosfatemi, hipokalsemi, hipokalemi, hipernatremik dehidratasyon ve asidoz olu�arak etkileyebilen di�er ila�larla birlikte dikkatli kullan�lmal�d�r.
PHOSPHO-SODA al�m� s�ras�nda gastrointestinal kanaldan ila�lar�n absorpsiyonu gecikebilir veya t�m�yle engellenebilir. D�zenli olarak al�nan oral ila�lar�n (�r. oral kontraseptifler, antiepileptik ila�lar, antidiyabetikler ve antibiyotikler) etkinli�i azalabilir ya da t�m�yle ortadan kalkabilir. QT aral���n� uzatt��� bilinen ila�lar� alan hastalarda da dikkatli olunmas� �nerilir.
Paratiroid hormonu kullanan hastalarda dikkatli kullan�lmal�d�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
Pediyatrik pop�lasyon:
18 ya��n alt�ndaki �ocuklarda kullan�m� kontrendike oldu�u i�in bu pop�lasyon ile etkile�im �al��mas� yap�lmam��t�r.
4.6. Gebelik ve laktasyon
:Gebelik kategorisi: C
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon): PHOSPHO-SODA ile tedavide oral kontraseptiflerin etkilili�i azalabilir ya da t�m�yle ortadan kalkabilir. �ocuk do�urma potansiyeli bulunan kad�nlar tedavi s�resi boyunca etkin bir do�um kontrol y�ntemi kullanmal�d�r.
Gebelik d�nemi:
PHOSPHO-SODA'n�n gebe kad�nlarda kullan�m�na ili�kin yeterli veri mevcut de�ildir.
Hamilelikte maruziyet hakk�nda herhangi bir klinik veri yoktur. Hayvanlar �zerinde gebelik, embriyonal/fetal geli�imi, do�um ve do�um sonras� geli�im �zerindeki etkiler bak�m�ndan yap�lm�� herhangi bir �al��ma mevcut de�ildir. �nsanlara y�nelik potansiyel risk bilinmemektedir. PHOSPHO-SODA gerekli olmad�k�a gebelik s�ras�nda kullan�lmamal�d�r.
Laktasyon d�nemi:
PHOSPHO-SODA'n�n insan s�t�ne ge�ip ge�medi�i bilinmemektedir. Sodyum fosfat insan s�t�ne ge�ebilece�inden, ba��rsak temizleme ��zeltisinin ilk dozundan itibaren ikinci dozun 24 saat sonras�na kadar s�t�n sa��larak at�lmas� tavsiye olunur. Kad�nlar, PHOSPHO-SODA'n�n ikinci dozunu ald�ktan sonra 24 saat s�reyle bebeklerini emzirmemelidir.
�reme yetene�i/Fertilite:
PHOSPHO-SODA'n�n erkek ve di�i fertilitesi �zerine etkileri ile ilgili herhangi bir �al��ma mevcut de�ildir, veri bulunmamaktad�r.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
PHOSPHO-SODA dehidrasyondan dolay� ba� d�nmesine neden olabilir. PHOSPHO-SODA ara� veya makine kullan�m�n� hafif-orta d�zeyde etkileyebilir.
4.8. �stenmeyen etkiler
Advers reaksiyonlar a�a��dakilere kar��l�k gelen s�kl�klara g�re rapor edilmi�tir:
�ok yayg�n (≥ 1/10), yayg�n (≥ 1/100, <1/10), yayg�n olmayan (≥ 1/1.000, <1/100), seyrek (≥ 1/10.000, <1/1.000), �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). Her s�kl�k grubu i�inde, istenmeyen etkiler azalan ciddiyet s�ras�na g�re sunulmu�tur.
Ba����kl�k sistemi hastal�klar�:
�ok seyrek: Hipersensitivite
Metabolizma ve beslenme hastal�klar�:
Yayg�n olmayan: Dehidratasyon
�ok seyrek: Hiperfosfatemi, hipokalsemi, hipokalemi, hipernatremi, metabolik asidoz, tetani Bilinmiyor: Konf�zyon, koma veya konv�lsiyon gibi n�rolojik bozukluklar ile komplike hiponatremi
Sinir sistemi hastal�klar�:
�ok yayg�n: Ba� d�nmesi Yayg�n: Ba� a�r�s�
�ok seyrek: Bilin� kayb�, parestezi
Kardiyak hastal�klar:
�ok seyrek: Miyokard enfarkt�s�, aritmi
Vask�ler hastal�klar:
�ok seyrek: Hipotansiyon
Gastrointestinal hastal�klar:
�ok yayg�n: Diyare, abdominal a�r�, abdominal distansiyon, bulant�
Yayg�n: Kusma, anormal kolonoskopi (rektosigmoid b�lgede klinik a��dan anlaml� olmayan ve tedavi edilmeden spontan olarak kaybolan tek veya �ok say�da aftoid benzeri noktasal lezyonlar)
Deri ve deri alt� doku hastal�klar�:
�ok seyrek: Alerjik dermatit
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar�:
�ok seyrek: Kas kramp�
B�brek ve idrar yolu hastal�klar�:
Seyrek: Akut fosfat nefropatisine sekonder geli�en nefrokalsinozis �ok seyrek: Akut renal yetmezlik, kronik renal yetmezlik,
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar:
�ok yayg�n: �rperme, asteni Yayg�n: G���s a�r�s�
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e- posta: tufam@titck.gov.tr; tel: 0800 314 00 08; faks: 0312 218 35 99).
4.9. Doz a��m� ve tedavisi
PHOSPHO-SODA a��r� dozlarda kullan�ld���nda, �ocuklara verildi�inde veya sindirim kanal�nda t�kan�kl��� olan hastalara verildi�inde hipokalsemi, hipernatremi ve asidozun e�lik etti�i �l�mc�l hiperfosfatemi olgular� vard�r.
A��r� doz al�m� hastalarda a�a��daki semptomlara neden olmaktad�r: dehidratasyon, hipotansiyon, ta�ikardi, bradikardi, takipne, kardiyak arrest, �ok, solunum yetmezli�i, dispne, konv�lsiyonlar, paralitik ileus, anksiyete, a�r�. A��r� doz al�nmas� serumdaki sodyum ve fosfat d�zeylerinde art��a, kalsiyum ve potasyum d�zeylerinde azalmaya yol a�abilir. Bu vakalarda hipernatremi, hiperfosfatemi, hipokalsemi, hipokalemi ve asidoz olu�abilir.
A��r� dozlarda, yanl��l�kla PHOSPHO-SODA verilen �ocuklarda ve obstr�ksiyonlu hastalarda belgelenmi� t�m�yle iyile�me olgular� da vard�r. Bu hastalardan biri, normal dozun alt� kat� olan a��r� doz alm��t�r.
A��r� al�ma ba�l� toksik etkiyi rehidratasyonla tedavi etmek m�mk�nd�r, intraven�z yoldan
%10'luk kalsiyum glukonat verilmesi gerekebilir.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Ozmotik etkili laksatifler ATC kodu: A06AD17
PHOSPHO-SODA ozmotik olarak ince ba��rsak l�meninde s�v� tutulmas�n� artt�rarak etki g�steren tuzlu laksatiftir. �leum i�erisindeki s�v� toplanmas� �i�kinlik olu�turur ve s�ras�yla peristaltik hareketleri ve ba��rsaklar�n bo�alt�m�n� artt�r�r.
5.2. Farmakokinetik �zellikler
Genel �zellikler:Oral sodyum fosfat ��zeltisinin uygulanmas�, sa�l�kl� g�n�ll�lerde ge�ici serum elektrolit de�i�ikliklerine neden olmu�tur. �ki ya� ve iki cinsiyet grubundaki elektrolit de�i�imlerinin derecesini ve s�recini de�erlendirmek i�in oral sodyum fosfat ��zeltisi alan 24 sa�l�kl� yeti�kin g�n�ll�yle a��k etiketli bir �al��ma ger�ekle�tirilmi�tir. �al��ma, s�v� diyeti, sodyum fosfat dozlar�n�n zamanlamas� ve uygun hidrasyon da dahil olmak �zere, kolonoskopi �ncesi yayg�n olarak kullan�lan ba��rsak haz�rl���na benzeyecek �ekilde tasarlanm��t�r. Takip edilen 2 x 45 ml oral sodyum fosfat dozu ve kat� partik�l i�ermeyen s�v� ilavesi, �r�n�n onaylanm�� dozlama rejimine uygun olmu�tur. �al��ma pop�lasyonu cinsiyet ve ya� i�in dengelenmi�tir. Ara�t�rmaya kat�lanlar�n yar�s� 65 ya� ve �st� g�n�ll�lerden olu�mu�tur.
Sonu�lar her bir dozdan sonra serum sodyum ve fosfat konsantrasyonlar�nda bir art�� g�stermi� ancak potasyum ve kalsiyum azalm��t�r.
T�m g�n�ll�ler i�in ortalama serum fosfat konsantrasyonu ba�lang��ta 3,33 mg / dL olarak �l��lm��; daha sonra 3.saatte 6,26 mg / dL olarak doru�a ula�m��t�r. �kinci dozdan hemen �nce (12.saat) 4,70 mg / dL'ye d��m�� ve 14.saatte tekrar 6,86 mg/dL ile zirveye ��kt��� g�r�lm��t�r.
36. saatte, t�m serum fosfat konsantrasyonlar� normale d�nm��t�r.
A�a��daki �ekil, her ya� cinsiyet alt grubu i�in ortalama serum fosfat konsantrasyonunun zaman dilimini g�stermektedir. Ya�l� kad�nlar en �ok de�i�en de�erleri g�stermi�tir.
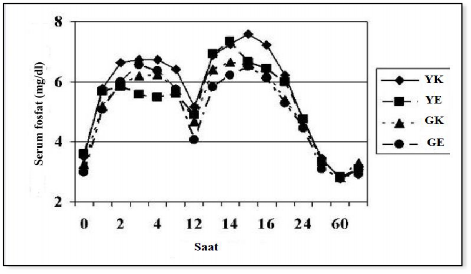
Ortalama serum sodyum konsantrasyonu normal aral�kta (134-147 mmol/L) dalgalanma g�stermi� ancak 4 ki�i normalin �st s�n�r�n�n �zerinde sodyum de�erlerine sahip olmu�tur.
Serum potasyum ve kalsiyum konsantrasyonlar�ndaki d���� normal bireysel aral�kta dalgalanm��t�r ve daha sonra ikinci dozun uygulanmas�ndan 12 saat sonra ba�lang�� de�erlerine geri d�nm��t�r. G�n�ll�lerin %29'unda ilk dozun uygulanmas�ndan sonra 36.saate kadar normal alt s�n�r�n (8,5 mg/dL) alt�ndaki serum kalsiyum de�erleri bildirilmi�tir. Bununla birlikte, hi�bir klinik hipokalsemi vakas� kaydedilmemi�tir.
Sonu� olarak, sa�l�kl� yeti�kin g�n�ll�lere 2 x 45 mL sodyum fosfat uygulanmas� ile serum elektrolit konsantrasyonunda meydana gelen de�i�iklikler klinik olarak anlaml� bulunmam��t�r. Bu de�i�iklikler ge�ici olmu� ve ba��rsak haz�rl��� tedavisinin tamamlanmas�ndan sonraki 12 ila 24 saat i�inde normale d�nm��t�r.
Emilim:
Lokal aktivite g�sterir ancak ilac�n bir k�sm� sistemik olarak emilebilir.
Da��l�m:
Emilime u�rayan fosfatlar dola��m sistemi taraf�ndan da��l�r ve b�brekler taraf�ndan elimine edilir.
Biyotransformasyon:
Biyotransformasyonu beklenmemektedir.
Eliminasyon:
Renal ve fekal eliminasyon meydana gelir.
Hastalardaki karakteristik �zellikler
B�brek yetmezli�i
B�brek yetmezli�i olan hastalarda bu durumun PHOSPHO-SODA farmakokineti�i �zerindeki etkisi ara�t�r�lmam��t�r. Bu verilerin sa�l�kl� g�n�ll�lerden risk alt�ndaki hastalara (�rne�in b�brek hastalar�) uyarlanmas� m�mk�n de�ildir (Bkz. B�l�m 4.3, 4.4).
5.3. Klinik �ncesi g�venlilik verileri
PHOSPHO-SODA ile hayvanlarda �reme toksisitesi ile ilgili herhangi bir �al��ma yap�lmam��t�r.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Gliserol
Sodyum sakkarin Sodyum benzoat (E211)
Saf su
Zencefil-limon aromas�:
Oleorezin Zencefil Alkol
Limon Ya��
K�smen Deterpine Limon Ya�� Sitrik Asit
Saf Su
6.2. Ge�imsizlikler
Uygulanabilir de�ildir.
6.3. Raf �mr�
36 ay
Kutu a��ld�ktan sonra hemen kullan�lmal�d�r. Kullan�lmam�� ��zelti at�lmal�d�r.
6.4. Saklamaya y�nelik �zel tedbirler
25°C alt�ndaki oda s�cakl���nda saklay�n�z.
6.5. Ambalaj�n niteli�i ve i�eri�i
PHOSPHO-SODA 45 mL ve 90 mL ��zelti kutuda, plastik kapakl� polietilen �i�ede sunulmaktad�r.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Bu �r�n kullan�lmadan �nce su ile seyreltilmelidir.
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj ve Ambalaj At�klar�n�n Kontrol� Y�netmeli�i”ne uygun olarak imha edilmelidir.
 Mide Kanseri
Mide kanseri genellikle mideyi t�m�yle kaplayan ve mukus �retmekle g�revli h�crelerde ba�lar. Bu kanser tipine adenokarsinom denir.
Mide Kanseri
Mide kanseri genellikle mideyi t�m�yle kaplayan ve mukus �retmekle g�revli h�crelerde ba�lar. Bu kanser tipine adenokarsinom denir. |
 �izofrenlik
�izofrenli�in psikiatrik te�hisi hakk�nda �ok fazla anla�mazl�k vard�r. Bu
sayfadaki bilgiler, �izofrenli�in te�hisi, nedenleri ve tedavisi hakk�ndaki fakl� teoriler
hakk�nda bilgi verecektir.
�izofrenlik
�izofrenli�in psikiatrik te�hisi hakk�nda �ok fazla anla�mazl�k vard�r. Bu
sayfadaki bilgiler, �izofrenli�in te�hisi, nedenleri ve tedavisi hakk�ndaki fakl� teoriler
hakk�nda bilgi verecektir. |
 |
Depresyonu Anlamak Depresyon farkl� ki�ileri farkl� bi�imlerde etkiler. Duygusal veya fiziksel olmak �zere geni� alanda belirtilere sebep olabilir.Depresyona neler sebep olur? |
 |
Rahim Boyu ( Serviks ) Kanseri Rahim boynu (serviks) kanseri 35 ya� alt� kad�nlarda g�r�len vakalarda meme kanserinden sonra ikinci s�ray� al�r.Serviks kanserinin geli�mesi y�llarca s�rebilir. |
 |
Mesane Kanseri Mesane kanseri her zaman mukozada ba�lar. Erken safhalarda bu tabakada s�n�rl� kal�r ve h�cre i�indeki karsinom olarak nitelendirilir. |
�LA� GENEL B�LG�LER�
Recordati �la� Sanayi ve Ticaret A.�.
| Geri �deme Kodu | A03048 |
| Sat�� Fiyat� | 109.86 TL [ 1 Dec 2025 ] |
| �nceki Sat�� Fiyat� | 109.86 TL [ 24 Nov 2025 ] |
| Original / Jenerik | Jenerik �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699559650082 |
| Etkin Madde | Dibazik Sodyum Fosfat + Monobazik Sodyum Fosfat |
| Yerli ve Be�eri bir ila�d�r. |