PIMREVA 200 mg ve 50 mg film kapl� tablet (56 tablet) K�sa �r�n Bilgisi
{ Alpelisib }
1. BE�ER� TIBB� �R�N�N ADI
P�MREVA 200 mg ve 50 mg Film Kapl� Tablet
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Alpelisib 200 mg veya 50 mg
Yard�mc� maddeler
Yard�mc� maddeler i�in, 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Film kapl� tablet.
200 mg film kapl� tablet: A��k k�rm�z�, ovaloid, kavisli, e�imli kenarlara sahip, bir taraf�nda “YL7”, di�er taraf�nda “NVR” bask�s� bulunan film kapl� tablet
50 mg film kapl� tablet: A��k pembe, yuvarlak, kavisli, e�imli kenarlara sahip, bir taraf�nda “L7”, di�er taraf�nda “NVR” bask�s� bulunan film kapl� tablet
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
P�MREVA hormon resept�r� (HR) pozitif, insan epidermal b�y�me fakt�r� resept�r� 2 (HER2) negatif, PIK3CA mutasyonlu ileri evre veya metastatik meme kanseri olan, kontrols�z diyabeti olmayan, metastatik hastal�k i�in kemoterapi almam�� olan, metastatik hastal�k i�in bir basamak endokrin tedavi alan ve sonras�nda progresyon geli�en postmenopozal kad�n ve erkek hastalarda fulvestrant ile kombinasyon halinde endikedir.
4.2. Pozoloji ve uygulama �ekli
P�MREVA tedavisi antikanser terapilerde deneyimli bir hekim taraf�ndan ba�lat�lmal�d�r.
P�MREVA tedavisi i�in HR-pozitif, HER2-negatif ileri evre meme kanseri olan hastalar, ge�erli bir test kullan�larak t�m�r veya plazma �rneklerinde bir PIK3CA mutasyonunun varl���na dayanarak se�ilmelidir. Bir plazma �rne�inde mutasyon tespit edilmezse, varsa t�m�r dokusu test edilmelidir.
Pozoloji/uygulama s�kl��� ve s�resi
�nerilen doz, s�rekli olarak g�nde bir kez tok karn�na al�nan 300 mg alpelisibtir (2 x 150 mg film kapl� tablet). P�MREVA, her g�n yakla��k olarak ayn� saatte, yemekten hemen sonra al�nmal�d�r (bkz. B�l�m 5.2). P�MREVA'n�n �nerilen maksimum g�nl�k dozu 300 mg'd�r.
Hastal�k progresyonu veya kabul edilemez toksisite olu�ana kadar tedaviye devam edilmelidir.
Bir P�MREVA dozu ka��r�l�rsa, normalde al�nd��� zamandan sonraki 9 saat i�inde olmak kayd�yla, yemekten hemen sonra al�nabilir. 9 saatten fazla bir s�re sonra, o g�n�n dozu atlanmal�d�r. P�MREVA ertesi g�n her zamanki gibi al�nmal�d�r. E�er hasta P�MREVA dozunu ald�ktan sonra kusarsa, hasta o g�n ek bir doz almamal� ve ertesi g�n normal zamanda normal doz program�na devam etmelidir.
P�MREVA, fulvestrant ile birlikte uyguland���nda, �nerilen fulvestrant dozu, 1, 15 ve 29. g�nlerde ve daha sonra ayda bir kez 500 mg'd�r. Fulvestrant�n pozolojisi i�in ilgili �r�n�n K�sa �r�n Bilgisine bak�n�z.
Tedavi, klinik fayda g�zlemlendi�i s�rece veya kabul edilemez toksisite ortaya ��kana kadar devam etmelidir. Tolerabiliteyi artt�rmak i�in doz modifikasyonlar� gerekli olabilir.
Doz ayarlamalar�
�iddetli veya tolere edilemeyen advers ila� reaksiyonlar�, ge�ici olarak doza ara verilmesi ve/veya P�MREVA'n�n kesilmesini gerektirebilir. Doz azaltman�n gerekti�i duruumlar i�in, doz azaltma k�lavuzlar� Tablo-1'de listelenmektedir. En fazla 2 doz azalt�m� �nerilmektedir, bundan sonra hastan�n P�MREVA ile tedavisi kal�c� olarak kesilmelidir. Doz azaltma, �nceki en k�t� toksisiteye dayanmal�d�r.
Tablo 1 P�MREVA i�in advers reaksiyonlarda �nerilen doz azaltma k�lavuzu
P�MREVA doz d�zeyi | Doz ve program | Tablet say�s� ve dozu |
Ba�lang�� dozu | G�nde bir kez 300 mg | 2 x 150 mg tablet |
�lk doz azalt�m� | G�nde bir kez 250 mg | 1 x 200 mg tablet ve 1x 50 mg tablet |
�kinci doz azalt�m� | G�nde bir kez 200 mg | 1 x 200 mg tablet |
Tablo 2-5'te, spesifik advers reaksiyonlar�n y�netiminde, P�MREVA dozlar�na ge�ici olarak ara verilmesi, dozlar�n azalt�lmas� ve/veya tedavinin kesilmesi ile ilgili �neriler �zetlenmektedir. Tedavi eden doktorun klinik karar�, gerekli g�r�lmesi halinde laboratuvar de�erlerinin do�rulanmas� da dahil olmak �zere, P�MREVA tedavisi i�in bireysel fayda/risk de�erlendirmesine dayal� olarak her hastan�n doz y�netim plan�na rehberlik etmelidir.
Hiperglisemi
Prediyabetik veya a�l�k glukozu (FG) >250 mg/dl veya 13,9 mmol/l, v�cut kitle indeksi (BMI)
≥30 veya ya�� 75 veya daha b�y�k olan hastalar i�in hiperglisemi tedavisinde deneyimli bir sa�l�k uzman� ile kons�ltasyon, her zaman de�erlendirilmelidir ve tavsiye edilir.
Diyabetli hastalarda, diyabet uzman� ya da hiperglisemi tedavisi konusunda deneyimli bir sa�l�k uzman� taraf�ndan her zaman kons�ltasyon ger�ekle�tirilmelidir.
Tablo 2 Hiperglisemi i�in doz modifikasyonu ve y�netimi
A�l�k plazma glukoz (APG)/Kan glukoz de�erleri | �neri |
Doz modifikasyonu ve doz y�netimi yaln�zca a�l�k glikozu (plazma/kan) de�erine ba�l� olarak ger�ekle�tirilmelidir. | |
APG>N�S-160 mg/dl veya >N�S- 8,9 mmol/l | P�MREVA doz ayarlamas� gerekmez. Antidiyabetik tedavi ba�lat�l�r veya yo�unla�t�r�l�r. |
APG>160-250 mg/dl veya >8,9- 13,9 mmol/l | P�MREVA doz ayarlamas� gerekmez. Antidiyabetik tedavi ba�lat�l�r veya daha da yo�unla�t�r�l�r. Uygun antidiyabetik tedavi ile APG 21 g�n i�inde ≤160 mg/dl veya 8,9 mmol/l'ye d��mezse, P�MREVA dozu 1 doz d�zeyinde azalt�l�r ve APG de�erine �zg� �neriler izlenir. |
>250-500 mg/dl veya >13,9-27,8 mmol/l | P�MREVA tedavisine ara verilir. Oral antidiyabetik tedavi ba�lat�l�r veya yo�unla�t�r�l�r ve hiperglisemi d�zelene kadar 1-2 g�n boyunca ek antidiyabetik t�bbi �r�nleri d���n�l�r. �ntraven�z hidrasyon uygulan�r ve uygun tedavi d���n�l�r (�rn. elektrolit/ketoasidoz/hiperosmolar bozukluklara m�dahale). APG, uygun antidiyabetik tedavi alt�nda 3 ila 5 g�n i�inde ≤160 mg/dl veya 8,9 mmol/l'ye d��erse, bir d���k doz d�zeyinde P�MREVA'ya devam edilir. APG, uygun antidiyabetik tedavi alt�nda 3 ila 5 g�n i�inde ≤160 mg/dl veya 8,9 mmol/l'ye d��mezse, hiperglisemi tedavisinde uzman bir sa�l�k uzman�na dan��ma �nerilir. APG, uygun antidiyabetik tedaviyi takip eden 21 g�n i�inde ≤160 mg/dl veya 8,9 mmol/l'ye d��mezse, P�MREVA tedavisi bir daha ba�lanmamak �zere kesilir. |
>500 mg/dl veya >27,8 mmol/l | P�MREVA tedavisine ara verilir. Uygun antidiyabetik tedavi ba�lat�l�r veya yo�unla�t�r�l�r (intraven�z hidrasyon uygulan�r ve uygun tedavi d���n�l�r [�rn. elektrolit/ketoasidoz/hiperosmolar bozukluklara m�dahale]), 24 saat i�inde ve klinik durumun gerektirdi�i �ekilde APG tekrar kontrol edilir. |
| APG ≤500 mg/dl veya ≤27,8 mmol/l'ye d��erse, <500 mg/dl i�in Derece 3 APG de�erine �zg� �neriler uygulan�r. APG > 500 mg/dl veya > 27,8 mmol/l olarak teyit edilirse, P�MREVA tedavisi bir daha ba�lanmamak �zere kesilir. |
Metformin ve ins�lin duyarl�la�t�r�c�lar (tiazolidindionlar veya dipeptidil peptidaz- 4 inhibit�rleri gibi) dahil, uygulanabilir antidiyabetik t�bbi �r�nler ba�lat�lmal� ve lokal diyabetik tedavi k�lavuzlar� da dahil olmak �zere dozlama ve doz titrasyon �nerileri i�in ilgili re�eteleme bilgileri g�zden ge�irilmelidir. Faz III klinik �al��mada metformin, �u k�lavuz bilgilere g�re �nerilmi�tir: Metformin g�nde bir kez 500 mg'da ba�lat�lmal�d�r. Tolebiliteye dayanarak, metformin dozu g�nde iki kez 500 mg'a, ard�ndan kahvalt� ile 500 mg'a ve ak�am yeme�i ile 1000 mg'a ��kar�labilir, ard�ndan gerekirse g�nde iki kez 1000 mg'a ��kar�labilir (bkz. B�l�m 4.4). | |
Ba�lang�� diyabetik ve prediyabetik durum, ba�lang�� v�cut kitle indeksinin (BMI) 30 ve �st� olmas� (≥30) ve ba�lang�� ya��n�n 75 ve daha b�y�k olmas� (≥75), alpelisib ile tedavi edilen hastalarda hiperglisemi i�in risk fakt�rleri oldu�u belirlenmi�tir. Bu risk fakt�rleri, herhangi bir derece hiperglisemiye sahip hastalar�n % 74,7'sinde ve Derece 3 veya 4 hiperglisemiye sahip hastalar�n % 86,2'sinde g�zlemlenmi�tir (bkz. B�l�m 4.4).
D�k�nt�
Oral antihistaminik uygulamas�, P�MREVA tedavisinin ba�lang�c�nda profilaktik olarak d���n�lebilir. Ek olarak, d�k�nt� semptomlar�n� y�netmek i�in antihistaminikler �nerilir.
D�k�nt�n�n ilk belirtilerinde topical kortikosteroidler ba�lat��mal�d�r. Orta ve �iddetli d�k�nt�ler i�in ise sistemik kortikosteroidler d���n�lmelidir. Tablo 3'de belirtildi�i �zere d�k�nt�n�n �iddetine ba�l� olarak, P�MREVA dozuna ara verilmesi, doz azalt�lmas� veva doz kesilmesi gerekebilir (bkz. B�l�m 4.8).
Tablo 3 D�k�nt� i�in doz modifikasyonu ve y�netimi
Derece | �neri |
T�m dereceler | Her zaman dermatolojiye dan���lmas� d���n�lmelidir. |
Derece 1 (Aktif deri toksisitesi ile birlikte < %10 v�cut y�zey alan� [VYA]) | P�MREVA doz ayarlamas� gerekmez. Topikal kortikosteroid tedavisi ba�lat�l�r. Semptomlar� y�netmek i�in oral antihistaminik tedavi eklemek d���n�l�r. |
| Uygun tedaviden sonraki 28 g�n i�erisinde d�k�nt� iyile�mezse, d���k doz sistemik kortikosteroid eklenir. |
Derece 2 (Aktif deri toksisitesi ile birlikte %10-30 VYA) | P�MREVA doz ayarlamas� gerekmez. Topikal kortikosteroid ve oral antihistaminik tedavisi ba�lat�l�r veya yo�unla�t�r�l�r D���k doz oral kortikosteroid tedavisi d���n�l�r. 10 g�n i�erisinde d�k�nt� ≤ 1. dereceye iyile�irse, sistemik kortikosteroid kesilebilir. |
Derece 3 (�rn. t�bbi tedaviye yan�t vermeyen �iddetli d�k�nt�)
(Aktif deri toksisitesi ile birlikte > %30 VYA) | P�MREVA'ya ara verilir. Topikal/oral kortikosteroid ve antihistaminik tedavi ba�lat�l�r veya yo�unla�t�r�l�r. ≤1. dereceye iyile�me olduktan sonra, P�MREVA tedavisine bir sonraki d���k doz d�zeyinde devam edilir. |
Derece 4 (�rn. �iddetli b�ll�z, kabart�l� veya eksfolyatif deri rahats�zl�klar�) (intraven�z antibiyotiklerin endike oldu�u yayg�n s�perenfeksiyon ile ili�kili herhangi bir VYA y�zdesi; hayat� tehdit eden sonu�lar) | P�MREVA tedavisi bir daha ba�lanmamak �zere kesilir. |
Diyare veya kolit
Tablo 4 Diyare veya kolit i�in doz modifikasyonu ve y�netimi
Derece | �neri |
Derece 1 | P�MREVA doz ayarlamas� gerekmez. Uygun t�bbi tedavi ba�lat�l�r ve klinik durumun gerektirdi�i �ekilde izlem yap�l�r. |
Derece 2 | P�MREVA dozuna ara verilir. Uygun t�bbi tedavi ba�lat�l�r veya yo�unla�t�r�l�r ve klinik durumun gerektirdi�i �ekilde izlem yap�l�r. Diyare veya kolitte ≤1 derecesine iyile�me oldu�unda, P�MREVA'ya ayn� doz d�zeyinde devam edilir. ≥2. derece diyare veya kolit tekrarlarsa, P�MREVA dozuna ≤1. dereceye iyile�me olana kadar ara verilir ve P�MREVA'ya bir sonraki d���k doz d�zeyinde devam edilir. |
Derece 3 | P�MREVA dozuna ara verilir. Uygun t�bbi tedavi ba�lat�l�r veya yo�unla�t�r�l�r ve klinik |
| derecesine iyile�me olursa, P�MREVA'ya bir sonraki d���k doz d�zeyinde devam edilir. |
Derece 4 | P�MREVA tedavisi kal�c� olarak kesilir. |
Di�er toksisiteler
Tablo 5 Di�er toksisiteler i�in doz modifikasyonu ve y�netimi (hiperglisemi ve d�k�nt� ve diyare veya kolit hari�)
Derece | �neri |
Derece 1 veya 2 | P�MREVA doz ayarlamas� gerekmez. Uygun t�bbi tedavi ba�lat�l�r ve klinik durumun gerektirdi�i �ekilde izlem yap�l�r. |
Derece 3 | ≤1 derecesine iyile�me olana kadar P�MREVA tedavisine ara verilir, ard�ndan bir sonraki d���k doz d�zeyinde P�MREVA'ya devam edilir. |
Derece 4 | P�MREVA bir daha ba�lanmamak �zere kesilir. |
Uygulama �ekli
P�MREVA a��zdan al�n�r. P�MREVA tabletleri b�t�n olarak yutunuz. Tabletler yutulmadan �nce �i�nenmemeli, ezilmemeli veya b�l�nmemelidir. K�r�lm��, �atlam�� veya b�t�nl��� ba�ka �ekilde bozulmu� hi�bir tablet yutulmamal�d�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
B�brek yetmezli�i:
Pop�lasyon farmakokinetik analizine g�re, hafif veya orta derecede b�brek yetmezli�i olan hastalarda doz ayarlamas� gereklide�ildir(bkz.b�l�m5.2). �iddetli b�brek yetmezli�i olan
Karaci�er yetmezli�i:
Karaci�er fonksiyon bozuklu�u olan kanserli olmayan hastalarda yap�lan bir karaci�er yetmezli�i �al��mas�na dayanarak, hafif, orta veya �iddetli karaci�er yetmezli�i olan hastalarda doz ayarlamas� gerekli de�ildir (s�ras�yla Child Pugh s�n�f A,B ve C) (bkz. B�l�m 5.2).
Pediatrik pop�lasyon:
P�MREVA'n�n 0-18 ya��ndaki �ocuklarda g�venlili�i ve etkilili�i belirlenmemi�tir. Hi�bir veri mevcut de�ildir.
Geriyatrik pop�lasyon:
65 ya� ve �zeri hastalarda doz rejimi ayarlamas� gerekli de�ildir (bkz. B�l�m 5.2). ≥75 ya��ndaki hastalarda ve �zellikle ≥85 ya��ndaki hastalarda s�n�rl� veri bulunmaktad�r.
4.3. Kontrendikasyonlar
P�MREVA, etkin maddeye veya 6.1 b�l�m�nde listelenen yard�mc� maddelerden herhangi birine kar��l�k a��r� duyarl�l��� olan hastalarda kontrendikedir.
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Fulvestrant
Daha �nce fulvestrant kullanan hastalardaki s�n�rl� veriler nedeniyle (n=39, CBYL719X2101 �al��mas�), bu pop�lasyonda etkilili�in yerle�ik oldu�u kabul edilmemektedir (bkz. b�l�m 5.1).
A��r� duyarl�l�k (anafilaktik reaksiyonlar� i�eren)
P�MREVA ile tedavi edilen hastalarda dispne, k�zarma, d�k�nt�, ate� veya ta�ikardi dahil ancak bunlarla s�n�rl� olmamak �zere semptomlarla kendini g�steren a��r� duyarl�l�k reaksiyonlar� (anafilaktik reaksiyon, anafilaktik �ok ve anjiyo�demi i�eren) bildirilmi�tir (bkz. B�l�m 4.8).
Ciddi a��r� duyarl�l�k reaksiyonlar� olan hastalarda P�MREVA tamamen kesilmeli ve tekrar kullan�lmamal�d�r. Derhal uygun tedaviye ba�lanmal�d�r.
�iddetli kutan�z reaksiyonlar
P�MREVA ile tedavi edilen hastalarda �iddetli kutan�z reaksiyonlar bildirilmi�tir.
Faz III klinik �al��mada, Stevens-Johnson sendromu (SJS) ve eritema multiforme (EM) s�ras�yla 1 (% 0,4) ve 3 (% 1,1) hastada bildirilmi�tir. PIMREVA ile tedavi edilen hastalarda, pazarlama sonras� deneyimde eozinofili ve sistemik semptomlar�n e�lik etti�i ila� reaksiyonu (DRESS) bildirilmi�tir (bkz. B�l�m 4.8.).
�iddetli kutan�z reaksiyon �yk�s� olan hastalarda P�MREVA tedavisi ba�lat�lmamal�d�r. Hastalar, �iddetli deri reaksiyonlar�n�nbelirti vesemptomlar� (�rn. ate� prodromu, grip benzeri
semptomlar, mukozal lezyonlar veya progresif deri d�k�nt�s�) hakk�nda bilgilendirilmelidir. �iddetli kutan�z reaksiyonlar�n belirtileri veya semptomlar� ortaya ��karsa, reaksiyonun etiyolojisi belirlenene kadar P�MREVA tedavisi kesilmelidir. Dermatolo�a dan���lmas� �nerilir.
�iddetli kutan�z reaksiyon do�rulan�rsa, P�MREVA bir daha ba�lanmamak �zere kesilmelidir. Daha �nce P�MREVA tedavisi s�ras�nda �iddetli kutan�z reaksiyonlar ya�ayan hastalarda P�MREVA tekrar kullan�lmaya ba�lanmamal�d�r.
�iddetli kutan�z reaksiyon do�rulanmad�ysa, P�MREVA i�in Tablo 3'te tarif edildi�i gibi tedaviye ara verilmesi, doz azalt�lmas� veya tedavinin kesilmesi gerekebilir (bkz. B�l�m 4.2).
Hiperglisemi
P�MREVA ile tedavi edilen hastalarda �iddetli hiperglisemi, baz� durumlarda hiperglisemik hiperosmolar nonketotik sendrom (HHNKS) ya da ketoasidoz ile ili�kili, bildirilmi�tir. Pazarlama sonras� deneyimde, baz� �l�mle sonu�lanan ketoasidoz vakalar� bildirilmi�tir.
Faz III klinik �al��mada, diyabetik hastalarda (12 hastan�n 0'�nda [%0] derece 1-2 ve 12 hastan�n 10'unda [%83,3] derece 3-4), pre-diyabetik hastalarda (159 hastan�n 42'sinde [%26,4] derece 1-2 ve 159 hastan�n 77'sinde [%48,4] derece 3-4), taramada VK�'si ≥30 olan hastalarda (74 hastan�n 13'�nde [%17,6] derece 1-2 ve 74 hastan�n 38'inde [%51,4] derece 3-4) veya ≥75 ya��nda olan
hastalarda (34 hastan�n 6's�nda [%17,6] derece 1-2 ve 34 hastan�n 19'unda [%55,9] derece 3-4) hiperglisemi daha s�k g�r�lm��t�r.
Tedaviye ba�lad�ktan sonra hiperglisemi h�zl� bir ba�lang��la meydana gelebilece�inden, ilk 4 haftada ve �zellikle tedavinin ilk 2 haftas�nda hastan�n s�k s�k ve klinik durumun gerektirdi�i �ekilde kendi kendine izlem yapmas� �nerilir. Tablo 6'da a�l�k glukoz izlemi i�in �zel bir program �nerilmektedir.
Faz III klinik �al��mada diyabet �yk�s� olan hastalar, P�MREVA tedavisi s�ras�nda antidiyabetik t�bbi �r�nlerin kullan�m�n� yo�unla�t�rm��t�r.
T�m hastalar hiperglisemiyi azaltabilecek ya�am tarz� de�i�iklikleri (�rn. diyet k�s�tlamalar� ve fiziksel aktivite) konusunda bilgilendirilmelidir.
Tablo 6 A�l�k glukoz izleme program�
| P�MREVA ile tedavi edilen t�m hastalarda a�l�k glukoz ve HbA1c'nin izlemi i�in �nerilen program | P�MREVA ile tedavi edilen diyabetik, prediyabetik, v�cut kitle indeksi ≥30 olan veya 75 ya� ve �st� hastalarda a�l�k glukozu ve HbA1c d�zeylerinin izlemi i�in �nerilen program |
Tarama zaman�nda, P�MREVA | A�l�k plazma glukozu (APG), HbA1c i�in test yap�l�r ve hastan�n kan glukoz d�zeyi optimize edilir (bkz. Tablo 2) | |
tedavisine ba�lanmadan �nce |
| |
P�MREVA tedavisine ba�land�ktan sonra | Tedavi ba�lad�ktan sonraki 1,2,4,6 ve 8. haftalarda ve sonras�nda ayl�k olarak APG izlenir. | |
�lk 4 haftada daha s�k olmak �zere ve �zellikle de tedavinin ilk 2 haftas�nda bir sa�l�k profesyonelinin talimatlar� do�rultusunda a�l�k glukozu izlenir/�zizlenir*. | Tedavinin ilk 2 haftas�nda a�l�k glukozu haftada en az iki kez veya glukoz de�erlerine g�re klinik durumun gerektirdi�i �ekilde daha s�k izlenir/�zizlenir. Daha sonra bir sa�l�k profesyonelinin talimatlar�na g�re hiperglisemiyi y�netmek i�in a�l�k glukozu gerekli s�kl�kla izlenmeye devam edilir*. | |
HbA1c, 4 haftal�k tedaviden sonra ve daha sonra her 3 ayda bir izlenmelidir. | ||
P�MREVA tedavisine ba�land�ktan sonra hiperglisemi ortaya ��karsa | A�l�k glukozu lokal tedavi standard�na g�re ve en az�ndan a�l�k glukozu normal seviyelere d��ene kadar d�zenli olarak izlenir. | |
Antidiyabetik ila�larla tedavi s�ras�nda, a�l�k glukozu 8 hafta boyunca haftada en az bir kez, ard�ndan 2 haftada bir takip edilmeye devam edilir ve a�l�k glukozu, hipergliseminin tedavisi konusunda uzmanl��� olan bir sa�l�k profesyonelinin talimatlar�na g�re izlenir. | ||
*T�m glukoz izlemeleri, hekimin takdirinde klinik durumun gerektirdi�i �ekilde ger�ekle�tirilmelidir. | ||
Hastalara hiperglisemi belirtileri ve semptomlar� konusunda bilgi verilmelidir (�rn. a��r� susama, normalden daha s�k idrara ��kma veya normalden daha fazla idrar, kilo kayb� birlikte i�tah art���).
Hiperglisemili 190 hastan�n %87,4'� (166/190) antidiyabetik ila�la tedavi edilmi�tir ve %75,8'i (144/190) metforminin tek ajan olarak veya di�er antidiyabetik ila�lar (�rn. ins�lin, dipeptidil peptidaz-4 (DPP-4) inhibit�rleri, SGLT2 inhibit�rleri ve s�lfonil�reler) ile kombine kullan�ld���n� bildirmi�tir.
154 hastada, oral antidiyabetik ila� tedavisi kullan�lm��t�r. Bu 154 hastadan, 17'si (% 11,0) hiperglisemiye ba�l� olarak �al��ma tedavisini b�rakm��t�r. 54 hastada e�lik eden ins�lin ilac� kullan�lm��t�r; bunlar aras�nda 13 hastada (% 24,1) hiperglisemiye ba�l� olarak �al��ma tedavisi kesilmi�tir.
Derece ≥2 hiperglisemisi olan 162 hastadan 155'inde en az 1 derece iyile�me mevcuttur. �lk olaydan itibaren ge�en medyan iyile�me s�resi 8 g�nd�r (% 95 GA: 8 ila 10 g�n).
P�MREVA'y� b�rakt�ktan sonra fulvestrant tedavisine devam eden y�ksek APG'li hastalar�n (n = 58) %98,3'�nde (n = 57) APG seviyeleri ba�lang�� seviyesine (normal) geri d�nm��t�r.
Tip 1 ve kontrols�z Tip 2 diyabetli hastalarda P�MREVA'n�n g�venlili�i belirlenmemi�tir ��nk� bu hastalar faz III klinik �al��maya dahil edilmemi�tir. Tip 2 diyabet �yk�s� olan hastalar dahil
edilmi�tir. Diyabet �yk�s� olan hastalarda yo�un diyabetik tedavi gerekebilir ve bu hastalar yak�ndan izlenmelidir.
Hipergliseminin �iddetine ba�l� olarak, P�MREVA i�in, Tablo 2'de tarif edildi�i gibi tedaviye ara verme, doz azalt�m� veya tedavinin kesilmesini gerekebilir (bkz. B�l�m 4.2).
Pn�monit
Klinik �al��malarda P�MREVA ile tedavi edilen hastalarda ciddi pn�monit ve akut interstisyel akci�er hastal��� vakalar� dahil olmak �zere pn�monit vakalar� bildirilmi�tir. Hastalar, yeni veya k�t�le�en solunum yolu semptomlar�n� derhal bildirmeleri konusunda bilgilendirilmelidir. Yeni veya k�t�le�en solunum yolu semptomlar� olan veya pn�monit geli�ti�inden ��phelenilen hastalarda P�MREVA tedavisi derhal kesilmeli ve hasta pn�monit a��s�ndan de�erlendirilmelidir. Hipoksi, �ks�r�k, dispne veya radyolojik muayenede interstisyel infiltrasyonlar gibi spesifik olmayan solunum bulgular� ve semptomlar� olan ve uygun incelemeler ile enfeksiy�z, neoplastik nedenlerin ve di�er nedenlerin d��land��� hastalarda enfeksiy�z olmayan pn�monit tan�s� d���n�lmelidir. Pn�moniti do�rulanan t�m hastalarda P�MREVA bir daha ba�lanmamak �zere kesilmelidir.
�shal veya kolit
Diyare veya kar�n a�r�s� ve d��k�da mukus veya kan gibi kolitin di�er semptomlar� i�in hastalar izlenmelidir.
P�MREVA ile tedavi s�ras�nda �iddetli ishal ve klinik sonu�lar�, dehidratasyon ve akut b�brek hasar� olan vakalar bildirilmi�tir ve uygun m�dahale ile giderilmi�tir. Hastalar�n % 59,5'inde (n=169) P�MREVA tedavisi s�ras�nda ishal g�r�lm��t�r. Hastalar�n %7'sinde (n = 20) derece 3 ishal meydana gelmi�tir ve derece 4 ishal raporlanmam��t�r. Derece 2 veya 3 ishal (n = 76) olan hastalarda olay ba�lang�c�na kadar ge�en medyan s�re 50 g�nd�r (aral�k: 1 ila 954 g�n).
�shal nedeniyle hastalar�n % 5,6's�nda P�MREVA dozunun azalt�lmas� gerekmi�tir ve hastalar�n
%2,8'inde P�MREVA tedavisi bir daha ba�lanmamak �zere kesilmi�tir. �shal ge�iren 169 hastada, semptom kontrol� i�in % 64,5 (109/169) oran�nda antidiyare ila�lar� (�rn., loperamid) gerekmi�tir.
�shalin veya kolitin ciddiyetine ba�l� olarak, P�MREVA i�in Tablo 4'te tarif edildi�i gibi doza ara verilmesi, dozun azalt�lmas� veya kesilmesi gerekebilir (bkz. B�l�m 4.2).
Hastalar, P�MREVA al�rken ishal veya kolitin di�er semptomlar� meydana gelirse antidiyare tedavisine ba�lamas�, oral s�v�lar� artt�rmas� ve doktoruna bildirmesi konusunda bilgilendirilmelidir. Kolit g�r�lmesi halinde, steroid gibi ilave tedaviler klinik durum gerektirdi�i s�rece d���n�lebilir.
�ene Osteonekrozu
P�MREVA ve bifosfonatlar veya RANK-ligand inhibit�rleri (�rn., denosumab) ayn� anda veya arka arkaya kullan�ld���nda dikkatli olunmal�d�r. P�MREVA, bifosfonatlar veya denosumab ile �nceki veya e�zamanl� tedaviden kaynaklanan �ene osteonekrozu tedavisi devam eden hastalarda ba�lat�lmamal�d�r. Hastalar, P�MREVAtedavisis�ras�ndayeni veya k�t�le�en oral semptomlar�
(di� hareketlili�i, a�r� ve �i�lik, iyile�meyen a��z yaralar� veya ak�nt� gibi) derhal bildirilmeleri konusunda bilgilendirilmelidir.
P�MREVA ile tedavi s�ras�nda �ene osteonekrozu geli�en hastalarda, standart t�bbi tedavi ba�lat�lmal�d�r.
Semptomatik viseral hastal�k
Semptomatik viseral hastal��a sahip hastalarda bu t�bbi �r�n�n etkilili�i ve g�venlili�i �al���lmam��t�r.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
P�MREVA plazma konsantrasyonunu artt�ran t�bbi �r�nler
BCRP inhibit�rleri
Alpelisib, BCRP in vitro i�in bir substratt�r. BCRP, alpelisibin hepatobiliyer at�l�m� ve ba��rsak salg�lanmas�nda rol oynar, bu nedenle BCRP'nin karaci�erde ve ba��rsakta eliminasyon s�ras�nda inhibisyonu, alpelisibin sistemik maruziyetinde bir art��a neden olabilir. Bu nedenle, P�MREVA BCRP inhibit�rleri (�rn., eltrombopag, lapatinib, pantoprazol) ile birlikte kullan�ld���nda, toksisite a��s�ndan dikkat edilmeli ve izlem yap�lmal�d�r.
P�MREVA plazma konsantrasyonunu azaltan t�bbi �r�nler
Asit azalt�c� maddeler
H2 resept�r antagonisti ranitidinin, tek bir 300 mg oral alpelisib dozu ile birlikte uygulanmas�, alpelisibin biyoyararlan�m�n� hafif�e azaltm��t�r ve alpelisibin genel maruziyetinde azalmaya neden olmu�tur. D���k ya�l� d���k kalorili (DYDK) bir ���n�n varl���nda, ranitidin ile EAAinf ortalama %21 ve Cmaks %36 azalm��t�r. Bu etki g�da yoklu�unda daha belirgin olmu�, birlikte ranitidinin uygulanmad��� a�l�k duruma k�yasla, ranitidin ile EAAinf de�erinde %30 azalma, Cmaks de�erinde de %51 azalma meydana gelmi�tir. Pop�lasyon farmakokinetik analizi, proton pompas� inhibit�rleri, H2 resept�r antagonistleri ve antasitler dahil olmak �zere asit indirgeyici ajanlar�n birlikte uygulanmas�n�n alpelisib farmakokineti�i �zerinde anlaml� bir etkisi g�stermemi�tir. Bu nedenle, alpelisib, alpelisibin yemekten hemen sonra al�nmas� kayd�yla, asit azalt�c� ajanlarla birlikte uygulanabilir (bkz. B�l�m 4.2).
CYP3A4 ind�kleyicileri
7 g�n boyunca g�nde bir kez 600 mg rifampinin (g��l� bir CYP3A4 ind�kleyicisi) uygulamas�n� takiben 8. g�nde tek bir 300 mg oral alpelisib dozu ile birlikte uygulanmas�, sa�l�kl� yeti�kinlerde alpelisib Cmaks'�n� %38 ve EAA's�n� %57 azaltm��t�r (N=25). 15 g�n boyunca g�nde bir kez 600 mg rifampinin 8. g�nden ba�layarak g�nde bir kez 300 mg alpelisib ile birlikte uygulanmas�, kararl� durum alpelisib Cmaks'�n� %59 ve EAA's�n� %74 oran�nda azaltm��t�r.
G��l� bir CYP3A4 ind�kleyicisi ile birlikte uygulama, alpelisib EAA's�n� azalt�r ki bu, alpelisib etkilili�ini azaltabilir. Alpelisibin g��l� CYP3A4 ind�kleyicileri (�rn. apalutamid, karbamazepin, enzalutamid, mitotan, fenitoin, rifampin, sar� kantaron) ile birlikte uygulanmas�ndan ka��n�lmal�
ve CYP3A4'� ind�kleme potansiyeli olmayan veya minimum d�zeyde olan alternatif bir e�zamanl� t�bbi �r�n se�imi yap�lmal�d�r.
Plazma konsantrasyonlar� P�MREVA taraf�ndan de�i�tirilebilen t�bbi �r�nler
Metabolik in vitro ind�ksiyon ve inhibisyon �al��malar�n�n sonu�lar�na dayanarak, alpelisib, in vivo ortamda yeterince y�ksek konsantrasyonlar elde edildi�i takdirde CYP2B6, CYP2C9 ve CYP3A taraf�ndan metabolize edilen birlikte uygulanan t�bbi �r�nlerin metabolik klirensini ind�kleyebilir ve CYP2C8,CYP2C9,CYP2C19 ve CYP3A4 taraf�ndan metabolize edilen birlikte uygulanan t�bbi �r�nlerin metabolik klirensini inhibe edebilir (zamana ba��ml� inhibisyon).
CYP3A4 substratlar�
P�MREVA, CYP3A4 substratlar� (�r. everolimus, midazolam) ile birlikte uygulan�rken doz ayarlamas�na gerek yoktur.
Bir ila�-ila� etkile�imi �al��mas�nda, alpelisibin hassas bir CYP3A4 substrat� olan everolimus ile birlikte uygulanmas�, alpelisib ile CYP3A4 substratlar� aras�nda klinik olarak anlaml� farmakokinetik etkile�imlerin (EAA de�erinde %11,2 art��) olmad���n� do�rulam��t�r. 250 ila 300 mg aras�nda de�i�en alpelisib dozlar�nda everolimus maruziyetinde bir de�i�iklik g�zlenmemi�tir.
P�MREVA, CYP3A4 �zerinde kendi metabolizmas�n� etkileyen ek bir zamana ba�l� inhibisyon ve ind�ksiyon potansiyeline sahip CYP3A4 substratlar� ile kombinasyon halinde kullan�ld���nda dikkatli olunmal�d�r (�rn. rifampisin, ribosiklib, encorafenib).
Dar terap�tik indekse sahip CYP2C9 substratlar�
CYPC29 ile ilgili klinik verilerin yoklu�unda, dikkatli olunmas� �nerilir. In vitro de�erlendirmeler, varfarin gibi dar bir terap�tik indekse sahip CYP2C9 substratlar�n�n farmakolojik aktivitesinin alpelisibin CYP2C9 ind�ksiyon etkileri ile azalt�labilece�ini g�stermi�tir.
Dar terap�tik indekse sahip CYP2B6 duyarl� substratlar
Alpelisib, bu t�r t�bbi �r�nlerin klinik aktivitesini azaltabilece�inden, duyarl� CYP2B6 substratlar� (�rn. bupropion) veya dar bir terap�tik pencereye sahip CYP2B6 substratlar�, P�MREVA ile kombinasyon halinde dikkatle kullan�lmal�d�r.
Ta��y�c�lar�n substratlar� olan maddeler
In vitro de�erlendirmeler, alpelisibin (ve/veya BZG791 metabolitinin) OAT3 ila� ta��y�c�lar�n�n ve ba��rsak BCRP ve P-gp'nin aktivitelerini inhibe etme potansiyeline sahip oldu�unu g�stermi�tir. P�MREVA, dar bir terap�tik indeks sergileyen bu ta��y�c�lar�n duyarl� substratlar� ile kombinasyon halinde dikkatli kullan�lmal�d�r ��nk� P�MREVA bu substratlar�n maruziyetini art�rabilir.
Hormonal kontraseptifler
Alpelisib ve hormonal kontraseptifler aras�ndaki ila�-ila� etkile�imi potansiyelini de�erlendiren hi�bir klinik �al��ma yap�lmam��t�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
Etkile�im a��s�ndan �zel pop�lasyonlara ili�kin veri bulunmamaktad�r.
Pediyatrik pop�lasyon:
Etkile�im a��s�ndan pediyatrik pop�lasyona ili�kin veri bulunmamaktad�r.
4.6. Gebelik ve laktasyon
Gebelik kategorisi: C
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
Hayvan verilerine ve etki mekanizmas�na dayanarak, P�MREVA gebe bir kad�na uyguland���nda fetal zarara neden olabilir. S��an ve tav�anlar ile yap�lan embriyo-fetal geli�tirme �al��malar�nda, P�MREVA'n�n organogenez s�ras�nda oral yoldan verilmesinin embriyotoksisite, fetotoksisite ve teratojenisiteyi ind�kledi�ini g�stermi�tir.
�reme potansiyeli olan kad�nlar�n P�MREVA tedavisi s�ras�nda ve son dozu takip eden 1 hafta boyunca etkili do�um kontrol y�ntemleri (�rn., �ift bariyer metodu) kullan�lmal�d�r.
Erkekler
Gebe olan, gebe olma ihtimali bulunan veya gebe kalabilecek cinsel partnerleri olan erkek hastalar, P�MREVA al�rken ve P�MREVA ile tedaviyi b�rakt�ktan sonra en az 1 hafta boyunca prezervatif ve etkili do�um kontrol� kullanmal�d�r.
Fulvestrant�n K�sa �r�n Bilgisi B�l�m 4.6'ya bak�n�z.
Gebelik d�nemi
P�MREVA'n�n gebe kad�nlarda kullan�m�na ili�kin yeterli veri mevcut de�ildir.
Hayvanlar �zerinde yap�lan ara�t�rmalar, �reme toksisitesinin bulundu�unu g�stermi�tir (bkz. B�l�m 5.3). �nsanlara y�nelik potansiyel risk bilinmemektedir.
P�MREVA, gerekli olmad�k�a gebelik d�neminde kullan�lmamal�d�r.
P�MREVA tedavisine ba�lanmadan �nce �reme potansiyeli olan kad�nlarda gebelik durumu do�rulanmal�d�r.
Laktasyon d�nemi
Alpelisibin insan ya da hayvan s�t� ile at�ld���na iliskin yetersiz/s�n�rl� bilgi mevcuttur. Alpelisibin s�t ile at�lmas�na y�nelik fizikokimyasal ve eldeki farmakodinamik/toksikolojik veriler nedeniyle memedeki �ocuk a��s�ndan bir risk oldu�u g�z ard� edilemez. P�MREVA emzirme d�neminde kullan�lmamal�d�r.
Emzirilen bebekte ciddi advers reaksiyon potansiyeli nedeniyle, kad�nlar�n tedavi s�ras�nda ve son P�MREVA dozundan sonraenaz1haftaboyuncaemzirmemesi �nerilir.
�reme yetene�i/Fertilite
P�MREVA'n�n fertilite �zerindeki etkisi ile ilgili mevcut klinik veri bulunmamaktad�r. Hayvanlarda uygulanan tekrarl� doz toksisite ve fertilitesi �al��malar�na dayanarak, P�MREVA, erkek ve kad�nlarda �reme potansiyelini azaltabilir (bkz. B�l�m 5.3.).
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
P�MREVA'n�n ara� ve makine kullan�m� �zerinde min�r etkiye sahiptir. Hastalara, tedavi s�ras�nda yorgunluk veya bulan�k g�r�� hissetmeleri durumunda ara� veya makine kullan�rken dikkatli olmalar� �nerilmelidir (bkz. B�l�m 4.8).
4.8. �stenmeyen etkiler
G�venlilik profilinin �zeti
G�venlilik profili, �ift k�r, plasebo kontroll� Faz III �al��mas�n�n P�MREVA art� fulvestrant kolundaki 284 hastan�n verilerine dayanmaktad�r.
En yayg�n advers reaksiyonlar (kombine mutant ve mutant olmayan �al��ma pop�lasyonunda
>%20 s�kl�kla bildirilmi�tir) plazma glukoz art��� (%79,2), kreatinin art��� (%67,6), ishal (%59,5), gama-glutamiltransferaz art��� (%53,2), d�k�nt� (%51,8), lenfosit say�s� azalmas� (%55,3), bulant� (%46,8), alanin aminotransferaz art��� (%44,0), anemi (%44,0), yorgunluk (%43,3), lipaz art���
(%42,6), i�tah azalmas� (%35,9), stomatit (%30,3), kusma (%28,5), kilo kayb� (%27,8), hipokalsemi (%27,8), plazma glukozu azalmas� (%26,8), aktive parsiyel tromboplastin s�resi (aPTT) uzamas� (%22,2) ve alopesi (%20,4) olmu�tur.
En yayg�n derece 3 veya 4 advers reaksiyonlar (≥%2 s�kl�kla bildirilmi�tir) plazma glukoz art��� (%39,1), d�k�nt� (%19,4), gama-glutamiltransferaz art��� (%12,0), lenfosit say�s�nda azalma
(%9,2), ishal (%7,0), lipaz art��� (%7,0), hipokalemi (%6,3), yorgunluk (%5,6), kilo azalmas�
(%5,3), anemi (%4,9), hipertansiyon (%4,6), alanin aminotransferaz art��� (%4,2), bulant� (%2,8),
kreatinin art��� (%2,8), stomatit (%2,5), hipokalsemi (%2,1) ve mukozal enflamasyon (%2,1) olmu�tur.
Tedavinin kesilmesine yol a�an en yayg�n advers reaksiyonlar hiperglisemi (%6,3), d�k�nt� (%4,2), ishal (%2,8) ve yorgunluktur (%2,5).
Advers reaksiyonlar�n tablo halinde listesi
Faz III klinik �al��ma ve pazarlama sonras� deneyimlerden tespit edilen advers reaksiyonlar (Tablo 7) MedDRA sistem organ s�n�f� taraf�na g�re listelenmi�tir. Her bir sistem organ s�n�f� i�inde, advers reaksiyonlar s�kl��a g�re s�ralanmaktad�r ve ilk �nce en s�k g�r�len reaksiyonlar belirtilmektedir. Her bir s�kl�k grubunda, advers ila� reaksiyonlar� azalan ciddiyet s�ras�na g�re sunulmaktad�r. Ek olarak, her advers ila� reaksiyonu i�in kar��l�k gelen s�kl�k kategorisi, a�a��daki sisteme dayanmaktad�r:
�ok yayg�n (≥1/10); yayg�n (≥1/100 ila <1/10); yayg�n olmayan (≥1/1,000 ila <1/100); seyrek (≥1/10,000 ila <1/1,000); �okseyrek(<1/10.000),bilinmiyor(eldeki verilerden hareketle tahmin
edilemiyor).
Tablo 7 Faz III klinik �al��mada g�zlenen ve pazarlama sonras� tecr�be edilen advers reaksiyonlar
Advers ila� reaksiyonu | S�kl�k | ||
| Herhangi bir derece (%) | Derece 3 ya da 4 (%) | |
Enfeksiyonlar ve enfestasyonlar | |||
�drar yolu enfeksiyonu | �ok yayg�n | 29 (10,2) | 2 (0,7)* |
Kan ve lenfatik sistem hastal�klar� | |||
Anemi | �ok yayg�n | 125 (44,0) | 14 (4,9)* |
Lenfosit say�s�nda azalma | �ok yayg�n | 157 (55,3) | 26 (9,2) |
Trombosit say�s�nda azalma | �ok yayg�n | 43 (15,1) | 4 (1,4)* |
Ba����kl�k sistemi hastal�klar� | |||
A��r� duyarl�l�k | Yayg�n | 11 (3,9) | 2 (0,7)* |
Metabolizma ve beslenme hastal�klar� | |||
Plazma glukoz art��� | �ok yayg�n | 225 (79,2) | 111 (39,1) |
Plazma glukoz azalmas� | �ok yayg�n | 76 (26,8) | 1 (0,4) |
��tah azalmas� | �ok yayg�n | 102 (35,9) | 2 (0,7)* |
Hipokalemi | �ok yayg�n | 42 (14,8) | 18 (6,3) |
Hipokalsemi | �ok yayg�n | 79 (27,8) | 6 (2,1) |
Magnezyum azalmas� | �ok yayg�n | 34 (12,0) | 1 (0,4) |
Dehidrasyon | Yayg�n | 10 (3,5) | 1 (0,4)* |
Ketoasidoz | Yayg�n olmayan | 2 (0,7) | 2 (0,7) |
Hiperglisemik hiperosmolar nonketotik sendrom (HHNKS) | Bilinmiyor | Bilinmiyor | Bilinmiyor |
Psikiyatrik hastal�klar | |||
Uykusuzluk | Yayg�n | 22 (7,7) |
|
Sinir sistemi bozukluklar� | |||
Ba� a�r�s� | �ok yayg�n | 55 (19,4) | 2 (0,7)* |
Disguzi | �ok yayg�n | 44 (15,5) | 1 (0,4)* |
G�z hastal�klar� | |||
Bulan�k g�rme | Yayg�n | 15 (5,3) | 1 (0,4)* |
Kuru g�z | Yayg�n | 10 (3,5) |
|
Vask�ler hastal�klar� | |||
Hipertansiyon | Yayg�n | 27 (9,5) | 13 (4,6) |
Lenf�dem | Yayg�n | 16 (5,6) |
|
Solunum, g���s hastal�klar� ve mediastinal hastal�klar | |||
Pn�monit | Yayg�n | 5 (1,8) | 1 (0,4)* |
Gastrointestinal hastal�klar� | |||
�shal | �ok yayg�n | 169 (59,5) | 20 (7,0)* |
Mide bulant�s� | �ok yayg�n | 133 (46,8) | 8 (2,8)* |
Stomatit | �ok yayg�n | 86 (30,3) | 7 (2,5)* |
Kusma | �ok yayg�n | 81 (28,5) | 2 (0,7)* |
Kar�n a�r�s� | �ok yayg�n | 50 (17,6) | 4 (1,4)* |
Haz�ms�zl�k | �ok yayg�n | 33 (11,6) |
|
Di� a�r�s� | Yayg�n | 13 (4,6) | 1 (0,4)* |
Di�eti iltihab� | Yayg�n | 11 (3,9) | 1 (0,4)* |
Di�eti a�r�s� | Yayg�n | 9 (3,2) |
|
Keilit | Yayg�n | 8 (2,8) |
|
Pankreatit | Yayg�n olmayan | 1 (0,4) | 1 (0,4) |
Kolit | Bilinmiyor | Bilinmiyor | Bilinmiyor |
Deri ve deri alt� doku hastal�klar� | |||
D�k�nt� | �ok yayg�n | 147 (51,8) | 55 (19,4)* |
Alopesi | �ok yayg�n | 58 (20,4) |
|
Ka��nt� | �ok yayg�n | 53 (18,7) | 2 (0,7)* |
Kuru cilt | �ok yayg�n | 53 (18,7) | 1 (0,4)* |
Eritem | Yayg�n | 18 (6,3) | 2 (0,7) |
Dermatit | Yayg�n | 10 (3,5) | 2 (0,7)* |
Palmar-plantareritrodisestezi sendromu | Yayg�n | 5 (1,8) |
|
Stevens-Johnson sendromu | Yayg�n olmayan | 1 (0,4) | 1 (0,4)* |
Eozinofili ve sistemik semptomlar�n e�lik etti�i ila� reaksiyonu (DRESS) | Bilinmiyor | Bilinmiyor | Bilinmiyor |
Anjiyo�dem | Bilinmiyor | Bilinmiyor | Bilinmiyor |
Kas-iskelet, ba� dokusu ve kemik hastal�klar� | |||
Kas spazmlar� | Yayg�n | 22 (7,7) |
|
Kas a�r�s� | Yayg�n | 19 (6,7) | 1 (0,4)* |
�ene osteonekrozu | Yayg�n | 16 (5,6) | 5 (1,8)* |
B�brek ve idrar yolu hastal�klar� | |||
Akut b�brek hasar� | Yayg�n | 16 (5,6) | 5 (1,8) |
Genel bozukluklar ve uygulama b�lgesine ili�kin durumlar | |||
Yorgunluk | �ok yayg�n | 123 (43,3) | 16 (5,6)* |
Mukozal enflamasyon | �ok yayg�n | 56 (19,7) | 6 (2,1)* |
Periferik �dem | �ok yayg�n | 47 (16,5) |
|
Y�ksek ate� | �ok yayg�n | 45 (15,8) | 2 (0,7) |
Mukozal kuruluk | �ok yayg�n | 36 (12,7) | 1 (0,4) |
�dem | Yayg�n | 18 (6,3) |
|
�ncelemeler | |||
Kilo kayb� | �ok yayg�n | 79 (27,8) | 15 (5,3)* |
Kan kreatinin art��� | �ok yayg�n | 192 (67,6) | 8 (2,8)* |
Gama-glutamiltransferaz art��� | �ok yayg�n | 151 (53,2) | 34 (12,0) |
Alanin aminotransferaz art��� | �ok yayg�n | 125 (44,0) | 12 (4,2)* |
Lipaz art��� | �ok yayg�n | 121 (42,6) | 20 (7,0) |
Aktive parsiyel tromboplastin s�resi (aPTT) uzamas� | �ok yayg�n | 63 (22,2) | 2 (0,7) |
Alb�min azalmas� | �ok yayg�n | 41 (14,4) | 1 (0,4) |
Glikozile hemoglobin art��� | Yayg�n | 8 (2,8) | 0 |
* Derece 4 advers ila� reaksiyonu g�zlenmemi�tir �drar yolu enfeksiyonu:ayr�catekbir�rosepsis vakas�n�da i�erir o�rulama Kodu: 1ZW56Q3NRM0FyM0FyZW56ZW56S3k0SHY3 | |||

Hipersensitivite: ayr�ca alerjik dermatiti de i�erir Ketoasidoz: ayr�ca diyabetik ketoasidozu da i�erir Disguzi: ayr�ca aguzi, hipoguziyi de i�erir
Pn�monit: ayr�ca interstisyel akci�er hastal���n� da i�erir Stomatit: ayr�ca aft�z �lser ve a��z �lserini de i�erir
D�k�nt�: ayr�ca makulopap�ler d�k�nt�, mak�ler d�k�nt�, yayg�n d�k�nt�, pap�ler d�k�nt�, ka��nt�l� d�k�nt�y� de i�erir
Kuru deri: ayr�ca deri �atlaklar�, kseroz, kserodermay� da i�erir Eritem: ayr�ca yayg�n eritemi de i�erir
Dermatit: ayr�ca dermatit akneiformu da i�erir Yorgunluk: asteniyi de i�erir
Mukozal kuruluk: ayr�ca a��z kurulu�u, vulvovajinal kurulu�u da i�erir
�dem: ayr�ca y�z �i�mesi, y�z �demi, g�z kapa�� �demini de i�erir
Se�ilen advers reaksiyonlar�n tan�m�
Hiperglisemi
190 (%66,9) hastada hiperglisemi (APG >160 mg/dl) bildirilmi�tir; derece 2 (APG 160-250
mg/dl), 3 (APG> 250-500 mg/dl) ve 4 (APG> 500 mg/dl) olaylar s�ras�yla hastalar�n %16,2, %33,8 ve %4,6's�nda rapor edilmi�tir.
Ba�lang�� APG ve HbA1c de�erlerine dayanarak, hastalar�n %56's� prediyabetik (APG> 100-126 mg/dl [5,6 ila 6,9 mmol/l] ve/veya HbA1c %5,7-6,4) ve %4,2'si diyabetik (APG ≥126 mg/dl [≥7,0 mmol/l] ve/veya HbA1c ≥%6,5) kabul edilmi�tir. Ba�lang��ta diyabetik olan hastalar�n %74,8'inde alpelisib ile tedavi edildi�inde hiperglisemi (herhangi bir derece) g�r�lm��t�r. ≥2 derece hiperglisemi (APG ≥160 mg/dl) olan t�m hastalar aras�nda, olay�n ilk ortaya ��kma s�resi medyan 15 g�n olmu�tur (aral�k: 5 g�n ila 900 g�n) (laboratuvar bulgular�na g�re). Derece 2 hiperglisemi medyan s�resi 10 g�n olmu�tur (%95 GA: 8 ila 13 g�n). Derece 2 hiperglisemisi olan hastalarda, medyan iyile�me s�resi (ilk olaydan en az bir derece) 8 g�n olmu�tur (%95 GA: 8 ila 10 g�n). P�MREVA'y� b�rakt�ktan sonra fulvestrant kullanmaya devam eden t�m hastalarda APG seviyeleri ba�lang�� seviyesine (normal) d�nm��t�r.
Hiperglisemi, antidiyabetik t�bbi �r�nlerle tedavi edilmi�tir (bkz. B�l�m 4.4)
D�k�nt�
153 hastada (%53,9) d�k�nt� olaylar� (makulopap�ler, mak�ler, jeneralize, pap�ler ve ka��nt�l� d�k�nt�, dermatit ve dermatit akneiform dahil) bildirilmi�tir. D�k�nt� a��rl�kl� olarak hafif veya orta �iddetli olmu� (derece 1 veya 2) ve tedaviye yan�t vermi�tir ve baz� durumlarda d�k�nt�ye ka��nt� ve kuru cilt e�lik etmi�tir. Hastalar�n s�ras�yla %13,7 ve %20,1'inde maksimum derece 2 ve 3 d�k�nt� olay� bildirilmi� olup ba�lang�ca kadar ge�en medyan s�re 12 g�nd�r (Aral�k:2 g�n
ila 220 g�n).
Antihistaminikler de dahil olmak �zere profilaktik d�k�nt� tedavisi alan hastalar aras�nda d�k�nt� genel pop�lasyona g�re daha az bildirilmi�tir; t�m dereceler i�in %26,1'e kar�� %53,9, derece 3 i�in %11,4'e kar�� %20,1 ve P�MREVA'n�n kal�c� olarak kesilmesine yol a�an d�k�nt� i�in
%3,4'e kar�� %4,2. Buna g�re, antihistaminikler, P�MREVA ile tedavinin ba�lamas� s�ras�nda profilaktik olarak ba�lat�labilir.
Gastrointestinal toksisite (bulant�, ishal, kusma)
Hastalar�n s�ras�yla %59,5, %46,8 ve %28,5'inde ishal, bulant� ve kusma bildirilmi�tir (bkz. Tablo 7).
Hastalar�n s�ras�yla %19,7 ve %7,0'�nda derece 2 ve 3 ishal olaylar� bildirilmi� olup derece ≥2 ishal ba�lang�c�na kadar medyan s�re ortalama 50 g�nd�r (aral�k: 1 g�n ila 954 g�n).
P�MREVA ile tedavi s�ras�nda �iddetli ishal ve dehidrasyon ve akut b�brek hasar� gibi klinik sonu�lar bildirilmi�tir ve uygun m�dahale ile bunlar giderilmi�tir (bkz. Tablo 4). Semptomlar� y�netmek i�in s�ras�yla 28/153 (%17,6) ve 109/169 (%64,5) hastada antiemetikler (�rn. ondansetron) ve anti-diyare t�bbi �r�nleri (�rn. loperamid) kullan�lm��t�r.
�ene osteonekrozu
P�MREVA art� fulvestrant kolundaki %5,6 hastada (16/284) �ene osteonekrozu bildirilmi�tir. �ene osteonekrozu ya�ayan 15 hasta e�lik eden bisfosfonatlar (�rn. zoledronik asit) yada RANK- ligand inhibit�r� (�rn. denosumab) kullanm��t�r. Dolay�s�yla, P�MREVA ve bisfosfonatlar yada RANK-ligand inhibit�r� alan hastalarda, artm�� �ene osteonekrozu geli�me riski olas�l�k d��� b�rak�lamamaktad�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
Geriyatrik pop�lasyon:
Alpelisib art� fulvestrant ile tedavi edilen 65 ya��n �zerindeki hastalarda, 65 ya��n alt�ndaki hastalara (%33,5) k�yasla derece 3-4 hiperglisemi insidans� (%45,3) daha y�ksek iken, 75 ya��n alt�ndaki hastalarda derece 3-4 hiperglisemi %36 ve ≥75 ya� grubunda %55,9 olmu�tur.
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar / risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr; e- posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99)
4.9. Doz a��m� ve tedavisi
Semptomlar
Tedavi
Gerekti�inde t�m doz a��m� vakalar�nda genel semptomatik ve destekleyici �nlemler al�nmal�d�r. P�MREVA i�in bilinen bir antidot yoktur.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Antineoplastik ajanlar, di�er antineoplastik ajanlar ATC kodu: L01EM03
Etki mekanizmas�
Alpelisib, a��rl�kl� olarak PI3Kα'ya kar��l�k �nleyici aktiviteye sahip bir fosfatidilinositol-3- kinaz (PI3K) inhibit�r�d�r. PI3K'n�n katalitik α alt birimini kodlayan gendeki (PIK3CA) fonksiyon kazanma mutasyonlar�, in vitro ve in vivo modellerde PI3Kα ve AKT sinyallemesinin aktivasyonuna, h�cresel transformasyona ve t�m�r olu�umuna yol a�ar.
Meme kanseri h�cre dizilerinde, alpelisib, AKT dahil PI3K a�a�� ak�m hedeflerinin fosforilasyonunu inhibe etmi� ve bir PIK3CA mutasyonu bar�nd�ran h�cre dizilerinde aktivite g�stermi�tir.
�n vivo ortamda, alpelisib, PI3K/Akt sinyal yolunu inhibe etmi� ve meme kanseri modelleri de dahil olmak �zere ksenograft modellerinde t�m�r b�y�mesini azaltm��t�r.
Alpelisib tedavisi ile PI3K inhibisyonunun meme kanseri h�crelerinde �strojen resept�r� (ER) transkripsiyonunda bir art��a neden oldu�u g�sterilmi�tir. Alpelisib ve fulvestrant kombinasyonu, ER pozitif, PIK3CA mutasyona u�ram�� meme kanseri h�cre dizilerinden t�retilen ksenograft modellerinde tek ba��na tedaviye k�yasla artm�� antit�m�r aktivitesi g�stermi�tir.
PI3K/AKT sinyal yolu, glukoz homeostaz�ndan sorumludur ve hiperglisemi, PI3K inhibisyonunun hedeflenen bir advers reaksiyonudur.
Klinik etkililik ve g�venlilik
P�MREVA, hastal��� aromataz inhibit�r� bazl� bir tedavi (CDK4/6 kombinasyonu olsun veya olmas�n) s�ras�nda veya sonras�nda progrese olmu� veya n�ks etmi� olan, HR+, HER2- ilerlemi� (lokal-b�lgesel tekrarlayan veya metastatik) meme kanseri olan postmenopozal kad�nlarda ve erkeklerde pivotal, faz III, randomize, �ift k�r, plasebo kontroll� bir �al��mada de�erlendirilmi�tir.
Toplam 572 hasta, biri PIK3CA mutasyonu olan, di�eri ise PIK3CA mutasyonu olmayan meme kanserini i�eren iki kohorta al�nm��t�r. Hastalar alpelisib 300 mg art� fulvestrant veya plasebo art� fulvestrant almak �zere 1: 1 oran�nda randomize edilmi�tir. Randomizasyon, akci�er ve/veya karaci�er metastaz� varl��� ve CDK4/6 inhibit�r�/inhibit�rleri ile �nceden tedaviye g�re stratifiye edilmi�tir.
PIK3CA mutasyonu olan kohortta, bir veya daha fazla PIK3CA mutasyonu olan (C420R, E542K, E545A, E545D [sadece 1635G> T], E545G, E545K, Q546E, Q546R, H1047L, H1047R veya
H1047Y) 169 hasta fulvestrant ile kombinasyon halinde alpelisib almak i�in randomize edilmi�tir ve 172 hasta fulvestrant ile kombinasyon halinde plasebo almak �zere randomize edilmi�tir. Bu kohortta 170 (%49,9) hastada karaci�er/akci�er metastaz� vard�r ve 20 (%5,9) hastaya �nceden CDK4/6 inhibit�r tedavisi uygulanm��t�r.
Hastalar�n medyan ya�� 63't�r (aral�k: 25 ila 92 y�l). Hastalar�n %44,9'u ≥65 ya��nda ve ≤85 ya��ndad�r. Dahil edilen hastalar Beyaz (%66,3), Asyal� (%21,7) ve Siyah veya Afro-Amerikand�r (%1,2). �al��ma pop�lasyonu, PIK3CA mutant kohortuna kay�tl� ve alpelisib ve fulvestrant ile tedavi edilen bir erkek olguyu i�ermi�tir. Olgular�n %66,0 ve %33,4'�nde ECOG performans durumu s�ras�yla 0 ve 1'dir.
Hastalar�n %97,7'si daha �nce endokrin tedavisi alm��t�r. Olgular�n %67,7'sinde �al��maya giri� �ncesinde son tedavi endokrin tedavisidir. Letrozol ve anastrozol en s�k kullan�lan endokrin tedaviler olmu�tur. �al��maya kaydolmadan �nce son endokrin tedavisi, olgular�n %47,8'inde terap�tik ve olgular�n %51,9'unda adjuvan tedavidir. Genel olarak, hastalar�n %85,6's�n�n endokrine diren�li bir hastal��� oldu�u d���n�lm��t�r; primer endokrin direnci (de novo direnci) hastalar�n %13,2 ve sekonder endokrin direnci (ba�lang�� yan�t�n� takiben n�ks/progresyon)
%72,4'�nde g�zlenmi�tir.
Demografik �zellikler ve �al��ma ba�lang�c�ndaki hastal�k �zellikleri, ECOG performans durumu, t�m�r y�k� ve �nceki antineoplastik tedavi �al��ma kollar� aras�nda iyi dengelenmi�tir.
Randomize tedavi faz� s�ras�nda, alpelisib 300 mg veya plasebo g�nde bir kez s�rekli olarak oral yoldan uygulanm��t�r. Fulvestrant 500 mg, birinci siklusun 1 ve 15. g�nlerde ve daha sonra tedavi a�amas�nda 28 g�nl�k bir siklusun 1. g�n�nde (uygulama ± 3 g�n) intram�sk�ler uygulanm��t�r.
Hastalar�n �al��ma s�ras�nda veya hastal�k ilerledikten sonra plasebodan alpelisibe ge�mesine izin verilmemi�tir.
�al��ma i�in birincil sonlan�m noktas�, PIK3CA mutasyonlu ileri evre kanseri olan hastalarda ara�t�rmac� de�erlendirmesine dayanan RECIST v1.1 kullan�larak progresyonsuz sa�kal�m (PFS) olmu�tur. �nemli ikincil sonlan�m noktas� PIK3CA mutasyon durumu olan hastalar i�in genel sa�kal�md�r (OS).
Di�er ikincil sonlan�m noktalar� aras�nda PIK3CA mutasyonu olmayan hastalar i�in PFS, PIK3CA mutasyonu olmayan hastalar i�in OS yer alm��t�r.
Birincil etkililik analizi
�al��ma, nihai PFS analizinde birincil hedefine ula�arak (veri kesme tarihi 12 Haziran 2018), PIK3CA mutant kohortunda plasebo art� fulvestrant alan hastalara k�yasla alpelisib art� fulvestrant alan hastalarda ara�t�rmac� de�erlendirmesine g�re alpelisib art� fulvestrant ile tedavi lehine hastal�k progresyonu veya �l�m riskinde tahmini %35 azalma ile (bkz. Tablo 8) PFS'de istatistiksel olarak anlaml� bir iyile�me oldu�unu g�stermi�tir.
Tablo 8 �al��ma C2301- Birincil etkililik analizi -RECIST'e (FAS, PIK3CA mutasyonlu kohort) dayal� etkililik sonu�lar�n��n �zeti. Veri kesme tarihi: 12 Haziran 2018
| P�MREVA + fulvestrant (n=169) | Plasebo + fulvestrant (n=172) |
Medyan progresyonsuz sa�kal�m (PFS) (ay, %95 GA) | ||
Ara�t�rmac�n�n radyolojik de�erlendirmesi | ||
PIK3CA mutant kohort | 11,0 | 5,7 |
(N=341) | (7,5-14,5) | (3,7-7,4) |
Tehlike oran� (% 95 GA) | 0,65 (0,50-0,85) | |
p-de�eri | 0,00065 | |
K�r ba��ms�z inceleme komitesi de�erlendirmesi* | ||
PIK3CA mutant kohort | 11,1 | 3,7 |
(N=173) | (7,3-16,8) | (2,1-5,6) |
Tehlike oran� (% 95 GA) | 0,48 (0,32-0,71) | |
p-de�eri | N/A | |
GA = g�ven aral���; N = hasta say�s�; N/A = uygulanamaz, tek tarafl� tabakal� log-s�ra testinden elde edilen p de�eri. RECIST 1.1'e g�re * %50 denetime dayal� yakla��ma dayan�r | ||
PIK3CA mutasyonu olan kohortta, randomizasyon stratifikasyon fakt�rleri ile ara�t�rmac� de�erlendirmesine g�re PFS alt grup analizleri, akci�er/karaci�er metastazlar�n�n varl���ndan veya yoklu�undan ba��ms�z olarak alpelisib kolu lehine homojen ve genel olarak tutarl� bir tedavi etkisi g�stermi�tir.
�nceden CDK4/6 inhibit�r� kullanan 20 hasta aras�nda tehlike oran� (HR) 0,48'dir (%95 GA: 0,17, 1,36); medyan PFS, plasebo art� fulvestrant kolunda 1,8 ay (%95 GA: 1,7, 3,6) ve alpelisib
art� fulvestrant kolunda ise 5,5 (%95 GA: 1,6, 16,8) ayd�r.
12 Haziran 2018 veri kesme tarihi kullan�larak, endokrin diren�li hastalar (HR = 0,64; %95 GA: 0,49, 0,85, n = 292) ve endokrin duyarl� hastalar (HR = 0,87; %95 GA: 0,35, 2,17, n = 39) alt gruplar� i�in PFS sonu�lar� alpelisib art� fulvestrant kolu lehine bulunmu�tur. PIK3CA mutasyonu olan endokrin duyarl� hastalar�n say�s� s�n�rl�d�r (n = 39) ve sonu�lar dikkatle yorumlanmal�d�r.
12 Haziran 2018 veri kesme tarihi kullan�larak, ba�lang��ta �l��lebilir hastal��� olan hastalarda genel yan�t oran�, alpelisib art� fulvestrant kolunda %35,7 (%95 GA: 27,4, 44,7) ve plasebo art� fulvestrant kolunda %16,2'dir (%95 GA: 10,4, 23,5).
Nihai OS analizinin yap�ld��� zamanda (veri kesme tarihi 23 Nisan 2020), PFS verileri i�in a��klay�c� bir takip etkililik analizi yap�lm��t�r. Randomizasyondan veri kesmeye kadar yakla��k 42 ayl�k medyan s�re ile rapor edilen PFS sonu�lar�, birincil PFS analizinden elde edilenlerle tutarl�d�r. Alpelisib art� fulvestrant ile tedavi lehine progresyon veya �l�m riskinde tahmini
%36'l�k bir azalma s�z konusu olmu�tur (HR=0.64; %95 GA: 0.50, 0.81) (�ekil 1).
�ekil 1 �al��ma C2301 - Ara�t�rmac� de�erlendirmesine g�re PFS'nin Kaplan-Meier grafi�i (FAS, PIK3CA mutant kohortu): 23 Nisan 2020 veri kesme tarihi ile a��klay�c� g�ncelleme
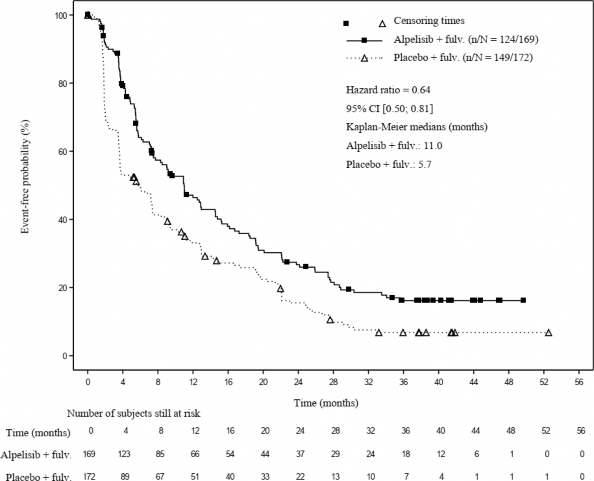
Nihai genel hayatta kalma analizi
Son OS analizinde, �al��ma temel ikincil hedefini kar��lamam��t�r. 23 Nisan 2020 veri kesme tarihi itibariyle alpelisib art� fulvestrant kolunda toplam 87 (%51,5) ve plasebo art� fulvestrant kolunda toplam 94 (%54,7) �l�m bildirilmi�tir. HR 0.86 bulunmu�tur (%95 GA: 0.64, 1,15; p=0,15, tek tarafl�) ve �nceden belirlenmi� O'Brien-Fleming etkililik s�n�r� p ≤0,0161 ge�ilmemi�tir. Medyan OS, alpelisib art� fulvestrant kolunda 39,3 ay (%95 GA: 34,1, 44,9) ve plasebo art� fulvestrant kolunda 31,4 ayd�r (%95 GA: 26,8, 41,3) (�ekil 2).
�ekil 2 �al��ma C2301 temel ikincil analizi –23 Nisan 2020 veri kesme tarihli OS'nin Kaplan-Meier grafi�i (FAS, PIK3CA mutant kohortu)
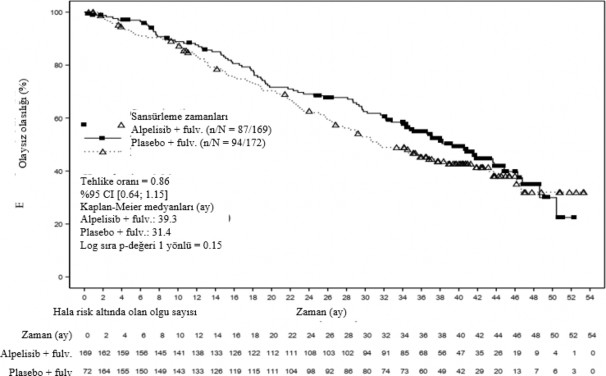
Daha �nce CDK4/6i tedavisi alan hastalarda (n=20), alpelisib art� fulvestrant kolundaki medyan OS 29,8 ay (%95 GA: 6,7, 38,2), plasebo art� fulvestrant kolunda ise 12,9 ayd�r (%95 GA: 2,5,
34,6). (HR=0,67; %95 GA: 0,21, 2,18).
PIK3CA mutasyonu olmayan kohort
T�m�rlerinde PIK3CA doku mutasyonu olmayan hastalarda PFS yarar� g�zlenmemi�tir.
CBYL719X2102'de �nceden fulvestrant kullan�m� olan hastalar
�nceden fulvestrant kullan�m� olan hastalar pivotal �al��maya dahil edilmemi�tir. Faz I �al��ma CBYL719X2101'de, 39 olgu daha �nce fulvestrant kullan�ld���n� bildirmi�tir. PIK3CA mutasyonlar� ve ba�lang��ta �l��lebilir hastal��� olan 21 olgu i�in alpelisib art� fulvestrant ile tedaviye en iyi genel cevaplar 7 olguda k�smi yan�t, 11 olguda stabil hastal�k ve 2 olguda progresif hastal�k olmu�tur. Bu nedenle, �u anda s�n�rl� veri nedeniyle daha �nce fulvestrant ile tedavi edilen hastalarda bu tedavinin etkilili�ine dair kan�t elde edilmemi�tir (bkz. B�l�m 4.4).
5.2. Farmakokinetik �zellikler
Alpelisibin farmakokineti�i, g�nde 30 ila 450 mg aras�nda de�i�en bir oral dozaj rejimindeki hastalarda ara�t�r�lm��t�r. Sa�l�kl� g�n�ll�lere 300 ila 400 mg aras�nda tekli oral dozlar verilmi�tir. Farmakokinetikhemonkolojihastalar�ndahemdesa�l�kl� ki�ilerde benzer olmu�tur.
Genel �zellikler
Emilim
Alpelisibin oral uygulamas�n� takiben, pik plazma konsantrasyonuna (Tmaks) ula�mak i�in ge�en medyan s�re, doz, zaman veya rejimden ba��ms�z olarak 2,0 ila 4,0 saat aras�nda de�i�mi�tir. Emilim modellemesine dayanarak, biyoyararlan�m�n tokluk ko�ullar� alt�nda �ok y�ksek (>%99), ancak a�l�k ko�ullar� alt�nda (300 mg dozda ~%68,7) daha d���k oldu�u tahmin edilmi�tir. G�nl�k dozlamadan sonra alpelisibin kararl� durum plazma d�zeylerine, �o�u hastada tedavinin ba�lamas�ndan sonraki 3. g�nde ula��lmas� beklenebilir.
G�da etkisi
Alpelisibin emilimi g�dadan etkilenir. A�l�k durumuna k�yasla tek bir 300 mg oral alpelisib dozundan sonra sa�l�kl� g�n�ll�lerde, y�ksek ya�l� y�ksek kalorili (YYYK) bir yemek (58,1 g ya� i�eren 985 kalori) EAAinf de�erini %73 ve Cmaks de�erini %84 artt�rm��t�r ve bir DYDK yeme�i (8,7 g ya� i�eren 334 kalori), EAAinf de�erini %77, Cmaks de�erini ise %145 artt�rm��t�r. 0,978 (GA: 0,876, 1,09) geometrik ortalama oran� ile LFLC ile HFHC aras�nda EAAinf de�erinde anlaml� bir fark bulunmayarak ya� i�eri�inin ya da genel kalori al�m�n�n emilim �zerinde �nemli bir etkiye sahip olmad���n� g�stermi�tir. G�da al�m�na yan�t olarak salg�lanan safra ile gastrointestinal ��z�n�rl�kteki art��, g�da etkisinin potansiyel nedenidir. Bu nedenle, P�MREVA, her g�n yakla��k ayn� saatte yemekten hemen sonra al�nmal�d�r.
Da��l�m
Alpelisib, konsantrasyondan ba��ms�z olarak %10,8 serbest fraksiyon ile proteine orta derecede ba�lan�r. Alpelisib, k�rm�z� kan h�creleri ile plazma aras�nda ortalama 1,03 in vivo kan-plazma oran� ile e�it olarak da��lm��t�r. Alpelisib, insan d��a ak�� ta��y�c�lar�n�n bir substrat� oldu�undan, insanlarda kan-beyin bariyerini ge�mesi beklenmez. Alpelisibin kararl� durumdaki da��l�m hacminin (Vss/F) 114 litre oldu�u tahmin edilmektedir (g�n�ll�ler aras� CV %46).
Biyotransformasyon
�n vitro �al��malar, kimyasal ve enzimatik amid hidrolizi ile hidroliz metaboliti BZG791'in olu�umunun maj�r bir metabolik yol oldu�unu ve bunu CYP3A4'�n k���k katk�s�n�n izledi�ini g�stermi�tir. Alpelisib hidrolizi, sistematik olarak hem kimyasal ayr��ma hem de karaci�erle s�n�rl� olmayan her yerde ayn� anda eksprese edilen y�ksek kapasiteli enzimler (esterazlar, amidazlar, kolin esteraz) yoluyla enzimatik hidroliz ile meydana gelir. CYP3A4 arac�l� metabolitler ve glukuronidler dozun ~%15'ine tekab�l etmi�tir; BZG791, dozun ~%40-45'ini olu�turmu�tur. �drar ve fe�este de�i�memi� alpelisib olarak bulunan dozun geri kalan� ya alpelisib olarak at�l�r ya da emilmez.
Eliminasyon
Tokluk ko�ullar� alt�ndaki pop�lasyon farmakokinetik analizine dayanarak alpelisib, 9,2 l/saat (%CV %21) ile d���k klirens g�sterir. Pop�lasyondan t�retilen yar�lanma �mr�, doz ve zamandan ba��ms�z olarak g�nde bir kez 300 mg dozu ile kararl� durumda 8 ila 9 saattir.
Bir insan k�tle dengesi �al��mas�nda, oral uygulamadan sonra, alpelisib ve metabolitleri, esas olarak alpelisibin hepatobiliyer ge�i�i ve/veya ba��rsak salg�lanmas� yoluyla d��k�ya (%81,0) at�lm��t�r veya BZG791'e metabolizeedilmi�tir. �drardaat�l�m k���kt�r (%13,5), de�i�memi�
alpelisib oran� %2'dir. Tek bir oral [14C] -alpelisib dozunu takiben, verilen toplam radyoaktif dozun %94,5'i 8 g�n i�inde tespit edilmi�tir.
Do�rusall�k/do�rusal olmayan durum
Farmakokineti�in, 30 ila 450 mg aras�ndaki tokluk ko�ullar� alt�nda doz ve zamana g�re do�rusal oldu�u bulunmu�tur. �oklu dozlardan sonra, kararl� durumda alpelisib maruziyeti (EAA) tek bir dozdan sadece biraz daha y�ksektir ve g�nl�k dozlama rejimi ile ortalama birikim 1,3 ila 1,5'tir.
Metabolik etkile�im
CYP3A4 substratlar�
Hassas CYP3A4 substrat� everolimus ile yap�lan bir ila�-ila� etkile�imi �al��mas�nda EAA %11,2 artm��t�r. CYP3A4 substratlar� ile ila� etkile�imi sonucunda klinik olarak anlaml� bir de�i�iklik beklenmemektedir.
CYP3A4 ind�kleyicileri
G��l� bir CYP3A4 ind�kleyicisi olan alpelisib ve rifampinin birlikte uyguland��� bir ila�-ila� etkile�im �al��mas�nda, alpelisib ve g��l� CYP3A4 ind�kleyicileri aras�nda klinik olarak anlaml� bir farmakokinetik etkile�im oldu�unu do�rulam��t�r (bkz. B�l�m 4.5).
Ta��y�c� tabanl� etkile�im
�n vitro verilere dayanarak, terap�tik doz alan hastalarda renal organik anyon ta��y�c� OAT3'�n alpelisib (ve/veya onun metaboliti BZG791) taraf�ndan inhibisyonu olas�l�k d��� b�rak�lamamaktad�r.
Alpelisib, her yerde ayn� anda eksprese edilen geri ak�� ileticilerine (P-gp, BCRP, MRP2, BSEP), karaci�er giri�indeki ��z�nen ta��y�c� ileticilerine (OATP1B1, OATP1B3, OCT1) ve b�brekte ��z�nen ta��y�c� ileticilerine (OAT1, OAT2, MATE1, MATE2K) kar�� sadece zay�f in vitro inhibisyon g�stermi�tir. Hem terap�tik dozda hem de maksimum tolere edilen dozda ba�lanmam�� sistemik kararl� durum konsantrasyonlar� (veya karaci�er giri�indeki konsantrasyonlar), deneysel olarak belirlenen ba�lanmam�� inhibisyon sabitlerinden veya IC50'den �nemli �l��de d���k oldu�undan, bu inhibisyon klinik �neme sahip olmayacakt�r. Ba��rsak l�menindeki y�ksek alpelisib konsantrasyonlar� nedeniyle, ba��rsak P-gp ve BCRP �zerindeki bir etki tamamen olas�l�k d��� b�rak�lamamaktad�r.
Hastalardaki karakteristik �zellikler
B�brek yetmezli�i
Normal b�brek fonksiyonu olan 117 hasta (eGFR ≥90 ml/dak/1,73 m)/(CLcr ≥90 ml/dak), hafif b�brek yetmezli�i (eGFR 60 ila <90 ml/dak/1,73 m)/(CLcr 60 ila <90 ml/dak) olan 108 hasta ve orta derecede b�brek yetmezli�i olan 45 hastan�n (eGFR 30 ila <60 ml/dak/1,73 m) ) yer ald��� bir pop�lasyon farmakokinetik analizine dayanarak, hafif ve orta derecede b�brek yetmezli�inin alpelisib maruziyeti �zerinde hi�bir etkisi yoktur (bkz. B�l�m 4.2).
Karaci�er yetmezli�i
Karaci�er yetmezli�i olan hastalarda yap�lan farmakokinetik bir �al��maya dayanarak, orta ve �iddetli karaci�er yetmezli�ialpelisibmaruziyeti�zerindeihmal edilebilir bir etkiye sahiptir (bkz.
B�l�m 4.2). Alpelisib i�in ortalama maruziyet, �iddetli karaci�er yetmezli�i olan hastalarda 1,26 kat artm��t�r (GMR: Ci�in 1,00; EAA/ EAAi�in 1,26).
Normal karaci�er fonksiyonuna sahip 230 hasta, hafif karaci�er yetmezli�i olan 41 hasta i�eren ve orta derecede karaci�er yetmezli�i olan hasta i�ermeyen bir pop�lasyon farmakokinetik analizine dayanarak, spesifik karaci�er yetmezli�i �al��mas�ndan elde edilen bulgular� destekleyecek �ekilde, hafif ve orta �iddette karaci�er yetmezli�inin alpelisib maruziyeti �zerinde herhangi bir etkisi g�r�lmemi�tir (bkz. b�l�m 4.2).
Ya�, a��rl�k ve cinsiyetin etkisi
Pop�lasyon farmakokinetik analizi, ya�, v�cut a��rl��� veya cinsiyetin, alpelisibin sistemik maruziyeti �zerinde P�MREVA dozunda ayarlama gerektiren klinik olarak anlaml� bir etkisi olmad���n� g�stermi�tir.
Irk/etnisite
Japon kanser hastalar�nda yap�lan bir faz I �al��mas�n�n pop�lasyon farmakokinetik analizleri ve farmakokinetik analizleri, etnik k�kenin P�MREVA'n�n sistemik maruziyeti �zerinde klinik olarak anlaml� bir etkisi olmad���n� g�stermi�tir.
Japon hastalar i�in tek ve �oklu g�nl�k P�MREVA dozlar�ndan sonra kompartman d��� farmakokinetik parametreler, Beyaz pop�lasyonda bildirilenlere �ok benzer bulunmu�tur.
Pediatrik pop�lasyon
0-18 ya� aras� �ocuklarda P�MREVA'n�n farmakokineti�i belirlenmemi�tir. Veri bulunmamaktad�r.
Geriyatrik pop�lasyon
Faz III �al��mada P�MREVA alan 284 hastan�n (alpelisib art� fulvestrant kolunda) 117'si ≥65 ya� ve 34 hasta 75 ile 87 ya� aral���ndad�r. Bu hastalar ve gen� hastalar aras�nda P�MREVA maruziyetinde genel bir fark g�zlenmemi�tir (bkz. B�l�m 4.2).
5.3. Klinik �ncesi g�venlilik verileri
G�venlilik farmakolojisi ve tekrarlanan doz toksisitesi
G�zlenen alpelisib etkilerinin �o�unlu�u, artm�� kan bas�nc� riski ve hiperglisemi ile sonu�lanan glukoz homeostaz� �zerindeki etki gibi, alpelisibin PI3K yola��n�n p110α spesifik inhibit�r� olarak farmakolojik aktivitesi ile ili�kili bulunmu�tur. Kemik ili�i ve lenfoid doku, pankreas ve her iki cinsiyetin baz� �reme organlar�, olumsuz etkiler i�in ana hedef organlard�r. Kemik ili�i ve lenfoid doku �zerindeki etkiler genellikle tedavinin kesilmesi ile geri d�n��l� olmu�tur. Pankreas ve �reme organlar� �zerindeki etkiler tam olarak geri d�n��l� olmam�� fakat geri d�n�� e�ilimi g�stermi�tir. Ke�fedici s��an �al��malar�nda, deride enflamatuar de�i�ikliklere dair kan�tlar bulunmu�tur.
Kardiyovask�ler g�venlilik farmakolojisi
�nerilen 300 mg/g�n dozunda insanlardaki maruziyetten ~13 kat daha y�ksek konsantrasyonlarda HERG kanallar�n�n in vitro inhibisyonu (IC9,4 µM) g�sterilmi�tir. K�peklerde �nemli elektrofizyolojik etki g�r�lmemi�tir.
Karsinojenisite ve mutajenite
Herhangi bir karsinojenisite �al��mas� yap�lmam��t�r.
Alpelisib ile yap�lan standart in vitro genotoksisite �al��malar�n�n sonu�lar� negatif olmu�tur. Mikron�kleus analizinin entegre edildi�i bir tekrarlanan doz s��an toksisite �al��mas�nda, alpelisib, �nerilen insan dozu olan 300 mg'�n yakla��k iki kat� maruz kalma seviyelerinde (EAA) genotoksik de�ildir.
�reme toksisitesi
S��anlarda ve tav�anlarda embriyo-fetal geli�im �al��malar�, organogenez s�ras�nda alpelisibin oral yoldan uygulanmas�n�n embriyotoksisite, fetotoksisite ve teratojenisiteye neden oldu�unu g�stermi�tir. S��anlarda ve tav�anlarda, alpelisibe prenatal maruziyetin ard�ndan implantasyon �ncesi ve sonras� kay�p insidanslar�nda art��, fetal a��rl�klarda azalma ve fetal anormallik insidans�nda art�� (geni�lemi� beyin ventrik�l�, kemik osifikasyonu ve iskelet malformasyonlar�) insanda �nerilen en y�ksek doz olan 300 mg'�n alt�ndaki d�zeylerde ba�lad��� g�zlenmi� olup bu sonu�lar klinik a��dan olas� bir ili�kiye i�aret etmektedir.
Tekrarlanan doz toksisitesi �al��malar�nda, EAA baz�nda ilgili klinik dozlarda s��anlarda vajinal veya uterus atrofisi ve �strus d�ng�s� varyasyonlar�, s��anlarda ve k�peklerde prostat ve testis a��rl���nda azalmalar ve k�peklerde prostat atrofisi gibi advers olaylar g�zlenmi�tir.
Erkek ve di�i s��anlarda yap�lan fertilite �al��malar�nda fertilite �zerinde benzer etkiler g�zlenmi�tir. Di�ilerde, �nerilen insan dozu olan 300 mg'�n yakla��k iki kat� maruz kalma seviyelerinde (EAA), implantasyon b�lgelerinin ve canl� embriyolar�n say�s�nda azalmaya yol a�an implantasyon �ncesi ve sonras� kay�plarda art�� g�zlenmi�tir. Erkeklerde, sperm say�s� ve hareketlilik parametreleri dahil olmak �zere do�urganl�k ve �reme performans�, �nerilen 300 mg dozda insanlardaki tahmini maruziyetin (EAA) yakla��k iki kat� maruz kalma seviyelerinde etkilenmemi�tir. Bununla birlikte, �nerilen 300 mg'l�k insan dozundaki veya alt�ndaki maruz kalma seviyelerinde (EAA), yard�mc� bez a��rl�klar� (seminal vezik�ller, prostat) azalm�� ve mikroskobik olarak s�ras�yla prostat ve seminal vezik�llerde atrofi ve/veya azalm�� sekresyon ile ili�kilendirilmi�tir.
Fototoksisite
Fare Balb/c 3T3 fibroblast h�cre hatt� �zerinde ger�ekle�tirilen bir in vitro fototoksisite testi, alpelisib i�in ilgili bir fototoksisite potansiyelini tan�mlamam��t�r.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Tablet �ekirde�i
Mikrokristalin sel�loz Mannitol
Sodyum ni�asta glikolat Hipromelloz Magnezyum stearat
Film kaplama
Hipromelloz
Demir oksit, siyah (E 172) Demir oksit, k�rm�z� (E 172) Titanyum dioksit (E 171) Makrogol
Talk
6.2. Ge�imsizlikler
Ge�erli de�il.
6.3. Raf �mr�
36 ay
6.4. Saklamaya y�nelik �zel tedbirler
30°C alt�ndaki oda s�cakl���nda saklay�n�z. Nemden korumak i�in orijinal ambalaj�nda saklay�n�z.
6.5. Ambalaj�n niteli�i ve i�eri�i
28 veya 56 film kapl� tablet i�eren PVC/PCTFE/Alu blisterler
28 film kapl� tablet (14 adet 50 mg film kapl� tablet ve 14 adet 200 mg film kapl� tablet) veya 56 film kapl� tablet (28 adet 50 mg film kapl� tablet ve 28 adet 200 mg film kapl� tablet) i�eren ambalajlar
�r�n, 250 mg g�nl�k dozu kar��lamak i�in bir adet 200 mg ve bir adet 50 mg film kapl� tabletin ayn� anda al�nmas�n� gerektirmektedir. Bu sebeple ayn� kutu i�erisinde 200 mg ve 50 mg film kapl� tabletler bulunmaktad�r.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj ve Ambalaj At�klar�n�n Kontrol� Y�netmeli�i”ne uygun olarak imha edilmelidir.
 Mide Kanseri
Mide kanseri genellikle mideyi t�m�yle kaplayan ve mukus �retmekle g�revli h�crelerde ba�lar. Bu kanser tipine adenokarsinom denir.
Mide Kanseri
Mide kanseri genellikle mideyi t�m�yle kaplayan ve mukus �retmekle g�revli h�crelerde ba�lar. Bu kanser tipine adenokarsinom denir. |
 Diyabet Hastal���
Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r.
Diyabet Hastal���
Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r. |
 |
HIV ve Aids HIV, Human Immunodeficiency Virus’d�r (�nsanlarda Ba����kl�k Sistemini Bozan Vir�sd�r). Bu vir�s AIDS hastal���na sebep olur. |
 |
�nme �nme, beynin hasar g�rmesinin sonucudur. Bu hasar, beynin bir k�sm�ndaki ya bir kanama ya da akut kan eksikli�i nedeniyle o k�sm�n ge�ici ya da kal�c� olarak i�levini yapamamas�na yol a�ar. |
 |
�izofrenlik �izofrenli�in psikiatrik te�hisi hakk�nda �ok fazla anla�mazl�k vard�r. Bu sayfadaki bilgiler, �izofrenli�in te�hisi, nedenleri ve tedavisi hakk�ndaki fakl� teoriler hakk�nda bilgi verecektir. |
�LA� GENEL B�LG�LER�
Farmanova Sa�l�k Hizmetleri Ltd. �ti
| Sat�� Fiyat� | 105547.26 TL [ 17 Dec 2024 ] |
| �nceki Sat�� Fiyat� | 105547.26 TL [ 2 Dec 2024 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | K�s�tlanm�� Beyaz Re�eteli bir ila�d�r. |
| Barkodu | 8699074090936 |
| Etkin Madde | Alpelisib |
| ATC Kodu | L01EM03 |
| Birim Miktar | 200+50 |
| Birim Cinsi | MG |
| Ambalaj Miktar� | 56 |
| Antineoplastik ve �mm�nomod�lat�r Ajanlar |
| �thal ( ref. �lke : Isvicre ) ve Be�eri bir ila�d�r. |