POMALEM 4 mg sert kapsül (21 sert kapsül) Kısa Ürün Bilgisi
{ Pomalidomid }
1. BEŞERİ TIBBİ ÜRÜNÜN ADI
POMALEM 4 mg sert kapsül
2. KALİTATİF VE KANTİTATİF BİLEŞİM
Her bir kapsülde;
Etkin madde
Pomalidomid 4 mg
Yardımcı maddeler
Laktoz anhidrus (inek sütünden elde edilir) 100 mg
Yardımcı maddeler için Bölüm 6.1'e bakınız.
3. FARMASÖTİK FORMU
Sert kapsül
“DEVA†baskılı, opak koyu mavi kapak ve “4 mg†baskılı açık mavi opak gövdeli 2 numara kapsül içinde açık sarı-sarı renkli, yabancı partikül içermeyen toz
4. KLİNİK ÖZELLİKLER
4.1. Terapötik endikasyonlar
POMALEM, bortezomib ve deksametazon ile kombinasyon halinde, daha önce lenalidomid de dahil olmak üzere en az bir tedavi rejimi alan, bu tedavilere dirençli veya nüks eden multipl miyelomlu erişkin hastaların tedavisinde endikedir.
POMALEM, deksametazonla kombinasyon halinde, aşağıda belirtilen koşulları taşıyan multipl miyelom tanılı yetişkin hastaların tedavisinde endikedir:
Otolog kök hücre nakline uygun olmayan hastalarda bortezomib ve lenalidomid dahil en az iki dizi tedavi sonrası nüks eden veya bu tedavilere dirençli hastalık varlığında endikedir.
4.2. Pozoloji ve uygulama şekli
Tedavi, multipl miyelom tedavisinde deneyimli bir hekimin denetiminde başlatılmalı ve izlenmelidir.
Klinik veya laboratuvar bulgularına göre doza devam edilebilir veya doz ayarlaması yapılabilir (bkz. Bölüm 4.4).
Pomalidomidin bortezomib ve dekzametazon ile kombinasyonu
Önerilen başlangıç dozu, tekrarlanan 21 günlük sikluslar halinde 1 ve 14. günler arası günde bir defa ağızdan 4 mg POMALEM'dir.
Pomalidomid, Tablo 1'de gösterildiği gibi, bortezomib ve deksametazon ile kombinasyon halinde uygulanır.
Bortezomibin önerilen başlangıç dozu, Tablo 1'de gösterilen günlerde günde bir kez intravenöz veya subkütan olarak 1,3 mg/m2'dir. Önerilen deksametazon dozu, Tablo 1'de gösterilen günlerde günde bir kez oral olarak 20 mg'dır.
Bortezomib ve deksametazon ile kombine edilen pomalidomid tedavisi, hastalığın ilerlemesi veya kabul edilemez toksisite oluşana kadar verilmelidir.
Tablo 1. Bortezomib ve deksametazon ile kombinasyon halinde POMALEM için önerilen dozaj şeması
1-8.Sikluslar | Gün (21 günlük döngü) | ||||||||||||||||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 |
Pomalidomid (4 mg) | • | • | • | • | • | • | • | • | • | • | • | • | • | • |
|
|
|
|
|
|
|
Bortezomib (1,3 mg/m) | • |
|
| • |
|
|
| • |
|
| • |
|
|
|
|
|
|
|
|
|
|
Deksametazon (20 mg) * | • | • |
| • | • |
|
| • | • |
| • | • |
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||||
9.Siklus sonrası | Gün (21 günlük döngü) | ||||||||||||||||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 |
Pomalidomid (4 mg) | • | • | • | • | • | • | • | • | • | • | • | • | • | • |
|
|
|
|
|
|
|
Bortezomib (1,3 mg/m) | • |
|
|
|
|
|
| • |
|
|
|
|
|
|
|
|
|
|
|
|
|
Deksametazon (20 mg) * | • | • |
|
|
|
|
| • | • |
|
|
|
|
|
|
|
|
|
|
|
|
* 75 yaş üstü hastalar için bkz. Özel popülasyonlara ilişkin ek bilgiler.
Pomalidomid doz ayarlaması veya ara verilmesi
Yeni bir pomalidomid siklusunu başlatmak için nötrofil sayısının ≥1x10/L ve trombosit sayısının ≥50x 10/L olması gerekmektedir.
Advers reaksiyonlarla ilgili olarak pomalidomid tedavisine ara verilmesi veya dozunun azaltılması ile ilgili bilgiler, Tablo 2'de ve doz seviyeleri Tablo 3'de belirtilmiştir:
Tablo 2: Pomalidomidin doz ayarlaması için bilgiler
Toksisite | Doz ayarlaması | ||||||
Nötropeni* MNS** <0,5 x 10/L veya Febril nötropenik ateş (ateş ≥ 38,5°C ve MNS <1x 10/L) | Siklusun geri kalanı için pomalidomid tedavisine ara verilir. Haftalık TKS*** takibi yapılır. | ||||||
MNS ≥1 x 10/L'ye döndüğünde | Pomalidomid tedavisine önceki seviye düşük doz ile tekrar başlanır. | dozdan | bir | ||||
Takip eden <0,5 x 10/L'nin altına her düşüşte | Pomalidomid tedavisine ara verilir. | ||||||
MNS ≥1 x 10/L'ye döndüğünde | Pomalidomid tedavisine önceki seviye düşük doz ile tekrar başlanır. | dozdan | bir | ||||
Trombositopeni Trombosit sayısı <25 x 10/L | Siklusun geri kalanı için pomalidomid tedavisine ara verilir. Haftalık TKS*** takibi yapılır. | ||||||
Trombosit döndüğünde | sayısı | ≥50 | x | 10/L'ye | Pomalidomid tedavisine önceki seviye düşük doz ile tekrar başlanır. | dozdan | bir |
Takip eden <25 x 10/L'nin altına her düşüşte | Pomalidomid tedavisine ara verilir. | ||||||
Trombosit sayısı ≥50 x 10/L'ye döndüğünde | Pomalidomid tedavisine önceki seviye düşük doz ile tekrar başlanır. | dozdan | bir | ||||
Döküntü Döküntü = 2-3. Derece | Doz kesilmesi veya pomalidomid tedavisinin kesilmesi düşünülmelidir. | ||||||
Döküntü = Derece 4 veya kabarma (anjiyoödem, anafilaktik reaksiyon, eksfolyatif veya büllöz döküntü dahil veya Stevens-Johnson sendromu (SJS), Toksik Epidermal Nekroliz (TEN) veya Eozinofili ve Sistemik Semptomlarla İlaç Reaksiyonundan (DRESS) ile ilaç reaksiyonu şüphesi varsa) | Tedaviyi kalıcı olarak durdurun (bkz. Bölüm 4.4). | ||||||
Diğer
Diğer ≥ Derece 3 pomalidomid ile ilgili advers reaksiyonlar | Siklusun geri kalanı için pomalidomid tedavisi durdurulur. Bir sonraki döngüde tedaviye önceki dozdan bir seviye düşük doz ile devam edilir (Dozlama başlamadan önce advers reaksiyonlar geçmeli ya da ≤2. dereceye dönmelidir). | ||||||
∠Bu tabloda yer alan doz ayarlama bilgileri, hem pomalidomid, bortezomib ve deksametazon kombinasyonu hem de pomalidomid dekzametazon kombinasyonu için geçerlidir.
* Nötropeni durumunda hekim büyüme faktörlerinin kullanımını göz önünde bulundurmalıdır. **MNS–Mutlak Nötrofil Sayısı; ***TKS–Tam Kan Sayımı
Tablo 3. Pomalidomid doz azaltma basamakları âˆ
Doz Düzeyi | Pomalidomid dozu |
Başlangıç dozu | 4 mg |
Doz seviyesi -1 | 3 mg |
Doz seviyesi -2 | 2 mg |
Doz seviyesi -3 | 1 mg |
∠Bu tabloda yer alan doz ayarlama bilgileri, hem pomalidomid, bortezomib ve deksametazon kombinasyonu hem de pomalidomid dekzametazon kombinasyonu için geçerlidir.
Dozun 1 mg'a düşürülmesi sonrasında advers reaksiyonlar ortaya çıkarsa, ilaç kesilmelidir. Güçlü CYP1A2 inhibitörleri
Güçlü CYP1A2 inhibitörleri (örn., siprofloksasin, enoksasin ve fluvoksamin) pomalidomid ile birlikte uygulanırsa pomalidomid dozu %50 azaltılmalıdır.
Bortezomib doz modifikasyonu veya kesilmesi
Bortezomibe bağlı advers reaksiyonlar için doz kesilmesi veya azaltmaları ile ilgili talimatlar için, hekimler bortezomib (KÜB)'ne başvurmalıdır.
Deksametazon doz modifikasyonu veya kesilmesi
Düşük doz deksametazona bağlı advers reaksiyonlar için doz kesilmesi veya azaltmaları ile ilgili talimatlar Tablo 4 ve 5'te özetlenmiştir.
Tablo 4. Deksametazon doz ayarlaması için bilgiler
Toksisite | Doz Değişikliği |
Dispepsi = 1-2. Derece
Dispepsi ≥3. Derece | Aynı dozda devam edilir ve histamin (H) blokörleri veya eşdeğerleri ile tedavi edilir. Semptomlar devam ederse, doz bir düzey azaltılır.
Semptomlar kontrol altına alınana kadar tedaviye ara verilir. Deksametazona ara verilse dahi pomalidomid tedavisine devam edilir. Tedaviye önceki dozdan daha düşük bir doz düzeyinde devam edilir ve H2 blokörü veya eşdeğeri eklenir. |
Ödem ≥3. Derece | Gerektiğinde diüretikler kullanılır ve doz bir düzey azaltılır. |
Konfüzyon veya duygu durum değişikliği ≥2. Derece | Semptomlar düzelene kadar tedaviye ara verilir. Tedaviye önceki dozdan daha düşük bir doz düzeyinde devam edilir. |
Kas güçsüzlüğü ≥2. Derece | Kas güçsüzlüğü ≤1. dereceye dönene kadar |
| tedaviye ara verilir. Tedaviye önceki dozdan daha düşük bir doz düzeyinde devam edilir. |
Hiperglisemi ≥3. Derece | Doz, bir düzey azaltılır. Gerektiğinde insülin veya oral hipoglisemik ilaçlarla tedavi edilir. |
Akut pankreatit | Deksametazon tedavi rejiminden çıkarılır. |
Diğer ≥ 3. Derece deksametazonla ilgili advers reaksiyonlar | Advers reaksiyonlar ≤2. dereceye dönene kadar deksametazon dozu durdurulur. Tedaviye önceki dozdan daha düşük bir doz düzeyinde devam edilir. |
Eğer toksisitelerin düzelmesi 14 günden fazla sürerse, deksametazon dozu bir önceki dozdan daha düşük bir doz seviyesinde devam edecektir.
Tablo 5. Deksametazon doz azaltma basamakları
Doz Düzeyi | ≤ 75 yaş Doz (Siklus 1-8: 21 günlük siklusun 1, 2, 4, 5, 8, 9, 11, 12 günleri Siklus ≥ 9: 21 günlük siklusun 1, 2, 8, 9 günleri) | > 75 yaş Doz (Siklus 1-8: 21 günlük siklusun 1, 2, 4, 5, 8, 9, 11, 12 günleri Siklus ≥ 9: 21 günlük siklusun 1, 2, 8, 9 günleri) |
Başlangıç dozu | 20 mg | 10 mg |
Doz seviyesi -1 | 12 mg | 6 mg |
Doz seviyesi -2 | 8 mg | 4 mg |
Eğer 75 yaş ve altındaki hasta 8 mg'ı veya 75 yaş üstü hasta 4 mg'ı tolere edemezse deksametazon kesilmelidir.
Tedavi rejiminin herhangi bir bileşeninin kalıcı olarak kesilmesi durumunda, kalan diğer tıbbi ürünlerin devamlılığı doktorun takdirine bağlıdır.
4.3. Kontrendikasyonlar
Gebelik,
Gebelik önleme programının tüm koşullarına uymadığı takdirde, çocuk doğurma potansiyeli olan kadınlar (bkz. bölüm 4.4 ve 4.6),
Gerekli doğum kontrol önlemlerini takip edemeyen veya önlemlerine uyamayan erkek hastalar (bkz. bölüm 4.4),
Etkin madde
POMALEM ile kombinasyon halinde verilen diğer tıbbi ürünler hakkında bilgi için, ilgili güncel KÜB'e bakınız.
4.4. Özel kullanım uyarıları ve önlemleri
Teratojenisite
Pomalidomid ile teratojenik bir etki beklendiğinden gebelik sırasında alınmamalıdır. Pomalidomid yapısal olarak talidomide benzerdir. Talidomid, insanlarda yaşamı tehdit edici ciddi doğumsal kusurlara neden olduğu bilinen bir teratojendir. Pomalidomidin, sıçanlarda ve tavşanlarda majör organogenez döneminde kullanıldığında teratojenik olduğu bulunmuştur (bkz. bölüm 5.3).
Çocuk doğurma potansiyeli olmadığını gösteren güvenilir kanıtlara sahip olanların dışındaki tüm hastalarda, gebelik önleme programı koşullarına mutlaka tam olarak uyulmalıdır.
Çocuk doğurma potansiyeli olmayan kadınlar için kriterler
Aşağıdaki kriterlerden en az biri bulunduğunda, bir kadın hastanın ya da bir erkek hastanın eşinin çocuk doğurma potansiyelinin olmadığı düşünülür:
Yaş ≥ 50 ve doğal olarak ≥ 1 yıl amenore durumunda (Kanser tedavisini takip eden veya laktasyon sürecindeki amenore, çocuk doğurma potansiyelini ekarte ettirmez.)
Uzman bir jinekolog tarafından onaylanan prematüre over yetmezliği
Bilateral salpingo-ooferektomi veya histerektomi hikayesi
XY genotipi, Turner sendromu, uterus agenezi
Danışmanlık
Çocuk doğurma potansiyeli olan kadınlar için aşağıdakilerin tümü sağlanmadıkça pomalidomid kullanımı kontrendikedir:
Doğmamış çocuk için beklenen teratojenik riski anlaması,
Tedaviye başlamadan en az 4 hafta önce, tüm tedavi boyunca (doza ara vermeler de dahil olmak üzere) ve tedavinin sonlanmasından en az 4 hafta sonrasına kadar, etkili bir doğum kontrol yönteminin kesintisiz olarak uygulanması gerektiğini anlaması,
Çocuk doğurma potansiyeli bulunan bir kadın amenore olsa dahi, etkili doğum kontrolü konusundaki tüm önerileri izlemelidir,
Etkili doğum kontrol yöntemlerine uyabilme kapasitesinde olması,
Gebeliğin potansiyel sonuçlarını ve gebelik riski bulunuyorsa hemen doktoruna danışmasının gerekliliği konusunda bilgi verilmesi ve bunu anlaması,
Negatif bir gebelik testini takiben pomalidomid reçete edilir edilmez tedaviye başlaması gerektiğini anlaması,
Teyit edilmiş tubal sterilizasyon haricinde, en az her 4 haftada bir gebelik testi yapılması gereğini anlaması ve kabul etmesi,
Pomalidomid kullanımı ile ilgili tehlikeleri ve gerekli önlemleri anladığını belirtmesi.
İlacı reçeteleyen doktorlar, çocuk doğurma potansiyeli olan kadınlar için aşağıdakileri sağlamalıdır:
Hastanın Gebelik Önleme Programının koşullarını yeterli derecede anlama kapasitesine sahip olduğundan ve bu koşullara uygun davranacağından emin olması,
Hastanın önceden bahsedilen bu koşulları onaylamış olması.
Pomalidomid kullanan erkek hastalar için farmakokinetik veriler, pomalidomidin tedavi süresince insan semenine geçebildiğini göstermiştir. Önlem olarak ve karaciğer yetmezliği gibi uzamış eliminasyon zamanına sahip özel popülasyonlar dikkate alınarak, pomalidomid kullanan tüm erkek hastalar aşağıdaki koşulları sağlamalıdır:
Gebe veya çocuk doğurma potansiyeli olan bir kadınla cinsel ilişkiye girmesi durumunda beklenen teratojenik riski anlamalıdır,
Tedavi süresi boyunca, tedavi kesildikten sonra ve dozlara ara verildikten ve/veya tedavi kesildikten sonraki 7 gün süreyle gebe bir kadınla veya etkili bir doğum kontrol yöntemi kullanmayan çocuk doğurma potansiyeli olan bir kadınla cinsel ilişkiye girmesi durumunda prezervatif kullanması gerektiğini anlamalıdır. Sperm olmasa dahi seminal sıvı pomalidomid içerebileceğinden, vazektomi geçirmiş erkek hastalar da dahil olmak üzere gebe bir kadın veya çocuk doğurma potansiyeli olan bir kadın ile cinsel ilişkiye girmesi durumunda prezervatif kullanmalıdır.
Pomalidomid kullandığı süre içerisinde ya da pomalidomid kullanmayı bıraktıktan 7 gün sonra eğer eşi gebe kalırsa, derhal tedaviden sorumlu hekime haber vermesi gerektiğini ve eşi için, değerlendirme ve tavsiye amacıyla teratoloji konusunda uzman ya da deneyimli bir hekime başvurması gerektiğini anlamalıdır.
Doğum Kontrolü
Çocuk doğurma potansiyeli olan kadınlar tedavinin en az 4 hafta öncesinden başlayarak, tedavi sırasında ve pomalidomid tedavisinden en az 4 hafta sonrasına kadar ve doza ara verildiğinde dahi; hasta cinsel ilişkiden bütünüyle ve sürekli olarak uzak duracağını her ay taahhüt etmedikçe, etkili bir doğum kontrol yöntemlerinden en az birini kullanmalıdır. Etkili bir yöntem belirlenmediyse, hasta etkili bir korunmanın başlatılması için uygun şekilde eğitim almış bir sağlık profesyoneline yönlendirilmelidir.
Aşağıdakiler uygun doğum kontrol yöntemlerine örnek olarak değerlendirilebilir:
İmplant,
Levonorgestrel salan rahim içi araçlar (RİA)
Medroksiprogesteron asetat deposu
Tubal sterilizasyon
Sadece vazektomi uygulanmış erkek partner ile cinsel ilişki; vazektomi iki negatif semen analiziyle doğrulanmalıdır
Sadece progesteron içeren ovülasyon inhibitörü haplar (örneğin, desogestrel).
Pomalidomid ve deksametazon kullanan multipl miyelomlu hastalarda venöz tromboembolizm riskinin artması nedeniyle, kombine oral kontraseptif haplar önerilmez (bkz.
bölüm 4.5). Eğer hasta kombine bir oral kontraseptif kullanıyorsa, yukarıda listelenen etkili yöntemlerden birine geçmelidir. Venöz tromboembolizm riski kombine oral kontrasepsiyonun kesilmesi sonrası 4-6 hafta boyunca sürer. Deksametazon ile birlikte kullanılması kontraseptif steroidlerin etkililiğini azaltabilir (bkz. bölüm 4.5).
İmplantlar ve levonorgestrel salan rahim içi sistemler, düzensiz vajinal kanama ve yerleştirme anında artmış enfeksiyon riski ile ilişkilidir. Özellikle nötropenili hastalarda profilaktik antibiyotiklerin kullanılması düşünülmelidir.
Bakır salan rahim içi araçların, ciddi derecede nötropeni veya ciddi derecede trombositopenili hastalarda hastaları tehlikeye sokabilecek menstrüel kan kaybı ve yerleştirme sırasında olası enfeksiyon riski gibi potansiyel riskleri yüzünden önerilmemektedir.
Gebelik testleri
Yerel uygulamaya göre, çocuk doğurma potansiyeli olan kadınlar için sensitivitesi minimum
25 mIU/mL olan ve tıbbi olarak denetlenmiş gebelik testleri aşağıda belirtildiği şekilde uygulanmalıdır. Bu gereklilik, bütünüyle ve sürekli olarak cinsel ilişkiden uzak duracağını taahhüt eden çocuk doğurma potansiyelindeki kadınları da kapsar. İdeal olarak gebelik testi, reçetenin yazılması ve ilacın verilmesi aynı gün içinde olmalıdır. Çocuk doğurma potansiyelinde olan kadınlara pomalidomid temin edilmesi, reçete tarihinden itibaren 7 gün içinde gerçekleşmelidir.
Tedaviye başlanmadan önce
Tıbbi olarak doğrulanmış gebelik testi, pomalidomid reçetelendiği konsültasyon sırasında uygulanmalı veya en az 4 hafta boyunca etkili bir korunma yöntemi kullanan hastanın reçeteyi yazacak doktoru ziyaret etmesinden önceki 3 gün içinde uygulanmalıdır. Bu test, hasta pomalidomid ile tedaviye başladığında gebelik olmadığını göstermelidir.
İzleme ve tedavinin sona ermesi
Onaylanmış tubal sterilizasyon durumu hariç, tıbbi olarak doğrulanmış gebelik testi, tedavinin sona ermesinden sonraki 4 hafta dahil en az her 4 haftada bir tekrarlanmalıdır. Bu gebelik testleri ilacın reçetelendiği gün veya reçeteyi yazacak doktoru ziyaretten önceki 3 gün içinde uygulanmış olmalıdır.
Ek önlemler
Hastalar, bu ilacı başka bir kişiye vermemeleri gerektiği ve kullanılmayan kapsüllerin tedavi sonunda eczacılara teslim edilmesi gerektiği konusunda bilgilendirilmelidir.
Hastalar tedavi sırasında (doza ara vermeler de dahil) ve pomalidomidi bıraktıktan sonra 7 gün süreyle kan, semen veya sperm bağışı yapmamalıdır.
Sağlık profesyonelleri ve bakıcılar, blister veya kapsülü tutarken tek kullanımlık eldiven giymelidir. Hamile olan veya hamile olabileceğinden şüphelenen kadınlar, blister veya kapsüle dokunmamalıdır (bkz. bölüm 6.6).
Eğitim malzemeleri, reçeteleme ve dağıtma kısıtlamaları
Pomalidomidin fetal maruziyetini önlemede hastalara yardımcı olmak amacıyla, RUHSAT SAHİBİ, pomalidomidin beklenen teratojenisitesi konusundaki uyarıları vurgulamak, tedaviye başlanmadan önce doğum kontrolü konusunda tavsiye ve gebelik testinin gerekliliği konusunda rehberlik sağlamak için sağlık profesyonellerine eğitim malzemesi temin edecektir. İlacı reçete eden kişi beklenen teratojenik risk ve Gebelik Önleme Programında belirtilen sıkı gebelik önleme tedbirleri hakkında erkek ve kadın hastaları bilgilendirmelidir ve hastalara uygun hasta eğitim broşürü ve ülkede uygulanan sisteme göre bir materyal sağlamalıdır. Ulusal Sağlık Otoritesi ile iş birliği içerisinde ulusal kontrollü dağıtım sistemi uygulamaya koyulmuştur. Bu kontrollü dağıtım sistemi, reçete edilme ve/veya dağıtım için Ulusal Sağlık Otoritesi'nin belirlediği bir materyalin kullanımını içermektedir. Tercihen gebelik testi ve reçete yazma ile ilaç dağıtım işlemleri aynı gün olmalıdır. Çocuk doğurma potansiyeli olan bir kadına pomalidomid tıbbi olarak doğrulanmış, negatif hamilelik testi sonrası reçete edildikten itibaren 7 gün içinde sağlanmalıdır. Çocuk doğurma potansiyeli olan kadınlara verilen reçeteler, onaylanmış endikasyonlara göre dozaj rejimleri maksimum 4 haftalık bir tedavi süresi ve diğer tüm hastalar için verilen reçeteler maksimum 12 hafta süresi için olabilir (bkz. Bölüm 4.2).
Hematolojik olaylar
Nötropeni, nüks/dirençli multipl miyelom hastalarında en sık bildirilen 3. veya 4. derece hematolojik advers reaksiyondur, nötropeniyi anemi ve trombositopeni takip etmektedir. Hastalar, hematolojik advers reaksiyonlar, özellikle de nötropeni açısından izlenmelidir. Hastalara febril nöbetlerini derhal bildirmeleri konusunda tavsiyede bulunulmalıdır. Hekimler burun kanamaları dahil kanama belirtileri açısından, özellikle de kanama riskini artırdığı bilinen ilaçların eş zamanlı kullanımı sırasında, hastaları gözlemelidir (bkz. bölüm 4.8).
Tam kan sayımları
tedaviye başlamadan,
tedavinin ilk 8 haftası boyunca her hafta,
4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri
Diğer tıbbi ürünlere pomalidomidin etkisi
Pomalidomidin, P450 izoenzimlerinin substratları veya taşıyıcıları ile birlikte uygulanmasının, P450 izoenzim inhibisyonu veya indüksiyonu veya taşıyıcı inhibisyonuna bağlı klinik olarak anlamlı farmakokinetik ilaç-ilaç etkileşmelerine neden olması beklenmemektedir. Bu tür ilaç-ilaç etkileşim potansiyeli, pomalidomidin kombine oral kontraseptiflerin farmakokinetiği üzerine potansiyel etkisi dahil olmak üzere, klinik olarak değerlendirilmemiştir (bkz. bölüm 4.4).
Diğer tıbbi ürünlerin pomalidomide etkisi
Pomalidomid, CYP1A2 ve CYP3A4/5 tarafından kısmi olarak metabolize edilir. Ayrıca P- glikoproteinin de bir substratıdır. Pomalidomidin güçlü CYP3A4/5 ve P-gp inhibitörü olan ketokonazol ile veya güçlü CYP3A4/5 indükleyicisi olan karbamazepin ile eş zamanlı uygulanmasının, pomalidomide maruziyet üzerinde klinik olarak anlamlı etkisi bulunmamaktadır. Güçlü CYP1A2 inhibitörü olan fluvoksaminin pomalidomid ile ketokonazol varlığında eş zamanlı olarak uygulanması, pomalidomid ve ketokonazole kıyasla,
pomalidomide ortalama maruziyeti %90 güven aralığı ile [%91 ila %124] %107 oranında artırmıştır. Tek başına bir CYP1A2 inhibitörünün metabolizma değişikliklerine katkısını değerlendirmek üzere yapılan ikinci bir çalışmada, pomalidomid ile tek başına fluvoksaminin eş zamanlı olarak uygulanması pomalidomide ortalama maruziyeti, tek başına pomalidomide kıyasla %90 güven aralığı ile [%98 ila %157) %125 artırmıştır. Güçlü CYP1A2 inhibitörleri (örn., siprofloksasin, enoksasin ve fluvoksamin) pomalidomid ile eş zamanlı olarak uygulanırsa, pomalidomid dozu %50 azaltılmalıdır.
Pomalidomidin güçlü CYP1A2 inhibitörleri (örn., siprofloksasin, enoksasin ve fluvoksamin) ile eşzamanlı uygulanması halinde, hastalar advers reaksiyonlar açısından yakından takip edilmelidir.
DeksametazonMultipl miyelom hastalarında 4 mg'a kadar olan çoklu pomalidomid dozlarıyla, 20 mg ila 40 mg arasında deksametazonun (CYP3A dahil çeşitli CYP enzimlerinin hafif ila orta derecede indükleyicisi) eş zamanlı olarak uygulanmasının, pomalidomidin tek başına uygulanmasına kıyasla, pomalidomidin farmakokinetiği üzerine herhangi bir etkisi olmamıştır.
Deksametazonun, varfarin üzerine olan etkisi bilinmemektedir. Tedavi sırasında varfarin konsantrasyonunun yakından takip edilmesi tavsiye edilir.
Özel popülasyonlara iliskin ek bilgiler Pediyatrik popülasyon:
Multipl Miyelom endikasyonu için 0-17 yaş arası çocuklarda pomalidomidin uygun bir kullanımı yoktur.
POMALEM ile kombine edilen ürünlerin diğer ilaçlar ile etkileşimleri hakkında ek bilgi için ilgili ilaçların güncel KÜB'ne bakınız.
4.6. Gebelik ve laktasyon
Gebelik Kategorisi: X
Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)
Çocuk doğurma potansiyeli olan kadınlar etkili doğum kontrol yöntemi kullanmalıdır. Pomalidomid insan semeninde bulunmaktadır. Önlem olarak pomalidomid kullanmakta olan tüm erkek hastalar, eşleri gebe ise ya da eşlerin çocuk doğurma potansiyelinin olması ve herhangi bir doğum kontrol yöntemi kullanmaması durumunda tedavi süresince, tedaviye ara verilmesi sırasında ve tedavi kesildikten sonra 7 gün süreyle prezervatif kullanmalıdır (bkz. bölüm 4.3 ve 4.4).
Çocuk doğurma potansiyeli olan kadınlar tedaviye başlamadan 4 hafta önce ve süresince (ve tedavinin ardından 4 haftaya kadar) etkili doğum kontrolü uygulamak zorundadırlar (bkz. bölüm 4.3 ve 4.4).
Pomalidomid gebelik boyunca ve gebeliği önlemek için tüm koşullara uyulmadıkça, çocuk doğurma potansiyeli olan kadınlarda kontrendikedir (bkz. bölüm 4.3 ve 4.4).
Gebelik dönemi
POMALEM gebelik döneminde kontrendikedir (bkz. bölüm 4.3).
Pomalidomidin insanlarda teratojenik etkisi olması beklenmektedir.
Pomalidomid ile tedavi edilen kadınlarda gebelik ortaya çıkması halinde, tedavi durdurulmalıdır ve hasta değerlendirme ve tavsiye için teratoloji konusunda uzman veya deneyimli bir hekime sevk edilmelidir. Pomalidomid kullanmakta olan bir erkeğin eşinde gebelik ortaya çıkması halinde, erkeğin eşinin değerlendirme ve tavsiye için teratoloji konusunda uzman veya deneyimli bir hekime sevk edilmesi önerilir.
Laktasyon dönemi
Pomalidomidin insan sütüyle atılıp atılmadığı bilinmemektedir. Pomalidomid anneye uygulandıktan sonra, emziren sıçanların sütünde tespit edilmiştir. Anne sütü alan bebeklerde pomalidomide bağlı advers reaksiyon görülme olasılığı nedeniyle, çocuk için emzirmenin ve kadın için terapinin faydalarını dikkate alarak, emzirmenin mi yoksa tedavinin mi kesileceğine dair bir karar verilmelidir.
Üreme yeteneği/Fertilite
Pomalidomidin hayvanlarda fertiliteyi olumsuz olarak etkilediği ve hayvanlarda teratojenik olduğu gösterilmiştir. Gebe tavşanlara uygulandıktan sonra, pomalidomid plasentaya geçmiştir ve fetal kanda tespit edilmiştir (bkz. bölüm 5.3).
4.7. Araç ve makine kullanımı üzerindeki etkiler
Pomalidomidin araç ve makine kullanma yeteneği üzerine hafif veya orta derecede bir etkisi bulunmaktadır.
Pomalidomid kullanımı ile yorgunluk, depresif bilinç düzeyi, konfüzyon ve baş dönmesi bildirilmiştir. Hastalar pomalidomid ile tedavi edilirken araç, makine kullanmamaları veya tehlikeli işler yapmamaları konusunda uyarılmalıdır.
4.8. İstenmeyen etkiler
Güvenlilik profili özeti
Pomalidomidin bortezomib ve dekzametazon ile kombinasyonu
En sık bildirilen kan ve lenf sistemi hastalıkları nötropeni (%46,8), trombositopeni (%36,7) ve anemidir (%28,4). En sık bildirilen advers reaksiyon periferik duyusal nöropatidir (%47,8). En sık bildirilen 3. veya 4. derece advers reaksiyonlar, nötropeni (%41,7), trombositopeni (%27,3) ve anemi (14,0) gibi kan ve lenf sistemi hastalıklarıdır. En sık bildirilen ciddi advers reaksiyon pnömonidir (%11,5). Bildirilen diğer ciddi advers reaksiyonlar arasında pireksi (%4,0), alt solunum yolu enfeksiyonu (%2,9), pulmoner emboli (%2,9), influenza (%2,9) ve akut böbrek hasarı (%2,9) yer almaktadır.
4.9. Doz aşımı ve tedavisi
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: İmmünosupresanlar, diğer immünosupresanlar ATC kodu: L04AX06
Etki mekanizması:
Pomalidomid direkt antimiyelom tümorisidal ve immünomodülatör aktiviteye sahiptir ve multipl miyelom tümör hücrelerinin çoğalmasında rol oynayan stromal hücre desteğini inhibe eder. Pomalidomid spesifik olarak hematopoietik tümör hücrelerinin proliferasyonunu inhibe
eder ve apopitozisi indükler. Ek olarak, pomalidomid lenalidomide dirençli multipl miyelom hücre dizilerinin proliferasyonunu inhibe eder ve lenalidomide duyarlı ve lenalidomide dirençli hücre dizilerinin her ikisinde de tümör hücrelerinin apopitozisi indüklemede deksametazon ile sinerjistik etki gösterir. Pomalidomid T hücreleri ve Doğal Öldürücü (Natural Killer, NK) hücrelerinin düzenlediği bağışıklığı güçlendirir ve monositler tarafından pro-enflamatuvar sitokinlerin (örn., TNF-α ve IL-6) üretilmesini inhibe eder. Pomalidomid, endotel hücrelerinin göçü ve adhezyonunu engelleyerek, anjiyogenezi de inhibe eder.
Pomalidomid, deoksiribonükleik asit (DNA) hasar bağlayıcı protein 1 (DDB1), cullin 4 (CUL4) ve cullins-1 regülatörünü (Roc1) içeren bir E3 ligaz kompleksinin bir parçası olan protein sereblonuna (CRBN) doğrudan bağlanır ve kompleks içinde CRBN'nin otomatik ubikütinasyonunu inhibe edebilir. E3 ubikütin ligazları, çeşitli substrat proteinlerinin poli- ubikütinasyonundan sorumludur ve pomalidomid tedavisi ile gözlenen pleyiotropik hücresel etkileri kısmen açıklayabilir.
Pomalidomid in vitro varlığında substrat proteinleri Aiolos ve Ikaros, ubikütinasyon ve daha sonra doğrudan sitotoksik ve immünomodülatör etkilere yol açan bozulma için hedeflenir. İn vivo olarak, pomalidomid tedavisi, nükseden lenalidomid-refrakter multipl miyelomlu hastalarda Ikaros seviyelerinde azalmaya yol açmıştır.
Klinik etkililik ve güvenlilik
Pomalidomidin bortezomib ve deksametazon ile kombinasyon tedavisinde
Lenalidomid de dahil olmak üzere en az bir dizi tedavi almış ve son tedavide veya sonrasında hastalık progresyonu göstermiş daha önce tedavi edilen multipl miyelomlu erişkin hastalarda bortezomib ve düşük doz deksametazon (Pom+Btz+DD-Deks) ile kombinasyon halinde pomalidomidin etkililiği ve güvenliliği, Faz III çok merkezli, randomize, açık etiketli çalışmada (CC-4047-MM-007) bortezomib ve düşük doz deksametazon (Btz+DD-Dks) ile karşılaştırılmıştır. Çalışmaya toplam 559 hasta katılmıştır. 281 hasta Pom+Btz+DD-Deks kolunda ve 278 hasta Btz+DD-Deks kolunda randomize edilmiştir. Hastaların %54'ü erkektir ve genel nüfusun medyan yaşı 68'dir (min: 27 – maks: 89 yaş). Hastaların yaklaşık %70'i lenalidomid tedavisine cevap vermemiştir (Pom+Btz+DD-Deks'te %71,2, Btz+DD-Deks'te
%68,7). Hastaların yaklaşık %40'ı 1. relapstadır ve hastaların yaklaşık %73'ü önceki tedavi olarak bortezomib almıştır.
Pom+Btz+DD-deks kolundaki hastalara uygulanmıştır. Her 21 günlük siklusun 1 ila 14. günlerinde oral olarak 4 mg pomalidomid uygulanmıştır. Her iki çalışma kolundaki hastalara, 1 ila 8 siklusları için 21 günlük bir siklusun 1, 4, 8 ve 11. günlerinde ve 9 ve sonrası sikluslar için 21 günlük bir siklusun 1 ve 8. günlerinde bortezomib (1,3 mg/m2/doz) uygulanmıştır. Her iki çalışma kolundaki hastalara 1 ila 8 arasındaki sikluslar için 21 günlük bir siklusun 1, 2, 4,
5, 8, 9, 11 ve 12. günlerinde ve 9. siklustan itibaren sonraki 21 günlük döngünün 1, 2, 8 ve 9 günlerinde düşük doz deksametazon (20 mg/gün [≤ 75 yaşında] veya 10 mg/gün [> 75 yaşında]) uygulanmıştır. Toksisiteyi yönetmek için gerektiğinde dozlar azaltılmış ve tedavi geçici olarak kesilmiş veya durdurulmuştur. (bkz. Bölüm 4.2).
Tedavi amaçlı popülasyon (ITT) için birincil etkililik sonlanım noktası, IMWG kriterlerine dayalı olarak Bağımsız Değerlendirme Kararlaştırma Kurulunun (IRAC) değerlendirmesine göre progresyonsuz sağkalım (Progression Free Survival - PFS)'dır. Ortalama 15,9 aylık takipten sonra, Pom+Btz+DD-deks kolunda medyan PFS süresi 11,20 aydır (%95 GA: 9,66; 13,73). Btz + DD-deks kolunda, medyan PFS süresi 7,1 aydır (%95 GA: 5,88; 8,48).
26 Ekim 2017 tarihli veri kesme tarihi kullanılarak genel etkililik veri özeti Tablo 10'da sunulmuştur. ITT popülasyonunda PFS için Kaplan-Meier eğrisi Şekil 1'de gösterilmektedir.
Tablo 10- Genel etkililik özeti
| Pom+Btz+DD-Deks (N = 281) | Btz+DD-Deks (N = 278) |
PFS (ay) |
| |
Medyana zaman (% 95 GA) | 11,20 (9,66; 13,73) | 7,10 (5,88; 8,48) |
HR (% 95 GA), P-değeri | 0,61 (0,49; 0,77); <0,0001 | |
ORR, n (%) | % 82,2 | % 50,0 |
sCR | 9 (3,2) | 2 (0,7) |
CR | 35 (12,5) | 9 (3,2) |
VGPR | 104 (37,0) | 40 (14,4) |
PR | 83 (29,5) | 88 (31,7) |
OR (95% GA) , P-değeri | 5,02 (3,35; 7,52); <0,001 | |
DoR (ay) |
| |
Medyana zaman (% 95 GA) | 13,7 (10,94 ; 18,10) | 10,94 (8,11 ; 14,78) |
HR (% 95 GA) | 0,76 (0,56; 1,02) | |
Btz = bortezomib; GA = Güven aralığı; CR = Tam yanıt; DoR = Yanıt süresi; HR = Tehlike oranı; DD-Deks = düşük doz deksametazon; OR = Olasılık oranı; ORR = Genel yanıt oranı; PFS = progresyonsuz sağkalım; POM = pomalidomid; PR = Kısmi yanıt; sCR = Kati tam yanıt VGPR = Çok iyi kısmi yanıt.
≤ 5,5 mg/L'ye karşı> 5,5 mg/L) ile CMH testine bağlıdır.
Pom+Btz+DD-deks kolunda medyan tedavi süresi 8,8 ay (12 tedavi siklusu) ve Btz+DD-deks kolunda 4,9 aydır (7 tedavi siklusu).
PFS avantajı, yalnızca bir önceki tedavi rejimini alan hastalarda daha belirgindir. Önceden bir 26 antimiyelom tedavisi alan hastalarda ortalama PFS süresi Pom+Btz+DD-deks kolunda 20,73 ay (% 95 GA: 15,11; 27,99) ve Btz+DD-deks kolunda 11,63 aydır (%95 GA: 7,52,
15,74).
Pom+Btz+DD-deks tedavisi ile %46 risk azalması gözlendi (HR = 0,54; %95 GA: 0,36;
0,82).
Şekil 1. IMWG Kriterlerine Dayalı olarak IRAC Değerlendirmesi ile Progresyonsuz Sağkalım (Sınıflandırılmış Log Sıra Testi) (ITT Popülasyonu)
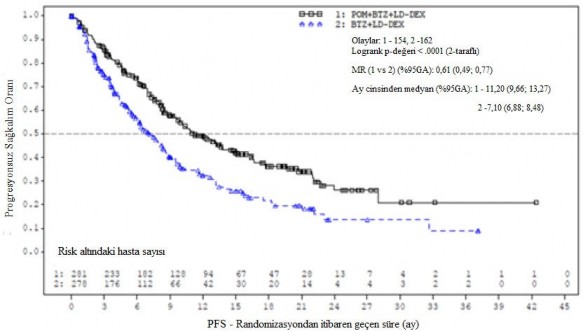
Veri kesim tarihi: 26 Ekim 2017
Genel sağkalım (OS) için 15 Eylül 2018 tarihli veri kesimi kullanılarak (26,2 aylık medyan takip süresi) yakın zamandaki ara analizine göre, Kaplan-Meier tahminleri ile medyan OS zamanı Pom+Btz+DDdeks kolu için 40,5 ay ve Btz +DDdeks kolu için 30,5 aydır (Genel olay oranı %43,3 ile birlikte HR = 0,91, % 95 GA: 0,70; 1,18,).
5.2. Farmakokinetik özellikler
Genel ÖzelliklerEmilim:
Pomalidomid, maksimum plazma konsantrasyonuna (C) doz uygulamasından sonraki 2 ila 3 saat içerisinde ulaşacak şekilde, tek oral doz olarak uygulamayı takiben en az %73 oranında emilir. Pomalidomidin sistemik maruziyeti (EAA) yaklaşık olarak doğrusal ve dozla orantılı bir şekilde artar. Çoklu dozları takiben, EAA'da pomalidomid %27 ila %31 arası bir birikim oranına sahiptir.
Yüksek yağlı ve yüksek kalorili öğünle birlikte uygulanması ortalama plazma C'ını yaklaşık %27'ye kadar azaltarak emilim hızını yavaşlatır, ancak ortalama EAA'da %8'lik bir azalmayla genel emilim miktarı üzerinde minimal bir etkiye sahiptir. Pomalidomid yemeklerle birlikte veya yemeklerden ayrı olarak alınabilir.
Dağılım:
Pomalidomid kararlı durumda 62 ve 138 L arasında bir ortalama sanal dağılım hacmine (Vd/F) sahiptir. Pomalidomid, günde bir defa 2 mg dozunda 4 gün boyunca uygulandıktan
sonra, doz sonrası 4. saatte (yaklaşık olarak T) sağlıklı bireylerin semenine, plazma düzeyinin %67'si kadar bir konsantrasyonda dağılır. In vitro pomalidomid enantiyomerlerinin insan plazmasındaki proteinlere bağlanma oranı %12 ila %44 arasında değişmektedir ve konsantrasyona bağımlı değildir.
Biyotransformasyon:
Pomalidomid, tek bir oral doz [C]-pomalidomid (2 mg) uygulanmış sağlıklı bireylerde in vivo ortamda dolaşımdaki majör bileşendir (yaklaşık olarak plazma radyoaktivitesinin %70'i). Ana veya plazma toplam radyoaktivitesine göre >%10 oranında herhangi bir metabolit bulunmamıştır.
Atılan radyoaktivitenin baskın metabolik yolları, sonraki glukuronidasyon ile hidroksilasyon veya hidrolizdir. In vitro, CYP1A2 ve CYP3A4 pomalidomidin CYP-aracılı hidroksilasyonunda yer alan birincil enzimler olarak belirlenirken, CYP2C19 ve CYP2D6'nın küçük ek katkılarının olduğu saptanmıştır. Pomalidomid aynı zamanda in vitro bir P- glikoprotein substratıdır. Pomalidomidin güçlü CYP3A4/5 ve P-gp inhibitörü ketokonazol ile veya güçlü CYP3A4/5 indükleyicisi karbamazepin ile eş zamanlı uygulanmasının, pomalidomid maruziyeti üzerine klinik olarak anlamlı bir etkisi olmamıştır. Güçlü CYP1A2 inhibitörü fluvoksaminin ketokonazol varlığında pomalidomid ile birlikte uygulanması pomalidomid ile ketokonazole kıyasla pomalidomide ortalama maruziyeti %90 güven aralığı ile [%91 ila %124] %107'ye kadar artırmıştır. Tek başına bir CYP1A2 inhibitörünün metabolizma değişikliklerine etkisini değerlendirmek üzere yapılan ikinci bir çalışmada, pomalidomid ile tek başına fluvoksaminin eş zamanlı olarak uygulanması pomalidomide ortalama maruziyeti, tek başına pomalidomide kıyasla %90 güven aralığı ile [%98 ila %157)
%125 artırmıştır. Güçlü CYP1A2 inhibitörleri (örn., siprofloksasin, enoksasin ve fluvoksamin) pomalidomid ile eş zamanlı olarak uygulanırsa, pomalidomid dozu %50 azaltılmalıdır. CYP1A2 izoformunun tütün ile indüklendiği göz önünde bulundurularak, sigara içenlere pomalidomid uygulamasının, pomalidomidin sigara içmeyenlerdeki maruziyeti ile karşılaştırıldığında maruziyet ile ilgili olarak klinik etkisi olmamıştır.
In vitro verilere dayalı olarak pomalidomid sitokrom P-450 izoenzimlerinin bir inhibitörü veya indükleyicisi değildir ve çalışılmış herhangi bir ilaç taşıyıcısını inhibe etmemiştir. Pomalidomid bu yolakların substratları ile eş zamanlı uygulandığında, klinik olarak anlamlı ilaç-ilaç etkileşmeleri beklenmez.
Eliminasyon:
Pomalidomid, sağlıklı gönüllülerde yaklaşık 9,5 saatlik ve multipl miyelomu olan hastalarda yaklaşık 7,5 saatlik medyan plazma yarılanma ömrü ile elimine edilir. Pomalidomid, yaklaşık 7-10 L/s'lik ortalama toplam vücut klerensine (CL/F) sahiptir.
Sağlıklı bireylere tek doz oral [C]-pomalidomid (2 mg) uygulanmasını takiben radyoaktif dozun %73 ve %15'i sırasıyla idrar ve feçes ile atılırken, uygulanan radyoaktif karbon dozunun %2 ve %8'i idrar ve feçeste pomalidomid şeklinde atılmıştır.
Pomalidomid atılmadan önce büyük ölçüde metabolize edilir, ortaya çıkan metabolitler başlıca idrarla atılır. İdrardaki baskın 3 metabolit (hidroliz veya hidroksilasyon ve ardından glukuronidasyon ile oluşan), idrara geçen dozun sırasıyla yaklaşık %23, %17 ve %12'sini oluşturur.
CYP-bağımlı metabolitler, toplam atılan radyoaktivitenin yaklaşık %43'ünü oluştururken, CYP-bağımlı-olmayan hidrolitik metabolitler %25'ini ve değişmeden atılan pomalidomid de
%10'unu oluşturur (%2 idrarla ve %8 feçes ile).
Popülasyon Farmakokinetikleri
İki kompartmanlı bir modelin kullanıldığı popülasyon farmakokinetik analizine göre, sağlıklı gönüllüler ve MM hastaları benzer görünür klerense (CL/F) ve sanal santral dağılım hacmine (V/F) sahiptir. Pomalidomid periferik dokularda sağlıklı gönüllülerdekine göre 3,7 kat daha yüksek sanal periferik dağılım klerensi (Q/F) ve 8 kat daha yüksek sanal periferik dağılım hacmi (V/F) olacak şekilde tümörler tarafından daha yüksek oranda alınmıştır.
Hastalardaki karakteristik özellikler
Böbrek yetmezliği:
Bu popülasyonda yapılan farmakokinetik analizler böbrek yetmezliği olan hastalarda (kreatinin klerensi veya hesaplanmış glomerüler filtrasyon hızı [eGFR] ile tanımlanan) pomalidomid farmakokinetik parametrelerinin normal böbrek fonksiyonuna (CrCl ≥60 mL/dakika) sahip hastalarla önemli düzeyde farklılık göstermediği görülmüştür. Pomalidomide ortalama normalize EAA maruziyeti, normal böbrek fonksiyonuna sahip hastalara kıyasla orta şiddette böbrek yetmezliği olan hastalarda (eGFR ≥30 ila ≤ 45 mL/dakika/1,73 m) %90 güven aralığı ile [%77,4 ila %120,6] %98,2'dir. Pomalidomide ortalama normalize EAA maruziyeti normal böbrek fonksiyonuna sahip hastalara kıyasla diyaliz gerektirmeyen ciddi böbrek yetmezliği olan hastalarda (CrCl <30 mL/dakika veya eGFR <30 mL/dakika/1,73 m) %90 güven aralığı ile [%79,7 ila %127] %100,2'dir. Pomalidomide ortalama normalize EAA maruziyeti normal böbrek fonksiyonuna sahip hastalara kıyasla diyaliz gerektiren ciddi böbrek yetmezliği olan hastalarda (CrCl <30 mL/dakika, diyaliz gerektiren) %90 güven aralığı ile [%7,5 ila %70] %35,8 artmıştır. Bu böbrek yetmezliği gruplarının her birinde pomalidomide maruziyette ortalama değişiklikler doz ayarlaması gerektirecek bir boyutta değildir.
Karaciğer yetmezliği:
Farmakokinetik parametreler sağlıklı gönüllülere kıyasla karaciğer yetmezliği olan hastalarda (Child-Pugh kriterleri ile tanımlanan) çok hafif düzeyde değişiklik göstermiştir. Pomalidomide ortalama maruziyet sağlıklı gönüllülere kıyasla hafif düzeyde karaciğer yetmezliği olan hastalarda %90 güven aralığı ile [%9 ila %110] %51 artmıştır. Pomalidomide ortalama maruziyet sağlıklı gönüllülere kıyasla orta düzeyde karaciğer yetmezliği olan hastalarda %90 güven aralığı ile [%13 ila %119] %58 artmıştır. Pomalidomide maruziyet sağlıklı gönüllülere kıyasla ağır karaciğer yetmezliği olan hastalarda %90 güven aralığı ile [%24 ila %138] %72 artmıştır. Bu yetmezlik gruplarının her birinde pomalidomide
maruziyetteki ortalama artışlar doz şeması veya doz ayarlaması gerektirecek boyutta değildir (bkz. bölüm 4.2).
Pediyatrik popülasyon:
Nükseden veya progresif primer beyin tümörü olan çocuklarda ve genç erişkinlerde tek bir oral pomalidomid dozunu takiben, ortalama Tmaks değeri dozdan 2 ila 4 saat sonrasıdır ve 74,8 (%59,4), 79,2 (%51.7) ve 104 (%18,3) ng/mL geometrik ortalama Cmaks (%CV) değerleri sırasıyla 1,9, 2,6 ve 3,4 mg/m2 doz seviyelerine karşılık gelmektedir. EAAve EAA, düşük 2 dozda yaklaşık 700 ila 800 saat·ng/mL aralığında ve yüksek dozda yaklaşık 1200 saat·ng/mL aralığında toplam maruziyetle benzer eğilimleri izlemiştir. Tahmini yarı ömürleri, yaklaşık 5 ila 7 saat aralığındadır.
MTD'de yaşa ve steroid kullanımına göre tabakalaşmaya atfedilebilecek net bir eğilim yoktur. Genel olarak veriler, EAA'nın pomalidomid dozundaki artışla neredeyse orantılı olarak arttığını, C'taki artışın ise genellikle orantılı olandan daha az olduğunu göstermektedir.
1,9 mg/m/gün ila 3,4 mg/m/gün oral uygulama doz seviyelerini takiben pomalidomidin farmakokinetiği, tekrarlayan veya progresif pediyatrik beyin tümörlerinde bir Faz 1 ve Faz 2 çalışmasının entegre bir analizinde 4 ila 20 yaş arası 70 hastada belirlenmiştir. Pomalidomid konsantrasyon-zaman profilleri, birinci dereceden absorpsiyonlu ve eliminasyonlu sahip tek bölmeli bir PK modeli ile uygun bir şekilde tanımlanmıştır. Pomalidomid, orta derecede değişkenlikle doğrusal ve zamanla değişmeyen bir farmakokinetik (PK) sergiledi. CL/F, Vc/F, Ka, pomalidomidin gecikme süresinin tipik değerleri sırasıyla 3,94 L/saat, 43 L, 1,45 saat ve 0,454 saattir. Pomalidomidin terminal eliminasyon yarı ömrü 7,33 saattir. Vücut yüzey alanı (BSA) dışında, yaş ve cinsiyet dahil olmak üzere test edilen ortak değişkenlerin hiçbiri pomalidomid farmakokinetiği (PK) üzerinde etkiye sahip değildir. BSA, pomalidomid CL/F ve Vc/F'nin istatistiksel olarak anlamlı bir ortak değişkeni olarak tanımlanmış olmasına rağmen, BSA'nın maruziyet parametreleri üzerindeki etkisi klinik olarak anlamlı kabul edilmemiştir.
Genel olarak, çocuklar ve yetişkin hastalar arasında pomalidomid farmakokinetiği (PK) açısından önemli bir fark yoktur.
Geriyatrik hastalarda:
Sağlıklı gönüllülerde ve multipl miyelomlu hastalarda yapılan farmakokinetik analizlerde, hasta yaşının (19-83 yaş) pomalidomidin oral klerensi üzerinde anlamlı bir etkisi olmadığı gözlenmiştir. Klinik çalışmalarda, pomalidomid kullanan yaşlı (>65 yaş) hastalarda doz ayarlaması gerekmemiştir (bkz. bölüm 4.2).
5.3. Klinik öncesi güvenlilik verileri
Tekrarlanan doz toksisite çalışmaları
Sıçanlarda, pomalidomid 50, 250 ve 1000 mg/kg/gün dozunda 6 ay süreyle kronik olarak uygulandığında iyi tolere edilmiştir. 1000 mg/kg/güne kadar herhangi bir advers bulgu tespit edilmemiştir (4 mg klinik doza göre 175 kat maruziyet).
Pomalidomid, maymunlarda, 9 ay kadar süreyle tekrarlanan doz çalışmalarında incelenmiştir. Bu çalışmalarda maymunlar, pomalidomidin etkilerine sıçanlardan daha yüksek duyarlılık göstermiştir. Maymunlarda gözlenen başlıca toksisiteler, hematopoietik/lenforetiküler sistemle ilişkilendirilmiştir. Maymunlarda 0,05, 0,1 ve 1 mg/kg/gün dozları ile yapılan 9 aylık çalışmada, 1 mg/kg/gün dozunda 6 hayvanda morbidite ve erken ötenazi bildirilmiştir ve bu pomalidomide yüksek maruziyetteki (4 mg klinik doza göre 15 kat maruziyet oranı) immünosupresif etkilere (stafilokok enfeksiyonu, azalmış periferik kan lenfositleri, kalın bağırsakta kronik enflamasyon, histolojik lenfoid azalması ve kemik iliğinde hiposellülerite) bağlanmıştır. 4 maymunun erken ötenazisine neden olan bu immünosüpresif etkiler kötü sağlık koşulları (sulu dışkı, iştahsızlık, besin alımının azalması ve kilo kaybı) yüzündendir; bu hayvanların histopatolojik incelemeleri, kalın bağırsaklarda kronik enflamasyon ve ince bağırsaklarda villöz atrofi olduğunu göstermiştir. Stafilokok enfeksiyonu 4 maymunda görülmüştür; bu hayvanlardan 3'ü antibiyotik tedavisine yanıt vermiştir ve 1 hayvan tedavi edilmeden ölmüştür. Ayrıca, akut miyelojenöz lösemi ile uyumlu bulgular bir maymunun ötenazisine yol açmıştır; bu hayvanda gözlenen klinik gözlemler ve klinik patoloji ve/veya kemik iliği değişiklikleri immünosupresyon ile tutarlı olmuştur. ALP ve GGT düzeyindeki yükselmeler ile ilişkili minimum veya hafif safra kanalı proliferasyonu da 1 mg/kg/gün dozunda gözlenmiştir. İyileşen hayvanlar değerlendirildiğinde, 1 mg/kg/gün grubundaki 1 hayvanda görülen intrahepatik safra kanallarının proliferasyonu haricindeki, tüm tedaviyle ilişkili bulguların dozun kesilmesinden 8 hafta sonrasında geriye döndüğü görülmüştür. Advers Etkinin Gözlenmediği En Düşük Doz 0,1 mg/kg/gün olmuştur (4 mg klinik doza göre 0,5 kat maruziyet oranı).
Genotoksisite/karsinojenisite
Pomalidomid, bakteri ve memeli mutasyon deneylerinde, mutajenik olarak bildirilmemiştir ve insan periferik kan lenfositlerinde kromozomal sapmaları veya 2000 mg/kg/güne kadar olan dozların uygulandığı sıçanların kemik iliklerinde polikromatik eritrositlerde mikroçekirdek oluşmasını indüklememiştir. Karsinojenisite çalışmaları gerçekleştirilmemiştir.
Fertilite ve erken embriyonik gelişim
Sıçanlardaki fertilite ve erken embriyonik gelişim çalışmasında, pomalidomid erkek ve dişi sıçanlara 25, 250 ve 1.000 mg/kg/gün dozlarında uygulanmıştır. Gebeliğin 13. günündeki uterus muayenesinde ortalama canlı embriyo sayısında azalma ve tüm doz düzeylerinde implantasyon sonrası canlı embriyo kayıplarında artma görülmüştür. Bu nedenle, bu gözlenen etkiler için Advers Etkinin Gözlenmediği En Düşük Doz <25 mg/kg/gündür (Bu test edilen en düşük dozda EAA39.960 ng.s/mL (nanogram*saat/mililitre) ve maruziyet oranı 4 mg klinik doza göre 99 kattır). Bu çalışmada tedavi edilen erkekler, tedavi edilmemiş dişilerle çiftleştirildiklerinde, tüm uterus parametreleri kontroller ile benzer olmuştur. Bu sonuçlara dayalı olarak, gözlenen etkiler dişilerin tedavi edilmelerine bağlanmıştır.
Embriyo-fetal gelişim
Pomalidomidin, sıçanlar ve tavşanlara majör organogenez sırasında uygulandığında teratojenik olduğu bulunmuştur. Sıçan embriyofetal gelişim toksisite çalışmasında, idrar torbasının yokluğu, tiroit bezinin yokluğu ve lumbal ve torasik vertebral unsurların (merkezi
ve/veya nöral kemerler) birleşmesi ve yanlış dizilmesi şeklindeki malformasyonlar tüm doz düzeylerinde (25, 250 ve 1.000 mg/kg/gün) gözlenmiştir.
Bu çalışmada herhangi bir maternal toksisite gözlenmemiştir. Bu nedenle, maternal Advers Etkinin Gözlenmediği En Düşük Doz 1.000 mg/kg/gün ve gelişimsel toksisite için Advers Etkinin Gözlenmediği En Düşük Doz <25 mg/kg/gündür (EAAGebeliğin 17. gününde test edilen bu en düşük dozda 34.340 ng.s/mL ve maruziyet oranı 4 mg klinik doza göre 85 kattır). Pomalidomid, tavşanlara 10 ila 250 mg/kg arasında değişen dozlarla uygulandığında, embriyo-fetal malformasyonlar meydana getirmiştir. Tüm dozlarda özellikle 250 mg/kg/gün dozunda kardiyak anomalilerde artma görülmüştür. 100 ve 250 mg/kg/gün dozlarında, implantasyon sonrası kayıplarda hafif artışlar ve fetal vücut ağırlığında hafif azalmalar meydana gelmiştir. 250 mg/kg/gün dozunda, fetal malformasyonlar ekstremite anomalilerini (bükük ve/veya dönmüş ön- ve/veya arka-bacaklar, eklenmemiş veya eksik parmaklar) ve eşlik eden iskelet malformasyonlarını (kemikleşmemiş metakarpal, yanlış dizilmiş falanks ve metakarpal, eksik parmak, kemikleşmemiş falanks ve kısa kemikleşmemiş veya bükülmüş tibia); beyinde orta derecede lateral ventrikül genişlemesini; sağ subklavyen arterin anormal yerleşmesini; akciğerlerde orta lobun olmamasını; düşük-yerleşimli böbreği; değişmiş karaciğer morfolojisini; eksik veya kemikleşmemiş pelvisi; fazladan torasik kaburgalar için artmış bir ortalamayı ve kemikleşmiş tarsallar için azalmış bir ortalamayı içermektedir. 100 ve 250 mg/kg/gün dozlarında maternal vücut kilo alımında hafif azalma, trigliseridlerde belirgin azalma ve mutlak ve göreceli dalak ağırlıklarında belirgin azalma gözlenmiştir. Maternal Advers Etkinin Gözlenmediği En Düşük Doz 10 mg/kg/gün ve gelişimsel Advers Etkinin Gözlenmediği En Düşük Doz <10 mg/kg/gündür (EAA, Gebeliğin 19. gününde bu test edilen en düşük dozda 418 ng.s/mL olmuştur ve bu da 4 mg klinik dozdan elde edilen ile benzerdir).
6. FARMASÖTİK ÖZELLİKLER
6.1. Yardımcı maddelerin listesi
Laktoz anhidrus (inek sütünden elde edilir) Prejelatinize nişasta
Sodyum stearil fumarat Sert kapsül:
Titanyum dioksit Sarı demir oksit Jelatin (sığır jelatini)
İndigotin-FD&C Blue2 Eritrosin- FD&C Red3
6.2. Geçimsizlikler
Yeterli veri yoktur.
6.3. Raf ömrü
24 ay
6.4. Saklamaya yönelik özel tedbirler
25°C altındaki oda sıcaklığında saklayınız.
6.5. Ambalajın niteliği ve içeriği
Ürünümüzün primer ambalaj malzemesi PVC/Aklar– Alüminyum folyo blisterdir. Blisterler karton kutular içerisine paketlenir. Bir kutu içerisinde 21 adet sert kapsül blister ambalajlarda kullanma talimatı ile birlikte sunulmaktadır.
6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
Kapsüller açılmamalı veya ezilmemelidir. Pomalidomid tozu cilt ile temas ederse, cilt hemen ve iyice sabun ve su ile yıkanmalıdır. Pomalidomid mukoz membranlarla temas ederse bol su ile yıkanmalıdır.
Sağlık uzmanları ve bakıcılar, blister veya kapsülü tutarken tek kullanımlık eldivenler giymelidir. Eldivenler cildin maruz kalmasını önlemek için işi bittikten sonra dikkatlice çıkarılmalı, sızdırmaz plastik polietilen torbaya konulmalı ve bölgesel gerekliliklere uygun olarak atılmalıdır. Daha sonra eller su ve sabunla iyice yıkanmalıdır. Hamile olan veya hamile olabileceğinden şüphelenen kadınlar, blister veya kapsülü tutmamalıdır (bkz. Bölüm 4.4).
Kullanılmamış olan ürünler ya da atık materyaller “Tıbbi Atıkların Kontrolü Yönetmeliği†ve “Ambalaj Atıklarının Kontrolü Yönetmelikâ€lerine uygun olarak imha edilmelidir.
 Lösemi Kan Kanseri
Lösemi, kan kanseridir ve vücudunun kan oluşturan dokularının hastalanması anlamına gelir. Birçok lösemi türü vardır; bazı lösemi türleri çocuklarda bazıları da yetişkinlerde sık görülür.
Lösemi Kan Kanseri
Lösemi, kan kanseridir ve vücudunun kan oluşturan dokularının hastalanması anlamına gelir. Birçok lösemi türü vardır; bazı lösemi türleri çocuklarda bazıları da yetişkinlerde sık görülür. |
 Mesane Kanseri
Mesane kanseri her zaman mukozada başlar. Erken safhalarda bu tabakada sınırlı kalır ve
hücre içindeki karsinom olarak nitelendirilir.
Mesane Kanseri
Mesane kanseri her zaman mukozada başlar. Erken safhalarda bu tabakada sınırlı kalır ve
hücre içindeki karsinom olarak nitelendirilir. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| POMALEM | 8699525159731 | 94,767.89TL |
| Diğer Eşdeğer İlaçlar |
 |
Pankreas Kanseri Pankreas karnın alt kısmında yatay şekilde bulunan bir organdır. Sindirime yardımcı olan enzimleri ve kan şekerini yönetmeye yardımcı olan hormonları vücuda dağıtmakla görevlidir. |
 |
Grip, Soğuk Algınlığı ve Öksürük Grip ve soğuk algınlığı (nezle) semptomları arasındaki farkı bilmek önemlidir. Soğuk algınlığı gripten daha hafif belirtiler gösteren bir solunum yolu hastalığıdır. |
 |
Belsoğukluğu, Chlamydia ve Frengi Belsoğukluğu, bakterilerin sebep olduğu bir enfeksiyondur. Cinsel ilişki yoluyla bulaşır ve dölyatağı boynunda, idrar yollarında, anüste, makatta ve boğazda enfeksyona sebep olabilir. |
İLAÇ GENEL BİLGİLERİ
Deva Holding A.Ş.
| Satış Fiyatı | 98063.78 TL [ 2 May 2025 ] |
| Önceki Satış Fiyatı | 98063.78 TL [ 25 Apr 2025 ] |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8699525159762 |
| Etkin Madde | Pomalidomid |
| ATC Kodu | L04AX06 |
| Birim Miktar | 4 |
| Birim Cinsi | MG |
| Ambalaj Miktarı | 21 |
| Antineoplastik ve İmmünomodülatör Ajanlar > İmmünsupresif Ajanlar |
| Yerli ve Beşeri bir ilaçdır. |