RAPIFEN 0.5 mg 2 ml 5 ampül Kısa Ürün Bilgisi
{ Alfentanil }
1. BEŞERİ TIBBİ ÜRÜNÜN ADI
RAPIFEN 0,5 mg/ml 2 ml ampül2. KALİTATİF VE KANTİTATİF BİLEŞİM
Her mililitresinde 0,5 mg alfentanile eşdeğer alfentanil hidroklorür içerir.
Sodyum klorür 9.0 mg/ml
Enjeksiyonluk su y.m.
Yardımcı maddeler için 6.1.’e bakınız.
3. FARMASÖTİK FORMU
Enjeksiyonluk çözelti içeren ampul
RAPIFEN steril, koruyucu madde içermeyen, intravenöz kullanıma uygun izotonik sulu çözeltidir.
4.1. Terapötik endikasyonlar
RAPIFEN aşağıdaki durumlarda endikedir:
• Anestezi indüksiyon ajanı olarak
• Kısa (bolus enjeksiyonlar) ve uzun (bolus, doz artışlarıyla tamamlanan veya infüzyon şeklinde verilen) cerrahi girişimler için genel anestezide narkotik analjezik ve bölgesel anesteziye ek olarak
4.2. Pozoloji ve uygulama şekli
Pozoloji:
RAPIFEN dozu hastanın yaşı, vücut ağırlığı, fiziksel durumu, altta yatan patolojik durumlar, kullandığı diğer ilaçlar, cerrahi ve anestezinin tipine göre bireyselleştirilmelidir.
Başlangıç dozu yaşlılarda ve düşkün hastalarda azaltılmalıdır; sağlıklı çocuklarda ise doz arttırılabilir. Ek dozları belirlerken başlangıç dozunun etkisi göz önüne alınmalıdır.
Bradikardiyi önlemek için indüksiyondan hemen önce intravenöz yolla düşük dozda bir antikolinerjik verilmesi önerilir. Bulantı ve kusmayı önlemek amacıyla droperidol verilebilir.
Uygulama sıklığı, süresi ve uygulama şekli:
İndüksiyon ajanı olarak kullanımı
RAPIFEN’in 120 ^g/kg (17 ml/70 kg) ve üzerindeki intravenöz bolus dozları, yeterli kas gevşemesi sağlanan hastalarda uygun kardiyovasküler stabilitenin idame etmesini sağlarken aynı zamanda hipnoz ve analjeziyi indükleyecektir.
Kısa cerrahi girişimlerde ve ayaktan hastalarda kullanımı
RAPIFEN düşük dozlarda kullanıldığında daha çok minör, kısa ancak ağrılı cerrahi girişimlerde ve ayaktan hastalarda, iyi bir monitorizasyon donanımının bulunması şartıyla, yarar sağlamaktadır.
On dakikadan kısa süreli işlemlerde 7 - 15 ^g/kg’lık (1 - 2 ml/70 kg) bir intravenöz bolus dozu yeterli olacaktır. İşlemin süresi 10 dakikayı geçerse 10-15 dakikada bir veya gerektiğinde 7 - 15 ^g/kg (1 - 2 ml/70 kg) şeklinde ek dozlar verilmelidir.
Çoğu kez 7 ^g/kg (1 ml/70 kg) veya daha düşük bir dozla spontan solunum sürdürülebilir. Bu teknikte yavaş enjeksiyon koşuluyla 3,5 ^g/kg (0,5 ml/70 kg) şeklinde artışlar önerilir.
Derlenme süresini uzatabileceğinden ayaktan hastalara droperidol veya benzodiazepin uygulanmaması tercih edilmektedir. Ayaktan hastalarda tercih edilen teknik, antikolinerjik bir ajan, kısa etkili bir indüksiyon hipnotiği, RAPIFEN ve N2O/O2’den oluşmaktadır.
Postoperatif dönemde oluşabilen bulantı göreceli olarak kısa süreli olup konvansiyonel önlemlerle kolayca kontrol edilir.
Orta süreli cerrahi girişimlerde
Başlangıçtaki intravenöz bolus dozu aşağıdaki gibi cerrahi işlemin tahmini süresine göre ayarlanmalıdır:
Cerrahi girişimin süresi (dakika) | RAPIFEN i.v. bolus doz | |
^g/kg | ml/70 kg | |
10-30 | 20-40 | 3-6 |
30-60 | 40-80 | 6-12 |
> 60 | 80-150 | 12-20 |
Cerrahi daha uzun sürdüğü veya daha agresif olduğunda analjezi aşağıdaki gibi idame ettirilebilir:
• Gerektiğinde 15 ^g/kg’lık (2 ml/70 kg) artışlarla (postoperatif solunum depresyonundan kaçınmak için cerrahinin son 10 dakikası içinde RAPIFEN verilmemelidir)
• Ya da cerrahinin bitmesine 5- 10 dakika kalana kadar 1 ^g/kg/dakika (0,14 ml/70 kg/dakika) hızla infüzyon.
Dozdaki küçük artışlar veya infüzyon hızının geçici olarak artırılmasıyla çok ağrılı uyarı dönemleri kolayca atlatılabilir.
RAPIFEN, N2O/O2 veya başka bir inhalasyon anestetiği olmadan kullanıldığında daha yüksek bir RAPIFEN idame dozu gereklidir.
Uzun süreli cerrahi girişimlerde
Uzun süreli cerrahi işlemlerde, özellikle hızlı bir ekstübasyon gerektiğinde, anestezinin analjezik komponenti olarak RAPIFEN kullanılabilir.
Başlangıç intravenöz dozu bireyselleştirilerek ve infüzyon hızı cerrahi uyaranların şiddeti ve hastanın reaksiyonlarına göre düzenlenerek en uygun analjezi ve stabil bir otonomik durum sağlanabilir.
Uygulama şekli:
RAPIFEN bolus enjeksiyon veya intravenöz infüzyon şeklinde uygulanır.
Özel Popülasyonlara İlişkin Ek Bilgiler
Karaciğer Yetmezliği
Tek bir 50 p,g/kg i.v. doz uygulandığında, sirozlu hastalardaki terminal yarılanma ömrü kontrol grubuna göre istatistiksel olarak anlamlı derecelerde daha uzun olarak bulunmuştur. Dağılım hacmi değişmeden kalır. Alfentanilin serbest fraksiyonu, kontrol grubundaki %11.5’luk rakamlarla karşılaştırıldığında, sirozlu hastalarda %18.5’a yükselmektedir. Serbest fraksiyondaki bu artışla beraber, kontrol grubunda 3.06 mL/dak/kg olan klerensin, sirozlu hastalarda 1.60 mL/dak/kg’a düşmesi, etkinin daha uzun ve belirgin olmasına yol açacaktır (bkz Bölüm 4.4).
Böbrek Yetmezliği
Dağılım hacmi ve serbest fraksiyonun klerensi, böbrek yetmezliği olan hastalarla sağlıklı kontrol grubunda benzerdir. Alfentanilin serbest fraksiyonu, kontrol grubundaki %10.3-11.0’lik rakamlarla karşılaştırıldığında, böbrek yetmezliği olan hastalarda %12.4-19’a yükselmektedir. Bu artış alfentanilin klinik etkisinde bir artışa neden olabilir (bkz Bölüm 4.4).
Pediyatrik Popülasyon
Yenidoğan bebeklerde proteinlere bağlanma oranı %75’dir ve bu oran çocuklarda %85’e yükselir. Plazma klerensi yenidoğan bebeklerde yaklaşık 7.2 ± 3.2mL/kg/dak ve 4.5 ile 7.75 yaş arası çocuklarda 4.7± 1.7 mL/kg/dak.’dır. Kararlı durumdaki dağılım hacmi yenidoğan bebeklerde 1230 ± 520 mL/kg ve çocuklarda 163.5 ±110 mL/kg’dır. Yarılanma ömrü yenidoğan bebeklerde 146 ± 57 dakika ve çocuklarda 40.2 ± 8.9 dakikadır.
Geriyatrik popülasyon
4.3. Kontrendikasyonlar
4.4. Özel kullanım uyarıları ve önlemleri
Tüm güçlü opioidlerle olduğu gibi RAPIFEN aşağıdaki durumlarda dikkatle uygulanmalıdır;
Solunum depresyonu doza bağlıdır ve spesifik narkotik antagonistlerle (nalokson) geri
döndürülebilir ancak solunum depresyonu opioid antagonistin etki süresinden daha uzun
sürebildiğinden ek narkotik antagonist dozlarına gerek duyulabilir. Derin analjeziye;
postoperatif döneme de uzayabilen veya nüksedebilen belirgin solunum depresyonu ve bilinç
kaybı eşlik eder. Bu nedenle hastalar uygun gözetim altında kalmalıdır. Resüsitasyon
4
donanımı ve narkotik antagonistler kolayca ulaşılabilir durumda olmalıdır. Anestezi sırasında hiperventilasyon, hastanın CO2’e yanıtlarını değiştirerek postoperatif dönemdeki solunumu etkileyebilmektedir.
Göğüs kafesi kaslarını da etkileyebilen kas rijiditesi ortaya çıkabilir; ancak yavaş i.v. enjeksiyon (genellikle düşük dozlar için yeterli), benzodiyazepinlerle premedikasyon ve kas gevşeticilerinin kullanımı gibi önlemlerle bu durumdan kaçınılabilir.
Non-epileptik (miyo) klonik hareketler oluşabilir.
Hasta yetersiz dozda antikolinerjik aldığında veya RAPIFEN vagolitik olmayan kas gevşeticilerle kombine edildiğinde, bradikardi ve muhtemelen kardiyak arest oluşabilir. Bradikardi atropinle tedavi edilebilir.
Opioidler özellikle hipovolemik hastalarda hipotansiyonu tetikleyebilir. Stabil bir arter basıncını idame için uygun önlemler alınmalıdır.
İntraserebral kompliyansı olan hastalarda narkotiklerin hızlı bolus enjeksiyonlarından kaçınılmalıdır. Bu hastalarda ortalama arter basıncında geçici bir azalma, bazen serebral perfüzyon basıncının kısa süreli azalması ile birlikte görülebilmektedir.
Uzun süreli opioid tedavisi alanlar veya opioid suistimali öyküsü olan hastalar daha yüksek dozlara gerek duyabilir.
Yaşlılarda ve düşkün hastalarda dozun azaltılması önerilir. Kontrol altına alınamamış hipotiroidizm, akciğer hastalığı, respiratuvar rezervde azalma, alkolizm, karaciğer veya böbrek fonksiyon bozukluğu olan hastalarda opioidler dikkatle titre edilmelidir. Bu hastalarda ayrıca uzun süreli postoperatif izlem gereklidir.
4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri
Alfentanilin Etkisini Modifiye Eden İlaçlar
Barbitüratlar, benzodiyazepinler, nöroleptikler, halojenli gazlar ve diğer selektif olmayan santral sinir sistemi depresanları (örn: alkol) gibi ilaçlar narkotiklerin neden olduğu solunum depresyonunu potansiyalize edebilir.
Hastalar bu ilaçları aldığında, gerekli RAPİFEN dozu olağan dozdan daha düşük olacaktır. Benzer şekilde, RAPİFEN uygulaması ardından diğer SSS depresan ilaçların dozu da azaltılmalıdır.
Alfentanil büyük ölçüde insan sitokrom P450 3A4 enzimiyle metabolize edilmektedir. In vitro veriler, güçlü sitokrom P450 3A4 enzim inhibitörlerinin (örn. ketokonazol, itrakonazol, ritonavir) alfentanil metabolizmasını inhibe edebileceğini düşündürmektedir. Mevcut insan farmakokinetik verileri alfentanil metabolizmasının flukonazol, vorikonazol, eritromisin, diltiazem ve simetidinle (bilinen sitokrom P450 3A4 enzim inhibitörleri) inhibe edildiğini göstermiştir. Bu durum uzun süreli veya gecikmiş solunum depresyonu riskini arttırabilir. Bu ilaçların birlikte kullanımı özel hasta bakım ve gözlemini gerektirir; özellikle de RAPIFEN dozunun azaltılması gerekebilir.
Genellikle herhangi bir cerrahi veya anestezik işlemden 2 hafta önce monoamin oksidaz inhibitörlerinin kesilmesi önerilir.
Alfentanilin Diğer İlaçların Metabolizması Üzerindeki Etkisi
4.6. Gebelik ve laktasyon
Gebelikte Kullanım
Genel Tavsiye
Gebelik Kategorisi : C
Çocuk Doğurma Potansiyeli Bulunan Kadınlar/Doğum Kontrolü (Kontrasepsiyon)
Alfentanilin gebe kadınlarda kullanımına ilişkin yeterli veri mevcut değildir. Hayvanlar üzerinde yapılan çalışmalarda teratojenik veya akut embriyotoksik etkiye rastlanmamıştır (bkz; bölüm 5.3 Klinik öncesi güvenlilik verileri).
İnsanlara yönelik potansiyel risk bilinmemektedir.
Gebelik Dönemi
RAPIFEN plasentayı geçtiğinden ve fetüsün solunum merkezi opioidlere karşı özellikle duyarlı olduğundan doğum sırasında (sezaryen dahil) i.v. RAPIFEN kullanımı önerilmemektedir. Her şeye rağmen RAPIFEN verilmişse bebek için daima bir antidot hazır bulundurulmalıdır.
RAPIFEN gerekli olmadıkça gebelik döneminde kullanılmamalıdır.
Laktasyon Dönemi
RAPIFEN anne sütüne geçebilir. Bu yüzden, RAPIFEN uygulamasını takip eden 24 saat içinde emzirme önerilmemektedir.
Üreme yeteneği (Fertilite)
4.7. Araç ve makine kullanımı üzerindeki etkiler
RAPIFEN uygulamasının ardından ancak yeterli bir süre geçtikten sonra araç ve makine kullanılabilir.
4.8. İstenmeyen etkiler
RAPIFEN’in güvenliliği 18 klinik çalışmada yer alan 1157 denekte değerlendirilmiştir. RAPIFEN bu klinik çalışmalarda kısa, orta ve uzun süreli cerrahi girişimlerde anestezi indüksiyonunda ya da bölgesel ve genel anesteziye analjezi/anestezi açısından yardımcı olarak kullanılmıştır. Denekler en az bir doz RAPIFEN almışlar ve güvenlilikle ilgili veri sağlamışlardır. RAPIFEN uygulanmış deneklerin %1 ya da daha fazlasında görülen Advers İlaç Reaksiyonları Tablo 1’de gösterilmiştir:
Tablo 1, yukarıda belirtilen advers ilaç reaksiyonlarını (ADR) içerecek şekilde hem klinik hem de pazarlama sonrası deneyim sırasında RAPIFEN kullanımından elde edilen ADR’ leri yansıtmaktadır. Tabloda aşağıdaki terimler ve sıklık dereceleri kullanılmıştır:
Çok yaygın (>1/10); yaygın (>1/100 ila <1/10); yaygın olmayan (>1/1.000 ila <1/100); seyrek (>1/10.000 ila <1/1.000); çok seyrek (<1/10.000), izole raporlar dahil.
Tablo 1: RAPIFEN’ in 18 Klinik Çalışma Ve Pazarlama Sonrası Deneyimi Sırasında Tanımlanan Advers İlaç Reaksiyonlarının Sıklık Derecesi
_
Advers İlaç Reaksiyonları | |||||
Sıklık Kategorisi | |||||
Sistem Organ Sınıfı | Çok yaygın (>1/10) | Yaygın (>1/100 ile <1/10) | Yaygın olmayan (>1/1.000 ila <1/100) | Seyrek (>1/10.000 ila <1/1.000) | Bilinmiyor |
İmmün sistem Hastalıkları | Aşırı duyarlılık (anaflaktik reaksiyonlar, anaflaktoid reaksiyonlar ve ürtiker dahil) | ||||
Psikiyatik Hastalıklar | Öforik mizaç | Ajitasyon, Ağlama | Oriyantasyon bozukluğu | ||
Sinir Sistemi Hastalıkları | Hareket bozukluğu, Sersemlik hali, Sedasyon, Diskinezi | Başağrısı, Somnolans, Uyaranlara yanıt alınamaması | Bilinç kaybı (postoperatif dönemde), Konvülsiyon, Miyoklonus | ||
Göz Hastalıkları | Görme bozukluğu | Miyozis | |||
Kardiyak Hastalıklar | Bradikardi, Taşikardi | Aritmi, Kalp hızında azalma | Kardiyak arest | ||
Vasküler Hastalıklar | Hipotansiyon, Hipertansiyon, Kan basıncında azalma, Kan basıncında artış | Toplar damar ağrısı | |||
Solunum Sistemi, Göğüs ve Mediastinal Hastalıklar | Apne | Hıçkırık, Hiperkapni, Larinks spazmı, Solumun depresyonu (ölüm ile sonuçlanma dahil) | Bronkospazm, Burun kanaması | Solunum durması, öksürük | |
Tablo 1: RAPIFEN’ in 18 Klinik Çalışma Ve Pazarlama Sonrası Deneyimi Sırasında Tanımlanan Advers İlaç Reaksiyonlarının Sıklık Derecesi (Devamı)
_
Advers İlaç Reaksiyonları | |||||||||||||||||||||||||||||||||||
Sıklık Kategorisi | |||||||||||||||||||||||||||||||||||
Sistem Organ Sınıfı | Çok yaygın (>1/10) | Yaygın (>1/100 ile <1/10) | Yaygın olmayan (>1/1.000 ila <1/100) | Seyrek (>1/10.000 ila <1/1.000) | Bilinmiyor | ||||||||||||||||||||||||||||||
Gastrointestin al Hastalıklar | Bulantı, Kusma | ||||||||||||||||||||||||||||||||||
Deri ve Deri altı Doku Hastalıkları | Alerjik dermatit, Aşırı terleme | Kaşıntı | Eritem, Döküntü | ||||||||||||||||||||||||||||||||
Kas-İskelet Sistemi ve Bağ Dokusu Hastalıkları | Kas rijiditesi | ||||||||||||||||||||||||||||||||||
Genel Bozukluklar ve Uygulama Yeriyle İlişkili Durumlar | Ürperme, Enjeksiyon yerinde ağrı, Yorgunluk | Ağrı | Pireksi | ||||||||||||||||||||||||||||||||
Yaralanma, Zehirlenme ve Uygulamayla İlişkili Komplikasyon lar | Uygulamaya bağlı ağrı | Ameliyat sonrası ajitasyon, Anestezide havayolu komplikasyonu, Ameliyat sonrası konfüzyon | Nörolojik anestezi komplikasyonu, Uygulamaya bağlı komplikasyon, Endotrakeal entubasyon komplikasyonu | 4.9. Doz aşımı ve tedavisiBelirti ve Semptomlar RAPIFEN doz aşımının belirtileri farmakolojik etkilerinin bir uzantısıdır. Bireyin duyarlılığına bağlı olarak klinik tablo primer olarak bradipne ile apne arasında değişebilen solunum depresyonunun derecesi ile belirlenir. Önerilen Tedavi Hipoventilasyon veya apne varlığında oksijen verilmeli ve gerektiğinde solunuma yardımcı olunmalı veya solunum kontrol edilmelidir. Solunum depresyonunu kontrol için gerektiğinde nalokson gibi spesifik bir narkotik antagonist kullanılmalıdır. Bunun dışında gereken diğer acil önlemler de alınmalıdır. Solunum depresyonu, antagonistin etkisinden daha uzun sürebildiğinden ek antagonist dozları gerekli olabilir. Solunum depresyonu kas rijiditesi ile ilişkiliyse, destekli veya kontrollü solunumu kolaylaştırmak için bir intravenöz nöromüsküler bloker gerekebilir. Hasta dikkatle gözlenmeli, vücut sıcaklığı ve yeterli sıvı alımı sürdürülmelidir. Hipotansiyon şiddetliyse veya devam ederse hipovolemi olasılığı düşünülmeli ve mevcutsa uygun parenteral sıvı uygulaması ile kontrol edilmelidir. 5. FARMAKOLOJİK ÖZELLİKLER5.1. Farmakodinamik özelliklerFarmakoterapötik grup: Narkotik Analjezikler ATC Kodu: N01A H02 Alfentanil güçlü, hızlı ve kısa etkili bir narkotik analjezik olup kimyasal açıdan fentanile benzerdir. İntravenöz uygulamadan sonra alfentanil anında etkisini gösterir ve başlangıç etkisi fentanilin eşdeğer analjezi dozunun yalnızca dörtte birine ulaşır. 1-2 dakika içinde en yüksek analjezik ve solunumu baskılayıcı etki oluşur (morfinle 30 dakika içinde). Alfentanilin etki süresi fentanilin eşdeğer analjezi dozunun yalnızca üçte biri kadar olup doza bağlıdır. 60 dakikadan daha uzun süreli analjezi için infüzyon tercih edilebilir. Solunum hızı ve alveoler ventilasyon üzerindeki baskılayıcı etkileri de fentanilinkinden daha kısa olup çoğu kez analjezinin süresi solunum depresyonunun süresini aşmaktadır. Solunum depresyonunun süresi ve derecesi doza bağlı olma eğilimindedir. Alfentanilin yüksek dozları (> 120 ^g/kg) bilinç kaybına neden olduğundan anestezi indüksiyonu için kullanılabilir. İndüksiyon düzgün seyreder, ağrısız olup entübasyona karşı kardiyovasküler ve hormonal stres yanıtlarına neden olmaz. Alfentanilin güvenlik aralığı çok geniştir. Sıçanlarda en düşük düzeyde analjezi için LD50/ED50 oranı alfentanilde 1080, buna karşın petidin, morfin ve fentanilde sırasıyla 4,6, 69,5 ve 277’dir. Diğer narkotik analjeziklerle ortak olarak alfentanil doz ve uygulama hızına bağlı olarak hem kas sertliği hem de öfori, miyozis ve bradikardiye neden olabilir. Alfentanil 200 ^g/kg’a varan dozlarda histamin düzeylerinde anlamlı bir artış oluşturamamış veya histamin salınımının klinik kanıtlarını göstermemiştir. Alfentanil uygulamasından sonra iyileşme hızlı ve düzgün seyirli olup postoperatif bulantı ve kusma insidansı düşüktür. 5.2. Farmakokinetik özelliklerGenel Özellikler Alfentanil yalnızca intravenöz yoldan kullanılan ve ^-agonist farmakolojik etkileri olan sentetik bir opioiddir. Emilim: Alfentanil intravenöz olarak uygulandığından, geçerli değildir. Dağılım: Alfentanilin ardışık dağılım yarı ömürleri 0,4-2,2 ve 8-32 dakikadır. Düşük iyonizasyon derecesi (pH = 7,4’de %11) hızlı ancak kısıtlı doku dağılımına katkıda bulunmaktadır. Dağılım hacimleri 1,27-4,81 L (merkezi kompartımandaki dağılım hacmi) ve 12,1-98,2 L (kararlı durumdaki dağılım hacmi) bildirilmiştir. Alfentanilin plazma proteinlerine bağlanma oranı yaklaşık %92’dir. Metabolizma: Alfentanil esas olarak karaciğerde metabolize edilmektedir. İdrarda değişmeden atılan alfentanil miktarı ancak % 1 kadardır. Metabolitler inaktif formda olup % 70-80’i idrarla atılır. Eliminasyon: 5.3. Klinik öncesi güvenlilik verileriYalnızca insanlarda kullanılan en yüksek dozu yeterince aşkın olduğu düşünülen dozlarda gözlemlenen klinik öncesi etkiler klinik kullanım açısından pek anlam taşımamaktadır. Alfentanil, intravenöz (fare, sıçan, kobay, köpek) uygulama sonrası tek doz toksisiteyi; köpek ve sıçanda 1 aya kadar tekrarlayan doz toksisiteyi; sıçanda fertilite ve genel üreme performansını, sıçan ve tavşanlarda teratojenite ve embriyotoksisiteyi, sıçanlarda perinatal/postnatal üremeyi test eden intravenöz üreme çalışmaları dahil olmak üzere bir dizi klinik olmayan güvenlilik çalışmaları ile test edilmiştir. Mutajenisite, salmonella typhimurium üzerinde yapılan in vitro nokta ve/veya gen mutasyonu çalışmaları ve sıçanlarda kromozomal sapmaların incelenmesi için yapılan in vivo mikronükleus değerlendirmeler ve erkek ve dişi farelerde dominant lethal (öldürücü) doz testi dahil olmak üzere hem in vitro hem de in vivo çalışmalar ile değerlendirilmiştir. Ayrıca intra-arteriyel uygulamayı, histamin salınımını ve hemolizi değerlendiren bazı özel çalışmalar da yürütülmüştür. Tek ve tekrarlayan doz toksisiteleri, üreme, mutajenisite ve özel çalışmalara ilişkin raporların sonuçlarında alfentanilin iyi tolere edildiği ve hayvan ED50 değerleri ve farklı planlanan klinik doz rejimleri ile karşılaştırıldığında geniş bir güvenlik aralığına sahip olduğu gösterilmiştir. Bu hayvan modellerinde gözlenen toksisiteler ve mortalite genellikle önerilen klinik terapötik sınırın (2,6 ile 83 kez) üstündeki yüksek toksik dozlar veya sekonder olarak bu ilacın aşırı farmakolojik aktivitesi ile ilişkilidir. 6. FARMASÖTİK ÖZELLİKLER6.1. Yardımcı maddelerin listesi- Sodyum klorür 6.2. GeçimsizliklerEnjeksiyon için çözelti, diğer ürünlerle karıştırılıp kullanılmamalıdır. İstendiğinde, RAPIFEN, sodyum klorür veya glukoz intravenöz enfüzyonları ile karıştırılabilir. Bu tür seyreltiler plastik infüzyon setleriyle uyumludur. Bunların 24 saat içinde kullanılması gerekir. 6.3. Raf ömrü6.5. Ambalajın niteliği ve içeriği6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanıma Hazırlama Talimatları: 1. Ampulu baş ve işaret parmağınız arasında tutunuz. Ampulun ucunu boşta bırakınız. 2. Diğer elinizin işaret parmağını ampulun boynuna ve başparmağını renkli tanımlama halkasına (halkalarına) paralel olacak şekilde renkli noktaya koyarak ampulun ucunu tutunuz. Renkli - halka(lar) Renkli nokta Kırma düzeyi 3. Başparmağınızı bu nokta üzerinde tutup elinizle ampulun diğer kısmını sıkıca kavrayarak hızla ampulun ucunu kırınız. 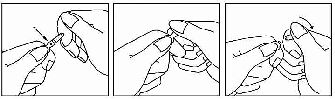
İLAÇ GENEL BİLGİLERİ
Johnson & Jonhson Sıhhi Malzeme San. ve Tic.Ltd.Şti.
| |||||||||||||||||||||||||||||||
| Satış Fiyatı | TL |
| Önceki Satış Fiyatı | |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Kırmızı Reçeteli bir ilaçdır. |
| Barkodu | 8699593755330 |
| Etkin Madde | Alfentanil |
| ATC Kodu | N01AH02 |
| Birim Miktar | 0.5 |
| Birim Cinsi | MG |
| Ambalaj Miktarı | 5 |
| Sinir Sistemi > Genel Anestezikler > Alfentanil |
| İthal ve Beşeri bir ilaçdır. |




