RAPILYSIN 10 U IV enj. için steril liyofilize toz içeren flakon Saklanması
{ Reteplaz }
Kan ve Kan Yapıcı Organlar > Antitrombotik İlaçlar > Reteplaz Actavis İlaçları A.Ş | Güncelleme : 14 November 20115.RAPILYSIN'in saklanması
25°C'nin altındaki oda sıcaklığında saklayınız.
Liyofilize tozu ışıktan korumak için flakonları ambalajında saklayınız. Kuru ortamda saklanmalıdır.
Belirtilen şekilde hazırlanan çözelti hemen kullanılmalıdır.
Uygulamadan önce renk değişikliği ve partikül oluşumu açısından gözlenmelidir.
RAPILYSIN'i çocukların göremeyeceği, erişemeyeceği yerlerde ve ambalajında saklayınız. Son kullanma tarihiyle uyumlu olarak kullanınız.
Ambalajdaki son kullanma tarihinden sonra RAPILYSIN'i kullanmayınız.
Ruhsat Sahibi:
ACTAVİS İLAÇLARI AŞ. Gültepe Mah. Harman Cad. Ali Kaya Sok. Polat İş Merkezi No:2 B Blok Kat:1-7-8 Levent-İSTANBUL
Üretim yeri:
Actavis Gorup PTC ehf /İzlanda lisansı ile,
Roche Diagnostics GmbH,
Sandhofer Str. 116, D-68305, Mannheim/Almanya
Çözücü su, Vetter Pharma_Fertigung GmbH&Co KG/Almanya tarafından üretilmektedir.
AŞAĞIDAKİ BİLGİLER BU İLACI UYGULAYACAK SAĞLIK PERSONELİ İÇİNDİR
Hazırlama boyunca aseptik teknik kullanılmalıdır.
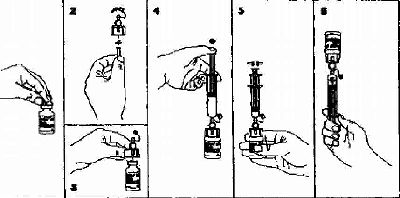
1. RAPILYSIN flakonundaki koruyucu kapağını çıkarınız ve plastik kapağı alkolle temizleyiniz.
2. Sulandırma adaptörünün bulunduğu ambalajı açıp, sulandırma adaptöründeki ki her iki koruyucu kapağı çıkarınız.
3. Sulandırma adaptörünün iğnesini RAPILYSIN flakonunun kauçuk kapağından içeri sokunuz.
4. Ambalajından 10 mL'lik enjektörü çıkarınız. Enjektörün ucundaki kapağı çıkararak enjektörü sulandırma adaptörüne takınız ve RAPILYSIN flakonuna 10 mL çözücü aktarınız.
5. Sulandırma adaptörü ve enjektör flakona takılı iken flakonu hafifçe çevirerek RAPILYSIN tozu çözünüz. ÇALKALAMAYINIZ.
6. Sulandırılmış ilaç berrak, renksiz bir çözelti halini alacaktır. Çözelti berrak veya renksiz değilse atılmalıdır.
7. Enjektöre tekrar 10 mL RAPILYSIN çözeltisini çekiniz. Fazla dolum nedeniyle flakonda küçük miktarda çözelti kalabilir.
8. Enjektörü sulandırma adaptöründen çıkartarak ambalajda bulunan steril iğneyi takınız. Doz intravenöz uygulama için artık hazırdır.
9. Heparin ve RAPILYSIN çözelti içerisinde karıştırıldıklarında geçimsizdirler. Diğer geçimsizlikler de mevcut olabilir. Enjeksiyon çözeltisine başka bir ilaç eklenmemelidir.
10. RAPILYSIN uygulaması için ayrılan damar yolundan RAPILYSIN uygulamasından önce veya sonra veya aynı anda başka bir ilaç kesinlikle uygulanmamalıdır. Bu uyarı tekrar tromboz oluşma riskini azaltmak için reteplaz uygulamasından önce veya sonra uygulanan heparin ve asetil salisilik asit dahil tüm ilaçlar için geçerlidir.
11. Aynı damar yolunun kullanılması gereken hastalarda, bu damar yolu (Y-bağlantı dahil olmak üzere) RAPILYSIN enjeksiyonundan önce ve sonra %0.9 sodyum klorür çözeltisi veya %5 dekstroz çözeltisi ile iyice yıkanmalıdır.
i
Tekrarlayan kullanımı
Henüz tekrarlayan RAPILYSIN kullanımına (yeniden uygulanması) ilişkin deneyim mevcut değildir. Bu nedenle tekrarlı kullanımı önerilmemektedir. Reteplaz molekülüne karşı antikor oluşumu görülmemiştir.
RAPILYSIN de dahil olmak üzere bazı önceden doldurulmuş enjektörlerin bazı iğnesiz bağlantılar ile uyumsuzluğu bildirilmiştir. Bu nedenle, cam enjektör ve intravenöz girişin uyumluluğu, kullanımdan önce garanti edilmelidir. Uyumsuzluk varsa, bir adaptör kullanılabilir ve uygulamadan hemen sonra cam şırınga ile birlikte çıkarılır.
 Kalbe giden kan akışı durduğunda kalp krizi meydana gelir.
Kalbe giden kan akışı durduğunda kalp krizi meydana gelir.
 HIV, Human Immunodeficiency Virus’dür (İnsanlarda Bağışıklık Sistemini Bozan
Virüsdür). Bu virüs AIDS hastalığına sebep olur.
HIV, Human Immunodeficiency Virus’dür (İnsanlarda Bağışıklık Sistemini Bozan
Virüsdür). Bu virüs AIDS hastalığına sebep olur.
 Astımlı kişilerin akciğerlerindeki hava boruları (bronşlar) hassastır. Bu kişiler belirli tetikleyici faktörlere maruz kaldıklarında, hava boruları nefes almalarını güçleştirecek şekilde daralır.
Astımlı kişilerin akciğerlerindeki hava boruları (bronşlar) hassastır. Bu kişiler belirli tetikleyici faktörlere maruz kaldıklarında, hava boruları nefes almalarını güçleştirecek şekilde daralır.
 İnme, beynin hasar görmesinin sonucudur. Bu hasar, beynin bir kısmındaki ya bir kanama
ya da akut kan eksikliği nedeniyle o kısmın geçici ya da kalıcı olarak işlevini yapamamasına
yol açar.
İnme, beynin hasar görmesinin sonucudur. Bu hasar, beynin bir kısmındaki ya bir kanama
ya da akut kan eksikliği nedeniyle o kısmın geçici ya da kalıcı olarak işlevini yapamamasına
yol açar.
 Grip ve soğuk algınlığı (nezle) semptomları arasındaki farkı bilmek önemlidir. Soğuk algınlığı gripten daha hafif belirtiler gösteren bir solunum yolu hastalığıdır.
Grip ve soğuk algınlığı (nezle) semptomları arasındaki farkı bilmek önemlidir. Soğuk algınlığı gripten daha hafif belirtiler gösteren bir solunum yolu hastalığıdır.
İLAÇ GENEL BİLGİLERİ
Actavis İlaçları A.Ş
| Geri Ödeme Kodu | A11803 |
| Satış Fiyatı | TL |
| Önceki Satış Fiyatı | |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8699517271533 |
| Etkin Madde | Reteplaz |
| ATC Kodu | B01AD07 |
| Birim Miktar | 10 |
| Birim Cinsi | IU/ML |
| Ambalaj Miktarı | 2 |
| Kan ve Kan Yapıcı Organlar > Antitrombotik İlaçlar > Reteplaz |
| İthal ( ref. ülke : Yunanistan ) ve Beşeri bir ilaçdır. |