REGINON 0.02 mg /0.075 mg 63 draje K�sa �r�n Bilgisi
{ Gestoden + Etinilestradiol }
1. BE�ER� TIBB� �R�N�N ADI
REG�NON 20 mcg/75 mcg kapl� tablet
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Her kapl� tablet etkin madde olarak 75 mcg gestoden ve 20 mcg etinilestradiol i�erir.
Yard�mc� maddeler
Her bir kapl� tablet
Laktoz monohidrat (s���r kaynakl�) 36,865 mg
�eker 19,631 mg i�erir.
Yard�mc� maddeler i�in 6.1'e bak�n�z
3. FARMAS�T�K FORMU
Kapl� tablet
Beyaz renkli, bikonveks, yuvarlak parlak kapl� tablet
Hafta: Kapl� tabletsiz d�nemin yakla��yor olmas� nedeni ile g�venilirlikte azalma riski y�ksektir. Yine de, kapl� tablet al�m�nda ayarlamalar yap�larak kontraseptif korumada azalma �nlenebilir. E�er unutulan kapl� tabletten �nceki 7 g�n boyunca kapl� tabletler do�ru olarak al�nd�ysa, a�a��daki iki se�enekten birinin uygulamas�yla ek bir kontraseptif y�nteme gerek kalmaz.
Tromboz veya kan p�ht�la�mas� ilk belirtileri (�rne�in, bacakta/bacaklarda ola�an d��� a�r�lar veya �i�me, g�zle g�r�l�r bir neden olmaks�z�n nefes al�rken veya �ks�r�rken b��ak gibi saplanan a�r�lar). G���ste a�r� veya s�k��ma hissi
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Oral kontrasepsiyon (do�um kontrol�)
REG�NON re�ete etme karar�, ven�z tromboembolizmi (VTE) olan kad�nlar ba�ta olmak �zere, her kad�n�n mevcut risk fakt�rleri ve REG�NON ile ortaya ��kan VTE riskinin di�er kombine hormonal kontraseptifler (KHK) ile kar��la�t�rmas� (bkz. b�l�m 4.3 ve b�l�m 4.4) dikkate al�narak verilmelidir.
4.2. Pozoloji ve uygulama �ekli
Kombine oral kontraseptifler (KOK), do�ru �ekilde kullan�ld�klar�nda y�lda yakla��k % 1 ba�ar�s�zl�k oran�na sahiptir. �la� unutuldu�unda ya da yanl�� kullan�ld���nda ba�ar�s�zl�k oran� artabilir.
Kapl� tabletler, paketin �st�nde g�sterildi�i y�nde, her g�n yakla��k ayn� zamanda bir miktar suyla al�nmal�d�r. Birbirini izleyen 21 g�n boyunca her g�n bir kapl� tablet al�n�r. Her bir sonraki pakete 7 g�nl�k, s�kl�kla �ekilme kanamas�n�n izlendi�i, kapl� tablet al�nmayan d�nemi takiben ge�ilir. Bu kanama genellikle son kapl� tabletin al�nmas�n� takiben 2.-3. g�n ba�lar ve bir sonraki pakete ba�land���nda kesilmemi� olabilir.
Uygulama �ekli:
Oral kullan�m i�indir. REG�NON'a ba�lang��
Bir �nceki ay hormonal kontraseptif kullan�m� yoksa: Kapl� tablet al�m�na kad�n�n normal siklusunun ilk g�n� (kanamas�n�n ilk g�n�) ba�lanmal�d�r. Kapl� tabletlere 2. ile 5. g�nler aras�nda ba�lanmas� da kabul edilebilir, ancak bu durumda ilk siklus i�in kapl� tablet al�nmaya ba�lanmas�ndan itibaren 7 g�n boyunca ilave olarak bir bariyer kontrasepsiyon y�ntemi kullan�lmal�d�r.
Bir kombine hormonal kontraseptiften ge�i� (kombine oral kontraseptif (KOK), vajinal halka, transdermal flaster): Tercihen �nceki kombine oral kontraseptif�n son aktif kapl� tabletini (hormon i�eren son kapl� tablet) izleyen g�n REG�NON al�m�na ba�lanmal�d�r. En ge� ise kapl� tabletsiz d�nemi ya da hormon i�ermeyen kapl� tablet d�neminin ertesi g�n�nde ba�lanabilir. Vajinal halka ya da transdermal flaster kullan�lmas� durumunda, kullan�c� d�ng� paketindeki son halkan�n ya da flasterin ��kar�ld��� g�n ya da en ge� bir sonraki uygulaman�n yap�lmas� gereken g�n REG�NON'a ba�lamal�d�r.
Yaln�z progestagen i�eren bir y�ntemden (minipil, enjeksiyon, implant) ya da progesteron sal�ml� rahim i�i sistemden (R�S) ge�i�: Minipilden herhangi bir g�nde, (implant veya R�S'in ��kar�ld��� g�n, enjeksiyonda ise bir sonraki enjeksiyonun yap�lmas� gereken g�n) ge�i�
yap�labilir. Ancak t�m bu ko�ullarda kapl� tablet al�m�n�n ilk 7 g�n� ek bir bariyer y�ntemi kullan�lmas� �nerilir.
�lk trimestr d�����n� takiben: Hemen ba�lanabilir. Ek kontraseptif �nlemler al�nmas�na ihtiya� duyulmaz.
Do�umu veya ikinci trimestr d�����n� takiben: Emziren kad�nlar i�in bkz. Gebelik ve laktasyon.
Emzirmeyen kad�nlar�n do�umu veya ikinci trimestr d�����n� takiben: 21.-28. g�nlerde ba�lanmas� �nerilir. Daha sonra ba�land��� takdirde kapl� tablet al�m�n�n ilk 7 g�n� ek bir bariyer y�ntemi kullan�lmal�d�r. E�er o zamana kadar ili�ki ger�ekle�tiyse, kombine oral kontraseptif kullan�m� ba�lamadan �nce gebelik ekarte edilmeli veya ilk menstruel kanama beklenmelidir.
Kapl� tablet al�m� unutuldu�unda: E�er kullan�c� kapl� tabletini almakta, 12 saatten daha az ge� kalm��sa kontraseptif koruyuculuk azalmaz. Hat�rlan�r hat�rlanmaz kapl� tablet al�nmal� ve sonraki kapl� tabletler de her zamanki gibi al�nmaya devam edilmelidir.
E�er 12 saatten daha fazla gecikme olmu�sa kontraseptif koruyuculuk azalm�� olabilir. Bu durumda 2 temel kural uygulan�r:
Kapl� tablet al�m�na hi� bir zaman 7 g�nden fazla ara verilmez.
4.3. Kontrendikasyonlar
KOK'lar a�a��da belirtilen durumlarda kullan�lmamal�d�r. KOK kullan�rken a�a��daki durumlardan herhangi birinin ilk kez g�r�lmesi halinde kullan�m derhal durdurulmal�d�r.
Etkin ya da yard�mc� maddelerden herhangi birine kar�� a��r� duyarl�l�k
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Uyar�lar
A�a��da belirtilen durum veya risk fakt�rlerinden herhangi biri varsa, REG�NON'un uygun olup olmad��� kad�n ile tart���lmal�d�r.
Bu durumlardan veya risk fakt�rlerinden herhangi birinin �iddetlenmesi veya ilk defa ortaya ��kmas� halinde, kad�n�n REG�NON kullan�m�n�n sonland�r�lmas�n�n gerekli olup olmad���n�n belirlenmesi i�in doktoru ile ileti�ime ge�mesi tavsiye edilmelidir.
Dola��m bozukluklar� VTE Riski
KHK kullanan kad�nlarda VTE riski kullanmayanlara g�re artar. Levonorgestrel, norgestimat veya noretisteron i�eren �r�nler en d���k VTE riski ile ili�kilendirilmi�tir. REG�NON gibi di�er �r�nlerde ise bu riskin iki kat�na kadar ��kabilir. En d���k VTE riskine sahip oldu�u bilinenlerden farkl� bir �r�n�n kullan�lmas� karar�, ancak kad�n�n REG�NON ile ili�kili VTE riskini, mevcut risk fakt�rlerinin bu riski nas�l etkiledi�ini ve VTE riskinin kullan�m�n�m ilk y�l�nda en y�ksek oldu�unu anlad���ndan emin olduktan sonra al�nmal�d�r. Ayr�ca KHK kullan�m�na 4 hafta veya daha uzun s�re ara verildikten sonra tekrar ba�land���nda riskin artt���n� g�steren baz� kan�tlar vard�r.
KHK kullanmayan ve gebe olmayan kad�nlarda, 10.000 ki�iden yakla��k 2'si bir y�ll�k s�re i�inde VTE geli�tirir. Bununla birlikte, herhangi bir kad�nda altta yatan risk fakt�rlerine ba�l� olarak s�z konusu risk �ok daha y�ksek olabilir (a�a�� bak�n�z).
Gestoden i�eren KHK kullanan 10.000 kad�ndan 9 ila 12'sinin bir y�l i�inde VTE geli�tirece�i tahmin edilmektedir; bu oran levonorgestrel i�eren KHK kullanan kad�nlarda 6 civar�ndad�r.
D���k dozlu KHK'ler ile bir y�ldaki VTE say�s� gebelikte veya postpartum d�nemde kad�nlarda beklenen say�dan d���kt�r.
VTE, bu vakalar�n %1-2'sinde �l�mc�l olabilir.
Bir y�l i�inde her 10.000 kad�nda g�r�len VTE vakas� say�s�
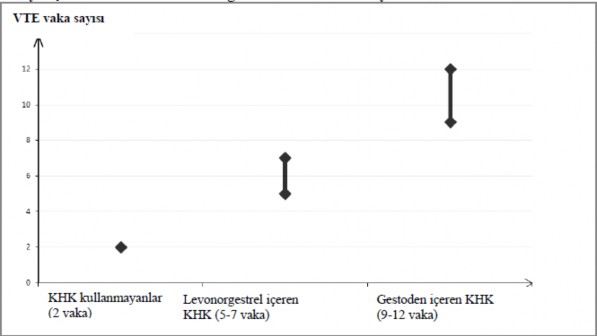
Son derece nadir olarak, KHK kullan�c�lar�nda di�er kan damarlar�nda (�rn. hepatik, mesenter, b�brek veya retinal toplardamarlar ve atardamarlar) tromboz meydana geldi�i rapor edilmi�tir.
VTE risk fakt�rleri
Ven�z tromboembolik komplikasyon riski KHK kullan�c�lar�nda �zellikle �oklu risk fakt�rleri oldu�unda, ilave risk fakt�rleri olan kad�nlarda ciddi �l��de artabilir (bkz. Tablo: VTE Risk fakt�rleri).
Y�ksek ven�z tromboz riski olu�turan �oklu risk fakt�rleri mevcut olan kad�nda REG�NON kullan�m� kontrendikedir (bkz. b�l�m 4.3). Bir kad�n birden fazla risk fakt�r�ne sahipse risk art��� t�m fakt�rlerin ayr� ayr� toplam�ndan fazla olabilir ve bu durumda toplam VTE riski dikkate al�nmal�d�r. Fayda ve risk dengesinin negatif oldu�u d���n�l�yorsa KHK re�ete edilmemelidir (bkz. b�l�m 4.3).
Tablo: VTE Risk fakt�rleri
Risk fakt�r�: | A��klama |
Obezite (v�cut kitle indeksi 30 kg/m'nin | V�cut kitle indeksi y�kseldi�inde risk ciddi |
�st�ndeyse) | �l��de artar. Di�er risk fakt�rleri mevcutsa �zellikle dikkate al�nmal�d�r. |
Uzun s�reli hareketsizlik, maj�r cerrahi m�dahale, bacaklara ve pelvise cerrahi m�dahale, n�rocerrahi, veya maj�r travma
Not: 4 saatten fazla hava yolu seyahati dahil ge�ici hareketsizlik de �zellikle di�er risk fakt�rleri olan kad�nlarda VTE i�in bir risk fakt�r� olabilir. | Bu durumlarda ilac� kesmek (cerrahi m�dahale durumunda en az 4 hafta) ve tamamen iyile�tikten iki hafta sonras�na kadar devam etmemek �nerilir. �stenmeyen gebeli�i �nlemek i�in ba�ka bir kontrasepsiyon y�ntemi kullan�lmal�d�r.
�nceden REG�NON kesilmemi�se, antitrombotik tedavi d���n�lmelidir. |
Pozitif aile ge�mi�i (Hi�bir ebeveyn ya da karde�te erken ya�larda (�rn. 50 ya��ndan gen�) VTE g�r�lmemi�se.) | Kal�t�msal bir e�ilimden ��pheleniliyorsa, KHK kullan�m�ndan �nce mutlaka bir uzmandan tavsiye al�nmal�d�r. |
VTE ile ili�kili di�er t�bbi durumlar | Kanser, sistemik lupus eritematoz, hemolitik �remik sendrom ve kronik inflamatuar ba��rsak hastal�klar� (Crohn hastal��� veya �lseratif kolit) ve orak h�cre hastal���. |
�lerleyen ya� | �zellikle 35 ya� �st� |
Varik�z venlerin ve y�zeysel tromboflebitin ven�z tromboembolideki olas� rol� konusunda g�r�� birli�i yoktur.
Gebelikte ve �zellikle 6 haftal�k puerperium periyodunda tromboemboli riskindeki art�� dikkate al�nmal�d�r (bkz. b�l�m 4.6).
VTE semptomlar� (Derin Ven Trombozu-DVT ve Pulmoner Emboli-PE)
Semptomlar olmas� halinde, kad�nlara acil t�bbi yard�m almalar� ve sa�l�k �al��anlar�n� KHK ald�klar� konusunda bilgilendirmeleri tavsiye edilmelidir.
DVT semptomlar� a�a��dakileri kapsayabilir:
bacakta/ayakta tek tarafl� ya da bacaktaki bir damar boyunca �i�me;
Elektif maj�r operasyondan (�rn. abdominal, ortopedik), herhangi bir bacak ameliyat�ndan, varisli damarlar veya uzun s�reli hareketsizlik (�rn. kazalar veya ameliyattan sonra) i�in t�bbi tedaviden alt� hafta �nce. Tam y�r�r hale geldikten sonra 2 hafta ge�inceye kadar yeniden ba�lamay�n. Acil cerrahi durumunda genellikle trombotik profilaksi endikedir, �rn. subkutan�z heparin.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Enzim �nd�kleyicileri
Mikromozal enzimleri ind�kleyen ila�lar (�zellikle sitokrom P450 3A4) ile aras�ndaki etkile�imler seks hormonu klerensinde art��a neden olabilir, bu durum da ara kanamaya ve/veya kontraseptif ba�ar�s�zl��a yol a�abilirler.
Birka� g�nl�k tedavinin ard�ndan enzim ind�ksiyonu g�zlemlenebilir. En fazla enzim ind�ksiyonu genellikle birka� hafta i�inde g�r�l�r. Enzim ind�ksiyonu, ila� tedavisinin kesilmesinin ard�ndan 4 hafta kadar s�rebilir.
Belirtilen ila�lardan herhangi biri ile tedavi edilmekte olan kad�nlar, KOK'a ek ge�ici bir bariyer y�ntemi kullanmal� ya da ba�ka bir kontrasepsiyon y�ntemi se�melidirler. �la�lar ile birlikte kullan�mlar� s�resince ve tedavinin kesilmesini takiben 28 g�n boyunca bariyer y�ntemi kullanmal�d�rlar. E�er bariyer y�ntemi kullan�lan d�nem KOK kutusundaki tabletlerin bitiminden sonra devam ediyorsa, bir sonraki kutuya ara vermeden devam edilmelidir. Bu durumda, ikinci paketin sonuna kadar �ekilme kanamas� beklenmemelidir. Hasta, ikinci paketin bitiminden sonraki tablet kullan�lmayan d�nemde �ekilme kanamas� ya�amazsa, sonraki pakete devam etmeden �nce gebelik olas�l���n�n elenmesi gerekir.
Enzim ind�kleyicilerle uzun s�reli tedavi alan kad�nlar i�in, ba�ka bir kontrasepsiyon y�ntemi kullan�lmal�d�r.
A�a��dakilerin KOK'larla klinik olarak anlaml� etkile�imlerinin oldu�u g�sterilmi�tir:
Antikonv�lsanlar: barbit�ratlar (fenobarbital dahil), primidon, fenitoin, karbamazepin, okskarbazepin, topiramat.
Antibiyotikler/antifungaller: griseofulvin, rifampisin.
Bitkisel ila�lar: St John's wort (kantaron - Hypericum perforatum) Antiretroviral ajanlar: ritonavir, nelfinavir, nevirapin.
Not: Cinsiyet hormonlar�n�n plazma konsantrasyonunu art�rabilen ba�ka antiretroviral ajanlar da vard�r.
KOK klerensini azaltan maddeler (enzim inhibit�rleri):
Azol antifungaller (�rn. itrakonazol, vorikonazol, flukonazol), verapamil, makrolidler (�rn. klaritromisin, eritromisin), diltiazem ve greyfurt suyu gibi kuvvetli ve orta d�zeyde CYP3A4 inhibit�rleri �strojen veya progesteron veya her ikisinin de plazma konsantrasyonunu art�rabilir.
60 - 120 mg/g�n etorikoksib dozlar�n�n 0,035 mg etinilestradiol i�eren KHK ile e� zamanl� olarak al�nd��� takdirde etinilestradiol�n plazma konsantrasyonlar�n� s�ras�yla 1,4 - 1,6 kat artt�rd��� g�r�lm��t�r.
KOK'lerin di�er t�bbi �r�nler �zerine etkisi:
Oral kontraseptifler di�er baz� ila�lar�n metabolizmas�n� etkileyebilir. Buna ba�l� olarak plazma ve doku konsantrasyonlar� artabilir (�rn. siklosporin, tizanidin, teofilin) ya da azalabilir (�rn. lamotrigin).
Farmakodinamik etkile�imler
Ribavirinli veya ribavirin i�ermeyen; Ombitasvir, paritaprevir, ritonavir ve dasabuvirin, kombinasyonlar�n� i�eren t�bbi �r�nlerin birlikte uygulanmas� ALT seviyelerinde artma riskini y�kseltebilir (bkz. b�l�m 4.3 ve b�l�m 4.4).
Bu nedenle, REG�NON kullan�c�lar�, bu kombinasyon ila� rejimiyle tedaviye ba�lamadan �nce alternatif bir kontrasepsiyon y�ntemine (�rne�in, sadece progestajenle kontrasepsiyon veya hormonal olmayan y�ntemler) ge�melidir. REG�NON, bu kombinasyon ila� rejimi ile tedavi tamamland�ktan 2 hafta sonra yeniden ba�lat�labilir.
Di�er etkile�im �ekilleri:
Laboratuvar Testleri
Oral kontraseptiflerin kullan�lmas�, �rn. kortikosteroid ba�lay�c� globulin ve lipid/lipoprotein fraksiyonlar�, karbonhidrat metabolizmas� parametreleri ve koag�lasyon ve fibrinoliz parametreleri gibi karaci�er, tiroid, adrenal ve renal fonksiyonun biyokimyasal parametreleri dahil olmak �zere belirli laboratuvar testlerinin sonu�lar�n� etkileyebilir. Bu nedenle laboratuvar testleri istendi�inde, laboratuvar personeline oral kontraseptif kullan�m� hakk�nda bilgi verilmelidir. Not: Olas� etkile�meleri belirlemek amac�yla e�zamanl� kullan�lacak ilac�n prospekt�s�ne (kullanma talimat�na) ba�vurulmal�d�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
�zel pop�lasyonda etkile�im �al��mas� yap�lmam��t�r. Pediyatrik pop�lasyon:
Pediyatrik pop�lasyonda etkile�im �al��mas� yap�lmam��t�r.
4.6. Gebelik ve laktasyon
Genel tavsiyeGebelik kategorisi: X
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon) REG�NON do�um kontrol� amac�yla kullan�lmaktad�r. Kullan�ld��� s�rece fertiliteyi engeller.
Gebelik d�nemi
REG�NON'un gebelikte kullan�m� kontrendikedir. Gestoden ve etinilestradiol gebelik d�neminde uyguland��� takdirde ciddi do�um kusurlar�na yol a�maktad�r.
REG�NON kullan�m� s�ras�nda gebelik meydana gelmesi durumunda kullan�m durdurulmal�d�r. Ancak, yayg�n epidemiyolojik �al��malar ne gebeli�inden �nce kombine oral kontraseptif kullanm�� olan kad�nlar�n �ocuklar�nda do�umsal kusur riskinde herhangi
bir art��� ne de erken gebeli�i s�resince yanl��l�kla kombine oral kontraseptif kullan�ld���nda olu�an bir teratojenik etkiyi g�stermemi�tir.
REG�NON kullan�m�na yeniden ba�larken postpartum d�nemi s�ras�nda artan VTE riski dikkate al�nmal�d�r (bkz. b�l�m 4.2 ve b�l�m 4.4.)
Laktasyon d�nemi
REG�NON'un emzirme d�neminde kullan�lmas� �retilen s�t hacminde azalmaya ve bile�iminde de�i�ikli�e neden olabilir. Etkin maddelerin �ok k���k bir miktar� s�tle at�l�r. Bu miktar, �ocu�u �zellikle do�umdan sonraki ilk 6 hafta i�inde etkiler. Emziren annelere, ba�ka bir kontrasepsiyon y�ntemi kullanmalar� �nerilebilir.
�reme yetene�i/Fertilite
REG�NON bir KHK'd�r. Kullan�ld��� s�rece fertiliteyi engeller.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
REG�NON'un ara� ve makine kullanma becerileri �zerinde bilinen bir etkisi bulunmamaktad�r.
4.8. �stenmeyen etkiler
REG�NON ile en yayg�n olarak bildirilen advers reaksiyonlar mide bulant�s�, abdominal a�r�, kilo art���, ba� a�r�s�, depresif ruh hali, duygu durum bozuklu�u, meme a�r�s�, meme hassasiyetidir. Kullan�c�lar�n ≥ %1'inde meydana gelir.
Ciddi advers reaksiyonlar ATE ve VTE'dir.
Pazarlama sonras� raporlanan advers reaksiyonlar Ba����kl�k sistemi hastal�klar�
Kal�tsal anjiyo�demin alevlenmesi
Sinir sistemi hastal�klar�
Korenin alevlenmesi
Gastrointestinal hastal�klar
�lseratif kolit
Hepatobiliyer hastal�klar
Karaci�er fonksiyon bozukluklar�
Deri ve deri alt� doku bozukluklar�:
Kloazma
�reme sistemi ve meme hastal�klar�
Azalm�� adet kanamas�, lekelenme, ani kanama, �ekilme kanamas� yoksunlu�u, tablet sonras� amenore
Advers reaksiyonlar, a�a��da sistem-organ s�n�f� (MedDRA) ve s�kl�k derecesine g�re listelenmektedir. S�kl�k dereceleri �u �ekilde tan�mlanmaktad�r; �ok yayg�n (>1/10), yayg�n (>1/100, <1/10), yayg�n olmayan (>1/1.000, <1/100), seyrek (>1/10.000 ila <1/1.000), �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Ba����kl�k sistemi hastal�klar�
Seyrek: A��r� duyarl�l�k
Metabolizma ve beslenme hastal�klar�
Yayg�n olmayan: S�v� tutulumu
Psikiyatrik hastal�klar
Yayg�n: Depresif duygu durumu, duygu durum de�i�iklikleri Yayg�n olmayan: Libido azalmas�
Seyrek: Libido art���
Sinir sistemi hastal�klar� Yayg�n: Ba� a�r�s� Yayg�n olmayan: Migren
G�z hastal�klar�
Seyrek: Kontakt lens intolerans�
Gastrointestinal hastal�klar Yayg�n: Bulant�, kar�n a�r�s� Yayg�n olmayan: Kusma, diyare
Vask�ler hastal�klar�
Seyrek: Ven�z tromboembolizm (VTE), arteryel tromboembolizm (ATE)
Deri ve deri alt� doku hastal�klar�
Yayg�n olmayan: D�k�nt�, �rtiker
Seyrek: Eritema nodozum, eritema multiforme
�reme sistemi ve meme hastal�klar� Yayg�n: Meme a�r�s�, meme hassasiyeti Yayg�n olmayan: Memede hipertrof� Seyrek: Vajinal ak�nt�, memede ak�nt�
Ara�t�rmalar
Yayg�n: Kiloda art�� Seyrek: Kilo kayb�
Se�ilmi� advers reaksiyonlar�n tan�m�
KHK kullanan kad�nlarda �zel kullan�m uyar�lar� ve �nlemleri b�l�m�nde daha ayr�nt�l� olarak ele al�nm�� miyokard infarkt�s�, inme, ge�ici iskemik ataklar, ven�z tromboz ve pulmoner emboli dahil olmak �zere arteriyel ve ven�z trombotik ve tromboembolik olaylarda art�� riski g�zlemlenmi�tir. KOK kullanan kad�nlarda bildirilen, “�zel kullan�m uyar�lar� ve �nlemleri” b�l�m�nde bahsi ge�en ciddi advers olaylar:
Ven�z tromboembolik bozukluklar
4.9. Doz a��m� ve tedavisi
Doz a��m�na ba�l� bildirilen ciddi yan etki yoktur. G�r�lebilecek belirtiler, bulant�, kusma ve �ekilme kanamas�d�r. �ekilme kanamas�, ilac� yanl��l�kla almalar� halinde k�z �ocuklar�nda menar�tan �nce bile g�r�lebilir. Antidotu yoktur ve tedavisi semptomatik olmal�d�r.
Sar�l�k ba�lang�c�, hepatit, t�m v�cutta ka��nt�
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: �strojenler ve progestojenler, f�ks kombinasyonlar ATC kodu: G03AA10
Etki mekanizmas�
Bu �strojen-progestojen kombinasyonu, luteinizan hormonun orta d�ng� art���n� bast�rarak yumurtlamay� inhibe etmek, rahim a�z� mukusunu dehidrasyon yoluyla koyultarak sperm i�in bir bariyer olu�turmak ve endometriyumu implantasyona kapal� hale getirmek suretiyle etki g�sterir.
Ruhsatland�rma sonras� g�venlilik �al��mas� (PASS) VTE tan�s� s�kl���n�n d���k �strojen dozlu (<50 μg etinilestradiol) KOK kullan�c�lar�nda y�lda 7 ila 10/10000 aral���nda oldu�u g�sterilmi�tir. En yeni veriler VTE tan�s� s�kl���n�n gebe olmayan KOK kullanmayan ki�ilerde y�lda yakla��k 4/10000, gebe kad�nlarda ya da post partum s�re�te ise 20 ila 30/10 000 oldu�unu ileri s�rmektedir.
KOK kullan�m� ile ili�kili VTE riski �strojen bile�eninden kaynaklan�r. KOK'lar�n progesteron bile�eni taraf�ndan VTE riski �zerinde herhangi bir mod�le etki etti�i halen tart���lmaktad�r. Etinilestradiol/gestoden i�eren KOK'lar�n levonorgestrel i�eren KOK'lara k�yasla VTE risk art���n� g�steren epidemiyolojik �al��malar VTE riskinin hi� artmad���n� veya 3 kata kadar artt�rd���n� g�steren farkl� sonu�lar bildirmi�tir.
KOK'lar gebelikten korumalar�n�n yan� s�ra, sahip olduklar� baz� olumsuz �zellikler d���nda (Bkz. �zel kullan�m uyar�lar� ve �nlemleri, 4.8. �stenmeyen Etkiler) do�um kontrol y�ntemi se�mede y�nlendirici olabilecek ek yararlar sunabilmektedir. Sikluslar daha d�zenli, kanamalar s�kl�kla daha az a�r�l� ve daha hafiftir. Kanamalar�n daha hafif olmas� demir yetmezli�i g�r�lme olas�l���n� azalt�r. Bunlar�n d���nda, endometriyum ile ovaryum kanserlerinde azalma g�sterilmi�tir. Ayr�ca, daha y�ksek dozlu KOK'lar�n (0.,05 mg etinilestradiol), ovaryum kistlerinde, pelvik inflamatuvar hastal�k, benign meme hastal��� ve ektopik gebelik g�r�lme s�kl�klar�nda azalma sa�lad��� g�sterilmi�tir. Bunlar�n d���k doz KOK'lar i�in de ge�erli oldu�u hen�z g�sterilmemi�tir.
5.2. Farmakokinetik �zellikler
Genel �zelliklerGestoden Emilim:
A��zdan al�nan gestoden h�zla ve tamamen emilir. Tek al�m� takiben yakla��k 1 saat sonra 4 ng/ml olan en y�ksek plazma konsantrasyonlar�na ula��l�r. Gestodenin mutlak biyoyararlan�m�, uygulanan dozun %99'u olarak belirlenmi�tir.
Da��l�m:
Gestodenin belirgin da��l�m hacmi 0,7 l/kg olarak belirlenmi�tir. Gestoden serum albuminine ve seks hormonu ba�lay�c� globuline (SHBG) ba�lan�r. Yakla��k olarak % 50-70 oran�nda spesifik olarak SHBG'lere ba�lan�r ve total serum d�zeylerinin yaln�zca %l-2si serbest steroid halinde bulunur.
Ba��l da��l�m (serbest, alb�mine ba�l�, SHBG'ye ba�l�) serumdaki SHBG konsantrasyonlar�na ba�l�d�r. Ba�lay�c� proteinin ind�klenmesinin ard�ndan, ba�lanmam�� ve alb�mine ba�l� fraksiyonlar azal�rken, SHBG'ye ba�l� fraksiyon artar.
Biyotransformasvon:
Biyotransformasyon, steroid metabolizmas�n�n bilinen yolaklar�n� takip eder. Bilinen farmakolojik olarak aktif metabolit bulunmamaktad�r. Serumdan metabolik klerens oran� yakla��k 0,8 ml/dak/kg olarak belirlenmi�tir. Eliminasvon:
Gestoden serum d�zeyleri iki fazda azal�r. Terminal dispozisyon faz� 12-15 saatlik bir yanlanma �mr� ile karakterizedir. Gestoden, de�i�memi� formda de�il, yakla��k 1 g�nl�k bir yar�lanma �mr� ile elimine edilen metabolitler olarak at�l�r. Gestoden metabolitleri yakla��k 6: 4 olan idrar/safra oran�nda at�l�r.
Do�rusall�k / do�rusal olmavan durum:
G�nl�k REG�NON uygulamas�n�n tekrarlanmas�n�n ard�ndan, serumdaki gestoden konsantrasyonlar� 2,8 kat artmaktad�r. Ortalama serum seviyeleri, tedavi d�ng�s�n�n ikinci yar�s� boyunca ula��lan kararl� durum ko�ullar�nda d�rt kat daha fazlad�r. Gestoden farmakokineti�i SHBG serum seviyelerinden etkilenir. REG�NON ile tedavi s�ras�nda, ilk tedavi d�ng�s�nde serum SHBG seviyelerinde �� katl�k bir art�� g�zlemlenmi�tir. Gestoden, SHBG'ye spesifik olarak ba�land��� i�in SHBG seviyelerindeki art��a neredeyse paralel olarak gestoden serum seviyelerinde art�� olu�ur. �� tedavi d�ng�s�nden sonra, d�ng� ba��na SHBG ind�ksiyonunun kapsam� art�k de�i�mez. Etinilestradiol
Emilim:
Oral olarak al�nan etinilestradiol h�zla ve tamamen emilir. REG�NON'un al�nmas�n�n ard�ndan 1,4 saat i�inde 82 pg/ml'lik maksimum ila� seviyesi konsantrasyonuna eri�ilir. Da��l�m:
Etinilestradiol i�in yakla��k 5 L/kg'l�k g�r�n�r da��l�m hacmi ve serumdan yakla��k 5 ml/dak/kg'lik metabolik bir klerens h�z� belirlenmi�tir. Etinilestradiol, serum alb�minine y�ksek d�zeyde ba�lan�r ancak spesifik olarak ba�lanmaz. Yakla��k %2'lik ila� seviyeleri ba�lanmam�� olarak kal�r. Biyotransformasvon:
Etinilestradiol, absorpsiyon ve ilk karaci�er ge�i�i s�ras�nda metabolize olarak mutlak ve de�i�ken oral biyoyararlan�m� azal�r. Eliminasvon:
Etinilestradiol serum seviyeleri, 1-2 saat ve yakla��k 20 saatlik yar� �m�r ile karakterize iki a�amada d��er. Analitik nedenlere ba�l� olarak bu parametreler ancak daha y�ksek dozlar�n uygulanmas�ndan sonra hesaplanabilir.
De�i�meyen ila� at�lmaz. Etinilestradiol metabolitleri, yakla��k 1 g�nl�k bir yar� �m�rle 4:6 olan idrar/safra oran�nda at�l�r.
Do�rusall�k / do�rusal olmavan durum:
Serum ve g�nl�k al�m terminal dispozisyon evresinin yar�lanma �mr�ne g�re, kararl� durum serum seviyelerine 3-4 g�n sonra ula��lmakta olup, kararl� durum seviyeleri tekli bir doza k�yasla %30-40 daha y�ksektir.
Laktasyon d�neminde, g�nl�k anne dozunun %0,02'si yenido�ana s�t ile aktar�labilir.
Etinilestradiol�n sistemik yararlan�m�, di�er ila�larca her iki y�nde etkilenebilir. Bununla birlikte, y�ksek dozlarda C vitamini ile etkile�im yoktur. Etinilestradiol, s�rekli kullan�m s�ras�nda SHBG ve CBG'nin (kortikoid ba�lay�c� glob�lin) hepatik sentezini ind�kler. Ancak SHBG ind�ksiyonunun kapsam�, kimyasal yap�ya ve e�zamanl� olarak uygulanan progestojenin dozuna g�re de�i�ir. REG�NON ile tedavi s�ras�nda, serumdaki SHBG konsantrasyonlar�, 69 nmol/L'den ba�lay�p birinci d�ng�de 198 nmol/L'ye ve ���nc� d�ng�de 210 nmol/l'e y�kselmi�tir. Serum CBG konsantrasyonlar� 37 μg/ml'den ba�lay�p ilk d�ng�de 85 μg/ml'ye ��km�� ve bundan sonra sabit kalm��t�r.
5.3. Klinik �ncesi g�venlilik verileri
:Di�er kontraseptif steroidlerle oldu�u gibi etinilestradiol ve gestoden kombinasyonu, s��an karaci�erinde artan neoplastik nod�l insidans� ile ili�kilidir. Bunun insanla ili�kisi
bilinmemektedir. Uzun s�reli oral kontraseptif kullananlarda nadiren k�t� huylu karaci�er t�m�rleri bildirilmi�tir.
�lac� re�ete edeni ilgilendirebilecek ve K�B'�n di�er ilgili b�l�mlerine hen�z dahil edilmemi� olan ba�ka klinik �ncesi g�venlik verisi mevcut de�ildir.
Kan bas�nc�nda �nemli art��
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Laktoz monohidrat (s���r kaynakl�) Sodyum kalsiyum EDTAM�s�r ni�astas� P.V.P(K 30)
Magnezyum stearat �eker
Talk
Montan glycol wax Kalsiyum karbonat Polietilen glikol 6000 Saf su
6.2. Ge�imsizlikler
Ge�erli de�il.
6.3. Raf �mr�
36 ay
6.4. Saklamaya y�nelik �zel tedbirler
25°C alt�ndaki oda s�cakl���nda saklay�n�z.
6.5. Ambalaj�n niteli�i ve i�eri�i
21 ve 63 kapl� tabletlik takvimli Al/PVC blister ambalaj
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller "T�bbi At�klar�n Kontrol� Y�netmeli�i" ve "Ambalaj ve Ambalaj At�klar�n�n Kontrol� Y�netmeliklerine uygun olarak imha edilmelidir.
 L�semi Kan Kanseri
L�semi, kan kanseridir ve v�cudunun kan olu�turan dokular�n�n hastalanmas� anlam�na gelir. Bir�ok l�semi t�r� vard�r; baz� l�semi t�rleri �ocuklarda baz�lar� da yeti�kinlerde s�k g�r�l�r.
L�semi Kan Kanseri
L�semi, kan kanseridir ve v�cudunun kan olu�turan dokular�n�n hastalanmas� anlam�na gelir. Bir�ok l�semi t�r� vard�r; baz� l�semi t�rleri �ocuklarda baz�lar� da yeti�kinlerde s�k g�r�l�r. |
 A��r� Alkol Kullan�m�, Alkolizm
Alkol ba��ml�l���, alkol kullan�m� ve alkol sorunlar� aras�ndaki fark� a��klamak g��t�r.
�rne�in, ge�mi�te alkol kullanm�� olan bir kimsenin mutlaka alkol ba��ml�s� olmas�
gerekmez.
A��r� Alkol Kullan�m�, Alkolizm
Alkol ba��ml�l���, alkol kullan�m� ve alkol sorunlar� aras�ndaki fark� a��klamak g��t�r.
�rne�in, ge�mi�te alkol kullanm�� olan bir kimsenin mutlaka alkol ba��ml�s� olmas�
gerekmez. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| REGINON | 8699828120049 | |
| Di�er E�de�er �la�lar |
 |
Diyabet Hastal��� Diyabet, ins�lin hormonu ile ilgili problemlerden kaynaklanan bir hastal�kt�r. |
 |
Ruh ve Ak�l Sa�l���m�z� Geli�tirmek �yi ak�l ve ruh sa�l��� sahip olmaktan ziyade, yapt���n�z �eylerdir. Ak�l ve ruhsal olarak sa�l�kl� olmak i�in kendinize de�er vermeli ve kendinizi kabul etmelisiniz. |
 |
Kalp Krizi Kalbe giden kan ak��� durdu�unda kalp krizi meydana gelir. |
�LA� GENEL B�LG�LER�
Ko�ak Farma �la� ve Kimya Sanayi A.�.
| Sat�� Fiyat� | 395.17 TL [ 22 Sep 2023 ] |
| �nceki Sat�� Fiyat� | 395.17 TL [ 15 Sep 2023 ] |
| Original / Jenerik | Jenerik �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699828120056 |
| Etkin Madde | Gestoden + Etinilestradiol |
| ATC Kodu | G03AA10 |
| Birim Miktar | 0,02+0,075 |
| Birim Cinsi | MG |
| Ambalaj Miktar� | 63 |
| �rogenital Sistem ve Cinsiyet Hormonlar� > Sistemik Hormonal Gebeli�i �nleyici �la�lar > Gestoden + etinilestradiol |
| Yerli ve Be�eri bir ila�d�r. |