RISPERDAL CONSTA 37.5 mg 1 enjekt�r K�sa �r�n Bilgisi
{ Risperidon }
1. BE�ER� TIBB� �R�N�N ADI
RISPERDAL CONSTA 37,5 mg IM enjeksiyonluk uzat�lm�� sal�ml� s�spansiyon Steril
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Risperidon 37,5 mg
Suland�r�ld�ktan sonra, 1 ml s�spansiyon 18,75 mg risperidon i�erir.
Yard�mc� maddeler
Her 1 ml s�spansiyonda:
Sodyum klor�r 6 mg
Sodyum hidroksit 0,54 mg
Karmeloz sodyum 40mPa.s 22,5 mg Disodyum hidrojen fosfat dihidrat 1,27 mg
Yard�mc� maddeler i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Enjeksiyonluk uzat�lm�� sal�ml� s�spansiyon
Beyaz-beyaz�ms� serbest ak�c� toz i�eren flakon ve berrak, renksiz, seyreltici i�eren kullan�ma haz�r dolu enjekt�r
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
RISPERDAL CONSTA �izofreni ve �izoafektif bozukluk tedavisinde endikedir. RISPERDAL CONSTA, pozitif (hal�sinasyon, del�zyon, d���nce bozukluklar�, sald�rganl�k, ��phecilik) ve/veya negatif (k�nt afekt, emosyonel ve sosyal �ekingenlik ve konu�ma yetersizli�i) semptomlar�n belirgin oldu�u, erken d�nem psikozlar, akut �izofrenik alevlenmeler, kronik �izofreni ve di�er psikotik durumlar dahil �izofreni hastalar�n�n tedavisinde endikedir.
RISPERDAL CONSTA �izofreni ile ilgili afektif semptomlar� (depresyon, su�luluk duygusu, endi�e) da azalt�r.
RISPERDAL CONSTA (risperidon), duygu durum epizotlar�n�n olu�mas�n� geciktirmek amac�yla bipolar I bozuklu�un tedavisinde monoterapi veya lityum ve valproat tedavisine ek olarak kullan�labilir. (bkz. B�l�m 5.1).
RISPERDAL CONSTA, bipolar I bozuklu�u olan hastalarda, duygu durum epizotlar�n�n olu�mas�n� geciktirmek amac�yla destekleyici idame tedavisi olarak endikedir (bkz. B�l�m 5.1).
4.2. Pozoloji ve uygulama �ekli
Pozoloji:RISPERDAL CONSTA iki haftada bir uygulanmal�d�r. Yeti�kinler
�nerilen doz iki haftada bir intram�sk�ler 25 mg'd�r. Baz� hastalarda 37,5 mg ya da 50 mg gibi daha y�ksek dozlarla yarar sa�lanabilir. Klinik �al��malarda, �izofreni hastalar�nda 75 mg ile ek fayda g�zlenmemi�tir. Bipolar bozuklu�u olan hastalarda 50 mg'�n �zerindeki dozlar �al���lmam��t�r. �ki haftada bir 50 mg'dan daha y�ksek dozlar �nerilmemektedir.
�lk RISPERDAL CONSTA enjeksiyonundan sonraki �� haftal�k gecikme d�neminde yeterli d�zeyde oral risperidon veya bir �nceki antipsikotik ila� deste�i verilmelidir (bkz. B�l�m 5.2).
Ba�lang�� dozu
�nerilen doz iki haftada bir intram�sk�ler 25 mg'd�r. �ki hafta veya daha uzun s�re sabit dozda oral risperidon kullanan hastalar i�in a�a��da verilen d�ng� dikkate al�nmal�d�r. 4 mg veya daha d���k dozda oral risperidon ile tedavi edilen hastalar 25 mg RISPERDAL CONSTA, daha
y�ksek oral dozlarla tedavi edilen hastalar i�in ise 37,5 mg'l�k daha y�ksek RISPERDAL CONSTA dozu d���n�lmelidir.
Hastalar halihaz�rda oral risperidon alm�yorsa, I.M. ba�lang�� dozunu se�erken oral �n tedavi dozaj� d���n�lmelidir. �nerilen ba�lang�� dozu iki haftada bir 25 mg RISPERDAL CONSTA'd�r. Oral antipsikotiklerin daha y�ksek dozlar�n� kullananan hastalar i�in 37,5 mg'l�k daha y�ksek RISPERDAL CONSTA dozu d���n�lmelidir.
�lk RISPERDAL CONSTA enjeksiyonundan sonraki �� haftal�k gecikme d�neminde oral risperidon veya bir �nceki antipsikotik ile yeterli antipsikotik koruma sa�land���ndan emin olunmal�d�r. (bkz. B�l�m 5.2).
RISPERDAL CONSTA, ilk RISPERDAL CONSTA enjeksiyonunu takiben �� haftal�k gecikme d�neminde oral risperidon veya bir �nceki antipsikotik ile yeterli antipsikotik koruma sa�lanmadan �izofreninin akut alevlenmelerinde kullan�lmamal�d�r.
�dame dozu
�o�u hasta i�in �nerilen doz iki haftada bir kas i�ine 25 mg'd�r. Baz� hastalar 37,5 mg veya 50 mg �eklinde daha y�ksek dozlardan fayda sa�layabilirler.
Klinik �al��malarda 75 mg ile ek bir yarar g�zlenmemi�tir. 2 haftada bir 50 mg'dan y�ksek dozlar �nerilmez.
Uygulama s�kl��� ve s�resi:
Art�rma y�n�ndeki doz ayarlamalar� 4 haftadan s�k aral�klarla yap�lmamal�d�r. Bu doz ayarlamas�n�n etkisinin, ilk y�ksek doz uygulamas�ndan sonraki 3 haftadan �nce etkili olmas� beklenmemelidir.
Uygulama �ekli:
Daha �nce risperidon kullanmam�� hastalarda, RISPERDAL CONSTA tedavisine ba�lanmadan �nce oral risperidonun tolere edilebilirli�inin tayin edilmesi �nerilir.
RISPERDAL CONSTA uygun emniyetli i�ne kullan�larak, kal�adan (gluteal uygulama) veya omuzdan (deltoid uygulama) derin intram�sk�ler enjeksiyon yolu ile uygulanmal�d�r. Omuzdan enjeksiyon i�in 1-inch'lik i�ne kullan�lmal�d�r ve enjeksiyon omuzlar aras�nda d�n���ml� olarak yap�lmal�d�r. Kal�adan enjeksiyon i�in 2-inch'lik i�ne kullan�lmal�d�r ve enjeksiyon
kal�alar aras�nda d�n���ml� olarak yap�lmal�d�r. �ntraven�z yolla uygulanmamal�d�r (bkz. B�l�m 4.4).
�r�n� uygulamadan �nce rekonstr�ksiyon ile ilgili talimatlar i�in b�l�m 6.6'ya bak�n�z.
�zel pop�lasyonlara ili�kin ek bilgiler B�brek/Karaci�er yetmezli�i:
Karaci�er veya b�brek yetmezli�i bulunan hastalarda RISPERDAL CONSTA kullan�m�na ili�kin bir �al��ma yap�lmam��t�r.
Karaci�er veya b�brek yetmezli�i bulunan hastalar�n RISPERDAL CONSTA ile tedavi edilmeleri gerekirse ilk hafta boyunca g�nde iki defa 0,5 mg oral risperidon ba�lang�� dozu �nerilir. Tedavinin ikinci haftas�nda g�nde iki defa 1 mg ya da g�nde bir defa 2 mg verilebilir. En az 2 mg d�zeyindeki toplam g�nl�k oral doz iyi tolere edilebiliyorsa iki haftada bir 25 mg RISPERDAL CONSTA enjeksiyonu uygulanabilir.
�lk RISPERDAL CONSTA enjeksiyonunu takiben �� haftal�k gecikme s�resi boyunca yeterli antipsikotik koruma sa�lanmal�d�r (bkz. B�l�m 5.2).
Pediyatrik pop�lasyon:
RISPERDAL CONSTA'n�n g�venlili�i ve etkilili�i 18 ya��n alt�ndaki �ocuklarda �al���lmam��t�r. Veri bulunmamaktad�r.
Geriyatrik pop�lasyon:
Doz ayarlamas� gerekmez. �nerilen doz, iki haftada bir kas i�ine 25 mg'd�r.
Hastalar hali haz�rda oral risperidon alm�yorsa, �nerilen doz iki haftada bir 25 mg RISPERDAL CONSTA'd�r. �ki hafta veya daha uzun bir s�redir sabit bir oral risperidon dozu ile tedavi edilen hastalar i�in, a�a��daki d�n���m �emas� dikkate al�nmal�d�r. 4 mg veya daha d���k dozda oral risperidon ile tedavi edilen hastalar 25 mg RISPERDAL CONSTA al�rken, daha y�ksek oral dozlarla tedavi edilen hastalar i�in daha y�ksek olan 37,5 mg RISPERDAL CONSTA dozu d���n�lmelidir.
�lk RISPERDAL CONSTA enjeksiyonunu takiben �� haftal�k bir gecikme s�resi boyunca yeterli antipsikotik koruma sa�lanmal�d�r (bkz. B�l�m 5.2). Ya�l�larda RISPERDAL CONSTA klinik verileri s�n�rl�d�r. RISPERDAL CONSTA ya�l�larda dikkatli kullan�lmal�d�r.
4.3. Kontrendikasyonlar
RISPERDAL CONSTA etkin madde veya B�l�m 6.1'de listelenen yard�mc� maddelerden herhangi birine kar�� a��r� duyarl� oldu�u bilinen hastalarda kontrendikedir.
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Daha �nce risperidon kullanmam�� hastalarda, RISPERDAL CONSTA tedavisine ba�lanmadan �nce oral risperidonun tolere edilebilirli�inin tayin edilmesi �nerilir (bkz. B�l�m 4.2).
Demansl� ya�l� hastalar
Konvansiyonel ve atipik antipisikotik ila�lar demansa ba�l� psikozu olan ya�l� hastalar�n tedavisinde kullan�ld���nda serebrovask�ler olaylar, enfeksiyon, kalp yetmezli�i ile ani �l�m vb. nedenlerle �l�m riskinde art��a neden olmaktad�r.
RISPERDAL CONSTA ile demansl� ya�l� hastalar �zerinde �al��ma yap�lmam��t�r; bu nedenle, bu hasta grubunda kullan�m i�in endike de�ildir. RISPERDAL CONSTA, demansa ba�l� davran��sal bozukluklar�n tedavisi i�in ruhsatland�r�lmam��t�r.
Demansl� ya�l�larda artm�� mortalite
Oral RISPERDAL dahil, atipik antipsikotiklerle y�r�t�len 17 kontroll� ara�t�rman�n meta analizinde, atipik antipsikotiklerle tedavi edilen demansl� ya�l� hastalarda, mortalitede plaseboya k�yasla art�� g�r�lm��t�r. Bu pop�lasyonda oral RISPERDAL ile y�r�t�len plasebo kontroll� ara�t�rmalarda mortalite insidans�, RISPERDAL tedavisindeki hastalarda % 4 iken, plasebo tedavisindeki hastalarda % 3,1 olmu�tur. Olas�l�k oran� (% 95 tam g�ven aral���) 1,21 (0,7-2,1). �len hastalar�n ortalama ya�� 86'yd� (aral�k 67-100). �ki geni� g�zlemsel �al��man�n verileri, konvansiyonel antipsikotiklerle tedavi edilen demansl� ya�l� ki�ilerde de, tedavi g�rmeyenlere k�yasla, �l�m riskinde k���k bir art�� oldu�unu g�stermi�tir. Mevcut veriler, riskin ger�ek boyutunun tam bir �ekilde tahmin edilmesi i�in yetersizdir ve risk art���n�n nedeni
bilinmemektedir. G�zlemsel �al��malardaki mortalite art��� bulgular�n�n hangi oranda antipsikotik ilaca veya hastalar�n sahip olduklar� baz� �zelliklere ba�lanabilece�i a��k de�ildir.
Furosemidle birlikte kullan�m
Demans� olan ya�l� hastalarda oral RISPERDAL ile y�r�t�len plasebo kontroll� �al��malarda, tek ba��na risperidon (% 3,1; ortalama ya� 84 (ya� aral��� 70-96)) veya tek ba��na furosemid alanlara (% 4,1; ortalama ya� 80 (ya� aral��� 67-90)) g�re, furosemid+risperidon ile tedavi edilen hastalarda (% 7,3; ortalama ya� 89 (ya� aral��� 75-97)) daha y�ksek mortalite oranlar� g�zlenmi�tir. Furosemid+risperidon tedavisi ile hastalarda mortalitede art�� 4 klinik �al��man�n 2'sinde g�zlenmi�tir. Risperidonun di�er di�retiklerle birlikte uygulanmas� (esas olarak d���k dozda kullan�lan tiyazid di�retikleri) benzer bulgular ile ili�kili de�ildir.
Bu bulguyu a��klayacak bir patofizyolojik mekanizma tan�mlanamam�� ve �l�m nedeni belli bir sebeple ba�lant�l� bulunmam��t�r. Ancak kullan�m karar�ndan �nce dikkat edilmeli ve bu kombinasyonun veya di�er g��l� di�retiklerle birlikte uygulaman�n risk ve yararlar� de�erlendirilmelidir. Risperidon ile birlikte di�er di�retiklerin kullan�m�nda hastalarda artan mortalite insidans�na rastlanmam��t�r. Tedaviden ba��ms�z olarak dehidratasyon, mortalite i�in genel bir risk fakt�r�d�r ve bu nedenle demans� olan ya�l� hastalarda dikkatle ka��n�lmas� gerekir.
Serebrovask�ler advers olaylar
Demansl� pop�lasyonda, baz� atipik antipsikotiklerle yap�lan randomize plasebo kontroll� klinik �al��malarda serebrovask�ler advers olay riskinde yakla��k 3 kat art�� g�r�lm��t�r. �o�unlukla demansl� ya�l� hastalarda (>65 ya�) RISPERDAL ile alt� plasebo kontroll� �al��madan toplanan veriler, serebrovask�ler advers olaylar�n (ciddi ve ciddi olmayan, birlikte) risperidon ile tedavi edilen hastalar�n % 3,3'�nde (33/1009) ve plasebo ile tedavi edilen hastalar�n % 1,2'sinde (8/712) meydana geldi�ini g�stermi�tir. Olas�l�k oran� (% 95 tam g�ven aral���) 2,96'd�r (1,34; 7,5). Bu artan riske y�nelik mekanizma bilinmemektedir. Di�er antipsikotikler ve di�er hasta pop�lasyonlar�nda artan risk g�z ard� edilemez.
RISPERDAL CONSTA inme i�in risk fakt�r� ta��yan hastalarda dikkatli kullan�lmal�d�r.
Ortostatik hipotansiyon
Risperidonun alfa-adrenerjik resept�rleri bloke etmesine ba�l� olarak �zellikle tedavinin ba�lang�� d�neminde (ortostatik) hipotansiyon g�r�lebilir. Pazarlama sonras�nda risperidon ve antihipertansif tedavinin e�zamanl� kullan�lmas� ile klinik olarak belirgin hipotansiyon g�zlenmi�tir. Risperidon kardiyovask�ler hastal��� (�rne�in, kalp yetmezli�i, miyokard enfarkt�s�, ileti anomalileri, dehidratasyon, hipovolemi veya serebrovask�ler hastal�k) oldu�u bilinen hastalarda dikkatle kullan�lmal�d�r. Klinik a��dan belirgin ortostatik hipotansiyon devaml� olarak g�r�l�rse RISPERDAL CONSTA tedavisinin devam�n�n yarar/risk de�erlendirmesi yap�lmal�d�r.
L�kopeni, n�tropeni ve agran�lositoz
RISPERDAL CONSTA dahil olmak �zere, antipsikotik ajanlarla l�kopeni, n�tropeni ve agran�lositoz olaylar� bildirilmi�tir. Pazarlama sonras� izlemde agran�lositoz �ok nadiren (<1/10.000 hasta) bildirilmi�tir.
Klinik olarak anlaml� d�zeyde d���k beyaz kan h�cresi (WBC) say�m� veya ila�la tetiklenmi� l�kopeni/n�tropeni �yk�s�ne sahip hastalar tedavinin ilk birka� ay� boyunca izlenmeli ve ortada ba�ka nedensel fakt�rler yokken WBC'de klinik olarak anlaml� bir d����e y�nelik ilk belirtide RISPERDAL CONSTA kullan�m�na son verilmesi d���n�lmelidir.
Klinik olarak anlaml� n�tropenisi olan hastalar ate� veya di�er enfeksiyon semptomlar� veya belirtileri a��s�ndan dikkatle izlenmeli ve bu t�r semptomlar veya belirtilerin ortaya ��kmas� halinde derhal tedavi edilmelidir. �iddetli n�tropenisi olan hastalar (mutlak n�trofil say�m� <1 X 109/L) RISPERDAL CONSTA kullan�m�na son vermeli ve hasta iyile�ene kadar WBC d�zeylerini takip ettirmelidir.
Tardif diskinezi/ekstrapiramidal semptomlar (TD/EPS)
Dopamin resept�r antagonisti �zelli�e sahip olan ila�lar, �zellikle dil ve/veya y�zde istemsiz ritmik hareketler ile karakterize tardif diskinezi geli�imi ile ilgili bulunmu�tur. Ekstrapiramidal semptomlar�n g�r�lmesinin tardif diskinezi geli�iminde bir risk fakt�r� oldu�u bildirilmi�tir. Tardif diskinezi bulgu veya semptomlar� g�r�l�rse t�m antipsikotiklerin kesilmesi d���n�lmelidir.
Psikostimulanlarla (�rne�in; metilfenidat) risperidonu birlikte kullanan hastalarda, ila�lardan birini veya her ikisini ayarlarken ekstrapiramidal semptomlar ortaya ��kabilece�i i�in dikkatli olunmal�d�r. Stimulan tedavisinin kademeli olarak kesilmesi �nerilir (bkz. B�l�m 4.5).
N�roleptik malign sendrom (NMS)
Hipertermi, kas rijiditesi, otonom instabilite, bilin� de�i�ikli�i ve serum kreatinin fosfokinaz d�zeyinin y�kselmesi ile karakterize olan N�roleptik Malign Sendromunun, antipsikotiklerin kullan�m�na ba�l� olarak olu�tu�u bildirilmi�tir. �lave belirtiler, miyoglobin�ri (rabdomiyoliz) ve akut b�brek yetmezli�i olabilir. Bu durumda, RISPERDAL CONSTA dahil olmak �zere t�m antipsikotikler kesilmelidir.
Parkinson hastal��� ve Lewy cisimlerinin bulundu�u demans
Parkinson Hastal��� veya Lewy Cisimcikli Demans� (LCD) olan hastalara RISPERDAL dahil antipsikotikler re�ete edilirken, hekimler risk/yarar de�erlendirmesi yapmal�d�r. Parkinson hastal��� risperidon ile k�t�le�ebilir. Her iki grupta da antipsikotik ila�lara duyarl�l�k artabilece�i gibi N�roleptik Malign Sendrom riski de artabilir. Bu hastalar klinik ara�t�rmalar�n d���nda tutulmu�lard�r. Bu artan duyarl�l���n semptomlar� aras�nda, ekstrapiramidal semptomlara ek olarak, konf�zyon, obtundasyon ve s�k d��melerin oldu�u postural instabilite bulunabilir.
A��r� duyarl�l�k reaksiyonlar�
RISPERDAL CONSTA ile tedaviye ba�lamadan �nce oral risperidon ile tolere edilebilirlik belirlenmesine ra�men, pazarlama sonras� deneyimlerde �nceden oral risperidonu tolere etmi� hastalarda nadiren anafilaktik reaksiyon meydana geldi�i rapor edilmi�tir (bkz. b�l�m 4.2 ve B�l�m 4.8).
E�er hipersensitive reaksiyonlar� meydana gelirse, RISPERDAL CONSTA kullanmaya devam etmeyiniz, klinik olarak uygun genel destekleyici tedbirleri ba�lat�n�z ve belirtiler ve semptomlar ortadan kalk�ncaya kadar hastay� g�zlemleyiniz (bkz. B�l�m 4.3. ve B�l�m 4.8).
Hiperglisemi ve diabetes mellitus
RISPERDAL CONSTA tedavisi s�ras�nda hiperglisemi, diabetes mellitus ve �nceden var olan diyabetin alevlendi�i bildirilmi�tir.
Baz� olgularda, v�cut a��rl���nda �nceden meydana gelen art���n yatk�nl�k kazand�r�c�/zemin haz�rlayan bir etmen olabilece�i bildirilmi�tir. Ketoasidoz ile ili�ki �ok nadir olarak ve diyabetik koma ile ili�ki nadir olarak rapor edilmi�tir. Uygun klinik izlem, kullan�lan antipsikotik k�lavuz kurallar�na uygun olarak tavsiye edilebilir. RISPERDAL dahil olmak �zere herhangi bir atipik antipsikotik ile tedavi edilen hastalarda hiperglisemi semptomlar� (�rne�in, polidipsi, poli�ri, polifaji ve halsizlik gibi) izlenmelidir ve diyabet hastalar� glukoz kontrol�n�n k�t�le�mesi a��s�ndan d�zenli olarak takip edilmelidir.
Kilo al�m�
RISPERDAL CONSTA kullan�m�nda anlaml� kilo al�m� bildirilmi�tir. V�cut a��rl��� d�zenli olarak izlenmelidir.
Hiperprolaktinemi
Hiperprolaktinemi, R�SPERDAL CONSTA tedavisinde g�r�len yayg�n bir yan etkidir. Prolaktin ili�kili yan etki belirtilerinin (�rne�in; jinekomasti, menstrual d�zensizlikler, anov�lasyon, fertilite bozukluklar�, libido kayb�, erektil disfonksiyon ve galaktore) g�r�ld��� hastalarda prolaktin plazma seviyelerinin de�erlendirilmesi tavsiye edilmektedir.
Doku k�lt�r� �al��malar�, insan meme t�m�rlerinde h�cre b�y�mesinin prolaktin taraf�ndan stimule edilebilece�ini belirtmektedir. Klinik ve epidemiyolojik �al��malarda antipsikotik kullan�m� ile ili�kisi a��k bir �ekilde g�sterilememi� olsa da, ilgili t�bbi �yk�s� olan hastalarda dikkatli olunmas� �nerilmektedir. RISPERDAL CONSTA daha �nceden hiperprolaktinemisi ve olas� bir prolaktine ba�l� t�m�r� olan hastalarda dikkatli kullan�lmal�d�r.
QT uzamas�
QT aral��� uzamas�, pazarlama sonras�nda �ok seyrek rapor edilmi�tir. Di�er antipsikotikler ile oldu�u gibi, RISPERDAL CONSTA, aritmojenik etkiyi artt�rabilece�inden kardiyovask�ler hastal��� olan ki�ilerde, aile �yk�s�nde QT uzamas�, bradikardi veya elektrolit d�zensizli�i olan hastalarda (hipokalemi, hipomagnezemi) ve QT aral���n� uzatt��� bilinen ila�lar ile birlikte
kullan�l�rken dikkatli olunmal�d�r. Uzam�� QT Sendromu / Torsades de Pointes'e neden olabilece�inden, tan�s� konmu� veya ��pheli konjenital uzam�� QT sendromu veya Torsades de Pointes hastalar�nda R�SPERDAL CONSTA kullan�lmamal�d�r.
N�betler
RISPERDAL CONSTA, n�bet e�i�ini potansiyel olarak d���ren durumlarda veya n�bet hikayesi olan hastalarda dikkatli kullan�lmal�d�r.
Priapizm
Alfa-adrenerjik blok�r �zelli�inden dolay� RISPERDAL CONSTA ile tedavi s�ras�nda priapizm g�r�lebilir.
V�cut s�cakl���n�n d�zenlenmesi
V�cudun v�cut s�cakl���n� d���rme yetene�inin bozulmas� antipsikotik ila�larla ili�kilendirilmi�tir. A��r egzersiz, a��r� s�ca�a maruz kalma, e� zamanl� antikolinerjik ila�larla tedavi g�rme veya dehidratasyona u�rama gibi v�cut �s�s�n�n artmas�na katk�da bulunabilecek durumlar�n g�r�lebilece�i hastalarda RISPERDAL CONSTA re�ete edilirken, uygun koruma �nlemleri al�nmal�d�r.
Ven�z tromboembolik olay
Antipsikotik ila�larla ven�z tromboembolizm (VTE) vakalar� bildirilmi�tir. Antipsikotik ila� tedavisi g�ren hastalarda �o�unlukla kazan�lm�� VTE risk fakt�rleri bulundu�u i�in, VTE i�in t�m olas� risk fakt�rleri, RISPERDAL CONSTA ile tedaviden �nce ve tedavi s�ras�nda tan�mlanmal� ve koruyucu �nlemler al�nmal�d�r.
Intraoperatif Gev�ek �ris Sendromu
Katarakta ameliyat� s�ras�nda RISPERDAL CONSTA dahil alfa 1a adrenerjik antagonist etki g�steren ila�lar� kullanan hastalarda Intraoperatif Gev�ek �ris Sendromu (IFIS) g�zlenmi�tir. IFIS, ameliyat s�ras�nda ve sonras�nda g�z komplikasyonlar� riskini artt�rabilir (bkz B�l�m 4.8).
Ameliyat �ncesinde hastan�n alfa 1a adrenerjik antagonist ila�lar� ge�mi�te kullanm�� veya halen kullanmakta oldu�u g�z cerrah�na mutlaka iletilmelidir.
Katarakt ameliyat� �ncesinde alfa 1 blok�r tedavisinin kesilmesinin potansiyel faydas� kan�tlanmam��t�r ve antipsikotik tedavinin kesilmesinin olu�turabilece�i risk g�z �n�nde bulundurulmal�d�r.
Antiemetik etki
Risperidon ile yap�lan klinik �ncesi �al��malarda antiemetik etki g�zlenmi�tir. Bu etki, e�er insanlarda olu�ursa, ba��rsak t�kanmas�, Reye sendromu ve beyin t�m�r� gibi durumlar� veya belli ila�lar�n a��r� doz bulgu ve semptomlar�n� maskeleyebilir.
Uyku apnesi sendromu
RISPERDAL CONSTA kullanan hastalarda uyku apnesi sendromu rapor edilmi�tir. E� zamanl� olarak santral sinir sistemi depresan� kullanan hastalar ile uyku apnesi �yk�s� olan ya da uyku apnesi riski ta��yan (�rne�in; a��r� kilolu/obezler veya erkekler) hastalarda RISPERDAL CONSTA kullan�l�rken dikkatli olunmal�d�r.
B�brek veya karaci�er yetmezli�i
Oral risperidon �al���lm�� olmakla birlikte, RISPERDAL CONSTA b�brek veya karaci�er yetmezli�i olan hastalarda �al���lmam��t�r. Bu hastalarda RISPERDAL CONSTA kullan�rken dikkatli olunmal�d�r (bkz. B�l�m 4.2).
Uygulama
RISPERDAL CONSTA'n�n kaza ile kan damarlar� i�ine uygulanmas�ndan ka��n�lmas�na dikkat edilmelidir.
Yard�mc� maddeler
Bu t�bbi �r�n, doz ba��na 1 mmol (23 mg)'dan daha d���k sodyum i�ermektedir, yani esas�nda “sodyum i�ermez” olarak kabul edilebilir.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
RISPERDAL CONSTA'n�n di�er ila�larla birlikte kullan�m�n�n etkile�imleri sistematik olarak de�erlendirilmemi�tir. Bu b�l�mde sa�lanan ila� etkile�imi verileri oral R�SPERDAL ile yap�lan �al��malara dayanmaktad�r.
Farmakodinamik etkile�imler
QT aral���n� uzatt��� bilinen ila�lar
Di�er antipsikotiklerde oldu�u gibi, antiaritmikler (�rne�in; kinidin, dizopiramid, prokainamid, propafenon, amiyodaron, sotalol), trisiklik antidepresanlar (�rne�in; amitiriptilin), tetrasiklik antidepresanlar (�rne�in; maprotilin), baz� antihistaminikler, di�er antipsikotikler, baz� antimalaryal ila�lar (�rne�in; kinidin ve meflokin) gibi QT aral���n� uzatt��� bilinen ila�lar ile birlikte risperidon re�ete edilirken dikkatli olunmal�d�r. Ayn� �ekilde elektrolit dengesizli�i (hipokalemi, hipomagnezemi) ve bradikardiye yol a�abilen ya da risperidonun hepatik metabolizmas�n� inhibe eden ila�larla birlikte re�ete edilirken dikkatli olunmal�d�r. Bu liste bilgi vericidir, kapsaml� de�ildir.
Merkezi sinir sistemini etkileyen ila�lar ve alkol
Risperidon, alkol, opiyatlar, antihistaminikler ve benzodiazepinleri de i�eren di�er merkezi sinir sistemini etkileyen maddelerle kombinasyon halinde kullan�l�rken sedasyon riskinin artmas�na kar�� dikkatli olunmal�d�r.
Levodopa ve dopamin agonistleri
RISPERDAL CONSTA, levodopa ve di�er dopamin agonistlerinin etkilerini antagonize edebilir. E�er bu kombinasyon �zellikle Parkinson hastal���n�n son a�amas�nda gerekli g�r�l�rse, her tedavinin en d���k etkili dozu re�ete edilmelidir.
Hipotansif etkili ila�lar
Pazarlama sonras�nda risperidon ve antihipertansif tedavinin e�zamanl� kullan�lmas� ile klinik olarak belirgin hipotansiyon g�zlenmi�tir.
Psikostimulanlar
Psikostimulanlar�n (�rne�in; metilfenidat) risperidon ile birlikte kullan�m�, tedavinin birinde ya da her ikisinde de�i�iklik yap�ld���nda ekstrapiramidal semptomlara yol a�abilir (bkz. b�l�m 4.4).
Farmakokinetik etkile�imler
Risperidon, temel olarak CYP2D6 ile ve daha az olarak CYP3A4 ile metabolize edilir. Risperidon ve etkin metaboliti olan 9-hidroksirisperidon, P-glikoprotein (P-gp) substratlar�d�r. CYP2D6 aktivitesini de�i�tiren maddeler veya CYP3A4 ve/veya P-gp aktivitesini g��l� olarak inhibe eden veya ind�kleyen maddeler, risperidon etkin antipsikotik fraksiyonunun farmakokinetiklerini etkileyebilir.
G��l� CYP2D6 inhibit�rleri
RISPERDAL CONSTA'n�n g��l� bir CYP2D6 inhibit�r� ile birlikte uygulanmas�, risperidonun plazma konsantrasyonlar�n� art�rabilir, ancak etkin antipsikotik fraksiyonun plazma konsantrasyonlar�n� daha az art�r�r. G��l� CYP2D6 inhibit�r�n�n y�ksek dozlar�, risperidon etkin antipsikotik fraksiyonunun (�rne�in; paroksetin, a�a�� bak�n�z) konsantrasyonlar�n� art�rabilir. Kinidin gibi ba�ka CYP2D6 inhibit�rlerinin, risperidon plazma konsantrasyonlar�n� benzer �ekilde etkileyebilecekleri beklenmektedir. �zellikle y�ksek dozlarda olmak �zere paroksetin, kinidin veya ba�ka bir g��l� CYP2D6 inhibit�r� ile birlikte uygulama ba�lat�ld���nda veya kesildi�inde, hekim RISPERDAL CONSTA'n�n dozlamas�n� tekrar de�erlendirmelidir.
CYP3A4 ve/veya P-gp inhibit�rleri
RISPERDAL CONSTA'n�n g��l� bir CYP3A4 ve/veya P-gp inhibit�r� ile birlikte uygulanmas�, risperidon etkin antipsikotik fraksiyonunun plazma konsantrasyonunu �nemli �l��de art�rabilir. �trakonazol veya ba�ka bir g��l� CYP3A4 ve/veya P-gp inhibit�r� ile birlikte
uygulama ba�lat�ld���nda veya kesildi�inde, hekim RISPERDAL CONSTA'n�n dozlamas�n� tekrar de�erlendirmelidir.
CYP3A4 ve/veya P-gp ind�kleyicileri
RISPERSAL CONSTA'n�n g��l� bir CYP3A4 ve/veya P-gp ind�kleyicisi ile birlikte uygulanmas�, risperidon etkin antipsikotik fraksiyonunun plazma konsantrasyonlar�n� d���rebilir. Birlikte karbamazepin veya ba�ka bir g��l� CYP3A4 ve/veya P-gp ind�kleyicileri ba�lat�ld���nda veya kesildi�inde, RISPERDAL CONSTA dozu hekim taraf�ndan tekrar de�erlendirilmelidir. CYP3A4 ind�kleyicileri etkilerini zamana ba�l� bir �ekilde g�sterir ve ba�lama sonras�nda maksimal etkiye ula��lmas� en az 2 hafta s�rebilir. Di�er taraftan, kesilmesi durumunda, CYP3A4 ind�ksiyonunda azalma en az 2 hafta s�rebilir.
Proteine y�ksek oranda ba�lanan ila�lar
RISPERDAL CONSTA, proteine y�ksek oranda ba�lanan ila�larla birlikte al�nd���nda, her iki ilac�n da plazma proteinlerinden klinik olarak anlaml� oranda ayr�lmas� s�z konusu de�ildir.
�la�lar�n birlikte kullan�m�nda, metabolizma yoluna veya muhtemel dozaj ayarlama ihtiyac�na ili�kin bilgiler i�in ilgili �r�n bilgisine bak�lmal�d�r.
�rnekler
Potansiyel olarak etkile�ime giren veya risperidonla etkile�ime girmedi�i g�sterilen ila� �rnekleri a�a��da listelenmi�tir:
Di�er T�bbi �r�nlerin Risperidonun Farmakokineti�i �zerindeki Etkisi
Antibakteriyel �la�lar:
Orta dereceli bir CYP3A4 ve P-gp inhibit�r� olan eritromisin, risperidon ve aktif antipsikotik fraksiyonunun farmakokineti�ini de�i�tirmez.
4.6. Gebelik ve laktasyon
Gebelik kategorisi C
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
RISPERDAL CONSTA'n�n �ocuk do�urma potansiyeli bulunan kad�nlarda kontrasepsiyon gereklili�ine i�aret edecek yeterli bilgi mevcut de�ildir.
Gebelik d�nemi
Risperidonun gebe kad�nlarda kullan�m� ile ilgili yeterli veri bulunmamaktad�r. Hayvan �al��malar�nda risperidonun teratojenik etkisine rastlanmam��; fakat di�er �reme toksisitesi tipleri g�r�lm��t�r (bkz. B�l�m 5.3). �nsanlara y�nelik potansiyel risk bilinmemektedir.
Gebeli�in ���nc� trimesterinde antipsikotik ila�lara (RISPERDAL CONSTA da dahil) maruz kalan yeni do�anlar, do�umu takiben �iddeti ve s�resi de�i�ebilen, ekstrapiramidal ve/veya ila� kesilme semptomlar�n� i�eren advers etkiler a��s�ndan risk alt�ndad�rlar. Bu semptomlar, ajitasyon, hipertoni, hipotoni, tremor, somnolans, respiratuar distres veya beslenme
bozukluklar�n� i�ermektedir. Yeni do�anlar dikkatle izlenmelidir. RISPERDAL CONSTA kesinlikle gerekli olmad�k�a gebelik s�ras�nda kullan�lmamal�d�r.
Laktasyon d�nemi
Hayvan �al��malar�nda, risperidon ve 9-hidroksi-risperidon s�t ile at�lmaktad�r. Risperidon ve 9-hidroksi-risperidonun az miktarlarda anne s�t�ne de ge�ti�i kan�tlanm��t�r. Emzirilen bebeklerdeki advers reaksiyonlar ile ilgili herhangi bir veri mevcut de�ildir. Bu nedenle, emzirmenin �ocuk a��s�ndan faydas�, �ocu�un kar��la�aca�� potansiyel risklere kar�� de�erlendirilmelidir.
�reme yetene�i/Fertilite
Dopamin D2 resept�rlerini antagonize eden di�er ila�larda oldu�u gibi, RISPERDAL CONSTA prolaktin d�zeyini y�kseltir. Hiperprolaktinemi, hipotalamik GnRH'� bask�layabilir ve pit�iter gonadotropin salg�lanmas�nda azalmaya yol a�abilir. Bu durum daha sonra, hem kad�n hem de erkek hastalarda, gonadal steroidogenezi bozarak, reprod�ktif fonksiyonu inhibe edebilir.
Klinik d��� �al��malarda konuya ili�kin etkiler g�zlenmemi�tir.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
RISPERDAL CONSTA, sinir sistemi ve g�rme duyusuna ili�kin potansiyel etkileri nedeniyle (bkz. B�l�m 4.8), ara� ve makine kullanma becerileri �zerinde min�r ya da orta derecede etki g�sterir. Bu nedenle hastalar�n, bireysel duyarl�l�klar� anla��l�ncaya kadar, ara� ve makine kullanmalar� �nerilmez.
4.8. �stenmeyen etkiler
En s�k bildirilen advers ila� reaksiyonlar� (insidans ≥1/10); insomnia, anksiyete, ba� a�r�s�, �st solunum yolu enfeksiyonu, parkinsonizm ve depresyon olmu�tur.
Doza ba�l� olduklar� g�r�len advers ila� reaksiyonlar�, parkinsonizm ve akatizidir.
Pazarlama sonras� d�nemde, enjeksiyon b�lgesinde nekroz, apse, sel�lit, �lser, hematom, kist ve nod�l gibi ciddi enjeksiyon b�lgesi reaksiyonlar� bildirilmi�tir. Bunlar�n s�kl�k dereceleri bilinmemektedir. �ok az say�daki olguda cerrahi giri�im gerekli olmu�tur.
A�a��da verilen listede, risperidon klinik ara�t�rmalar�nda ve pazarlama sonras� d�nemde bildirilen b�t�n advers ila� reaksiyonlar�, RISPERDAL CONSTA klinik ara�t�rmalar�nda yap�lan tahminler do�rultusundaki s�kl�k gruplar�yla verilmektedir. A�a��daki terimler ve s�kl�klar kullan�lm��t�r: �ok yayg�n (≥1/10); yayg�n (≥1/100 ila <1/10); yayg�n olmayan (≥1/1000 ila <1/100); seyrek (≥1/10.000 ila <1/1000); �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Sistem Organ S�n�f� | Advers �la� Reaksiyonlar� | |||||
S�kl�k | ||||||
�ok yayg�n |
Yayg�n |
Yayg�n Olmayan |
Seyrek | �ok Seyrek |
Bilinmiyor | |
Enfeksiyonlar ve enfestasyonlar | �st solunum yolu enfeksiyonu | Pn�moni, bron�it, sin�zit, idrar yolu enfeksiyonu, grip | Solunum sistemi enfeksiyonu, sistit, kulak enfeksiyonu, g�z enfeksiyonu, tonsillit, onikomikoz, sel�lit, enfeksiyon, lokalize enfeksiyon, viral enfeksiyon, akarodermatit, subkutan apse |
|
|
|
Kan ve lenf sistemi hastal�klar� |
| Anemi | Beyaz kan h�cresi say�s�nda azalma, trombositopeni, hematokrit de�erinde (k�rm�z� kan h�crelerinin plazmadan ayr�lm�� k�sm�) azalma | Agranulasitoz n�tropeni, eozinofil say�s�nda art�� |
|
|
Ba����kl�k sistemi hastal�klar� |
|
| A��r� duyarl�l�k | Anafilaktik reaksiyon |
|
|
Endokrin hastal�klar� |
| Hiperprolakti- nemi | �drarda glukoz bulunmas� | Uygun olmayan antidi�retik hormon salg�lama |
|
|
Metabolizma ve beslenme hastal�klar� |
| Hiperglisemi, kilo al�m�, kilo kayb� ,i�tah art���, i�tah azalmas� | Diyabetes mellitus, anoreksi, kan kolesterol d�zeyinde y�kselme, kan trigliserit d�zeyinde y�kselme | Su intoksikasyonu, hipoglisemi, hiperins�linemi, polidipsi | Diyabetik ketoasidoz |
|
Psikiyatrik hastal�klar | �nsomnia , depresyon, anksiyete | Uyku bozukluklar�, ajitasyon, libido azalmas� | Mani, kabus, konf�zyonal durum, sinirlilik, anorgazmi | Katatoni, k�nt duygulan�m, somnambulizm, uyku ile ili�kili yeme bozuklu�u |
|
|
Sinir sistemi hastal�klar� | Ba� a�r�s�, parkinsonizm | Somnolans/se- dasyon akatizi, distoni, diskinezi, tremor, sersemlik | Tardif diskinezi, serebral iskemi, bilin� kayb�, konv�lsiyon, senkop, psikomotor hiperaktivite, denge bozuklu�u, anormal koordinasyon, postural sersemlik, dikkat bozuklu�u, disartri, tat alma duyusunda bozulma, hipoestezi, parestezi | N�roleptik malign sendrom, serebrovask�ler bozukluk, uyaranlara yan�t vermeme, depresif bilin� durumu, diyabetik koma, ba�ta titreme |
|
|
G�z hastal�klar� |
| Bulan�k g�rme | Konjunktivit, g�z kurulu�u, g�z ya�armas�nda artma, ok�ler hiperemi | Retinal arter t�kanmas�, glokom, g�z hareket bozuklu�u, g�z k�resinin hareketlili�i, fotofobi , g�zkapa�� kenar�nda kabuklanma fotofobi, intraoperatif floppy iris sendromu (IFIS) |
|
|
Kulak ve i� kulak hastal�klar� |
|
| Vertigo, kulak ��nlamas�, kulak a�r�s� |
|
|
|
Kardiyak hastal�klar |
| Ta�ikardi | Atriyal fibrilasyon, atrioventrik�ler blok, iletim bozuklu�u, elektrokardiyogram da QT uzamas�, bradikardi, normal olmayan elektrokardiyogram, palpitasyonlar | Sin�s aritmisi |
|
|
Vask�ler hastal�klar |
| Hipertansiyon, hipotansiyon | Ortostatik hipotansiyon | Akci�er embolisi, ven�z tromboz, k�zarma |
|
|
Solunum, g���s bozukluklar� ve mediastinal hastal�klar |
| Dispne, faringolaringe- al a�r�, �ks�r�k, burun t�kan�kl��� | Hiperventilasyon, solunum yolu t�kan�kl���, h�r�lt�l� solunum, burun kanamas� | Uyku apnesi sendromu, aspirasyon, pn�monisi, pulmoner t�kan�kl�k, raller, disfoni, solunum bozuklu�u |
|
|
Gastro- intestinal hastal�klar |
| Abdominal a�r�, kusma, abdominal rahats�zl�k, diyare, bulant�, konstipasyon, gastroenterit, di� a�r�s�, dispepsi, a��z kurulu�u | Gaita ka��rma, disfaji, midede veya ba��rsakta gaz birikimi | Pankreatit, ba��rsak t�kan�kl���, dudak iltihab� (�ilit), �i�mi� dil, fekalom | �leus |
|
Hepato-bilier hastal�klar |
| Transaminaz- larda art���, gama- glutamiltrans- ferazlarda art��� | Hepatik enzim art��� | Sar�l�k |
|
|
Deri ve deri alt� doku hastal�klar� |
| D�k�nt� |
Ka��nt�, alopesi, egzama, kuru cilt, eritem, deride renk de�i�ikli�i, akne, seboreik dermatit | �la� d�k�nt�s�, kepek, �rtiker, hiperkeratozis, cilt rahats�zl���, cilt lezyonu | Anjiyo�- dem | Stevens- Johnson sendromu/ toksik epidermal nekroliz |
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar� |
| Kas spazmlar�, kas-iskelet a�r�s�, s�rt a�r�s�, artralji | Kan kreatin fosfokinaz d�zeyinde art��, eklem sertli�i, eklem �i�li�i, kas | Rabdomiyoliz, duru� anormalli�i |
|
|
|
|
| zay�fl���, boyun a�r�s� |
|
|
|
B�brek ve idrar yolu hastal�klar� |
| �drar tutamama | Pollak�ri, idrar retansiyonu, diz�ri |
|
|
|
Gebelik, puerperiyum durumlar� ve perinatal hastal�klar� |
|
|
| Yenido�anda ila� yoksunluk sendromu |
|
|
�reme sistemi ve meme hastal�klar� |
| Erektil disfonksiyon, amenore, galaktore | Bo�alma bozuklu�u, menstr�asyonda gecikme, menstr�el bozukluk, jinekomasti, seks�el disfonksiyon, meme a�r�s�, meme rahats�zl���, vajinal ak�nt� | Priapizm, meme dolgunlu�u, meme ak�nt�s�, meme b�y�mesi |
|
|
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar |
| �dem y�ksek ate�, g���s a�r�s�, asteni, yorgunluk, a�r�, enjeksiyon b�lgesinde reaksiyon | Y�zde �dem, titreme, v�cut s�cakl���nda art��, anormal y�r�y�� bi�imi, susama, g���ste rahats�zl�k hissi, keyifsizlik, anormal hissetme, endurasyon | Hipotermi, v�cut s�cakl���nda azalma, periferik so�ukluk, ila� yoksunluk sendromu, rahats�zl�k |
|
|
Yaralanma, zehirlenme ve enjeksiyon s�ras�nda komplikas- yonlar |
| D��me | Enjeksiyon s�ras�nda a�r� |
|
|
|
a Hiperprolaktinemi baz� olgularda jinekomasti, menstr�el bozukluklar, amenore, anov�lasyon, fertilite bozukluklar�, libido kayb� ve erektil disfonksiyon ve galaktoreye yol a�abilir.
b Plasebo kontroll� ara�t�rmalarda, diabetes mellitus risperidon ile tedavi edilen hastalarda % 0,18 oran�nda, plasebo grubunda ise % 0,11 oran�nda bildirilmi�tir. T�m klinik ara�t�rmalardaki genel insidans�, risperidon tedavisi g�ren t�m hastalarda % 0,43 olmu�tur.
c RISPERDAL CONSTA klinik �al��malar�nda g�zlenmemi�, ama risperidon ile pazarlama sonras� d�nemde g�zlenmi�tir.
d Ekstrapiramidal bozukluk ortaya ��kabilir: Parkinsonizm (t�k�r�k salg�s�nda art��, kas- iskelet kat�l���, parkinsonizm, a��zda sulanma, di�li �ark rijiditesi, bradikinezi, hipokinezi, maske y�z, kaslarda gerginlik, akinezi, ense sertli�i, kaslarda sertlik, parkinsoniyen ad�m, anormal glabella refleksi, parkinsoniyen dinlenme tremoru), akatizi (akatizi, huzursuzluk, hiperkinezi ve huzursuz bacak sendromu), tremor, diskinezi (diskinezi, kaslarda se�irme, koreatetozis, atetozis ve miyoklonus), distoni. Distoni �unlar� kapsamaktad�r; distoni, hipertoni, tortikollis, istemsiz kas kas�lmalar�, kas kas�lmas�, blefarospazm, okulogirasyon, dilde paralizi, fasyal spazm, laringospazm, miyotoni, opistotonus, orofaringeal spazm, pl�rototonus, dilde spazm ve trismus. Mutlaka ekstrapiramidal orijine sahip olmas� gerekmeyen, daha geni� bir semptom spektrumunun verildi�ine dikkat edilmelidir. �nsomnia �unlar� i�erir; ba�lang��ta g�zlenen uykusuzluk, orta d�nem uykusuzlu�u. Konv�lsiyon �unlar� i�erir; grand-mal konv�lsiyon. Menstr�el bozukluk �unlar� i�erir; d�zensiz menstr�asyon, oligomenore. �dem �unlar� i�erir; yayg�n �dem, periferik �dem, gode b�rakan �dem.
Paliperidon form�lasyonlar�yla kaydedilen istenmeyen etkiler
Paliperidon, risperidonun aktif metabolitidir. Bu nedenle, bu bile�enlerin advers reaksiyon profilleri (hem oral hem de enjektabl form�lasyonlar dahil) birbirleri i�in ge�erlidir. Yukar�daki advers reaksiyonlara ek olarak, paliperidon �r�nleriyle a�a��daki advers reaksiyon kaydedilmi�tir ve RISPERDAL CONSTA ile de meydana gelmesi beklenebilir:
Kardiyak hastal�klar
Post�ral ortostatik ta�ikardi sendromu Anaflaktik reaksiyon
Pazarlama sonras� deneyimde, �nceden oral risperidonu tolere etmi� hastalarda ender olarak, RISPERDAL CONSTA enjeksiyonundan sonra anafilaktik reaksiyon olgular� bildirilmi�tir (bkz; b�l�m 4.4).
S�n�f etkileri
Di�er antipsikotiklerde oldu�u gibi, risperidon ile pazarlama sonras� d�nemde �ok ender olarak QT uzamas� olgular� bildirilmi�tir. QT aral���n� uzatan antipsikotikler ile bildirilen s�n�fla ili�kili di�er kardiyak etkiler ventrik�ler aritmi, ventrik�ler fibrilasyon, ventrik�ler ta�ikardi, ani �l�m, kardiyak arrest ve Torsades de Pointes'dir.
Ven�z tromboembolizm
Antipsikotik ila�larla ven�z tromboembolizm olgular� (pulmoner embolizm dahil) ve derin ven trombozu olgular� bildirilmi�tir (s�kl�k bilinmemektedir).
Kilo art���
On iki haftal�k �ift k�r, plasebo kontroll� �al��mada, RISPERDAL CONSTA kullanan hastalar�n % 9'u, plasebo ile tedavi edilen hastalar�n % 6's� ile kar��la�t�r�ld���nda, sonlan�m noktas�nda v�cut a��rl���n�n ≥ % 7'lik bir a��rl�k art��� g�r�lm��t�r. Bir y�l s�reli a��k etiketli RISPERDAL CONSTA �al��mas�nda, hasta bireylerdeki v�cut a��rl��� de�i�imleri, genellikle ba�lang�� d�neminin ± % 7 s�n�rlar� aras�ndayd�; hastalar�n % 25'inde v�cut a��rl���nda ≥ % 7'lik bir art�� g�r�ld�.
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr, e-posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99)
4.9. Doz a��m� ve tedavisi
Parenteral uygulama ile doz a��m� g�r�lme olas�l��� oral uygulamaya g�re daha d���k oldu�undan, oral uygulamaya ili�kin bilgiler sunulmu�tur.
Belirtiler
Genellikle, bildirilen bulgu ve belirtiler ilac�n bilinen farmakolojik etkilerinin artmas� �eklindedir. Bunlar, sersemlik ile sedasyon, ta�ikardi ile hipotansiyon ve ekstrapiramidal semptomlard�r. Doz a��m�nda QT uzamas� ve konv�lsiyonlar bildirilmi�tir. Oral RISPERDAL ve paroksetinin birlikte kullan�m�ndaki doz a��m� ile ili�kili olarak Torsades de Pointes bildirilmi�tir.
Akut doz a��m� durumlar�nda birden fazla ila� ihtimali d���n�lmelidir.
Tedavi
Solunum yolu a��lmal� ve a��k tutulmal�, yeterli oksijenlenme ve ventilasyon sa�lanmal�d�r. Hemen kardiyovask�ler izleme ba�lat�lmal� ve s�rekli elektrokardiyografi ile muhtemel aritmiler takip edilmelidir.
RISPERDAL'e �zg� bir antidot yoktur. Bu y�zden uygun destekleyici �nlemler al�nmal�d�r. Hipotansiyon ve dola��m kollaps�, intraven�z s�v� ve/veya sempatomimetiklerle gerekti�i gibi tedavi edilmelidir. �iddetli ekstrapiramidal belirtilerde antikolinerjik tedavi uygulanmal�d�r. Hasta durumu d�zelinceye kadar yak�n t�bbi g�zlem alt�nda tutulmal� ve izlenmelidir.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik Grup: Di�er antipsikotikler ATC Kodu: N05AX08Etki mekanizmas�
Risperidon benzersiz �zellikleri olan se�ici bir monoaminerjik antagonisttir. Serotonin 5-HTve dopamin Dresept�rlerine y�ksek oranda ba�lan�r. Alfa-adrenerjik resept�rlere, daha az oranda H-histamin resept�rlerine ve alfa-adrenerjik resept�rlere de ba�lan�r. Risperidonun kolinerjik resept�rlere afinitesi yoktur. Risperidon, g��l� bir dopamin Dresept�r� antagonisti olarak, �izofrenideki pozitif semptomlar� d�zeltir. Motor aktivitede depresyona ve katalepsi olu�umuna klasik n�roleptiklerden daha az neden olur. Dengeli bir santral serotonin ve dopamin resept�rleri antagonizmas�, ekstrapiramidal yan etkileri azaltabilir ve tedavinin etkilili�ini �izofreninin negatif ve pozitif semptomlar�na yayabilir.
Klinik etkinlik
RISPERDAL CONSTA'n�n (25 mg ve 50 mg), psikotik bozukluk (�izofreni/�izoafektif bozukluk) belirtilerinin kontrol alt�na al�nmas�ndaki etkilili�i, �izofreni i�in DSM-IV kriterlerine uyan yeti�kin psikotik hastalarda (yatan ve ayakta tedavi g�ren), 12 haftal�k, plasebo kontroll� bir �al��ma ile ispatlanm��t�r.
Stabil �izofreni hastalar� �zerinde yap�lan 12 haftal�k kar��la�t�rmal� bir �al��mada, RISPERDAL CONSTA'n�n oral tablet form�lasyonu kadar etkili oldu�u g�sterilmi�tir. Ayr�ca a��k etiketli bir �al��mada, RISPERDAL CONSTA'n�n uzun-d�nem (50 hafta) g�venlilik ve etkilili�i, �izofreni veya �izoafektif bozukluk i�in DSM-IV kriterlerine uyan stabil psikotik
![]()
![]()
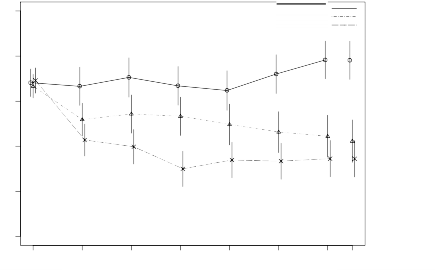
hastalar (yatan ve ayakta tedavi g�ren) �zerinde de�erlendirilmi�tir. Bu zaman i�erisinde RISPERDAL CONSTA ile etkililik kal�c� olmu�tur (�ekil 1).
�ekil 1. �izofreni hastalar�nda zaman i�inde toplam PANSS skoru ortalamas� (LOCF).
5.2. Farmakokinetik �zellikler
Genel �zelliklerEmilim:
RISPERDAL CONSTA'dan risperidonun emilimi tamd�r.
Tek intramusk�ler RISPERDAL CONSTA enjeksiyonundan sonra sal�n�m profili ��yledir: Ba�lang��ta az miktarda risperidon (dozun < % 1'i) sal�verilir ve bunu 3 haftal�k bir gecikme s�resi izler. Risperidonun as�l sal�n�m� 3. haftadan sonra ba�lar, 4. haftadan 6. haftaya kadar devam eder ve 7. haftada azal�r. Bu nedenle RISPERDAL CONSTA tedavisinin ilk 3 haftas� s�resince oral antipsikotik deste�i sa�lanmal�d�r (bkz. B�l�m 4.2).
Sal�n�m profili ve doz uygulama rejiminin kombinasyonu (her iki haftada bir intramusk�ler enjeksiyon), kal�c� terap�tik plazma konsantrasyonlar�yla sonu�lan�r. Terap�tik plazma konsantrasyonlar�, son RISPERDAL CONSTA enjeksiyonundan 4 ile 6 hafta sonras�na kadar devam eder.
25 ya da 50 mg RISPERDAL CONSTA ile iki haftada bir tekrarl� intramusk�ler enjeksiyonlardan sonra, aktif antipsikotik fraksiyonun medyan �ukur ve doruk
konsantrasyonlar�, s�ras�yla 9,9-19,2 ng/ml ve 17,9-45,5 ng/ml aras�nda dalgalanma g�sterir. �ki haftada bir 25-50 mg enjekte edilen hastalarda uzun d�nemli (12 ay) kullan�m s�ras�nda risperidon birikimi g�zlenmemi�tir.
Yukar�daki �al��malar kal�aya intramusk�ler enjeksiyon ile yap�lm��t�r. Ayn� dozlardaki intramusk�ler omuz ve kal�a enjeksiyonlar� biyoe�de�erdir ve b�ylelikle birbirlerinin yerine kullan�labilir niteliktedirler.
Da��l�m:
Risperidon h�zla da��l�r. Da��l�m hacmi 1-2 L/kg'd�r. Risperidon plazmada albumin ve alfa- asit glikoproteinine ba�lan�r. Plazma proteinlerine ba�lanma oranlar� risperidon i�in % 90, aktif metaboliti 9-hidroksi-risperidon i�in % 77'dir.
Biyotransformasyon:
Risperidon, CYP2D6 arac�l��� ile farmakolojik aktivitesi risperidona benzeyen 9-hidroksi- risperidona metabolize olur. Risperidon ve 9-hidroksi-risperidon birlikte aktif antipsikotik fraksiyonu olu�turur. CYP2D6 genetik polimorfizm g�stermektedir. H�zl� CYP2D6 metabolize ediciler risperidonu h�zla 9-hidroksi-risperidona d�n��t�r�rken, yava� CYP2D6 metabolize edicilerde bu d�n���m �ok daha yava� ger�ekle�ir. H�zl� metabolize ediciler, yava� CYP2D6 metabolize edicilere k�yasla daha d���k risperidon ve daha y�ksek 9-hidroksi-risperidon konsantrasyonlar�na sahip olmakla birlikte, risperidon ve 9-hidroksi-risperidon kombinasyonunun (yani, aktif antipsikotik fraksiyon) farmakokineti�i, tek ve �oklu dozlardan sonra, h�zl� ve yava� CYP2D6 metabolize edicilerde benzer niteliktedir.
Risperidonun ba�ka bir metabolik yola�� N-dealkilasyondur. �nsan karaci�er mikrozomlar�yla yap�lan in vitro �al��malarda, klinikteki kullan�m konsantrasyonlar�ndaki risperidonun, sitokrom P450 izoenzimleriyle (CYP1A2, CYP2A6, CYP2C8/9/10, CYP2D6, CYP2E1, CYP3A4 ve CYP3A5) metabolize edilen ila�lar�n metabolizmalar�n� �nemli �l��de inhibe etmedi�i g�sterilmi�tir.
Eliminasyon:
Oral risperidon uygulamas�ndan bir hafta sonra, dozun % 70'i idrar ve % 14'� fe�es ile itrah edilir. �drardaki risperidon ve 9-hidroksi-risperidon, oral yolla uygulanan dozun % 35-45'ini temsil eder. Geri kalan k�s�m inaktif metabolitlerdir. Eliminasyon faz�, son RISPERDAL CONSTA enjeksiyonundan yakla��k 7-8 hafta sonra tamamlanmaktad�r.
Do�rusall�k /Do�rusal Olmayan Durum:
�ki haftada bir enjekte edilen 25-50 mg doz aral���ndaki risperidonun farmakokineti�i do�rusald�r.
Hastalardaki karakteristik �zellikler
Ya�l�lar:
Oral risperidon ile yap�lan bir tek-doz farmakokinetik �al��mas�nda, ya�l�larda ortalama olarak
% 43 daha y�ksek aktif antipsikotik fraksiyon plazma konsantrasyonlar�, % 38 daha uzun bir yar� �m�r ve aktif antipsikotik fraksiyonun klirensinde % 30 azalma g�r�lm��t�r.
B�brek yetmezli�i:
Orta derecede b�brek yetmezli�i olan yeti�kinlerde aktif fraksiyonun klirensi, sa�l�kl� gen� yeti�kinlerinkinin yakla��k % 48' dir (ya� aral��� 25-35 ya�). �iddetli derecede b�brek yetmezli�i olan yeti�kinlerde aktif fraksiyonun klirensi, sa�l�kl� gen� yeti�kinlerinkinin yakla��k % 31' dir. Aktif fraksiyonun yar�lanma �mr� gen� yeti�kinlerde 16,7 saat, orta derecede b�brek yetmezli�i olan yeti�kinlerde 24,9 saat (ya da gen� yeti�kinlerden yakla��k 1,5 kat daha uzun) ve �iddetli b�brek yetmezli�i olanlarda 28,8 saat (gen� yeti�kinlerden yakla��k 1,7 kat daha uzun)' dur.
Karaci�er yetmezli�i:
Karaci�er yetmezli�i olan hastalarda risperidonun plazma konsantrasyonlar� normaldir ancak plazmadaki ortalama serbest risperidon fraksiyonu yakla��k % 37,1 artm��t�r. Bu verilere g�re orta ve �iddetli karaci�er yetmezli�i olan yeti�kinlerde, risperidon ve risperidonun aktif fraksiyonunun oral klirensi ve eliminasyon yar� �mr� gen� sa�l�kl� yeti�kinlerden anlaml� derecede farkl� de�ildir.
Farmakokinetik/farmakodinamik ili�kiler:
Etkinlik ve g�venlili�in de�erlendirildi�i Faz-III �al��malar�n�n hi�birinde de�erlendirme vizitleri aras�nda aktif antipsikotik fraksiyonun plazma konsantrasyonlar� ile total PANNS (Pozitif ve Negatif Sendrom �l�e�i) ve total ESRS (Ekstrapiramidal Semptom Derecelendirme �l�e�i) puanlar�ndaki de�i�iklikler aras�nda herhangi bir ili�ki g�zlenmemi�tir.
Cinsiyet, �rk ve sigara al��kanl���:
Bir pop�lasyon farmakokinetik analizinde, cinsiyet, �rk ya da sigara al��kanl���n�n risperidon ya da aktif antipsikotik fraksiyonun farmakokinetikleri �zerinde belirgin etki g�stermedikleri belirlenmi�tir.
5.3. Klinik �ncesi g�venlilik verileri
S��an ve k�peklerde risperidon ile yap�lan (sub)kronik toksisite �al��malar�na benzer �ekilde, RISPERDAL CONSTA ile tedavinin (12 aya dek intram�sk�ler enjeksiyon) maj�r etkileri, risperidonun farmakodinamik aktivitesiyle ili�kili olarak prolaktin-arac�l� meme bezi stim�lasyonu, erkek ve di�i �reme sistemlerinde de�i�iklikler ve santral sinir sistemi (SSS) etkileridir. Gen� s��anlarla oral risperidon ile yap�lan bir toksisite �al��mas�nda, artan yavru mortalitesi ve fiziksel geli�imde gecikme g�zlenmi�tir. Oral risperidon tedavisi g�ren gen� k�peklerle yap�lan 40 haftal�k �al��mada cinsel olgunla�ma gecikmi�tir. EAA (E�ri Alt� Alan) temelinde, k�peklerde uzun kemik geli�imi, adolesanlarda uygulanan maksimum insan oral dozunun 3,6 kat� dozlarda (1,5 mg/g�n) etkilenmemi� iken, uzun kemikler ve cinsel olgunla�ma �zerindeki etkiler adolesanlarda uygulanan maksimum insan oral dozunun 15 kat� dozlarda g�zlenmi�tir.
Risperidon s��an ve tav�anlarda teratojenik bulunmam��t�r. Risperidon ile y�r�t�len s��an �reme �al��malar�nda, anne-baban�n �iftle�me davran��lar� �zerinde ve yavrular�n do�um a��rl�klar� ve hayatta kalmalar� �zerinde advers etkiler g�r�lm��t�r. S��anlarda intrauterin risperidon maruziyeti, yeti�kin d�nemde kognitif defisitler ile ili�kili bulunmu�tur. Ba�ka dopamin antagonistleri gebe hayvanlara uyguland���nda, yavrular�n ��renme ve motor geli�imleri �zerinde negatif etkilere yol a�m��t�r.
Erkek ve di�i s��anlara 12 ve 24 ay boyunca 40 mg/kg/2 hafta dozlar�nda yap�lan RISPERDAL CONSTA uygulamas� osteodistrofiye neden olmu�tur. Osteodistrofi i�in s��anlarda etkili olan doz, mg/m2 baz�nda incelendi�inde, �nerilen maksimum insan dozunun 8 kat� olmu�tur ve �nerilen maksimum dozda insanlarda beklenen maksimum maruziyetin iki kat� bir plazma maruziyeti ile ili�kilidir. 12 ay boyunca 20 mg/kg/2 hafta'ya kadar dozlarda RISPERDAL CONSTA tedavisi alan k�peklerde osteodistrofi g�zlenmemi�tir. Bu doz, insanlarda �nerilen maksimum dozun 14 kat� plazma maruziyeti sa�lamaktad�r.
Genotoksik potansiyele ili�kin hi�bir bulgu yoktur.
G��l� bir dopamin D2-antagonistinden beklenece�i gibi, s��anlar ve fareler �zerinde y�r�t�len oral karsinojenite �al��malar�nda, hipofiz bezi adenomalar� (fare), endokrin pankreas adenomalar� (s��an) ve meme bezi adenomalar�nda (her iki t�r) art�� g�r�lm��t�r.
Wistar (Hannover) s��anlar� �zerinde RISPERDAL CONSTA ile (5 ve 40 mg/kg/2 hafta dozlar) y�r�t�len bir intram�sk�ler karsinojenite �al��mas�nda, 40 mg/kg dozda endokrin pankreas, hipofiz bezi ve adrenal medulla t�m�rleri insidans�nda art�� g�zlenirken, 5 ve 40 mg/kg dozlarda ise meme bezi t�m�rleri geli�mi�tir. Oral ve intramusk�ler doz uygulamas�yla g�zlenen bu t�m�rler, uzun s�reli dopamin D2 antagonizmas� ve hiperprolaktinemiye ba�l� olabilir. Doku k�lt�r� �al��malar�, insan meme t�m�rlerindeki h�cre b�y�mesinin prolaktin taraf�ndan uyar�labilece�ini g�stermektedir. RISPERDAL CONSTA ile tedavi edilen s��anlardaki adrenal medulla t�m�rlerinin insidans�n� art�rd��� varsay�lan hiperkalsemi ise, her iki doz grubunda da g�zlenmi�tir. Hiperkalseminin insanlarda feokromasitomaya yol a�t���na dair bulgu yoktur.
40 mg/kg/2 hafta dozlarda RISPERDAL CONSTA ile tedavi edilen erkek s��anlarda, renal tub�ler adenomalar meydana gelmi�tir. D���k doz grubunda, NaCl % 0,9 grubunda ya da mikrok�re ta��y�c�l� kontrol grubunda renal t�m�r g�zlenmemi�tir. RISPERDAL CONSTA ile tedavi edilen erkek Wistar (Hannover) s��anlar�ndaki renal t�m�rlerin mekanizmas� bilinmemektedir. Oral risperidon ile yap�lan karsinojenite �al��malar�nda, Wistar (Wiga) s��anlarda ya da Swiss farelerde tedavi ile ili�kili renal t�m�r insidans�nda art�� ortaya ��kmam��t�r. T�rler aras�nda t�m�r organ profilleri aras�ndaki farkl�l��� ortaya koymak i�in yap�lan �al��malar, karsinojenite �al��mas�nda kullan�lan Wistar (Hannover) t�r�n�n, oral karsinojenite �al��malar�nda kullan�lan Wistar (Wiga) t�r�ne g�re, spontan ya�a ba�l� non- neoplastik renal de�i�iklikler, serum prolaktin art��lar� ve risperidona ba��ml� renal de�i�iklikler a��s�ndan b�y�k �l��de farkl�l�k g�sterdi�ini ortaya koymu�tur. Kronik olarak RISPERDAL CONSTA tedavisi alan k�peklerde b�brek ile ilgili de�i�iklikler oldu�una dair veri yoktur.
Osteodistrofinin, prolaktin ile ili�kili t�m�rlerin ve s��an t�rlerine spesifik olduklar� varsay�lan renal t�m�rlerin insandaki risk a��s�ndan �nemi bilinmemektedir.
Y�ksek doz RISPERDAL CONSTA uygulamalar�ndan sonra k�pekler ve s��anlarda enjeksiyon b�lgesinde lokal irritasyon g�zlenmi�tir. S��anlarda yap�lan 24 ay s�reli IM karsinojenite �al��mas�nda, ta��y�c� veya aktif ila� grubunda enjeksiyon b�lgesi t�m�rlerinde art�� g�zlenmemi�tir.
In vitro ve in vivo hayvan modellerinde, risperidonun y�ksek dozlarda QT aral���nda uzamaya neden olabilece�i g�sterilmi�tir; bu uzama hastalarda teorik olarak Torsades de Pointes riskinde art�� ile ili�kilendirilmi�tir.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
![]()
RISPERDAL CONSTA uzat�lm�� sal�ml� enjeksiyonluk s�spansiyon i�in toz
7525 DLJN1 poli-(d,l-laktid-ko-glikolid) polimer
Seyreltici
Polisorbat 20
Karmeloz sodyum 40mPa.s Disodyum hidrojen fosfat dihidrat Susuz sitrik asit
Sodyum klor�r Sodyum hidroksit Enjeksiyonluk su
6.2. Ge�imsizlikler
RISPERDAL CONSTA b�l�m 6.6'da s�z� edilenlerin d���nda herhangi bir ila� veya s�v� ile kar��t�r�lmamal� veya seyreltilmemelidir.
6.3. Raf �mr�
36 ay (2-8 °C'de)
Seyreltildikten sonra: Kullan�m s�ras�ndaki fiziksel ve kimyasal stabilitesinin 25°C'de 24 saat oldu�u kan�tlanm��t�r. Mikrobiyolojik a��dan bak�ld���nda �r�n hemen kullan�lmal�d�r. Hemen kullan�lmad��� takdirde, kullan�m s�ras�ndaki saklama s�resi ve ko�ullar�, kullan�c�n�n sorumlulu�undad�r ve normal �artlarda ��z�nd�rme, kontroll� ve valide edilmi� aseptik ko�ullarda ger�ekle�tirilmedi�i s�rece seyreltildikten sonra 25°C'de 6 saatten fazla saklanmamal�d�r.
6.4. Saklamaya y�nelik �zel tedbirler
2-8°C aras� s�cakl�klarda (buzdolab�nda) saklay�n�z. I��ktan koruyunuz.
25°C �zerindeki s�cakl�klara maruz b�rakmay�n�z.
E�er buzdolab�nda saklanam�yorsa, RISPERDAL CONSTA uygulamadan �nce en fazla 7 g�n s�resince 25°C alt�ndaki oda s�cakl�klar�nda saklanmal�d�r.
Buzdolab�nda saklanmayan �r�n� 25°C �zerindeki s�cakl�klara maruz b�rakmay�n�z.
6.5. Ambalaj�n niteli�i ve i�eri�i
��nesiz flakon kullan�m aparat�
RISPERDAL CONSTA 25 mg uzat�lm�� sal�ml� enjeksiyonluk s�spansiyon i�eren bir flakon
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj At�klar�n�n Kontrol� Y�netmeli�i''ne uygun olarak imha edilmelidir.
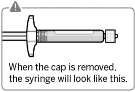
�nemli bilgiler
![]()
RISPERDAL CONSTA ba�ar�l� bir �ekilde uygulanmas� i�in bu Kullanma Talimat�ndaki maddelere s�k� bir �ekilde uyulmas� gereklidir.
30 dakika bekleyiniz
Doz ambalaj�n� buzdolab�ndan ��kararak suland�rma �ncesinde en az 30 dakika oda s�cakl���nda bekletiniz.
Ba�ka herhangi bir �ekilde �s�tmay�n�z.
Verilen par�alar� kullan�n�z
Bu doz ambalaj�ndaki bile�enler �zel olarak RISPERDAL CONSTA ile birlikte kullan�m i�in tasarlanm��t�r. RISPERDAL CONSTA yaln�zca doz ambalaj�nda verilen seyrelticide seyreltilmelidir.
Doz ambalaj�ndaki HERHANG� bir bile�eni de�i�tirmeyiniz. S�spansiyonu suland�rma sonras�nda saklamay�n�z
��kelmeyi �nlemek i�in dozu suland�rma sonras�nda en k�sa s�re i�erisinde uygulay�n�z.
Uygun dozaj
![]()
TEK KULLANIMLIK C�HAZ
Ama�lanan RISPERDAL CONSTA dozunun verildi�inden emin olmak i�in flakonun t�m i�eri�i uygulanmal�d�r.
Tekrar kullanmay�n�z. T�bbi cihazlar ama�lanan �ekilde uygulanmak a��s�ndan �zg�n materyal �zellikler gerektirir. Bu �zellikler yaln�zca tek kullan�ma y�nelik olarak do�rulanm��t�r. Sonraki kullan�m�na y�nelik olarak cihaz�n tekrar uygulanmas�na y�nelik herhangi �aba, cihaz�n b�t�nl���n� olumsuz olarak etkileyebilir veya performansta bozulmaya neden olabilir.
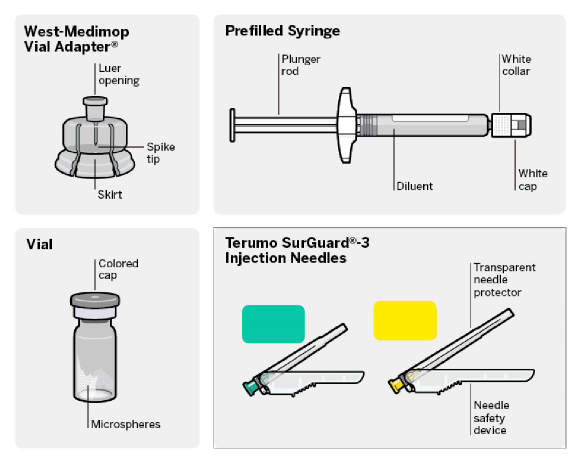
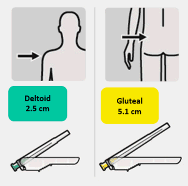
Deltoid
2.5 cm
Gluteal
5.1 cm
Flakon Adapt�r�
Kullan�ma Haz�r Enjekt�r
Enjeksiyon ��neleri
Flakon
Doz ambalaj� i�erikleri
Bile�enler kurulur
Ad�m 1
Flakon adapt�r� flakona ba�lan�r
Flakonun kapa�� ��kar�l�r Flakonun renkli kapa�� ��kar�l�r.
Flakon adapt�r� haz�rlan�r
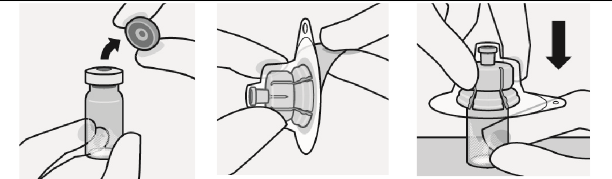
Steril blister g�sterildi�i gibi tutulur. Koruyucu ka��t soyularak ��kar�l�r.
Flakon adapt�r� flakona ba�lan�r
Flakon sert bir y�zeye konur ve alt�ndan tutulur. Flakon adapt�r� gri kau�uk t�pa
Gri t�pan�n �st k�sm� alkoll� pamuk ile silinir.
A��k havada kurumaya b�rak�l�r.
Gri kau�uk t�pa
��kar�lmaz.
Flakon adapt�r� blisterden
��kar�lmaz.
Sivri uca herhangi bir zamanda dokunulmaz. Bu, kontaminasyona neden olur.
�zerinde ortalan�r. Flakon adapt�r�, yerine sabit bir �ekilde oturana kadar flakonun �zerine do�ru bast�r�l�r.
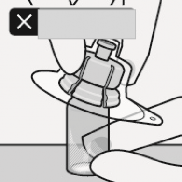
Yanl��
Flakon adapt�r� a��l� olarak yerle�tirilmemelidir; aksi takdirde seyreltici flakona transfer �zerinde s�z�nt� yapabilir.
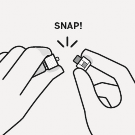
Kullan�ma haz�r enjekt�r flakon adapt�r�ne ba�lan�r
![]()
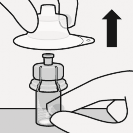
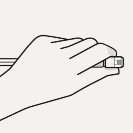
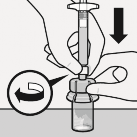

Steril blister ��kar�l�r
Flakon s�z�nt�y� �nlemek i�in dik konumda tutulur. Flakonun alt k�sm� tutulur ve ��karmak i�in steril blister �ekilir.
�alkalanmaz.
Uygun �ekilde kavran�r Enjekt�r�n ucundaki beyaz man�ondan tutulur.
Enjekt�r kurulum s�ras�nda cam silindirden tutulmaz.
Kapak ��kar�l�r Beyaz man�on tutularak beyaz kapak �ekilir.
Beyaz kapak d�nd�r�lmez veya kesilmez.
Enjekt�r ucuna dokunulmaz. Bu, kontaminasyona neden olacakt�r.
Enjekt�r flakon adapt�r�ne ba�lan�r
Flakon adapt�r� sabit kalmas� i�in etekten tutulur.
Enjekt�r, beyaz man�ondan tutulur, ard�ndan ucu, flakon adapt�r�n�n luer a��kl���na tak�l�r.
Cam enjekt�r silindiri tutulmaz. Bu, beyaz man�onun gev�emesine veya
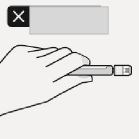
Yanl��
Flakon adapt�r�n�n �zerindeki a��k luer a��kl���na dokunulmaz. Bu, kontaminasyona neden olur.
K�r�lm�� kapak at�labilir.
��kmas�na neden olur.
Enjekt�r flakon adapt�r�ne sert bir saat y�n�nde d�n�� hareketi ile tam oturana kadar tak�l�r.
Mikrok�reler suland�r�l�r
Ad�m 2
Fazla s�k�lmaz. Fazla s�k�lma enjekt�r ucunun k�r�lmas�na neden olabilir.
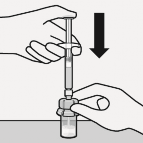
Seyreltici enjekte edilir
Tam miktarda seyreltici enjekt�rden flakona enjekte edilir.
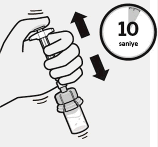
Mikrok�reler seyrelticide ask�ya al�n�r
![]()

Piston �ubu�u tutularak, g�sterildi�i gibi en az 10 saniye �iddetli bir �ekilde �alkalan�r.
S�spansiyon kontrol edilir. Uygun �ekilde kar��t�r�ld���nda, s�spansiyon tek d�ze, yo�un ve s�t benzeri bir renkte g�r�l�r.
Mikrok�reler s�v�da g�r�n�r olacakt�r.
S�spansiyonun ��kelmemesi i�in derhal sonraki ad�ma ge�ilir.
S�spansiyon enjekt�re aktar�l�r
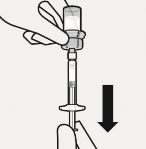
Flakon tamamen ters �evrilir. T�m i�eri�i flakondan enjekt�re �ekmek i�in piston �ubu�u yava��a a�a�� do�ru �ekilir.
Flakon adapt�r� ��kar�l�r
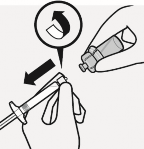
Beyaz man�on enjekt�r �zerinde tutulur ve flakon adapt�r�nden s�k�l�r.
Flakon etiketi b�l�m� delikli yerden y�rt�l�r. ��kar�lm�� etiket tan�ma ama�lar�na y�nelik olarak enjekt�re uygulan�r.
Flakon ve flakon adapt�r� uygun �ekilde at�l�r.
��ne tak�l�r
Ad�m 3
Uygun i�ne se�ilir Enjeksiyon konumuna dayanarak uygun i�ne se�ilir (gluteal veya deltoid)
��ne tak�l�r
Blister kesesi k�smen soyulur ve i�nenin alt k�sm�n� g�sterildi�i gibi tutmak i�in kullan�l�r
Enjekt�rdeki beyaz man�onu tutarak, enjekt�r sert bir saat y�n�nde d�nme hareketiyle tam oturana kadar i�ne luer ba�lant�s�na tak�l�r.
��ne luer a��kl���na dokunulmaz. Bu, kontaminasyona neden olur.
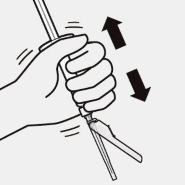
Mikrok�reler tekrar ask�ya al�n�r
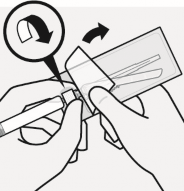
Blister kesesi tamamen ��kar�l�r.
Enjeksiyondan hemen �nce, ��kelme meydana gelmi� olabilece�inden enjekt�r sert bir �ekilde tekrar �alkalan�r.
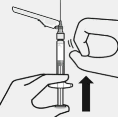
Doz enjekte edilir
Ad�m 4
�effaf i�ne koruyucu ��kar�l�r
��ne g�venlik cihaz� g�sterildi�i gibi enjekt�rden geriye do�ru ��kar�l�r.
Ard�ndan enjekt�r �zerindeki beyaz man�on tutularak �effaf i�ne koruyucu dikkatli bir �ekilde d�z olarak �ekilir.
Luer ba�lant�s� gev�eyebilece- �inden �effaf i�ne koruyucusu d�nd�r�lmez.
Hava baloncuklar� ��kar�l�r ��ne dik
konumda tutulur ve hava baloncuklar�n�n �ste ��kmas� i�in hafif�e vurulur. Havay� uzakla�t�rmak i�in yava��a ve dikkatli bir �ekilde piston �ubu�u yukar� do�ru itilir.
Enjekte edilir
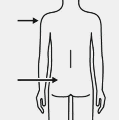
Enjekt�r�n t�m i�eri�i intramuskuler olarak (IM) hastan�n gluteal veya deltoid kas�na derhal enjekte edilir.
Gluteal enjeksiyon, gluteal alan�n �st d�� �eyre�ine yap�lmal�d�r.
�ntraven�z olarak uygulanmaz.
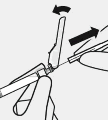
��ne g�venlik cihaz�na sabitlenir.
Bir eli kullanarak, i�ne g�venlik cihaz�, 45 derecelik a�� ile sert ve d�z bir y�zey �zerinde tak�l�r. ��ne g�venlik cihaz�na tamamen tak�lana kadar sert, h�zl� bir hareketle bast�r�l�r
��ne batma yaralanmalar� �nlenir:
�ki el kullan�lmaz
��ne g�venlik cihaz� kasten ��kar�lmaz veya yanl�� kullan�lmaz.
��nenin b�k�lmesi veya zarar g�rmesi durumunda i�ne d�z hale getirilmez veya g�venlik cihaz� tak�lmaz.
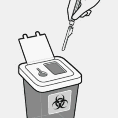
��neler uygun �ekilde bertaraf edilir
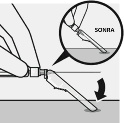
��ne g�venlik cihaz�n�n tamamen tak�ld���ndan emin olmak i�in kontrol edilir.
Uygun keskici ve delici alet at�k kutusuna at�l�r.
Ayr�ca doz ambalaj�nda verilen kullan�lmam�� i�ne de at�l�r.
 Kalp Krizi
Kalbe giden kan ak��� durdu�unda kalp krizi meydana gelir.
Kalp Krizi
Kalbe giden kan ak��� durdu�unda kalp krizi meydana gelir. |
 A��r� Alkol Kullan�m�, Alkolizm
Alkol ba��ml�l���, alkol kullan�m� ve alkol sorunlar� aras�ndaki fark� a��klamak g��t�r.
�rne�in, ge�mi�te alkol kullanm�� olan bir kimsenin mutlaka alkol ba��ml�s� olmas�
gerekmez.
A��r� Alkol Kullan�m�, Alkolizm
Alkol ba��ml�l���, alkol kullan�m� ve alkol sorunlar� aras�ndaki fark� a��klamak g��t�r.
�rne�in, ge�mi�te alkol kullanm�� olan bir kimsenin mutlaka alkol ba��ml�s� olmas�
gerekmez. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| NEORIS | 8697930021292 | |
| NODIREP | 8699821090110 | |
| PERILIFE | 8699559090079 | |
| RESTELA | 8699525094384 | |
| RICUS | 8699578095413 | 55.47TL |
| Di�er E�de�er �la�lar |
 |
Ast�m Ast�ml� ki�ilerin akci�erlerindeki hava borular� (bron�lar) hassast�r. Bu ki�iler belirli tetikleyici fakt�rlere maruz kald�klar�nda, hava borular� nefes almalar�n� g��le�tirecek �ekilde daral�r. |
 |
Asperger Sendromu Asperger sendromu, otistik gurubun bir b�l�m� olan bir �z�rd�r. Bu genelde, gurubun daha ”y�ksek” taraf�nda yer ald��� d���n�len ki�ilere uygun bir tan�d�r. |
 |
S�rt A�r�s� S�rt a�r�s� birden bire ortaya ��k�p �iddetli (akut) olabilir veya zamanla geli�ip daha uzun s�reli sorunlara (kronik) neden olabilir. |
�LA� GENEL B�LG�LER�
Johnson & Jonhson S�hhi Malzeme San. ve Tic.Ltd.�ti.
| Geri �deme Kodu | A06815 |
| Sat�� Fiyat� | 2018.9 TL [ 1 Dec 2025 ] |
| �nceki Sat�� Fiyat� | 2018.9 TL [ 24 Nov 2025 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699593781025 |
| Etkin Madde | Risperidon |
| �thal ( ref. �lke : Yunanistan ) ve Be�eri bir ila�d�r. |