SANDOSTATIN LAR 30 mg 1 flakon K�sa �r�n Bilgisi
{ Oktreotid }
1. BE�ER� TIBB� �R�N�N ADI
SANDOSTAT�N® LAR® 30 mg enjeksiyonluk s�spansiyon i�in toz ve ��z�c� Steril
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Oktreotid* (serbest peptid olarak) 30 mg (*33,6 mg oktreotid asetat'a e�de�erdir.)
Yard�mc� maddeler
Sodyum karboksi metil sel�loz 14 mg
Yard�mc� maddeler
3. FARMAS�T�K FORMU
Enjeksiyonluk s�spansiyon i�in toz ve ��z�c�
Enjeksiyonluk kuru etkin madde i�eren renksiz cam flakon ve ��z�c� i�eren ��r�nga.
Flakonlar, beyaz ila sar�ms� bir renk tonu i�eren beyaz toz halinde etkin madde i�erir. Enjeksiyonluk s�spansiyon i�in verilen ��z�c� berrak ve renksiz ila hafif sar� veya kahverengi renktedir.
Ad�m
Seyreltici ��zelti ile dolu enjekt�r�n ba�l���n� ��kar�n ve
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Cerrahi tedavinin veya radyoterapinin uygun olmad��� ya da etkisiz kald��� hastalarda veya radyoterapinin tam etkisini g�stermesine kadar ge�en ara d�nemde akromegali tedavisinde (bkz. B�l�m 4.2).
Karsinoid sendromun �zelliklerini ta��yan karsinoid t�m�rler gibi fonksiyonel gastro- entero-pankreatik endokrin t�m�rlere e�lik eden semptomlar� olan hastalar�n tedavisinde (bkz. B�l�m 5.1).
Orta ba��rsaktan kaynaklanan veya primer kayna�� bilinmeyen ancak orta ba��rsak d��� b�lgelerden kaynaklanan t�m�rlerin ekarte edilmi� oldu�u, ilerlemi� n�roendokrin t�m�rleri olan hastalar�n tedavisinde.
TSH salg�layan hipofiz adenomlar�n�n tedavisinde:
Cerrahi tedavi ve/veya radyoterapiden sonra salg� normalize olmad���nda
4.2. Pozoloji ve uygulama �ekli
Akromegalide:Tedaviye 3 ay boyunca her 4 haftada bir 20 mg SANDOSTAT�N LAR kullanarak ba�lanmas� �nerilir. SANDOSTAT�N LAR tedavisi, son uygulanan subkutan SANDOSTAT�N dozundan sonraki g�n ba�lat�labilir. Daha sonraki dozaj ayarlamalar�, klinik semptomlar ve serumdaki b�y�me hormonu (GH) ve ins�lin-benzeri b�y�me fakt�r� 1/somatomedin C (IGF 1) d�zeyleri g�z �n�nde bulundurularak yap�lmal�d�r.
Bu 3 ayl�k uygulama s�ras�nda klinik semptomlar� ve biyokimyasal parametreleri (GH; IGF 1) tamamen kontrol alt�na al�namayan (GH konsantrasyonlar� hala 2,5 mikrogram/litreden y�ksek olan) hastalarda doz, her 4 haftada bir 30 mg'a y�kseltilebilir. E�er 3 ay sonra hastan�n biyokimyasal parametreleri (GH; IGF 1) ve/veya klinik semptomlar� 30 mg'l�k dozda tamamen kontrol alt�na al�nam�yorsa, doz her 4 haftada bir 40 mg'a y�kseltilebilir. 40 mg �zerindeki dozlar �nerilmez.
3 ay boyunca her 4 haftada bir uygulanan 20 miligraml�k dozla GH konsantrasyonlar� daima < 1 mikrogram/litre bulunan, serum IGF 1 konsantrasyonlar� normale d�nen ve akromegalinin reversibl nitelikteki hemen b�t�n belirtileri/semptomlar� ortadan kalkan hastalarda tedaviye, her 4 haftada bir 10 mg SANDOSTAT�N LAR kullanarak devam edilebilir. Ancak �zellikle bu hasta grubunda olmak �zere d���k SANDOSTAT�N LAR dozlar�n�n kullan�lmas� s�ras�nda serum GH ve IGF 1 konsantrasyonlar�n�n ve klinik belirtilerin/semptomlar�n yeterince kontrol alt�nda olup olmad���n�n yak�ndan izlenmesi �nerilir.
Stabil SANDOSTAT�N LAR dozu alan hastalarda her 6 ayda bir GH ve ins�lin-benzeri b�y�me fakt�r� (IGF 1) de�erlerine bak�lmal�d�r.
Gastro-entero-pankreatik endokrin t�m�rlerde:
Fonksiyonel gastro-entero-pankreatik endokrin t�m�rler ile ili�kili semptomlar� olan hastalar�n tedavisi:
Tedaviye 4 haftada bir 20 mg SANDOSTAT�N LAR kullan�larak ba�lanmas� �nerilir. �lk SANDOSTAT�N LAR enjeksiyonunu izleyen 2 hafta boyunca, �nceden etkili oldu�u bilinen subkutan SANDOSTAT�N dozlar�n�n kullan�lmaya devam edilmesi gerekir.
3 ayl�k tedaviyle semptomlar� ve biyolojik parametreleri iyi bir �ekilde kontrol alt�na giren hastalarda doz, her 4 haftada bir 10 mg SANDOSTAT�N LAR olarak d���r�lebilir.
3 ayl�k tedaviyle semptomlar� yaln�zca k�smen kontrol alt�na al�nabilen hastalarda doz,
her 4 haftada bir 30 mg SANDOSTAT�N LAR olmak �zere y�kseltilebilir.
SANDOSTAT�N LAR tedavisi s�ras�nda gastro-entero-pankreatik t�m�rlere e�lik eden semptomlar� artabilen hastalarda, SANDOSTAT�N LAR tedavisinde �nce kullan�lmakta olan dozda subkutan SANDOSTAT�N kullan�lmas� �nerilir. Bu durum daha �ok, SANDOSTAT�N LAR tedavisinin ilk 2 ay�nda, oktreotid konsantrasyonlar� terap�tik de�erlere ula��ncaya kadar g�zlenebilmektedir.
Orta ba��rsaktan kaynaklanan veya primer kayna�� bilinmeyen ancak orta ba��rsak d��� b�lgelerden kaynaklanan t�m�rlerin ekarte edilmi� oldu�u ilerlemi� n�roendokrin t�m�rleri olan hastalar�n tedavisi:
�nerilen SANDOSTAT�N LAR dozu, 4 haftada bir uygulanan 30 mg'd�r (bkz. B�l�m 5.1). T�m�r progresyonu yokken t�m�r kontrol� i�in SANDOSTAT�N LAR tedavisine devam edilmelidir.
TSH salg�layan adenomlar�n tedavisi:
SANDOSTAT�N LAR ile tedaviye, herhangi bir doz ayarlamas� d���n�lmeden 3 ay s�reyle 4 haftal�k aral�klarla 20 mg dozunda ba�lanmal�d�r. Doz daha sonra TSH ve tiroid hormonu yan�t�na ba�l� olarak ayarlan�r.
Uygulama �ekli:
Doktor taraf�ndan ba�ka �ekilde tavsiye edilmedi�i takdirde;
SANDOSTAT�N LAR, yaln�zca derin intragluteal (derin intram�sk�ler) enjeksiyon yoluyla uygulanmal�d�r. Arka arkaya yap�lacak enjeksiyonlarda sa� ve sol kal�alar s�rayla kullan�lmal�d�r (bkz. B�l�m 6.6).
�zel pop�lasyonlara ili�kin ek bilgiler:
B�brek yetmezli�i:
B�brek fonksiyonlar�n�n bozuk olmas�, subkutan SANDOSTAT�N tedavisi s�ras�nda oktreotid EAA de�erini etkilememi� oldu�undan bu gibi hastalarda SANDOSTAT�N LAR dozunun de�i�tirilmesi gerekmez.
Karaci�er yetmezli�i:
SANDOSTAT�N subkutan ve intraven�z olarak kullan�ld��� bir �al��mada eliminasyon kapasitesinin karaci�er sirozu vakalar�nda azalabildi�i, ya�l� karaci�er hastal�klar�nda ise b�yle bir azalman�n s�z konusu olmad��� g�sterilmi�tir. Baz� durumlarda karaci�er yetmezli�i olan hastalarda doz ayarlamas� gerekebilir.
Pediyatrik pop�lasyon:
![]()
SANDOSTAT�N LAR'�n �ocuklarda kullan�lmas� konusundaki deneyimler s�n�rl�d�r.
Geriyatrik pop�lasyon:
Ya�� 65 veya daha fazla olan vakalarda subkutan SANDOSTAT�N kullan�larak yap�lan bir �al��mada herhangi bir doz ayarlanmas�na ihtiya� duyulmam�� oldu�undan bu hasta grubunda SANDOSTAT�N LAR dozunun ayarlanmas�na ihtiya� yoktur.
4.3. Kontrendikasyonlar
Oktreotide veya bile�iminde yer alan (bkz. B�l�m 6.1) herhangi bir yard�mc� maddeye kar�� bilinen a��r� duyarl�l��� olan hastalarda kontrendikedir.
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Genel:
B�y�me hormonu salg�layan hipofiz t�m�rleri bazen b�y�yerek g�rme alan� kusurlar� gibi a��r komplikasyonlara neden olabildi�inden, b�t�n hastalar�n dikkatle izlenmesi �artt�r. T�m�r�n b�y�d���n� g�steren kan�tlar ortaya ��karsa, daha ba�ka tedavi yakla��mlar�na ba�vurulmas� �nerilir.
Akromegalik kad�n hastalarda GH d�zeylerindeki azalman�n terap�tik yararlar� ve IGF-1 konsantrasyonunun normale d�nmesi fertilitenin geri d�nmesini sa�layabilmektedir. �ocuk do�urma potansiyeline sahip kad�n hastalara oktreotid ile tedavi s�ras�nda gerekirse uygun do�um kontrol� kullanmalar� tavsiye edilmelidir.
Oktreotid ile uzun s�reli tedavilerde hastalarda tiroid fonksiyonlar� izlenmelidir.
Oktreotid tedavisi esnas�nda hepatik fonksiyon izlenmelidir.
Kardiyovask�ler ili�kili olaylar:
Yayg�n bradikardi vakalar� bildirilmi�tir. Beta-blok�rler, kalsiyum kanal blok�rleri, veya s�v� elektrolit dengesini kontrol eden ila�lar�n doz ayarlanmas� gerekebilir (bkz. B�l�m 4.5).
Safra kesesi ve ili�kili olaylar:
Kolelitiyazis, SANDOSTAT�N tedavisi esnas�nda olduk�a yayg�n g�r�len bir olay olup, kolesistit ve safra kanal�nda dilatasyonla ili�kilendirilebilir (bkz. B�l�m 4.8). Ek olarak, pazarlama sonras� deneyime g�re, SANDOSTAT�N LAR alan hastalarda kolelityazisin bir komplikasyonu olarak kolanjit vakalar� bildirilmi�tir. SANDOSTAT�N LAR tedavisine ba�lanmadan �nce ve daha sonra da her 6 ayda bir safra kesesinin ultrasonla muayenesi �nerilir.
Glukoz metabolizmas�:
B�y�me hormonu, glukagon ve ins�lin salg�lanmas�n� inhibe etmesi nedeniyle SANDOSTAT�N LAR glukoz kontrol�n� etkileyebilir. ���n sonras� glukoz tolerans� bozulabilir. SANDOSTAT�N subkutan ile tedavi edilen hastalarda bildirildi�i gibi baz� vakalarda, kronik uygulaman�n sonucu olarak inat�� hiperglisemi durumu geli�ebilir. Hipoglisemi de rapor edilmi�tir.
Ayn� zamanda Tip I diabetes mellitusu olan hastalarda, SANDOSTAT�N LAR muhtemelen glikoz reg�lasyonu �zerine etki eder ve ins�lin gereksinimini azaltabilir. Non-diyabetik ve k�smi bozulmam�� ins�lin rezervli Tip II diyabetiklerde SANDOSTAT�N Subkutan uygulanmas� ���n sonras� gliseminin artmas� ile sonu�lan�r. B�ylece bu hastalarda glikoz tolerans�n�n ve antidiabetik tedavinin izlenmesi �nerilir.
�nsulinomas� olan hastalarda, GH ve glukagon salg�s�n� inhibe etme g�c�n�n ins�line k�yasla daha fazla olmas� ve ins�lin �zerindeki inhibit�r etkisinin daha k�sa s�rmesi nedeniyle oktreotid, hipogliseminin s�resini ve derinli�ini art�rabilir. Bu hastalar yak�ndan izlenmelidir.
Beslenme:
Oktreotid, baz� hastalarda diyet ile al�nan ya�lar�n emilimini de�i�tirebilir.
Oktreotid tedavisi kullanan baz� hastalarda, azalm�� vitamin B12 d�zeyleri ve anormal Schilling testleri g�zlemlenmi�tir. Vitamin B12 eksikli�i hikayesi olan hastalarda SANDOSTAT�N LAR ile tedavi s�resince vitamin B12 seviyelerinin izlenmesi tavsiye edilir.
Pankreas fonksiyonu:
Gastroenteropankreatik n�roendokrin t�m�rleri i�in oktreotid tedavisi alan baz� hastalarda pankreas ekzokrin yetmezli�i (PEY) g�zlenmi�tir. PEY semptomlar� aras�nda steatore, gev�ek d��k�, abdominal �i�kinlik ve kilo kayb� say�labilir. Semptomatik hastalarda PEY i�in klinik k�lavuzlara g�re tarama ve uygun tedavi d���n�lmelidir.
Sodyum ��eri�i:
Bu t�bbi �r�n her “doz”unda 1 mmol (23 mg)'dan daha az sodyum ihtiva eder; yani asl�nda “sodyum i�ermez”.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
SANDOSTAT�N LAR, birlikte e�zamanl� olarak kullan�ld���nda beta blok�rler, kalsiyum kanal� blok�rleri veya s�v� ve elektrolit dengesini kontrol eden ajanlar gibi t�bbi �r�nlerin dozunda ayarlama gerekli olabilir (bkz. B�l�m 4.4).
SANDOSTAT�N LAR, birlikte e�zamanl� olarak kullan�ld���nda ins�lin ve anti- diyabetik t�bbi �r�nlerin dozunda ayarlamalar gerekli olabilir (bkz. B�l�m 4.4).
Oktreotidin barsaklardaki siklosporin emilimini azaltt��� ve simetidin emilimini
geciktirdi�i bulunmu�tur.
Oktreotid ve bromokriptinin birlikte e� zamanl� olarak kullan�lmas�, bromokriptin biyoyararlan�m�n� art�r�r.
S�n�rl� say�da yay�nlanm�� literat�r somatostatin analoglar�n�n, b�y�me hormonunun bask�lanmas� sonucu sitokrom P450 enzim sistemi ile metabolize edildi�i bilinen bile�iklerin metabolik klerensini azaltabildi�ini g�stermektedir. Oktreotid'in bu etkiye sahip olabilece�i g�z ard� edilemeyece�inden ba�l�ca CYP3A4 yoluyla metabolize olan di�er ila�lardan d���k terap�tik indekse sahip olanlar�n (kinidin, terfenadin) dikkatli kullan�lmas� gerekir.
Radyoaktif somatostatin analoglar� ile birlikte e� zamanl� kullan�m
Somatostatin ve oktreotid gibi analoglar�, somatostatin resept�rlerine yar��mal� olarak ba�lan�r ve radyoaktif somatostatin analoglar�n�n etkilili�ine m�dahale edebilir. Somatostatin resept�rlerine ba�lanan bir radyofarmas�tik olan Lutesyum (177 Lu) oksodotreotid uygulamas�ndan en az 4 hafta �nce SANDOSTAT�N LAR uygulamas�ndan ka��n�lmal�d�r. Gerekirse hastalar, lutesyum (177Lu) oksodotreotid uygulamas�ndan 24 saat �ncesine kadar k�sa etkili somatostatin analoglar� ile tedavi edilebilir.
Lutesyum (177Lu) oksodotreotid uygulamas�ndan sonra, SANDOSTAT�N LAR ile tedaviye 4 ila 24 saat i�inde devam edilebilir ve bir sonraki lutesyum (177Lu) oksodotreotid uygulamas�ndan 4 hafta �nce SANDOSTAT�N LAR ile tedavi tekrar kesilmelidir.
�zel pop�lasyonlara ili�kin ek bilgiler B�brek yetmezli�i:
B�brek yetmezli�i pop�lasyonu i�in etkile�im �al��mas� bulunmamaktad�r.
Karaci�er yetmezli�i:
Karaci�er yetmezli�i pop�lasyonu i�in etkile�im �al��mas� bulunmamaktad�r.
Pediyatrik pop�lasyon:
Pediyatrik pop�lasyon i�in etkile�im �al��mas� bulunmamaktad�r.
Geriyatrik pop�lasyon:
Geriyatrik pop�lasyon i�in etkile�im �al��mas� bulunmamaktad�r.
4.6. Gebelik ve laktasyon
Gebelik kategorisi B'dir.
�ocuk do�urma potansiyeli bulunan kad�nlar / Do�um kontrol� (Kontrasepsiyon)
Oktreotid tedavisi boyunca �ocuk do�urma potansiyeli olan kad�n hastalar i�in uygun ve etkili kontrasepsiyon kullan�lmas� tavsiye edilmelidir.
Gebelik d�nemi
Gebe kad�nlarda oktreotid kullan�m�nda veriler k�s�tl�d�r (<300 gebelik sonucu) ve vakalar�n ��te birinde gebelik sonu�lar� bilinmemektedir. Raporlar�n �o�u pazarlama sonras� oktreotid kullan�m�ndan sonra al�nm�� olup, maruz kalan gebeliklerin
%50'sinden fazlas� akromegali hastalar�nda bildirilmi�tir. �o�u kad�n oktreotide gebeli�in ilk trimestresi s�ras�nda 100-1200 mikrogram/g�n SANDOSTAT�N Subkutan veya 10-40 mg/ay SANDOSTAT�N LAR aras�nda de�i�en dozlarda maruz kalm��t�r. Gebelik vakalar�n�n yakla��k %4'�nde konjenital anomaliler bildirilmi� olup, sonu�lar� bilinmemektedir. Bu vakalar i�in oktreotid ile nedensel bir ili�kiden ��phe edilmemektedir.
Hayvan �al��malar� �reme toksisitesi a��s�ndan do�rudan veya dolayl� zararl� etkiler
g�stermemektedir (bkz. B�l�m 5.3).
Bir �nlem olarak gebelik s�ras�nda SANDOSTAT�N LAR kullan�m�ndan ka��n�lmas�
tercih edilir (bkz. B�l�m 4.4).
Laktasyon d�nemi
Oktreotidinin insan s�t�yle at�l�p at�lmad��� bilinmemektedir. Hayvanlar �zerinde yap�lan �al��malar, oktreotidinin s�tle at�ld���n� g�stermektedir. SANDOSTAT�N LAR tedavisi s�ras�nda emzirme yap�lmamal�d�r.
�reme yetene�i / Fertilite:
Oktreotidin insan fertilitesi �zerinde bir etkiye sahip olup olmad��� bilinmemektedir. Gebelik ve laktasyon s�ras�nda tedavi edilen di�ilerin erkek yavrular�nda testislerin ge� indi�i tespit edilmi�tir. Bununla birlikte oktreotid g�nde 1 mg/kg v�cut a��rl���na kadar olan dozlarda erkek ve di�i s��anlarda fertiliteyi bozmam��t�r. (bkz. B�l�m 5.3).
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
SANDOSTAT�N LAR'�n ara� ve makine kullanma becerisi �zerinde etkisi yoktur veya ihmal edilebilir d�zeyde etkiye sahiptir. Hastalara SANDOSTAT�N LAR ile tedavi s�ras�nda ba� d�nmesi, bitkinlik/yorgunluk veya ba� a�r�s� ya�amalar� durumunda ara� veya makine kullan�rken dikkatli olmalar� tavsiye edilmelidir.
4.8. �stenmeyen etkiler
G�venlilik profilinin �zeti
Oktreotid tedavisi boyunca rapor edilen en s�k yan etkiler gastrointestinal hastal�klar, sinir sistemi hastal�klar�, hepato-bilier hastal�klar ve metabolizma ve beslenme hastal�klar� i�ermektedir.
Oktreotid uygulamalar� ile klinik uygulamada rapor edilen �ok yayg�n yan etkiler diyare, kar�n a�r�s�, bulant�, ba� a�r�s�, barsakta a��r� gaz, safra kesesi ta��, hiperglisemi ve kab�zl�k. Di�er yayg�n rapor edilen yan etkiler ba� d�nmesi, lokal enjeksiyon b�lgesi a�r�s�, safra �amuru, tiroid disfonksiyonu (tiroid stimule eden hormonun (TSH), Total
T4 ve serbest T4'�n azalmas� vs), gev�ek d��k�, glukoz tolerans�n�n bozulmas�, asteni, kusma ve hipoglisemidir.
A�a��daki yan etkiler, oktreotidle yap�lan klinik �al��malardan toplanm��t�r:
�ok yayg�n (≥1/10); yayg�n (≥1/100 ila <1/10); yayg�n olmayan (≥1/1.000 ila <1/100); seyrek ≥.1/10.000 ila <1/1000); �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Her s�kl�k grubu i�inde advers reaksiyonlar azalan ciddiyet s�ras�yla dizilmi�tir.
Endokrin hastal�klar�
Yayg�n: Hipotiroidizm, tiroid bozuklu�u (tiroid stimule eden hormonun (TSH), Total T4 ve serbest T4'�n azalmas� gibi)
Metabolizma ve beslenme hastal�klar�
�ok yayg�n: Hiperglisemi
Yayg�n: Hipoglisemi, glukoz tolerans bozuklu�u, anoreksia Yayg�n olmayan: Dehidratasyon
Sinir sistemi hastal�klar� �ok yayg�n: Ba� a�r�s� Yayg�n: Ba� d�nmesi Kardiyak hastal�klar� Yayg�n: Bradikardi
Yayg�n olmayan: Ta�ikardi
Solunum, g���s bozukluklar� ve mediastinal hastal�klar�
Yayg�n: Dispne
Gastrointestinal hastal�klar�
�ok yayg�n: Diyare, kar�n a�r�s�, bulant�, kab�zl�k, flatulans
Yayg�n: Dispepsi, kusma, kar�nda �i�kinlik, steatore, d��k� k�vam�nda azalma, fe�este renk de�i�ikli�i
Hepato-bilier hastal�klar�
�ok yayg�n: Kolelitiyazis
Yayg�n: Kolesistit, safra �amuru, hiperbilirubinemi
Deri ve deri alt� doku hastal�klar�
Yayg�n: Ka��nt�, d�k�nt�, alopesi
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar�
�ok yayg�n: Enjeksiyon b�lgesi reaksiyonlar� Yayg�n: Asteni
Ara�t�rmalar
Yayg�n: Transaminaz seviyelerinde art�� Pazarlama sonras� deneyim:
Spontan olu�mu� yan etkiler g�n�ll� olarak rapor edilmi�tir, s�kl�k veya ila� etkile�imi ile ili�kisini g�venle yay�nlamak her zaman m�mk�n de�ildir.
Kan ve lenf sistemi hastal�klar�
Trombositopeni
Ba����kl�k sistemi hastal�klar�
Anafilaksi, alerji/a��r� hassasiyet reaksiyonlar�
Kardiyak hastal�klar�
Aritmi
Hepato-bilier hastal�klar
Akut pankreatit, kolestaz�n e�lik etmedi�i akut hepatit, kolestatik hepatit, kolestaz,
sar�l�k, kolestatik sar�l�k.
Deri ve deri alt� doku hastal�klar�
�rtiker
Ara�t�rmalar
Alkalin fosfataz seviyesinde art��, gama glutamil transferaz seviyesinde art��.
Se�ili advers reaksiyonlar�n tan�m�
Safra kesesi ve ili�kili reaksiyonlar
Somatostatin analoglar�n�n safra kesesinin kontraktilitesini inhibe edip safra salg�s�n� azaltt��� ve bu durumun safra kesesinde anormalliklere veya �amura neden olabilece�i kan�tlanm��t�r. Uzun s�reli S.C. SANDOSTAT�N kullan�c�lar�n�n %15-30'unda safra kesesi ta�� olu�tu�u bildirilmi�tir. Genel pop�lasyondaki (40-60 ya� aras�) insidans yakla��k %5-20'dir. Akromegali veya gastro-entero pankreatik t�m�rleri olan hastalarda uzun s�reli SANDOSTAT�N LAR maruziyeti, SANDOSTAT�N LAR tedavisinin S.C. tedaviye k�yasla safra kesesi ta�� olu�ma insidans�n� art�rmad���n� g�stermektedir. Safra kesesi ta�lar� olu�ursa bunlar genellikle asemptomatik olmaktad�r; semptomatik ta�lar safra asitleriyle eritme tedavisi uygulanarak veya cerrahiyle tedavi edilmelidir.
Gastrointestinal hastal�klar
Nadir durumlarda, gastrointestinal yan etkiler, progresif kar�n �i�li�i, �iddetli epigastrik a�r�, abdominal hassasiyet ve sak�nman�n e�lik etti�i akut ba��rsak t�kan�kl���n� and�rabilir.
Gastrointestinal advers olaylar�n s�kl���n�n kesintisiz tedavi ile zaman i�erisinde azald��� bilinmektedir.
A��r� duyarl�l�k reaksiyonlar� ve anafilaktik reaksiyonlar
Pazarlama sonras�nda a��r� duyarl�l�k reaksiyonlar� ve alerjik reaksiyonlar bildirilmi�tir. Bu reaksiyonlar meydana geldi�i zaman �o�unlukla deriyi, nadiren a�z� ve solunum yollar�n� etkilemektedir. �zole anafilaktik �ok vakalar� bildirilmi�tir.
Enjeksiyon b�lgesi reaksiyonlar�
A�r�, k�zar�kl�k, hemoraji, ka��nt�, �i�lik veya end�rasyon dahil enjeksiyon b�lgesi ile ili�kili reaksiyonlar SANDOSTAT�N LAR kullanan hastalarda yayg�n olarak bildirilmi�tir; bununla birlikte, bu olaylar vakalar�n �o�unda hi�bir klinik giri�im gerektirmemi�tir.
Metabolizma ve beslenme hastal�klar�
�l��len fekal ya� at�l�m� artabilse de, bug�ne kadar oktreotid ile uzun vadeli tedavinin malabsorpsiyon nedeniyle n�trisyonel eksikli�e yol a�t���na dair bir kan�ta rastlanmam��t�r.
Pankreatik enzimler
�ok nadir durumlarda, SANDOSTAT�N S.C. tedavisinin ilk birka� saati veya g�n� i�inde akut pankreatit bildirilmi� ve ilac�n kesilmesi ile d�zelmi�tir. Ayr�ca, uzun vadeli SANDOSTAT�N S.C. tedavisi g�ren hastalar i�in kolelityaz ile ind�klenen pankreatit bildirilmi�tir.
Kardiyak hastal�klar
Bradikardi, somatostatin analoglar� kullan�m� esnas�nda yayg�n g�r�len bir advers reaksiyondur. Hem akromegali hem de karsinoid sendrom hastalar�nda, QT uzamas�, eksen kaymalar�, erken repolarizasyon, d���k voltaj, R/S ge�i�, erken R dalgas� progresyonu ve spesifik olmayan ST-T dalgas� de�i�iklikleri gibi EKG de�i�iklikleri g�zlenmi�tir. Bu olaylar�n oktreotid asetat ile ili�kisi, bu hastalar�n �o�u altta yatan kardiyak hastal�klara sahip oldu�undan belirlenmemi�tir (bkz. B�l�m 4.4).
Trombositopeni
Trombositopeni pazarlama sonras� deneyimde karaci�er sirozu olan hastalarda �zellikle SANDOSTAT�N (�.V.) tedavisi esnas�nda ve SANDOSTAT�N LAR tedavisi esnas�nda bildirilmi�tir. Tedavi b�rak�ld�ktan sonra d�zelmektedir.
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar / risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr; e- posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35
99)
4.9. Doz a��m� ve tedavisi
S�n�rl� say�da SANDOSTAT�N LAR'�n kazara al�nan a��r� dozlar� rapor edilmi�tir. Dozlar ayda 100 mg ila 163 mg SANDOSTAT�N LAR aras�nda de�i�mektedir. Rapor edilen tek yan etki s�cak basmas�d�r.
Kanser hastalar�n�n ayda 60 mg ve 2 haftada 90 mg'a kadar kulland��� SANDOSTAT�N LAR dozlar� bildirilmi�tir. Genelde dozlar iyi tolare edildiyse de a�a��daki yan etkiler rapor edilmi�tir: s�k idrara ��kma, yorgunluk, depresyon, anksiyete, konsantrasyon eksikli�i.
Doz a��m�nda semptomatik tedavi uygulanmal�d�r.
Ad�m
Bu a�amada hastay� enjeksiyon i�in haz�rlay�n.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grubu: Somatostatin ve analoglar� ATC kodu: H01CB02.Oktreotid, do�al somatostatinin, benzer farmakolojik etkilere sahip olan, ancak etki s�resi �ok daha uzun, sentetik bir oktapeptit t�revidir. Patolojik olarak artm�� bulunan GH ve gastro-entero-pankreatik (GEP) endokrin sistemdeki serotonin ve peptit salg�lanmas�n� inhibe eder.
Hayvanlarda, oktreotid, somatostatine g�re daha g��l� bir GH, glukagon ve ins�lin sal�m� inhibit�r�d�r ve GH ve glukagon supresyonu a��s�ndan daha y�ksek bir se�icili�e sahiptir.
Sa�l�kl� insanlarda oktreotidin, aynen somatostatin gibi a�a��daki inhibit�r etkilere sahip
oldu�u g�sterilmi�tir:
arjinin, efor ve ins�line ba�l� hipoglisemi etkisiyle uyar�lan b�y�me hormonu salg�lanmas�n�
5.2. Farmakokinetik �zellikler
Genel �zellikler:Emilim:
Bir tek intram�sk�ler SANDOSTAT�N LAR enjeksiyonundan sonra serum oktreotid konsantrasyonu, sonraki 1 saat i�inde ge�ici olarak maksimal de�erlere y�kselir ve bunu, oktreotid d�zeylerinin 24 saat i�erisinde �l��lemeyen de�erlere indi�i bir d�nem izler. Birinci g�ndeki bu maksimal d�zeyden sonraki 7 g�n boyunca hemen b�t�n hastalardaki oktreotid d�zeyleri subterap�tik de�erlerde kal�r ve daha sonra tekrar y�kselerek 14. g�n dolay�nda bir plato �izmeye ba�lar ve sonraki 3-4 hafta boyunca nispeten sabit kal�r. 1. g�n elde edilen maksimal d�zey, plato faz�ndakinden daha d���kt�r ve ilk g�n total
dozun en �ok %0,5'i sal�verilir. Yakla��k 42. g�nden sonra oktreotid konsantrasyonlar� yava� yava� azal�r ve bu, dozaj formundaki polimer matriksin terminal par�alanma faz�na e�lik eder.
Akromegali vakalar�nda 10, 20 ve 30 miligraml�k tek doz SANDOSTAT�N LAR uygulamalar�ndan sonraki ortalama oktreotid plato d�zeyleri, s�ras�yla litrede 358, 926 ve 1710 nanogram olarak �l��lm��t�r. 4 hafta arayla yap�lan 3 enjeksiyondan sonra elde edilen kararl� serum d�zeyleri, bu de�erlerden yakla��k 1,6-1,8 kat daha y�ksek olup 20 ve 30 miligraml�k �oklu SANDOSTAT�N LAR enjeksiyonlar�ndan sonra litrede s�ras�yla 1557 ve 2384 nanogram olarak �l��lm��t�r.
Karsinoid t�m�r vakalar�nda 4 hafta arayla uygulanan 10, 20 ve 30 miligraml�k �oklu SANDOSTAT�N LAR enjeksiyonlar�ndan sonra serumdaki ortalama (ve medyan) kararl� oktreotid d�zeyleri de yine doz artt�k�a y�kselmi� ve s�ras�yla litrede 1231 (894), 2620 (2270) ve 3928 (3010) nanogram bulunmu�tur.
Da��l�m:
28 aya kadar SANDOSTAT�N LAR enjeksiyonunu kapsayan bir s�re boyunca ortaya ��kan �rt��en serbest b�rakma profillerine dayanarak, beklenenin �zerinde bir oktreotid birikimi meydana gelmemi�tir.
SANDOSTAT�N LAR enjeksiyonunu izleyen farmakokinetik oktreotid profili, polimer matriksten ger�ekle�en sal�verilmeyi ve bu matriksin biyodegradasyonunu yan�s�t�r. Sistemik dola��ma sal�verildi�inde, oktreotid, subkutan uygulama i�in tarif edilen, bilinen farmakokinetik �zelliklerine g�re da��l�r. Oktreotidin kararl� durumda da��l�m hacmi 0.27 L/kg ve toplam v�cut klirensi 160 mL/dakika'd�r. Plazma protein ba�lama oran� %65'tir ve kan h�crelerine neredeyse hi� ila� ba�lanmaz.
7-17 ya� aras�, ayda bir SANDOSTAT�N LAR 40 mg almakta olan, hipotalamik obeziteli pediatrik hastalardan al�nan s�n�rl� kan �rnekleriyle elde edilen farmakokinetik veriler, ilk enjeksiyondan sonra 1,395 ng/L ve kararl� durumda 2,973 ng/L d�zeyinde ortalama oktreotid �ukur plazma konsatrasyonlar� g�zlendi�ini g�stermektedir. G�n�ll�ler aras�nda y�ksek bir de�i�kenlik g�zlenmektedir.
Kararl� durumdaki �ukur oktreotid konsantrasyonlar�n�n ya� ve VK� (V�cut kitle indeksi) ile korelasyon g�stermedi�i ancak v�cut a��rl���yla (52,3 – 133 kg) orta dereceli bir korelasyon g�sterdi�i belirlenmi� olup, erkek ve kad�n hastalar aras�nda anlaml� derecede farkl� oldu�u, yani kad�n hastalarda yakla��k %17 oran�nda daha y�ksek oldu�u g�r�lm��t�r.
Biyotransformasyon:
Biyotransformasyon ile ilgili ek bir veri yoktur.
Eliminasyon:
Total v�cut klerensi 160 ml/dakikad�r. Do�rusall�k/Do�rusal Olmayan Durum:
28 aya kadar uzayabilen s�reler boyunca 4 haftada bir yap�lan SANDOSTAT�N LAR uygulamalar�ndan sonra v�cutta oktreotid, sal�verme profillerinin �st�ste gelmesiyle beklenenden daha fazla birikmemi�tir.
Hastalardaki karakteristik �zellikler
Bu b�l�me ait bilgi bulunmamaktad�r.
5.3. Klinik �ncesi g�venlilik verileri
Hayvanlarda y�r�t�len akut ve tekrarlanan doz toksikolojisi, genotoksisite, karsinojenisite ve �reme toksikolojisi �al��malar� insanlar i�in spesifik g�venlilik problemi ortaya koymam��t�r.
Hayvanlarda y�r�t�len �reme �al��malar� 1 mg/kg/g�ne varan parental dozlarda oktreotide ba�l� teratojenik, embriyo/f�tal veya di�er �reme etkilerine dair bir kan�t ortaya koymam��t�r. S��an yavrular�nda a��r� farmakodinamik aktivitenin neden oldu�u GH inhibisyonuna ba�l� ve ge�ici �zellikte bir miktar fiziksel b�y�me gerili�i not edilmi�tir (bkz. B�l�m 4.6).
J�venil s��anlarda spesifik �al��malar y�r�t�lmemi�tir. Pre- ve post-natal geli�im �al��malar�nda, t�m gebelik ve laktasyon periyodu boyunca oktreotid verilen di�ilerin F1 d�llerinde azalm�� b�y�me ve olgunla�ma g�zlenmi�tir. Erkek F1 d�ller i�in ge� testis inmesi g�zlenmekle birlikte etkilenmi� F1 erkek yavrular�n fertilitesi normal kalm��t�r. Bu nedenle yukar�da bahsedilen g�zlemler ge�ici olup, GH inhibisyonundan kaynakland�klar� d���n�lmektedir.
Ad�m
Doyurma a�amas�ndan sonra, pistonu sonuna kadar enjekt�re do�ru bast�rd���n�zdan emin olun.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Toz (Flakon):
Poli (DL-laktit-ko-glikolit) Steril mannitol
��z�c� i�eren ��r�nga (parenteral kullan�m):
Sodium karboksimetil sel�loz Mannitol
Poloksamer 188
Enjeksiyonluk su
6.2. Ge�imsizlikler
Ge�imlilik �al��malar� bulunmad���ndan, bu t�bbi �r�n di�er t�bbi �r�nlerle
kar��t�r�lmamal�d�r.
6.3. Raf �mr�
36 ay
Suland�r�ld�ktan sonra saklanmamal�d�r, derhal kullan�lmal�d�r.
6.4. Saklamaya y�nelik �zel tedbirler
2-8 C aras�nda buzdolab�nda saklay�n�z. Dondurmay�n�z. I��ktan korumak i�in flakonu kutunun i�inde saklay�n�z.
SANDOSTAT�N LAR, enjeksiyon g�n� 25°C'nin alt�ndaki oda s�cakl���nda kalabilir.
Ancak s�spansiyon intram�sk�ler enjeksiyondan hemen �nce haz�rlanmal�d�r.
6.5. Ambalaj�n niteli�i ve i�eri�i
Mikrok�reler floroelastomer kapl� bir lastik t�pas� olan, 6 ml'lik, koyu mavi renkli
al�minyum bir ge�me kapak ile yal�t�larak kapat�lm�� bir cam flakon i�indedir.
Ta��y�c� ��zelti iki lastik t�pa ile kapat�lm�� olan (bir �n ve bir piston t�pas�) kullan�ma haz�r dolu bir cam enjekt�r i�inde paketlenmi�tir.
Flakon adapt�r�.
Bir g�venlik enjeksiyon i�nesi [40 mm (1,5 in�), 19 gauge].
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj At�klar�n�n Kontrol� Y�netmeli�i”ne uygun olarak imha edilmelidir.
�LACIN UYGULANMASI �LE �LG�L� B�LG�LER
�r�n�n uygulanmas� ile ilgili daha detayl� bilgi i�in B�l�m 4.2'ye bak�n�z.
SANDOSTAT�N LAR �.M. kullanma talimat�
YALNIZCA DER�N �NTRAM�SK�LER ENJEKS�YON ���ND�R.
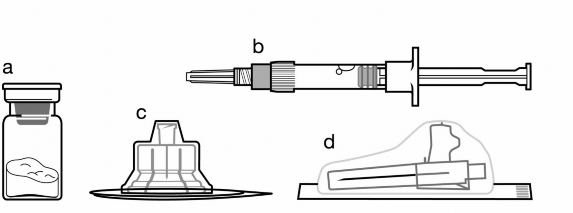
��erik
| |
a | SANDOSTAT�N LAR toz i�eren bir flakon |
b | Bitmi� �r�n� s�spansiyon haline getirmek i�in ta��y�c� ��zeltisini i�eren bir kullan�ma haz�r dolu enjekt�r (2 ml) |
c | Bitmi� �r�n� s�spansiyon haline getirmek haz�rlamak i�in bir flakon adapt�r� |
d | Bir adet 19G x 1,5” g�venlik enjeksiyon i�nesi |
Derin intragluteal (intram�sk�ler) enjeksiyondan �nce SANDOSTAT�N LAR'�n uygun bi�imde haz�rlanmas�n� sa�lamak i�in a�a��daki talimatlar� dikkatle izleyiniz.
SANDOSTAT�N LAR'�n suland�r�larak haz�rlanmas�nda 3 kritik ad�m bulunmaktad�r.
Bunlar�n takip edilmemesi ilac�n uygun �ekilde uygulanamamas�na yol a�abilir.
Enjeksiyon kiti oda s�cakl���na gelmelidir. Enjeksiyon kitini buzdolab�ndan ��kar�n ve suland�rarak haz�rlamadan �nce en az 30 dakika oda s�cakl���nda bekletiniz; fakat 24 saati ge�irmeyiniz.
Ad�m
Enjeksiyon b�lgesini alkoll� bir bezle temizleyin.
 Asperger Sendromu
Asperger sendromu, otistik gurubun bir b�l�m� olan bir �z�rd�r. Bu genelde,
gurubun daha ”y�ksek” taraf�nda yer ald��� d���n�len ki�ilere uygun bir tan�d�r.
Asperger Sendromu
Asperger sendromu, otistik gurubun bir b�l�m� olan bir �z�rd�r. Bu genelde,
gurubun daha ”y�ksek” taraf�nda yer ald��� d���n�len ki�ilere uygun bir tan�d�r. |
 Rahim Boyu ( Serviks ) Kanseri
Rahim boynu (serviks) kanseri 35 ya� alt� kad�nlarda g�r�len vakalarda meme kanserinden
sonra ikinci s�ray� al�r.Serviks kanserinin geli�mesi y�llarca s�rebilir.
Rahim Boyu ( Serviks ) Kanseri
Rahim boynu (serviks) kanseri 35 ya� alt� kad�nlarda g�r�len vakalarda meme kanserinden
sonra ikinci s�ray� al�r.Serviks kanserinin geli�mesi y�llarca s�rebilir. |
 |
Omurilik zedelenmeleri Omurilik zedelenmesini takip eden birka� g�n i�inde, hi�kimse hasarin ne kadar olacagini tahmin edemez. Buradaki sorun, omuriligin herhangi bir zedelenmesinden hemen sonra, bir omurilik sokunun olusmasidir. |
 |
�izofrenlik �izofrenli�in psikiatrik te�hisi hakk�nda �ok fazla anla�mazl�k vard�r. Bu sayfadaki bilgiler, �izofrenli�in te�hisi, nedenleri ve tedavisi hakk�ndaki fakl� teoriler hakk�nda bilgi verecektir. |
 |
Ast�m Ast�ml� ki�ilerin akci�erlerindeki hava borular� (bron�lar) hassast�r. Bu ki�iler belirli tetikleyici fakt�rlere maruz kald�klar�nda, hava borular� nefes almalar�n� g��le�tirecek �ekilde daral�r. |