SPRYTINIB 80 mg film kaplı tablet (30 tablet) Farmakolojik Özellikler
{ Dasatinib }
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Antineoplastik ajanlar, Protein kinaz inhibitörü ATC kodu: L01EA06
Farmakodinami
Dasatinib c-KIT, efrin (EPH), reseptör kinazlar ve PDGFβ reseptörü dahil bir takım başka seçilmiş onkojen kinazlar ile birlikte BCR-ABL kinaz ile SRC ailesi kinazlarının aktivitesini inhibe eder. Dasatinib potensini 0,6-0,8 nM'de gösteren güçlü bir subnanomolar BCR-ABL kinaz inhibitörüdür. BCR-ABL enziminin hem inaktif hem de aktif konformasyonuna bağlanır.
Etki mekanizması
İmatinibe duyarlı ve dirençli hastalık değişkenleri olan lösemi hücresi serilerinde dasatinib in vitro olarak aktiftir. Bu klinik olmayan çalışmalar dasatinibin aşırı BCR-ABL ekspresyonundan, BCR- ABL kinaz parça mutasyonlarından, SRC ailesi kinazları (LYN, HCK) içeren alternatif sinyal yolaklarının aktivasyonundan, ve çoklu ilaç direnç (MDR) geninin aşırı ekspresyonundan kaynaklanan imatinib direncini yenebileceğini göstermektedir. Bundan başka, dasatinib SRC ailesi kinazlarını subnanomolar konsantrasyonda inhibe eder.
In vivo, fare veya sıçan KML modellerinin kullanıldığı ayrı deneylerde dasatinib kronik KML'nin blastik faza progresyonunu engellemiş ve merkezi sinir sistemi dahil farklı yerlerde büyüyen, hastalardan elde edilmiş KML hücresi serilerini taşıyan farelerde sağkalımı uzatmıştır.
Klinik etkililik ve güvenlilik
Faz I çalışmada, tedavi edilen ve 27 ay takip edilen ilk 84 hastada KML'nin tüm fazlarında ve Ph+ ALL'de hematolojik ve sitogenetik yanıtlar gözlenmiştir. Yanıtlar KML ve Ph+ ALL'nin tüm fazlarında sürekli olmuştur.
İmatinibe dirençli olan veya tolere edemeyen kronik, hızlanmış veya miyeloid blastik evredeki KML'li hastalarda dasatinibin güvenlilik ve etkililiğini değerlendirmek üzere dört tek kollu, kontrolsüz, açık Faz II klinik çalışma gerçekleştirilmiştir. Başlangıçta 400 veya 600 mg imatinib tedavisi başarısız olan kronik fazdaki hastalarda bir randomize, karşılaştırmalı olmayan çalışma yürütülmüştür. Başlangıç dozu günde iki kez 70 mg dasatinib idi. Etkinliğin iyileştirilmesi veya toksisitelerin yönetimi için doz değişikliklerine izin verilmiştir (Bkz. Bölüm 4.2).
Günde iki kez uygulanan dasatinibe kıyasla günde bir kez uygulanan dasatinibin etkililiğini değerlendirmek üzere iki randomize, açık etiketli Faz III çalışma yürütülmüştür. Buna ek olarak, yeni kronik faz KML tanısı konmuş yetişkin hastalarda bir açık etiketli, randomize, karşılaştırmalı Faz III çalışma yapılmıştır.
Dasatinibin etkililiği, hematolojik ve sitogenetik yanıt oranlarına dayalıdır.
Yanıt sürekliliği ve tahmini sağkalım oranları, dasatinibin klinik yararı açısından ilave kanıt sağlamaktadır.
Klinik çalışmalarda toplam 2712 hasta değerlendirilmiş olup, bunların %23'ü ≥ 65 yaş ve %5'i ≥ 75 yaşındaydı.
Kronik faz KML – Yeni tanı konmuş
Yeni kronik faz KML tanısı konmuş yetişkin hastalarda bir uluslararası, açık etiketli, çok merkezli, randomize, karşılaştırmalı Faz III çalışma yapılmıştır. Hastalar günde bir kez Dasatinib 100 mg veya günde bir kez imatinib 400 mg almak üzere randomize edilmiştir. Primer sonlanma noktası 12 ay içindeki doğrulanmış tam sitogenetik yanıt oranı (cCCyR) idi. Sekonder sonlanma noktaları cCCyR'de geçen süre (yanıt sürekliliğinin ölçümü), cCCyR'ye kadar geçen süre, majör moleküler yanıt (MMR) oranı, MMR'ye kadar geçen süre, progresyonsuz sağkalım (PFS) ve genel sağkalımdı (OS). Diğer ilişkili etkililik sonuçları CCyR ve tam moleküler yanıt (CMR) oranlarını içermiştir. Çalışma devam etmektedir.
Toplam 519 hasta bir tedavi grubuna randomize edilmiştir: 259'u Dasatinib ve 260'ı imatinib grubuna. Başlangıç özellikleri yaş (medyan yaş Dasatinib grubunda 46 ve imatinib grubunda 49 olup hastaların sırasıyla %10 ve %11'i 65 yaş veya üzerindeydi), cinsiyet (sırasıyla %44 ve %37'si kadın) ve ırk (sırasıyla Beyaz %51 ve %55; Asyalı %42 ve %37) açısından iki tedavi grubu arasında iyi şekilde dengelenmiştir. Başlangıçta, Hasford Skorlarının dağılımı Dasatinib ve imatinib tedavi gruplarında benzerdi (sırasıyla düşük risk: %33 ve %34; orta risk %48 ve %47; yüksek risk:
%19 ve %19).
En az 12 aylık takiple, Dasatinib grubuna randomize olan hastaların %85'i ve imatinib grubuna randomize olan hastaların %81'i halen birinci basamak tedavi almaktaydı. Hastalık progresyonundan dolayı 12 ay içinde tedaviyi kesme oranı Dasatinib grubunda %3 ve imatinib grubunda %5 idi.
En az 60 aylık takiple, Dasatinib grubuna randomize olan hastaların %60'ı ve imatinib grubuna randomize olan hastaların %63'ü halen birinci basamak tedavi almaktaydı. Hastalık progresyonundan dolayı 60 ay içinde tedaviyi kesme oranı Dasatinib grubunda %11 ve imatinib grubunda %14 idi.
Etkililik sonuçları Tablo 2'de sunulmuştur. Tedavinin ilk 12 ayında imatinib grubuna kıyasla Dasatinib grubundaki hastaların istatistiksel olarak anlamlı şekilde daha yüksek bir bölümünde cCCyR elde edilmiştir. Dasatinibin etkililiği, yaş, cinsiyet ve başlangıç Hasford skorları dahil farklı alt gruplarda tutarlı şekilde gösterilmiştir.
Tablo 8: Yeni Tanı Konmuş Kronik Faz KML Hastalarında Yapılan bir Faz 3 Çalışmadan Alınan Etkililik Sonuçları
|
|
![]()
Yanıt oranı (%95 GA)
![]()
Sitogenetik Yanıt
12 Ayda |
|
|
|
cCCyR | %76,8 (71,2-81,8) | %66,2 (60,1-71,9) | p<0,007* |
CCyRP | %85,3 (80,4-89,4) | %73,5 (67,7-78,7) | - |
24 Ayda |
|
|
|
cCCyR | %80,3 | %74,2 | - |
CCyR | %87,3 | %82,3 | - |
36 Ayda |
|
|
|
cCCyR | %82,6 | %77,3 | - |
CCyRP | %88,0 | %83,5 | - |
48 Ayda |
|
|
|
cCCyR | %82,6 | %78,5 | - |
CCyR | %87,6 | %83,8 | - |
60 Ayda |
|
|
|
cCCyR | %83.0 | %78.5 | - |
CCyR %88.0 %83.8 - | |||
Majör Moleküler Yanıt
12 aylık %52,1(45,9-58,3) | %33,8 (28,1-39,9) | p<0,00003* |
24 aylık %64,5(58,3-70,3) %50 (43,8-56,2) -
36 aylık %69,1(63,1- 74,7) | %56,2 (49,9-62,3) |
|
48 aylık %75,7(70,0–80,8) | %62,7 (56,5-68,6) |
|
60 aylık %7Saklamaya yönelik özel tedbirler tedbirler (70.8-81.5) | %64.2% (58.1-70.1) | p=0.0021 |
Risk Oranı (% 99,99GA)(12 aylık) | ||
cCCyR'a kadar geçen süre | 1,55 (1,0-2,3) | p<0,0001* |
MMR'a kadar geçen süre | 2,01 (1,2-3,4) | p<0,0001* |
cCCyR süresi | 0,7 (0,4-1,4) | p<0,035* |
Risk Oranı (%95 GA)(24 aylık) | ||
cCCyR'a kadar geçen süre | 1,49 (1,22-1,82) | - |
MMR'a kadar geçen süre | 1,69 (1,34-2,12) | - |
cCCyR süresi | 0,77 (0,55-1,10) | - |
Risk Oranı (%95 GA)(36 aylık) | ||
cCCyR'a kadar geçen süre | 1,48 (1,22-1,80) | - |
MMR'a kadar geçen süre | - | |
/www.turkiye.go-v.tr/saglik | ||
Risk Oranı (%95 GA)(48 aylık) | ||
cCCyR'a kadar geçen süre | 1,45 (1,20-1,77) | - |
MMR'a kadar geçen süre | 1,55 (1,26-1,91) | - |
cCCyR süresi | 0,81 (0,56-1,17) | - |
Risk Oranı (%95 GA)(60 aylık) | ||
cCCyR'a kadar geçen süre | 1.46 (1.20-1.77) | p=0.0001 |
MMR'a kadar geçen süre | 1.54 (1.25-1.89) | p<0.0001 |
cCCyR süresi | 0.79 (0.55-1.13) | p=0.1983 |
![]()
* Hasford Skoru'na göre ayarlanmış ve istatistiksel önemi önceden belirlenmiş nominal bir önem düzeyine göre gösterilmiştir.
GA = güven aralığı
60 aylık takipten sonra, doğrulanmış CCyR ile cCCyR'ye ulaşmak için gereken medyan süre Dasatinib grubunda 3,1 ay ve imatinib grubunda 5,8 ay olmuştur. 60 aylık takipten sonra, bir MMR olan hastalarda MMR'ye ulaşmak için gereken medyan süre Dasatinib grubunda 9,3 ay ve imatinib gubunda 15,0 ay olmuştur. Bu sonuçlar 12, 24 ve 36. aylarda gözlenen sonuçlarla uyumludur.
MMR'ye kadar geçen süre Şekil 1'de grafik olarak gösterilmektedir. MMR'ye kadar geçen süre dasatinib ile tedavi edilen hastalarda, imatinib ile tedavi edilen hastalara kıyasla tutarlı şekilde daha kısa olmuştur.
Şekil 1. Majör moleküler yanıta (MMR) kadar geçen sürenin Kaplan-Meier kestirimi
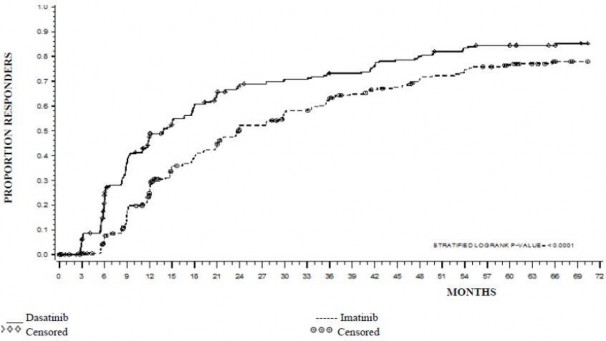
GRUP | # YANIT VERENLER / # RANDOMİZE EDİLENLER | RİSK ORANI (%95 GA) |
Dasatinib | 198/259 |
|
İmatinib | 167/260 |
|
İmatinib karşısında dasatinib |
| 1,54 (1,25 – 1,89) |
Dasatinib ve imatinib tedavi gruplarında sırasıyla 3 ay (%54 ve %30), 6 ay (%70 ve %56), 9 ay
(%75 ve %63), 24 ay (%80 ve %74), 36 ay (%83 ve %77), 48 ay (%83 ve %79) ve 60 ay (%83 ve
%79) içindeki cCCyR oranları primer sonlanma noktası ile uyumluydu. Dasatinib ve imatinib tedavi gruplarında sırasıyla 3 ay (%8 ve %0,4), 6 ay (%27 ve %8), 9 ay (%39 ve %18), 12 ay (%46
ve %28), 24 ay (%64 ve %46), 36 ay (%67 ve %55), 48 ay (%73 ve %60) ve 60 ay (%76 ve %64)
içindeki MMR oranları da primer sonlanma noktası ile uyumluydu.
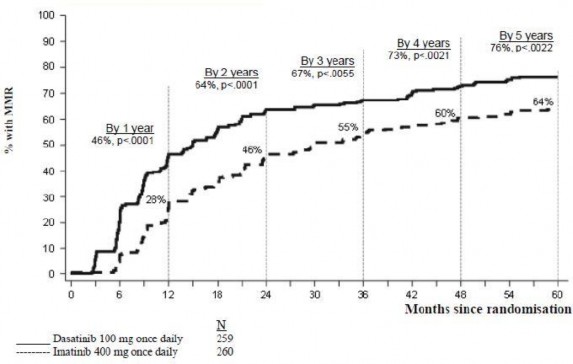
Spesifik zaman noktalarındaki MMR oranları Şekil 2'de grafik olarak gösterilmektedir. MMR oranları dasatinib ile tedavi edilen hastalarda, imatinib ile tedavi edilen hastalara kıyasla tutarlı şekilde daha yüksek olmuştur.
Şekil 2. Zaman içindeki MMR oranları – yeni kronik faz KML tanısı konmuş hastalarda yapılan faz 3 çalışmaya randomize edilen tüm hastalar
Herhangi bir zamanda BCR-ABL oranı ≤ %0,01 (4-log azalma) olan hastaların oranı Dasatinib grubunda, imatinib grubuna kıyasla daha yüksekti (%54,1 karşısında %45). Herhangi bir zamanda
BCR-ABL oranı ≤%0,0032 (4,5-log azalma) olan hastaların oranı Dasatinib grubunda, imatinib grubuna kıyasla daha yüksekti (%44 karşısında %34).
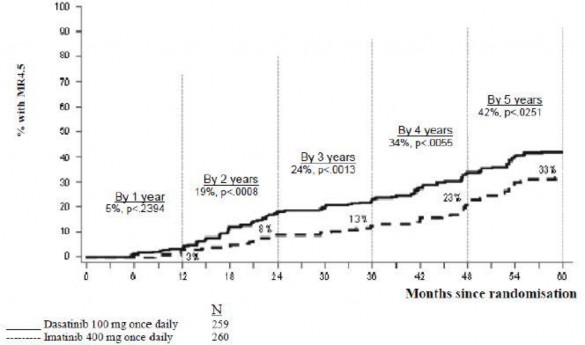
Zaman içindeki MR 4.5 oranları Şekil 3'te grafik olarak gösterilmektedir. MR 4.5 oranları dasatinib ile tedavi edilen hastalarda, imatinib ile tedavi edilen hastalara kıyasla tutarlı şekilde daha yüksek olmuştur.
Şekil 3. Zaman içindeki MR 4,5 oranları–yeni kronik faz KML tanısı konmuş hastalarda yapılan faz 3 çalışmaya randomize edilen tüm hastalar
Hasford skoru ile belirlenen her bir risk grubunda herhangi bir zamandaki MMR oranı imatinib grubuna kıyasla Dasatinib grubunda daha yüksekti (sırasıyla düşük risk: %90 ve %69; orta risk:
%71 ve %65; yüksek risk: %67 ve %54).
Bir ek araştırma analizinde imatinib tedavisi uygulanan hastalarla karşılaştırıldığında (%64) dasatinible tedavi uygulanan daha fazla sayıda hastada (%84) erken moleküler yanıt (3 aylık BCR- ABL seviyelerinin ≤ %10 olması şeklinde tanımlanmıştır) elde edildiği görülmüştür. Tablo 3'de görüldüğü gibi, erken moleküler yanıt elde edilen hastalarda transformasyon riski daha düşük, progresyonsuz sağ kalım (PFS) oranı ile genel sağ kalım (OS) oranı daha yüksekti.
Tablo 9: 3 Aylık BCR-ABL düzeyleri ≤ %10 ve > %10 olan Dasatinib Hastaları
Dasatinib N = 235 | 3 Aylık BCR-ABL Seviyeleri ≤%10 Olan Hastalar | 3 Aylık BCR-ABL Seviyeleri ABL > %10 Olan Hastalar |
60. Ayda transformasyon, n/N(%) | 6/198 (3,0) | 5/37 (13,5) |
60. Ayda PFS Oranı (%95 GA) | %92.0 (89,6, 95.2) | %73.8 (52.0, 86.8) |
60. Ayda OS Oranı (%95 GA) | %93.8 (89.3, 9Saklamaya yönelik özel tedbirler tedbirler%) | %80.6 (63.5, 90.2) |
![]()
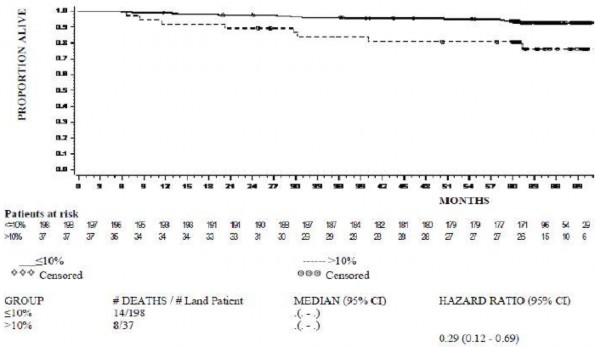
Spesifik zaman noktasıyla OS oranı Şekil 4'te grafikle gösterilmektedir. Dasatinible tedavi uygulanan ve 3 ayda ≤ %10 şeklinde bir BCR-ABL düzeyine ulaşan hastalarda OS oranının ulaşmayanlara kıyasla tutarlı şekilde daha yüksek olduğu görülmüştür.
Şekil 4. Yeni kronik KML tanısı konmuş olan hastalarda yapılan bir faz 3 çalışmada 3. ayda BCR-ABL düzeyine göre (≤ %10 veya > %10) genel sağkalım için sınır noktası grafiği
Hastalık ilerlemesi uygun terapötik idareye karşın akyuvar hücrelerinde artış, CHR, kısmi CyR veya CCyR kaybı, hızlanmış evreye veya blast evresine ilerleme ya da ölüm şeklinde tanımlanmıştır. Tahmin edilen 60 aylık PFS oranı dasatinib ve imatinib tedavi grubunun her ikisi içinde % 88,9dur (GA: %84 - %92,4). 60 ayda, akselere ya da blast faza geçiş dasatinib (n = 8; %3) ile tedavi edilen hastalarda imatinib ile tedavi edilen hastalardan (n = 15; %5) daha seyrek olarak gerçekleşmiştir. Dasatinib ve imatinib ile tedavi edilen vakalardaki tahminî 60 aylık sağkalım oranları sırasıyla %90,9 (GA: %86,6 - %93,8) ve %89,6 (GA: %85,2 - %92,8) olmuştur. Dasatinib and imatinib arasında OS (Risk Oranı 1.01, %95 GA: 0.58-1.73, p= 0.9800) ve PFS (Risk Oranı 1.00, %95 GA: 0.58-1.72, p = 0.9998) açısından herhangi bir fark tespit edilmemiştir.
Yeni kronik faz KML tanısı konmuş hastalarla yürütülen faz III çalışmasında, dasatinib veya imatinib tedavileri kesilen hastalardan alınan kan örneklerinde BCR-ABL sekansı yapılmıştır. Dasatinib alan hastalardaT315I,F317I/LveV299Lmutasyonları saptanmıştır. İmatinib grubunda
farklı bir mutasyon spektrumu saptanmamıştır. In vitro verilere göre, dasatinib, T315I mutasyonuna karşı aktif görünmemektedir.
Kronik faz KML – Önceki İmatinib Tedavisine Direnç ya da İntolerans
İmatinibe dirençli ya da intoleransı olan hastalarda iki klinik çalışma yürütülmüştür; bu çalışmalardaki primer etkinlik sonlandırma kriteri Majör Sitogenetik Yanıttı (MCyR):
Çalışma 1
400 ya da 600 mg imatinib ile başlangıç tedavileri başarısız olan hastalarda açık etiketli, randomize, karşılaştırmalı olmayan çok merkezli bir çalışma yürütülmüştür. Hastalara randomize olarak (2:1) ya dasatinib (günde iki kere 70 mg) ya da imatinib (günde iki kere 400 mg) verilmiştir. Hastada doz değişikliği ile kontrol altına alınmayan hastalık progresyonu veya intoleransa dair bir bulgu olması durumunda, alternatif tedavi koluna geçiş yapılmasına izin verilmiştir. Primer sonlanma noktası 12. haftada MCyR idi. Sonuçlar 150 hasta için mevcuttur:
101 hasta dasatinib ve 49 hasta imatinib koluna randomize edilmiştir (tümü imatinibe dirençli). Teşhisten randomizasyona kadar geçen medyan süre dasatinib grubunda 64 ay ve imatinib grubunda 52 ay olmuştur. Tüm hastalar önceden yoğun tedavi görmüştür. Genel hasta popülasyonunun %93'ü önceden imatinibe tam hematolojik yanıt (CHR) vermiştir. Sırasıyla dasatinib ve imatinib kollarındaki hastalarının %28'inde ve %29'unda önceden imatinibe MCyR görülmüştür.
Medyan tedavi süresi dasatinib için 23 ay (hastaların %44'ü günümüze dek > 24 ay tedavi edilmiştir) ve imatinib için 3 ay (hastaların %10'u günümüze dek > 24 ay tedavi edilmiştir) olmuştur.
Çapraz geçişten önce dasatinib kolundaki hastaların %93'ü ve imatinib kolundaki hastaların
%82'sinde bir CHR elde edilmiştir.
3 aylık takipte dasatinib kolunda (%36) imatinib kolundakinden (%29) daha sık MCyR görülmüştür. Dasatinib kolundaki hastaların %22'sinde tam sitogenetik yanıt (CCyR) rapor edilmiş ancak imatinib kolunda bu oran yalnızca %8 olarak bildirilmiştir. Daha uzun süreli tedavi ve takiple (medyan 24 ay), çaprazlama öncesi Dasatinib ile tedavi edilen hastaların %53'ü (%44'ünde CCyR), imatinib ile tedavi edilenlerin %33'ünde (%18'inde CCyR) McyR'ye ulaşılmıştır. Çalışmaya girmeden önce 400 mg imatinib almış olan hastalar arasında Dasatinib kolunda hastaların %61'inde, imatinib kolunda hastaların %50'sinde MCyR'ye ulaşılmıştır.
Kaplan-Meier'in tahminlerine dayanarak, 1 yıl MCyR devam ettiren hastaların oranı Dasatinib (CCyR %97, % 95 GA: [%92-%100]) için %92 (%95 GA: [%85-%100]) ve imatinib (CCyR %100)
için %74 olmuştur (95% GA: [%49-%100]). MCyR'yi 18 ay boyunca devam ettiren hastaların oranı Dasatinib (CCyR %94, %95 GA: [%87-%100]) için %90 (%95 GA: [%82-%98]) ve imatinib
(CCyR 100%) için %74'tü (%95 GA: [%49-%100]).
Kaplan-Meier'in tahminlerine dayanarak, 1 yıl boyunca ilerleme olmadan hayatta kalan [progression-free survival (PFS)] hastaların oranı Dasatinib için %91 (%95 GA: [%85-%97]) ve imatinib için %73 olmuştur (%95 GA: [%54-%91]). İkinci yılda PFS'ye sahip hastaların oranı Dasatinib için %86 (%95 GA: [%78-%93]) ve imatinib için %65 (%95 GA: [%43-%87]) olmuştur.
Dasatinib kolundaki hastaların toplam %43'ünün ve imatinib kolundakilerin %82'sinin tedavileri başarısız olmuştur; yani, ya hastalıkları ilerlemiştir ya da diğer tedaviye çapraz geçiş yapmışlardır (yanıt alınmadığı, çalışma ilacı tolere edilmediği için vs.)
Çapraz geçiş öncesi majör moleküler yanıt oranları (periferik kan örneklerinde BCR-ABL/kontrol transkriplerinin RQ-PCR ile <% 0,1 olması ile tanımlanır) dasatinib için %29 ve imatinib için %12 olmuştur.
Çalışma 2
İmatinibe intolerans veya direnç geliştiren (yani, imatinib tedavisi sırasında tedaviye devam etmeyi olanaksız hale getiren önemli toksisite geliştiren hastalar) hastalarda açık etiketli, tek kollu, çok merkezli bir çalışma yürütülmüştür.
Toplam 387 hasta (288'i direnç, 99'u intolerans) günde iki kere 70 mg dasatinib almıştır. Teşhisten tedavinin başlangıcına kadar medyan süre 61 ay idi. Direnç geliştiren hastaların çoğu (%72) >600 mg imatinib almıştı. Imatinibe ilaveten, hastaların %35'i daha önce sitotoksik kemoterapi görmüştü, % 65'i daha önce interferon almıştı ve % 10'una önceden kök hücre transplantasyonu yapılmıştı. Başlangıçta hastaların % 38'inin imatinib direncini oluşturan mutasyonları vardı. Dasatinib tedavisinin medyan süresi 24 ay olmuş, hastaların %51'i bugüne kadar > 24 ay tedavi edilmiştir. Majör sitogenetik yanıt (MCyR) imatinibe dirençli hastaların %55'inde, imatinib intolerans hastaların %82'sinde gelişmiştir.
Minimum 24 ay takip süresinde önceden MCyR gösteren 240 hastanın 21'inde ilerleme olmuş ve medyan MCyR süresine ulaşılmamıştır.
Kaplan-Meier'in tahminlerine dayanarak, hastaların %95'i (%95 GA: [%92-%98]) MCyR'yi 1 yıl boyunca ve %88'i (%95 GA: [%83-%93]) 2 yıl boyunca sürdürmüşlerdir. CCyR'yi 1 yıl boyunca sürdüren hastaların oranı %97 (%95 GA: [%94-%99]) ve 2 yıl sürdüren hastaların %90 (%95 GA: [%86-%95]) olmuştur. Daha önce imatinibe karşı hiç MCyR'ye sahip olmayan imatinib dirençli hastaların (n= 188) % 42'si dasatinib ile MCyR'ye ulaşmıştır.
Bu çalışmaya kaydedilen hastaların %38'inde 45 farklı BCR-ABL mutasyonu mevcuttu. T315I hariç olmak üzere imatinib direnci ile ilişkili çeşitli BCR-ABL mutasyonları bulunan hastalarda tam hematolojik yanıt veya MCyR elde edilmiştir. İkinci yılda MCyR oranları, hastalara başlangıç BCR-ABL mutasyonu, P-loop mutasyonu olmasına veya herhangi bir mutasyon bulunmamasına bağlı olmaksızın benzerdi (sırasıyla %63, %61 ve %62).
İmatinibe dirençli hastalar arasında tahmin edilen PFS oranı 1 yılda %88 (%95 GA: [%84-%92]) ve 2 yılda %75'ti (%95 GA: [%69-%81]). İmatinibi tolere edemeyen hastalar arasında tahmin edilen PFS oranı 1 yılda %98 (%95 GA: [%95-%100]) ve 2 yılda %94 (%95 GA: [%88-%99]) olmuştur.
24. ayda majör moleküler yanıt oranı %45 idi (imatinibe dirençli hastalar için %35 ve imatinibi tolere edemeyen hastalar için %74).
Akselere Faz KML
İmatinibe dirençli veya intoleran olan hastalarda açık etiketli, tek kollu, çok merkezli bir çalışma yapılmıştır. Toplam 174 hasta(imatinibdirençli:161,intoleranslı: 13) günde iki kere 70 mg
tedavisinin medyan süresi 14 ay olmuş, hastaların %31'i bugüne kadar > 24 ay tedavi edilmiştir. 24 ayda majör moleküler yanıt oranı %46'dır (Tam sitogenetik yanıtı (CCyR) olan 41 hastada değerlendirilmiştir).
Myeloid Blastik Faz KML
İmatinibe intoleransı veya direnci olan hastalarda açık etiketli, tek kollu, çok merkezli bir çalışma yapılmıştır. Toplam 109 hasta (imatinib direnci: 99, intoleransı: 10) günde iki kere 70 mg dasatinib almıştır. Teşhisten tedavi başlangıcına kadar geçen medyan süre 48 ay olmuştur. Dasatinib tedavisinin medyan süresi 3,5 ay olmuş, hastaların %12'ü bugüne kadar > 24 ay tedavi edilmiştir. 24 ayda majör moleküler yanıt oranı %68'dir (Tam sitogenetik yanıtı (CCyR) olan 19 hastada değerlendirilmiştir. İlave etkililik bulguları Tablo 10'da bildirilmiştir.
Lenfoid Blastik Faz KML ve Ph+ ALL
Daha önceki imatinib tedavisine direnç veya intolerans geliştiren lenfoid blastik faz KML veya Ph+ ALL hastalarında açık etiketli, tek kollu, çok merkezli bir çalışma yapılmıştır. Toplam 48 lenfoid blastik KML hastası (imatinib dirençli: 42, intoleranslı: 6) günde iki kere 70 mg dasatinib almıştır. Teşhisten tedavi başlangıcına kadar medyan 28 ay geçmiştir. Dasatinib tedavisinin medyan süresi 3 ay olmuş, bugüne kadar tedavisi > 24 ay süren hasta oranı %2 olmuştur. 24 ayda majör moleküler yanıt oranı %50'dir (Tam sitogenetik yanıtı (CCyR) olan 22 hastada). Ayrıca 46 Ph+ ALL hastası da günde iki kere 70 mg dasatinib almıştır (imatinibe dirençli: 44, intoleranslı: 2). Teşhisten tedavi başlangıcına kadar medyan 18 ay geçmiştir. Dasatinib tedavisinin medyan süresi 3 ay olup bugüne kadar > 24 ay tedavi edilen hasta oranı %7 olmuştur. 24 ayda majör moleküler yanıt oranı %52'dir (Tam sitogenik yanıtı (CCyR) olan 25 hastada). Majör hematolojik yanıtların (MaHR) çabuk elde edilmiş olması dikkate değerdir (lenfoid blastik KML hastalarında ilk dasatinib uygulamasından itibaren 35 gün, Ph+ ALL hastalarında ise 55 gün içinde).
Tablo 10: Faz II Dasatinib tek kollu klinik çalışmalarında etkililik
![]()
Kronik (N=387) | Hızlanmış (n=174) | Myeloidblast (n=109) | Lenfoid blast (n=48) | Ph+ALL (n=46) | |
Hematolojik yanıt oranı(%) | |||||
MaHR(%95CI) | n/a | %64 (57- 72) | %33 (24- 43) | %35 (22- 51) | %41 (27-57) |
CHR (%95 CI) | %91 (88-94) | %50 (42-58) | %26 (18-35) | %29 (17-44) | %35 (21-50) |
NEL (%95 CI) | n/a | %14 (10-21) | %7 (3-14) | %6 (1-17) | %7 (1-18) |
MaHR süresi (%; Kaplan-Meier kestirimleri) | |||||
1 year | n/a | %79 (71-87) | %71 (55-87) | %29 (3-56) | %32 (8-56) |
2 year | n/a | %60 (50-70) | %41 (21-60) | %10 (0-28) | %24 (2-47) |
Sitogenetik yanıt (%) | |||||
MCyR(%95CI) | %62 (57-67) | %40 (33-48) | %34 (25-44) | %52 (37-67) | %57 (41-71) |
CCyR(%95 CI) | %54 (48-59) | %33 (26-41) | %27 (19-36) | %46 (31-61) | %54 (39-69) |
Sağkalım (%; Kaplan-Meier kestirimleri) | |||||
Progresyonsuz Sağkalım | |||||
2 yıl | %80 (75-84) | %46 (38-54) | %20 (11-29) | %5 (0-13) | %12 (2-23) |
Genel |
|
|
|
|
|
1 yıl | %97 (95-99) | %83 (77-89) | %48 (38-59) | %30 (14-47) | %35 (20-51) |
2 yıl | %94 (91-97) | %72 (64-79) | %38 (27-50) | %26 (10-42) | %31 (16-47) |
![]()
Bu tabloda açıklanan veriler günde iki kez 70 mg'lık başlangıç dozu kullanılan çalışmalardan alınmıştır. Önerilen başlangıç dozu için bölüm 4.2'ye bakınız.
CHR (kronik KML): WBC < kurumsal ULN, trombosit < 450,000 W, periferik kanda blast veya promyelositler yok, periferik kanda < %5 miyelositler + metamiyelositler, periferik kanda <%20 bazofiller ve ekstramedüller tutulum yok.
CHR (ileri evre KML/Ph+ ALL): WBC < kurumsal ULN, ANC >1,000 W, trombosit > 1.000 W, periferik kanda blast veya promyelositler yok, periferik kanda < %5 kemik iliği blastı, <%5 miyelositler + metamiyelositler, periferik kanda <%20 bazofiller ve ekstramedüller tutulum yok.
NEL: CHR ile aynı kriterler ancak ANC > 500W ve < 1,000/mm veya trombosit > 20,000/mm ve
<100,000W.
n/a = geçerli değil; GA = güven aralığı; ULN = normal aralığın üst sınırı.
Dasatinibden sonra kemik iliği transplantı yapılan hastaların sonuçları tam olarak değerlendirilmemiştir.
İmatinibe dirençli veya intoleran olan kronik, akselere ya da myeloid blast faz KML ve Ph+ALL hastalarında Faz III Klinik Çalışmalar
Günde bir kere uygulanan Dasatinib ile günde iki kere uygulanan Dasatinibin etkinliğini değerlendirmek üzere randomize, açık-etiketli iki çalışma yürütülmüştür: Aşağıdaki sonuçlar dasatinib tedavisine başladıktan sonra minimum 2 yıllık ve 7 yıllık takiplere dayanmaktadır.
Çalışma 1
Kronik faz KML çalışmasında, primer sonlandırma kriteri imatinibe dirençli hastalarda MCyR'tır. Başlıca sekonder sonlandırma kriteri imatinibe dirençli hastalarda toplam günlük dozda MCyR'tır. 497'i imatinibe dirençli olan toplam 670 hasta günde bir kere 100 mg, günde bir kere 140 mg, günde iki kere 50 mg ya da günde iki kere 70 mg Dasatinib grubuna randomize edilmiştir. Tüm hastalar için 7 yıllık takipte medyan tedavi süresi 29,8 ay olmuştur (aralık <1-92.9 ay).
Tüm Dasatinib tedavi gruplarında etkinlik elde edilmiştir ve primer sonlanım noktasında günde tek doz uygulaması günde iki kere uygulamaya göre (MCyR farkı %1,9; %95 güven aralığı [-%6,8 -
%10,6]) kıyaslanabilir bir etkinlik (daha az olmayan) göstermiştir. Ancak, günde bir kez 100 mg'lık rejimde güvenlilik ve tolerabilitede artış gözlenmiştir. Etkililik sonuçları Tablo 5 ve 6'de açıklanmaktadır.
Tablo 11: Faz III Doz Optimizasyon Çalışmasında Dasatinibin Etkinliği: İmatinibe Dirençli
veya İntolerant Kronik Faz KML (2 yıllık sonuçlar)
Tüm Hastalar | n=167 |
| |
Imitanibe dirençli hastalar | n=124 |
Hematolojik Yanıt Oranı (%95 GA) |
|
CHR | %92 (86-95) |
Sitogenetik Yanıt (%) (%95 GA) |
|
MCyR |
|
Tüm hastalar | %63 (56-71) |
Imatinibe Dirençli Hastalar | %59 (50-68) |
CCyR |
|
Bütün hastalar | %50 (42-58) |
Imatinibe Dirençli Hastalar | %44 (35-53) |
CCyR Elde Edilen Hastalarda Majör Moleküler Yanıt (%) (%95 GA)
Bütün Hastalar | %69 (58-79) |
İmatinibe Dirençli Hastalar | %72 (58-83) |
![]()
Tam Hematolojik Yanıt (THY) (kronik KML): lökosit ≤ kurum üst sınırı, trombositler <450,000/mm, periferal kanda blast ya da promyelosit yok, periferal kanda <%5 myelosit artı metamyelosit, periferal kanda bazofil <%20 ve hiç bir ekstramedüler tutulum yok.
GA = güven aralığı ULN = Normal Aralığın Üst Sınırı.
Tablo 12: Dasatinibin Faz III Doz Optimizasyonu Çalışmasındaki Uzun Dönemli Etkinliği: İmatinibe Dirençli veya İntolerant Kronik Faz KML Hastaları
Minimum Takip Süresi
1 yıl 2 yıl 5 yıl 7 yıl
Majör Moleküler Yanıt | ||||
Tüm hastalar | Geçerli değil | % 37(57/154) | % 44 (71/160) | % 46 (73/160) |
Imatinibe dirençli hastalar | Geçerli değil | % 35 (41/117) | % 42 (50/120) | % 43 (51/120) |
Imatinibe intoleran hastalar | Geçerli değil | % 43 (16/37) | % 53 (21/40) | % 55 (22/40) |
Progresyonsuz Sağkalım (PFS) | ||||
Tüm hastalar | % 90 (86,95) | % 42 (33, 51) | ||
Imatinibe dirençli hastalar | % 88 (82, 94) | % 77 (68, 85) | % 49 (39, 59) | % 39 (29, 49) |
Imatinibe intoleran hastalar | % 97 (92, 100) | % 87 (76, 99) | % 56 (37, 76) | % 51(32, 67) |
Genel Sağkalım |
|
|
|
|
Tüm hastalar | % 96 (93, 99) | % 91 (86, 96) | % 78 (72, 85) | % 65 (56, 72) |
Imatinibe dirençli hastalar | % 94 (90, 98) | % 89 (84, 95) | % 77 (69, 85) | % 63 (53, 71) |
Imatinibe intoleran hastalar | % 100 (100, 100) | % 95 (88, 100) | % 82 (70, 94) | %70 (52, 82) |
![]()
Çalışma 2 İleri faz KML ve Ph+ ALL çalışmasının primer sonlandırma kriteri MaHR'tı. Toplam 611 hasta ya günde bir kere 140 mg ya da günde iki kere 70 mg Dasatinib grubuna randomize edilmişti. Medyan tedavi süresi yaklaşık 6 aydı (aralık 0,03-31 ay).
Primer etkinlik sonlanım kriterine göre, günde bir kere uygulaması, günde iki kere uygulaması ile karşılaştırılabilir (daha az olmayan) bir etkinlik göstermiştir (MaHR farkı %0,8; %95 güven aralığı [-%7,1-%8,7]) ancak, günde bir kez 140 mg rejimi iyileşmiş güvenlilik ve tolerabilite göstermiştir. Yanıt oranları Tablo 13'te belirtilmektedir.
Tablo 13: Dasatinibin Faz III Doz Optimizasyonu Çalışmasındaki Etkinliği: İleri Faz KML ve Ph+ ALL (2 yıllık sonuçlar)
Günde bir kez 140 mg | Günde iki kez 70 mg | |||||||
|
Akselere (n= 158) | Miyeloid Blast (n= 75) | Lenfoid Blast (n= 33) |
Ph+ALL (n= 40) |
Akselere (n= 159) | Miyeloid Blast (n= 74) | Lenfoid Blast (n= 28) |
Ph+ALL (n= 44) |
MaHY | %66 | %28 | %42 | %38 | %68 | %28 | %32 | %32 |
(%95 GA) | (59-74) | (18-40) | (26-61) | (23-54) | (60-75) | (19-40) | (16-52) | (19-48) |
THY | %47 | %17 | %21 | %33 | %52 | %18 | %14 | %25 |
(%95 GA) | (40-56) | (10-28) | (9-39) | (19-49) | (44-60) | (10-28) | (4-33) | (13-40) |
NEL | %19 | %11 | %21 | %5 | %16 | %11 | %18 | %7 |
(%95 GA) | (13-26) | (5-20) | (9-39) | (1-17) | (11-23) | (5-20) | (6-37) | (1-19) |
MSY | %39 | %28 | %52 | %70 | %43 | %30 | %46 | %52 |
(%95 GA) | (31-47) | (18-40) | (34-69) | (54-83) | (35-51) | (20-42) | (28-66) | (37-68) |
TSY | %32 | %17 | %39 | %50 | %33 | %23 | %43 | %39 |
(%95 GA) | (25-40) | (10-28) | (23-58) | (34-66) | (26-41) | (14-34) | (25-63) | (24-55) |
Hematolojik yanıt kriterleri(bütünyanıtlar4haftadansonra teyid edilmiştir): Majör hematolojik
THY: lökosit ≤ kurumun ULN'si, ANC ≥ 1,000/mm, trombosit ≥ 100,000/mm, periferik kanda blast ya da promiyelosit yok, kemik iliğinde blast ≤ %5, periferik kanda miyelosit artı metamiyelosit < %5, periferik kanda bazofil <%20 ve kemik iliği dışı tutulum yok.
NEL: THY ile aynı kriterler ama ANC ≥ 500/mm ve < 1,000/mm, ya da trombosit ≥ 20,000/mm ve ≤ 100,000/mm
Günde bir defa 140 mg rejimi ile tedavi uygulanan hızlanmış faz CML hastalarında medyan MaHR süresi ve medyan genel sağkalıma ulaşılmamıştır ve medyan PFS'nin 25 ay olduğu tespit edilmiştir.
Günde bir defa 140 mg rejimi ile tedavi uygulanan miyeloid blast fazı CML hastalarında medyan MaHR süresinin 8 ay, medyan PFS'nin 4 ay, medyan genel sağkalımın ise 8 ay olduğu tespit edilmiştir. Günde bir defa 140 mg rejimi ile tedavi uygulanan lenfoid blast fazı CML hastalarında medyan MaHR süresinin 5 ay, medyan PFS'nin 5 ay, medyan genel sağkalımın ise 11 ay olduğu tespit edilmiştir.
Günde bir defa 140 mg rejimi ile tedavi uygulanan Ph+ ALL hastalarında medyan MaHR süresinin 5 ay, medyan PFS'nin 4 ay, medyan genel sağkalımın ise 7 ay olduğu tespit edilmiştir.
Pediyatrik popülasyon
Pediyatrik KML hastaları
İki pediyatrik çalışmada tedavi edilen kronik faz KML'li 130 pediyatrik hastada (biri Faz I, açık etiketli, randomize olmayan doz aralığı bulma çalışması ve diğeri Faz II, açık etiketli, randomize olmayan çalışma), 84 hasta (sadece Faz II çalışmadan kaydedilen) yeni tanı konan kronik faz KML ve 46 hasta (17 hasta Faz I çalışmadan ve 29 hasta Faz II çalışmadan kaydedilmiştir) imatinib ile önceki tedaviye dirençliydi veya bu tedaviyi tolere edememiştir. Kronik faz KML'li 130 pediyatrik hastanın 97'si günde bir kez Dasatinib tablet 60 mg/m2 ile tedavi edilmemiştir (yüksek BSA'lı hastalar için günde bir defa 100 mg'lık maksimum doz). Hastalar hastalık progresyonuna veya kabul edilemez toksisiteye kadar tedavi edilmiştir.
Kilit etkililik sonlanma noktaları şöyleydi: tam sitogenetik yanıt (CCyR), majör sitogenetik yanıt (MCyR) ve majör moleküler yanıt (MMR). Sonuçlar Tablo 14'te gösterilmektedir.
| 3 ay | 6 ay | 12 ay | 24 ay |
CCyR (%95 GA) Yeni tanı konan (N = 51) |
%43,1, (29,3, 57,8) %45,7 |
%66,7 (52,1,79,2) %71,7 |
%96,1 (86,5, 99,5) %78,3 |
%96,1 (86,5,99,5) %82,6 |
Önceki imatinib (N = 46) | (30,9, 61,0)
| (56,5, 84,0)
| (63,6, 89,1)
| (68,6, 92,2) |
MCyR |
Tablo 14: Dasatinib'in kronik faz KML'li pediyatrik hastalarda etkililiği – Minimum takip döneminde zaman içinde kümülatif yanıt
(%95 GA) Yeni tanı konan (N = 51) |
%60,8 (46,1, 74,2) %60,9 |
%90,2 (78,6, 96,7) %82,6 |
%98,0 (89,6, 100) %89,1 |
%98,0 (89,6, 100) %89,1 |
Önceki imatinib (N = 46) | (45,4, 74,9) | (68,6, 92,2) | (76,4, 96,4) | (76,4, 96,4) |
MMR (%95 GA) Yeni tanı konan (N = 51) |
%7,8 (2,2, 18,9) %15,2 |
%31,4 (19,1, 45,9) %26,1 |
%56,9 (42,2, 70,7) %39,1 |
%74,5 (60,4, 85,7) %52,2 |
Önceki imatinib (N = 46) | (6,3, 28,9) | (14,3, 41,1) | (25,1, 54,6) | (36,9, 67,1) |
![]()
Faz I pediyatrik çalışmada, imatinibe dirençli veya tolere edemeyen kronik faz KML'li hastalar arasında en az 7 yıllık takipten sonra, medyan PFS süresi 53,6 ay ve OS oranı %82,4 idi.
Faz II pediyatrik çalışmada, tablet formülasyonu alan hastalarda yeni tanı alan kronik faz KML'li 51 hasta arasında tahmini 24 aylık PFS oranı %94,0 iken (82,6, 98,0) imatinibe dirençli/tolere
edemeyen kronik faz KML'li 29 hastada bu oranı %81,7 (61,4, 92,0) bulunmuştur. 24 aylık takipten sonra, yeni tanı konan hastalarda OS %100 ve imatinibe dirençli/tolere edemeyen hastalara %96,6 idi.
Faz II pediyatrik çalışmada, yeni tanı konan 1 hastada ve imatinibe dirençli/tolere edemeyen 2 hastada hastalık blastik faz KML'ye ilerlemiştir.
Dasatinib oral süspansiyon hazırlamaya yönelik toz formülasyonu alan (72 mg/m2 dozunda) 33 yeni tanı konmuş kronik faz KML'li pediyatrik hasta mevcuttu. Bu doz önerilen doza kıyasla %30 daha düşük maruziyeti temsil etmektedir. Bu hastalarda, CCyR ve MMR 12. ayda CCyR: %87,9 [%95 GA: (71,8-96,6)] ve MMR: %45,5 [%95 GA: (28,1-63,6)] olarak bulunmuştur.
Daha önce imatinib almış olan dasatinib ile tedavi edilen kronik faz KML hastaları arasında, tedavi sonunda şu mutasyonlar tespit edilmiştir: T315A, E255K ve F317L. Ancak, tedaviden önce E255K ve F317L de tespit edilmiştir. Tedavi sonunda yeni tanı konan kronik faz KML hastalarında herhangi bir mutasyon tespit edilmemiştir.
ALL'li pediyatrik hastalar
Dasatinib'in kemoterapi ile kombinasyon halinde etkililiği, yeni tanı konan Ph+ ALL'li bir yaşın üzerindeki hastalarda yapılan bir pivot çalışmada değerlendirilmiştir.
hasta, kemoterapi ile kombinasyon halinde 24 aya varan sürekli doz rejimi ile günlük 60 mg/m2'lik doz almıştır. Hastaların 82'si sadece dasatinib tablet alırken 24 hasta en az bir kez dasatinib oral süspansiyon hazırlamak için toz formülasyonunu almıştır (bunların 8'i sadece dasatinib oral süspansiyon hazırlamak için toz formülasyonunu almıştır). Arka plandaki kemoterapi rejimi AIEOP-BFM ALL 2000 çalışmasında kullanılanla aynıydı (kemoterapötik standart çok ajanlı kemoterapi protokolü). Primer etkililik sonlanma noktası 3 yıllık olaysız sağkalım olup (EFS),
%65,5 olarak bulunmuştur (55,5, 73,7).
Ig/TCR tekrar düzenlemesi ile değerlendirilen minimum rezidüel hastalık (MRD) negativite oranı, konsolidasyon sonunda tedavi edilen tüm hastalarda %71,7 idi. Bu oran değerlendirilebilir Ig/TCR değerlendirmeleri olan 85 hastaya dayandırıldığında, oran %89,4 idi. İndüksiyon ve konsolidasyon sonunda akış sitometrisi ile ölçülen şekilde MRD negativite oranları sırasıyla %66,0 ve %84,0 idi.
5.2. Farmakokinetik özellikler
Genel ÖzelliklerDasatinibin farmakokinetiği 229 yetişkin sağlıklı gönüllülerde ve 84 hastada değerlendirilmiştir.
Emilim:
Oral uygulamayı takiben hastalar dasatinibi hızla absorbe ederler, pik konsantrasyonlar 0,5-3 saatte görülür. Oral uygulamayı takiben, ortalama maruziyette ki artış (EAARÏ„R) günde iki kere 25 mg - 120 mg aralığındaki dozlarda doz artışıyla yaklaşık olarak orantılıdır. Dasatinibin genel ortalama terminal yarılanma ömrü hastalarda yaklaşık 5-6 saattir.
Çok yağlı bir yemekten 30 dakika sonra 100 mg'lık tek bir dasatinib dozu uygulanan sağlıklı gönüllülerde alınan veriler dasatinibin ortalama EAA'ında %14 artış göstermiştir.
Dasatinibden 30 dakika önce yenilen az yağlı bir yemek dasatinibin ortalama EAA'ını %21 arttırmıştır. Gıdaların gözlenen etkileri ilaç alımında klinik açıdan önem taşıyan değişikliklere yol açmamıştır. Dasatinib maruziyetinde görülen değişkenlik, az yağlı (%39 CV) ve çok yağlı yemeğe (%32 CV) kıyasla açlık koşullarında daha yüksektir (%47 CV).
Hasta popülasyonu FK analizine göre, dasatinib maruziyetinde görülen değişkenliğin temelde durumlar arası biyoyararlanım değişkenliğinden (%44 CV) ve daha düşük ölçüde bireyler arası biyoyararlanım değişkenliğinden ve bireyler arası klirens değişkenliklerinden (sırasıyla, %30 ve
%32) kaynaklandığı tahmin edilmiştir. Maruziyetteki durumlar arası rastgele değişkenliğin kümülatif maruziyeti ve etkililik veya güvenliliği etkilemesi beklenmemektedir.
Dağılım:
Hastalarda dasatinibin görünür dağılım hacmi yüksek olup (2,505 L) tıbbi ürünün ekstravasküler yerde yaygın olarak dağıldığını gösterir. In vitro deneyimlere göre, dasatinib klinik olarak önemli konsantrasyonlarda plazma proteinlerine yaklaşık %96 oranında bağlanmaktadır.
Biyotransformasyon:
Dasatinib insanlarda, metabolitlerin oluşumunda görev alan multipl enzimler ile yaygın olarak metabolize edilir. 100 mg [C] işaretli dasatinib uygulanan sağlıklı gönüllülerde plazmada dolaşan radyoaktivitenin %29'u değişmemiş dasatinib olarak bulunmuştur. Plazma konsantrasyonu ve ölçülen in vitro aktivite dasatinibin metabolitlerinin ürünün gözlenen farmakolojisinde majör bir rol oynama olasılıklarının düşükolduğunugöstermektedir.CYP3A4 dasatinibin metabolizmasından
Eliminasyon:
Dasatinibin ortalama terminal yarı ömrü 3 ila 5 saat arasındadır. Ortalama aparent oral klirensi
363.8 L/saattir (% 81.3 CV). Eliminasyon başlıca feçeste, çoğunlukla metabolitler halinde gerçekleşir. Tek doz [ C] işaretli dasatinib verilmesini takiben, dozun yaklaşık %89'u 10 gün içinde atılmış, radyoaktivitenin %4'ü idrarda ve %85'i feçeste bulunmuştur. İdrardaki ve feçesteki değişmemiş dasatinib oranları sırasıyla dozun %0,1'i ve %19'u olmuş, dozun kalanı ise metabolit olmuştur.
Doğrusallık/Doğrusal Olmayan Durum:
Farmakokinetiği yaklaşık olarak doğrusaldır.
Hastalardaki karakteristik özellikler
Yaşlılarda: Yaş, dasatinibin farmakokinetiğini etkilemez. Yaşlı hastalarda doz ayarlamasına gerek yoktur.
Cinsiyet: Cinsiyet, dasatinibin farmakokinetiğini etkilemez. Cinsiyet baz alınarak doz ayarlamasına gerek yoktur.
Pediyatrik hastalar: Pediyatrik hastalarda dasatinibin farmakokinetiği çalışılmamıştır.
Güvenlilik ve etkililik verileri olmadığından, Dasatinib 18 yaşından küçük çocuklarda ve adölesanlarda kullanılması önerilmez (Bkz Bölüm 5.1).
Böbrek yetmezliği: Dasatinib ile böbrek fonksiyonları azalmış olan hastalarda herhangi bir klinik çalışma yapılmamıştır (serum kreatinin konsantrasyonu normal aralığın üst sınırının >1,5 katı olan hastalar çalışmalara alınmamıştır). Dasatinibin ve metabolitlerinin böbrek klerensi < %4 olduğu için, böbrek yetmezliği olan hastalarda total vücut klerensinde bir azalma beklenmez.
Dasatinib ve metabolitleri böbreklerden minimal düzeyde atılmaktadır.
Karaciğer yetmezliği:
Karaciğer yetmezliğinin dasatinibin tek-doz farmakokinetiği üzerine etkileri, 50 mg uygulanan orta düzeyde karaciğer yetmezliği olan 8 hastada ve 20 mg uygulanan şiddetli karaciğer yetmezliği olan 5 hastada, 70 mg uygulanan eşleştirilmiş sağlıklı gönüllülerle karşılaştırılarak değerlendirilmişir. Orta düzeyde karaciğer yetmezliği olan hastalar normal karaciğer fonksiyonu olanlarla karşılaştırıldığında dasatinibin 70 mg doza göre ayarlanmış ortalama C ve EAA değerleri sırasıyla %47 ve %8 oranında azalmıştır. Şiddetli karaciğer yetmezliği olan hastalar normal karaciğer fonksiyonu olan gönüllüler ile karşılaştırıldığında dasatinibin 70 mg doza göre ayarlanmış ortalama C ve EAA değerleri sırasıyla %43 ve %28 oranında azalmıştır. (Bkz Bölüm 4.2 ve 4.4)
Pediyatrik popülasyon
Dasatinib farmakokinetiği lösemi veya solid tümörleri olan 104 pediyatrik hastada değerlendirilmiştir (tablet formülasyonu alan 72 ve oral süspansiyon hazırlamak için toz formülasyonu alan 32).
Yapılan bir pediyatrik farmakokinetik çalışmada, doza göre normalize edilen dasatinib maruziyeti (C, C ve C) kronikfazKML'li21hastavePh+ALL'li 16 hasta arasında benzer olmuştur.
Dasatinib tablet formülasyonunun farmakokinetiği, tekrarlayan veya dirençli lösemili veya solid tümörleri olan 72 pediyatrik hastada günde bir defa 60 ila 120 mg/m2 ve günde iki defa 50 ila 110 mg/m2 arasında değişen oral dozlarda değerlendirilmiştir. Veriler iki çalışmada birleştirilmiştir ve dasatinib'in hızla emildiğini göstermiştir. Ortalama Tmaks 0,5 ve 6 saat arasında gözlenirken ortalama yarı ömür tüm doz ve yaş gruplarında 2 ila 5 saat arasında bulunmuştur. Dasatinibin FK profili, pediyatrik hastalarda maruziyette dozla ilişkili artışla birlikte dozla orantılı olmuştur. Çocuklar ve adölesanlar arasında dasatinib FK profili açısından anlamlı bir fark görülmemiştir. Doza göre normalleştirilmiş dasatinib C, EAA (0-T) ve EAA (INF) parametrelerine ait geometrik ortalamaların farklı doz düzeylerinde çocuklar ve adölesanlar arasında benzer olduğu bulunmuştur. Bir PFK modele dayalı simülasyon, Bölüm 4.2'de tablet için önerilen vücut ağırlığına dayalı dozlamın, 60 mg/m2 tablet formülasyonu ile benzer bir maruziyet sağlayacağını göstermiştir.
5.3. Klinik öncesi güvenlilik verileri
Dasatinibin klinik olmayan güvenlilik profili bir dizi ve farelerde, sıçanlarda, maymunlarda ve tavşanlarda yapılan in vivo ve in vitro çalışmada değerlendirilmiştir.
Primer toksisiteler gastrointestinal, hematopoietik ve lenfoid sistemlerde ortaya çıkmıştır. Bağırsak daima hedeflenen bir organ olduğu için, sıçanlarda ve maymunlarda gastrointestinal toksisite dozu sınırlamıştır. Sıçanlarda eritrosit parametrelerindeki minimal ve hafif düşüşlere kemik iliğindeki değişiklikler eşlik etmiştir; maymunlarda benzer değişiklikler daha düşük bir insidans ile görülmüştür. Sıçanlarda lenfoid toksisite lenf nodüllerinde, dalakta ve timusta lenfoid azalması ve lenfoid organların ağırlıklarında düşüşler ile kendini göstermiştir. Tedavinin kesilmesini takiben gastrointestinal, hematopoetik ve lenfoid sistemlerdeki değişiklikler geri dönüşümlü olmuştur.
9 aya kadar tedavi edilen maymunlarda arka plan böbrek mineralizasyonunda artış ile sınırlı böbrek değişiklikleri gözlenmiştir. Maymunlarda ≥ 15 mg/kg akut tek dozun uygulandığı bir oral çalışmada kütanöz hemoraji gözlenmiş, fakat ne maymunlarda ne de sıçanlarda tekrarlanan dozların uygulandığı çalışmalarda görülmemiştir. Sıçanlarda dasatinib trombosit agregasyonunu in vitro olarak inhibe etmiş ve tırnak eti kanamasını in vivo olarak uzatmıştır. Ancak spontan kanama görülmemiştir.
hERG ve Purkinje lif tayinleri; in vitro dasatinib aktivitesinin kardiyak ventriküler repolarizasyonu (QT aralığı) uzatma potansiyeli olabileceğini göstermiştir. Ancak bilinci açık maymunlarda ölçümlenen bir in vivo tek doz çalışmasında QT aralığında veya EKG dalgası formunda bir değişiklik görülmemiştir.
Dasatinib in vitro bakteri hücresi tayinlerinde (Ames testi) mutajenik ve bir in vivo sıçan mikronükleus çalışmasında genotoksik bulunmamıştır. Bölünmekte olan Çin hamsteri over hücrelerinde in vitro klastojenik etki göstermiştir.
Sıçan fertilitesi ve erken embriyonik gelişimle ilgili konvansiyonel bir çalışmada dasatinib erkek veya dişilerin fertilitesini etkilememiştir ancak insanlardaki klinikte kullanılan doz seviyelerinde embriyoletaliteyi indüklemiştir. Embriyofetal gelişim çalışmalarında dasatinib benzer şekilde, sıçanlarda yavruların boylarındaki düşüş ve hem sıçanlarda hem de tavşanlarda fetüsün iskeletinde farklılıklar ile birlikte olan embriyoletaliteyi indüklemiştir. Bu etkiler maternel toksisiteye yol açmayan dozlarda ortaya çıkmıştır; bu da dasatinibin implantasyondan organojenezin tamamlanmasına kadar geçensüredeselektifreprodüktiftoksik madde olduğunu göstermektedir.
Farelerde dasatinib doza bağlı olan ve doz azaltılarak ve/veya dozaj planı değiştirilerek etkinlikle tedavi edilen immunosupresyonu indüklemiştir. Dasatinib fare fibroblastlarında yürütülen bir in vitro nötral kırmızı uptake fototoksisite tayininde fototoksik potansiyel göstermiştir. Dasatinibin dişi tüysüz farelere tek dozluk oral uygulama sonrası önerilen standard terapötik doz ile insan maruziyetinin 3 katına kadarki maruziyette (EAA'ya göre) in vivo olarak non-fototoksik olarak değerlendirilmiştir.
İki yıllık bir karsinojenisite çalışmasında, sıçanlara günlük 0,3, 1 ve 3 mg/kg dozlarında oral dasatinib uygulanmıştır. En yüksek doz genellikle günlük 100 mg ila 140 mg arasında değişen önerilen başlangıç dozunda insanlarda gözlenen maruziyetle eşdeğer bir plazma maruziyet (EAA) düzeyi ile sonuçlanmıştır. Yüksek doz uygulanan dişilerde uterus ve rahimde skuamöz hücreli karsinomalar ve papillomaların birleşik insidansında ve düşük doz uygulanan erkeklerde prostat adenomalarının insidansında istatistiksel olarak anlamlı bir artış kaydedilmiştir. Sıçanlarda karsinojenisite çalışmalarından elde edilen bu bulguların insanlar için önemi bilinmemektedir.
Dasatinib sıçanlarda klinikte gözlemlenene yakın düzeyde plazma dasatinib maruziyetinin görüldüğü 3 mg/kg/gün dozuna kadar karsinojen olmamıştır.
 Yüksek Tansiyon
Hipertansiyon sürekli anormal derecede yüksek olan kan basıncıdır. Tansiyon
atardamarlarınızdaki kanın basıncıdır.
Yüksek Tansiyon
Hipertansiyon sürekli anormal derecede yüksek olan kan basıncıdır. Tansiyon
atardamarlarınızdaki kanın basıncıdır. |
 Belsoğukluğu, Chlamydia ve Frengi
Belsoğukluğu, bakterilerin sebep olduğu bir enfeksiyondur. Cinsel ilişki
yoluyla bulaşır ve dölyatağı boynunda, idrar yollarında, anüste, makatta ve
boğazda enfeksyona sebep olabilir.
Belsoğukluğu, Chlamydia ve Frengi
Belsoğukluğu, bakterilerin sebep olduğu bir enfeksiyondur. Cinsel ilişki
yoluyla bulaşır ve dölyatağı boynunda, idrar yollarında, anüste, makatta ve
boğazda enfeksyona sebep olabilir. |
İLAÇ GENEL BİLGİLERİ
Dem İlaç San. Tic. Ltd. Şti.
| Satış Fiyatı | 22517.85 TL [ 10 Jan 2025 ] |
| Önceki Satış Fiyatı | 22517.85 TL [ 3 Jan 2025 ] |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Kısıtlanmış Beyaz Reçeteli bir ilaçdır. |
| Barkodu | 8699769090166 |
| Etkin Madde | Dasatinib |
| ATC Kodu | L01EA02 |
| Birim Miktar | 80 |
| Birim Cinsi | MG |
| Ambalaj Miktarı | 30 |
| Antineoplastik ve İmmünomodülatör Ajanlar |
| İthal ( ref. ülke : Fransa ) ve Beşeri bir ilaçdır. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| Eşdeğer bir ilaç bulunamadı |
 |
Travma Sonrası Bunalımı Travmatik bir olay, günlük olağan olayların dışında olan ve kişiyi derinden rahatsız eden bir olaydır.Birçok olay böyle bir etki gösterebilir. |
 |
Doğum Sonrası Depresyonu Doğum sonrası depresyonu, doğumdan sonra her on kadından biri tarafından tecrübe edilen stresli bir durumdur. |
 |
Lösemi Kan Kanseri Lösemi, kan kanseridir ve vücudunun kan oluşturan dokularının hastalanması anlamına gelir. Birçok lösemi türü vardır; bazı lösemi türleri çocuklarda bazıları da yetişkinlerde sık görülür. |