TAGRISSO 80 mg 28 film kaplı tablet Kısa Ürün Bilgisi
{ Mertinib Mesilat }
1. BEŞERİ TIBBİ ÜRÜNÜN ADI
TAGRISSO 80 mg film kaplı tablet
2. KALİTATİF VE KANTİTATİF BİLEŞİM
Etkin madde
Her film kaplı tablet 80 mg osimertinibe eşdeğer 95,4 mg osimertinib mesilat içerir.
Yardımcı maddeler
Yardımcı maddeler için 6.1'e bakınız.
3. FARMASÖTİK FORMU
Film kaplı tablet.
Bir yüzünde “AZ†ve “80†baskısı bulunan, diğer yüzü düz, bej, 7.25 x 14.5 mm, oval, bikonveks tablet.
4. KLİNİK ÖZELLİKLER
4.1. Terapötik endikasyonlar
TAGRISSO monoterapi olarak:
Tam tümör rezeksiyonu ardından ve adjuvan kemoterapi kullanılması halinde adjuvan kemoterapisinin tamamlanmasının ardından tümörlerinde epidermal büyüme faktörü reseptörü (EGFR) ekson 19 delesyonu veya ekson 21 L858R mutasyon pozitifliği tespit edilmiş olan Evre IB -IIIA küçük hücreli dışı akciğer kanseri (KHDAK) olan yetişkin hastaların adjuvan tedavisinde nükse dek veya maksimum 3 yıl süreyle,
Epidermal büyüme faktörü reseptörü (EGFR) ekson 19 delesyonu ve/veya ekson 21 mutasyon pozitifliği tespit edilmiş olan lokal ileri evre veya metastatik küçük hücreli dışı akciğer kanseri (KHDAK) olan yetişkin hastaların birinci basamak tedavisinde ve
Epidermal büyüme faktörü reseptörü (EGFR) T790M mutasyon pozitifliği tespit edilmiş olan, EGFR tirozin kinaz inhibitörü (TKI) tedavisinde veya sonrasında progrese olmuş lokal ileri veya metastatik küçük hücreli dışı akciğer kanseri (KHDAK) olan yetişkin hastaların tedavisinde endikedir.
TAGRISSO kullanan hastalarda progresyon gelişmesi halinde diğer EGFR-TKI'lar kullanılamaz.
4.2. Pozoloji ve uygulama şekli
TAGRISSO tedavisi, antikanser tedavilerinin kullanımında deneyimli bir hekim tarafından başlatılmalıdır.
TAGRISSO kullanılması düşünüldüğünde valide edilmiş bir test yöntemi kullanılarak, adjuvan tedavi için tümör numunelerinde ve lokal ileri veya metastatik hastalık için tümör veya plazma numunelerindeki EGFR mutasyonu durumu belirlenmelidir (bkz. Bölüm 4.4):
Pozoloji/uygulama sıklığı ve süresi:
Önerilen doz, günde bir kez 80 mg osimertinibdir.
Adjuvan tedavi alan hastalar, hastalık tekrarlayana ya da kabul edilemez toksisiteye kadar tedavi görmelidir. 3 yılı aşan tedavi süresi incelenmemiştir.
Lokal ileri veya metastatik akciğer kanseri olan hastalar hastalık progresyonuna ya da kabul edilemez toksisiteye kadar tedavi görmelidir.
Eğer bir TAGRISSO dozu unutulursa, bir sonraki doza 12 saatten fazla bir süre olması durumunda doz telafi edilmelidir.
TAGRISSO, her gün aynı vakitte aç veya tok karnına alınabilir. Doz ayarlamaları
Bireysel güvenlilik ve tolerabiliteye göre dozlamanın durdurulması ve/veya doz azaltılması gerekebilir.
Doz azaltılması gerekirse doz, günde bir kez 40 mg'ye azaltılmalıdır.
Advers reaksiyonlar/toksisiteler için doz azaltma rehberleri Tablo 1'de verilmiştir.
Tablo 1: TAGRISSO için önerilen doz değişiklikleri
Hedef organ | Advers reaksiyon | Doz değişikliği |
Pulmoner | İAH/Pnömonit | TAGRISSO kesilir.(bkz. Bölüm 4.4.) |
Kardiyak | En az 2 ayrı EKG'de 500 milisaniye (msn)'den uzun QTc aralığı | TAGRISSO tedavisine, QTc aralığı 481 milisaniye (msn)'nin altına inene kadar veya başlangıçtaki değere tekrar ulaşılana kadar (başlangıçtaki değer 481 msn ve üzerinde ise) ara verilmeli, sonrasında ise düşük dozda (40 mg) tekrar başlanmalıdır. |
QTc aralığı uzaması ile birlikte ciddi aritmi bulguları/belirtileri | TAGRISSO kalıcı olarak kesilir | |
Diğer | Derece 3 veya daha yüksek advers reaksiyon | TAGRISSO 3 hafta süreyle kullanılmaz |
| Derece 3 veya daha yüksek advers reaksiyonda, 3 haftalık TAGRISSO ara verilmesinden sonra Derece 0-2'ye iyileşme görülürse | TAGRISSO, aynı dozda (80 mg) veya daha düşük bir dozda (40 mg) yeniden başlatılabilir |
Derece 3 veya daha yüksek advers reaksiyonda, 3 haftaya kadar ara verilmesinden sonra Derece 0-2'ye iyileşme görülmezse | TAGRISSO kalıcı olarak kesilir |
EKG: Elektrokardiyogram; QTc: Kalp hızına göre düzeltilmiş QT aralığı; İAH: İnterstisyel akciğer hastalığı
Uygulama şekli:
Bu tıbbi ürün oral yoldan kullanılır. Tablet, bütün olarak suyla yutulmalıdır ve ezilmemeli, bölünmemeli veya çiğnenmemelidir.
Hasta tableti yutamıyorsa, tablet öncelikle 50 ml karbonat içermeyen su içinde dağıtılabilir. Ezmeden suya atılmalı, dağılana kadar karıştırılmalı ve hemen yutulmalıdır. Herhangi bir kalıntının kalmadığından emin olmak için bardağa ek olarak 50 ml su eklenmeli ve sonrasında hemen içilmelidir. Başka bir sıvı eklenmemelidir.
Nazogastrik tüp ile uygulama gerekiyorsa, yukarıdaki ile aynı işlem uygulanmalı ancak ilk dağıtma için 15 ml ve kalıntı yıkaması için 15 ml hacimleri kullanılmalıdır. Ortaya çıkan 30 ml sıvı, nazogastrik tüp imalatçısının talimatlarına göre ve uygun yıkama suyu ile uygulanmalıdır. Dispersiyon ve kalıntılar, tabletlerin suya eklenmesinden sonraki 30 dakika içinde uygulanmalıdır.
Özel popülasyonlara ilişkin ek bilgiler:
Hastanın yaşı, vücut ağırlığı, cinsiyeti, etnik kökeni ve sigara içme durumuna göre dozaj ayarlaması gerekli değildir (bkz. Bölüm 5.2).
Karaciğer yetmezliği
Klinik çalışmalara göre, hafif hepatik yetersizlik (Child Pugh A) veya orta seviyeli hepatik yetersizlik (Child Pugh B) görülen hastalarda herhangi bir doz ayarlaması gerekli değildir. Benzer şekilde hafif karaciğer yetmezliği (toplam bilirubin ≤ normalin üst sınırı (ULN) ve aspartat aminotransferaz (AST) >ULN ya da toplam bilirubin >1,0 ila 1,5x ULN aralığında ve herhangi bir AST) ya da orta düzeyde karaciğer yetmezliği (toplam bilirubin 1,5 ila 3kat ULN aralığında ve herhangi bir AST) olan hastalar için doz ayarlaması önerilmemektedir ancak bu hastalara TAGRISSO uygulanırken dikkatli olunmalıdır. Bu tıbbi ürünün güvenliliği ve etkililiği, şiddetli karaciğer yetmezliği olan hastalarda gösterilmemiştir. Ek veriler elde edilene kadar, şiddetli karaciğer yetmezliği olan hastalarda kullanılması önerilmez (bkz. Bölüm 5.2).
Böbrek yetmezliği
Klinik çalışmalar ve popülasyon PK analizlerine göre hafif, orta ya da ağır böbrek bozukluğu
olan hastalarda doz ayarlamaları gerekli değildir. Bu tıbbi ürünün güvenlilik ve etkililiği son evre böbrek hastalığı bulunan [Cockcroft and Gault denklemi ile hesaplanan kreatinin klirensi (CLcr) 15 mL/dak'dan az] ya da diyaliz altındaki hastalarda ortaya konmamıştır. Ciddi ve son evre böbrek bozukluğu bulunan hastalar tedavi edilirken dikkatli olunmalıdır (bkz. bölüm 5.2).
Pediyatrik popülasyon
TAGRISSO'nun güvenliliği ve etkililiği, 18 yaş altı çocuklarda ve adölesanlarda gösterilmemiştir. Veri bulunmamaktadır.
Geriyatrik popülasyon
Yaşlı hastalar (>65yaş) derece 3 veya daha yüksek advers olaylar gelişmesi açısından daha yüksek risk altında olabilir. Bu hastalarda yakın takip önerilir (bkz. Bölüm 4.8).
4.3. Kontrendikasyonlar
Etkin madde
Sarı Kantaron otu (St. John's Wort), TAGRISSO ile birlikte kullanılmamalıdır (bkz. Bölüm 4.5).
4.4. Özel kullanım uyarıları ve önlemleri
EGFR mutasyon durumunun değerlendirilmesi
KHDAK hastalarında tam tümör rezeksiyonundan sonra adjuvan tedavi olarak TAGRISSO kullanılması düşünüldüğünde, EFGR mutasyonu pozitif durumunun (ekson 19 delesyonları (Ex19del) ya da ekson 21 L858R ikame mutasyonları (L858R)) tedaviye uygunluğu göstermesi önemlidir. Biyopsi ya da cerrahi numunelerinden alınan tümör doku DNA'sı kullanılarak klinik laboratuvarda valide edilmiş bir test gerçekleştirilmelidir.
TAGRISSO'nun, lokal olarak ileri evre veya metastatik KHDAK tedavisi olarak kullanımını değerlendirirken, EGFR mutasyonu pozitif durumunun belirlenmesi önemlidir. Bir doku numunesinden elde edilmiş bir tümör dokusu DNA'sı ya da bir plazma numunesinden elde edilmiş dolaşımdaki tümör DNA'sı (ctDNA) kullanılarak, valide edilmiş bir test gerçekleştirilmelidir.
Doku bazlı veya plazma bazlı bir test kullanılarak EGFR mutasyon durumunun pozitif tespiti (birinci basamak tedavi için aktifleyici EGFR mutasyonları veya EGFR TKI tedavisi esnasında ya da sonrasında progresyonun ardından T790M mutasyonu) TAGRISSO ile tedavi için uygunluğu gösterir.
Ancak plazma-kaynaklı ctDNA testi kullanılırsa ve sonuç negatif ise, plazma-kaynaklı test kullanıldığında görülebilen yanlış negatif sonuçlar potansiyeli nedeniyle mümkün olduğunda doku testi ile tekrarlanması önerilir.
EGFR mutasyon durumunun tespitinde yalnızca faydası kanıtlanmış dayanıklı, güvenilir ve duyarlı testler kullanılmalıdır.
İnterstisyel akciğer hastalığı (İAH)
Klinik çalışmalarda TAGRISSO tedavisi alan hastalarda şiddetli, hayatı tehdit eden veya ölümcül İnterstisyel Akciğer Hastalığı (İAH) ya da İAH-benzeri advers reaksiyonlar (örn., pnömonit) gözlenmiştir. Çoğu vakada tedavi kesildiğinde advers olaylarda gerileme veya iyileşme görülmüştür. Geçmişte İAH, ilaca bağlı İAH, steroid tedavisi gereken radyasyon pnömoniti tıbbi öyküsü ya da klinik olarak aktif İAH'ye ilişkin herhangi bir kanıt bulunan hastalar, klinik çalışmalardan hariç tutulmuştur (bkz. Bölüm 4.8).
İnterstisyel Akciğer Hastalığı (İAH) ya da İAH-benzeri advers reaksiyonlar ADAURA, FLAURA ve AURA çalışmalarında TAGRISSO alan 1479 hastanın %3,7'sinde bildirilmiştir. Lokal ileri veya metastatik tedavide beş ölümcül vaka bildirilmiştir. Adjuvan tedavide ölümcül vakalar bildirilmemiştir. İAH insidansı Japon hastalarda %10,9, diğer Asyalı hastalarda %1,6 ve Asyalı olmayan hastalarda %2,5 olmuştur. (bkz. Bölüm 4.8)
Akut başlangıçlı ve/veya pulmoner belirtilerinde (dispne, öksürük, ateş) açıklanamayan kötüleşme olan hastaların tümünde, İAH'yi dışlamak için dikkatli değerlendirme yapılmalıdır. Bu tıbbi ürünle tedavi, bu belirtilerin araştırılması sürecinde durdurulmalıdır. İAH tanısı konursa, TAGRISSO kesilmeli ve gereken uygun tedavi başlatılmalıdır. TAGRISSO'ya yeniden başlanması, sadece her bir hastadaki yarar ve riskler dikkatlice değerlendirildikten sonra düşünülmelidir.
Stevens-Johnson sendromu
TAGRISSO tedavisi ile ilgili olarak nadiren Stevens-Johnson sendromu (SJS) olgu raporları bildirilmiştir. Tedaviye başlamadan önce hastalara SJS belirti ve semptomları hakkında bilgi verilmelidir. Eğer SJS düşündüren belirti ve semptomlar ortaya çıkarsa derhal TAGRISSO'ya ara verilmeli ya da ilaç bırakılmalıdır.
QTc aralığı uzaması
TAGRISSO ile tedavi uygulanan hastalarda QTc aralığında uzama meydana gelmektedir. QTc aralığında uzama ventriküler taşiaritmi (örneğin torsade de pointes) veya ani ölüm riskinin artmasına neden olabilir. ADAURA, FLAURA veya AURA çalışmalarında aritmik olay bildirilmemiştir (bkz. Bölüm 4.8). İstirahat sırasında elektrokardiyogram (EKG) ile ölçüldüğü üzere ritim ve iletimde klinik olarak önemli anormallikler (örn. 470 ms'den büyük QTc aralığı) sergileyen hastalar bu çalışmalara dahil edilmemiştir (bkz. Bölüm 4.8).
Mümkünse, osimertinibin konjenital uzun QT sendromu olan hastalarda kullanımından kaçınmak gerekir. Konjestif kalp yetmezliği, elektrolit anomalileri olan ya da QTc aralığını uzattığı bilinen tıbbi ürünler kullanan hastalarda periyodik elektrokardiyogram (EKG) ve elektrolit izlemi dikkate alınmalıdır. En az 2 ayrı EKG'de 500 msn'den uzun QTc aralığı gelişen hastalarda, QTc aralığı 481 msn'nin altına düşene ya da başlangıç QTc aralığı 481 msn'ye eşit veya bundan uzunsa başlangıca dönüş görülene kadar tedavi bekletilmeli, daha sonra ise Tablo 1'de anlatılan şekilde azaltılmış dozda TAGRISSO'ya devam edilmelidir. Osimertinib, aşağıdakilerden herhangi biriyle birlikte QTc aralığı uzaması gelişen hastalarda kalıcı olarak kesilmelidir: Torsade de pointes, polimorfik ventriküler taşikardi, ciddi aritmi bulguları/belirtileri.
Kalp kasılmasında değişiklikler
Klinik çalışmalarda TAGRISSO ile tedavi edilen, başlangıçta ve en az bir takipte Sol Ventrikül Ejeksiyon Fraksiyonu (LVEF) değerlendirmesi yapılmış olan hastaların %3.2'sinde (40/1233), LVEF'te 10 yüzdelik puan'a eşit ya da daha fazla azalma ve %50'inin altına düşüş meydana gelmiştir. Kardiyak risk faktörleri bulunan hastalarda ve LVEF'i etkileyebilecek koşullara sahip olanlarda, başlangıçta ve tedavi sırasında LVEF değerlendirmesi de dahil olmak üzere kardiyak takip yapılması düşünülmelidir. Tedavi sırasında anlamlı kardiyak bulguları/belirtileri gelişen hastalarda LVEF değerlendirmesi de dahil olmak üzere kardiyak izlem dikkate alınmalıdır. Adjuvan plasebo kontrollü bir çalışmada (ADAURA), TAGRISSO ile tedavi edilen hastaların %1,6'sında (5/312) ve plasebo ile tedavi edilen hastaların
%1,5'inde (5/331) LVEF'te 10 yüzdelik puan'a eşit ya da daha fazla azalma ve %50'inin altına düşüş görülmüştür
Keratit
ADAURA, FLAURA ve AURA çalışmalarında TAGRISSO ile tedavi edilen 1479 hastanın
%0.7'sinde (n=10) keratit bildirilmiştir. Akut ya da kötüleşen göz inflamasyonu, lakrimasyon, ışığa duyarlılık, bulanık görme, göz ağrısı ve/veya gözde kızarma gibi keratiti düşündüren belirti ve bulguları olan hastalar derhal bir oftalmoloji uzmanına sevk edilmelidir (bkz. Bölüm 4.2 Tablo 1).
Yaş ve vücut ağırlığı
Yaşlı hastalar (>65yaş) veya vücut ağırlığı düşük olan hastalar (< 50 kg) derece 3 veya daha yüksek advers olaylar gelişmesi açısından daha yüksek risk altında olabilir. Bu hastalarda yakın takip önerilir (bkz. Bölüm 4.8).
4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri
Farmakokinetik etkileşimler
Güçlü CYP3A4 indükleyiciler, osimertinib maruziyetini azaltabilir. Osimertinib, meme kanseri direnç protein (BCRP) ve P-glikoprotein substratlarının maruziyetini arttırabilir.
Osimertinib plazma konsantrasyonlarını arttırabilen etkin maddeler
İn vitro çalışmalarda, osimertinibin Faz I metabolizmasının ağırlıklı olarak CYP3A4 ve CYP3A5 aracılığıyla olduğu gösterilmiştir. Hastalarda yapılan bir klinik farmakokinetik çalışmasında, günde iki kez 200 mg itrakonazol (güçlü bir CYP3A4 inhibitörü) ile birlikte uygulamanın osimertinib maruziyeti üzerinde klinik olarak anlamlı bir etkisi olmamıştır (eğri altındaki alan (EAA) %24 artmış ve C%20 azalmıştır). Bu nedenle CYP3A4 inhibitörlerinin, osimertinib maruziyetini etkileme ihtimali düşüktür. Başka katalizleyici enzim tanımlanmamıştır.
Osimertinib plazma konsantrasyonlarını azaltabilen etkin maddeler
Hastalarda yapılan bir klinik çalışmada, rifampisin (21 gün boyunca günlük 600 mg) ile birlikte uygulanan osimertinibin kararlı durum EAA'sı, %78 azalmıştır. Benzer şekilde
AZ5104 metabolitine maruziyet, EAA için %82 ve Ciçin %78 azalmıştır. Güçlü CYP3A indükleyicilerinin (örn., fenitoin, rifampisin ve karbamazepin) TAGRISSO ile birlikte kullanımından kaçınılması önerilir. Orta dereceli CYP3A4 indükleyicileri (örn., bosentan, efavirenz, etravirin, modafinil) de osimertinib maruziyetini azaltabilir ve dikkatli kullanılmalıdır ya da mümkünse birlikte kullanımdan kaçınılmalıdır. Bir TAGRISSO doz ayarlaması önermek için klinik veri mevcut değildir. Sarı Kantaron otu ile birlikte kullanım kontrendikedir (bkz. Bölüm 4.3).
Gastrik asit azaltıcı etkin maddelerin osimertinib üzerindeki etkisi
Klinik farmakokinetik bir çalışmada, omeprazol ile birlikte uygulama, osimertinib maruziyetlerinde klinik olarak önemli değişikliklere yol açmamıştır. Gastrik pH değiştirici ajanlar, TAGRISSO ile birlikte herhangi bir kısıtlama olmadan kullanılabilir.
Plazma konsantrasyonları TAGRISSO nedeniyle değişebilecek etkin maddeler
İn vitro çalışmalara göre, osimertinib BCRP taşıyıcılarının yarışmalı inhibitörüdür.
Bir klinik farmakokinetik çalışmasında, TAGRISSO'nun rosuvastatin (duyarlı BCRP substratı) ile birlikte kullanılması rosuvastatinin EAA ve Cdeğerlerini sırasıyla %35 ve
%72 arttırmıştır. Dağılımı BCRP'ye bağlı ve terapötik indeksi dar olan ilaçları eş zamanlı kullanan hastalar, TAGRISSO kullanırken eş zamanlı kullanılan ilacın maruziyet artışından kaynaklanabilecek tolerabilite değişikliği bulguları açısından yakından izlenmelidir (bkz. Bölüm 5.2).
Bir klinik farmakokinetik çalışmasında, TAGRISSO'nun simvastatin (duyarlı CYP3A4 substratı) ile birlikte kullanılması simvastatinin EAA ve Cdeğerlerini sırasıyla %9 ve %23 azaltmıştır. Bu değişiklikler azdır ve klinik olarak anlamlı gözükmemektedir. CYP3A4 substratları ile klinik farmakokinetik etkileşimleri olasılığı düşüktür. Hormonal kontraseptiflere maruziyet azalması riski hariç tutulamaz.
Klinik bir Pregnan X Reseptörü (PXR) etkileşimi çalışmasında, TAGRISSO'nun feksofenadin (P-gp substratı) ile birlikte uygulanması, feksofenadinin EAA ve Cdeğerini tek bir dozun ardından sırasıyla %56 (%90 GA 35, 79) ve %76 (%90 GA 49, 108), kararlı durumda ise %27
(%90 GA 11, 46) ve %25 (%90 GA 6, 48) artırmıştır. Dağılımları Pgp'ye bağımlı olan ve dar terapötik endekse sahip olan eşzamanlı ilaçlar (örneğin, digoksin, dabigatran, aliskiren) alan hastalar, TAGRISSO alırken eşzamanlı ilaca maruziyette artış meydana gelmesinin bir sonucu olarak değişen tolerabilite belirtileri açısından yakından izlenmelidir (bkz. Bölüm 5.2).
Özel popülasyonlara ilişkin ek bilgiler: Pediyatrik popülasyon
Veri bulunmamaktadır.
4.6. Gebelik ve laktasyon
Genel tavsiyeGebelik kategorisi: D
Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon) Doğurganlık potansiyeline sahip kadınlara, TAGRISSO kullanırken gebe kalmaktan kaçınmaları tavsiye edilmelidir. Hastalara, bu tıbbi ürün ile tedavinin tamamlanmasından sonra aşağıdaki süreler boyunca etkili kontrasepsiyon kullanmaları tavsiye edilmelidir: kadınlar için en az 2 ay ve erkekler için en az 4 ay. Hormonal kontraseptiflerin maruziyet düzeyinde azalma riski hariç tutulamamaktadır.
TAGRISSO, ejekülata geçebilir. Bu nedenle erkeklerin de etkili doğum kontrolü kullanması önemlidir.
Gebelik dönemi
Gebe kadınlarda osimertinib kullanımına ilişkin veri bulunmamaktadır ya da sınırlı miktardır. Hayvanlar üzerinde yapılan araştırmalar üreme toksisitesinin (embriyoletalite, azalmış fetal gelişme ve neonatal ölüm) bulunduğunu göstermiştir (bkz. Bölüm 5.3). Etki mekanizmasına ve klinik öncesi verilere göre osimertinib, gebe kadınlara uygulandığında fetal hasara yol açabilir.
TAGRISSO kadının klinik durumu osimertinib tedavisini gerekli kılmadıkça gebelik döneminde kullanılmamalıdır.
Osimertinib'in gebelik ve/veya fetüs/yenidoğan üzerinde zararlı farmakolojik etkileri bulunmaktadır.
Laktasyon dönemi
Osimertinibin veya metabolitlerinin anne sütüne geçip geçmediği bilinmemektedir. Osimertinibin veya metabolitlerinin hayvan sütüne geçmesine ilişkin bilgiler yetersizdir. Ancak osimertinib ve metabolitleri, emzirilen yavrularda tespit edilmiştir ve yavru büyümesi ve sağkalımı üzerindeki advers etkiler görülmüştür (bkz. Bölüm 5.3). Bu nedenle emzirilen çocuğa olan risk hariç tutulamaz. TAGRISSO tedavisi sırasında emzirme sonlandırılmalıdır.
Üreme yeteneği/Fertilite
TAGRISSO'nun insan fertilitesi üzerindeki etkilerine ilişkin veri yoktur. Hayvan çalışmalarının sonuçları, osimertinibin erkek ve kadın üreme organları üzerinde etkileri olduğunu ve fertiliteyi bozabileceğini göstermiştir (bkz. Bölüm 5.3).
4.7. Araç ve makine kullanımı üzerindeki etkiler
TAGRISSO'nun, araç ve makine kullanımı üzerinde etkisi yoktur ya da var olan etkisi ihmal edilebilir düzeydedir.
4.8. İstenmeyen etkiler
Güvenlilik profilinin özeti
EGFR mutasyonu pozitif KHDAK hastalarında yapılan çalışmalar.
Aşağıda tanımlanan veriler, EGFR mutasyonu pozitif küçük hücreli dışı akciğer kanseri bulunan 1479 hastada TAGRISSO maruziyetini yansıtmaktadır. Bu hastalar üç randomize Faz 3 çalışmada (ADAURA-adjuvan; FLAURA - birinci basamak, ve AURA3 – sadece ikinci basamak,) iki tek-kollu çalışmada (AURAex ve AURA2 – ikinci basamak veya sonrası ve bir Faz 1 çalışmada (AURA1, birinci basamak veya sonrası) günde 80 mg dozunda TAGRISSO
almıştır (bkz. Bölüm 5.1).. Çoğu advers reaksiyonu şiddeti Derece 1 veya 2'ydi. En yaygın bildirilen advers ilaç reaksiyonları (AİR) diyare (%47) ,döküntü (%45), paronişi (%33), cilt kuruluğu (%32) ve stomatit (%24) idi.. Çalışmalar genelinde derece 3 ve derece 4 advers olaylar sırasıyla %10 ve %0.1'idi. Günde bir kez 80 mg TAGRISSO tedavisi alan hastalarda, advers reaksiyonlar nedeniyle doz azaltması hastaların %3,4'ünde yapıldı. Advers reaksiyonlar nedeniyle tedaviyi bırakma %4,8 oranındaydı.
Geçmişinde bir İAH, ilaç kaynaklı İAH, steroid tedavisi gerektiren radyasyon pnömoniti öyküsü olan ya da klinik açıdan aktif herhangi bir İAH kanıtı olan hastalar klinik çalışmalardan dışlanmıştır İstirahat elektrokardiyogramında (EKG) ölçüldüğü üzere klinik açıdan önemli ritim ve ileti anormallikleri olan hastalar (örn. 470 ms'den fazla QTc aralığı) bu çalışmalardan dışlanmıştır Hastalar tarama sırasında ve daha sonra 12 haftada bir LVEF açısından değerlendirilmiştir.
Advers reaksiyonların listesi
Advers reaksiyonlar, mümkün olduğunda ADAURA, FLAURA, AURA3, AURAex, AURA 2 ve AURA1 çalışmalarında günde 80 mg dozunda TAGRISSO alan 1479 EGFR mutasyonu pozitif KHDAK hastasını içeren havuzlanmış bir veri setindeki karşılaştırılabilir advers olay bildirimlerinin insidansı temel alınarak sıklık kategorilerine ayrılmıştır.
Advers reaksiyonlar MedDRA'daki sistem organ sınıfına (SOC) göre verilmiştir. Her sistem organ sınıfı içinde, advers ilaç reaksiyonları, en sık olan reaksiyonlar başta olacak şekilde sıklıklarına göre sıralanmıştır. Her bir sıklık gruplaması içerisinde advers reaksiyonlar azalan ciddiyet sırasında sunulmaktadır. Ek olarak her advers reaksiyon için ilgili sıklık kategorisi CIOMS III kurallarına dayalıdır ve aşağıdaki şekilde tanımlanmaktadır: Çok yaygın (≥ 1/10); yaygın (≥ 1/100 ila < 1/10); yaygın olmayan (≥ 1/1.000 ila < 1/100); seyrek (≥ 1/10.000 ila < 1/1.000); çok seyrek (< 1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
ADAURA, FLAURA ve AURA çalışmalarında bildirilen advers reaksiyonlar
Metabolizma ve beslenme hastalıkları
Çok yaygın: İştah azalması (%19) (%1.1'i derece 3 veya daha yüksek)
Göz hastalıkları
Yaygın olmayan Keratit (%0,7) (%0,1'i derece 3 veya daha yüksek)
Solunum, göğüs hastalıkları ve mediastinal hastalıklar
Yaygın : İnterstisyel akciğer hastalığı (%3,7) (%1,1'iderece 3 veya daha yüksek), Epistaksis (%5)
Gastrointestinal hastalıklar
Çok yaygın : Diyare (% 47) (%1,4'ü derece 3 veya daha yüksek), stomatit (%24) (% 0,5'i derece 3 veya daha yüksek)
Deri ve deri altı doku hastalıkları
Çok yaygın : Döküntü(% 45) (%0,7'si derece 3 veya daha yüksek), cilt kuruluğu (%32) (%0,1'i derece 3 veya daha yüksek), paronişi (%33) (%0,4'ü derece 3 veya daha yüksek), kaşıntı (%17) (%0,1'i derece 3 veya daha yüksek)Yaygın: Alopesi (%4.6), ürtiker (%1.9) (%0.1'i derece 3 veya daha yüksek), palmar-plantar eritrodisestezi sendromu (%1.7)
Yaygın olmayan: Eritema multiforme (%0,35) Kutanöz vaskülit (%0.3)
Seyrek :Stevens-Johnson sendromu (% 0.02)
Kas-iskelet ve bağ dokusu hastalıkları
Seyrek: Miyozit (%0.07)
Araştırmalar
Yaygın olmayan QTc aralığı uzaması (%0,9)
Yaygın: Kan kreatin fosfokinaz yüksekliği (%1.6) (%0,3'ü derece 3 veya daha yüksek)
Bulgular (CTCAE derece kaymalar şeklinde sunulan test sonuçlarına dayalı bulgular) Çok yaygın : Trombosit sayısında azalma (%53) (% 1,2'sinde derece 3 veya daha yüksek), lökosit azalması(% 65) (% 1,2'si derece 3 veya daha yüksek), lenfosit azalması (%62) (% 6,1'inde derece 3 veya daha yüksek), nötrofil azalması (%33) (%3,2'si derece 3 veya daha yüksek)
Yaygın : Kan kreatininin artması (% 9)
![]()
![]()
Seçilmiş olan advers reaksiyonların tanımı İnterstisyel akciğer hastalığı (İAH)
ADAURA, FLAURA ve AURA çalışmalarında, İAH insidansının Japon etnik kökenli hastalarda %11, Japon olmayan Asya etnik kökenli hastalarda %1,6, Asya kökenli olmayan hastalarda ise %2,5 olduğu görülmüştür. İAH veya İAH benzeri advers reaksiyonların başlangıcına kadar geçen medyan süre 84 gün olmuştur (bkz. Bölüm 4.4).
QTc aralığı uzaması
ADAURA, FLAURA ve AURA çalışmalarında yer alan ve TAGRISSO 80 mg ile tedavi uygulanan 1479 hastanın %0,8'inin (n = 12), 500 msn'den daha büyük bir QTc'ye sahip olduğu ve hastaların % 3,1'inde (n = 46) başlangıçtaki QTc'ye kıyasla 60 msn'nin üzerinde artış meydana geldiği bulunmuştur. TAGRISSO ile yapılan bir farmakokinetik / farmakodinamik analizde QTc aralığı uzamasında konsantrasyona bağımlı bir artış
öngörülmüştür. ADAURA, FLAURA veya AURA çalışmalarında QTc ile ilişkili herhangi bir aritmi bildirilmemiştir (bkz. Bölüm 4.4 ve 5.1).
Gastrointestinal etkiler
ADAURA, FLAURA ve AURA çalışmalarında hastaların %47'sinde diyare bildirilmiştir ve bunların %38'inin Derece 1, %7,9'unun Derece 2 ve %1,4'ünün Derece 3 olaylar olduğu belirlenmiştir; Derece 4 veya 5 olay bildirilmemiştir. Hastaların %0,3'ünde dozun azaltılması,
%2'sinde ise doza ara verilmesi gerekmiştir. Dört olay (%0,3) tedavinin bırakılmasına neden olmuştur. ADAURA, FLAURA ve AURA3'te olayın başlamasına kadar geçen medyan süre sırasıyla 22 gün, 19 gün ve 22 gün olmuştur ve Derece 2 olayların medyan süresi sırasıyla 11 gün, 19 gün ve 6 gün olarak belirlenmiştir.
Hematolojik olaylar
TAGRISSO ile tedavi uygulanan hastalarda lökosit, lenfosit, nötrofil ve trombositlere ilişkin medyan laboratuvar sayımlarında erken azalmalar gözlenmiştir fakat bu azalmalar zamanla stabilize olmuş ve normalin alt sınırının üzerinde kalmıştır. Lökopeni, lenfopeni, nötropeni ve trombositopeni advers olayları bildirilmiştir, bunların çoğunun hafif veya orta şiddetli olduğu ve doza ara verilmesine neden olmadığı görülmüştür.
Yaşlılar
ADAURA, FLAURA ve AURA3'te (N = 1479), hastaların %43'ünün 65 yaş ve üstü,
%12'sinin ise 75 yaş ve üstü olduğu belirlenmiştir. Daha genç gönüllülerle (<65) karşılaştırıldığında, 65 yaş ve üzeri daha fazla gönüllü ilaç dozunda değişikliklere (ara verme veya azaltma) neden olan advers reaksiyonlar bildirmiştir (%16'ya karşılık %9). Bildirilen advers olay tiplerinin yaştan bağımsız şekilde benzer olduğu gözlenmiştir. Yaşlı hastalar, genç hastalara kıyasla daha fazla Derece 3 veya üzeri advers reaksiyon bildirmiştir (%13 'e karşılık
%8). Bu gönüllüler ile daha genç gönüllüler arasında etkililik açısından genel bir fark gözlenmemiştir. AURA Faz 2 çalışmalarının analizinde güvenlilik ve etkililik sonuçlarında tutarlı bir model gözlenmiştir.
Düşük vücut ağırlığı
Düşük vücut ağırlığı (<50 kg) olan TAGRISSO 80 mg alan hastalarda daha yüksek vücut ağırlığı olan (≥50 kg) hastalardan daha yüksek frekanslarda derece 3 veya daha yüksek advers olaylar (%46'ya karşı %31) ve QTc uzaması (%12'ye karşı %5) raporlanmıştır.
Şüpheli advers reaksiyonların raporlanması
Ruhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesine olanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu Türkiye Farmakovijilans Merkezi (TÜFAM)'ne bildirilmesi gerekmektedir (www.titck.gov.tr; e-posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz aşımı ve tedavisi
TAGRISSO klinik çalışmalarda, doz sınırlayıcı toksisiteler olmadan günlük 240 mg'ye kadar TAGRISSO tedavisi alan hastalar sınırlı sayıda olmuştur. Bu çalışmalarda, 160 ve 240 mg günlük TAGRISSO dozları ile tedavi edilen hastalarda, 80 mg doza kıyasla bir grup tipik EGFR-TKI'ya bağlı advers olayın (başlıca diyare ve cilt döküntüsü) sıklığında ve şiddetinde artış görülmüştür. İnsanlarda kazara doz aşımına ilişkin deneyim sınırlıdır. Tüm olgular, yanlışlıkla fazladan bir tane günlük TAGRISSO dozu alan izole hasta durumları olmuştur ve
herhangi bir klinik sonuç görülmemiştir.
TAGRISSO doz aşımı durumunda özgün bir tedavi yoktur. Doz aşımından şüphelenilmesi durumunda TAGRISSO bekletilmeli ve semptomatik tedavi başlatılmalıdır.
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Antineoplastik ajanlar, protein kinaz inhibitörleri; ATC kodu: L01EB04.
Etki mekanizması
Osimertinib bir Tirozin kinaz İnhibitörüdür (TKI). Duyarlılaştırıcı mutasyonlar (EGFRm) ve TKI-direnç mutasyonu T790M taşıyan Epidermal Büyüme Faktörü Reseptörlerinin (EGFR) geri dönüşümsüz inhibitörüdür.
Farmakodinamik etkiler
İn vitro çalışmalarda osimertinibin, tamamı klinik olarak geçerli EGFR duyarlılaştırıcı mutasyonu ve T790M mutasyonu olan küçük hücreli dışı akciğer kanseri (KHDAK) hücre dizisi aralığında EGFR'ye karşı yüksek potensi ve inhibitör aktivitesi olduğu gösterilmiştir (belirgin IC'ler 6 nM ila 54 nM arasında, fosfo-EGFR'ye karşı). Bu, hücre büyümesinde inhibisyona neden olur ancak doğal-tip hücre dizilerinde EGFR'ye karşı anlamlı düzeyde daha az aktivite gösterir (belirgin IC'ler 480 nM ila 1,8 μM arasında, fosfo-EGFR'ye karşı). Osimertinibin in vivo oral uygulanması, EGFRm ve T790M KHDAK ksenogreft ve transgenik fare akciğer tümörü modellerinde tümör küçülmesi sağlamıştır.
Kardiyak elektrofizyoloji
TAGRISSO'nun QTc aralığını uzatma potansiyeli, AURA2'de günlük 80 mg osimertinib alan
210 hastada değerlendirilmiştir. Osimertinibin QTc aralıkları üzerindeki etkisini değerlendirmek için tek dozu takiben ve kararlı durumda seri EKG'ler çekilmiştir. Yapılan bir farmakokinetik/farmakodinamik analizde, 80 mg'nin ilaç-ilişkili QTc aralığı uzatmasının 14 msn ve üst sınırının 16 msn (%90 GA) olduğu predikte edilmiştir.
Klinik etkililik ve güvenlilik
Daha önceki adjuvan kemoterapi olsun ya da olmasın EGFR mutasyonu pozitif KHDAK'nin adjuvan tedavisi, - ADAURA
Önceden adjuvan kemoterapi ile veya olmadan tam tümör rezeksiyonu geçirmiş EGFR mutasyonu pozitif (Ex19del veya L858R) KHDAK hastalarının adjuvan tedavisi için TAGRISSO'nun etkililiği ve güvenliliği, randomize, çift kör, plasebo kontrollü bir çalışmada kanıtlanmıştır (ADAURA).
Evre IB - IIIA rezeke edilebilir tümörleri bulunan uygun hastaların (Amerikan Ortak Kanser Komisyonu [AJCC] 7. baskıya göre), merkezi bir laboratuvarda biyopsi veya cerrahi numune kullanılarak prospektif olarak gerçekleştirilen cobas EGFR Mutasyon Testi ile tanımlanan EGFR mutasyonlarının (Ex19del veya L858R) bulunması gerekiyordu.
Hastalar, ameliyattan ve uygulanması halinde standart adjuvan kemoterapiden sonra TAGRISSO (n = 339, günde bir defa 80 mg oral) veya plasebo (n = 343) alacak şekilde 1:1
oranında randomize edilmiştir. Adjuvan kemoterapi almayan hastalar 10 hafta içinde ve adjuvan kemoterapi alan hastalar cerrahiyi takip eden 26 hafta içinde randomize edilmiştir. Randomizasyon, EGFR mutasyon tipi (Ex19del veya L858R), etnik köken (Asyalı veya Asyalı olmayan) ve AJCC 7. baskıya göre perkütan transtorasik iğne biyopsisine (pTNM) (IB veya II veya IIIA) dayalı evreleme ile katmanlandırılmıştır. Tedavi, hastalığın nüksetmesine, kabul edilemez toksisiteye kadar veya 3 yıl süreyle uygulanmıştır.
Ana etkililik sonuç ölçütü evre II-IIIA popülasyonunda araştırmacı değerlendirmesine göre hastalıksız sağkalımdır (DFS). Evre IB-IIIA popülasyonunda (genel popülasyon) araştırmacı değerlendirmesine göre DFS ek etkililik sonucu ölçütüdür. Diğer ek etkililik sonucu ölçütleri arasında DFS oranı, genel sağkalım (OS), OS oranı ve sağlıkla ilişkili yaşam kalitesinde (HRQoL) SF-36'da bozulmaya kadar geçen süre yer almaktadır.
Genel popülasyonun başlangıçtaki demografik özellikleri ve hastalık karakteristikleri şu şekildeydi: medyan yaş 63 (aralık 30-86), ≥75 yaş (%11), kadın (%70), Asyalı (%64), hiç
sigara kullanmamış (%72), Dünya Sağlık Örgütü (WHO) performans durumu 0 (%64) veya 1 (%36), evre IB (%31), evre II (%34) ve IIIA (%35). EGFR mutasyonu durumu açısından
%55'i ekson 19 delesyonu ve %45'i ekson 21 L858R ikame mutasyonlarıydı; 9 (%1) hastada aynı zamanda eşzamanlı de novo T790M mutasyonu vardı. Hastaların büyük çoğunluğu (%60) randomizasyondan önce adjuvan kemoterapi almıştır (%26 IB; %71 IIA; %73 IIB;
%80 IIIA). Veri kesim tarihinde, 205 (%61) hasta halen aktif olarak tedavi görüyordu; 3 yıllık tedavi süresini tamamlama fırsatı bulan 73 (%11) hastadan 40'ı (%12) osimertinib kolunda ve 33'ü (%10) plasebo kolundaydı.
TAGRISSO ile hastalığı nükseden 37 hasta vardı. Nüksün en sık bildirildiği bölgeler şunlardı: akciğer (19 hasta); lenf nodları (10 hasta) ve MSS (5 hasta). Plasebo ile hastalığı nükseden 157 hasta vardı. En sık bildirilen bölgeler şunlardı: akciğer (61 hasta); lenf nodları (48 hasta) ve MSS (34 hasta).
ADAURA, evre II-IIIA popülasyonunda plasebo ile tedavi edilen hastalara kıyasla TAGRISSO ile tedavi edilen hastalar için hastalık nüksü veya ölüm riskinde istatistiksel olarak anlamlı bir azalma göstermiştir. Evre IB-IIIA popülasyonunda da benzer sonuçlar gözlenmiştir. DFS analizi sırasında genel sağkalım (OS) verileri olgun değildi. Araştırmacı değerlendirmesine göre ADAURA'dan elde edilen etkililik sonuçları Tablo 2'de özetlenmiştir.
Tablo 2: Araştırmacı değerlendirmesine göre ADAURA çalışmasından elde edilen etkililik sonuçları
| Evre II-IIIA popülasyonu | Evre IB-IIIA popülasyonu | ||
Etkililik Parametreleri | TAGRISSO (N=233) | Plasebo (N=237) | TAGRISSO (N=339) | Plasebo (N=343) |
Hastalıksız Sağkalım (DFS) | ||||
Olay sayısı (%) | 26 (11) | 130 (55) | 37 (11) | 159 (46) |
Rekürren hastalık (%) | 26 (11) | 129 (54) | 37 (11) | 157 (46) |
Ölümler (%) | 0 | 1 (0,4) | 0 | 2 (0,6) |
Medyan, ay (%95 GA) | NC (38,8, NC) | 19,6 (16,6, 24,5) | NC (NC, NC) | 27,5 (22,0, 35,0) |
| Evre II-IIIA popülasyonu | Evre IB-IIIA popülasyonu | ||
Etkililik Parametreleri | TAGRISSO (N=233) | Plasebo (N=237) | TAGRISSO (N=339) | Plasebo (N=343) |
HR (%99,06 GA); P-değeri | 0,17 (0,11, 0,26); < 0,0001 | 0,20 (0,14, 0,30); < 0,0001 | ||
12 ayda DFS oranı (%) (%95 GA) | 97 (94, 99) | 61 (54, 67) | 97 (95, 99) | 69 (63, 73) |
24 ayda DFS oranı (%) (%95 GA) | 90 (84, 93) | 44 (37, 51) | 89 (85, 92) | 52 (46, 58) |
36 ayda DFS oranı (%) (%95 GA) | 78 (65, 87) | 28 (19, 38) | 79 (69, 86) | 40 (32, 48) |
HR = Tehlike Oranı; GA= Güven Aralığı, NC = Hesaplanamaz Araştırmacı değerlendirmesine dayanan DFS sonuçları
HR <1 TAGRISSO lehinedir
TAGRISSO alan hastalar için DFS medyan takip süresi 22,1 ay, plasebo alan hastalar (evre II-IIIA popülasyonu) için 14,9 ay ve plasebo alan hastalar (evre IB-IIIA popülasyonu) için 16,6 aydı.
Şekil 1: Araştırmacı değerlendirmesine göre evre II-IIIA hastalarda Kaplan-Meier Hastalıksız Sağkalım Eğrisi
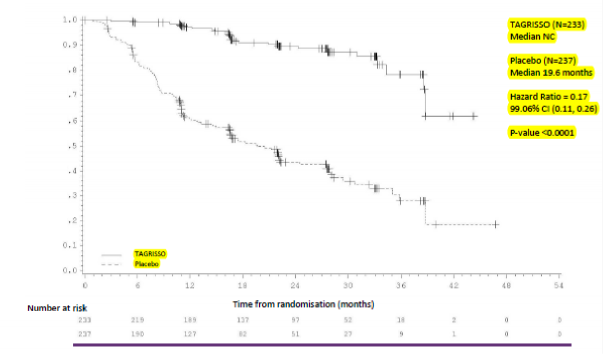
Şekil 2: Araştırmacı değerlendirmesine göre evre IB-IIIA hastalarda (genel popülasyon) Kaplan-Meier Hastalıksız Sağkalım Eğrisi
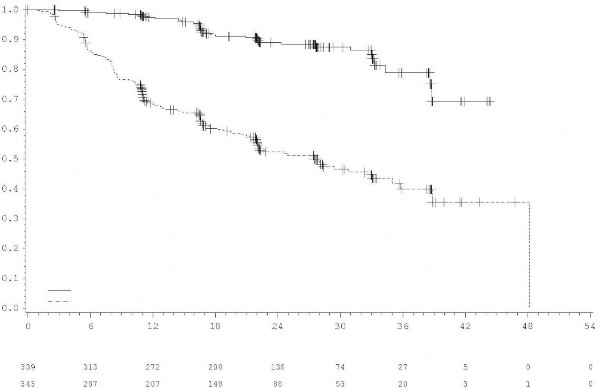
Plaseboya kıyasla TAGRISSO'nun DFS yararı, etnik köken, yaş, cinsiyet ve EGFR mutasyon tipi (Ex19Del veya L858R) dahil olmak üzere analiz edilen tüm önceden tanımlanmış alt gruplarda tutarlıydı.
Plasebo alan hastalara kıyasla TAGRISSO kullanan hastalar için MSS DFS'nin (MSS nüksüne veya ölüme kadar geçen süre) keşifsel bir analizinde genel popülasyon (evre IB-IIIA) için HR'nin 0,18 (%95 GA: 0,10, 0,33; p <0,0001) olduğu görülmüştür.
Hasta Tarafından Bildirilen Sonuçlar
ADAURA'da sağlıkla ilişkili yaşam kalitesi (HRQL), Kısa Form (36) Sağlık Araştırması versiyon 2 (SF-36v2) anketi kullanılarak değerlendirilmiştir. SF-36v2, 12. haftada, 24. haftada ve tedavi tamamlanana veya kesilene kadar randomizasyona göre her 24 haftada bir uygulanmıştır. Genel olarak, HRQL her iki kolda da 30 aya kadar korunmuş olup, evre II-IIIA popülasyonundaki hastaların en az %70'inde SF-36'nın fiziksel bileşeninde klinik olarak anlamlı bir bozulma ya da ölüm (plasebo karşısında TAGRISSO için %76'ya karşılık %70) veya SF-36'nın zihinsel bileşeninde klinik olarak anlamlı bir bozulma ya da ölüm meydana gelmemiştir (plasebo karşısında TAGRISSO için %71'e karşılık %70).
Daha önce tedavi uygulanmamış EGFR mutasyonu pozitif lokal olarak ilerlemiş veya metastatik KHDAK – FLAURA
Daha önce ilerlemiş hastalık için sistemik tedavi uygulanmamış EGFR mutasyonu pozitif lokal ileri, küratif cerrahi ya da radyoterapiye uygun olmayan, veya metastatik KHDAK görülen hastaların tedavisinde TAGRISSO'nun etkililiği ve güvenliliği randomize, çift kör, aktif kontrollü bir çalışmada (FLAURA) ortaya konmuştur. Hastanın tümör dokusu numunelerinin yerel veya merkezi testlerle tespit edildiği üzere EGFR TKI duyarlılığı ile ilişkili olduğu bilinen iki yaygın EGFR mutasyonundan birine (Ex19del veya L858R) sahip olması gerekmiştir.
Hastalar TAGRISSO (n=279, günde bir defa oral yolla 80 mg) veya EGFR TKI karşılaştırma ilacı (n=277; günde bir defa oral yolla 250 mg gefitinib veya günde bir defa oral yolla 150 mg erlotinib) almak üzere 1/1 oranında randomize edilmiştir. Randomizasyon EGFR mutasyonu tipine (Ex19del veya L858R) ve etnisiteye (Asyalı olanlar veya olmayanlar) göre basamaklandırılmıştır. Hastalar tedaviye intolerans ortaya çıkana veya araştırmacı tarafından hastanın artık klinik yarar görmüyor olduğunda karar verilene kadar çalışma tedavisi almıştır. EGFR TKI karşılaştırma ilacı alan hastalarda tümör numunelerinin T790M mutasyonu açısından pozitif sonuç vermesi koşuluyla progresyon sonrası açık etiketli TAGRISSO'ya çaprazlama yapılmasına izin verilmiştir. Primer etkililik sonlanım noktası araştırmacı tarafından değerlendirilen progresyonsuz sağkalım (PFS) olarak belirlenmiştir.
Genel çalışma popülasyonunun başlangıçtaki demografik özellikleri ve hastalık karakteristikleri şöyledir: medyan yaş 64 (aralık 26-93), ≥75 yaş (%14), kadın (%63), Beyaz (%36), Asyalı (%62), hiç sigara kullanmamış (%64), Dünya Sağlık Örgütü (WHO) performans durumu 0 veya 1 (%100), metastatik kemik hastalığı (%36), ekstra-torasik viseral metastazlar (%35), MSS metastazları (%21, başlangıçta MSS lezyonu, tıbbi öykü ve/veya daha önce MSS metastazları için cerrahi ve/veya daha önce radyoterapi uygulanmış olması ile tanımlanan).
TAGRISSO, EGFR TKI komparatörüne kıyasla PFS'de klinik açıdan anlama sahip ve
istatistiksel olarak anlamlı bir iyileşme ortaya koymuştur (sırasıyla medyan 18,9 ay ve 10,2 ay, HR=0,46, %95 GA: 0,37,0,57; P<0,0001). Araştırmacı değerlendirmesine göre FLAURA'dan elde edilen etkililik sonuçları Tablo 3'de özetlenmiştir ve PFS'ye ilişkin Kaplan-Meier eğrisi Şekil 3'de gösterilmektedir. Genel sağkalıma ilişkin nihai analizde (%58 olgunluk) EGFR TKI komparatörüne kıyasla TAGRISSO'ya randomize edilen hastalarda 0.799 HR (% 95,05 GA, 0,641, 0,997) ile istatistiksel olarak anlamlı bir iyileşme ve klinik olarak anlamlı daha uzun medyan sağkalım süresi gösterilmiştir. 12., 18., 24. ve 36. ayda hayatta olanların oranının TAGRISSO ile tedavi uygulanan hastalarda (sırasıyla %89, %81,
%74 ve %54) EGFR TKI komparatörü ile tedavi uygulanan hastalardakine kıyasla (sırasıyla
%83, %71, %59 ve %44) daha yüksek olduğu belirlenmiştir. Progresyon sonrası sonlanım noktaların analizi, PFS yararının takip eden tedavi basamaklarında da korunduğunu göstermiştir.
Tablo 3. Araştırmacının değerlendirmesine göre FLAURA'nın etkililik sonuçları
Etkililik Parametresi |
TAGRISSO (N=279) | EGFR TKI karşılaştırma ilacı (gefitinib veya erlotinib) (N=277) |
Progresyonsuz Sağkalım | ||
Olay sayısı (%62 olgunluk) | 136 (49) | 206 (74) |
Medyan, ay (%95 GA) | 18.9 (15.2, 21.4) | 10.2 (9.6, 11.1) |
HR (%95 GA); P değeri | 0.46 (0.37, 0.57); P<0.0001 | |
Genel Sağkalım | ||
Ölümlerin sayısı, (%58 olgunluk) | 155 (56) | 166 (60) |
Ay olarak medyan OS (%95 GA) | 38.6 (34.5, 41.8) | 31.8 (26.6, 36.0) |
HR (%95.05 GA); P değeri | 0.799 (0.641, 0.997); P=0.0462 ) | |
Objektif Yanıt Oranı⃰ | ||
Yanıt sayısı (n), % Yanıt Oranı (%95 GA) | 223 80 (75, 85) | 210 76 (70, 81) |
Odds oranı (%95 GA); P değeri | 1.3 (0.9, 1.9); P=0.2421 | |
Etkililik Parametresi |
TAGRISSO (N=279) | EGFR TKI karşılaştırma ilacı (gefitinib veya erlotinib) (N=277) |
Yanıt Süresi (DoR)⃰ | ||
Medyan, Ay (%95 GA) | 17.2 (13.8, 22.0) | 8.5 (7.3, 9.8) |
İlk takip eden tedavinin başlangıcından sonra ikinci PFS (PFS2) | ||
İkinci progresyonun gözlendiği hastaların sayısı (%) | 73 (26) | 106 (38) |
Medyan PFS2, Ay (%95 GA) | NC (23.7, NC) | 20.0 (18.0 NC) |
HR (%95 GA); P değeri | 0.58 (0.44, 0.78); P=0.0004 | |
Randomizasyondan takip eden ilk tedaviye veya ölüme kadar geçen süre (TFST) | ||
Takip eden ilk tedaviyi gören veya ölen hastaların sayısı (%) | 115 (41) | 175 (63) |
Medyan TFST, ay (%95 GA) | 23.5 (22.0, NC) | 13.8 (12.3, 15.7) |
HR (%95 GA); P değeri | 0.51 (0.40, 0.64); P<0.0001 | |
Randomizasyondan takip eden ikinci tedaviye veya ölüme kadar geçen süre (TSST) | ||
Takip eden ikinci tedaviyi gören veya ölen hastaların sayısı (%) | 75 (27) | 110 (40) |
Medyan TSST, ay (%95 GA) | NC (NC, NC) | 25.9 (20.0, NC) |
HR (%95 GA); P değeri | 0.60 (0.45, 0.80); P=0.0005 | |
HR=Tehlike oranı; GA=Güven aralığı, NC=Hesaplanabilir değil, PFS, ORR, DOR ve PFS2 sonuçları RECIST araştırmacı değerlendirmesini temel almaktadır
Doğrulanmış olmayan yanıta göre
Medyan takip süresinin TAGRISSO alan hastalar için 15,0 ay, EGFR TKI karşılaştırma ilacı alan hastalar içinse 9,7 ay olduğu hesaplanmıştır.
TAGRISSO alan hastalarda medyan sağkalım takip süresi 35.8 ay ve EGFR TKI karşılaştırıcısı alan hastalar için 27.0 aydı.
PFS, ORR, DoR, PFS2, TFST ve TSST sonuçları 12 Haziran 2017 tarihli veri kesiminden
alınmıştır. Genel sağkalım sonuçları 25 Haziran 2019 tarihli veri kesiminden alınmıştır.
< 1'lik bir HR TAGRISSO lehinedir, >1'lik bir Odds oranı TAGRISSO lehinedir
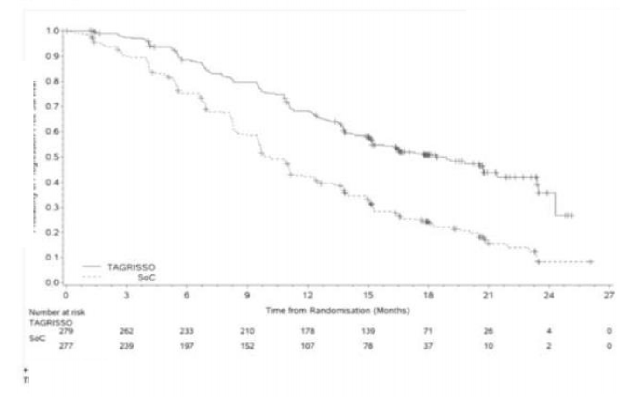
Şekil 3: FLAURA'da araştırmacı tarafından değerlendirilen Progresyonsuz Sağkalımın Kaplan-Meier Eğrileri
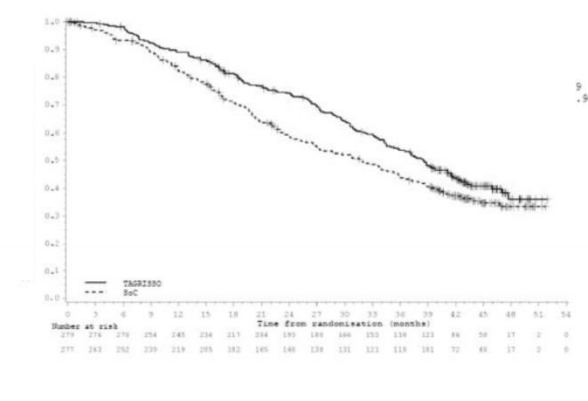
Şekil 4: FLAURA'da Genel Sağkalımın Kaplan-Meier Eğrileri
TAGRISSO'nun EGFR TKI karşılaştırma ilacına kıyasla PFS açısından sağladığı yararın etnisite, yaş, cinsiyet, sigara kullanımı öyküsü, çalışmaya girişteki MSS metastazı durumu ve EGFR mutasyonu tipinin (Ekson 19 delesyonu veya L858R) de aralarında olduğu önceden tanımlanmış olan tüm analiz edilmiş alt gruplarda tutarlılık sergilediği görülmüştür.
FLAURA çalışmasında MSS metastazı etkililik verileri
Nörolojik durumları definitif tedavinin ve steroidlerin tamamlanmasını takip eden en az iki hafta süresince stabil olan steroid gerektirmeyen MSS metastazlı hastalar FLAURA çalışmasında randomize edilmek açısından uygun kabul edilmiştir. 556 hasta içinden 200 hastanın başlangıçta beyin taramalarının mevcut olduğu görülmüştür. MSS metastazlarına sahip 128/556 (%23) hastadan oluşan bir alt grupta bu taramalar üzerinde yapılan bir BICR değerlendirmesi sonuçlanmıştır ve ilgili veriler Tablo 4'de özetlenmektedir. FLAURA'da RECIST v1.1'e göre MSS etkililiği, MSS PFS'de olarak istatistiksel açıdan anlamlı iyileşme olduğunu ortaya koymuştur (HR=0,48, %95 GA 0,26, 0,86; P=0,014).
Tablo 4. FLAURA'da başlangıçtaki bir beyin taramasında MSS metastazları gözlenen hastalarda BICR ile MSS etkililiği
Etkililik Parametreleri | TAGRISSO N = 61 | EGFR TKI komparatörü (gefitinib veya erlotinib) N=67 |
MSS progresyonsuz sağkalım | ||
Olay Sayısı (%) | 18 (30) | 30 (45) |
Medyan, Ay (%95 GA) | NC (16,5, NC) | 13,9 (8,3, NC) |
HR (%95 GA); P-değeri | 0,48 (0,26, 0,86); P = 0,014 | |
6. ayda MSS progresyonsuz ve hayatta (%) (%95 GA) | 87 (74, 94) | 71 (57, 81) |
12. ayda MSS progresyonsuz ve hayatta (%) (%95 GA) | 77 (62, 86) | 56 (42, 68) |
HR = Tehlike Oranı; GA= Güven Aralığı, NC = Hesaplanamaz
HR < 1 TAGRISSO tedavisi lehine iken >1 Odds Oranı (Odds Oranı-OR) TAGRISSO lehinedir
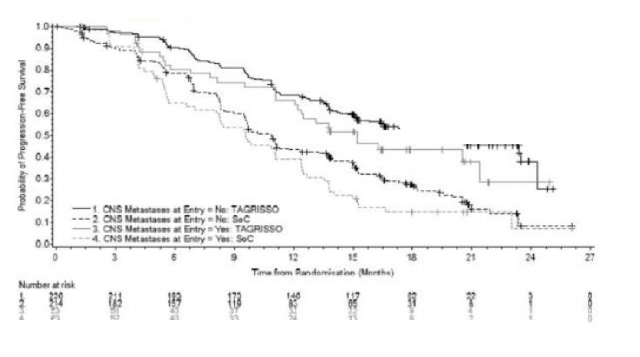
FLAURA'da çalışmaya girişte MSS metastazı durumuna (başlangıçtaki MSS lezyonu bölgesi, tıbbi öykü ve/veya MSS metastazları için uygulanan önceki cerrahi ve/veya önceki radyoterapiye göre tanımlanmıştır) dayalı bir önceden belirlenmiş PFS alt grubu oluşturulmuştur ve Şekil 5'de gösterilmektedir. Çalışmaya girişteki MSS lezyonu durumundan bağımsız olarak, TAGRISSO kolundaki hastalar, EGFR TKI komparatörü kolundakilere kıyasla bir etkililik yararı ortaya koymuştur ve TAGRISSO kolunda yeni MSS lezyonları görülen hastaların sayısının EGFR TKI komparatörü kolundakilere kıyasla daha az sayıda olduğu belirlenmiştir (TAGRISSO, 11/279 [%3,9], EGFR TKI komparatörü, 34/277 [%12,3]). Başlangıçta MSS lezyonu olmayan hastalardan oluşan alt grupta, TAGRISSO kolunda EGFR TKI komparatörü kolundakine kıyasla daha az sayıda yeni MSS lezyonu gözlenmiştir (sırasıyla 7/226 [%3,1], 15/214 [%7,0]).
5.2. Farmakokinetik özellikler
Genel özelliklerOsimertinib farmakokinetik parametreleri, sağlıklı gönüllülerde ve KHDAK hastalarında karakterize edilmiştir. Popülasyon farmakokinetiği analizine göre, osimertinibin belirgin plazma klirensi 14,3 L/sa, belirgin dağılım hacmi 918 L ve terminal yarı ömrü yaklaşık 44 saattir. EAA ve C, 20 ila 240 mg doz aralığında dozla orantılı artış göstermiştir. Osimertinibin günde bir kez uygulanması, yaklaşık 3 kat birikime neden olur ve kararlı durum maruziyetlerine 15 günlük dozlama ile ulaşılır. Kararlı durumda, dolaşımdaki plazma konsantrasyonları 24 saatlik dozlama aralığında tipik olarak 1,6 kat aralığında tutulur.
Emilim:
TAGRISSO'nun oral uygulanmasını takiben osimertinibin pik plazma konsantrasyonlarına 6 (3-24) saatlik medyan (min-maks) tsüresinde ulaşılmıştır ve bazı hastalarda ilk 24 saatte birkaç pik gözlenmiştir. TAGRISSO'nun mutlak biyoyararlanımı 70% (90% GA 67, 73). Hastalardaki klinik farmakokinetik çalışmasına göre 80 mg düzeyinde, besinler osimertinibin biyoyararlanımını klinik olarak anlamlı derecede değiştirmemektedir. (EAA artışı %6 (%90 GA -5, 19) ve Cazalması %7 (%90 GA-19, 6)). Gastrik pH'nin 5 günlük omeprazol dozlamasıyla yükseltildiği ve 80 mg tablet uygulanan sağlıklı gönüllülerde osimertinib maruziyeti etkilenmemiştir (EAA ve Cartışları sırasıyla %7 ve %2) ve maruziyet oranı için
%90 GA, %80-125 sınırları dahilinde tutulmuştur.
Dağılım:
Osimertinibin, kararlı durumda hesaplanan popülasyon ortalama dağılım hacmi (V/F) 918 L olup, dokuya geniş bir dağılıma işaret etmektedir. Osimertinibin plazma protein bağlanması,
%94,7'dir. (% 5.3'i serbest).Osimertinibin aynı zamanda, sıçan ve insan plazma proteinlerine, insan serum albumini ve sıçan ve insan hepatositlerine kovalan bağlandığı gösterilmiştir.
Biyotransformasyon:
İn vitro çalışmalar, osimertinibin ağırlıklı olarak CYP3A4 ve CYP3A5 ile metabolize edildiğine işaret etmektedir. Bununla birlikte, mevcut verilerle alternatif metabolik yollar tamamen göz ardı edilemez. İn vitro çalışmalara göre, klinik öncesi türlerin plazmasında ve insanlarda oral osimertinib dozlamasından sonra 2 tane farmakolojik olarak aktif metabolit (AZ7550 ve AZ5104) tanımlanmıştır; AZ7550, TAGRISSO'ya benzer bir farmakolojik profil göstermiş, buna karşılık AZ5104, mutant ve doğal-tip EGFR için daha yüksek potens göstermiştir. Her iki metabolit de, TAGRISSO'nun hastalara uygulanmasından sonra plazmada yavaşça ortaya çıkmıştır ve medyan (min-maks) tsüreleri sırasıyla 24 (4-72) ve 24 (6-72) saat olmuştur. İnsan plazmasında toplam radyoaktivitenin %0,8'inden ana osimertinib sorumlu olmuştur, 2 metabolit %0,08 ve %0,07 oranlarında katkı göstermiştir ve radyoaktivitenin büyük çoğunluğu kovalan olarak plazma proteinlerine bağlanmıştır. AZ5104 ve AZ7550'nin her ikisinin EAA'ya göre maruziyetlerinin geometrik ortalaması, kararlı durumdaki osimertinib maruziyetinin yaklaşık %10'u olmuştur.
Osimertinibin ana metabolik yolağı, oksidasyon ve dealkilasyondu. İnsanlarda toplu idrar ve fekal numunelerde 5 bileşen dozun >%1'ini oluşturacak şekilde en az 12 bileşen gözlenmiştir; dozun yaklaşık %1,9, %6,6 ve %2,7'sinden değişmemiş osimertinib, AZ5104 ve AZ7550 sorumlu olmuştur ve ayrıca bir sisteinil katılma ürünü (M21) ve bilinmeyen bir metabolit (M25) sırasıyla dozun %1,5 ve %1,9'undan sorumlu olmuştur.
İn vitro çalışmalara göre osimertinib, klinik olarak geçerli konsantrasyonlarda CYP 3A4/5'in kompetitif inhibitörüdür ancak CYP1A2, 2A6, 2B6, 2C8, 2C9, 2C19, 2D6 ve 2E1'in değildir. İn vitro çalışmalara göre osimertinib, hepatik olarak klinik önemli konsantrasyonlarda UGT1A1 ve UGT2B7'nin inhibitörü değildir. UGT1A1'in intestinal inhibisyonu olasıdır ancak klinik etki bilinmemektedir.
Eliminasyon:
20 mg'lik tek oral dozu takiben dozun %67,8'i feçeste geri kazanıldı (%1,2'si ana bileşik olarak), buna karşılık 84 günlük numune alımında uygulanan dozun %14,2'si idrarda bulundu (%0,8 ana bileşik olarak). Değişmemiş osimertinib, %0,8'i idrarda ve %1,2'si feçeste olmak üzere eliminasyonun yaklaşık %2'sinden sorumlu olmuştur.
Doğrusallık/Doğrusal olmayan durum:
EAA ve C, 20 ila 240 mg doz aralığında dozla orantılı artış göstermiştir.
Taşıyıcı proteinlerle etkileşimler:
İn vitro çalışmalarda osimertinibin, OATP1B1 ve OATP1B3 substratı olmadığı gösterilmiştir. İn vitro ortamda osimertinib, klinik olarak geçerli konsantrasyonlarda P-g (P-glikoprotein), OAT1, OAT3, OATP1B1, OATP1B3, MATE1, OCT2 ve MATE2K'yi inhibe etmez. (bkz.
Bölüm 4.5)
İn vitro çalışmalara göre osimertinib, P-gp ve BCRP'nin bir substratıdır, ancak klinik dozlarda klinik olarak anlamlı ilaç etkileşimleri olası değildir.
İn vitro verilere göre osimertinib, BCRP ve P-gp'nin inhibitörüdür.
Hastalardaki karakteristik özellikler
Popülasyon tabanlı bir farmakokinetik analizinde (n=1367), predikte edilen kararlı-durum
maruziyeti (EAA) ve hastanın yaşı (aralık: 25 ila 91 yaş), cinsiyeti (%65 kadın), etnik kökeni (Beyaz, Asyalı, Japon, Çinli ve Asyalı-olmayan-Beyaz-olmayan hastalar) tedavi basamağı ve sigara içme durumu (n=34 sigara içenler, n=419 daha önceden sigara içmiş olanlar) arasında klinik olarak anlamlı ilişki tanımlanmamıştır. Popülasyon FK analizi, vücut ağırlığının anlamlı eş değişken olduğuna işaret etmiş, ve 61 kg medyan vücut ağırlığı için EAA'ye kıyasla 88 kg ve 43 kg (%95 ila %5'lik dilimler) vücut ağırlığı aralığı genelinde beklenen osimertinib EAAdeğişikliği %20'den az olmuştur. Vücut ağırlığının uç noktaları, <43 kg ile
>88 kg aralığı, açısından AZ5104 metabolit oranları sırasıyla %11,8 ila %9,6 aralığında, buna karşılık AZ7550 için sırasıyla %12,8 ila %8,1 aralığında olmuştur. Popülasyon PK analizine göre, 39 g/L şeklindeki medyan başlangıç albümini için EAAile karşılaştırıldığında, 29 ila 46 g/L albümin aralığında beklenen osimertinib EAAdeki değişimin <%30olmasıyla serum albümini anlamlı bir değişken olarak belirlenmiştir. Vücut ağırlığı farklıkları ya da başlangıçtaki albüminden kaynaklanan bu maruziyet değişikliklerinin klinik olarak önemli olmadığı değerlendirilmektedir.
Karaciğer yetmezliği:
Osimertinib daha çok karaciğer yoluyla eliminasyona uğramaktadır. Yapılan bir klinik çalışmada, tek bir 80 mg TAGRISSO dozundan sonra normal karaciğer fonksiyonuna sahip hastalara kıyasla (n=10) farklı türde ileri evre solid tümörleri olan ve hafif (Child Pugh A, ortalama skor = 5,3, n=7) veya orta karaciğer yetmezliğine sahip (Child Pugh B, ortalama skor= 8,2, n=5) hastalarda maruziyette artış gözlenmemiştir. Normal karaciğer fonksiyonuna sahip hastalardaki maruziyete kıyasla, osimertinib EAA ve Ciçin geometrik ortalama oran (%90 GA) hafif karaciğer yetmezliği olan hastalarda %63,3 (47,3; 84,5) ve %51,4 (36;6;
72,3) ve orta şiddetli karaciğer yetmezliği olanlar hastalarda %68,4 (49,6; 94,2) ve %60,7 (41,6; 88,6) idi; AZ5104 metabolit için EAA ve Chafif karaciğer yetmezliği olan hastalarda %66,5 (43,4; 101,9) ve %66,3 (45,3; 96;9) ve orta şiddetli karaciğer yetmezliği
olanlar hastalarda %50,9 (31,7; 81,6) ve %44,0 (28,9; 67,1) idi. Popülasyon FK analizine dayanarak, hepatik fonksiyon belirteçleri (ALT, AST, bilirubin) ve osimertinib maruziyeti arasında herhangi bir ilişki yoktu. Hepatik yetmezlik belirteci serum albümin, osimertinib farmakokinetiğinde bir etki göstermiştir. Yapılan klinik çalışmalarda AST veya ALT değerleri üst normal sınırın (ULN) 2,5 katından yüksek olan hastaları veya altta yatan bir maligniteye bağlı ise, >1,5x ULN toplam bilirubin değeri ile >5,0 x ULN olan hastalar hariç tutulmuştur. Hafif karaciğer yetmezliğine sahip 134 hastanın, orta karaciğer yetmezliğine sahip 8 hastanın ve normal karaciğer fonksiyonuna sahip 1216 hastanın farmakokinetik analizine dayanarak, osimertinib maruziyetleri benzerdi. Şiddetli karaciğer yetmezliğine sahip hastalarda veri mevcut değildir (bkz. Bölüm 4.2).
Böbrek yetmezliği:
Bir klinik çalışmada, tek bir oral 80 mg'lık TAGRISSO dozunun ardından ciddi böbrek yetmezliği olan hastalar (CLcr 15 ila < 30 mL/dak; n=7) normal böbrek fonksiyonu olanlarla (CLcr ≥ 90 mL/dak; n=8) karşılaştırıldığında AUC'de 1.85 katlık (%90 GA; 0.94, 3.64) ve Cda 1.19 katlık (%90 GA: 0.69, 2.07) bir artışı ortaya koymuştur. Ayrıca hafif böbrek bozukluğu olan 593 hasta (CLcr 60 ila < 90 mL/dak), orta düzeyde böbrek bozukluğu olan 254 hasta (CLcr 30 ila < 60 mL/dak), ciddi böbrek bozukluğu olan 5 hasta (CLcr 15 ila < 30 mL/dak) ve normal böbrek fonksiyonuna sahip 502 hastanın (CLcr ≥ 90 mL/dak) popülasyon farmakokinetik analizine göre, osimertinib maruziyetleri benzer olmuştur. CLcr ≤ 10 mL/dak olan hastalar klinik çalışmalara dahil edilmemiştir.
5.3. Klinik öncesi güvenlilik verileri
Sıçanlarda ve köpeklerde yapılan tekrarlı doz toksisitesi çalışmalarında gözlenen ana bulgular; dalaktaki sekonder değişiklikler ile birlikte, kornea epitelini (oftalmoloji muayenesinde köpeklerde korneal translüsensilerin ve opasitelerin eşlik ettiği), gastrointestinal sistem (dil dahil), cilt ve erkek ve dişi reprodüktif sistemlerini etkileyen atrofik, inflamatuvar ve/veya dejeneratif değişikliklerden oluşuyordu. Bu bulgular, 80 mg terapötik dozdaki hastalarda görülenlerin altındaki plazma konsantrasyonlarında görüldü. Dozlamanın 1 ayını takiben ortaya çıkan bulgular 1 aylık dozlama kesilmesi uygulandığında, bazı korneal değişikliklerde kısmi iyileşme görülmesi haricinde büyük oranda geri dönüşümlüydü.
Sıçanlarda yapılan 104 haftalık bir karsinojenisite çalışmasında, günde bir kez 80 mg'lık önerilen klinik dozda, insan EAA'sının 0,2 katı maruziyetlerde lens lifi dejenerasyonu tespit edilmiştir. Lens opasiteleri ilk olarak bu çalışmanın 52. haftasından itibaren fark edilmiş ve artan doz süresi ile insidans ve şiddette kademeli bir artış göstermiştir. Bu bulgunun klinik önemi göz ardı edilemez.
Osimertinib, sinomolgus maymunu (i.v. dozlama), sıçan ve farenin (oral uygulama) sağlam kan-beyin bariyerine nüfuz etmiştir.
Klinik dışı veriler, osimertinib ve metabolitinin (AZ5104) h-ERG kanalını inhibe ettiğine işaret etmektedir ve QTc uzatıcı etki hariç tutulamaz.
Karsinojenite ve mutajenite:
Osimertinib, in vitro ve in vivo analizlerde genetik hasara neden olmamıştır. Osimertinib, 26 hafta boyunca Tg rasH2 transgenik farelere oral yoldan uygulandığında hiçbir karsinojenik potansiyel göstermemiştir.
Sıçanlarda yapılan 104 haftalık karsinojenisite çalışmasında, önerilen günde bir kez 80 mg klinik dozda EAA'nın 0,2 katı maruziyetlerde mezenterik lenf düğümünde proliferatif vasküler lezyonların (anjiyomatöz hiperplazi ve hemanjiyom) insidansında artış gözlenmiştir; bunun insanlar için anlamlı olması muhtemel değildir.
Üreme toksisitesi:
≥ 1 ay boyunca osimertinibe maruz kalan sıçanların ve köpeklerin testislerinde dejeneratif değişiklikler mevcuttu ve sıçanlarda, 3 aylık osimertinib maruziyetini takiben erkek fertilitesinde bir azalma vardı. Bu bulgular, klinik olarak geçerli plazma konsantrasyonlarında görüldü. 1 aylık dozlamayı takiben görülen testislerdeki patoloji bulguları, sıçanlarda geri dönüşümlüydü ancak köpekler için bu lezyonların geri dönüşümlü olduğuna ilişkin kesin bir açıklama yapılamamaktadır.
Hayvanlarda yapılan araştırmalara göre, dişi fertilitesi osimertinib tedavisi ile bozulabilir. Tekrarlanan doz toksisite çalışmalarında, klinik olarak ilgili plazma konsantrasyonlarında osimertinibe ≥1 ay boyunca maruz kalan sıçanlarda yumurtalıklarda anöstrus, korpus luteum dejenerasyonu ve uterus ile vajinada epitel incelmesi insidansında artış görülmüştür. 1 aylık dozlamayı takiben yumurtalıklarda görülen bulgular geri dönüşümlüdür. Sıçanlarda yapılan bir dişi fertilite çalışmasında, 20 mg/kg/gün osimertinib uygulamasının (önerilen günlük 80 mg'lık klinik doza yaklaşık olarak eşit) östrus döngüsü veya gebe kalan dişilerin sayısı üzerinde hiçbir etkisi olmamış, ancak erken embriyonik ölümlere neden olmuştur.Bu bulgular,
1 aylık doz kesilmesinin ardından geri dönüşlü olduğuna dair kanıtlar gösterdi.
Sıçanlarda yapılan bir modifiye embriyofetal gelişim çalışmasında osimertinib, embriyonik implantasyon öncesinde gebe sıçanlarda uygulandığında embriyoletaliteye neden olmuştur. Bu etkiler, annenin tolere edebildiği 20 mg/kg'lik dozda görülmüştür, bu dozun maruziyeti insanlarda önerilen günlük 80 mg'nin maruziyetine (toplam EAA'ya göre) eşdeğerdir. Organogenez sırasında 20 mg/kg ve üzerindeki dozlarda maruziyet, fetal ağırlıkların azalmasına yol açmıştır ancak eksternal veya visseral fetal morfoloji üzerinde advers etki görülmemiştir. Osimertinib, gestasyon döneminde ve sonrasında erken laktasyon dönemine kadar gebe dişi sıçanlara uygulandığında, emzirilen yavrularda osimertinib ve metabolitlerine gösterilebilir maruziyet ve ilaveten yavru sağkalımında azalma ve yavru büyümesinde geri kalma (20 mg/kg ve üzerindeki dozlarda) görülmüştür.
6. FARMASÖTİK ÖZELLİKLER
6.1. Yardımcı maddelerin listesi
Mannitol Mikrokristalin selüloz
Düşük substitüsyonlu hidroksipropil selüloz Sodyum stearil fumarat
Polivinil alkol
Titanyum dioksit (E 171) Makrogol 3350
Talk
Sarı demir oksit (E 172) Kırmızı demir oksit (E 172) Siyah demir oksit (E 172) Saf su
6.2. Geçimsizlikler
Geçerli değildir.
6.3. Raf ömrü
36 ay.
6.4. Saklamaya yönelik özel tedbirler
30 C altındaki oda sıcaklığında saklayınız.
6.5. Ambalajın niteliği ve içeriği
Al/Al perfore birim doz blisterleri. 28 x 1 tablet (4 blister) içeren kartonlar.
6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
Herhangi kullanılmamış tıbbi ürün ya da atık materyaller, bölgesel gerekliliklere uygun olarak imha edilmelidir.
Kullanılmamış olan ürünler yada atık materyaller ‘Tıbbi atıkların kontrolü yönetmeliği' ve ‘ Ambalaj Atıklarının Kontrolü yönetmelikleri'ne uygun olarak imha edilmelidir.
 En Yaygın Alerji Türleri
Bağışıklık sistemi, polen, arı zehiri veya evcil hayvan gibi yabancı bir maddeye veya çoğu insanda reaksiyona neden olmayan bir yiyeceğe tepki gösterdiğinde alerjiler meydana gelir.
En Yaygın Alerji Türleri
Bağışıklık sistemi, polen, arı zehiri veya evcil hayvan gibi yabancı bir maddeye veya çoğu insanda reaksiyona neden olmayan bir yiyeceğe tepki gösterdiğinde alerjiler meydana gelir. |
 Mide Kanseri
Mide kanseri genellikle mideyi tümüyle kaplayan ve mukus üretmekle görevli hücrelerde başlar. Bu kanser tipine adenokarsinom denir.
Mide Kanseri
Mide kanseri genellikle mideyi tümüyle kaplayan ve mukus üretmekle görevli hücrelerde başlar. Bu kanser tipine adenokarsinom denir. |
 |
Artrit Artrit, oldukça yaygın bir hastalıktır ancak iyi anlaşılamamıştır. Aslında “artrit” tek bir hastalığın adı değildir; eklem ağrısı veya eklem hastalıklarını adlandırmanın gayri resmi yoludur. |
 |
Mesane Kanseri Mesane kanseri her zaman mukozada başlar. Erken safhalarda bu tabakada sınırlı kalır ve hücre içindeki karsinom olarak nitelendirilir. |
 |
Astım Astımlı kişilerin akciğerlerindeki hava boruları (bronşlar) hassastır. Bu kişiler belirli tetikleyici faktörlere maruz kaldıklarında, hava boruları nefes almalarını güçleştirecek şekilde daralır. |
İLAÇ GENEL BİLGİLERİ
AstraZeneca Türkiye İlaç Sanayi ve Ticaret Ltd.Şti.
| Geri Ödeme Kodu | A16807 |
| Satış Fiyatı | 187779.8 TL [ 18 Apr 2025 ] |
| Önceki Satış Fiyatı | 187779.8 TL [ 14 Apr 2025 ] |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8699786092877 |
| Etkin Madde | Mertinib Mesilat |
| ATC Kodu | L01EB04 |
| Birim Miktar | 80 |
| Birim Cinsi | MG |
| Ambalaj Miktarı | 28 |
| Antineoplastik ve İmmünomodülatör Ajanlar |
| İthal ( ref. ülke : Isvec ) ve Beşeri bir ilaçdır. |