TEMODAL 250 mg 5 kapsül Farmakolojik Özellikler
{ Temozolomid }
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Antineoplastik ajanlar - Diğer alkilleyici ajanlar ATC Kodu: L01AX03
Etki mekanizması
Temozolomid fizyolojik pH'da hızlı bir kimyasal dönüşüm göstererek aktif bileşen olan monometil triazenoimidazol karboksamide (MTİK) dönüşen bir triazendir. MTİK'nin sitotoksisitesinin, primer olarak guaninin O pozisyonunun alkilasyonundan ve ilaveten N pozisyonunda alkilasyonundan ileri geldiği düşünülmektedir. Bunu takiben gelişen sitotoksik lezyonların, metil katılımının anormal onarımı ile ilgili olduğu düşünülmektedir.
Klinik etkililik ve güvenlilik
Yeni teşhis edilen glioblastoma multiforme
Toplam 573 hasta TEMODAL + RT (n=287) veya tek başına RT (n=286) almak üzere randomize edilmiştir. TEMODAL + RT kolundaki hastalar RT'nin ilk gününden itibaren RT'nin son gününe kadar 42 gün süreyle (maksimum 49 gün) günde bir kez eş zamanlı TEMODAL (75 mg/m) almıştır. Bunu RT'nin bitiminden sonraki 4 haftadan başlayarak 6 küre kadar, 28 günlük her bir kürün 1-5. günlerinde verilen TEMODAL monoterapisi (150-
200 mg/m) izlemiştir. Kontrol kolun dakih astalaryalnızca RT almıştır. RT ve kombine
TEMODAL tedavisi süresince Pnemocytis jirovecii pnömonisine (PCP) yönelik profilaksi
gerekmiştir.
Tek başına RT kolundaki 282 hastadan 161'i (% 57) ve TEMODAL + RT kolundaki 277
hastadan 62'sine (% 22) takip döneminde kurtarıcı tedavi olarak TEMODAL uygulanmıştır.
Genel sağkalım için tehlike oranı (HR) 1,59'dur (HR için % 95 güven aralığı (GA) =1,33 - 1,91) ve log-rank p değeri TEMODAL kolunun lehine < 0,0001'dir. Hesaplanan 2 yıl veya daha uzun süre hayatta kalma olasılığı (% 26'ya karşı % 10) RT + TEMODAL kolunda daha yüksektir. Yeni teşhis edilmiş glioblastoma multiformeli hastaların tedavisinde RT'ye eş zamanlı TEMODAL eklenmesi ve ardından TEMODAL monoterapisi tek başına RT'ye kıyasla genel sağkalımda (OS) istatistiksel olarak anlamlı iyileşme göstermiştir (Şekil 1).
ITT Popülasyonu: Genel Sağkalım
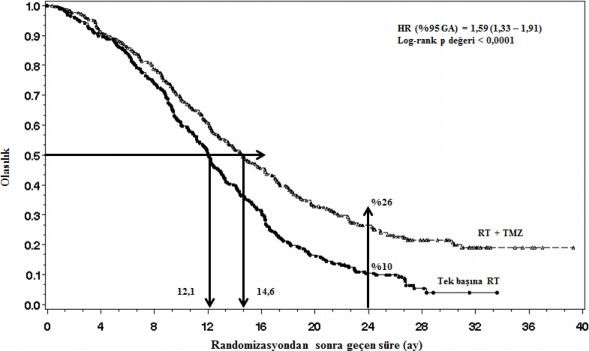
Şekil 1. Genel sağkalım için Kaplan-Meier eğrileri (ITT (tedavi amaçlı) popülasyon)
Çalışmanın sonuçları performans durumu kötü olan bir hasta alt grubunda (WHO PS=2, n=70) tutarlı değildir ve bu alt grupta genel sağkalım ve progresyona kadar geçen süre her iki kolda benzerdir. Ancak bu hasta grubunda kabul edilemez risklerin mevcut olmadığı anlaşılmaktadır.
Nüks eden veya ilerleyen malign glioma
Cerrahiden ve RT'den sonra ilerleyen veya nüks eden glioblastoma multiformeli hastalarda (Karnofski performans durumu [KPS] ≥ 70) klinik etkinlik verileri oral TEMODAL ile yürütülen iki klinik çalışmaya dayanmaktadır. Bunlardan biri 138 hastada (% 29'u daha önce kemoterapi almıştı) yürütülen karşılaştırmasız bir çalışma, diğeri ise toplam 225 hastada (% 67'si daha önce nitrozoüreye dayalı kemoterapi almıştı) yürütülen, TEMODAL'in prokarbazin ile karşılaştırıldığı randomize, aktif-kontrollü bir çalışmadır. Her iki çalışmada, birincil son nokta manyetik rezonans görüntülemesi veya nörolojik kötüleşme ile tanımlanan progresyonsuz sağkalımdır (PFS). Karşılaştırmasız çalışmada 6 ayda PFS % 19, progresyonsuz medyan sağkalım süresi 2,1 ay ve medyan genel sağkalım 5,4 aydır. MR görüntülemelerine dayananobjektifyanıtoranı(O RR)%8'dir.
Randomize, aktif-kontrollü çalışmada TEMODAL ile 6 ayda PFS prokarbazine göre anlamlı olarak daha fazladır (% 21'e karşı % 8 – ki-kare p = 0,008) ve medyan PFS sırasıyla 2,89 ay ve 1,88 aydır (log sıra p = 0,0063). TEMODAL ve prokarbazin için medyan sağkalım süresi sırasıyla 7,34 ay ve 5,66 aydır (log sıra p = 0,33). Altı ayda, TEMODAL kolunda hayatta kalan hastaların oranı (% 60) prokarbazin koluna kıyasla(% 44) anlamlı olarak daha yüksektir (ki-kare p = 0,019). Daha önce kemoterapi almış hastalarda yarar KPS ≥ 80 olan hastalarda gösterilmiştir.
Nörolojik durumda kötüleşmeye kadar geçen süreye ilişkin veriler ve performans durumunda kötüleşmeye kadar geçen süreye ilişkin veriler prokarbazine göre TEMODAL lehinedir (KPS'nin < 70'e gerilemesi veya en az 30 puan azalma). Bu son noktalarda progresyona kadar geçen medyan süreler prokarbazine kıyasla TEMODAL ile 0,7 – 2,1 ay daha uzundur (log sıra p = < 0,01 - 0,03).
Nüks eden anaplastik astrositoma
Anaplastik astrositomalı hastaların ilk relapstaki tedavisinde oral TEMODAL'in güvenliliğini ve etkililiğini değerlendiren çok-merkezli, ileriye dönük bir faz II çalışmada, 6 ayda PFS
% 46 ve medyan PFS 5,4 aydır. Medyan genel sağkalım süresi 14,6 aydır. Merkezi gözden geçirmeyi yapan araştırmacının değerlendirmesine dayanan yanıt oranı tedavi amaçlı popülasyonda (ITT) (n=162) % 35'dir (13 tam yanıt ve 43 kısmi yanıt). 43 hastada stabil hastalık bildirilmiştir. ITT popülasyonunda 6 aylık olaysız sağkalım oranı % 44 ve medyan olaysız sağkalım süresi 4,6 aydır; bu rakamlar progresyonsuz sağkalım sonuçlarıyla benzerdir. Uygun nitelikteki histoloji popülasyonunda etkinlik sonuçları benzerdir. Radyolojik objektif yanıta ulaşılması veya progresyonsuz durumun korunması yaşam kalitesinin korunması veya iyileşmesiyle güçlü biçimde ilişkili bulunmuştur.
Pediyatrik hastalar:
Oral TEMODAL, 28 günde bir 5 gün boyunca günlük olarak uygulanmış bir rejimde nüks eden beyin sapı glioması ya da nüks eden yüksek evreli astrositomu olan pediyatrik hastalarda (3-18 yaş arası) incelenmiştir. TEMODAL'e tolerans erişkinlerdekine benzerdir.
5.2. Farmakokinetik özellikler
Genel ÖzelliklerTemozolomid fizyolojik pH'de esas olarak aktif tür olan 3-metil-(triazen-1-il)imidazol-4- karboksamide (MTİK) kendiliğinden hidrolize olur. MTİK, pürin ve nükleik asit biyosentezinde bilinen bir ara madde olan 5-amino-imidazol-4-karboksamide (AİK) ve aktif alkilleyici tür olduğuna inanılan metilhidrazine kendiliğinden hidrolize olur. MTİK sitotoksisitesinin, esas olarak guaninin O ve N pozisyonlarında olmak üzere DNA alkillenmesinden kaynaklandığı düşünülmektedir. Temozolomid EAA'sına kıyasla MTİK ve AİK'ye maruz kalım sırasıyla ~% 2,4 ve % 23'tür. İn vivo koşullarda MTİK'in t'si temozolomidinkine (1,8 saat) benzerdir.
Emilim:
Erişkin hastalarda oral yoldan uygulandıktan sonra temozolomid hızla emilmekte ve dozdan sonra 20 dakika gibi kısa bir sürede doruk konsantrasyona ulaşmaktadır (ortalama süre 0,5 ile 1,5 saat). C ile işaretlenmiş TEMODAL oral yolla uygulandıktan sonra C'nin dozdan sonra 7 gün boyunca feçes ile ortalama atılım oranı % 0,8 bulunmuştur; bu oran tam emilimi gösterir.
Dağılım:
Temozolomid proteinlere düşük oranda bağlanır (% 10-% 20) ve proteine yüksek oranda
bağlanan maddelerle etkileşmesi beklenmez.
5.3. Klinik öncesi güvenlilik verileri
ve insanlarda yapılan PET çalışmaları, temozolomidin kan beyin bariyerini hızla geçtiğini ve beyin-omurilik sıvısında (BOS) bulunduğunu düşündürmektedir. Beyin omurilik sıvısına penetrasyonu 1 hastada doğrulanmıştır ve temozolomidin eğri altında kalan alanına göre BOS maruz kalımı plazmadakinin yaklaşık % 30'u kadardır; bu bulgu hayvan verileriyle paraleldir.
Biyotransformasyon;
Oral uygulamayı takiben dozun ortalama % 5-% 10'u 24 saat içinde idrarla değişmeden ve geriye kalanı ise temozolomid asidi, 5-aminoimidazol-4-karboksamid (AİK) veya tanımlanmamış polar metabolitler şeklinde atılmaktadır. Plazma konsantrasyonları doza- bağımlı bir tarzda artmaktadır.
Eliminasyon:
Plazma yarılanma ömrü (t) yaklaşık 1,8 saattir. C'nin eliminasyonu esas olarak
böbreklerde gerçekleşir.
Doğrusallık/Doğrusal olmayan durum:
Plazma konsantrasyonları doza bağlı olarak artar. Plazma klerensi, dağılım hacmi ve
yarılanma ömrü dozdan bağımsızdır.
Özel popülasyonlara ilişkin ek bilgiler
Temozolomidin popülasyon bazlı farmakokinetik analizi sonucunda plazma temozolomid klerensinin yaş, böbrek fonksiyonu veya tütün kullanımından bağımsız olduğu bulunmuştur. Diğer bir farmakokinetik çalışmada hafif ilâ orta dereceli hepatik disfonksiyonu bulunan hastaların, normal hepatik fonksiyonu olan hastalar ile benzer plazma farmakokinetik profilleri olduğu gözlenmiştir.
Pediyatrik hastalarda eğri altında kalan alan (EAA) daha büyüktür; ancak, maksimum tolere
edilebilen doz (MTD) hem çocuklar hem de erişkinlerde kür başına 1000 mg/m dir.
5.3. Klinik öncesi güvenlilik verileri
ve insanlarda yapılan PET çalışmaları, temozolomidin kan beyin bariyerini hızla geçtiğini ve beyin-omurilik sıvısında (BOS) bulunduğunu düşündürmektedir. Beyin omurilik sıvısına penetrasyonu 1 hastada doğrulanmıştır ve temozolomidin eğri altında kalan alanına göre BOS maruz kalımı plazmadakinin yaklaşık % 30'u kadardır; bu bulgu hayvan verileriyle paraleldir.
Sıçanlarda ve köpeklerde tek kürlük (5 gün dozaj, 23 günlük tedavisiz dönem), üç ve altı kürlük toksisite çalışmaları yürütülmüştür. Toksisitenin primer hedefleri kemik iliği, lenforetiküler sistem, testisler ve gastrointestinal kanaldı ve daha yüksek dozlarda (test edilen sıçanların ve köpeklerin % 60-100'ünde ölümcül olmuştur) retina dejenerasyonu gözlenmiştir. Erkek üreme sistemi ve retina dejenerasyonunu içeren istenmeyen olaylar hariç, toksisitenin büyük kısmı geri dönüşlü olma bulguları sergilemiştir. Ancak retina dejenerasyonundan sorumlu tutulan dozlar ölümcül doz aralığında olduğundan ve klinik çalışmalarda benzer bir etki gözlenmediğinden, bu bulgunun klinik yönden önemli olduğu düşünülmemiştir.
Temozolomid embriyotoksik, teratojenik ve genotoksik alkilleyici ajandır. Temozolomid sıçan ve köpeklerde insanlara göre daha toksiktir ve klinik doz sıçan ve köpeklerde minimum ölümcül doza yakındır. Lökositlerin ve trombositlerin doza bağlı olarak azalmaları, toksisitenin duyarlı birer göstergesidir. Altı kürlük sıçan çalışmasında meme karsinomları, deride keratoakantoma ve bazal hücreli adenomu içeren çeşitli neoplazmlar gözlenmiş ancak köpek çalışmalarında tümörler veya preneoplastik değişiklikler gözlenmemiştir. Sıçanların TEMODAL'in onkojenik etkilerine özellikle duyarlı olduğu anlaşılmaktadır ve ilk tümörler
dozaja başlandıktan sonra 3 ay içinde görülmüştür. Bu latent dönem bir alkilleyici ajan için bile çok kısadır.
Ames/Salmonella ve İnsan Periferik Kan Lenfositi (HPBL) kromozom aberasyonu testlerinin sonuçlarında pozitif bir mutajenik yanıt görülmüştür.
 En Yaygın Alerji Türleri
Bağışıklık sistemi, polen, arı zehiri veya evcil hayvan gibi yabancı bir maddeye veya çoğu insanda reaksiyona neden olmayan bir yiyeceğe tepki gösterdiğinde alerjiler meydana gelir.
En Yaygın Alerji Türleri
Bağışıklık sistemi, polen, arı zehiri veya evcil hayvan gibi yabancı bir maddeye veya çoğu insanda reaksiyona neden olmayan bir yiyeceğe tepki gösterdiğinde alerjiler meydana gelir. |
 Parkinson Hastalığı
Hastalık ilk kez 1817 de İngiliz doktor James Parkinson tarafından tanımlanmış ve Dr. Parkinson hastalığı “sallayıcı felç” olarak kaleme almış.
Parkinson Hastalığı
Hastalık ilk kez 1817 de İngiliz doktor James Parkinson tarafından tanımlanmış ve Dr. Parkinson hastalığı “sallayıcı felç” olarak kaleme almış. |
İLAÇ GENEL BİLGİLERİ
Merck İlaç Ecza ve Kimya Ticaret AŞ
| Geri Ödeme Kodu | A07743 |
| Satış Fiyatı | 8327.14 TL [ 17 Dec 2024 ] |
| Önceki Satış Fiyatı | 8489.12 TL [ 2 Dec 2024 ] |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8699636150528 |
| Etkin Madde | Temozolomid |
| ATC Kodu | L01AX03 |
| Birim Miktar | 250 |
| Birim Cinsi | MG |
| Ambalaj Miktarı | 5 |
| Antineoplastik ve İmmünomodülatör Ajanlar > Alkilleyici Ajanlar > Temozolomid |
| İthal ( ref. ülke : Yunanistan ) ve Beşeri bir ilaçdır. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| Eşdeğer bir ilaç bulunamadı |
 |
Asperger Sendromu Asperger sendromu, otistik gurubun bir bölümü olan bir özürdür. Bu genelde, gurubun daha ”yüksek” tarafında yer aldığı düşünülen kişilere uygun bir tanıdır. |
 |
Mesane Kanseri Mesane kanseri her zaman mukozada başlar. Erken safhalarda bu tabakada sınırlı kalır ve hücre içindeki karsinom olarak nitelendirilir. |
 |
Lösemi Kan Kanseri Lösemi, kan kanseridir ve vücudunun kan oluşturan dokularının hastalanması anlamına gelir. Birçok lösemi türü vardır; bazı lösemi türleri çocuklarda bazıları da yetişkinlerde sık görülür. |