TIBERSID 500 mg/ 3 ml inf. çöz. içeren 1 ampül { Menta Pharma } Kısa Ürün Bilgisi
{ Ornidazol }
1. BEŞERİ TIBBİ ÜRÜNÜN ADI
TİBERSİD 500 mg/3 ml IV infüzyon için enjeksiyonluk çözelti
Steril
2. KALİTATİF VE KANTİTATİF BİLEŞİM
Etkin madde
Her bir ampul (3 ml) 500 mg ornidazol içerir.
Yardımcı maddeler
Etanol (susuz) 900 mg
Propilen glikol 1600 mg
Yardımcı maddeler için 6.1.'e bakınız.
3. FARMASÖTİK FORMU
İnfüzyon için çözelti içeren ampul
Şeffaf ampule doldurulmuş steril, berrak ve açık sarı renkli çözelti.
4. KLİNİK ÖZELLİKLER
4.1. Terapötik endikasyonlar
Anaerob bakterilere bağlı enfeksiyonlarda; septisemi, menenjit, peritonit, postoperatif yara enfeksiyonları, doğum sonrası septisemi, septik abortus ve söz edilen bakterilerin ispatlandığı veya varlığından şüphelenilen endometrit vakalarında,
4.2. Pozoloji ve uygulama şekli
Pozoloji/uygulama sıklığı ve süresi:
Doktor tarafından başka şekilde tavsiye edilmediği taktirde;
Önemli: Ampul içeriği kısa infüzyon şeklinde verilmeli, seyreltilmeden hiçbir şekilde enjekte
edilmemelidir.
Anaerob bakterilere bağlı enfeksiyonlar
Anerob bakterilere bağlı enfeksiyonların tedavisi: 500-1000 mg'lık (1-2 ampul) infüzyonla başlanır, daha sonra her 12 saatte bir 500 mg'lık (1 ampul) veya 5-10 gün boyunca her 24 saatte bir 1 g'lık infüzyon yapılır. Hastanın durumu izin verdiği zaman parenteral tedavi yerini oral tedaviye bırakmalıdır. Örn. her 12 saatte bir 500 mg (2 tablet).
4.3. Kontrendikasyonlar
Ornidazol, diğer nitroimidazol türevleri veya ilacın içerdiği yardımcı maddelerden herhangi birine karşı aşırı duyarlılığı olduğu bilinen hastalarda TİBERSİD kullanımı kontrendikedir.
4.4. Özel kullanım uyarıları ve önlemleri
Merkezi sinir sistemi hastalığı (örn. epilepsi veya multipl skleroz) olan hastalarda ve ağır karaciğer hastalığı olanlarda dikkatli olmak gerekir.
Ampuller etanol ve propilen glikol içermektedir. Propilen glikol içerdiği için alkol benzeri semptomlara neden olabilir. Bu tıbbi üründe (3 ml'lik çözelti) hacmin %38'i kadar etanol (alkol) vardır; örneğin, her dozda 22,5 ml biraya veya her dozda 9,36 ml şaraba eşdeğer 900
mg etanol (alkol) içerir. Alkol bağımlılığı olanlar için zararlı olabilir. Hamile veya emziren kadınlar, çocuklar ve karaciğer hastalığı ya da epilepsi gibi yüksek risk grubundaki hastalarda dikkate alınmalıdır.
Diğer ilaçların etkisi artabilir veya azalabilir.
Duyarlı kişilerde aşırı duyarlılık reaksiyonları gelişebilir.
4.5. Diğer tıbbi ürünler ile etkileşimler ve diğer etkileşim şekilleri
Ornidazol kullanırken ve ilaç kesildikten sonra en az 3 gün boyunca alkol alınmamalıdır. Ornidazol, kumarin-tipi oral antikoagülanların etkisini potansiyelize eder. Antikoagülanın dozu bu doğrultuda ayarlanmalıdır.
Simetidin (antihistaminik), fenitoin ve fenobarbital gibi antiepileptik ilaçlar ve lityum ile
birlikte kullanılırken dikkatli olunmalıdır.
Ornidazol, vekuronyum bromürün adale gevşetici etkisini uzatır.
Özel popülasyonlara ilişkin ek bilgiler
Özel popülasyonlara ilişkin etkileşim çalışması yapılmamıştır.
Pediyatrik popülasyon:
Pediyatrik popülasyonlar ile ilgili hiçbir etkileşim çalışması yapılmamıştır.
4.6. Gebelik ve laktasyon
Gebelik kategorisi: C
Çocuk doğurma potansiyeli bulunan kadınlar/Doğum kontrolü (Kontrasepsiyon)
Ornidazol için, gebeliklerde maruz kalmaya ilişkin klinik veri mevcut değildir.
Hayvanlar üzerinde yapılan çalışmalar, gebelik/embriyonal/fetal gelişim/doğum ya da doğum sonrası gelişim ile ilgili olarak doğrudan ya da dolaylı zararlı etkiler olduğunu göstermemektedir.
Ornidazolün çocuk doğurma potansiyeli bulunan kadınlara ve doğum kontrolü yöntemlerine
etkisi bilinmemektedir.
Gebelik dönemi
Ornidazol için, gebeliklerde maruz kalmaya ilişkin klinik veri mevcut değildir.
Hayvanlar üzerinde yapılan çalışmalar, gebelik/embriyonal/fetal gelişim/doğum ya da doğum sonrası gelişim ile ilgili olarak doğrudan ya da dolaylı zararlı etkiler olduğunu göstermemektedir.
Değişik türlerde yapılan yaygın çalışmalarda ilaç herhangi bir teratojenik veya fetotoksik etki göstermemiştir. Bununla beraber gebe kadınlarda kontrollü bir çalışma yapılmamıştır. Genel bir prensip olarak TİBERSİD gebeliğin erken dönemlerinde gerekli olmadıkça verilmemelidir.
Laktasyon dönemi
TİBERSİD genel bir prensip olarak emziren annelere gerekli olmadıkça verilmemelidir.
Üreme yeteneği/Fertilite
Ornidazol, erkek farelerde 400 mg/kg/gün gibi yüksek dozda uygulandığında, düşük sperm hızı bakımından epididimal sperm motilitesini inhibe ederek infertilite meydana getirmektedir.
İnsanlar üzerinde yapılan çalışmalardan elde edilmiş veri bulunmamaktadır.
4.7. Araç ve makine kullanımı üzerindeki etkiler
TİBERSİD alan hastalarda uyku hali, baş dönmesi, tremor, rijidite, koordinasyon bozuklukları, nöbet, vertigo veya geçici bilinç kaybı görülebilir. Bu gibi etkiler araç ve makine kullanımı gibi dikkat gerektiren işleri etkileyebilir.
4.8. İstenmeyen etkiler
Ornidazol ile yapılan klinik çalışmalarda görülen yan etkiler sistem organ sınıflarına ve sıklık gruplarına göre aşağıda verilmiştir:
Çok yaygın (≥1/10); yaygın (≥1/100 ila <1/10); yaygın olmayan (≥ 1/1000 ila <1/100); seyrek (≥1/10000 ila <1/1000); çok seyrek (<1/10000); bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor.)
Kan ve lenf sistemi hastalıkları
Seyrek: Lökopeni
Sinir sistemi hastalıkları
Çok seyrek: Uyku hali, baş ağrısı, baş dönmesi, tremor, rijidite, koordinasyon bozuklukları, nöbet, yorgunluk, vertigo, geçici bilinç kaybı ve duyusal veya karışık periferal nöropati
Gastrointestinal hastalıklar
Yaygın olmayan: Bulantı, kusma, ishal, epigastrik rahatsızlık, ağız kuruluğu ve iştahsızlık Seyrek: Tat alma bozukluğu
Hepatobilier hastalıklar
Bilinmiyor: Sarılık, anormal karaciğer fonksiyon testleri
Deri ve deri altı doku hastalıkları
Seyrek: Kaşıntı ve cilt reaksiyonları
Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklar
Bilinmiyor: İntravenöz infüzyon sırasında, aşırı duyarlılık ve lokal ağrı
Şüpheli advers reaksiyonların raporlanması
Ruhsatlandırma sonrası şüpheli ilaç advers reaksiyonlarının raporlanması büyük önem taşımaktadır. Raporlama yapılması, ilacın yarar/risk dengesinin sürekli olarak izlenmesine olanak sağlar. Sağlık mesleği mensuplarının herhangi bir şüpheli advers reaksiyonu Türkiye Farmakovijilans Merkezi (TÜFAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr; e-posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99)
4.9. Doz aşımı ve tedavisi
Doz aşımında istenmeyen etkiler kısmında kayıtlı semptomlar daha ciddi olarak seyreder.
Spesifik antidotu yoktur. Kramp oluştuğunda diazepam verilmesi tavsiye edilir.
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Enfeksiyona karşı kullanılan ilaçlar
ATC kodu: P01AB03
Ornidazol 5-nitroimidazol türevi antibakteriyel ve antiprotozoal bir ilaçtır. İnvazif nitelikteki amebiyazis olgularında güçlü etkinlik gösterir. TİBERSİD, Bacteroides ve Clostridium türleri, Fusobacterium ve anaerob koklar gibi anaerob bakterilere ve Entomoeba hisyolytica'ya karşı etkilidir.
5.2. Farmakokinetik özellikler
Genel özelliklerEmilim:
İntravenöz yolla parenteral uygulanmaktadır.
Dağılım:
IV uygulamadan sonra ortalama dağılım hacmi kg başına 1 litredir. Ornidazolün plazma proteinlerine bağlanma oranı %13'tür. TİBERSİD'in etkin maddesi serebrospinal sıvıya, vücut sıvılarına ve dokulara etkili konsantrasyonlarda geçer. Değişik endikasyonlara göre plazma konsantrasyonlarının (6-36 mg/l) optimal aralıkta olduğu tahmin edilmektedir. Sağlıklı gönüllülerde 12 saatte bir tekrarlanan uygulamalardan sonra birikme faktörü 1,5-2,5 olarak hesaplanmıştır.
Biyotransformasyon:
Ornidazol karaciğerde başlıca 2-hidroksimetil ve α-hidroksimetil metabolitlerine metabolize olur. Değişmeyen ornidazole göre, bu iki metabolit Trichomonas vaginalis ve anaerobik bakterilere karşı daha az etkilidir.
Eliminasyon:
Yarı ömrü yaklaşık 13 saattir. Alınan tek dozun, %85'i çoğu metabolize olarak ilk 5 gün içinde atılır. Dozun %4'ü değişmeyen bileşik olarak idrarla atılmaktadır.
Doğrusallık/doğrusal olmayan durum Bulunmamaktadır.
5.3. Klinik öncesi güvenlilik verileri
Geçerli değildir.
6. FARMASÖTİK ÖZELLİKLER
6.1. Yardımcı maddelerin listesi
Etanol (susuz) Propilen glikol
6.2. Geçimsizlikler
250 ml serum fizyolojik veya dekstroz solüsyonunda 1 g ornidazol ve 2 g seftriakson fiziksel
ve kimyasal olarak geçimlidir. Ancak bu tıbbi ürün diğer tıbbi ürünlerle karıştırılmamalıdır.
6.3. Raf ömrü
36 ay
6.4. Saklamaya yönelik özel tedbirler
25°C altındaki oda sıcaklığında, ışıktan koruyarak saklayınız.
Uygulama için hazırlanan seyreltilmiş çözeltilerin mümkün olan en kısa zamanda kullanılması önerilir.
Bir defalık kullanım içindir. Kullanılmayan kısmı atınız. Son kullanma tarihiyle uyumlu olarak kullanınız.
Ambalajdaki son kullanma tarihinden sonra TİBERSİD'i kullanmayınız.
Eğer üründe ve/veya ambalajında bozukluklar fark ederseniz, TİBERSİD'i kullanmayınız.
6.5. Ambalajın niteliği ve içeriği
Şeffaf, Tip I cam ampullere doldurulmuş ürün, 3 ml'lik 1adet ampul içeren karton kutu içinde ambalajlıdır.
6.6. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemler
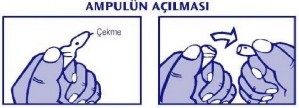
Nokta yukarıda bulunacak şekilde tutulur.
 Deri Kanseri
Deri kanseri çok rastlanan bir hastalıktır. Üç ana türü bulunur ;genelde kemirici ülser olarak bilinen bazal hücreli karsinom, yassı hücreli karsinom ve kötü huylu tümör.
Deri Kanseri
Deri kanseri çok rastlanan bir hastalıktır. Üç ana türü bulunur ;genelde kemirici ülser olarak bilinen bazal hücreli karsinom, yassı hücreli karsinom ve kötü huylu tümör. |
 Kolon, Rektum yada Bağırsak Kanseri
Bağırsak kanseri kolon veya rektumda
(arka geçit) herhangi bir bölgede ortaya çıkabilir.Kolorektal kanser erken safhalarda teşhis edilmesi halinde daha kolay ve daha başarılı bir
şekilde tedavi edilir.
Kolon, Rektum yada Bağırsak Kanseri
Bağırsak kanseri kolon veya rektumda
(arka geçit) herhangi bir bölgede ortaya çıkabilir.Kolorektal kanser erken safhalarda teşhis edilmesi halinde daha kolay ve daha başarılı bir
şekilde tedavi edilir. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| BITAZOL | 8699508750757 | 71.21TL |
| BITERAL | 8699525094667 | 241.20TL |
| BORNERAL | 8699623090011 | |
| DAGLEX | 8699479750411 | 71.21TL |
| ENFEXOL | 8680760091313 | |
| Diğer Eşdeğer İlaçlar |
 |
Artrit Artrit, oldukça yaygın bir hastalıktır ancak iyi anlaşılamamıştır. Aslında “artrit” tek bir hastalığın adı değildir; eklem ağrısı veya eklem hastalıklarını adlandırmanın gayri resmi yoludur. |
 |
Belsoğukluğu, Chlamydia ve Frengi Belsoğukluğu, bakterilerin sebep olduğu bir enfeksiyondur. Cinsel ilişki yoluyla bulaşır ve dölyatağı boynunda, idrar yollarında, anüste, makatta ve boğazda enfeksyona sebep olabilir. |
 |
Yüksek Tansiyon Hipertansiyon sürekli anormal derecede yüksek olan kan basıncıdır. Tansiyon atardamarlarınızdaki kanın basıncıdır. |
İLAÇ GENEL BİLGİLERİ
Menta Pharma İlaç San. Ve Tic. Ltd. Şti.
| Geri Ödeme Kodu | A12414 |
| Satış Fiyatı | 71.21 TL [ 18 Apr 2025 ] |
| Önceki Satış Fiyatı | 71.21 TL [ 14 Apr 2025 ] |
| Original / Jenerik | Jenerik İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8681332750072 |
| Etkin Madde | Ornidazol |
| ATC Kodu | J01XD03 |
| Birim Miktar | 500 |
| Birim Cinsi | MG |
| Ambalaj Miktarı | 1 |
| Enfeksiyona Karşı Kullanılan (Antienfektif) İlaçlar > Diğer Antibakteriyeller > Ornidazol |
| Yerli ve Beşeri bir ilaçdır. |