VENAPERTA 10000 ANTI-XA IU/1 ml enjeksiyonluk ��zelti i�eren kullan�ma haz�r enjekt�r (2 adet) K�sa �r�n Bilgisi
{ Enoksaparin Sodyum }
1. BE�ER� TIBB� �R�N�N ADI
VENAPERTA 10000 Anti-XA IU/1 mL enjeksiyonluk ��zelti i�eren kullan�ma haz�r enjekt�r Steril
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Enoksaparin sodyum: 100 mg (10.000 anti-Xa IU'ya e�de�er)
Enoksaparin sodyum, domuz intestinal mukozas�ndan �retilen heparin benzil esterin alkalin depolimerizasyonuyla elde edilen biyobenzer bir maddedir.
Yard�mc� maddeler
Yard�mc� maddeler i�in 6.1 'e bak�n�z.
3. FARMAS�T�K FORMU
Enjeksiyonluk ��zelti i�eren kullan�ma haz�r enjekt�r. Berrak, renksiz ��zelti
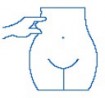
Karn�n�z�n sa� veya sol taraf�nda yanlar�na do�ru ve g�be�inizden en az 5 cm uzakta bir b�lge se�iniz.
UNUTMAYINIZ:
Enjeksiyonu g�be�inizden ve mevcut morluklar veya yara izlerinden en az 5 cm. uzak olacak bir noktaya yapmal�s�n�z. Enjeksiyon noktas�n� karn�n�z�n sa� ve sol yan�nda d�n���ml� olarak de�i�tirmelisiniz.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
VENAPERTA yeti�kinlerde a�a��daki durumlar�n tedavisinde endikedir:
�zellikle ortopedik cerrahi veya kanser cerrahisi dahil genel cerrahi ge�irenler olmak �zere, orta ve y�ksek riskli cerrahi uygulanan hastalarda ven�z tromboemboli profilaksisinde (venlerde p�ht� olu�umunun �nlenmesi)
Ven�z tromboemboli riski y�ksek akut kalp yetmezli�i, solunum yetmezli�i, ciddi enfeksiyonlar ve romatizmal hastal�klar� i�eren akut medikal hastal�klar� olan ve mobilitesi azalm�� hastalarda ven�z tromboemboli profilaksisinde
Hemodiyaliz s�ras�nda ekstrakorporeal dola��mda tromboz olu�umunun �nlenmesinde
Derin ven trombozu ve trombolitik tedavi veya cerrahi gerektirme ihtimali olan pulmoner emboli hari�, pulmoner emboli tedavisinde
Akut koroner sendrom:
Oral asetilsalisilik asit ile kombinasyon halinde, karars�z angina ve non ST-segment y�kselmeli miyokard infarkt�s� (NSTEMI) tedavisinde.
Medikal olarak tedavi edilen ya da daha sonra Perk�tan Koroner Giri�im uygulanan hastalar da dahil olmak �zere, akut ST-segment y�kselmeli miyokard infarkt�s�n�n (STEMI) tedavisi.
4.2. Pozoloji ve uygulama �ekli
Orta ve y�ksek riskli cerrahi hastalar�nda ven�z tromboemboli hastal���n�n profilaksisi:
Orta derecede tromboemboli riski olan hastalarda, �nerilen enoksaparin sodyum dozu subk�tan enjeksiyon yoluyla g�nde bir kez 2.000 IU'dur. (20 mg). Enoksaparin sodyumun
2.000 IU'luk (20 mg) preoperatif ba�lang�� dozunun (cerrahiden 2 saat �nce), orta derecede riskli cerrahide etkili ve g�venli oldu�u kan�tlanm��t�r.
Orta d�zeyde riskli hastalarda, iyile�me durumu (�rn. mobilite) ne olursa olsun, enoksaparin sodyum tedavisine en az 7-10 g�n devam edilmelidir. Hastan�n �nemli derecede azalm�� olan mobilitesinde d�zelme g�r�l�nceye kadar profilaksiye devam edilmelidir.
Y�ksek derecede tromboemboli riski olan hastalarda �nerilen enoksaparin sodyum dozu, tercihen cerrahiden 12 saat �nce ba�lat�lan ve subk�tan enjeksiyon ile g�nde bir kez verilen 4.000 IU 'dur (40 mg). Enoksaparin sodyum ile preoperatif profilaksiye 12 saatten daha �nce ba�lanmas� gerekiyorsa (�rn. ertelenmi� bir ortopedik cerrahiyi beklemekte olan y�ksek riskli hastalar), son enjeksiyon cerrahiden en ge� 12 saat �nce yap�lm�� olmal� ve cerrahiden 12 saat sonra tekrar ba�lanmal�d�r.
Maj�r ortopedik cerrahi uygulanan hastalar i�in, 5 haftaya varan geni�letilmi� tromboprofilaksi �nerilir.
Kanser nedeniyle abdominal ya da pelvik cerrahi ge�iren ven�z tromboembolizm (VTE) riski y�ksek hastalar i�in 4 haftaya varan geni�letilmi� tromboprofilaksi �nerilir.
4.3. Kontrendikasyonlar
Enoksaparin sodyum a�a��daki durumlarda kontrendikedir:
Enoksaparin sodyum, heparin ya da di�er d���k molek�l a��rl�kl� heparinler (DMAH) dahil olmak �zere heparin t�revlerine ya da B�l�m 6.1'de belirtilen yard�mc� maddelerden herhangi birine kar�� a��r� duyarl�l�k,
Son 100 g�n i�inde imm�n sistem arac�l� heparin ili�kili trombositopeni (HIT) �yk�s� veya dola��mda antikor varl��� (ayr�ca Bkz. B�l�m 4.4)
Klinik a��dan anlaml� aktif kanama ya da yak�n zamanda ge�irilmi� hemorajik inme, gastrointestinal �lser, y�ksek kanama riski olan malign neoplazm varl���, yak�n zamanda ge�irilmi� beyin, spinal veya oftalmik cerrahi, bilinen ya da ��phelenilen �zofageal varisler, arteriyoven�z malformasyonlar, vask�ler anevrizmalar ya da maj�r intraspinal veya intraserebral vask�ler anormallikler dahil y�ksek hemoraji riski olan durumlar
�nceki 24 saat i�inde tedavi i�in enoksaparin sodyum kullan�ld���nda spinal ya da epidural anestezi veya lokal-b�lgesel anestezi (Bkz. B�l�m 4.4)
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Genel:
Enoksaparin sodyum, di�er DMAH'lerle d�n���ml� olarak (bir birime bir birim) kullan�lamaz. Bu t�bbi �r�nler �retim prosesi, molek�ler a��rl�k, spesifik anti-Xa ve anti-IIa aktiviteleri, birim, dozaj ve klinik etkinlik ile g�venlilik a��s�ndan farkl�d�rlar. Bu da farmakokinetik ve ili�kili biyolojik aktivitelerinin (�rn. antitrombin aktivitesi ve trombosit etkile�imleri) farkl� olmas�na yol a�ar. Bu y�zden her �r�n�n spesifik kullan�m �ekline �zellikle dikkat edilmesi ve talimatlara uyulmas� gerekmektedir.
HIT �yk�s� (>100 g�n):
Son 100 g�n i�inde imm�n sistem arac�l� HIT �yk�s� veya dola��mda antikor varl��� s�z konusu olan hastalarda enoksaparin sodyum kullan�m� kontrendikedir. (Bkz. B�l�m 4.3). Antikorlar birka� y�l dola��mda kalabilir.
Enoksaparin sodyum, dola��mda antikor izlenmeyen heparin ili�kili trombositopeni �yk�s� (>100 g�n) olan hastalarda �ok dikkatli kullan�lmal�d�r. Bu tip durumlarda enoksaparin sodyum kullanma karar� yaln�zca dikkatli bir fayda-risk de�erlendirmesinden sonra ve heparin d��� alternatif tedavilerin (�rn. danaparoid sodyum veya lepirudin) d���n�lmesinin ard�ndan verilmelidir.
Trombosit say�lar�n�n izlenmesi:
Antikor arac�l� HIT riski DMAH'lerde de s�z konusudur. Trombositopeni ortaya ��karsa, genellikle enoksaparin sodyum tedavisinin ba�lang�c�n� takip eden 5. ve 21. g�nler aras�nda g�r�l�r.
Postoperatif hastalarda HIT riski daha y�ksektir ve genelde kardiyak cerrahi sonras� ile kanser hastalar�nda meydana gelir.
Bu y�zden enoksaparin sodyum ile tedaviye ba�lamadan �nce ve daha sonra tedavi s�ras�nda d�zenli olarak trombosit say�lar�n�n �l��lmesi tavsiye edilir.
HIT d���nd�ren klinik semptomlar s�z konusuysa (herhangi bir yeni arteriyel ve/veya ven�z tromboembolizm olay�, enjeksiyon yerinde herhangi bir a�r�l� cilt lezyonu, tedavi s�ras�nda herhangi bir alerjik ya da anafilaktoid reaksiyon), trombosit say�s� �l��lmelidir. Hastalar bu semptomlar�n meydana gelebilece�ini bilmeli ve e�er olursa birinci basamak hekimlerine bilgi vermelidir.
Pratikte trombosit say�s�nda do�rulanm�� anlaml� bir azalma g�zlenirse (ba�lang�� de�erinin
%30-50'si) enoksaparin sodyum tedavisi hemen kesilmeli ve hasta heparin d���nda alternatif ba�ka bir antikoag�lan tedavisine ge�irilmelidir.
Hemoraji:
Di�er antikoag�lanlarla oldu�u gibi herhangi bir yerde kanama meydana gelebilir. E�er kanama meydana gelirse hemorajinin k�keni ara�t�r�lmal� ve uygun tedavi tayin edilmelidir.
T�m di�er antikoag�lan tedavilerinde oldu�u gibi enoksaparin sodyum da, kanama potansiyelinin artt��� a�a��daki durumlarda dikkatle kullan�lmal�d�r:
Bozulmu� hemostaz,
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
E�zamanl� kullan�m �nerilmez:
Hemostaz� etkileyen ila�lar (Bkz. B�l�m 4.4)
E�er kesin olarak endike de�ilse hemostaz� etkileyen ajanlar�n enoksaparin sodyum tedavisinden �nce kesilmesi �nerilmektedir. Kombinasyon endikasyonu varsa, enoksaparin sodyum uygun durumlarda dikkatli klinik ve laboratuvar takip e�li�inde kullan�lmal�d�r. Bu ajanlar aras�nda a�a��daki gibi t�bbi �r�nler bulunmaktad�r:
4.6. Gebelik ve laktasyon
Genel tavsiye
Gebelik kategorisi: B
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
Deneysel ara�t�rmalar bir fetotoksisite veya teratojenite bulgusu ortaya koymam��t�r.
Gebelik d�nemi
�nsanlarda, enoksaparin sodyumun gebeli�in ikinci ve ���nc� trimesteri s�ras�nda plasenta bariyerini ge�ti�ine ili�kin herhangi bir bulgu yoktur. Birinci trimesterle ilgili herhangi bir bilgi bulunmamaktad�r.
Hayvanlardaki �al��malarda herhangi bir fetotoksisite ya da teratojenite bulgusu ile kar��la��lmam��t�r (Bkz. B�l�m 5.3). Hayvanlardaki verilere g�re enoksaparin sodyumun plasentadan ge�i�i minimaldir. �nsanlara y�nelik potansiyel risk bilinmemektedir.
Gebe kad�nlara verilirken tedbirli olunmal�d�r.
Enoksaparin sodyum gebelikte yaln�zca hekimin a��k�a gerekli g�rd��� durumlarda kullan�lmal�d�r.
Enoksaparin sodyum kullanan gebe kad�nlar kanama ya da a��r� antikoag�lasyon a��s�ndan yak�ndan takip edilmeli ve hemorajik risk konusunda uyar�lmal�d�r. Gebe kad�nlarda gebe olmayan kad�nlara g�re hemoraji, trombositopeni ya da osteoporoz riskinde art�� oldu�una ili�kin genel bir bulgu yoktur ve bu riskler prostetik kalp kapa�� olan kad�nlarla s�n�rl�d�r (Bkz. B�l�m 4.4).
Epidural anestezi planlanan kad�nlarda i�lem �ncesinde enoksaparin sodyum tedavisinin kesilmesi �nerilir (Bkz. B�l�m 4.4).
Laktasyon d�nemi
Enoksaparin sodyumun insan s�t�ne de�i�meden ge�ip ge�medi�i bilinmemektedir. Emziren s��anlarda, Enoksaparin sodyum ya da metabolitlerinin s�te ge�i�i �ok azd�r. Enoksaparin sodyumun oral emilim olas�l��� d���kt�r. VENAPERTA emzirme s�ras�nda kullan�labilir.
�reme yetene�i/Fertilite
Enoksaparin sodyumun fertilite �zerindeki etkilerine ili�kin klinik veri mevcut de�ildir. Hayvanlardaki �al��malarda fertilite �zerinde herhangi bir etki g�r�lmemi�tir (Bkz. B�l�m 5.3).
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
Ara� ve makine kullan�m� �zerine bilinen herhangi bir etkisi bulunmamaktad�r.
4.8. �stenmeyen etkiler
G�venlilik profilinin �zeti
Enoksaparin, klinik �al��malarda enoksaparin alan 15.000'den fazla hastada de�erlendirilmi�tir. Bunlar, tromboembolik komplikasyonlar a��s�ndan risk alt�ndaki hastalarda ortopedik veya abdominal cerrahiyi takiben derin ven trombozunun profilaksisi i�in 1.776, hareket yetene�i �iddetli �l��de k�s�tlanm�� akut medikal hastalarda derin ven trombozunun profilaksisi i�in 1.169, pulmoner embolizmin e�lik etti�i veya etmedi�i derin ven trombozunun tedavisi i�in
559, karars�z angina ve Q-dalgas�z miyokard infarkt�s�n�n tedavisi i�in 1.578 ve akut ST- y�kselmeli miyokard infarkt�s�n�n tedavisi i�in 10.176 hastay� i�ermi�tir.
Bu klinik �al��malarda uygulanan enoksaparin sodyum rejimi endikasyonlara ba�l� olarak farkl�l�k g�stermektedir. Cerrahi ge�iren ya da mobilitesi ciddi �ekilde k�s�tlanm�� akut hastal��� bulunan olgularda derin ven trombozu profilaksisi i�in kullan�lan enoksaparin sodyum dozu g�nde bir kez olmak �zere S.C. yolla 4.000 IU (40 mg)'d�r. Pulmoner embolizmin (PE) e�lik etti�i veya etmedi�i derin ven trombozunun (DVT) tedavisinde, enoksaparin alan hastalar 12 saatte bir 100 IU/kg (1 mg/kg) subk�tan dozu ya da g�nde bir kez 150 IU/kg (1,5 mg/kg) subk�tan dozu ile tedavi edilmi�tir. Karars�z angina ve Q-dalgas�z miyokard infarkt�s�n�n tedavisi i�in klinik �al��malarda, dozlar 12 saatte bir 100 IU/kg (1 mg/kg) subk�tan olmu� ve akut ST-y�kselmeli miyokard infarkt�s�n�n tedavisi i�in klinik �al��mada enoksaparin sodyum rejimi 3.000 IU'luk (30 mg) IV bolusu takiben 12 saatte bir 100 IU/kg (1 mg/kg) subk�tan olmu�tur.
Enoksaparin tedavisi ile ili�kili olarak akut generalize ekzantemat�z p�st�loz (AGEP) bildirilmi�tir (Bkz. B�l�m 4.4).
Klinik �al��malarda en s�k bildirilen reaksiyonlar hemoraji, trombositopeni ve trombositozdur (Bkz. B�l�m 4.4 ve a�a��da “Se�ilmi� advers reaksiyonlar�n tan�m�”).
Bu klinik �al��malarda g�zlenen ve pazarlama sonras� deneyimde bildirilen advers etkiler a�a��da ayr�nt�l� olarak verilmektedir.
�stenmeyen etkiler a�a��daki s�kl�k derecelerine g�re s�n�fland�r�l�r:
�ok yayg�n (≥ 1/10); yayg�n (≥ 1/100 ila < 1/10); yayg�n olmayan (≥ 1/1.000 ila < 1/100); seyrek (≥ 1/10.000 ila <1/1.000); ve �ok seyrek (< 1/10.000); bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Kan ve lenf sistemi hastal�klar�
Yayg�n: Hemoraji, hemorajik anemi *, trombositopeni, trombositoz
Seyrek: Eozinofili*, tromboz ile birlikte imm�no-alerjik trombositopeni geli�en vakalar; bunlar�n baz�lar�nda tromboz ile birlikte organ enfarkt�s� ya da ekstremite iskemisi g�r�lm��t�r (Bkz. B�l�m 4.4).
Ba����kl�k sistemi hastal�klar�
Yayg�n: Alerjik reaksiyon
Seyrek: Anafilaktik/anafilaktoid reaksiyonlar (�ok dahil)*
Sinir sistemi hastal�klar�
Yayg�n: Ba� a�r�s� *
Vask�ler hastal�klar�
Seyrek: Spinal hematom * (ya da n�raksiyal hematom). Bu reaksiyonlar uzun s�reli ya da kal�c� paraliz dahil de�i�ik derecelerde n�rolojik hasara yol a�m��t�r (Bkz. B�l�m 4.4).
Hepato-bilier hastal�klar�
�ok yayg�n: Karaci�er enzimlerinde art�� (ba�l�ca: transaminaz d�zeyi > 3 x normal �st s�n�r) Yayg�n olmayan: Hepatosel�ler karaci�er hasar� *
Seyrek: Kolestatik karaci�er hasar� *
Deri ve deri alt� doku hastal�klar� Yayg�n: �rtiker, ka��nt�, eritem Yayg�n olmayan: B�ll�z dermatit
Seyrek: Alopesi *, Kutan�z vask�lit*, genellikle enjeksiyon b�lgesinde cilt nekrozu* (bu fenomenlerden �nce genellikle a�r�l� ve infiltratif purpura ya da eritemat�z plaklar g�r�lm��t�r) Enjeksiyon b�lgesinde nod�ller* (kistik enoksaparin i�eri�i olmayan enflamatuvar nod�ller). Birka� g�n i�inde iyile�mekte ve tedavinin b�rak�lmas�na yol a�mamaktad�rlar.
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar�
Seyrek: Uzun s�reli tedavinin ard�ndan osteporoz * (tedavi s�resi > 3 ay)
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar�
Yayg�n: Enjeksiyon b�lgesinde hematom, enjeksiyon b�lgesinde a�r�, enjeksiyon b�lgesinde di�er reaksiyonlar (�rn. �dem, hemoraji, hipersensitivite, enflamasyon, kitle, a�r� ya da reaksiyon)
Yayg�n olmayan: Enjeksiyonb�lgesinde cilt nekrozu, lokal irritasyon
Ara�t�rmalar
Seyrek: Hiperkalemi * (Bkz. B�l�m 4.4 ve 4.5)
Se�ilmi� advers reaksiyonlar�n tan�m� Hemorajiler
Bunlar aras�nda hastalar�n en fazla % 4,2' sinde (cerrahi hastalar) bildirilen maj�r hemorajiler bulunmaktad�r. Bu olgular�n baz�lar� �l�mle sonu�lanm��t�r. Cerrahi hastalarda hemorajik komplikasyonlar a�a��daki durumlarda maj�r kabul edilmi�tir: (1) hemoraji �nemli bir klinik olaya yol a�t���nda ya da (2) hemoglobinde ≥ 2 g/dL d����le birlikte ger�ekle�ti�inde veya ≥ 2 �nite kan �r�n� transf�zyonu gerektirdi�inde. Retroperitoneal ve intrakraniyal hemorajiler her durumda maj�r kabul edilmi�tir.
Di�er antikoag�lanlarda oldu�u gibi, hemoraji a�a��daki gibi ili�kili risk fakt�rlerinin varl���nda ortaya ��kabilir: Kanamaya yatk�n organik lezyonlar, invazif i�lemler ya da hemostaz� etkileyen ila�lar�n e� zamanl� kullan�m� (Bkz. B�l�m 4.4 ve 4.5).
Sistem organ s�n�f� | Cerrahi hastalar�nda profilaksi | Medikal hastalarda profilaksi | DVT (PE varl���nda ve yoklu�unda) | Karars�z angina ve Q- dalgas�z MI olan hastalarda tedavi | Akut STEMI olan hastalarda tedavi |
Kan ve lenf sistemi hastal�klar � | �ok yayg�n: Hemoraji*
Seyrek: Retroperitonea l hemoraji | Yayg�n: Hemoraji * | �ok yayg�n: Hemoraji*
Yayg�n olmayan: �ntrakraniyal hemoraji, Retroperitonea l hemoraji | Yayg�n: Hemoraji*
Seyrek: Retroperitonea l hemoraji | Yayg�n: Hemoraji*
Yayg�n olmayan: �ntrakraniyal hemoraji, Retroperitonea l hemoraji |
*: �rn. hematom, enjeksiyon b�lgesi d���ndaki ekimoz, yarada hematom, hemat�ri, epistaksis ve gastrointestinal kanama.
Trombositopeni ve trombositoz
Sistem organ s�n�f� | Cerrahi hastalar�nda profilaksi | Medikal hastalarda profilaksi | DVT (PE varl���nda ve yoklu�unda) | Karars�z angina ve Q- dalgas�z MI olan hastalarda tedavi | Akut STEMI olan hastalarda tedavi |
Kan ve lenf sistemi hastal�klar | �ok yayg�n: Trombositoz*
Yayg�n: Trombositope ni | Yayg�n olmayan: Trombosit openi | �ok yayg�n: Trombositoz *
Yayg�n: Trombositop eni | Yayg�n olmayan: Trombositop eni | Yayg�n: Trombositoz* Trombositopeni
�ok seyrek: �mmuno-alerjik trombositopeni |
*: Trombosit art��� > 400 g/L
Pediyatrik pop�lasyon
�ocuklarda enoksaparin sodyumun etkililik ve g�venlili�i belirlenmemi�tir (Bkz. B�l�m 4.2).
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)' ne bildirmeleri gerekmektedir. (www.titck.gov.tr; e- posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0312 218 35 99)
4.9. Doz a��m� ve tedavisi
Belirti ve semptomlar:
�ntraven�z, ekstrakorporeal veya subk�tan enoksaparin sodyumun kazara doz a��m� hemorajik komplikasyonlara yol a�abilir. B�y�k dozlarda olsa dahi oral uygulamay� takiben enoksaparin sodyumun absorbe olmas� m�mk�n de�ildir.
Antidotu ve tedavisi:
Antikoag�lan etkiler protaminin yava� intraven�z enjeksiyonu ile b�y�k �l��de n�tralize edilebilmektedir. Protamin dozu enjekte edilen enoksaparin sodyum dozuna ba�l� olup, enoksaparin sodyum son 8 saat i�inde uygulanm�� ise 1 mg protamin 100 IU (1 mg) enoksaparin sodyumun antikoag�lan etkisini n�tralize etmektedir. Enoksaparin sodyum uygulanmas�n�n �st�nden 8 saatten daha uzun zaman ge�mi� ise veya ikinci bir protamin dozunun gerekli oldu�u belirlenmi� ise, 100 IU (1 mg) enoksaparin sodyum ba��na 0.5 mg protamin inf�zyonu uygulanabilir. Enoksaparin sodyum enjeksiyonundan 12 saat sonra, protamin uygulanmas�na gerek duyulmayabilir. Bununla birlikte, y�ksek protamin dozlar�yla dahi, enoksaparin sodyumun anti-Xa aktivitesi hi�bir zaman tam olarak n�tralize edilmez (maksimum yakla��k
%60) (Bkz. protamin tuzlar�n�n re�ete bilgileri).
��ne kapa��n� dikkatlice VENAPERTA enjekt�r�nden ��kar�n�z. Kapa�� atabilirsiniz. ��ne dolu ve kullan�ma haz�rd�r.
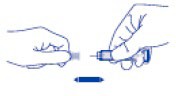
Hava kabarc�klar�n� uzakla�t�rmak amac�yla kendinize enjeksiyon yapmadan �nce enjekt�r pistonuna BASTIRMAYINIZ. Bu ilac�n miktar�n�n azalmas�na neden olabilir. Kapa��
��kard�ktan sonra, i�nenin temiz kalmas�n� (steril) sa�lamak i�in i�neyi herhangi bir yere temas ettirmeyiniz.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Heparinler, Antitrombotik ajan ATC kodu: B01AB05
Farmakodinamik etkiler
Enoksaparin ortalama molek�ler a��rl��� yakla��k 4.500 dalton olan ve standart heparinin antitrombotik ve antikoagulan aktivitelerini ayr��t�ran bir DMAH'dir. Etkin madde sodyum tuzudur.
VENAPERTA biyobenzer bir ila�t�r.
In vitro safla�t�r�lm�� sistemde enoksaparin sodyum y�ksek anti-Xa aktivite (yakla��k 100 IU/mg) ve d���k anti-IIa ya da anti-trombin aktivitesi g�sterir (yakla��k 28 IU/mg); bunlar aras�ndaki oran 3,6'd�r. Antikoagulan aktiviteye anti-trombin III (ATIII) etkisi arac�l�k eder ve insanlarda anti-trombotik aktivite sa�lan�r.
Sa�l�kl� ki�ilerde, hastalarda ve klinik d��� modellerde enoksaparinin anti-Xa/IIa aktivitesine ek
antitrombotik ve anti-inflamatuvar �zelliklere sahip oldu�u belirlenmi�tir.
Bunlar aras�nda, fakt�r VIIa gibi di�er koagulasyon fakt�rlerinin ATIII'e ba��ml� inhibisyonu, endojen Doku Fakt�r� Yola�� �nhibit�r (TFPI) sal�verilmesi ve vask�ler endotelden kan dola��m�na vWF (von Willebrand fakt�r�) sal�n�m�ndaki azalma bulunmaktad�r. Bu fakt�rlerin enoksaparin sodyumun genel antitrombotik etkisine katk� sa�lad�klar� bilinmektedir.
Profilaktik bir tedavi olarak kullan�ld���nda, enoksaparin sodyum aPTT'yi �nemli �l��de etkilemez. K�ratif tedavi olarak kullan�ld���nda, doruk aktivite esnas�nda aPTT kontrole g�re 1,5 - 2,2 kez uzayabilir.
Klinik etkililik ve g�venlilik
Cerrahiyle ili�kili ven�z tromboembolik hastal���n �nlenmesi
- Ortopedik cerrahi sonras� uzun s�reli VTE profilaksisi
Kal�a replasman cerrahisi uygulanan hastalarda uzun s�reli profilaksiyi de�erlendiren bir �ift k�r �al��mada, daha �nce ven�z tromboembolik hastal�k �yk�s� bulunmayan 179 hasta hastanede yat��lar� s�ras�nda 4.000 IU (40 mg) enoksaparin sodyum ile tedavi edilmi�ler ve taburculuk sonras� 3 hafta s�reyle g�nde bir kez S.C. yolla 4.000 IU enoksaparin sodyum (n=90) ya da plasebo kullanacak (n=89) �ekilde randomize edilmi�lerdir. Uzun s�reli profilaksi s�ras�nda DVT insidans� enoksaparin sodyum grubunda plaseboya g�re anlaml� �l��de daha d���k bulunmu� ve PE bildirilmemi�tir. Maj�r kanama kaydedilmemi�tir.
Etkililik verileri a�a��daki tabloda sunulmu�tur.
| Enoksaparin sodyum 4.000 IU (40 mg) g�nde bir kez S.C. n (%) | Plasebo g�nde bir kez S.C. n (%) |
Uzun S�reli Profilaksi Uygulanan T�m Hastalar | 90 (100) | 89 (100) |
Total VTE | 6 (6,6) | 18 (20,2) |
Total DVT (%) | 6 (6,6) | 18 (20,2) |
Proksimal DVT (%) | 5 (5,6) | 7 (8,8) |
*p de�eri plaseboya kar�� =0,008 #p de�eri plaseboya kar�� =0,537 | ||
�kinci bir �ift k�r �al��mada, VTE'si olmayan ve kal�a replasman cerrahisi uygulanan 262 hastaya ba�lang��ta hastanede yat�� s�ras�nda 4.000 IU (40 mg) S.C. enoksaparin sodyum uygulanm�� ve bu hastalar taburcu edildikten sonra 3 hafta s�reyle g�nde bir kez S.C. yolla
4.000 IU (40 mg) (n=131) enoksaparin sodyum ya da plasebo (n=131) kullanacak �ekilde randomize edilmi�lerdir. �lk �al��maya benzer �ekilde, uzun s�reli profilaksi s�ras�nda VTE insidans� enoksaparin grubunda hem total VTE (enoksaparin sodyum 21 (%16)'e kar�� plasebo 45 (%34,4); p=0,001) hem de proksimal DVT (enoksaparin sodyum 8 (%6,1)'e kar�� plasebo 28 (%21,4); p < 0,001) i�in daha d���k bulunmu�tur. Enoksaparin sodyum ve plasebo gruplar� aras�nda maj�r kanama a��s�ndan anlaml� fark belirlenmemi�tir.
Kanser cerrahisi sonras� uzun s�reli DVT profilaksisi
�ift k�r, �ok merkezli bir �al��mada abdominal ya da pelvik kanser nedeniyle elektif cerrahi uygulanan 332 hastada d�rt hafta ya da bir hafta s�reli enoksaparin sodyum profilaksisi etkililik ve g�venlilik a��s�ndan kar��la�t�r�lm��t�r. Hastalar 6-10 g�n s�reyle enoksaparin sodyum tedavisi alm��lar (4.000 IU (40 mg) S.C.) ve ard�ndan 21 g�n s�reyle enoksaparin sodyum ya da plasebo kullanacak �ekilde randomize edilmi�lerdir. Bilateral venografi 25-31. g�nler aras�nda ger�ekle�tirilmi�tir (ven�z tromboembolizm semptomlar� geli�irse daha erken). Hastalar �� ay s�reyle izlenmi�tir. Abdominal ya da pelvik kanser cerrahisi sonras�nda d�rt hafta s�reli enoksaparin sodyum profilaksisi, bir hafta s�reli enoksaparin sodyum profilaksisi ile kar��la�t�r�ld���nda venografi ile g�sterilmi� tromboz insidans�n� anlaml� �l��de azaltm��t�r. �ift k�r faz sonunda ven�z tromboembolizm oranlar� plasebo grubunda %12,0 (n=20) ve
enoksaparin sodyum grubunda %4,8 (n=8) olarak belirlenmi�tir (p=0,02). Bu farkl�l�k ���nc� ayda devam etmi�tir (%13,8'e kar�� %5,5 (n=23'e kar�� 9), p=0,01). �ift k�r fazda ya da izlem faz�nda kanama ya da di�er komplikasyonlar a��s�ndan farkl�l�k belirlenmemi�tir.
Hareket k�s�tl�l���na yol a�mas� beklenen akut hastal��� olan ki�ilerde ven�z tromboembolik hastal�k profilaksisi
Akut hastal�k s�ras�nda hareketlili�i �nemli �l��de k�s�tlanm�� (y�r�me mesafesi ≤ 3 g�n s�reyle < 10 metre) hastalarda DVT profilaksisi i�in g�nde bir kez 2.000 IU (20 mg) S.C. enoksaparin sodyum, g�nde bir kez 4.000 IU (40 mg) S.C. enoksaparin sodyum ve plasebo kar��la�t�rmak amac�yla �ift k�r, �ok merkezli, paralel gruplu bir �al��ma ger�ekle�tirilmi�tir. �al��maya kalp yetmezli�i (NYHA S�n�f� III ya da IV); akut solunum yetmezli�i ya da komplikasyonlu kronik solunum yetmezli�i, akut infeksiyonu, akut romatizmal hastal��� ve en az bir VTE risk fakt�r� (ya� ≥ 75, kanser, ge�irilmi� VTE, obezite, varik�z venler, hormon terapisi, kronik kalp hastal��� ya da solunum yetmezli�i) olan hastalar kat�lm��t�r.
�al��maya toplam 1.102 hasta kaydedilmi� ve 1.073 hasta tedavi edilmi�tir. Tedavi 6-14 g�n s�rd�r�lm��t�r (medyan tedavi s�resi 7 g�n). G�nde bir kez S.C. yolla uygulanan 4.000 IU (40 mg) enoksaparin sodyum, plasebo ile kar��la�t�r�ld���nda VTE insidans�n� anlaml� �l��de d���rm��t�r. Etkililikle ilgili veriler a�a��daki tabloda sunulmaktad�r.
| Enoksaparin sodyum 2.000 IU (20 mg) g�nde bir kez S.C. n (%) | Enoksaparin sodyum 4.000 IU (40 mg) g�nde bir kez S.C. n (%) | Plasebo n (%) |
Akut Hastal�k S�ras�nda Tedavi Edilen T�m Olgular |
287 (100) |
291(100) |
288 (100) |
Total VTE (%) | 43 (15,0) | 16 (5,5)* | 43 (14,9) |
Total DVT (%) | 43 (15,0) | 16 (5,5) | 40 (13,9) |
Proksimal DVT (%) | 13 (4,5) | 5 (1,7) | 14 (4,9) |
VTE = ven�z tromboembolik olaylar; bunlar aras�nda DVT, PE, ve tromboembolik k�kenli oldu�u d���n�len �l�m bulunmaktad�r * p de�eri, plaseboya kar�� =0,0002 | |||
�al��ma kay�t tarihinden yakla��k 3 ay sonra enoksaparin sodyum 4.000 IU (40 mg) grubundaki VTE insidans� plasebo grubuna anlaml� �l��de daha d���k kalmay� s�rd�rm��t�r. Total ve maj�r kanama olaylar�n�n s�kl��� plasebo grubunda %8,6 ve %1,1, enoksaparin sodyum 2.000 IU (20 mg) grubunda %11,7 ve %0,3 ve enoksaparin sodyum 4.000 IU (40 mg) grubunda ise
%12,6 ve %1,7 olarak belirlenmi�tir.
Pulmoner embolizmin e�lik etti�i ya da etmedi�i derin ven trombozunun tedavisi
PE'nin e�lik etti�i ya da etmedi�i akut alt ekstremite DVT'si olan 900 hastan�n kat�ld��� �ok merkezli, paralel gruplu bir �al��mada olgular hastanede a�a��daki tedavi gruplar�na randomize edilmi�tir: (i) enoksaparin sodyum 150 IU/kg (1,5 mg/kg) g�nde bir kez S.C., (ii) enoksaparin sodyum 100 IU/kg (1 mg/kg) her 12 saatte bir S.C., ya da (iii) heparin IV bolus (5,000 IU) ve sonras�nda s�rekli inf�zyon (aPTT 55-85 saniye olacak �ekilde). T�m hastalara ayn� zamanda, enoksaparin sodyum ya da standart heparin tedavisini izleyen ilk 72 saat i�erisinde varfarin sodyum tedavisi de ba�lanm�� (protrombin zaman�na g�re INR 2,0-3,0 olacak �ekilde) ve bu tedavi 90 g�n s�reyle devam ettirilmi�tir. Enoksaparin sodyum ya da standart heparin tedavisi minimum 5 g�n s�reyle ve hedeflenen varfarin sodyum INR'sine ula��lana kadar s�rd�r�lm��t�r. Her iki enoksaparin sodyum rejimi yineleyen ven�z tromboembolizm riskini (DVT ve/veya PE) azaltmak a��s�ndan standart heparin tedavisine e�de�er bulunmu�tur. A�a��daki tabloda etkililik verileri sunulmaktad�r.
| Enoksaparin sodyum 150 IU/kg (1,5 mg/kg) g�nde bir kez S.C. n (%) | Enoksaparin sodyum 100 IU/kg (1 mg/kg) g�nde iki kez S.C. n (%) | Heparin aPTT'ye g�re ayarl� IV Terapi n (%) |
PE'li ya da PE'siz tedavi edilmi� t�m DVT hastalar� |
298 (100) |
312 (100) |
290 (100) |
Total VTE (%) | 13 (4,4)* | 9 (2,9)* | 12 (4,1) |
Yaln�zca DVT (%) | 11 (3,7) | 7 (2,2) | 8 (2,8) |
Yaln�zca DVT (%) | 9 (3,0) | 6 (1,9) | 7 (2,4) |
PE (%) | 2 (0,7) | 2 (0,6) | 4 (1,4) |
VTE = ven�z tromboembolik olay (DVT ve/veya PE) *Total VTE i�in tedavi farklar�na ili�kin %95 g�ven aral���: | |||
Heparine kar�� g�nde bir kez enoksaparin sodyum (-3 ila 3,5)
5.2. Farmakokinetik �zellikler
Genel �zellikler
Enoksaparin sodyumun farmakokinetik parametreleri, esas olarak; plazma anti-Xa aktivitesinin zaman s�reci ve ayr�ca anti-IIa aktivitesi a��s�ndan, �nerilen dozaj aral�klar�nda; tekli ve tekrarlanan subk�tan uygulamadan sonra ve tekli intraven�z uygulamadan sonra incelenmi�tir.
Anti-Xa ve anti-IIa farmakokinetik aktivitelerin kantitatif tayini, validasyonu yap�lm�� amidolitik y�ntemler kullan�larak ger�ekle�tirilmi�tir.
Emilim:
Subk�tan enjeksiyonun ard�ndan anti-Xa aktivitesine dayanarak enoksaparin sodyumun mutlak biyoyararlan�m� % 100'e yak�nd�r.
Farkl� dozlar ve doz rejimleri kullan�labilir.
Ortalama maksimum plazma anti-Xa aktivitesi subk�tan enjeksiyondan 3-5 saat sonra g�zlenmekte ve 2.000 IU, 4.000 IU, 100 IU/kg ve 150 IU/kg (20 mg, 40 mg, 1 mg/kg ve 1,5 mg/kg) dozlar�n�n tek subk�tan uygulanmas�n� takiben s�ras�yla yakla��k 0,2; 0,4; 1 ve 1,3 anti- Xa IU/mL'ye ula�maktad�r.
3.000 IU (30 mg) dozda IV bolus ve hemen ard�ndan subk�tan yolla 12 saatte bir uygulanan 1 mg/kg, 1,16 IU/mL'lik ba�lang�� pik anti-Fakt�r Xa d�zeyleri (n = 16) ve sabit durum d�zeylerinin %88'ine kar��l�k gelen bir ortalama etkilenim sa�lam��t�r. Sabit duruma tedavinin ikinci g�n�nde ula��lmaktad�r.
Sa�l�kl� g�n�ll�lerde g�nde bir kez 4.000 IU (40 mg) ve g�nde bir kez 150 IU/kg (1,5 mg/kg) rejimlerinin tekrarlanan subk�tan uygulanmas�n� takiben, tek doz sonras�na k�yasla yakla��k
%15 daha y�ksek bir ortalama maruz kalma oran� ile sabit duruma 2. g�n ula��lmaktad�r. G�nde iki kez 100 IU/kg'l�k (1 mg/kg) rejiminin tekrarlanan subk�tan uygulanmas�n� takiben sabit duruma 3. g�n ile 4. g�n aras�nda ula��lmakta olup, tek doz sonras�na k�yasla yakla��k %65 daha y�ksek bir ortalama maruz kalma oran� ve s�ras�yla yakla��k 1,2 ve 0,52 IU/mL'lik ortalama pik ve taban d�zeyleri saptanmaktad�r.
Sa�l�kl� g�n�ll�lerde 100-200 mg/mL'lik doz aral���nda enjeksiyon hacmi ve doz konsantrasyonu farmakokinetik parametreleri etkilememektedir.
Enoksaparin sodyumun farmakokinetik profili �nerilen doz aral���nda lineer g�r�n�ml�d�r. Hastalar aras�nda ve ayn� hasta i�inde de�i�kenlik d���kt�r. Tekrarlanan S.C. uygulamalardan sonra birikim g�r�lmez.
Subk�tan uygulamadan sonra plazma anti-IIa aktivitesi anti-Xa aktivitesine k�yasla yakla��k 10 kat daha d���kt�r. Ortalama maksimum anti-IIa aktivitesi subk�tan uygulamadan yakla��k 3-4 saat sonra g�zlenmekte ve g�nde iki kez 100 IU/kg (1 mg/kg) ve g�nde bir kez 150 IU/kg'�n
(1,5 mg/kg) tekrarlanan uygulanmas�n� takiben s�ras�yla 0,13 IU/mL ve 0,19 IU/mL'ye ula�maktad�r.
Da��l�m:
Enoksaparin sodyum anti-Xa aktivitesinin da��l�m hacmi yakla��k 4,3 litredir ve kan hacmine yak�nd�r.
Biyotransformasyon:
Enoksaparin sodyum esas olarak karaci�erde, depolimerizasyon ve/veya des�lfasyon yoluyla son derece azalm�� biyolojik potense sahip d���k molek�l a��rl�kl� t�rlere metabolize olmaktad�r.
Eliminasyon:
Enoksaparin sodyum d���k klirensli bir ila�t�r ve 150 IU/kg'l�k (1,5 mg/kg) 6-saatlik IV
inf�zyondan sonra ortalama anti-Xa plazma klirensi 0,74 L/sa d�zeyindedir.
Eliminasyon monofazik g�r�n�ml�d�r ve yar�lanma �mr� tek S.C. doz sonras�nda 5 saat ve tekrarlanan dozlardan sonra 7 saat civar�ndad�r.
Aktif metabolitlerin renal klirensi uygulanan dozun yakla��k %10'unu ve aktif ve aktif olmayan metabolitlerin renal at�l�m� dozun %40'�n� temsil etmektedir.
Do�rusall�k/do�rusal olmayan durum:
Veri bulunmamaktad�r.
Hastalardaki karakteristik �zellikler Ya�l�lar:
Bir pop�lasyon farmakokinetik analizinin sonu�lar�na g�re, enoksaparin sodyumun kinetik profili b�brek fonksiyonu normal oldu�unda ya�l� bireylerde gen� bireylere k�yasla farkl�l�k g�stermemektedir. Bununla birlikte, b�brek fonksiyonu ya�la birlikte d��t���nden, ya�l� hastalarda enoksaparin sodyum eliminasyonu azalma g�sterebilir (Bkz. B�l�m 4.4, 4.2 ve 5.2).
Karaci�er yetmezli�i:
�leri evreli sirozu olan ve g�nde bir kez 4.000 IU (40 mg) enoksaparin sodyum ile tedavi edilen hastalarda, maksimum anti-Xa aktivitesindeki azalma ile hepatik yetmezli�in �iddetindeki art�� (Child-Pugh kategorisiyle de�erlendirilmi�tir) aras�nda ili�ki saptanm��t�r. Bu azalman�n ana sebebi, hepatik yetmezli�i olan hastalarda ATIII sentezindeki azalmaya ba�l� olarak ATIII d�zeylerinin de azalmas�d�r.
B�brek Yetmezli�i:
Sabit durumda anti-Xa plazma klirensi ile kreatinin klirensi aras�nda do�rusal bir ili�ki g�zlenmi�tir ve bu, b�brek fonksiyonu bozulmu� hastalarda enoksaparin sodyum klirensinin azald���n� g�stermektedir. Sabit durumda e�ri alt�nda kalan alan (EAA) ile ifade edilen anti-Xa maruz kalma, tekrarlanan g�nde bir kez subk�tan 4.000 IU (40 mg) dozlar�ndan sonra hafif b�brek yetmezli�i (kreatinin klirensi 50-80 mL/dk) ve orta derecede b�brek yetmezli�i
(kreatinin klirensi 30-50 mL/dk) olan hastalarda k���k bir art�� g�stermektedir. A��r b�brek yetmezli�i (kreatinin klirensi<30 mL/dk) olan hastalarda ise, sabit durumda EAA, tekrarlanan g�nde bir kez subk�tan 4.000 IU (40 mg) dozlar�ndan sonra ortalama %65 oran�nda anlaml� bir art�� g�stermektedir (Bkz. B�l�m 4.4 ve 4.2).
Kilo:
Tekrarlanan g�nde bir kez subk�tan 150 IU/kg (1,5 mg/kg) doz uygulamas�ndan sonra, anti-Xa aktivitesi i�in ortalama EAA sabit durumda obez sa�l�kl� g�n�ll�lerde (BMI 30-48 kg/m) obez olmayan kontrollere k�yasla biraz daha y�ksek olup, E(maksimum anti-Xa aktivitesi) artmamaktad�r. Obez bireylerde subk�tan doz uygulamas�yla daha d���k bir kiloya g�re ayarlanm�� klirens s�z konusudur.
Kiloya g�re ayarlanmam�� doz uyguland���nda, tek bir subk�tan 4.000 IU (40 mg) dozu takiben anti-Xa maruz kalma d�zeyinin, normal kilolu kontrollerle kar��la�t�r�ld���nda d���k kilolu kad�nlarda (< 45 kg) %52 ve d���k kilolu erkeklerde (< 57 kg) %27 daha y�ksek oldu�u saptanm��t�r (Bkz. B�l�m 4.4).
Hemodiyaliz:
25 IU, 50 IU ya da 100 IU/kg'l�k tek IV dozlardan (0,25, 0,5 ya da 1 mg/kg) sonra enoksaparin sodyumun farmakokinetik profili kontrol pop�lasyonundakine benzer bulunmu�, ancak EAA de�erinin kontrole g�re 2 kez daha y�ksek oldu�u g�r�lm��t�r.
Farmakokinetik etkile�imler:
E�zamanl� olarak birlikte uyguland���nda, enoksaparin sodyum ile trombolitikler aras�nda herhangi bir farmakokinetik etkile�im g�zlenmemi�tir.
5.3. Klinik �ncesi g�venlilik verileri
Enoksaparinin, Ames testi, fare lenfoma h�cresi ileriye d�n�k mutasyon testi dahil olmak �zere in vitro testlerde herhangi bir mutajenik aktivite g�stermemi�tir. Ayr�ca in vitro insan lenfosit kromozomal d�zensizlik testi ve in vivo s��an kemik ili�i kromozomal d�zensizlik testinde klastojenik etki de g�zlemlenmemi�tir.
Enoksaparinin, erkek ve di�i s��anlarda 20 mg/kg/g�n subk�tan doz d�zeylerine kadar fertilite ve reprod�ktif performans �zerinde hi�bir etkisinin olmad��� g�zlemlenmi�tir. Gebe s��an ve tav�anlarda, 30 mg/kg/g�n enoksaparin subk�tan doz d�zeylerine kadar herhangi bir teratojenik etki veya fetotoksisite bulgusuna rastlanmam��t�r.
Enoksaparinin antikog�lan etkilerinin yan� s�ra, 15 mg/kg/g�n doz uygulamas� ile hem s��an ve k�pekler �zerinde yap�lan 13 haftal�k subkutan toksisite ara�t�rmalar�nda hem de10 mg/kg/g�n doz uygulamas� ile s��an ve maymunlar �zerinde yap�lan 26 haftal�k subk�tan ve intraven�z toksisite ara�t�rmalar�nda hi�bir yan etki bulgusuna rastlanmam��t�r.
Enjekt�r� bir kalem tutuyormu� gibi elinize al�n�z. Di�er elinizle, karn�n�zda enjeksiyon i�in se�ti�iniz b�lgenin derisini nazik�e yakalay�n�z ve ba� ile i�aret parmaklar�n�z�n aras�nda hafif�e s�karak bir deri k�vr�m� olu�turunuz.
B�t�n enjeksiyon boyunca deri k�vr�m�n� tutmaya devam ediniz.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Enjeksiyonluk su
6.2. Ge�imsizlikler
Subk�tan Enjeksiyon:Di�er �r�nler ile kar��t�r�lmamal�d�r.
IV (Bolus) Enjeksiyon (yaln�zca akut STEMI endikasyonu i�in):
Enoksaparin sodyum, sudaki %5 dekstroz ya da normal serum fizyolojik ��zeltisi (%0,9) ile g�venle uygulanabilir (Bkz. B�l�m 4.2).
6.3. Raf �mr�
24 ay
6.4. Saklamaya y�nelik �zel tedbirler
25°C alt�ndaki oda s�cakl���nda ve ambalaj�nda saklay�n�z. Buzdolab�nda saklamay�n�z ve dondurmay�n�z.
�nceden doldurulmu� enjekt�rler tek kullan�ml�kt�r; kullan�lmayan k�s�m at�lmal�d�r.
6.5. Ambalaj�n niteli�i ve i�eri�i
1 mL ��zelti i�eren 2 adet kullan�ma haz�r enjekt�r
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i“ ve “Ambalaj At�klar�n�n Kontrol� Y�netmeli�i” ne uygun olarak imha edilmelidir.7. RUHSAT SAH�B�
POL�FARMA �LA� SANAY� VE T�C. A.�.
Vak�flar OSB Mahallesi, Sanayi Caddesi, No:22/1 Ergene/TEK�RDA�
Tel: 0 282 675 14 04
Faks: 0 282 675 14 05
e-mail: info@polifarma.com.tr
��neyi dik olarak (90° lik a��yla) deri k�vr�m�na sonuna kadar bat�r�n�z
 Artrit
Artrit, olduk�a yayg�n bir hastal�kt�r ancak iyi anla��lamam��t�r. Asl�nda �artrit� tek bir hastal���n ad� de�ildir; eklem a�r�s� veya eklem hastal�klar�n� adland�rman�n gayri resmi yoludur.
Artrit
Artrit, olduk�a yayg�n bir hastal�kt�r ancak iyi anla��lamam��t�r. Asl�nda �artrit� tek bir hastal���n ad� de�ildir; eklem a�r�s� veya eklem hastal�klar�n� adland�rman�n gayri resmi yoludur. |
 A��r� Alkol Kullan�m�, Alkolizm
Alkol ba��ml�l���, alkol kullan�m� ve alkol sorunlar� aras�ndaki fark� a��klamak g��t�r.
�rne�in, ge�mi�te alkol kullanm�� olan bir kimsenin mutlaka alkol ba��ml�s� olmas�
gerekmez.
A��r� Alkol Kullan�m�, Alkolizm
Alkol ba��ml�l���, alkol kullan�m� ve alkol sorunlar� aras�ndaki fark� a��klamak g��t�r.
�rne�in, ge�mi�te alkol kullanm�� olan bir kimsenin mutlaka alkol ba��ml�s� olmas�
gerekmez. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| CLEXANE | 8699809950344 | 302.68TL |
| CRUSIA | 8699769950415 | 778.61TL |
| ENOX | 8699717950061 | |
| OKSAPAR | 8699828950073 | |
| VENAPERTA | 8699606954743 | 88.07TL |
| Di�er E�de�er �la�lar |
 |
Do�um Sonras� Depresyonu Do�um sonras� depresyonu, do�umdan sonra her on kad�ndan biri taraf�ndan tecr�be edilen stresli bir durumdur. |
 |
Y�ksek Tansiyon Hipertansiyon s�rekli anormal derecede y�ksek olan kan bas�nc�d�r. Tansiyon atardamarlar�n�zdaki kan�n bas�nc�d�r. |
 |
Tiroid Kanseri En s�k g�r�len tiroid kanseri t�r� olan papiller tiroid kanseri, t�m tiroid kanserlerinin yakla��k %70'ini olu�turur. |
�LA� GENEL B�LG�LER�
Polifarma �la� San.ve Tic. A.�.
| Sat�� Fiyat� | 359.95 TL [ 1 Dec 2025 ] |
| �nceki Sat�� Fiyat� | 359.95 TL [ 24 Nov 2025 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699606954774 |
| Etkin Madde | Enoksaparin Sodyum |
| Yerli ve Be�eri bir ila�d�r. |