VERXANT 150 mg SC enjeksiyon i�in liyofilize toz i�eren 1 flakon K�sa �r�n Bilgisi
{ Sekukinumab }
1. BE�ER� TIBB� �R�N�N ADI
VERXANT 150 mg SC enjeksiyon i�in liyofilize toz i�eren flakon Steril
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Secukinumab 150 mg
Secukinumab ; �in Hamster Over (CHO) h�crelerinde �retilen bir rekombinant, tamamen
insan monoklonal antikordur.
Yard�mc� maddeler
Sukroz 92,43 mg
Yard�mc� maddelerin tam listesi i�in b�l�m 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Enjeksiyonluk ��zelti i�in toz Toz beyaz, kat� liyofilizatt�r.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Plak psoriasis
VERXANT, siklosporin, metotreksat veya PUVA gibi geleneksel sistemik tedavilere yan�t vermeyen, tolere edemeyen ya da bu t�r tedavilerin kontrendike oldu�u eri�kin hastalarda orta veya �iddetli derecede seyreden plak psoriasis tedavisinde endikedir.
Psoriatik artrit
VERXANT tek ba��na ya da metotreksat (MTX) ile kombinasyon halinde, �nceki hastal��� modifiye edici anti-romatizmal ila� (DMARD) tedavisine yan�t�n yetersiz oldu�u durumlarda aktif psoriatik artritli eri�kin hastalar�n tedavisinde endikedir (bkz. B�l�m 5.1).
Aksiyal spondiloartrit (axSpA)
Ankilozan spondilit (AS, radyografik kan�t� olan aksiyal spondiloartrit)
VERXANT eri�kinlerde konvansiyonel tedaviye yetersiz yan�t veren aktif ankilozan spondilitin tedavisinde endikedir.
4.2. Pozoloji ve uygulama �ekli
VERXANT endike oldu�u durumlar�n tan� ve tedavisinde deneyimli bir hekimin rehberli�i ve
g�zetimi alt�nda kullan�lmal�d�r.
Pozoloji:
Plak psoriasis
�nerilen doz subkutan enjeksiyon yoluyla 300 mg secukinumab olup ba�lang�� dozlar� hafta 0, 1, 2, 3 ve 4'te uygulan�r ve bunu ayl�k idame dozlar� takip eder. Her 300 mg doz, 150 mg'l�k iki subkutan enjeksiyon halinde verilir.
Baz� hastalarda 150 mg da kullan�labilir.
Psoriatik artrit
E�zamanl� orta ila �iddetli plak psoriasisi olan ya da anti-TNFα tedavisine yetersiz yan�t veren hastalarda (IR) �nerilen doz subkutan enjeksiyon ile 300 mg olup ba�lang�� dozlar� hafta 0, 1, 2, 3 ve 4'te uygulan�r ve bunu ayl�k idame dozlar� takip eder. Her bir 300 mg'l�k doz, 150 mg'l�k iki subkutan enjeksiyon �eklinde yap�l�r.
Di�er hastalarda �nerilen doz subkutan enjeksiyon ile 150 mg olup ba�lang�� dozlar� hafta 0, 1, 2, 3 ve 4'te uygulan�r ve bunu ayl�k idame dozlar� takip eder. Klinik yan�ta g�re doz 300 mg'a y�kseltilebilir.
Aksiyal spondiloartrit (axSpA)
Ankilozan spondilit (AS, radyografik kan�t� olan aksiyal spondiloartrit)
�nerilen doz subkutan enjeksiyon ile 150 mg olup ba�lang�� dozlar� hafta 0, 1, 2, 3 ve 4'te uygulan�r ve bunu ayl�k idame dozlar� takip eder. Hastalarda yan�t�n yetersiz oldu�u durumlarda (aktif ankilozan spondiliti devam eden hastalarda), doz 300 mg'a y�kseltilebilir. Her bir 300 mg'l�k doz, 150 mg'l�k iki subkutan enjeksiyon �eklinde yap�l�r.
4.3. Kontrendikasyonlar
Etkin madde
Klinik olarak �nemli, aktif enfeksiyonu olan hastalarda kontrendikedir (�rn. aktif t�berk�loz;
bkz. B�l�m 4.4).
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Enfeksiyonlar
Secukinumab, enfeksiyon riskini art�rma potansiyeline sahiptir. Pazarlama sonras� d�nemde secukinumab alan hastalarda ciddi enfeksiyonlar g�zlenmi�tir. Kronik enfeksiyonu ya da tekrarlayan enfeksiyon �yk�s� olan hastalarda secukinumab kullan�m� planlan�rken dikkatli olunmal�d�r.
Enfeksiyona i�aret edebilecek belirti ve semptomlar�n ortaya ��kmas� durumunda hastalara t�bbi �neri almalar� talimat� verilmelidir. E�er hastada ciddi enfeksiyon geli�irse, yak�ndan takip edilmelidir ve enfeksiyon d�zelene kadar secukinumab uygulanmamal�d�r.
Klinik �al��malarda, secukinumab alan hastalarda enfeksiyonlar g�zlenmi�tir (bkz. B�l�m 4.8). Bunlar�n �o�u nazofarenjit gibi hafif ila orta dereceli �st solunum yolu enfeksiyonlar� olmu�tur ve tedavinin sonland�r�lmas�n� gerektirmemi�tir.
Secukinumab'�n etki mekanizmas� ile ili�kili olarak ciddi olmayan mukokutan�z kandida enfeksiyonlar�, psoriasis klinik �al��malar�nda plasebo ile kar��la�t�r�ld���nda secukinumab i�in daha s�k bildirilmi�tir (secukinumab 300 mg i�in 3.55/100 hasta y�l� kar��s�nda plasebo i�in 1.00/100 hasta y�l�) (bkz. B�l�m 4.8).
Klinik �al��malardan, t�berk�loza artm�� duyarl�l�k bildirilmemi�tir. Yine de, aktif t�berk�lozu olan hastalara secukinumab verilmemelidir. Latent t�berk�lozu olan hastalarda secukinumab tedavisine ba�lanmadan �nce anti-t�berk�loz tedavisi d���n�lmelidir.
Enflamatuar ba��rsak hastal��� (Crohn hastal��� ve �lseratif kolit dahil)
Secukinumab ile yeni ba��rsak hastal��� vakalar� ya da alevlenmeler bildirilmi�tir (bkz. b�l�m 4.8). Secukinumab, enflamatuar ba��rsak hastal��� olan hastalarda �nerilmemektedir. E�er bir hasta enflamatuar ba��rsak hastal��� i�aret ve semptomlar� geli�tirirse ya da daha �nceden var olan enflamatuar ba��rsak hastal���nda bir alevlenme ya�arsa, secukinumab b�rak�lmal� ve uygun t�bbi tedavi ba�lat�lmal�d�r.
A��r� duyarl�l�k reaksiyonlar�
Klinik �al��malarda, secukinumab alan hastalarda nadir anafilaktik reaksiyon vakalar� g�zlenmi�tir. Anafilaktik ya da ba�ka bir ciddi alerjik reaksiyon ortaya ��karsa, secukinumab uygulamas� derhal durdurulmal� ve uygun tedavi ba�lat�lmal�d�r.
A��lar
Canl� a��lar, secukinumab ile bir arada uygulanmamal�d�r.
Secukinumab alan hastalar e�zamanl� olarak inaktif ya da canl� olmayan a��lar alabilir. Bir �al��mada, meningokok ve inaktif grip a��lamalar�ndan sonra, 150 mg secukinumab uygulanan sa�l�kl� g�n�ll�lerin, plasebo ile tedavi edilenlerle benzer bir oran� meningokok ve grip a��lar�na antikor titrelerinde en az 4 katl�k art��lar ile yeterli imm�n yan�t� verebilmi�tir. Bu veriler, secukinumab'�n meningokok ve grip a��lar�na humoral imm�n yan�t� bask�lamad���na i�aret etmektedir.
E�zamanl� imm�n sistemi bask�lay�c� tedavi
Psoriasis �al��malar�nda, secukinumab'�n biyolojik ajanlar veya fototerapi dahil olmak �zere imm�n sistemi bask�lay�c� tedaviler ile kombinasyon halinde uygulanmas� de�erlendirilmemi�tir. Secukinumab, artrit �al��malar�nda (psoriatik artrit ve ankilozan spondiliti olan hastalarda yap�lanlar dahil) metotreksat (MTX), s�lfasalazin ve/veya kortikosteroidlerle e�zamanl� olarak uygulanm��t�r. Di�er imm�nos�presanlarla secukinumab�n e�zamanl� kullan�m� d���n�ld���nde dikkatli olunmal�d�r. (ayr�ca bkz. B�l�m 4.5).
Takip edilebilirlik
Biyoteknolojik �r�nlerin takip edilebilirli�inin sa�lanmas� i�in uygulanan �r�n�n ticari ismi ve seri numaras� mutlaka hasta dosyas�na kaydedilmelidir.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Canl� a��lar, secukinumab ile e�zamanl� uygulanmamal�d�r (ayr�ca bkz. B�l�m 4.4).
Plak psoriyasisi olan g�n�ll�ler �zerinde ger�ekle�tirilen bir �al��mada, secukinumab ve
midazolam (CYP3A4 substrat�) aras�nda etkile�im g�zlenmemi�tir.
Artrit �al��malar�nda secukinumab, metotreksat (MTX) ve/veya kortikosteroidler ile e�zamanl� uyguland���nda herhangi bir etkile�im g�r�lmemi�tir (psoriatik artrit ve aksiyal spondiloartrit hastalar� da dahil).
4.6. Gebelik ve laktasyon
Gebelik kategorisi C'dir.
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
�ocuk do�urma potansiyeli bulunan kad�nlar tedavi boyunca ve tedaviden sonra en az 20 hafta s�reyle etkili bir do�um kontrol y�ntemi kullanmal�d�r.
Gebelik d�nemi
Gebe kad�nlarda secukinumab kullan�m� ile ilgili yeterli veri mevcut de�ildir. Hayvan �al��malar� gebelik, embriyonik/fetal geli�im, do�um ve do�um sonras� geli�im �zerinde dolayl� ya da do�rudan zararl� etkiler g�stermemektedir (bkz. B�l�m 5.3). Tedbir olarak gebelikte VERXANT kullan�m�ndan ka��n�lmas� tercih edilir.
Laktasyon d�nemi
Secukinumab�n insan s�t� ile at�l�p at�lmad��� bilinmemektedir. �mm�noglobulinler insan s�t� ile at�l�r ve secukinumab�n al�nd�ktan sonra sistemik olarak emilip emilmedi�i bilinmemektedir. Emzirilen bebeklerde secukinumab kaynakl� advers reaksiyonlar potansiyeli nedeniyle, emzirmenin bebek i�in faydalar� ve VERXANT tedavisinin anne i�in faydalar� g�z �n�nde bulundurularak, tedavi s�resince ve tedaviden sonra 20 haftaya kadar s�reyle emzirmenin durdurulup durdurulmayaca��na veya VERXANT tedavisinin durdurulup durdurulmayaca��na karar verilmelidir.
�reme yetene�i/Fertilite
Secukinumab�n insan fertilitesi �zerindeki etkisi de�erlendirilmemi�tir. Hayvan �al��malar�, fertilite a��s�ndan do�rudan veya dolayl� zararl� etkiler g�stermemektedir.
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
VERXANT'�n ara� ve makine kullan�m� �zerinde etkisi yoktur veya g�z ard� edilebilir etkileri vard�r.
4.8. �stenmeyen etkiler
G�venlilik profilinin �zetiEn s�k bildirilen advers ila� reaksiyonlar� (ADR'ler) �st solunum yolu enfeksiyonlar� (en s�k olarak nazofarenjit, rinit) olmu�tur.
Advers reaksiyonlar�n tablo halinde listesi
Klinik �al��malarda ve pazarlama sonras� raporlarda tespit edilen advers ila� reaksiyonlar� (Tablo 1) MedDRA sistem organ s�n�f�na g�re listelenmektedir. Her bir sistem organ s�n�f� i�inde ADR'ler s�kl��a g�re s�ralanmakta olup en s�k reaksiyonlar ba�ta listelenmektedir. Her bir s�kl�k grubu dahilinde advers ila� reaksiyonlar�, azalan ciddilik derecesine g�re g�sterilmektedir. Ayr�ca, her bir advers ila� reaksiyonunun kar��l�k geldi�i s�kl�k kategorisi, a�a��daki sisteme g�redir:
�ok yayg�n (≥1/10); yayg�n (≥1/100 ila <1/10); yayg�n olmayan (≥1/1.000 ila <1/100); seyrek (≥1/10.000 ila <1/1.000); �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
�e�itli endikasyonlara (plak psoriasis, psoriatik artrit, aksiyal spondiloartrit ve di�er otoimm�n hastal�klar) y�nelik toplam 30.565 hasta y�l� maruziyete kar��l�k gelen k�r ve a��k etiketli klinik �al��malarda, 18.000'den fazla hasta secukinumab ile tedavi edilmi�tir. Bu
hastalar�n 11.700'den fazlas� en az bir y�l s�reyle secukinumab'a maruz kalm��t�r. Secukinumab�n g�venlilik profili t�m endikasyonlarda tutarl�d�r.
Tablo 1: Klinik �al��malarda ve pazarlama sonras� deneyimde advers
reaksiyonlar�n listesi
Sistem organ s�n�f� | S�kl�k | Advers reaksiyon |
Enfeksiyonlar ve enfestasyonlar | �ok yayg�n | �st solunum yolu enfeksiyonlar� |
Yayg�n | Oral herpes | |
Tinea pedis | ||
Yayg�n olmayan | Oral kandidiyazis | |
Otitis externa | ||
Alt solunum yolu enfeksiyonlar� | ||
Bilinmiyor | Mukozal ve k�tan�z kandidiyazis (�zofageal kandidiyazis dahil) | |
Kan ve lenf sistemi hastal�klar� | Yayg�n olmayan | N�tropeni |
Ba����kl�k sistemi hastal�klar� | Seyrek | Anafilaktik reaksiyonlar |
Sinir sistemi hastal�klar� | Yayg�n | Ba� a�r�s� |
G�z hastal�klar� | Yayg�n olmayan | Konjunktivit |
Solunum, g���s hastal�klar� ve mediastinal hastal�klar | Yayg�n | Rinore |
Gastrointestinal hastal�klar | Yayg�n | Diyare |
Bulant� | ||
Yayg�n olmayan | Enflamatuar ba��rsak hastal��� | |
Deri ve deri alt� doku hastal�klar� | Yayg�n olmayan | �rtiker |
Seyrek | Eksfoliyatif dermatit | |
Genel bozukluklar ve uygulama yeri rahats�zl�klar� | Yayg�n | Yorgunluk |
Se�ilen advers reaksiyonlar�n tan�m�
Enfeksiyonlar
Plak psoriasis klinik �al��malar�n�n plasebo kontroll� d�neminde (12 hafta s�reyle toplam 1382 hastaya secukinumab ve 694 hastaya plasebo uygulanm��t�r) secukinumab ile tedavi edilen hastalar�n %28,7'sinde enfeksiyonlar bildirilirken ayn� oran plasebo uygulanan hastalarda %18,9 olmu�tur. Enfeksiyonlar�n �o�u nazofarenjit gibi hafif ila orta dereceli �st solunum yolu enfeksiyonlar� olmu�tur ve tedavinin sonland�r�lmas�n� gerektirmemi�tir. Etki mekanizmas� ile uyumlu olarak mukozal veya kutan�z kandidiyazda art�� olmu�tur ancak bu olgular hafif ila orta �iddetlidir, ciddi boyutta de�ildir ve standart tedaviye yan�t vermi�, tedavinin kesilmesini gerektirmemi�tir. Ciddi enfeksiyonlar, secukinumab uygulanan
hastalar�n %0,14'�nde ve plasebo uygulanan hastalar�n %0,3'�nde g�r�lm��t�r (bkz. B�l�m 4.4).
�al��ma d�neminin tamam�nda (hastalar�n b�y�k �o�unlu�u i�in 52 hafta s�reyle toplamda 3.430 hastaya secukinumab uygulanm��t�r), secukinumab ile tedavi edilen hastalar�n
%47,5'inde enfeksiyonlar bildirilmi�tir (hasta y�l� ba��na 0,9'luk izlem). secukinumab uygulanan hastalar�n %1,2'sinde ciddi enfeksiyonlar bildirilmi�tir (hasta y�l� ba��na 0,015 izlem).
Psoriatik artrit ve aksiyal spondiloartrit (ankilozan spondilit ve radyografik kan�t� olmayan aksiyal spondiloartrit) klinik �al��malar�nda g�zlenen enfeksiyon oran�, psoriasis �al��malar�nda g�zlenenler ile benzerdir.
N�tropeni
Psoriasis faz III klinik �al��malar�nda, n�tropeni, plaseboya k�yasla secukinumab ile daha s�k g�zlenmi�tir fakat olgular�n �o�u hafif, ge�ici ve geri d�n��l� olmu�tur. <l,0-0,5x10/l (CTCAE Derece 3) n�tropeni, secukinumab tedavisindeki 3.430 hastan�n 18'inde (%0,5) bildirilmi� olup 18 olgunun 15'inde doza ba��ml�l�k veya enfeksiyonlar ile zamansal ili�ki s�z konusu olmam��t�r. Bildirilmi� herhangi bir �iddetli n�tropeni vakas� bulunmamaktad�r. Di�er �� olguda standart tedaviye normal yan�t veren ve secukinumab tedavisinin kesilmesini gerektirmeyen, ciddi olmayan enfeksiyonlar bildirilmi�tir.
Psoriatik artrit ve aksiyal spondiloartrit (ankilozan spondilit ve radyografik kan�t� olmayan aksiyal spondiloartrit)teki n�tropeni s�kl���, psoriasisteki ile benzerdir.
Seyrek n�tropeni <0,5x10/l (CTCAE Derece 4) olgular� bildirilmi�tir.
A��r� duyarl�l�k reaksiyonlar�
Secukinumab'la yap�lan klinik �al��malarda, �rtiker ve nadir olarak anaflaktik reaksiyon vakalar� g�zlenmi�tir (ayr�ca bkz. B�l�m 4.4).
�mm�nojenisite
Psoriasis, psoriatik artrit ve aksiyal spondiloartrit (ankilozan spondilit ve radyografik kan�t� olmayan aksiyal spondiloartrit) klinik �al��malar�nda secukinumab ile tedavi edilen hastalar�n
%1'inden az�, 52 haftaya kadarki tedavide secukinumaba antikorlar geli�tirmi�tir. Tedavi kaynakl� anti-ila� antikorlar�n�n yakla��k yar�s� n�tralizan olmu�tur ancak bu durum, etkililik kayb� ya da farmakokinetik anormallikler ile ili�kilendirilmemi�tir.
��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar / risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir. (www.titck.gov.tr; e- posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99)
4.9. Doz a��m� ve tedavisi
Klinik �al��malarda, 30 mg/kg'a kadarki dozlar (yakla��k 2000 ila 3000 mg), doz s�n�rlay�c� toksisite olmaks�z�n intraven�z yolla uygulanm��t�r. Doz a��m� durumunda hastan�n advers
reaksiyonlara dair belirti ve i�aretler a��s�ndan izlenmesi ve derhal uygun semptomatik tedavinin ba�lat�lmas� �nerilir.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grubu: �mm�n sistemi bask�lay�c� ajanlar, interl�kin inhibit�rleri ATC kodu: L04AC10
Etki mekanizmas�:
Secukinumab; proenflamatuvar sitokin interl�kin-17A'ya (IL-17A) selektif olarak ba�lanan ve n�trle�tiren IgG1/κ yap�s�nda olan tamamen insan monoklonal antikorudur. Secukinumab, IL-17A'y� hedef al�r ve IL-17A'n�n keratinositler dahil �e�itli h�cre tiplerinde eksprese olan IL-17 resept�r� ile etkile�imini inhibe ederek etki g�sterir. Bunun sonucu olarak secukinumab; proenflamatuvar sitokinlerin, kemokinlerin ve doku hasar� arac�lar�n�n sal�verilmesini inhibe eder ve otoimm�n ve enflamatuvar hastal�klarda IL-17 arac�l� etkileri azalt�r. Klinik a��dan anlaml� sonu� elde edilecek d�zeylerde secukinumab deriye ula��r ve lokal enflamatuvar belirte�leri azalt�r. Bunun do�rudan sonucu olarak secukinumab tedavisi, plak psoriasis lezyonlar�ndaki eritemi, indurasyonu ve deskuamasyonu azalt�r.
IL-17A; normal enflamatuvar ve imm�n yan�tlar�nda rol oynayan do�al bir sitokindir. IL-17A, plak psoriasis, psoriatik artrit ve aksiyal spondiloartrit (ankilozan spondilit ve radyografik kan�t� olmayan aksiyal spondiloartrit) patojenezinde �nemli bir role sahiptir ve plak psoriasis hastalar�n�n lezyonlu olmayan derileri ile kar��la�t�r�ld���nda lezyonlu derilerinde ve psoriatik artrit hastalar�n�n sinoviyal dokusunda artm�� d�zeydedir. IL-17 �reten h�crelerin s�kl��� da ankilozan spondilit hastalar�ndan al�nan faset eklemlerinin subkondral kemik ili�inde anlaml� d�zeyde daha y�ksek olmu�tur. Radyografik kan�t� olmayan aksiyal spondiloartritli hastalarda artm�� say�da IL-17A �reten lenfosit de bulunmu�tur. IL-17A'n�n inhibisyonunun ankilozan spondilit tedavisinde etkili oldu�u g�sterilerek bu sitokinin aksiyal spondiloartritte anahtar rol� oldu�u netle�tirilmi�tir.
Farmakodinamik etkiler:
Secukinumab alan hastalarda 2 ila 7 g�n i�inde, toplam IL-17A (serbest ve secukinumaba ba�l� IL-17A) serum d�zeyleri ilk olarak, secukinumaba ba�l� IL-17A'n�n azalm�� klirensi nedeniyle artarak secukinumab�n, plak psoriasis patojenezinde kilit bir rol oynayan serbest IL- 17A'y� selektif olarak yakalad���n� g�sterir.
Secukinumab ile y�r�t�len bir �al��mada infiltre eden epidermal n�trofiller ve plak psoriasis hastalar�n�n lezyonlu derilerinde artm�� olan n�trofil ili�kili �e�itli belirte�ler, bir ila iki haftal�k tedaviden sonra anlaml� d�zeyde azalm��t�r.
Secukinumab�n, bir enflamasyon g�stergesi olan C-reaktif protein d�zeylerini d���rd��� g�sterilmi�tir (tedavinin 1 ila 2 haftas� i�inde).
Klinik etkililik ve g�venlilik: Plak psoriasis
Secukinumab'�n g�venlili�i ve etkilili�i, orta ila �iddetli derecede plak psoriasis hastas� olup fototerapi ve sistemik tedavi aday� olan hastalardaki d�rt randomize, �ift k�r, plasebo kontroll� faz 3 �al��mada de�erlendirilmi�tir [ERASURE, FIXTURE, FEATURE, JUNCTURE]. Secukinumab 150 mg ve 300 mg'�n g�venlili�i ve etkilili�i plasebo ya da etanersept kar��s�nda incelenmi�tir. Bunlara ek olarak, bir �al��mada ‘gerektik�e yeniden tedavi' rejimi kar��s�nda kronik tedavi rejimi de�erlendirilmi�tir [SCULPTURE].
Plasebo kontroll� �al��malara dahil edilen 2.403 hastan�n %79'u �nceden biyolojik �r�n kullanmam��, %45'inde biyolojik olmayan yakla��mlar ile ba�ar�s�z olunmu�, %8'inde biyolojik yakla��mlar ile ba�ar�s�z olunmu�tur (%6's�nda anti-TNF ile ve %2'sinde anti-p40 ile ba�ar�s�z olunmu�tur). Faz III �al��malardaki hastalar�n yakla��k %15 ila %25'inde ba�lang��ta psoriatik artrit (PsA) oldu�u tespit edilmi�tir.
Psoriasis �al��mas� 1'de (ERASURE) 738 hasta de�erlendirilmi�tir. Secukinumab tedavisine randomize edilen hastalar 0, 1, 2, 3 ve 4. haftalarda 150 mg veya 300 mg dozlar� alm��, ard�ndan, ayn� doz ayda bir uygulanm��t�r. Psoriasis �al��mas� 2'de (FIXTURE) 1306 hasta de�erlendirilmi�tir. Secukinumab'a randomize edilen hastalar 0, 1, 2, 3 ve 4. haftalarda 150 mg veya 300 mg dozlar� alm��, ard�ndan, ayn� dozlar ayda bir uygulanm��t�r. Etanersepte randomize edilen hastalar, 12 hafta s�reyle haftada iki kez 50 mg dozlar�, ard�ndan haftada bir 50 mg alm��lard�r. Gerek �al��ma 1 gerekse �al��ma 2'de 12. haftada yan�ts�z olan ve plasebo alacaklar� gruplara randomize edilen hastalar daha sonra, 12, 13, 14 ve 15. haftalarda secukinumab alacaklar� (150 mg ya da 300 mg), ard�ndan, 16. haftada ba�lanarak her ay ayn� dozu alacaklar� VERXANT koluna aktar�lm��t�r. T�m hastalar, �al��ma ilac�n�n ilk uygulamas�n� takiben 52 haftaya kadar takip edilmi�tir.
Psoriasis �al��mas� 3'te (FEATURE), kullan�ma haz�r enjekt�r ile secukinumab'�n hasta taraf�ndan uygulanmas�n�n g�venlili�i, tolerabilitesi ve kullan�labilirli�ini de�erlendirmek �zere, 12 hafta sonras�nda plasebo kar��s�nda kullan�ma haz�r enjekt�rler kullan�larak 177 hasta de�erlendirilmi�tir. Psoriasis �al��mas� 4'te (JUNCTURE), kullan�ma haz�r enjekt�r ile secukinumab'�n hasta taraf�ndan uygulanmas�n�n g�venlili�i, tolerabilitesi ve kullan�labilirli�ini de�erlendirmek �zere, 12 hafta sonras�nda plasebo kar��s�nda kullan�ma haz�r enjekt�rler kullan�larak 182 hasta de�erlendirilmi�tir. Gerek �al��ma 3 gerekse �al��ma 4'te secukinumab'a randomize edilen hastalar 0, 1, 2, 3 ve 4. haftalarda 150 mg veya 300 mg
dozlar� alm��, ard�ndan, ayn� dozlar ayda bir uygulanm��t�r. Hastalar ayr�ca 0, 1, 2, 3 ve 4. haftalarda ve ard�ndan, ayda bir ayn� dozlar� alacaklar� plasebo koluna randomize edilmi�tir.
Psoriasis �al��mas� 5'te (SCULPTURE) 966 hasta de�erlendirilmi�tir. T�m hastalar 0, 1, 2, 3,
4, 8 ve 12. haftalarda secukinumab 150 mg veya 300 mg alm��, ard�ndan, 12. haftadan ba�layarak her ay ayn� dozun uygulanaca�� idame rejimi alacaklar� ya da ayn� dozun ‘gerektik�e yeniden tedavi' rejimini alacaklar� gruplara randomize edilmi�tir. ‘Gerektik�e yeniden tedavi' rejimine randomize edilen hastalarda yeterli yan�t�n devaml�l��� sa�lanamam��t�r ve dolay�s�yla sabit ayl�k idame rejimi �nerilmektedir.
Plasebo kontroll� ve aktif kontroll� �al��malarda e� birincil sonlanma noktalar� 12. haftada plasebo kar��s�nda PASI 75 (Psoriasis Alan� ve �iddeti �ndeksi) yan�t�na ve IGA (Investigator Global Assessment- Ara�t�r�c� Global De�erlendirmesi) mod 2011 ‘temiz' ya da ‘neredeyse temiz' yan�tlar�na ula�an hastalar�n oran� olmu�tur (bkz. Tablo 2 ve 3). 300 mg dozu ile t�m �al��malarda PASI 75/90/100, ve IGA mod 2011 ‘temiz' ya da ‘neredeyse temiz' yan�tlar�
olarak belirlenen etkililik sonlanma noktalar�n�n t�m�nde daha iyi cilt d�zelmesi elde edilmi�, pik etkiler 16. haftada g�r�lm��t�r: bu nedenle bu doz �nerilmektedir.
Tablo 2 : Psoriasis �al��malar� 1, 3 ve 4'te (ERASURE, FEATURE ve JUNCTURE) PASI 50/75/90/100 & IGA⃰ mod 2011 ‘temiz' ‘neredeyse temiz' klinik yan�t �zeti
| 12. Hafta | 16. Hafta | 52. Hafta | ||||
�al��ma 1 | Placebo | 150 mg | 300 mg | 150 mg | 300 mg | 150 mg | 300 mg |
Hasta say�s� | 246 | 244 | 245 | 244 | 245 | 244 | 245 |
PASI 50 yan�t� n (%) | 22 (%8,9) | 203 (%83,5) | 222 (%90,6) | 212 (%87,2) | 224 (%91,4) | 187 (%77) | 207 (%84,5) |
PASI 75 yan�t� n (%) | 11 (%4,5) | 174 (%71,6)** | 200 (%81,6)** | 188 (%77,4) | 211 (%86,1) | 146 (%60,1) | 182 (%74,3) |
PASI 90 yan�t� n (%) | 3 (%1,2) | 95 (%39,1)** | 145 (%59,2)** | 130 (%53,5) | 171 (%69,8) | 88 (%36,2) | 147 (%60) |
PASI 100 yan�t� n (%) | 2 (%0,8) | 31 (%12,8) | 70 (%28,6) | 51 (%21) | 102 (%41,6) | 49 (%20,2) | 96 (%39,2) |
IGA mod 2011 “temiz” veya “neredeyse temiz” yan�t� n (%) |
6 (%2,4) |
125 (%51,2)** |
160 (%65,3)** |
142 (%58,2) |
180 (%73,5) |
101 (%41,4) |
148 (%60,4) |
�al��ma 3 |
|
|
|
|
|
|
|
Hasta say�s� | 59 | 59 | 58 | - | - | - | - |
PASI 50 yan�t� n (%) | 3 (%5,1) | 51 (%86,4) | 51 (%87,9) | ||||
PASI 75 yan�t� n (%) | 0 (%0) | 41 (%69,5)** | 44 (%75,9)** | ||||
PASI 90 yan�t� n (%) | 0 (%0) | 27 (%45,8) | 35 (%60,3) | ||||
PASI 100 yan�t� n (%) | 0 (%0) | 5 (%8,5) | 25 (%43,1) | ||||
IGA mod 2011 “temiz” veya “neredeyse temiz” yan�t� n (%) |
0 (%0) |
31 (%52,5)** |
40 (%69)** |
- |
- |
- |
- |
�al��ma 4 |
|
|
|
|
|
|
|
Hasta say�s� | 61 | 60 | 60 | - | - | - | - |
PASI 50 yan�t� n (%) | 5 (%8,2) | 48 (%80) | 58 (%96,7) | ||||
PASI 75 yan�t� n (%) | 2 (%3,3) | 43 (%71,7)** | 52 (%86,7)** | ||||
PASI 90 yan�t� n (%) | 0 (%0) | 24 (%40) | 33 (%55) | ||||
PASI 100 yan�t� n (%) | 0 (%0) | 10 (%16,7) | 16 (%26,7) | ||||
IGA mod 2011 “temiz” veya “neredeyse temiz” yan�t� n (%) |
0 (%0) |
32 (%53,3)** |
44 (%73,3)** |
- |
- |
- |
- |
*IGA mod 2011, be� kategorili bir �l�ek olup “0 = temiz”, “1 = neredeyse temiz”, “2 = hafif”, “3 = orta” ve “4 = �iddetli” kategorilerini i�erir: bu kategoriler, hastan�n, indurasyon, eritem ve pullanmaya odakl� genel psoriasis �iddeti de�erlendirmesini yans�t�r. “Temiz” veya “neredeyse temiz” �eklindeki tedavi ba�ar�s� psoriasis belirtisi olmamas�, normal veya pembe renkli lezyon rengi, plakta kal�nla�ma olmamas� ve fokal pullanman�n olmamas� veya minimal olmas�n� i�erir.
** p de�erleri plaseboya kar��d�r ve multiplisite(�e�itlilik) i�in d�zeltilmi�tir: p<0,0001
Tablo 3 : Psoriasis �al��mas� 2'de klinik yan�t �zeti (FIXTURE)
| ||||||||||
| ||||||||||
** p de�erleri etanersepte kar��d�r: p=0,025
Yap�lan ilave bir psoriasis �al��mas�nda (CLEAR) 676 hasta de�erlendirilmi�tir. Secukinumab 300 mg, 16. haftada PASI 90 yan�t�(birincil sonlan�m noktas�) 4. haftada PASI 75 yan�t�n�n ortaya ��kma h�z� ve 52. haftada uzun s�reli PASI 90 yan�t�na dayal� olarak, ustekinumaba g�re �st�nl�k sergileyerek birincil ve ikincil sonlan�m noktalar�n� sa�lam��t�r. PASI 75/90/100 ve IGA mod 2011 0 ya da 1 yan�t� (“temiz” veya “neredeyse temiz”) sonlan�m noktalar�na g�re, ustekinumabla kar��la�t�r�ld���nda secukinumab i�in daha y�ksek bir etkililik g�zlenmi� ve bu durum 52. haftaya kadar s�rd�r�lm��t�r.
Tablo 4: CLEAR �al��mas�nda g�zlenen klinik yan�t�n �zeti
| 4. Hafta | 16. Hafta | 52. Hafta | |||
| Secukinumab 300 mg | Ustekinumab* | Secukinumab 300 mg | Ustekinumab* | Secukinumab 300 mg | Ustekinumab* |
Hastalar�n say�s� | 334 | 335 | 334 | 335 | 334 | 335 |
PASI 75 yan�t� n (%) | 166 (%49,7)** | 69 (%20,6) | 311 (%93,1) | 276 (%82,4) | 306 (%91,6) | 262 (%78,2) |
PASI 90 yan�t� n (%) | 70 (%21,0) | 18 (%5,4) | 264 (%79)** | 192 (%57,3) | 250 (%74,9)*** | 203 (%60,6) |
PASI 100 yan�t� n (%) | 14 (%4,2) | 3 (%0,9) | 148 (%44,3) | 95 (%28,4) | 150 (%44,9) | 123 (%36,7) |
IGA mod 2011 “temiz” veya | 128 (%38,3) | 41 (%12,2) | 278 (%83,2) | 226 (%67,5) | 261 (%78,1) | 213 (%63,6) |
“neredeyse temiz” yan�t n (%) |
|
|
|
|
|
|
* Secukinumabla tedavi edilen hastalar 0., 1., 2. ve 3 ve 4. haftalarda 300 mg dozunu, ard�ndan 52. haftaya kadar her 4 haftada bir ayn� dozu alm��lard�r. Ustekinumabla tedavi edilen hastalar, 0. ve 4. haftalarda ve ard�ndan 52. haftaya kadar 12 haftada bir 45 mg ya da 90 mg ila� alm��t�r (onaylanm�� pozolojiye uygun olarak kiloya g�re doz uygulamas� yap�lm��t�r).
** Ustekinumabla kar��la�t�r�ld���nda p de�erleri; Hafta 16'da PASI 90 birincil sonlan�m noktas� i�in ve Hafta 4'te PASI 75 ikincil sonlan�m noktas� i�in p < 0,0001
*** Ustekinumab kar��s�nda p de�erleri; Hafta 52'de PASI 90 ikincil sonlan�m noktas� i�in p=0,0001
Secukinumab �nceden biyolojik ajan kullan�lmam��, biyolojik ajanlara/anti-TNF'e maruz kalm�� ve biyolojik ajanlar/anti-TNF ile ba�ar�s�z olunmu� hastalarda etkili olmu�tur. Ba�lang��ta e�zamanl� psoriatik artriti olan hastalarda PASI 75 d�zelmeleri, genel plak psoriasis pop�lasyonundaki ile benzer olmu�tur.
Secukinumab, 300 mg dozunda 3. hafta itibariyle ortalama PASI skorunda %50 d���� g�r�lm�� ve bu durum h�zl� etkililik ba�lang�c� ile ili�kilendirilmi�tir.
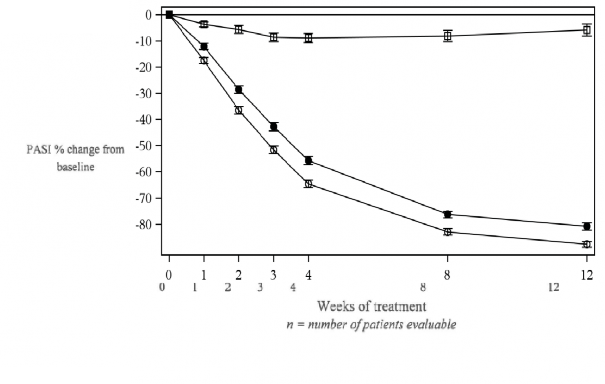
Secukinumab 150 mg (n=243) ○ Secukinumab 300 mg (n=245) □ Plasebo
5.2. Farmakokinetik �zellikler
Genel �zellikler:Plak psoriasis, psoriatik artrit ve ankilozan spondilit hastalar�nda g�zlemlenen �o�u farmakokinetik �zellik benzerdir.
Emilim:
Sa�l�kl� g�n�ll�lerde 300 mg'l�k tek subkutan dozunun s�v� form�lasyon halinde uygulanmas�n�n ard�ndan secukinumab, dozdan 2 ila 14 g�n sonra 43,2 ± 10,4 µg/ml pik serum konsantrasyonlar�na ula�m��t�r.
Pop�lasyon farmakokineti�i analizine dayan�larak, plak psoriasis hastalar�nda 150 mg ya da 300 mg'l�k tek subkutan dozunun ard�ndan secukinumab, dozdan 5 ila 6 s�n sonra s�ras�yla 13,7 ± 4,8 μg/ml ya da 27,3 ± 9,5 μg/ml pik serum konsantrasyonlar�na ula�m��t�r.
Pop�lasyon farmakokineti�i analizine dayan�larak, ilk ay boyunca ba�lang�� haftal�k dozlar�ndan sonra maksimum konsantrasyona ula�ma i�in ge�en s�re 31 ile 34 g�n aras�nda olmu�tur.
Sim�le verilere dayal� olarak, 150 mg ya da 300 mg dozlar�n�n subkutan uygulanmas�n�n ard�ndan kararl� durumdaki pik konsantrasyonlar� (C,) s�ras�yla 27,6 μg/ml ve 55,2 μg/ml olmu�tur. Pop�lasyon farmakokineti�i, ayl�k doz rejimleri ile kararl� duruma 20 hafta sonra ula��ld���n� g�stermektedir.
Pop�lasyon farmakokineti�inin g�sterdi�i �zere, tek doz sonras�ndaki maruziyet ile kar��la�t�r�ld���nda, idame s�resince tekrarl� ayl�k dozlardan sonra hastalar pik serum konsantrasyonlar�nda ve e�ri alt�ndaki alan (EAA) de�erinde 2 kat art�� sergilemi�tir.
Pop�lasyon farmakokineti�i analizi, secukinumab�n plak psoriasis hastalar�nda ortalama %73 mutlak biyoyararlan�m ile emildi�ini g�stermi�tir. �al��malar aras�nda %60 ile %77 aral���nda mutlak biyoyararlan�m de�erleri hesaplanm��t�r.
Da��l�m:
Plak psoriasis hastalar�nda tek intraven�z uygulaman�n ard�ndan terminal faz (V) s�resinde ortalama da��l�m hacmi 7,1 - 8,6 litre aral���nda bulunmu� olup bu, secukinumab�n periferik kompartmanlara da��l�m�n�n s�n�rl� oldu�una i�aret etmektedir.
Biyotransformasyon:
lgG eliminasyonunun b�y�k k�sm� h�cre i�i katabolizma yoluyla, s�v� faz veya resept�r arac�l� endositoz �eklinde ger�ekle�mektedir.
Eliminasyon:
Plak psoriasis hastalar�na tek intraven�z uygulama sonras�nda ortalama sistemik klirens (CL) 0,13 ila 0,36 l/g�n aral���nda bulunmu�tur. Bir pop�lasyon farmakokineti�i analizinde plak psoriasis hastalar�nda ortalama sistemik klirens (CL) 0,19 l/g�n olmu�tur. CL de�eri cinsiyetten etkilenmemi�tir. Klirens doza ve zamana ba�l� olmu�tur.
Bir pop�lasyon farmakokineti�i analizinde hesapland��� �zere, intraven�z uygulaman�n kullan�ld��� psoriasis �al��malar�nda plak psoriasis hastalar�nda ortalama eliminasyon yar� �mr� 27 g�n olup 18 ile 46 g�n aras�nda de�i�mektedir.
Do�rusall�k/do�rusal olmayan durum:
Plak psoriasis hastalar�nda secukinumab�n tek doz ve �oklu doz farmakokineti�i, 1 x 0,3 mg/kg ila 3 x 10 mg/kg aral���ndaki intraven�z dozlar�n ve 1 x 25 mg ila 300 mg'l�k �oklu doz aral���ndaki doz aral���n�n kullan�ld��� �e�itli �al��malarda belirlenmi�tir. T�m doz rejimlerinde maruziyetin doz ile orant�l� oldu�u g�r�lm��t�r.
Hastalardaki karakteristik �zellikler
Ya�l� hastalar:
S�n�rl� say�da ya�l� hastan�n (≥ 65 ya� i�in n=71 ve ≥ 75 ya� i�in n=7) dahil oldu�u pop�lasyon farmakokineti�i analizine dayan�larak, ya�l� hastalar ve 65 ya� alt� hastalardaki klirensin benzer oldu�u belirlenmi�tir.
B�brek veya karaci�er yetmezli�i olan hastalar:
B�brek veya karaci�er yetmezli�i olan hastalar ile ilgili farmakokinetik veri bulunmamaktad�r. Bir IgG monoklonal antikoru olan de�i�memi� VERXANT'�n renal eliminasyonunun d���k olmas� ve min�r �neme sahip olmas� beklenir. IgG'ler temelde katabolizma yoluyla elimine olur ve karaci�er bozuklu�unun VERXANT klirensini etkilemesi beklenmez.
Farmakokinetik �zerinde kilonun etkisi
Secukinumab�n klirensi ve da��l�m hacmi artan v�cut a��rl��� ile artar.
5.3. Klinik �ncesi g�venlilik verileri
Klinik d��� veriler, doku �apraz reaktivitesi, g�venlilik farmakolojisi, tekrarl� doz ve �reme toksisitesi konvansiyonel �al��malar�na dayal� olarak insanlar i�in �zel bir tehlike g�stermemi�tir.
Secukinumab�n karsinojen potansiyelini de�erlendiren hayvan �al��malar� ger�ekle�tirilmemi�tir.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Sukroz
L-histidin
L-histidin hidroklor�r monohidrat Polisorbat 80
Enjeksiyonluk su
6.2. Ge�imsizlikler
Bu t�bbi �r�n, b�l�m 6.6'da bahsedilen t�bbi �r�nler haricinde ba�ka t�bbi �r�nler ile
kar��t�r�lmamal�d�r.
6.3. Raf �mr�
36 ay
Suland�r�larak kullan�ma haz�rland�ktan sonra:
��zelti haz�rland�ktan sonra kimyasal ve fiziksel stabilitesinin 2°C-8°C'de 24 saat devam etti�i g�sterilmi�tir.
Mikrobiyolojik a��dan, suland�r�larak kullan�ma haz�rlama metodu mikrobiyal kontaminasyona engel olmad��� taktirde, inf�zyon ��zeltisinin hemen kullan�lmas� gerekir.
6.4. Saklamaya y�nelik �zel tedbirler
Buzdolab�nda 2-8 ºC'de saklay�n�z.
Suland�r�larak kullan�ma haz�rlanm�� t�bbi �r�n�n saklama ko�ullar� i�in bkz. b�l�m 3.
6.5. Ambalaj�n niteli�i ve i�eri�i
VERXANT, gri kaplama kau�uk t�pal� ve beyaz flip-off bile�enli al�minyum kapakl�, 150 mg
secukinumab i�eren renksiz cam flakonda sunulmaktad�r.
Ambalaj b�y�kl���: 1 flakon i�eren kutu.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj ve Ambalaj At�klar�n�n Kontrol� Y�netmeli�i”ne uygun olarak imha edilmelidir.
Tek kullan�ml�k flakonlar, steril enjeksiyonluk su ile suland�r�larak kullan�ma haz�rlanmak i�in 150 mg secukinumab i�ermektedir. Final ��zelti, berrak ve renksiz ila hafif sar� olmal�d�r. Liyofilize toz tamamen ��z�lmez ya da s�v�, g�zle kolayca g�r�lebilen partik�ller i�erirse, bulutlu bir g�r�n�m� olursa ya da belirgin bi�imde kahverengi ise kullanmay�n�z. Uygulamaya y�nelik ayr�nt�l� a��klamalar kullanma talimat�nda yer almaktad�r.
 L�semi Kan Kanseri
L�semi, kan kanseridir ve v�cudunun kan olu�turan dokular�n�n hastalanmas� anlam�na gelir. Bir�ok l�semi t�r� vard�r; baz� l�semi t�rleri �ocuklarda baz�lar� da yeti�kinlerde s�k g�r�l�r.
L�semi Kan Kanseri
L�semi, kan kanseridir ve v�cudunun kan olu�turan dokular�n�n hastalanmas� anlam�na gelir. Bir�ok l�semi t�r� vard�r; baz� l�semi t�rleri �ocuklarda baz�lar� da yeti�kinlerde s�k g�r�l�r. |
 Depresyonu Anlamak
Depresyon farkl� ki�ileri farkl� bi�imlerde etkiler. Duygusal veya fiziksel
olmak �zere geni� alanda belirtilere sebep olabilir.Depresyona neler sebep olur?
Depresyonu Anlamak
Depresyon farkl� ki�ileri farkl� bi�imlerde etkiler. Duygusal veya fiziksel
olmak �zere geni� alanda belirtilere sebep olabilir.Depresyona neler sebep olur? |
 |
A��r� Alkol Kullan�m�, Alkolizm Alkol ba��ml�l���, alkol kullan�m� ve alkol sorunlar� aras�ndaki fark� a��klamak g��t�r. �rne�in, ge�mi�te alkol kullanm�� olan bir kimsenin mutlaka alkol ba��ml�s� olmas� gerekmez. |
 |
Parkinson Hastal��� Hastal�k ilk kez 1817 de �ngiliz doktor James Parkinson taraf�ndan tan�mlanm�� ve Dr. Parkinson hastal��� “sallay�c� fel�” olarak kaleme alm��. |
 |
D�� Gebelik D�� gebelik, her 100 gebelikten birini etkileyen, s�k g�r�len ve �l�me sebep olabilecek bir durumdur. Bu, d�llenen yumurta, rahimin d���na yerle�irse, olu�an bir durumdur. Gebelik ilerledik�e, a�r�ya ve kanamalara sebep olur. |
�LA� GENEL B�LG�LER�
Farmanova Sa�l�k Hizmetleri Ltd. �ti
| Geri �deme Kodu | A16798 |
| Sat�� Fiyat� | 10103.47 TL [ 17 Dec 2024 ] |
| �nceki Sat�� Fiyat� | 11771.77 TL [ 2 Dec 2024 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699074790508 |
| Etkin Madde | Sekukinumab |
| ATC Kodu | L04AC10 |
| Birim Miktar | 150 |
| Birim Cinsi | MG |
| Ambalaj Miktar� | 1 |
| Antineoplastik ve �mm�nomod�lat�r Ajanlar > �mm�nsupresif Ajanlar |
| �thal ( ref. �lke : Isvicre ) ve Be�eri bir ila�d�r. |