VOPAZZI 400 mg film kapl� tablet (60 tablet) K�sa �r�n Bilgisi
{ Pazopanib }
1. BE�ER� TIBB� �R�N�N ADI
VOPAZZ� 400 mg film kapl� tablet Sitotoksik
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Her bir film kapl� tablet;
Etkin madde
Pazopanib hidroklor�r 433,4 mg (400 mg pazopanibe e�de�er)
Yard�mc� maddeler
Yard�mc� maddeler i�in b�l�m 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Film kapl� tablet.
Beyaz renkli, oval, film kapl� tablet
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Pazopanib, daha �nce herhangi bir VEGF-TKI (Vask�ler endotelyal b�y�me fakt�r�- Tirozin kinaz inhibit�r�) kullanmam�� rezeke edilemeyen lokal relaps veya metastatik renal h�creli kanseri olan hastalarda tek ajan olarak progresyona kadar kullan�mda endikedir.
VOPAZZ� metastatik hastal�k i�in en az bir seri kemoterapi/ en fazla iki seri kemoterapi kullan�lm�� ve sonras�nda progresyon g�stermi� metastatik sarkomun a�a��da belirtilen alt tiplerinde endikedir:
Fibroblastik sarkomlar (eri�kin fibrosarkom, miksofibrosarkom, sklerozan epiteloid fibrosarkom, malign soliter fibr�z t�m�r), fibrohistiositik sarkomlar (pleomorfik malign fibr�z histiositom, dev h�creli malign fibr�z histiositom (indiferansiye pleomorfik sarkom (UPS) olarak da bilinir), inflamatuar malign fibr�z histiositom), leiomyosarkom pleomorfik veya alveolar rabdomyosarkom, epiteloid hemanjioendotelyoma, anjiosarkomlar, epiteloid sarkomlar, sinoviyal sarkom, alveolar soft part sarkoma, malign glom�s t�m�r�, berrak h�creli sarkom, desmoplastik k���k yuvarlak h�creli sarkom, malign mezenkimoma, PEComa, intimal sarkom, malign periferik sinir k�l�f� t�m�rlerinde endikedir.
4.2. Pozoloji ve uygulama �ekli
VOPAZZ� tedavisi ancak kanser ila�lar�n�n uygulamas�nda deneyimli bir hekim taraf�ndan ba�lat�lmal�d�r.
Renal h�cre karsinomu (Renal Cell Carcinoma; RCC) veya yumu�ak doku sarkomu (Soft Tissue Sarkoma; STS) tedavisi i�in �nerilen pazopanib dozu g�nde bir kez oral al�nan 800 mg'd�r.
Dozun De�i�tirilmesi
�stenmeyen etkilerin kontrol� i�in sonraki doz de�i�iklikleri bireysel tolerabiliteye g�re kademeli �ekilde art�r�larak 200 mg'l�k dozlarla de�i�tirilmelidir. Pazopanib g�nl�k dozu 800 mg'� a�mamal�d�r.
Uygulama �ekli:
Pazopanib a� karn�na (yemeklerden en az bir saat �nce veya iki saat sonra) uygulanmal�d�r (bkz B�l�m 5.2). Tabletler, b�l�nmeden, par�alanmadan ve �i�nenmeden b�t�n olarak bol su ile yutularak al�nmal�d�r.
Bir dozun al�nmas� unutulursa ve sonraki doza 12 saatten daha az bir s�re kald�ysa unutulan doz al�nmamal�d�r.
�zel pop�lasyonlara ili�kin ek bilgiler:
B�brek yetmezli�i:
Pazopanib ve metabolitlerinin renal yolla at�lmas�n�n d���k oldu�u g�z �n�ne al�nd���nda b�brek yetmezli�inin pazopanib farmakokineti�inde klinik a��dan anlaml� bir etki yapmas� beklenmez (bkz B�l�m 5.2). Kreatinin klirensi 30 mL/dak'n�n �zerinde olan hastalarda dozaj ayarlamas� gerekli de�ildir. Ancak kreatin klirensi 30 ml/dak de�erinin alt�nda olan hastalarda pazopanib kullan�lacaksa dikkatli olunmal�d�r.
Karaci�er yetmezli�i:
Karaci�er yetmezli�i olan hastalarda dozaj �nerileri, de�i�ik derecelerde karaci�er fonksiyon bozuklu�u olan hastalarda pazopanib ile yap�lan farmakokinetik �al��malara dayanmaktad�r (bkz. B�l�m 5.2). Pazopanib tedavisine ba�lanmadan �nce ve tedavi s�ras�nda karaci�er bozukluklar�n�n olup olmad���n� belirlemek �zere t�m hastalara karaci�er fonksiyon testleri uygulanmal�d�r (bkz. B�l�m 4.4). Hafif ila orta �iddette karaci�er yetmezli�i olan hastalar, potansiyel olarak ilaca maruziyetin artmas� sebebiyle dikkatle ele al�nmal� ve izlenmelidirler. Karaci�er fonksiyon testlerinde hafif anormallik bulunan (normal bilirubin ve herhangi bir d�zeyde alanin aminotransferaz (ALT) art��� veya ALT de�erinden ba��ms�z olarak �st normal s�n�r�n (ULN) 1,5 kat� bilirubin (> %35 direkt) art��� olarak tan�mlanan) hastalarda tedaviye g�nde bir kez 800 mg pazopanib dozu ile ba�lan�lmas� �nerilir. Orta �iddetli karaci�er yetmezli�i olan hastalarda (ALT de�erlerinden ba��ms�z olarak bilirubinde > 1,5 x ila 3 x ULN kat art�� olarak tan�mlan�r) pazopanib dozunun g�nde bir kez 200 mg'a d���r�lmesi �nerilmektedir (bkz. B�l�m 5.2).
Pazopanib, �iddetli karaci�er yetmezli�i (ALT d�zeyinden ba��ms�z olarak total bilirubin de�erinin > 3 x ULN kat art��� �eklinde tan�mlan�r) olan hastalarda kontrendikedir (bkz B�l�m 4.3).
Karaci�er fonksiyonlar�n�n izlenmesi ve ila�la ind�klenen karaci�er toksisitesi olan hastalarda doz ayarlamas� i�in B�l�m 4.4'e bak�n�z.
Pediatrik pop�lasyon:
Organ b�y�mesi ve mat�rasyonu ile ilgili g�venlilik endi�eleri nedeniyle pazopanib 2 ya� alt� �ocuklarda kullan�lmamal�d�r (bkz. B�l�m 4.4 ve 5.3).
Pazopanibin 2 ile 18 ya� aras� �ocuklardaki g�venlili�i ve etkilili�i belirlenmemi�tir (bkz. B�l�m 5.1).
Geriyatrik pop�lasyon:
65 ya� ve �st�ndeki hastalarda pazopanib kullan�m�na ili�kin s�n�rl� veri mevcuttur. Pazopanib ile yap�lan klinik �al��malarda en az 65 ya��n �zerindeki hastalar ile daha gen� hastalar aras�nda pazopanibin g�venlili�ine ili�kin klinik a��dan anlaml� fark bulunmam��t�r. Bildirilen di�er klinik deneyimde ya�l� hastalar ile gen� hastalar aras�nda yan�t a��s�ndan bir fark tan�mlanmamakla birlikte baz� ya�l� hastalar�n daha duyarl� olabilece�i g�z ard� edilemez.
4.3. Kontrendikasyonlar
Etkin madde
VOPAZZ� gebelik d�neminde kullan�lmamal�d�r (bkz. B�l�m 4.6). 2 ya� alt�ndaki �ocuklarda kullan�lmamal�d�r.
4.4. �zel kullan�m uyar�lar� ve �nlemleri
Hepatik etkiler:
Pazopanib kullan�m� s�ras�nda karaci�er yetmezli�i vakalar� (�l�mle sonu�lananlar dahil) bildirilmi�tir. Hafif ila orta �iddette karaci�er yetmezli�i olan hastalara pazopanib uygulamas� dikkatli yap�lmal� ve bu hastalar yak�ndan izlenmelidir.
Serum karaci�er testlerinde hafif anormallik (ya normal bilirubin ve herhangi bir derece ALT y�kselmesi ya da ALT de�eri fark etmeksizin 1,5 x ULN'ye kadar bilirubin y�kselmesi �eklinde) olan hastalarda tedaviye g�nde bir kez 800 mg pazopanib dozu ile ba�lanmas� �nerilir. Orta �iddette karaci�er yetmezli�i olan hastalarda g�nde 200 mg'l�k azalt�lm�� pazopanib dozu �nerilmektedir (ALT de�eri fark etmeksizin > 1,5 ila 3 x ULN bilirubin y�kselmesi) (bkz. B�l�m 4.2 ve 5.2). Pazopanib, �iddetli karaci�er yetmezli�i olan hastalarda �nerilmez (ALT de�eri fark etmeksizin toplam bilirubin > 3 x ULN) (bkz. B�l�m 4.2 ve 5.2). Bu hastalarda 200 mg'l�k dozda maruziyet, her ne kadar olduk�a de�i�ken olsa da, belirgin �ekilde azalmaktad�r; de�erlerin, klinik a��dan anlaml� bir etki elde etmek i�in yeterli olmad��� d���n�lmektedir.
Pazopanib ile yap�lan klinik �al��malarda serum transaminazlar (ALT, aspartat aminotransferaz [AST]) ve bilirubin d�zeylerinde art��lar g�zlenmi�tir (bkz. B�l�m 4.8). Olgular�n �o�unda,
alkalin fosfataz ya da bilirubin art��lar�n�n e�lik etmedi�i izole ALT ve AST y�kselmeleri bildirilmi�tir. 60 ya��n �zerindeki hastalar hafif (>3xULN) ila �iddetli (>8xULN) ALT y�kselmesi a��s�ndan daha y�ksek risk alt�nda olabilir. HLA-B*57:01 aleli ta��yan hastalar pazopanib ile ili�kili ALT y�kselmeleri a��s�ndan daha y�ksek risk alt�ndad�r. Genotip ya da ya�a bak�lmaks�z�n pazopanib kullanan t�m hastalarda karaci�er i�levi izlenmelidir (bkz. B�l�m 5.1).
Pazopanib ile tedaviye ba�lanmadan �nce ve tedavinin 3, 5, 7 ve 9. haftalar�nda serum karaci�er testi izlenmelidir. Serum karaci�er testi daha sonra 3 ve 4. aylarda da yap�lmal� ve klinik durumun gerektirdi�i durumlarda di�er testler de izlenmelidir. Periyodik izlem, 4. ay sonras�nda devam etmelidir.
A�a��daki k�lavuzlar, ba�lang��ta toplam bilirubin de�erleri ≤ 1,5 x ULN ve AST ve ALT ≤ 2 x ULN olan hastalara y�neliktir.
Serum transaminaz d�zeylerinde 3 x ULN ila 8 x ULN aras�nda izole art��lar g�r�len hastalarda, serum transaminaz de�erleri evre 1 (NCI CTCAE) veya ba�lang�� d�zeyine d�nene kadar karaci�er fonksiyonu haftal�k olarak izlenerek pazopanib tedavisine devam edilebilir.
Serum transaminazlar�n�n de�eri > 8 x ULN olan hastalarda pazopanib tedavisi, serum transaminaz de�erleri evre 1 (NCI CTCAE) veya ba�lang�� d�zeyine d�nene kadar kesilmelidir. Pazopanib tedavisinin yeniden ba�lat�lmas�yla elde edilecek potansiyel yarar�n hepatotoksisite riskinden daha fazla oldu�u d���n�l�yorsa, pazopanib tedavisi g�nl�k 400 mg'l�k daha d���k dozda yeniden ba�lat�lmal� ve 8 hafta s�reyle haftada bir kez serum karaci�er testleri yap�lmal�d�r (bkz. B�l�m 4.2). Pazopanibin yeniden uygulanmas�n� takiben ALT de�erleri > 3 x ULN d�zeyinde yeniden artarsa, pazopanib tedavisi kal�c� olarak kesilmelidir.
Serum transaminazlar�n�n d�zeyleri > 3 x ULN ve bilirubin d�zeyleri > 2 x ULN d�zeyine y�kselirse pazopanib tedavisi kal�c� olarak kesilmelidir. Hastalar, evre 1 (NCI CTCAE) veya ba�lang�� d�zeyine d�nene kadar izlenmelidir. Pazopanib bir �ridin glukronosilat transferaz (uridine glucuronosyl transferase; UGT1A1) inhibit�r�d�r. Gilbert sendromu g�r�len hastalarda hafif, indirekt (konjuge edilmemi�) hiperbilirubinemi meydana gelebilir. Gilbert sendromu oldu�u bilinen veya ��phelenilen, sadece hafif indirekt hiperbilirubinemisi olan ve ALT de�erlerinde > 3 x ULN'lik art�� g�r�len hastalar, izole ALT art��lar�na y�nelik �neriler uyar�nca kontrol edilmelidir.
Pazopanib ve simvastatinin e�zamanl� kullan�m�, ALT d�zeylerinde art�� riskini art�rmaktad�r (bkz. B�l�m 4.5) ve bu ila�lar dikkatli bir �ekilde ve yak�n g�zetim alt�nda kullan�lmal�d�r.
Hipertansiyon:
Pazopanib ile yap�lan klinik �al��malarda, yeni tan� konmu� semptomatik y�kselmi� kan bas�nc� epizodlar� (hipertansif krizler) dahil olmak �zere hipertansiyon olaylar� meydana gelmi�tir. Pazopanib tedavisinden �nce kan bas�nc� iyi kontrol edilmelidir. Hastalar, tedaviye ba�lanmas�n�n hemen ard�ndan (pazopanib tedavisine ba�lad�ktan sonra bir haftay� ge�meyecek
�ekilde) hipertansiyon y�n�nden de�erlendirilmeli ve ondan sonra da s�kl�kla kan bas�nc�n� kontrol alt�nda tutmak amac�yla izlenmelidir. Pazopanib tedavisinin erken d�nemlerinde (vakalar�n yakla��k % 40'� 9. g�nden �nce meydana gelirken yakla��k % 90'� ilk 18 haftada meydana gelmi�tir) kan bas�nc�nda y�kselmeler (sistolik kan bas�nc� ≥ 150 veya diyastolik kan bas�nc� ≥ 100 mmHg) meydana gelmektedir. Kan bas�nc� izlenmeli ve anti-hipertansif tedavi ile pazopanib doz modifikasyonundan (klinik karara g�re tedaviye ara verme ve daha d���k bir dozda tekrar ba�lama) olu�an bir kombinasyon ile derhal kontrol alt�na al�nmal�d�r (bkz. B�l�m 4.2 ve 4.8). Hipertansif kriz y�n�nde bir g�sterge varsa ya da hipertansiyon �iddetli ise ve anti- hipertansif tedavi ve pazopanib dozunda azaltmaya ra�men devam ediyorsa pazopanib tedavisi kesilmelidir.
Posterior geri d�n���ml� ensefalopati sendromu (PRES)/Geri d�n���ml� posterior l�koensefalopati sendromu (RPLS)
PRES/RPLS pazopanib ile ili�kili olarak bildirilmi�tir. PRES/RPLS ba� a�r�s�, hipertansiyon, n�bet, letarji, konf�zyon, k�rl�k ve di�er g�rsel ve n�rolojik bozukluklar ile kendini g�sterebilir ve �l�mc�l olabilir. PRES/RPLS geli�en hastalarda pazopanib kal�c� olarak b�rak�lmal�d�r.
�nterstisyel akci�er hastal��� (ILD)/Pn�moni
Pazopanib ile ba�lant�l� olarak �l�mc�l olabilen ILD bildirilmi�tir (bkz. b�l�m 4.8). Hastalar, ILD'ye/pn�moniye i�aret edebilecek pulmoner semptomlar a��s�ndan izlenmelidir ve ILD ya da pn�moni geli�tiren hastalarda pazopanib tedavisi kesilmelidir.
Kardiyak Disfonksiyon/Kalp yetmezli�i
Tedavi �ncesinde kardiyak disfonksiyonu olan hastalarda tedaviye ba�lamadan �nce pazopanibin riskleri ve yararlar� g�z �n�ne al�nmal�d�r. Orta �iddet ila �iddetli kalp yetmezli�i olan veya normalin alt�nda LVEF olan hastalarda pazopanibin g�venlili�i ve farmakokineti�i �al���lmam��t�r.
Pazopanib ile y�r�t�len klinik �al��malarda konjestif kalp yetmezli�i ve sol ventrik�ler ejeksiyon fraksiyonu (LVEF) azalmas� gibi kardiyak fonksiyon bozuklu�u olaylar� bildirilmi�tir (bkz. B�l�m 4.8). RCC'de (VEG108844) pazopanib ile sunitinibin kar��la�t�r�ld��� randomize bir klinik �al��mada g�n�ll�lerin �al��ma ba�lang�c�nda ve sonras�nda LVEF �l��mleri yap�lm��t�r. Miyokard fonksiyon bozuklu�u, pazopanib kolundaki hastalar�n
%13'�nde (47/362) g�r�l�rken ayn� oran sunitinib kolunda %11 (42/369) olmu�tur. Konjestif kalp yetmezli�i her iki tedavi kolunda da %0,5 hastada g�zlenmi�tir. Faz III VEG110727 STS �al��mas�nda konjestif kalp yetmezli�i 240 olgunun 3'�nde bildirilmi�tir (%1). Ba�lang�� sonras� ve takip LVEF �l��mleri olan olgularda LVEF d����leri, pazopanib kolundaki hastalar�n %11'inde (15/140) g�r�l�rken ayn� oran plasebo kolunda %3 (1/39) bulunmu�tur.
Risk fakt�rleri: STS faz III �al��mas�n�n pazopanib kolundaki 15 hastan�n 13'�nde e�zamanl� hipertansiyon olup bu durum, kardiyak art y�k� art�rma suretiyle risk alt�ndaki hastalarda kardiyak fonksiyon bozuklu�unu k�t�le�tirmi� olabilir. Bu 15 hasta dahil olmak �zere STS faz
III �al��mas�na kat�lan hastalar�n %99'u (243/246) antrasiklin ile tedavi edilmi�tir. �nceki antrasiklin tedavisi, kardiyak fonksiyon bozuklu�u a��s�ndan bir risk fakt�r� olabilir.
Tedavi sonucu: Sonu� olarak 15 ki�inin 4'� tamamen iyile�irken (temel de�erin %5'inin i�erisinde) ve 5'i k�smen iyile�mi�tir (normal aral���n i�erisinde, fakat %5 temel de�erin alt�nda). Bir ki�i iyile�memi�tir ve di�er 5 ki�i i�in izleme verileri mevcut de�ildir.
Tedavi: LVEF'de �nemli azalmalar g�r�len hastalarda, klinik olarak endike oldu�u �ekilde, pazopanibin kesilmesi ve/veya dozunun azalt�lmas�na hipertansiyon (mevcutsa, yukar�daki hipertansiyon uyar� b�l�m�n� inceleyiniz) tedavisi de e�lik etmelidir. Hastalar konjestif kalp yetmezli�ini g�steren klinik belirti ve semptomlar i�in dikkatle izlenmelidir. Kardiyak disfonksiyon riski bulunan hastalarda ba�lang��ta ve periyodik olarak LVEF de�erlendirmesi �nerilmektedir.
QT uzamas� ve Torsade de Pointes:
Pazopanib ile yap�lan klinik �al��malarda QT uzamas� ve Torsade de Pointes vakalar� meydana gelmi�tir (bkz B�l�m 4.8). Pazopanib QT aral��� uzama hikayesi olan hastalarda, antiaritmikler veya QT aral���nda uzamaya neden olabilen di�er ila�lar� kullanan veya �nceden mevcut �nemli kardiyak hastal��� olan hastalarda dikkatli �ekilde kullan�lmal�d�r.
Pazopanib kullan�m� s�ras�nda EKG parametrelerinin ba�lang��ta ve periyodik olarak izlenmesi ve elektrolit dengesinin (�rn, kalsiyum, magnezyum, potasyum) normal aral�k dahilinde tutulmas� �nerilmektedir.
Arteriyel trombotik olaylar:
Pazopanib ile yap�lan klinik �al��malarda miyokard infarkt�s�, miyokardiyal iskemi, iskemik inme ve ge�ici iskemik atak g�zlenmi�tir (bkz. B�l�m 4.8). �l�mc�l olaylar g�zlenmi�tir. Pazopanib, trombotik olay riski y�ksek veya bir trombotik olay �yk�s� bulunan hastalarda dikkatli kullan�lmal�d�r. Pazopanib, ge�mi� 6 ay i�erisinde bir olay ya�am�� hastalarda incelenmemi�tir. Hastan�n bireysel yarar/risk durumu de�erlendirilerek bir tedavi karar� verilmelidir.
Ven�z tromboembolik olaylar:
Pazopanib ile yap�lan klinik �al��malarda, ven�z tromboz ve �l�mc�l pulmoner emboli dahil olmak �zere ven�z tromboembolik olaylar meydana gelmi�tir. Gerek RRC gerekse STS �al��malar�nda g�zlenmi� olmakla birlikte RCC pop�lasyonuna (%2) k�yasla STS pop�lasyonunda insidans daha y�ksek olmu�tur (%5).
Trombotik Mikroanjiyopati:
Monoterapi olarak, bevasizumab ile kombinasyon halinde ve topotekan ile kombinasyon halinde pazopanibe ili�kin klinik �al��malarda trombotik mikroanjiyopati (TMA) bildirilmi�tir (bkz..B�l�m 4.8). TMA geli�en hastalarda pazopanib kal�c� olarak b�rak�lmal�d�r. Tedavi b�rak�ld�ktan sonra TMA etkilerinde d�zelme g�zlenmi�tir. Pazopanib di�er ajanlarla kombinasyon halinde kullan�m i�in endike de�ildir.
Hemorajik olaylar:
Pazopanib ile yap�lan klinik �al��malarda hemorajik olaylar bildirilmi�tir (bkz. B�l�m 4.8). �l�mc�l hemorajik olaylar meydana gelmi�tir. Pazopanib son alt� ay i�erisinde hemoptizi, serebral veya klinik a��dan anlaml� gastrointestinal (GI) hemoraji �yk�s� bulunan hastalarda kullan�lmamal�d�r. Pazopanib anlaml� hemoraji riski bulunan hastalarda dikkatli �ekilde kullan�lmal�d�r.
Anevrizmalar ve arter diseksiyonlar�
VEGF yolak inhibit�rlerinin, hipertansiyonu olan veya olmayan hastalarda kullan�lmas�, anevrizmalar ve/veya arter diseksiyonlar� olu�umunu kolayla�t�rabilir. Pazopanib ba�lamadan �nce, hipertansiyon veya anevrizma �yk�s� gibi risk fakt�rleri olan hastalarda bu risk dikkatle de�erlendirilmelidir.
Gastrointestinal perforasyon ve fist�l:
Pazopanib ile yap�lan klinik �al��malarda GI perforasyon ve fist�l olaylar� meydana gelmi�tir (bkz. B�l�m 4.8). �l�mc�l perforasyon olaylar� meydana gelmi�tir. Pazopanib GI perforasyonu veya fist�l i�in y�ksek risk bulunan hastalarda dikkatli �ekilde kullan�lmal�d�r.
Yara iyile�mesi:
Yara iyile�mesinde pazopanibin etkisine ili�kin bir �al��ma yap�lmam��t�r. Vask�ler Endotelyal B�y�me Fakt�r� (VEGF) inhibit�rleri yara iyile�mesini geciktirebildi�i i�in pazopanib tedavisi planlanan cerrahiden en az 7 g�n �nce kesilmelidir. Cerrahiden sonra pazopanib tedavisine devam edilmesi karar� yeterli yara iyile�mesine ili�kin klinik de�erlendirmeye dayand�r�lmal�d�r. Yara a��lmas� bulunan hastalarda pazopanib kesilmelidir.
Hipotiroidizm:
Pazopanib ile yap�lan klinik �al��malarda hipotiroidizm olaylar� bildirilmi�tir (bkz. B�l�m 4.8). Tiroid fonksiyonlar� i�in ba�lang�� laboratuvar �l��mleri tavsiye edilir, hipotiroidizmli hastalar pazopanib tedavisine ba�lamadan �nce standart medikal uygulamalara ba�l� olarak tedavi edilmelidir. T�m hastalar pazopanib tedavisinde tiroid bozukluk belirtileri i�in yak�ndan takip edilmelidir. Tiroid fonksiyon testleri periyodik olarak izlenmeli ve standart medikal uygulamalara ba�l� olarak tedavi edilmelidir.
Protein�ri:
Pazopanib ile yap�lan klinik �al��malarda protein�ri rapor edilmi�tir. Tedavi s�resince, ba�lang��ta ve periyodik olarak idrar analizleri �nerilmektedir ve hastalar protein�rinin k�t�le�mesi a��s�ndan izlenmelidir. E�er hastada nefrotik sendrom geli�irse pazopanib kesilmelidir.
T�m�r lizis sendromu (TLS):
Pazopanib kullan�m� ile �l�mc�l TLS de dahil olmak �zere TLS olu�umu ili�kilendirilmi�tir (bkz. B�l�m 4.8). TLS riski artm�� olan hastalar; h�zl� b�y�yen t�m�rlere, y�ksek bir t�m�r y�k�ne, renal disfonksiyona veya dehidrasyona sahip hastalard�r. VOPAZZ� ba�lat�lmadan �nce, y�ksek �rik asit d�zeylerinin tedavisi ve intraven�z hidrasyon gibi �nleyici tedbirler
d���n�lmelidir. Risk alt�ndaki hastalar yak�ndan takip edilmeli ve klinik olarak endike oldu�u durumlarda tedavi edilmelidir.
Pn�motoraks:
�lerlemi� yumu�ak doku sarkomunda pazopanib ile yap�lan klinik �al��malarda, pn�motoraks vakalar� meydana gelmi�tir (bkz. B�l�m 4.8). Pazopanib tedavisi g�ren hastalar�n pn�motoraks belirtileri ve sendromlar� a��s�ndan yak�ndan izlenmesi gereklidir.
Enfeksiyonlar:
Baz�lar� �l�mle sonu�lanan ciddi enfeksiyon vakalar� (n�tropeni ile birlikte veya n�tropeni olmadan) bildirilmi�tir.
Di�er sistemik anti-kanser tedavileri ile kombinasyon:
Pazopanibin pemetrexed (k���k h�creli olmayan akci�er kanseri (NSCLC)) ve lapatinib (serviks kanseri) ile kombinasyon halinde kullan�ld��� klinik �al��malar, artan toksisite ve/veya mortalite sebebiyle ve bu rejimlerle g�venli ve efektif doz kombinasyonu belirlenemedi�i i�in erken a�amada sonland�r�lm��t�r.
Pediyatrik pop�lasyon:
Pazopanibin etki mekanizmas�, erken post natal geli�im d�neminde organ b�y�mesini ve olgunla�mas�n� ciddi �ekilde etkileyebildi�i i�in (bkz. B�l�m 5.3), pazopanib tedavisi 2 ya��ndan k���k pediyatrik hastalara uygulanmamal�d�r.
Gebelik:
Hayvanlar �zerinde y�r�t�len klinik �ncesi �al��malar �reme toksisite varl���n� g�stermi�tir (bkz. B�l�m 5.3). E�er pazopanib gebelik s�ras�nda kullan�l�yorsa ya da hasta pazopanib kullan�rken hamile kal�rsa, fet�s i�in olu�abilecek potansiyel tehlike hastaya anlat�lmal�d�r. Gebe kalma potansiyeli bulunan kad�nlara, pazopanib kulland�klar� s�re boyunca gebelikten ka��nmalar� �nerilmelidir (bkz. B�l�m 4.6).
Etkile�imler:
G��l� sitokrom P450(CYP)3A4, meme kanseri diren� proteini (BCRP) veya P-glikoprotein (P- gp) inhibit�rleri ile e� zamanl� kullan�m�, pazopanibe maruziyet riskini artt�rd��� i�in bu bile�iklerde beraber kullan�m�ndan ka��n�lmal�d�r. (bkz. B�l�m 4.5) CYP3A4, BCRP veya P- gp inhibisyon potansiyeli bulunmayan veya minimum olan t�bbi �r�nlerin alternatif kombinasyonlar�n�n se�imi g�z �n�nde bulundurulmal�d�r.
Pazopanib maruziyetini azaltma riskinden dolay� CYP3A4 ind�kleyicileri ile birlikte kullan�m�ndan ka��n�lmal�d�r (bkz. B�l�m 4.5).
Ketokonazol ile birlikte kullan�m�nda hiperglisemi vakalar� g�zlenmi�tir.
Pazopanib, �ridin difosfat glukuronil transferaz 1A1 (UGT1A1) inhibit�r� oldu�u i�in, pazopanib UGT1A1 substratlar� (�rn. irinotekan) ile birlikte uygulan�rken dikkat edilmelidir (bkz. B�l�m 4.5).
Pazopanib tedavisi s�ras�nda greyfurt suyu kullan�m�ndan ka��n�lmal�d�r (bkz. B�l�m 4.5).
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Di�er ila�lar�n pazopanib �zerindeki etkileri
�n vitro �al��malar insan karaci�er mikrozomlar�nda pazopanibin oksidatif metabolizmas�na temelde CYP3A4 enziminin arac�l�k etti�ini ve CYP1A2 ve CYP2C8 enzimlerinin min�r katk�da bulundu�unu d���nd�rm��t�r. Bu nedenle CYP3A4 inhibit�rleri ve ind�kleyicileri pazopanib metabolizmas�n� de�i�tirebilir.
CYP3A4, P-gp, BCRP inhibit�rleri
Pazopanib, CYP3A4, P-gp ve BCRP i�in bir substratt�r.
Pazopanibin (g�nde bir kez 400 mg) g��l� CYP3A4 ve P-gp inhibit�r�, ketokonazol (g�nde bir kez 400 mg) ile birlikte art arda 5 g�n uygulanmas� sonucunda; pazopanibin tek ba��na verilmesine (7 g�n boyunca g�nde bir kez 400 mg) k�yasla, ortalama pazopanib E�ri Alt� Alan (EAA)ve Cde�erlerinde s�ras�yla % 66 ve % 45 art�� meydana gelmi�tir. Tek ba��na pazopanib 800 mg uygulamas�ndan sonra ve pazopanib 400 mg art� ketokonazol 400 mg uygulamas�ndan sonra yap�lan pazopanib C(ortalamalar aral��� 27,5 ila 58,1 mikrogram/ml) ve EAA(ortalamalar aral��� 48,7 ila 1040 mikrogram*h/ml) farmakokinetik parametreleri kar��la�t�rmalar� (ortalama C59,2 mikrogram/ml, ortalama EAA1300 mikrogram*h/ml), g��l� CYP3A4 ve P-gp inhibit�r� varl���nda g�nde bir kez pazopanib 400 mg dozuna azaltman�n �o�u hastada, tek ba��na g�nde bir kez pazopanib 800 mg uygulamas�ndan sonra g�zlenen ile benzer sistemik maruziyet ile sonu�lanaca��n� g�stermi�tir. Ancak baz� hastalar tek ba��na g�nl�k 800 mg pazopanib uygulamas� sonras�nda g�zlenenden daha fazla sistemik maruziyet g�sterebilmektedir.
Pazopanib ile birlikte di�er g��l� CYP3A4 inhibit�rlerinin kullan�lmas� (�rn, itrakonazol, klaritromisin, atazanavir, indinavir, nefazodon, nelfinavir, ritonavir, saquinavir, telitromisin, vorikonazol) pazopanib konsantrasyonlar�n� art�rabilir. Greyfurt suyu bir CYP3A4 inhibit�r� i�ermekte olup ayr�ca plazmadaki pazopanib konsantrasyonlar�n� art�rabilir.
1500 mg lapatinib (CYP3A4 ve P-gp'nin zay�f bir inhibit�r� ve BCRP'nin potent bir inhibit�r�) ile 800 mg pazopanib uygulamas� tek ba��na 800 mg pazopanib uygulamas�na k�yasla ortalama pazopanib EAAve Cde�erlerinde yakla��k %50 ila %60 art��a neden olmu�tur. Lapatinib taraf�ndan P-gp ve/veya BCRP inhibisyonu, muhtemelen pazopanibe maruziyetin art���na katk�da bulunmu�tur.
Pazopanibin lapatinib gibi CYP3A4, P-gp ve BCRP inhibit�rleri ile birlikte uygulanmas� plazma pazopanib konsantrasyonlar�nda art��la sonu�lanacakt�r. G��l� P-gp veya BCRP inhibit�rleriyle birlikte uygulama ayr�ca, merkezi sinir sistemine (MSS) da��l�m da dahil olmak �zere pazopanibe maruziyeti ve pazopanibin da��l�m�n� de�i�tirebilir.
Pazopanibin g��l� bir CYP3A4 inhibit�r� ile e� zamanl� kullan�m�ndan ka��n�lmal�d�r (bkz. B�l�m 4.4). E�er g��l� bir CYP3A4 inhibit�r�ne t�bbi olarak uygun bir alternatif bulunmas� s�z konusu de�ilse, e� zamanl� kullan�m s�resince pazopanibin dozu g�nl�k 400 mg'a
azalt�lmal�d�r. Bu durumda advers reaksiyonlar a��s�ndan yak�ndan izlem yap�lmal�d�r ve ilave doz azalt�mlar�, ilaca ba�l� yan etkilerin g�zlenmesi halinde e�er uygunsa g�z �n�nde bulundurulabilir.
G��l� P-gp veya BCRP inhibit�rleri ile kombinasyondan ka��n�lmal�d�r veya P-gp veya BCRP i�in minimum inhibisyon potansiyeli olan veya hi� olmayan alternatif e�zamanl� ila� se�ilmesi �nerilmektedir.
CYP3A4, P-gp, BCRP ind�kleyiciler
Rifampin gibi CYP3A4 ind�kleyicileri plazma pazopanib konsantrasyonlar�n� d���rebilir. Pazopanibin potent P-gp veya BCRP ind�kleyiciler ile birlikte kullan�m� pazopanib maruziyetini ve MSS'ne yay�lma da dahil olmak �zere pazopanib da��l�m�n� de�i�tirebilir. Enzim veya ta��y�c� ind�ksiyonu potansiyeli en d���k d�zeyde olan veya hi� bulunmayan alternatif e�zamanl� ila� se�ilmesi �nerilmektedir.
Pazopanibin di�er ila�lar �zerindeki etkileri
�nsan karaci�er mikrozomlar� ile yap�lan in vitro �al��malar pazopanibin CYP enzimleri 1A2, 3A4, 2B6, 2C8, 2C9, 2C19 ve 2E1'i inhibe etti�ini g�stermi�tir. �nsan CYP3A4 enzimlerinin potansiyel ind�ksiyonu bir in vitro insan Pregnane X Receptor (PXR) testinde g�sterilmi�tir. G�nde bir kez 800 mg pazopanib ile yap�lan klinik farmakoloji �al��malar� pazopanibin kanser hastalar�nda kafein (CYP1A2 prob substrat�), varfarin (CYP2C9 prob substrat�) veya omeprazol (CYP2C19 prob substrat�) farmakokineti�inde klinik a��dan anlaml� bir etkiye sahip olmad���n� g�stermi�tir. Pazopanib ortalama midazolam EAA ve C(CYP3A4 prob substrat�) de�erlerinde yakla��k %30 art��a ve oral yolla dekstrometorfan (CYP2D6 prob substrat�) uyguland�ktan sonra idrardaki dekstrometorfan-dekstorfan konsantrasyonu oran�nda % 33 ila
% 64 art��a neden olmu�tur. G�nde bir kez 800 mg pazopanib ve haftada bir kez 80 mg/m paklitakselin (CYP3A4 ve CYP2C8 substrat�) birlikte uygulanmas� paklitaksel EAA ve Cde�erlerinde s�ras�yla ortalama %26 ve %31 art��a neden olmu�tur.
In vitro ICve in vivo Cde�erlerine dayanarak, pazopanibin GSK1268992 ve GSK1268997 metabolitleri, pazopanibin BCRP �zerinden net inhibit�r etkisine katk� sa�layabilmektedirler. Ayr�ca, gastrointestinal kanalda BCRP ve P-gp'nin pazopanib kullan�m� ile olu�abilecek inhibisyonu g�z ard� edilemez. Pazopanibin di�er oral BCRP ve P-gp substratlar� ile birlikte kullan�lmas� durumunda dikkatli olunmal�d�r.
�n vitro ko�ullarda pazopanib, insan organik anyon ta��y�c� polipeptidi (OATP1B1) inhibe etmi�tir. Pazopanibin, OATP1B1 substratlar�n�n (�rn. statinler, bkz. a�a��da “E�zamanl� Pazopanib ve Simvastatin kullan�m� �zerindeki etkisi”) farmakokinetik �zelliklerini de�i�tirme olas�l��� g�z ard� edilemez.
Pazopanib, in vitro ortamda �ridin difosfoglukuronil-transferaz 1A1 (UGT1A1) enziminin bir inhibit�r�d�r. �rinotekan�n aktif metaboliti SN-38 OATP1B1 ve UGT1A1 substrat�d�r. G�nde bir kez pazopanib 400 mg'�n setuksimab 250 mg/m ve irinotekan 150 mg/m ile bir arada
uygulanmas�, SN-38'e sistemik maruziyette yakla��k %20'lik bir art�� ile sonu�lanm��t�r. Yaban�l tip aleli olan bireyler ile kar��la�t�r�ld���nda UGT1A1*28 polimorfizmi olan bireylerde pazopanib, SN-38 dispozisyonu �zerinde daha b�y�k bir etkiye sahip olabilir. Ancak UGT1A1 genotipinin SN-38 dispozisyonu �zerindeki etkisinde her zaman prediktif niteli�inin olmad��� g�r�lm��t�r. Pazopanib, UGT1A1 substratlar� ile bir arada uygulan�rken dikkatli olunmal�d�r.
Pazopanibin OATP1B1 substratlar�n�n (�rn. rosuvastatin) farmakokineti�ini etkileyece�i g�z ard� edilemez.
Pazopanib ve simvastatinin e�zamanl� kullan�m�n�n etkisi
Pazopanib ve simvastatinin e�zamanl� kullan�m�, ALT de�erlerinde y�kseli� insidans�n� art�rmaktad�r. Pazopanib ile yap�lan klinik �al��malardan toplanan veriler kullan�larak yap�lan bir meta-analizin sonu�lar�, e�zamanl� simvastatin kullan�m� olan 11/41 (%27) hastayla kar��la�t�r�ld���nda statin kullanmam�� 126/485 (%14) hastada ALT >3x ULN bildirildi�ini g�stermektedir (p = 0,038). E�zamanl� simvastatin alan bir hastada ALT d�zeyleri artarsa, pazopanib dozaj k�lavuzlar� takip edilmeli ve simvastatin kesilmelidir (bkz. B�l�m 4.4). Di�er statinlerle pazopanib e�zamanl� uygulan�rken dikkatli olunmal�d�r ��nk� ALT d�zeyleri �zerine etkilerini belirlemek i�in yeterli veri mevcut de�ildir. Pazopanibin di�er statinlerin (�rn. atorvastatin, fluvastatin, pravastatin, rosuvastatin) farmakokineti�ini etkileme olas�l��� d��lanamaz.
Yiyecek ve i�ecek ile kullan�lmas�
Y�ksek oranda veya d���k oranda ya� i�eren ���nlerle birlikte pazopanib uygulanmas�, EAA ve Cde�erlerinde yakla��k 2 kat art��a neden olmu�tur. Bu nedenle pazopanib ���nlerden en az 1 saat �nce veya 2 saat sonra uygulanmal�d�r.
Mide asiditesini y�kselten ila�lar
Pazopanibin esomeprazol ile birlikte kullan�m� pazopanibin biyoyararlan�m�n� yakla��k olarak
% 40 (EAA ve C) d���rmektedir. Pazopanibin mide asiditesini y�kselten ila�lar ile birlikte uygulanmas�ndan ka��n�lmal�d�r. E�er proton pompa inhibit�r� (PPI) ile birlikte kullan�m� t�bbi a��dan gerekliyse, pazopanib dozunun g�nde 1 kez ak�am saatlerinde a� karn�na PPI ile birlikte al�nmas� �nerilmektedir. E�er H2-resept�r antagonisti ile birlikte uygulanmas� t�bbi a��dan gerekliyse, pazopanib H2-resept�r antagonist dozundan en az 2 saat �nce veya en az 10 saat sonra a� karn�na al�nmal�d�r. Pazopanib, k�sa etkili antiasit al�nmas�ndan 1 saat �nce veya 2 saat sonra al�nmal�d�r. PPI ve H2-resept�r antagonistlerinin birlikte nas�l uygulanaca�� ile ilgili tavsiyeler fizyolojik de�erlendirmelere ba�l�d�r.
4.6. Gebelik ve laktasyon
Gebelik kategorisi: D
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon) Do�urganl�k �a��ndaki kad�nlar, pazopanib tedavisi s�ras�nda ve tedaviden en az 2 hafta sonras�na kadar yeterli kontrasepsiyon kullanmalar� ve gebelikten ka��nmalar� konusunda uyar�lmal�d�r.
Erkek hastalar (vasektomi yapt�rm�� olanlar dahil) pazopanib kullan�rken ve son pazopanib dozunu takiben en az 2 hafta boyunca, �reme potansiyeline sahip kad�n partnerlerine ve gebe partnerlerine potansiyel ila� maruziyetinden ka��nmak �zere cinsel ili�ki s�ras�nda prezervatif kullanmal�d�r.
Gebelik d�nemi
Gebe kad�nlarda pazopanib kullan�m�na ili�kin yeterli veri mevcut de�ildir. Hayvanlar �zerinde yap�lan �al��malarda �reme toksisitesi g�r�lm��t�r (bkz. B�l�m 5.3). �nsanlara y�nelik potansiyel risk bilinmemektedir.
Gebelik s�ras�nda pazopanib kullan�l�rsa veya hasta pazopanib al�rken hamile kal�rsa, fet�se y�nelik potansiyel tehlike hastaya a��klanmal�d�r.
VOPAZZ�, hastan�n klinik durumu pazopanib ile tedaviyi gerektirmedik�e gebelik d�neminde kullan�lmamal�d�r.
Laktasyon d�nemi
Laktasyon s�ras�nda pazopanibin g�venli kullan�m� belirlenmemi�tir. Pazopanibin veya metabolitlerinin insan s�t� ile at�l�p at�lmad��� bilinmemektedir. Pazopanibin hayvan s�t� ile at�l�m�na ili�kin bilgi bulunmamaktad�r. Emzirilen �ocuk a��s�ndan risk g�z ard� edilemez. Pazopanib tedavisi s�ras�nda emzirme kesilmelidir.
�reme yetene�i / Fertilite
Hayvan �al��malar�, pazopanib ile tedavinin erkek ve kad�n fertilitesini etkileyebilece�ini g�stermektedir (bkz. B�l�m 5.3).
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
VOPAZZ�'nin ara� ve makine kullan�m� �zerinde etkisi yoktur ya da etki ihmal edilebilir d�zeydedir. Pazopanib farmakolojisi g�z �n�ne al�nd���nda bu aktiviteler �zerinde zararl� bir etkisi olup olmad��� �ng�r�lemez. Hastan�n muhakeme, motor veya kognitif yetenekler gerektiren i�leri yapabilme becerisi hastan�n klinik durumu ve pazopanibin istenmeyen etki profili g�z �n�nde bulundurularak de�erlendirilmelidir. Hastalar, ba� d�nmesi, yorgunluk ya da g��s�zl�k durumunda ara� ya da makine kullan�m�ndan ka��nmal�d�r.
4.8. �stenmeyen etkiler
RRC'li hastalarda pazopanibin (toplam n=1149) g�venlili�i ve tolerabilitesinin genel de�erlendirilmesinde pivotal RCC �al��mas� (VEG105192, n=290), uzatma �al��mas� (VEG107769, n=71), destekleyici Faz II �al��ma (VEG102616, n=225) ve randomize, a��k
etiketli, paralel grup Faz III e�it etkililik �al��mas�n�n (VEG108844, n=557) birle�tirilmi� verileri de�erlendirilmi�tir (bkz. B�l�m 5.1).
�nc� STS �al��mas� (VEG110727, n=369) ve destekleyici Faz II �al��madan (VEG20002, n=142) elde edilen birle�tirilmi� veriler, STS'li hastalarda (toplam g�venlilik pop�lasyonu say�s�=382) pazopanibin genel g�venlilik ve tolerabilite incelemesinde de�erlendirilmi�tir (bkz. B�l�m 5.1).
RCC veya STS �al��malar�nda tespit edilmi�, pazopanib tedavisi ile ili�kili en �nemli istenmeyen etkiler ge�ici iskemik atak, iskemik inme, miyokard iskemisi, miyokard infarkt�s� ve serebral infarkt�s, kardiyak disfonksiyon, gastrointestinal perforasyon ve fist�l, QT uzamas�, Torsade de Pointes ve pulmoner, gastrointestinal ve serebral hemoraji olup bu olaylar�n t�m� tedavi uygulanan hastalar�n %1'inden daha az�nda bildirilmi�tir. STS �al��malar�nda tan�mlanm�� di�er �nemli ciddi istenmeyen etkiler, ven�z tromboembolik olaylar, sol ventrik�l disfonksiyonu ve pn�motoraks olarak belirtilmi�tir.
Pazopanib ile muhtemelen ili�kili oldu�u d���n�len �l�mc�l olaylar aras�nda gastrointestinal hemoraji, pulmoner hemoraji/hemoptizi, anormal hepatik fonksiyon, intestinal perforasyon ve iskemik inme bulunmaktad�r.
RCC ve STS �al��malar�ndaki, tedavi ile ili�kili herhangi bir evredeki en yayg�n istenmeyen etkiler (hastalar�n en az %10'unda meydana gelen) a�a��dakilerden olu�maktad�r: Diyare, sa� renginde de�i�iklik, ciltte hipopigmentasyon, eksfolyatif d�k�nt�, hipertansiyon, bulant�, ba� a�r�s�, yorgunluk, anoreksi, kusma, tat alma duyusunda bozulma, stomatit, kilo azalmas�, a�r�, alanin aminotransferaz d�zeyinde art�� ve aspartat aminotransferaz d�zeyinde art��.
RCC ve STS hastalar�nda bildirilen tedavi ile ili�kili t�m evrelerdeki yan etkiler a�a��da MedDRA v�cut organ sistemi s�n�f�na g�re liste halinde sunulmaktad�r. S�kl�k kategorilendirilmesi i�in a�a��daki kategori �l�e�i kullan�lm��t�r:
�ok yayg�n (≥1/10); yayg�n (≥1/100 ila <1/10); yayg�n olmayan (≥1/1.000 ila <1/100); seyrek (≥1/10.000 ila <1/1.000); �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor).
Kategoriler klinik �al��ma verilerindeki mutlak s�kl�klar temelinde de�erlendirilmi�tir. T�m pazopanib klinik �al��malar�ndan ve spontan bildirimlerden g�venlilik ve tolerabiliteye ili�kin pazarlama sonras� veriler de de�erlendirilmi�tir. Her bir sistem organ s�n�f� i�inde, ayn� s�kl��a sahip advers reaksiyonlar azalan ciddiyet derecesine g�re sunulmaktad�r.
RCC �al��mas�nda (n=1149) veya pazarlama sonras� d�nemde rapor edilen tedavi ile ili�kili advers reaksiyonlar:
Enfeksiyonlar ve enfestasyonlar
Yayg�n: Enfeksiyonlar (n�tropeninin e�lik etti�i veya etmedi�i) Yayg�n olmayan: Di� eti enfeksiyonu, enfeksiy�z peritonit
�yi huylu ve k�t� huylu neoplazmalar (kist ve polipler dahil)
Yayg�n olmayan: T�m�r a�r�s�
Kan ve lenf sistemi hastal�klar�
Yayg�n: Trombositopeni, n�tropeni, l�kopeni Yayg�n olmayan: Polisitemi
Seyrek: Trombotik mikroanjiyopati (trombotik trombositopenik purpura ve hemolitik �remik sendrom dahil)
Endokrin hastal�klar�
Yayg�n: Hipotiroidizm
Metabolizma ve beslenme hastal�klar�
�ok yayg�n: ��tah azalmas�
Yayg�n: Dehidrasyon, hipofosfatemi Yayg�n olmayan: Hipomagnezemi Bilinmiyor: T�m�r lizis sendromu*
Psikiyatrik hastal�klar
Yayg�n: Uykusuzluk
Sinir sistemi hastal�klar�
�ok yayg�n: Tat alma duyusunda bozulma, ba� a�r�s�
Yayg�n: Sersemlik, letarji, parestezi, periferik duyusal n�ropati
Yayg�n olmayan: Hipoestezi, ge�ici iskemik atak, uyuklama, serebrovask�ler olay, iskemik inme
Seyrek: Posterior geri d�n��l� ensefalopati sendromu / Geri d�n��l� posterior l�koensefalopati sendromu
G�z hastal�klar�
Yayg�n: Bulan�k g�rme
Yayg�n olmayan: Retina dekolman� , retina y�rt�lmas� , kirpikte renksizle�me
Kardiyak hastal�klar
Yayg�n olmayan: Bradikardi, kardiyak disfonksiyon, miyokard infarkt�s�, miyokard iskemisi
Vask�ler hastal�klar
�ok yayg�n: Hipertansiyon
Yayg�n: S�cak basmas�, al basmas�, ven�z tromboembolik olaylar Yayg�n olmayan: Hemoraji, hipertansif kriz
Bilinmiyor: Anevrizmalar ve arter diseksiyonlar�
Solunum, g���s bozukluklar� ve mediastinal hastal�klar
Yayg�n: Epistaksis, disfoni, dispne, hemoptizi
Yayg�n olmayan: Pulmoner hemoraji, rinore, pn�motoraks Seyrek: �nterstisyel akci�er hastal���/ pn�moni †
Gastrointestinal hastal�klar
�ok yayg�n: Diyare, bulant�, kusma, kar�n a�r�s�
Yayg�n: Dispepsi, stomatit, flatulans (kar�nda gaz ve �i�kinlik), abdominal distansiyon, a��z kurulu�u, a��zda �lser
Yayg�n olmayan: Pankreatit, rektal hemoraji, hematokezi, gastrointestinal hemoraji, melena, s�k ba��rsak hareketleri, anal hemoraji, kal�n ba��rsak perforasyonu, a��zda hemoraji, �st gastrointestinal hemoraji, enterokutan fist�l, hematemez, hemoroidal hemoraji, ileum perforasyonu, �zofagus hemorajisi, retroperitoneal hemoraji
Hepato-biliyer hastal�klar
Yayg�n: Anormal hepatik fonksiyon, hiperbilirubinemi, hepatotoksisite Yayg�n olmayan: Sar�l�k, karaci�er yetmezli�i, ilaca ba�l� karaci�er hasar�
Deri ve deri alt� doku hastal�klar�
�ok yayg�n: Sa� renginde de�i�iklik, palmar-plantar eritrodizestezi sendromu, alopesi, d�k�nt�
Yayg�n: Deride hipopigmentasyon, eritem, prurit, deride depigmentasyon, ciltte kuruluk, hiperhidroz
Yayg�n olmayan: T�rnak bozukluklar�, foto-duyarl�l�k reaksiyonu, deride eksfolyasyon (soyulma), kabarc�kl� d�k�nt�, jeneralize pruritus, pap�ler d�k�nt�, plantar eritema, eritemat�z d�k�nt�, jeneralize d�k�nt�, mak�ler d�k�nt�, pruritik d�k�nt�, cilt bozuklu�u
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar�
Yayg�n: Miyalji, kas spazmlar�, artralji Yayg�n olmayan: Kas-iskelet a�r�s�
B�brek ve idrar yolu hastal�klar�
�ok yayg�n: Protein�ri
Yayg�n olmayan: �riner sistemde hemoraji
�reme ve meme hastal�klar�
Yayg�n olmayan: Menoraji, metroraji, vajinal hemoraji
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar
�ok yayg�n: Yorgunluk
Yayg�n: Asteni, mukozal inflamasyon, �dem, g���s a�r�s� Yayg�n olmayan: Mukoz membran bozuklu�u, �rperme
Ara�t�rmalar
�ok yayg�n: Alanin aminotransferaz art���, aspartat aminotransferaz art���
Yayg�n: Kilo kayb�, kanda kreatinin art���, kanda bilirubin art���, beyaz kan h�cresi say�s�nda azalma, lipaz art���, kan bas�nc�nda art��, kanda tiroidi uyar�c� hormon art���, gama- glutamiltransferaz art���, amilaz art���, anormal karaci�er fonksiyon testi, kanda �re art��� Yayg�n olmayan: Elektrokardiyogram QT uzamas�, kan glukozunda azalma, transaminaz art���, diastolik kan bas�nc�nda art��, anormal tiroid fonksiyon testi, sistolik kan bas�nc�nda art��, hepatik enzim art���
Advers reaksiyonlar�n tablo halinde listesi
Tablo 1: RCC �al��mas�nda (n=1149) veya pazarlama sonras� d�nemde rapor edilen tedavi ile ili�kili advers reaksiyonlar
Sistem Organ S�n�f� | S�kl�k (t�m evrelerde) | Advers reaksiyon | T�m evreler | Evre 3 Say� (%) | Evre 4 Say� (%) |
Enfeksiyonlar ve enfestasyonlar | Yayg�n | Enfeksiyonlar (n�tropeninin e�lik etti�i veya etmedi�i)† | Bilinmiyor | Bilinmiyor | Bilinmiyor |
| Yayg�n olmayan | Di� eti enfeksiyonu | 1 (<% 1) | 0 | 0 |
|
| Enfeksiy�z peritonit | 1 (<% 1) | 0 | 0 |
�yi huylu ve k�t� huylu neoplazmalar (kist ve polipler dahil) | Yayg�n olmayan | T�m�r a�r�s� | 1 (<% 1) | 1 (<% 1) | 0 |
Kan ve lenf sistemi hastal�klar� | Yayg�n | Trombositopeni | 80 (% 7) | 10 (<% 1) | 5 (<% 1) |
|
| N�tropeni | 79 (% 7) | 20 (% 2) | 4 (<% 1) |
|
| L�kopeni | 63 (% 5) | 5 (<% 1) | 0 |
| Yayg�n olmayan | Polisitemi | 6 (% 0,03) | 1 | 0 |
| Seyrek | Trombotik mikroanjiyopati (trombotik trombositopenik purpura ve hemolitik �remik sendrom dahil) † | Bilinmiyor | Bilinmiyor | Bilinmiyor |
Endokrin hastal�klar� | Yayg�n | Hipotiroidizm | 83 (% 7) | 1 (<% 1) | 0 |
Metabolizma ve beslenme hastal�klar� | �ok yayg�n | ��tah azalmas� | 317 (% 28) | 14 (% 1) | 0 |
| Yayg�n | Dehidrasyon | 16 (% 1) | 5 (<% 1) | 0 |
|
| Hipofosfatemi | 21 (% 2) | 7 (<% 1) | 0 |
| Yayg�n olmayan | Hipomagnezemi | 10 (<% 1) | 0 | 0 |
| Bilinmiyor | T�m�r lizis sendromu* | Bilinmiyor | Bilinmiyor | Bilinmiyor |
Psikiyatrik hastal�klar | Yayg�n | Uykusuzluk | 30 (% 3) | 0 | 0 |
Sinir sistemi hastal�klar� | �ok yayg�n | Tat alma duyusunda bozulma | 254 (% 22) | 1 (<% 1) | 0 |
|
| Ba� a�r�s� | 122 (% 11) | 11 (<% 1) | 0 |
| Yayg�n | Sersemlik | 55 (% 5) | 3 (<% 1) | 1 (<% 1) |
|
| Letarji | 30 (% 3) | 3 (<% 1) | 0 |
|
| Parestezi | 20 (% 2) | 2 (<% 1) | 0 |
|
| Periferik duyusal n�ropati | 17 (% 1) | 0 | 0 |
| Yayg�n olmayan | Hipoestezi | 8 (<%1) | 0 | 0 |
|
| Ge�ici iskemik atak | 7 (<%1) | 4 (<%1) | 0 |
|
| Uyuklama | 3 (<%1) | 1 (<%1) | 0 |
|
| Serebrovask�ler olay | 2 (<%1) | 1 (<%1) | 1 (<%1) |
|
| �skemik inme | 2 (<%1) | 0 | 1 (<%1) |
| Seyrek | Posterior geri d�n��l� ensefalopati sendromu / Geri d�n��l� posterior | Bilinmiyor | Bilinmiyor | Bilinmiyor |
|
| l�koensefalopati sendromu † |
|
|
|
G�z hastal�klar� | Yayg�n | Bulan�k g�rme | 19 (% 2) | 1 (<% 1) | 0 |
| Yayg�n olmayan | Retina dekolman� † | 1 (<% 1) | 1 (<% 1) | 0 |
|
| Retina y�rt�lmas� † | 1 (<% 1) | 1 (<% 1) | 0 |
|
| Kirpikte renksizle�me | 4 (<% 1) | 0 | 0 |
Kardiyak hastal�klar | Yayg�n olmayan | Bradikardi | 6 (<% 1) | 0 | 0 |
|
| Kardiyak disfonksiyon | 4 (<% 1) | 1 (<% 1) | 0 |
|
| Miyokard infarkt�s� | 5 (<% 1) | 1 (<% 1) | 4 (<% 1) |
|
| Miyokard iskemisi | 3 (<% 1) | 1 (<% 1) | 0 |
Vask�ler hastal�klar | �ok yayg�n | Hipertansiyon | 473 (% 41) | 115 (% 10) | 1 (<% 1) |
| Yayg�n | S�cak basmas� | 16 (% 1) | 0 | 0 |
|
| Al basmas� | 12 (% 1) | 0 | 0 |
|
| Ven�z tromboembolik olaylar | 13 (% 1) | 6 (<% 1) | 7 (<% 1) |
| Yayg�n olmayan | Hemoraji | 1 (<% 1) | 0 | 0 |
|
| Hipertansif kriz | 6 (<% 1) | 0 | 2 (<% 1) |
| Bilinmiyor | Anevrizmalar ve arter diseksiyonlar� | Bilinmiyor | Bilinmiyor | Bilinmiyor |
Solunum, g���s bozukluklar� ve mediastinal hastal�klar | Yayg�n | Epistaksis | 50 (% 4) | 1 (<% 1) | 0 |
|
| Disfoni | 48 (% 4) | 0 | 0 |
|
| Dispne | 42 (% 4) | 8 (<% 1) | 1 (<% 1) |
|
| Hemoptizi | 15 (% 1) | 1 (<% 1) | 0 |
| Yayg�n olmayan | Pulmoner hemoraji | 2 (<% 1) | 0 | 0 |
|
| Rinore | 8 (<% 1) | 0 | 0 |
|
| Pn�motoraks | 1 (<% 1) | 0 | 0 |
| Seyrek | �nterstisyel akci�er hastal���/ pn�moni † | Bilinmiyor | Bilinmiyor | Bilinmiyor |
Gastrointestinal hastal�klar | �ok yayg�n | Diyare | 614 (% 53) | 65 (% 6) | 2 (<% 1) |
|
| Bulant� | 386 (% 34) | 14 (% 1) | 0 |
|
| Kusma | 225 (% 20) | 18 (% 2) | 1 (<% 1) |
|
| Kar�n a�r�s� | 139 (% 12) | 15 (% 1) | 0 |
| Yayg�n | Dispepsi | 83 (% 7) | 2 (<% 1) | 0 |
|
| Stomatit | 96 (% 8) | 4 (<% 1) | 0 |
|
| Flatulans (kar�nda gaz ve �i�kinlik) | 43 (% 4) | 0 | 0 |
|
| Abdominal distansiyon | 36 (% 3) | 2 (<% 1) | 0 |
|
| A��z kurulu�u | 28 (% 2) | 3 (<% 1) | 0 |
|
| A��zda �lser | 27 (% 2) | 0 | 0 |
| Yayg�n olmayan | Pankreatit | 8 (<% 1) | 4 (<% 1) | 0 |
|
| Rektal hemoraji | 8 (<% 1) | 2 (<% 1) | 0 |
|
| Hematokezi | 6 (<% 1) | 0 | 0 |
|
| Gastrointestinal hemoraji | 4 (<% 1) | 2 (<% 1) | 0 |
|
| Melena | 4 (<% 1) | 1(<% 1) | 0 |
|
| S�k ba��rsak hareketleri | 3 (<% 1) | 0 | 0 |
|
| Anal hemoraji | 2 (<% 1) | 0 | 0 |
|
| Kal�n ba��rsak perforasyonu | 2 (<% 1) | 1 (<% 1) | 0 |
|
| A��zda hemoraji | 2 (<% 1) | 0 | 0 |
|
| �st gastrointestineal hemoraji | 2 (<% 1) | 1 (<% 1) | 0 |
|
| Enterokutan fist�l | 1 (<% 1) | 0 | 0 |
|
| Hematemez | 1 (<% 1) | 0 | 0 |
|
| Hemoroidal hemoraji | 1 (<% 1) | 0 | 0 |
|
| �leum perforasyonu | 1 (<% 1) | 0 | 1 (<% 1) |
|
| �zofagus hemorajisi | 1 (<% 1) | 0 | 0 |
|
| Retroperitoneal hemoraji | 1 (<% 1) | 0 | 0 |
Hepato-biliyer hastal�klar | Yayg�n | Anormal hepatik fonksiyon | 29 (% 3) | 13 (% 1) | 2 (<% 1) |
|
| Hiperbilirubinemi | 38 (% 3) | 2 (<% 1) | 1 (<% 1) |
|
| Hepatotoksisite | 18 (% 2) | 11(<% 1) | 2 (<% 1) |
| Yayg�n olmayan | Sar�l�k | 3 (<% 1) | 1 (<% 1) | 0 |
|
| Karaci�er yetmezli�i | 1 (<% 1) | 0 | 1 (<% 1) |
|
| �laca ba�l� karaci�er hasar� | 2 (<% 1) | 2 (<% 1) | 0 |
Deri ve deri alt� doku hastal�klar� | �ok yayg�n | Sa� renginde de�i�iklik | 404 (% 35) | 1 (<% 1) | 0 |
|
| Palmar-plantar eritrodizestezi sendromu | 206 (% 18) | 39 (% 3) | 0 |
|
| Alopesi | 130 (% 11) | 0 | 0 |
|
| D�k�nt� | 129 (% 11) | 7 (<% 1) | 0 |
| Yayg�n | Deride hipopigmentasyon | 52 (% 5) | 0 | 0 |
|
| Eritem | 25 (% 2) | 0 | 0 |
|
| Prurit | 29 (% 3) | 0 | 0 |
|
| Deride depigmentasyon | 20 (% 2) | 0 | 0 |
|
| Ciltte kuruluk | 50 (% 4) | 0 | 0 |
|
| Hiperhidroz | 17 (% 1) | 0 | 0 |
| Yayg�n olmayan | T�rnak bozukluklar� | Nail disorders | 11 (<% 1) | 0 |
|
| Foto-duyarl�l�k reaksiyonu | 7 (<% 1) | 0 | 0 |
|
| Deride eksfolyasyon (soyulma | 10 (<% 1) | 0 | 0 |
|
| Kabarc�kl� d�k�nt� | 6 (<% 1) | 0 | 0 |
|
| Jeneralize pruritus | 2 (<% 1) | 0 | 0 |
|
| Pap�ler d�k�nt� | 2 (<% 1) | 0 | 0 |
|
| Plantar eritema | 1 (<% 1) | 0 | 0 |
|
| Eritemat�z d�k�nt� | 6 (<% 1) | 0 | 0 |
|
| Jeneralize d�k�nt� | 2 (<% 1) | 1 (<% 1) | 0 |
|
| Mak�ler d�k�nt� | 4 (<% 1) | 0 | 0 |
|
| Pruritik d�k�nt� | 3 (<% 1) | 0 | 0 |
|
| Cilt bozuklu�u | 5 (<% 1) | 0 | 0 |
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar� | Yayg�n | Miyalji | 35 (% 3) | 2 (<% 1) | 0 |
|
| Kas spazmlar� | 25 (% 2) | 0 | 0 |
|
| Artralji | 48 (% 4) | 8 (<% 1) | 0 |
| Yayg�n olmayan | Kas-iskelet a�r�s� | 9 (<% 1) | 1 (<% 1) | 0 |
B�brek ve idrar yolu hastal�klar� | �ok yayg�n | Protein�ri | 135 (% 12) | 32 (% 3) | 0 |
| Yayg�n olmayan | �riner sistemde hemoraji | 1 (<% 1) | 0 | 0 |
�reme ve meme hastal�klar� | Yayg�n olmayan | Menoraji | 3 (<% 1) | 0 | 0 |
|
| Metroraji | 1 (<% 1) | 0 | 0 |
|
| Vajinal hemoraji | 3 (<% 1) | 0 | 0 |
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar | �ok yayg�n | Yorgunluk | 415 (% 36) | 65 (% 6) | 1 (<% 1) |
| Yayg�n | Asteni | 82 (% 7) | 20 (% 2) | 1 (<% 1) |
|
| Mukozal inflamasyon | 86 (% 7) | 5 (<% 1) | 0 |
|
| �dem | 72 (% 6) | 1 (<% 1) | 0 |
|
| G���s a�r�s� | 18 (% 2) | 2 (<% 1) | 0 |
| Yayg�n olmayan | Mukoz membran bozuklu�u | 1 (<% 1) | 0 | 0 |
|
| �rperme | 4 (<% 1) | 0 | 0 |
Ara�t�rmalar | �ok yayg�n | Alanin aminotransferaz art��� | 246 (% 21) | 84 (% 7) | 14 (% 1) |
|
| Aspartat aminotransferaz art��� | 211 (% 18) | 51 (% 4) | 10 (<% 1) |
| Yayg�n | Kilo kayb� | 96 (% 8) | 7 (<% 1) | 0 |
|
| Kanda kreatinin art��� | 55 (% 5) | 3 (<% 1) | 0 |
|
| Kanda bilirubin art��� | 61 (% 5) | 6 (<% 1) | 1 (<% 1) |
|
| Beyaz kan h�cresi say�s�nda azalma | 51 (% 4) | 3 (<% 1) | 0 |
|
| Lipaz art��� | 51 (% 4) | 21 (% 2) | 7 (<% 1) |
|
| Kan bas�nc�nda art�� | 15 (% 1) | 2 (<% 1) | 0 |
|
| Kanda tiroidi uyar�c� hormon art��� | 36 (% 3) | 0 | 0 |
|
| Gama- glutamiltransferaz art��� | 31 (% 3) | 9 (<% 1) | 4 (<% 1) |
|
| Amilaz art��� | 35 (% 3) | 7 (<% 1) | 0 |
|
| Anormal karaci�er fonksiyon testi | 12 (% 1) | 6 (<% 1) | 1 (<% 1) |
|
| Kanda �re art��� | 12 (% 1) | 1 (<% 1) | 0 |
| Yayg�n olmayan | Elektrokardiyogram QT uzamas� | 7 (<% 1) | 2 (<% 1) | 0 |
|
| Kan glukozunda azalma | 7 (<% 1) | 0 | 1 (<% 1) |
|
| Transaminaz art��� | 7 (<% 1) | 1 (<% 1) | 0 |
|
| Diastolik kan bas�nc�nda art�� | 2 (<% 1) | 0 | 0 |
|
| Anormal tiroid fonksiyon testi | 3 (<% 1) | 0 | 0 |
|
| Sistolik kan bas�nc�nda art�� | 1 (<% 1) | 0 | 0 |
|
| Hepatik enzim art��� | 11 (<% 1) | 4 (<% 1) | 3 (<% 1) |
*Yaln�zca pazarlama sonras� d�nemde bildirilmi� tedaviyle ili�kili advers reaksiyon. S�kl�k mevcut verilerden tahmin edilemez.
A�a��daki terimler birle�tirilerek sunulmu�tur.
N�tropeni, trombositopeni ve palmar- plantar eritrodisestezi sendromu Do�u Asya k�kenli hastalarda daha s�kl�kla g�zlenmi�tir.
STS �al��malar�nda (n=382) ya da pazarlama sonras� d�nemde raporlanan tedavi ile ili�kili advers reaksiyonlar
Enfeksiyonlar ve enfestasyonlar
Yayg�n: Gingiva enfeksiyonu
�yi huylu ve k�t� huylu neoplazmalar ile tan�mlanmam�� (kist ve polipler dahil)
�ok yayg�n: T�m�r a�r�s�
Kan ve lenf sistemi hastal�klar�
�ok yayg�n: L�kopeni, trombositopeni, n�tropeni
Yayg�n olmayan: Trombotik mikroanjiyopati (trombotik trombositopenik purpura ve hemolitik �remik sendrom dahil)
Endokrin hastal�klar�
Yayg�n: Hipotiroidizm
Metabolizma ve beslenme hastal�klar�
�ok yayg�n: Hipoalbuminemi, i�tah azalmas� Yayg�n: Dehidratasyon
Yayg�n olmayan: Hipomagnezemi Bilinmiyor: T�m�r lizis sendromu*
Psikiyatrik hastal�klar
Yayg�n: �nsomnia
Sinir sistemi hastal�klar�
�ok yayg�n: Tat alma duyusunda bozulma, ba� a�r�s� Yayg�n: Periferik duyusal n�ropati, sersemlik
Yayg�n olmayan: Somnolans, serebral infarkt�s, parestezi
G�z hastal�klar�
Yayg�n: Bulan�k g�rme
Kardiyak hastal�klar
Yayg�n: Kardiyak disfonksiyon, sol ventrik�l disfonksiyonu, bradikardi
Yayg�n olmayan: Miyokard infarkt�s�
Vask�ler hastal�klar
�ok yayg�n: Hipertansiyon
Yayg�n: Ven�z tromboembolik olay, s�cak basmas�, al basmas� Yayg�n olmayan: Hemoraji
Bilinmiyor: Anevrizmalar ve arter diseksiyonlar�
Solunum, g���s bozukluklar� ve mediastinal hastal�klar
Yayg�n: Epistaksis, disfoni, dispne, �ks�r�k, pn�motoraks, h��k�r�k, pulmoner hemoraji Yayg�n olmayan: Orofaringeal a�r�, bron�iyal hemoraji, rinore, hemoptizi
Seyrek: �nterstisyel akci�er hastal���/pn�moni
Gastrointestinal hastal�klar
�ok yayg�n: Diyare, bulant�, kusma, kar�n a�r�s�, stomatit
Yayg�n: Kar�n �i�li�i, a��z kurulu�u, dispepsi, a��zda hemoraji, flatulans,anal hemoraji
Yayg�n olmayan: Gastrointestinal hemoraji, rektal hemoraji, enterokutan�z fist�l, gastrik hemoraji, melena, �zofagus hemorajisi, peritonit, retroperitoneal
hemoraji, �st gastrointestinal hemoraji, ileum perforasyonu
Hepato-biliyer hastal�klar
Yayg�n olmayan: Anormal hepatik fonksiyon Bilinmiyor: Karaci�er yetmezli�i*
Deri ve deri alt� doku hastal�klar�
�ok yayg�n: Sa� renginde de�i�iklik, deride hipopigmentasyon, eksfolyatif d�k�nt� Yayg�n: Alopesi, cilt bozuklu�u, cilt kurulu�u, t�rnak bozuklu�u, pruritus,
eritem, hiperhidrozis
Yayg�n olmayan: Cilt �lseri, palmar-plantar eritrodizestezi sendromu, ����a duyarl�l�k reaksiyonu, pap�ler d�k�nt�, d�k�nt�
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar�
Yayg�n: Kas-iskelet a�r�s�, miyalji, kas spazmlar� Yayg�n olmayan: Artralji
B�brek ve idrar yolu hastal�klar�
Yayg�n olmayan: Protein�ri
�reme sistemi ve meme hastal�klar�
Yayg�n olmayan: Vajinal hemoraji, menoraji
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar
�ok yayg�n: Yorgunluk
Yayg�n: �dem, g���s a�r�s�, �rperme
Yayg�n olmayan: Mukoza enflamasyonu , asteni
Ara�t�rmalar
�ok yayg�n: Kilo kayb�
Yayg�n: Anormal kulak, burun, bo�az muayenesi , alanin aminotransferaz art���, anormal kan kolesterol d�zeyi, aspartat aminotransferaz art���, gama glutamiltransferaz art���
Yayg�n olmayan: Kan bilirubin seviyelerinde art��, aspartat aminotransferaz, alanin aminotransferaz, trombosit say�s�nda d����, elektrokardiyogramda QT uzamas�
Advers reaksiyonlar�n tablo halinde listesi
Tablo 2: STS �al��malar�nda (n=382) ya da pazarlama sonras� d�nemde raporlanan tedavi ile ili�kili advers reaksiyonlar
Sistem Organ S�n�f� | S�kl�k (t�m evrelerde) | Advers reaksiyon | T�m evreler | Evre 3 Say� (%) | Evre 4 Say� (%) |
Enfeksiyonlar ve enfestasyonlar | Yayg�n | Di� eti enfeksiyonu | 4 (<% 1) | 0 | 0 |
�yi huylu ve k�t� huylu neoplazmalar (kist ve polipler dahil) | �ok yayg�n | T�m�r a�r�s� | 121 (% 32) | 32 (% 8) | 0 |
Kan ve lenf sistemi hastal�klar� | �ok yayg�n | Trombositopeni | 86 (% 36) | 7 (% 3) | 2 (<% 1) |
|
| N�tropeni | 79 (% 33) | 10 (% 4) | 0 |
|
| L�kopeni | 106 (% 44) | 3 (% 1) | 0 |
| Yayg�n olmayan | Trombotik mikroanjiyopati (trombotik trombositopenik purpura ve hemolitik �remik sendrom dahil) | 1 (<% 1) | 1 (<% 1) | 0 |
Endokrin hastal�klar� | Yayg�n | Hipotiroidizm | 18 (% 5) | 0 | 0 |
Metabolizma ve beslenme hastal�klar� | �ok yayg�n | ��tah azalmas� | 108 (% 28) | 12 (% 3) | 0 |
|
| Hipoalb�minemi | 81 (% 34) | 2 (<% 1) | 0 |
| Yayg�n | Dehidrasyon | 4 (% 1) | 2 (<% 1) | 0 |
| Yayg�n olmayan | Hipomagnezemi | 1 (<% 1) | 0 | 0 |
| Bilinmiyor | T�m�r lizis sendromu* | Bilinmiyor | Bilinmiyor | Bilinmiyor |
Psikiyatrik hastal�klar | Yayg�n | Uykusuzluk | 5 (% 1) | 1 (<% 1) | 0 |
Sinir sistemi hastal�klar� | �ok yayg�n | Tat alma duyusunda bozulma | 79 (% 21) | 0 | 0 |
|
| Ba� a�r�s� | 54 (% 14) | 2 (<% 1) | 0 |
| Yayg�n | Sersemlik | 15 (% 4) | 0 | 0 |
|
| Periferik duyusal n�ropati | 30 (% 8) | 1 (<% 1) | 0 |
| Yayg�n olmayan | Parestezi | 1 (<%1) | 0 | 0 |
|
| Uyuklama | 3 (<%1) | 0 | 0 |
|
| Serebral infarkt�s | 1 (<%1) | 0 | 1 (<%1) |
G�z hastal�klar� | Yayg�n | Bulan�k g�rme | 15 (% 4) | 0 | 0 |
Kardiyak hastal�klar | Yayg�n | Bradikardi | 4 (% 1) | 0 | 0 |
|
| Kardiyak disfonksiyon | 21 (<% 5) | 3 (<% 1) | 1 (<% 1) |
|
| Sol ventrik�l disfonksiyonu | 13 (% 3) | 3 (<% 1) | 0 |
| Yayg�n olmayan | Miyokard infarkt�s� | 1 (<% 1) | 0 | 0 |
Vask�ler hastal�klar | �ok yayg�n | Hipertansiyon | 152 (% 40) | 26 (% 7) | 0 |
| Yayg�n | S�cak basmas� | 12 (% 3) | 0 | 0 |
|
| Al basmas� | 4 (% 1) | 0 | 0 |
|
| Ven�z tromboembolik olaylar | 13 (% 3) | 4 (% 1) | 5 (% 1) |
| Yayg�n olmayan | Hemoraji | 2 (<% 1) | 1 (<% 1) | 0 |
| Bilinmiyor | Anevrizmalar ve arter diseksiyonlar� | Bilinmiyor | Bilinmiyor | Bilinmiyor |
Solunum, g���s bozukluklar� ve mediastinal hastal�klar | Yayg�n | Epistaksis | 22 (% 6) | 0 | 0 |
|
| Disfoni | 20 (% 6) | 0 | 0 |
|
| Dispne | 14 (% 4) | 3 (<% 1) | 0 |
|
| �ks�r�k | 12 (% 3) | 0 | 0 |
|
| Pn�motoraks | 7 (% 2) | 2 (<% 1) | 1 (<% 1) |
|
| H��k�r�k | 4 (% 1) | 0 | 0 |
|
| Pulmoner hemoraji | 4 (% 1) | 1 (<% 1) | 0 |
| Yayg�n olmayan | Orofaringeal a�r� | 3 (<% 1) | 0 | 0 |
|
| Bron�iyal hemoraji | 2 (<% 1) | 0 | 0 |
|
| Rinore | 1 (<% 1) | 0 | 0 |
|
| Hemoptizi | 1 (<% 1) | 0 | 0 |
| Seyrek | �nterstisyel akci�er hastal���/ pn�moni † | Bilinmiyor | Bilinmiyor | Bilinmiyor |
Gastrointestinal hastal�klar | �ok yayg�n | Diyare | 174 (% 46) | 17 (% 4) | 0 |
|
| Bulant� | 167 (% 44) | 8 (% 2) | 0 |
|
| Kusma | 96 (% 25) | 7 (% 2) | 0 |
|
| Kar�n a�r�s� | 55 (% 14) | 4 (% 1) | 0 |
|
| Stomatit | 41 (% 11) | 1 (<% 1) | 0 |
| Yayg�n | Kar�n �i�li�i | 16 (% 4) | 2 (% 1) | 0 |
|
| A��z kurulu�u | 14 (% 4) | 0 | 0 |
|
| Dispepsi | 12 (% 3) | 0 | 0 |
|
| A��zda hemoraji | 5 (% 1) | 0 | 0 |
|
| Flatulans | 5 (% 1) | 0 | 0 |
|
| Anal hemoraji | 4 (% 1) | 0 | 0 |
| Yayg�n olmayan | Gastrointestinal hemoraji | 2 (<% 1) | 0 | 0 |
|
| Rektal hemoraji | 2 (<% 1) | 0 | 0 |
|
| Enterokutan fist�l | 1 (<% 1) | 1 (<% 1) | 0 |
|
| Gastrik hemoraji | 1 (<% 1) | 0 | 0 |
|
| Melena | 2 (<% 1) | 0 | 0 |
|
| �zofagus hemorajisi | 1 (<% 1) | 0 | 1 (<% 1) |
|
| Peritonit | 1 (<% 1) | 0 | 0 |
|
| Retroperitoneal hemoraji | 1 (<% 1) | 0 | 0 |
|
| �st gastrointestineal hemoraji | 1 (<% 1) | 1 (<% 1) | 0 |
|
| �leum perforasyonu | 1 (<% 1) | 0 | 1 (<% 1) |
Hepato-biliyer hastal�klar | Yayg�n olmayan | Anormal hepatik fonksiyon | 2 (<% 1) | 0 | 1 (<% 1) |
Deri ve deri alt� doku hastal�klar� | �ok yayg�n | Sa� renginde de�i�iklik | 93 (% 24) | 0 | 0 |
|
| Deride hipopigmentasyon | 80 (% 21) | 0 | 0 |
|
| Eksfolyatif d�k�nt� | 52 (% 14) | 2 (<% 1) | 0 |
| Yayg�n | Alopesi | 30 (% 8) | 0 | 0 |
|
| Cilt bozuklu�u | 26 (% 7) | 4 (% 1) | 0 |
|
| Cilt kurulu�u | 21 (% 5) | 0 | 0 |
|
| T�rnak bozuklu�u | 13 (% 3) | 0 | 0 |
|
| Pruritus | 11 (% 3) | 0 | 0 |
|
| Eritem | 4 (% 1) | 0 | 0 |
|
| Hiperhidroz | 18 (% 5) | 0 | 0 |
| Yayg�n olmayan | Cilt �lseri | 3 (<% 1) | 1 (<% 1) | 0 |
|
| Palmar-plantar eritrodizestezi sendromu | 2 (<% 1) | 0 | 0 |
|
| I���a duyarl�l�k reaksiyonu | 1 (<% 1) | 0 | 0 |
|
| Pap�ler d�k�nt� | 1 (<% 1) | 0 | 0 |
|
| D�k�nt� | 1 (<% 1) | 0 | 0 |
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar� | Yayg�n | Kas-iskelet a�r�s� | 35 (% 9) | 2 (<% 1) | 0 |
|
| Miyalji | 28 (% 7) | 2 (<% 1) | 0 |
|
| Kas spazmlar� | 8 (% 2) | 0 | 0 |
| Yayg�n olmayan | Artralji | 2 (<% 1) | 0 | 0 |
B�brek ve idrar yolu hastal�klar� | Yayg�n olmayan | Protein�ri | 2 (<% 1) | 0 | 0 |
�reme ve meme hastal�klar� | Yayg�n olmayan | Vajinal hemoraji | 3 (<% 1) | 0 | 0 |
|
| Menoraji | 1 (<% 1) | 0 | 0 |
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar | �ok yayg�n | Yorgunluk | 178 (% 47) | 34 (% 9) | 1 (<% 1) |
| Yayg�n | �dem | 18 (% 5) | 1 (<% 1) | 0 |
|
| G���s a�r�s� | 12 (% 3) | 4 (% 1) | 0 |
|
| �rperme | 10 (% 3) | 0 | 0 |
| Yayg�n olmayan | Mukoza enflamasyonu | 1 (<% 1) | 0 | 0 |
|
| Asteni | 1 (<% 1) | 0 | 0 |
Ara�t�rmalar | �ok yayg�n | Kilo kayb� | 86 (% 23) | 5 (% 1) | 0 |
| Yayg�n | Anormal kulak, burun, bo�az muayenesi | 29 (% 8) | 4 (% 1) | 0 |
|
| Alanin aminotransferaz art��� | 8 (% 2) | 4 (% 1) | 0 |
|
| Anormal kan kolesterol d�zeyi | 6 (% 2) | 0 | 0 |
|
| Aspartat aminotransferaz art��� | 5 (% 1) | 2 (<% 1) | 2 (<% 1) |
|
| Gama glutamiltransferaz art��� | 4 (% 1) | 0 | 3 (<% 1) |
| Yayg�n olmayan | Kan bilirubin seviyelerinde art�� | 2 (<% 1) | 0 | 0 |
|
| Aspartat aminotransferaz | 2 (<% 1) | 0 | 2 (<% 1) |
|
| Alanin aminotransferaz | 1 (<% 1) | 0 | 1 (<% 1) |
|
| Trombosit say�s�nda d���� | 1 (<% 1) | 0 | 0 |
|
| Elektrokardiyogramda QT uzamas� | 2 (<% 1) | 1 (<% 1) | 0 |
*Yaln�zca pazarlama sonras� d�nemde bildirilmi� tedaviyle ili�kili advers reaksiyon. S�kl�k mevcut verilerden tahmin edilemez.
A�a��daki terimler birle�tirilmi�tir:
N�tropeni, trombositopeni ve palmar- plantar eritrodisestezi sendromu Do�u Asya k�kenli hastalarda daha s�kl�kla g�zlenmi�tir.
Pediatrik pop�lasyon
Pediatrik hastalardaki g�venlilik profili, Faz I �al��ma ADVL0815'teki 44 pediatrik hastadan ve Faz II �al��ma PZP034X2203'teki 57 pediatrik hastadan al�nan verilere dayal� olarak onaylanm�� endikasyonlarda yeti�kinlerde pazopanib ile bildirilene benzerdir (bkz. B�l�m 5.1). ��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlama yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr; e- posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz a��m� ve tedavisi
2000 mg'a kadar olan pazopanib dozlar� klinik �al��malarda de�erlendirilmi�tir. G�nde 2000 mg ve 1000 mg doz uygulanm�� 3 hastadan 1'inde s�ras�yla Derece 3 yorgunluk (doz s�n�rlay�c� toksisite) ve Derece 3 hipertansiyon g�zlenmi�tir.
Tedavisi
Pazopanib doz a��m� i�in spesifik antidot mevcut de�ildir ve doz a��m� vakalar�nda genel destekleyici �nlemlerle tedavi uygulanmal�d�r.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grubu: Antineoplastik ve imm�nomod�lat�r ajanlar, protein-kinaz inhibit�rleri; di�er protein kinaz inhibit�rleri
ATC kodu: L01EX03
Etki mekanizmas�
Pazopanib oral yolla uygulamaya y�nelik, s�ras�yla 10, 30, 47, 71, 84 ve 74 nanomolarl�k ICde�erleri ile Vask�ler Endotelyal B�y�me Fakt�r Resept�rleri (VEGFR)-1, -2 ve -3, platelet- kaynakl� b�y�me fakt�r� (PDGFR)-α ve –β, ve k�k h�cre fakt�r resept�r�n�n (c-KIT) potent �ok hedefli tirozin kinaz inhibit�r�d�r (TKI). Preklinik deneylerde pazopanib h�crelerde VEGFR-2, c-Kit ve PDGFR-β resept�rlerin ligand kaynakl� oto-fosforilasyonunu doza ba�l� �ekilde inhibe etmi�tir. �n vivo, pazopanib fare akci�erlerinde VEGF-kaynakl� VEGFR-2 fosforilasyonu, �e�itli hayvan modellerinde anjiyogenezi ve farelerde �oklu insan t�m�r ksenogreftlerinin b�y�mesini inhibe etmi�tir.
Farmakogenomik
Monoterapi olarak ya da ba�ka ajanlarla kombinasyon halinde uygulanan pazopanib ile y�r�t�len 31 klinik �al��man�n verileri �zerinde ger�ekle�tirilen bir farmakogenomik meta- analizde 5 x ULN'nin �zerinde (NCI CTC Derece 3) ALT de�erleri, HLA-B*57:01 alel ta��y�c�lar�n�n %19'unda ve ta��y�c� olmayanlar�n %10'unda g�r�lm��t�r. Bu veri grubunda hastalar�n 133/2235'i (%6) HLA-B*57:01 aleli ta��y�c�s�d�r (bkz. B�l�m 4.4).
Klinik �al��malar
Renal H�cre Kanseri (RCC)
Pazopanibin g�venlilik ve etkilili�i bir randomize, �ift k�r, plasebo kontroll� �ok merkezli �al��mada renal h�cre kanserinde (RCC) de�erlendirilmi�tir. Lokal olarak ilerlemi� ve/veya metastatik RCC hastalar� (N= 435) g�nde bir kez pazopanib 800 mg veya plasebo uygulanmak �zere randomize edilmi�tir. �al��man�n birincil amac�, progresyonsuz sa�kal�m (PFS) a��s�ndan iki tedavi kolunu de�erlendirmek ve kar��la�t�rmak olmu�tur ve ana ikincil sonlanma noktas� genel sa�kal�m (OS) olarak belirlenmi�tir. Di�er ama�lar genel yan�t oran�n� ve yan�t s�resini de�erlendirmek olmu�tur.
Bu �al��madaki toplam 435 hastadan 233'�ne daha �nce tedavi uygulanmam�� olup 202 hastada daha �nce bir IL-2 veya INFα-bazl� tedavi uygulanm��t�r. Performans durumu (ECOG), pazopanib ve plasebo gruplar� aras�nda benzer olmu�tur (ECOG 0: % 42'ye kar�� % 41, ECOG 1: % 58'e kar�� % 59). Hastalar�n b�y�k �o�unlu�unda ya olumlu (% 39) ya da orta (% 54) MSKCC (Memorial Sloan Kettering Kanser Merkezi) / Motzer prognostik fakt�rleri s�z konusu olmu�tur. T�m hastalarda berrak h�creli histoloji veya a��rl�kl� olarak berrak h�creli histoloji belirlenmi�tir. Hastalar�n yakla��k yar�s�nda 3 veya daha fazla organda hastal�k tutulumu tespit edilmi�tir ve �o�u hastada, �al��ma ba�lang�c�nda metastaz yeri olarak akci�er (% 74) ve/veya lenf d���mleri (% 54) s�z konusu olmu�tur.
Her iki kolda benzer oranda hasta �nceden tedavi g�rmemi�tir veya sitokin �n tedavisi alm��t�r (pazopanib kolunda % 53 ve % 47, plasebo kolunda % 54 ve % 46 ). Sitokin �n tedavisi alan alt grupta hastalar�n b�y�k �o�unlu�u (% 75) interferon bazl� tedavi g�rm��t�r.
Her iki kolda benzer oranlarda hasta �nceden nefrektomi olmu� (pazopanib ve plasebo kollar�nda s�ras�yla % 89 ve % 88) ve/veya �nceden radyoterapi g�rm��t�r (pazopanib ve plasebo kollar�nda s�ras�yla % 22 ve % 15).
Birincil sonlanma noktas� PFS'nin birincil analizi, t�m �al��ma pop�lasyonunda (tedavi g�rmemi� veya sitokin �n tedavisi alm��) ba��ms�z radyolojik de�erlendirme ile hastal�k de�erlendirmesine dayal�d�r.
Tablo 3. Ba��ms�z de�erlendirme ile RCC'de genel etkililik bulgular� (VEG105192)
Sonlanma Noktalar�/�al��ma Pop�lasyonu | Pazopanib | Plasebo | HR (%95 GA) | P de�eri (tek y�nl�) |
PFS |
|
|
|
|
Genel * ITT | N = 290 | N = 145 |
|
|
Ortalama (ay) | 9,2 | 4,2 | 0,46 (0,34; 0,62) | <0,0000001 |
Yan�t oran� | N = 290 | N = 145 |
|
|
% (% 95 GA) | 30 (25,1; 35,6) | 3 (0,5, 6,4) |
| <0,001 |
|
|
| – |
|
HR = Risk oran�; ITT = Tedavi ama�l�; PFS = �lerlemesiz sa�kal�m. * - Tedavi Uygulanmam�� ve Sitokin Uygulanm�� Pop�lasyonlar, GA = G�ven Aral��� | ||||
�ekil 1. Genel pop�lasyon i�in (tedavi uygulanmam�� ve sitokin uygulanm�� pop�lasyonlar) ba��ms�z de�erlendirme ile ilerlemesiz sa�kal�m i�in Kaplan-Meier e�risi (VEG105192)
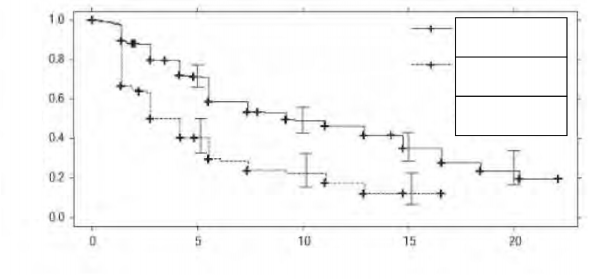
Ay
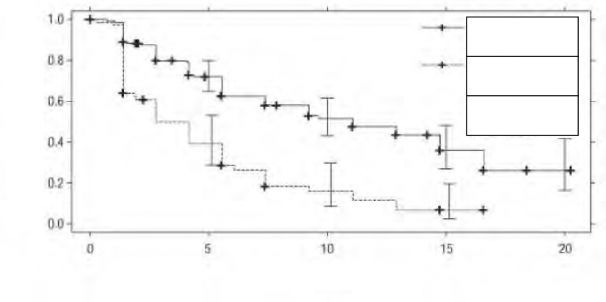
Ay
Progresyonsuz sa� kal�m oran�
Progresyonsuz sa� kal�m oran�
�ekil 2. Tedavi uygulanmam�� pop�lasyon i�in ba��ms�z de�erlendirme ile ilerlemesiz sa�kal�m i�in Kaplan-Meier e�risi (VEG105192)
�ekil 3. Sitokin uygulanm�� pop�lasyon i�in ba��ms�z de�erlendirme ile ilerlemesiz sa�kal�m i�in Kaplan-Meier e�risi
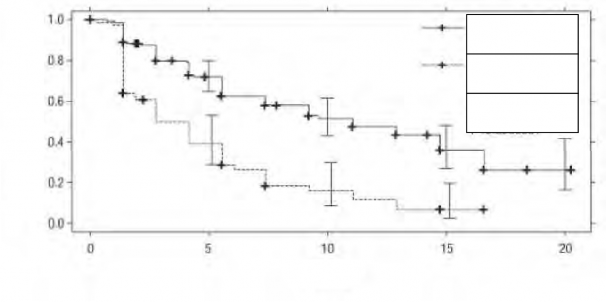
Ay
Progresyonsuz sa� kal�m oran�
Tedaviye yan�t veren hastalar i�in yan�t elde edilene kadar ge�en ortalama s�re ba��ms�z incelemeye g�re 11,9 hafta ve ortalama yan�t s�resi 58,7 haftayd� (VEG105192). Protokolde belirtilmi� nihai sa� kal�m analizindeki ortalama genel sa�kal�m (OS) verisi, pazopanib ve plasebo kollar�na randomize edilmi� hastalar i�in s�ras�yla 22,9 ay ve 20,5 ayd�r [HR = 0,91 (% 95 GA: 0,71, 1,16; p = 0,224)]. Plasebo kolundaki hastalar�n % 54'�, hastal���n ilerlemesi �zerine bu �al��man�n uzatma k�sm�nda pazopanib alm�� olduklar� i�in, OS sonu�lar� potansiyel sapmaya tabidir. Plasebo hastalar�n�n % 66's�, pazopanib alan hastalar�n % 30'una k�yasla, �al��ma sonras� tedavi alm��lard�r.
EORTC QLQ-C30 ve EuroQoL EQ-5D kullan�larak �l��len Global Ya�am Kalitesinde tedavi gruplar� aras�nda istatistiksel farkl�l�klar g�zlenmemi�tir.
Lokal n�ksl� ya da metastatik berrak h�creli renal h�cre karsinomu olan 225 hastan�n yer ald��� bir Faz 2 �al��mada, ba��ms�z de�erlendirmeye g�re objektif yan�t oran� %35 ve medyan yan�t s�resi 68 hafta olmu�tur. Medyan PFS 11,9 ay bulunmu�tur.
Sunitinibe kar�� pazopanibin g�venlili�i, etkilili�i ve kalitesi randomize, a��k etiketli, paralel gruplu Faz III bir “e�de�erlik” �al��mas�nda (VEG108844) de�erlendirilmi�tir.
VEG108844'te, daha �nce sistemik tedavi g�rmemi� lokal ilerleme g�steren ve/veya metastatik RCC'li hastalar (N = 1110), 4 haftal�k tedaviyi takiben 2 haftal�k tedavisiz d�nem �eklinde 6 haftal�k sikluslar ile g�nde bir kez 50 mg sunitinib veya kesintisiz g�nde 1 kez 800 mg pazopanib kullan�m�na randomize edilmi�tir.
Bu �al��man�n birincil hedefi pazopanib ile tedavi edilen hastalarda PFS'nin de�erlendirilmesi ve sunitinib ile tedavi edilenlerle kar��la�t�r�lmas�d�r. Demografik �zellikler tedavi kollar� aras�nda benzerdir. �lk tan�da ve taramadaki hastal�k �zellikleri tedavi kollar� aras�nda dengeli olup, hastalar�n b�y�k k�sm�nda berrak h�creli histoloji ve Evre IV hastal�k mevcuttur.
VEG108844 birincil sonlan�m noktas� PFS'yi elde etmi� ve tehlike oran� i�in %95 GA'n�n �st s�n�r� protokolde belirtilen e�de�erlik s�n�r� 1,25 de�erinden d���k oldu�u i�in pazopanibin sunitinibe e�de�er oldu�unu kan�tlam��t�r. Genel etkililik bulgular� Tablo 2'de �zetlenmektedir.
Tablo 4. Genel etkililik bulgular� (VEG108844)
Sonlan�m noktas� | Pazopanib N=557 | Sunitinib N=553 | HR (% 95 GA) |
PFS |
|
|
|
Genel |
|
|
|
Medyan (ay) | 8,4 | 9,5 | 1,047 |
(% 95 GA) | (8,3, 10,9) | (8,3, 11) | (0,898, 1,22) |
Genel Sa�kal�m | |||
Medyan (ay) | 28,3 | 29,1 | 0,915 |
(% 95 GA) | (26, 35,5) | (25,4, 33,1) | (0,786, 1,065) |
HR = Tehlike Oran�; PFS = Ba��ms�z inceleme komitesi (IRC) de�erlendirmesine dayal� olarak Progresyonsuz Sa�kal�m, GA = G�ven Aral��� | |||
�ekil 4. Genel pop�lasyon i�in ba��ms�z de�erlendirme ile progresyonsuz sa� kal�m i�in Kaplan-Meier e�risi (VEG108844)
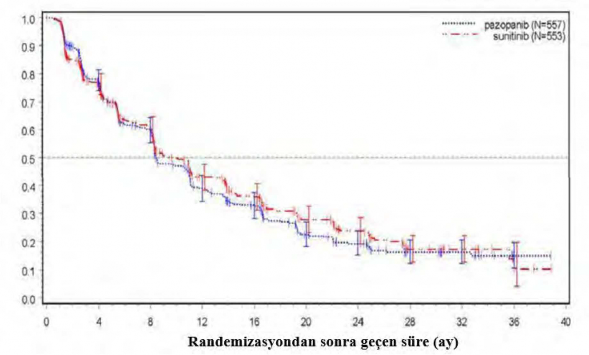
20 demografik ve prognostik fakt�r i�in PFS'nin alt grup analizleri ger�ekle�tirilmi�tir. T�m alt gruplar�n %95 g�ven aral�klar� 1 risk oran�n� i�ermektedir. Bu 20 alt grubun en k���k ���nde risk oran� i�in nokta tahmini 1,25'i a�m��t�r; yani �nceden nefrektomi olmam�� (n=186,
HR=1,403, %95 GA (0,955, 2,061)), ba�lang�� LDH de�eri > 1,5 x ULN (n=68, HR=1,72, %95
GA (0,943, 3,139)) ve MSKCC: zay�f risk (n=119, HR=1,472, 95% GA (0,937, 2,313))
de�erleri olan hastalar.
Yumu�ak Doku Sarkomu (Soft Tissue Sarcoma – STS)
Pazopanibin STS'deki etkilili�i ve g�venlili�i randomize, �ift k�r, plasebo kontroll�, �ok merkezli bir pivot faz III �al��mada de�erlendirilmi�tir (VEG110727). �lerlemi� STS'si olan toplam 369 hasta g�nde bir kez pazopanib 800 mg veya plasebo almak �zere randomize edilmi�tir. �nemli bir nokta olarak, bu �al��maya sadece STS'nin selektif histolojik alt tiplerine sahip hastalar�n kat�lmas�na izin verilmi�tir; bu nedenle, pazopanibin etkilili�i ve g�venlili�inin sadece bu alt STS gruplar� i�in tespit edildi�i kabul edilebilir ve pazopanib ile tedavinin bu STS alt tipleri ile s�n�rland�r�lmas� gerekir.
A�a��daki t�m�r tipleri uygun g�r�lm��t�r:
Fibroblastik (eri�kin fibrosarkomu, miksofibrosarkomu, sklerozan epitelioid fibrosarkom, malign soliter fibroz t�m�rler), fibrohistiyositik (pleomorfik malign fibr�z histiositom [MFH], dev h�creli MFH (indiferansiye pleomorfik sarkom (UPS) olarak da bilinir), enflamatuvar MFH), leiomyosarkom, malign glomus t�m�rleri, iskelet kaslar� (pleomorfik ve alveolar rabdomiosarkom), vask�ler (epitelioid hemanjioendotelyoma, anjiyosarkom), kesin olmayan diferansiyasyon (sinoviyal, epitelioid, alveolar yumu�ak k�s�m, berrak h�cre, desmoplastik k���k yuvarlak h�cre, ekstra-renal rabdoid, malign mezenkimom, PEComa, intimal sarkom), malign periferik sinir k�l�f� t�m�rleri, ba�ka bir tan�ma uymayan (NOS) farkl�la�mam�� (indiferansiye) yumu�ak doku sarkomlar� ve di�er sarkom tipleri (uygun olmayan listesine dahil edilmeyen).
A�a��daki t�m�r tiplerinin uygun olmad��� de�erlendirilmi�tir:
Adipositik sarkom (t�m alt tipleri), alveolar veya pleomorfik olmayan t�m rabdomiosarkomlar, kondrosarkom, osteosarkom, Ewing t�m�rleri/Primitif n�roektodermal t�m�rler (PNET), GIST, dermofibromatoz sarkom prot�berans, enflamatuvar miyofibroblastik sarkom, malign mezoteliom ve karma mezodermal rahim t�m�rleri.
Not: Adipositik sarkomu olan hastalar, bir preliminer faz II �al��mada (VEG20002) oldu�u gibi pivot faz III �al��man�n da d���nda tutulmu�tur; adipositikte pazopanib ile g�zlenen aktivite (hafta 12'de PFS), ek klinik testlere izin verilmesi i�in gerekli �n �art olan oran� kar��lamam��t�r.
VEG110727 �al��mas�n�n di�er �nemli uygunluk kriterleri �unlard�r: Metastatik hastal��a y�nelik tedavinin ilk 6 ay� i�erisinde y�ksek ya da orta dereceli malign STS y�n�nde histolojik kan�t veya hastal�k progresyonu veya (neo)-/adjuvan tedavinin ilk 12 ay� i�erisinde tekrarlama.
G�n�ll�lerin % 98'si �nceden doksorubisin, % 70'i �nceden ifosfamid alm��t�r ve % 65'i �al��maya al�nmadan �nce en az 3 veya daha fazla kemoterapi ajan� kullanm��t�r.
Hastalar, ba�lang��taki WHO performans durumu (WHO PS) (0 veya 1) fakt�rlerine ve ilerlemi� hastal��a y�nelik �nceki sistemik tedavi basama�� say�s�na (0 veya 1 kar��s�nda 2+) g�re s�n�fland�r�lm��t�r. Her tedavi grubunda ilerlemi� hastal�k i�in �nceden 2+ basamak sistemik tedavi g�rm�� olan hastalar�n y�zdesi, �nceden 0 veya 1 basamak sistemik tedavi g�rm�� olan hastalar ile kar��la�t�r�ld���nda (plasebo ve pazopanib tedavi kollar� i�in s�ras�yla
% 42 ve % 45) hafif daha y�ksek bulunmu�tur (plasebo ve pazopanib tedavi kollar� i�in s�ras�yla
% 58 ve % 55). Hastalar�n medyan takip s�resi (randomizasyon tarihinden son ileti�im veya �l��me kadar ge�en s�re �eklinde tan�ml�) iki tedavi kolu aras�nda benzer olmu�tur (plasebo i�in 9,36 ay [aral�k: 0,69 ila 23 ay] ve pazopanib i�in 10,04 ay [aral�k: 0,2 ila 24,3 ay].
�al��man�n birincil amac� progresyonsuz sa�kal�m de�erlendirmesidir (ba��ms�z radyolojik inceleme ile de�erlendirilen PFS); ikincil sonlanma noktalar� genel sa�kal�m� (OS), genel yan�t oran�n� ve yan�t s�resini i�ermi�tir.
Tablo 5. Ba��ms�z de�erlendirme ile STS'de genel etkinlik bulgular� (VEG110727)
Sonlanma noktalar�/ �al��ma pop�lasyonu | Pazopanib | Plasebo | HR (% 95 GA) | P de�eri (�ift tarafl�) | ||
PFS |
|
|
|
| ||
Genel ITT | N = 246 | N = 123 |
|
| ||
Medyan (ay) | 20 | 7 | 0,35 (0,26, 0,48) | <0,001 | ||
Leiomyosarkom | N = 109 | N = 49 |
|
| ||
Medyan (ay) | 20,1 | 8,1 | 0,37 (0,23, 0,6) | <0,001 | ||
Sinoviyal | sarkom | alt | N = 25 | N = 13 |
|
|
gruplar� |
| 4,1 | 0,43 (0,19, 0,98) | 0,005 | ||
Medyan (ay) | 17,9 |
|
|
| ||
‘Di�er STS' alt gruplar� | N = 112 | N = 61 |
|
| ||
Medyan (ay) | 20,1 | 4,3 | 0,39 (0,25, 0,6) | <0,001 | ||
OS |
|
|
|
| ||
Genel ITT | N = 246 | N = 123 |
|
| ||
Medyan (ay) | 12,6 | 10,7 | 0,87 (0,67, 1,12) | 0,256 | ||
Leiomyosarkom* | N = 109 | N = 49 |
|
| ||
Medyan (ay) | 16,7 | 14,1 | 0,84 (0,56, 1,26) | 0,363 | ||
Sinoviyal | sarkom | alt | N = 25 | N = 13 |
|
|
gruplar�* |
| 21,6 | 1,62 (0,79, 3,33) | 0,115 | ||
Medyan (ay) | 8,7 |
|
|
| ||
‘Di�er STS' alt gruplar�* | N = 112 | N = 61 |
|
| ||
Medyan (ay) | 10,3 | 9,5 | 0,84 (0,59, 1,21) | 0,325 | ||
|
|
|
|
| ||
Yan�t Oran� (CR+PR) % (%95 GA) Yan�t s�resi Medyan (hafta) (%95 GA) |
4 (2,3, 7,9)
38,9 (16,7, 40) |
0 (0, 3) |
|
|
HR = Risk oran�; ITT = Tedavi ama�l�; PFS = Progresyonsuz sa� kal�m; CR = Tam yan�t; PR = K�smi yan�t, GA = G�ven Aral���; OS = Genel sa�kal�m *�lgili STS histolojik alt gruplar� (leiomysosarkom, sinoviyal sarkom ve “Di�er” STS) i�in genel sa�kal�m, d���k olgu say�s� ve geni� g�ven aral�klar� nedeniyle dikkatle yorumlanmal�d�r. | ||||
Plasebo kolu ile kar��la�t�r�ld���nda pazopanib kolunda, ara�t�rmac� de�erlendirmesine dayal� olarak PFS'de benzer bir iyile�me g�zlenmi�tir (genel ITT pop�lasyonunda HR: 0,39; % 95 GA, 0,30 ila 0,52, p <0,001).
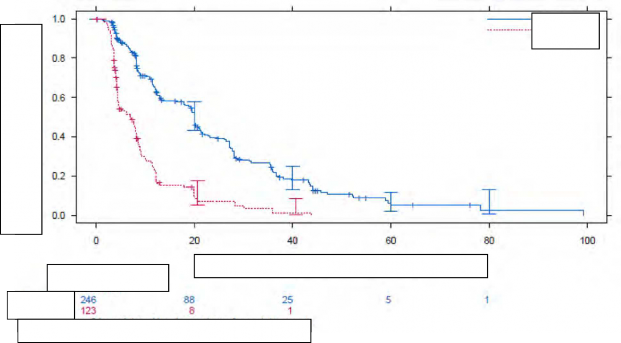
Tahmini Sa�kal�m Fonksiyonu
�ekil 5. Genel pop�lasyon i�in ba��ms�z de�erlendirme ile STS'de progresyonsuz sa� kal�m i�in Kaplan-Meier e�risi (VEG110727)
Olaylar�n %76's� (280-369) meydana geldikten sonra y�r�t�len nihai OS analizinde iki tedavi kolu aras�nda OS a��s�ndan anlaml� bir fark g�zlenmemi�tir (HR 0,87, %95 GA 0,67, 1,12 p=0,256).
Pediatrik pop�lasyon
Pazopanib ile ilgili bir Faz I �al��ma (ADVL0815), �e�itli tekrarlayan veya diren�li kat� t�m�rleri olan 44 pediatrik hastada y�r�t�lm��t�r. Birincil ama�, �ocuklarda pazopanibin
maksimum tolere edilen dozu (MTD), g�venlilik profilini ve farmakokinetik �zelliklerini ara�t�rmak olmu�tur. Bu �al��mada medyan maruz kalma s�resi 3 ayd�r (1-23 ay).
Rabdomyosarkom (N=12), rabdomyosarkom d��� yumu�ak doku sarkomu (N=11), Ewing sarkomu/pPNET (N=10), osteosarkom (N=10), n�roblastom (N=8) ve hepatoblastom (N=6) dahil olmak �zere refrakter solid t�m�r� olan 57 pediatrik hastada pazopanib ile ilgili bir Faz
II �al��ma (PZP034X2203) y�r�t�lm��t�r. �al��ma, pazopanibin 1 ila <18 ya� aras� �ocuklarda ve ad�lesanlarda terap�tik aktivitesini belirlemek i�in yap�lan tek ajanl�, kontrols�z, a��k etiketli bir �al��mad�r. Pazopanib tablet olarak g�nl�k 450 mg/m 2 /doz dozunda veya oral s�spansiyon olarak 225 mg/m 2 /doz olarak uygulanm��t�r. �zin verilen maksimum g�nl�k doz, tablet i�in 800 mg ve oral s�spansiyon i�in 400 mg'd�r. Medyan maruz kalma s�resi 1,8 ayd�r (1 g�n-29 ay).
Bu �al��man�n sonu�lar�, ilgili pediatrik pop�lasyonda herhangi bir anlaml� anti-t�m�r aktivitesi g�stermemi�tir. Bu nedenle pazopanib, pediatrik pop�lasyonda bu t�m�rlerin tedavisi i�in �nerilmemektedir (pediatrik kullan�m hakk�nda bilgi i�in bkz. B�l�m 4.2).
Avrupa �la� Ajans�, b�brek ve renal pelvis karsinomunun (nefroblastom, nefroblastomatozis, berrak h�creli sarkom, mezoblastik nefrom, renal med�ller karsinom ve b�bre�in rabdoid rabdoid t�m�r hari�)
tedavisinde pediatrik pop�lasyonun t�m alt gruplar�nda pazopanib ile yap�lan �al��malar�n sonu�lar�n� sunma zorunlulu�undan vazge�mi�tir (pediatrik kullan�m hakk�nda bilgi i�in bkz. B�l�m 4.2
5.2. Farmakokinetik �zellikler
Genel �zelliklerEmilim:
800 mg tek doz pazopanibin solid t�m�rl� hastalara oral yoldan uygulanmas�n� takiben, ortalama 3,5 saat sonra (1 ila 11,9 saat aral���nda) yakla��k 19 ± 13 mikrogram/mL'lik maksimum plazma konsantrasyonu (C) ve yakla��k 650 ± 500 mikrogram.saat/ml'lik EAA
EAA veya Cde�erlerinde 800 mg'�n �st�ndeki pazopanib dozlar�nda tutarl� art�� mevcut de�ildir.
Pazopanib i�in sistemik maruziyet g�dalarla birlikte uyguland���nda artmaktad�r. Y�ksek oranda veya d���k oranda ya� i�eren ���nlerle birlikte pazopanib uygulan�m� EAA ve Cde�erlerinde yakla��k 2 kat art��a neden olmu�tur. Bu nedenle pazopanib ���nlerden en az 1 saat �nce veya 2 saat sonra uygulanmal�d�r (bkz.B�l�m 4.2).
B�t�n olarak uygulanan tablet ile k�yasland���nda, par�alanm�� bir tek pazopanib 400 mg tabletin uygulanmas�, EAA'y� %46 ve C'� yakla��k 2 kat art�rm�� ve t'� yakla��k 2 saat azaltm��t�r. Bu sonu�lar, tabletlerin b�t�n uygulanmas�na k�yasla par�alanarak
uygulanmas�n�n ard�ndan biyoyararlan�m�n ve pazopanibin oral absorpsiyon h�z�n�n artt���n� g�stermektedir (bkz. B�l�m 4.2).
Da��l�m:
Pazopanibin insan plazma proteinine in vivo ba�lanmas� % 99'dan y�ksek olup 10-100 mikrogram/mL �zerindeki aral�kta konsantrasyona ba�l� de�ildir. �n vitro �al��malar pazopanibin P-gp ve BCRP i�in bir substrat oldu�unu d���nd�rmektedir.
Biyotransformasyon:
�n vitro �al��malar pazopanib metabolizmas�na esas olarak CYP3A4'�n arac�l�k etti�ini ve CYP1A2 ve CYP2C8 enzimlerinin min�r katk�da bulundu�unu g�stermi�tir. D�rt temel pazopanib metaboliti plazmadaki maruziyetin sadece %6's�n� olu�turmaktad�r. Bu metabolitlerden biri, VEGF ile uyar�lan insan umblikal ven endotel h�crelerinin �o�almas�n� pazopanibinkine benzer bir potens ile inhibe ederken di�erleri 10 ila 20 kat daha az aktiftirler. Bu nedenle, pazopanibin aktivitesi temel olarak ana pazopanib maruziyetine dayanmaktad�r.
Eliminasyon:
Pazopanib �nerilen 800 mg dozunun uygulanmas�ndan sonra ortalama 30,9 saatlik yar�lanma �mr� ile yava� elimine edilmektedir. Eliminasyon esas olarak fe�es arac�l���yla ger�ekle�mekte olup, renal eliminasyon yolu uygulanan dozun < % 4'�n� olu�turmaktad�r.
Hastalardaki karakteristik �zellikler
B�brek yetmezli�i:
Sonu�lar, oral uygulanm�� pazopanib dozunun %4'den az�n�n pazopanib ve metabolitleri �eklinde idrar ile at�ld���n� g�stermektedir. Pop�lasyon farmakokinetik modellemesinden elde edilen sonu�lar do�rultusunda (ba�lang�� CLCR de�erleri 30,8 mL/dak ila 150 mL/dak aral���nda de�i�en deneklerden elde edilen veriler) b�brek yetmezli�inin pazopanib farmakokineti�i �zerinde klinik olarak anlaml� bir etkisinin olmas� beklenmemektedir. Kreatinin klirensi 30 mL/dakika'n�n �zerinde olan hastalarda dozaj ayarlamas� gerekli de�ildir. Kreatinin klirensi 30 ml/dakika'n�n alt�nda olan hastalarda, bu hasta pop�lasyonunda pazopanib ile deneyim bulunmad��� i�in dikkatli olunmas� tavsiye edilir (bkz. B�l�m 4.2).
Karaci�er yetmezli�i:
Hafif:
G�nde bir kez 800 mg uyguland�ktan sonra karaci�er parametrelerinde hafif anormallikler (normal bilirubin ve herhangi bir derece ALT y�kselmesi �eklinde veya ALT de�eri fark etmeksizin bilirubin d�zeyinde 1,5 x ULN'ye kadar y�kselme �eklinde tan�ml�) olan hastalarda pazopanibin medyan kararl� durum Cve EAAde�erleri, karaci�er fonksiyonu normal olan hastalardaki medyan de�ere benzerdir (bkz. Tablo 4). G�nde bir kez 800 mg pazopanib, serum karaci�er testlerinde hafif anormallikler olan hastalarda �nerilen dozdur (bkz. B�l�m 4.2).
Orta dereceli:
Orta dereceli karaci�er bozuklu�u (ALT de�eri fark etmeksizin bilirubin d�zeyinde >1,5 x ila 3 x ULN y�kselme �eklinde tan�ml�) olan hastalarda maksimum tolere edilen pazopanib dozu (MTD) g�nde bir kez 200 mg olmu�tur. G�nde bir kez 200 mg uyguland�ktan sonra orta dereceli karaci�er bozuklu�u olan hastalarda pazopanibin medyan kararl� durum Cve EAAde�erleri, karaci�er fonksiyonu normal olan hastalarda g�nde bir kez 800 mg uygulanmas�ndan sonraki kar��l�k gelen medyan de�erlerin s�ras�yla yakla��k %44 ve %39'udur (bkz. Tablo 4). G�venlilik ve tolerabilite verilerine dayal� olarak, orta dereceli karaci�er bozuklu�u olan hastalarda pazopanib dozaj� g�nde bir kez 200 mg'a d���r�lmelidir (bkz. B�l�m 4.2).
�iddetli:
G�nde bir kez 200 mg uyguland�ktan sonra �iddetli karaci�er bozuklu�u olan hastalarda pazopanibin medyan kararl� durum Cve EAAde�erleri, karaci�er fonksiyonu normal olan hastalarda g�nde bir kez 800 mg uygulanmas�ndan sonraki kar��l�k gelen medyan de�erlerin s�ras�yla yakla��k %18 ve %15'idir. Azalan maruziyete ve s�n�rl� hepatik rezerve dayal� olarak pazopanib, �iddetli karaci�er bozuklu�u (ALT de�eri fark etmeksizin toplam bilirubin d�zeyinin > 3 x ULN olmas�) olan hastalarda �nerilmemektedir (bkz. B�l�m 4.2).
Tablo 6. Karaci�er bozuklu�u olan hastalarda �l��len medyan kararl� durum pazopanib farmakokineti�i
Grup | �ncelenen doz | C(mikrogram/ml) | EAA (mikrogram × saat/ml) | �nerilen doz |
Normal hepatik fonksiyon | 800 mg OD | 52 (17,1-85,7) | 888,2 (345,5-1482) | 800 mg OD |
Hafif karaci�er bozuklu�u | 800 mg OD | 33,5 (11,3-104,2) | 774,2 (214,7-2034,4) | 800 mg OD |
Orta dereceli karaci�er bozuklu�u | 200 mg OD | 22,2 (4,2-32,9) | 256,8 (65,7-487,7) | 200 mg OD |
�iddetli karaci�er bozuklu�u | 200 mg OD | 9,4 (2,4-24,3) | 130,6 (46,9-473,2) | Kullan�m� �nerilmez |
OD-G�nde bir kez | ||||
Pediatrik pop�lasyon
Pediatrik hastalarda pazopanib 225 mg/m (oral s�spansiyon olarak) uyguland���nda, farmakokinetik parametreler (C, Tve EAA), 800 mg pazopanib ile tedavi edilen eri�kin hastalarda daha �nce bildirilenlere benzer bulunmu�tur. Sonu�lar, �ocuklar ve eri�kinler aras�nda v�cut y�zey alan� ile normalize edilen pazopanib klirensinde belirgin bir fark olmad���n� g�stermi�tir.
5.3. Klinik �ncesi g�venlilik verileri
Pazopanibin klinik d��� g�venlilik profili fare, s��an, tav�an ve maymunlarda de�erlendirilmi�tir. Kemirgenlerde yap�lan tekrarl� doz �al��malar�nda �e�itli dokulardaki
(kemik, di�ler, t�rnak yataklar�, �reme organlar�, hematolojik dokular, b�brek ve pankreas) etkilerin VEGFR inhibisyon farmakolojisi ve/veya VEGF sinyal ileti yola��n�n bozulmas� ile ili�kili oldu�u d���n�lmekte olup bu etkilerin b�y�k bir b�l�m� klinikte g�zlenen de�erin alt�ndaki plazma maruziyet d�zeylerinde meydana gelmi�tir. Di�er g�zlenmi� etkiler, kilo kayb�, y�ksek lokal mukozal ila� maruziyetinin (maymunlarda) veya farmakolojik etkilerin (kemirgenlerde) neden oldu�u lokal gastrointestinal etkilere ba�l� ikincil sonu�lar olan diyare ve/veya morbiditeyi i�ermektedir. �nsan maruziyetinin EAA's�n�n 2,5 kat� maruziyetlerde di�i farelerde proliferatif hepatik lezyonlar (eozinofilik odaklar ve adenom) g�r�lm��t�r.
J�venil hayvanlarda yap�lan toksisite �al��malar�nda, s�tten kesilme �ncesi s��anlara do�umdan sonra 9. g�nden ba�layarak 14. g�ne kadar doz uyguland���nda pazopanib, eri�kin insanlarda EAA de�erine dayanarak klinik maruziyetin yakla��k 0,1 kat� dozda mortaliteye ve b�brek, akci�er, karaci�er ve kalpte anormal organ b�y�mesi/mat�rasyonuna neden olmu�tur. S�tten kesilme d�nemi sonras�ndaki s��anlara do�umdan sonraki 21. g�nden ba�lanarak do�umdan sonraki 62. g�ne kadar dozlama yap�ld���nda toksikolojik bulgular, kar��la�t�r�labilir maruziyetlerde yeti�kin s��anlardakiler ile benzer olmu�tur. Pediatrik hastalar, eri�kin hastalara k�yasla kemik ve di� etkileri a��s�ndan daha y�ksek risk alt�ndad�r zira b�y�me bask�lanmas� (daha k�sa uzuvlar), k�r�lgan kemikler ve di�lerin yeniden modellenmesi dahil bu de�i�iklikler
≥ 10 mg/kg/g�n dozlar�nda (eri�kin insanlarda EAA baz�nda klinik maruziyetin yakla��k 0,1- 0,2 kat�na e�it) j�venil s��anlarda mevcut g�r�lm��t�r (bkz. B�l�m 4.4).
�reme, fertilite ve teratojenik etkiler
Pazopanibin s��anlara ve tav�anlara, insan maruziyetinden > 300 kat daha d���k maruziyetlerde (EAA'ya g�re) uyguland���nda embriyotoksik ve teratojenik oldu�u g�sterilmi�tir. Bu etkiler di�ilerde azalan fertilite, artan preimplantasyon ve postimplantasyon kayb�, erken rezorpsiyon, embriyoletalite, �l�mc�l d�zeyde azalan v�cut a��rl��� ve kardiyovask�ler malformasyonu i�ermi�tir. Ayr�ca, kemirgenlerde azalan korpora lutea, kistlerde art�� ve over atrofisi g�zlenmi�tir. Bir erkek s��an fertilite �al��mas�nda �iftle�me ya da fertilite �zerinde etki olmam�� fakat insan maruziyetinin EAA baz�nda 0,3 kat� maruziyetlerde sperm �retim h�z�, sperm motilitesi ve epididimal ve testik�ler sperm konsantrasyonlar�nda d����ler ile birlikte testik�ler ve epididimal a��rl�klarda azalmalar g�zlenmi�tir.
Genotoksisite
Pazopanib genotoksisite testlerinde (Ames testi, insan periferik lenfosit kromozom aberasyon testi ve s��anlarda in vivo mikron�kleus testi) genetik hasara neden olmam��t�r. Bitmi� �r�nde de d���k miktarlarda bulunan, pazopanib �retiminde bir ara �r�n, Ames testinde mutajenik bulunmam��t�r fakat fare lenfoma ve in vivo fare mikron�kleus testinde genotoksik oldu�u g�r�lm��t�r.
Karsinojenisite
Pazopanib ile y�r�t�len iki y�ll�k karsinojenisite �al��malar�nda farelerde karaci�er adenomlar� ve s��anlarda duodenal adenokarsinomlar�n say�s�nda art�� oldu�u belirlenmi�tir. Kemirgenlere �zg� patojeneze ve bu bulgular�n mekanizmas�na dayanarak, bunlar�n pazopanib alan hastalarda daha y�ksek bir karsinojenik risk olu�turdu�u d���n�lmemektedir.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Tablet �ekirde�i:
Mikrokristalin sel�loz, Tip 102 Sodyum ni�asta glikolat, Tip A Povidon, K30
Magnezyum stearat
Tablet kaplamas�:
![]()
Opadry White YS-1-7706-G Titanyum dioksit Hipromelloz 2910 (6 cps)
Hipromelloz 2910 (3 cps) Makrogol
Polisorbat 80
6.2. Ge�imsizlikler
Ge�erli de�ildir.
6.3. Raf �mr�
:24 ay
6.4. Saklamaya y�nelik �zel tedbirler
30°C alt�ndaki oda s�cakl���nda saklanmal�d�r.
6.5. Ambalaj�n niteli�i ve i�eri�i
�r�n�m�z i�in primer ambalaj malzemesi olarak PVC/Aklar ve Aluminyum folyo blister ambalaj malzemeleri kullan�lm��t�r. Blisterler karton kutular i�erisine paketlenir. Bir kutu i�erisinde 60 adet tablet i�eren blister ambalajlarda kullanma talimat� ile birlikte sunulmaktad�r.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
T�m kullan�lmayan �r�n ve at�k maddeler “T�bbi At�klar�n Kontrol� Y�netmeli�i” ve “Ambalaj ve Ambalaj At�klar�n�n Kontrol� Y�netmeli�i” ne uygun olarak imha edilmelidir.
 Depresyonu Anlamak
Depresyon farkl� ki�ileri farkl� bi�imlerde etkiler. Duygusal veya fiziksel
olmak �zere geni� alanda belirtilere sebep olabilir.Depresyona neler sebep olur?
Depresyonu Anlamak
Depresyon farkl� ki�ileri farkl� bi�imlerde etkiler. Duygusal veya fiziksel
olmak �zere geni� alanda belirtilere sebep olabilir.Depresyona neler sebep olur? |
 �izofrenlik
�izofrenli�in psikiatrik te�hisi hakk�nda �ok fazla anla�mazl�k vard�r. Bu
sayfadaki bilgiler, �izofrenli�in te�hisi, nedenleri ve tedavisi hakk�ndaki fakl� teoriler
hakk�nda bilgi verecektir.
�izofrenlik
�izofrenli�in psikiatrik te�hisi hakk�nda �ok fazla anla�mazl�k vard�r. Bu
sayfadaki bilgiler, �izofrenli�in te�hisi, nedenleri ve tedavisi hakk�ndaki fakl� teoriler
hakk�nda bilgi verecektir. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| VOPAZZI | 8699525099716 | 9,702.70TL |
| VOTRIENT | 8699522091041 | |
| Di�er E�de�er �la�lar |
 |
Kalp Krizi Kalbe giden kan ak��� durdu�unda kalp krizi meydana gelir. |
 |
Pankreas Kanseri Pankreas karn�n alt k�sm�nda yatay �ekilde bulunan bir organd�r. Sindirime yard�mc� olan enzimleri ve kan �ekerini y�netmeye yard�mc� olan hormonlar� v�cuda da��tmakla g�revlidir. |
 |
Asperger Sendromu Asperger sendromu, otistik gurubun bir b�l�m� olan bir �z�rd�r. Bu genelde, gurubun daha ”y�ksek” taraf�nda yer ald��� d���n�len ki�ilere uygun bir tan�d�r. |
�LA� GENEL B�LG�LER�
Deva Holding A.�.
| Sat�� Fiyat� | 38432.05 TL [ 1 Dec 2025 ] |
| �nceki Sat�� Fiyat� | 38432.05 TL [ 24 Nov 2025 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | Normal Re�eteli bir ila�d�r. |
| Barkodu | 8699525099723 |
| Etkin Madde | Pazopanib |
| Yerli ve Be�eri bir ila�d�r. |