VYNDAQEL 61 mg yumuşak kapsül (30 kapsül) Farmakolojik Özellikler
{ Tafamidis }
5. FARMAKOLOJİK ÖZELLİKLER
5.1. Farmakodinamik özellikler
Farmakoterapötik grup: Diğer sinir sistemi ilaçları, ATC kodu: N07XX08Etki mekanizması
Tafamidis, TTR'nin seçici bir stabilizörüdür. Tafamidis, tiroksin bağlanma bölgelerinden TTR'ye bağlanarak tetrameri stabilize etmekte ve amiloidojenik süreçte hız sınırlayıcı adım olan monomerlere ayrışmayı yavaşlatmaktadır.
Farmakodinamik etkiler
Transtiretin amiloidozu, dokularda normal işlevi bozacak miktarlarda çeşitli çözünmeyen fibriler proteinlerin veya amiloidlerin birikmesinden kaynaklanan ciddi derecede zayıflatıcı bir durumdur. Transtiretin tetramerinin monomerlere ayrışması, transtiretin amiloidozunun patogenezindeki hız sınırlayıcı adımdır. Katlanmış monomerler, kısmi denatürasyona uğrayarak farklı şekilde katlanmış monomer amiloidojenik ara ürünler oluşturmaktadır. Bu ara ürünler daha sonra hatalı bir şekilde birleşerek çözünür oligomerler, profilamentler, filamentler ve amiloid fibrilleri haline gelmektedir. Tafamidis, tetramerik formda olan transtiretinin üzerindeki iki tiroksin bağlanma bölgesine bağlanarak monomerlere ayrışmayı önlemektedir. TTR tetramer ayrışmasının inhibisyonu, ATTR- KM hastalarında tafamidis kullanımının gerekçesini oluşturmaktadır.
Farmakodinamik bir belirteç olarak bir TTR stabilizasyon miktar tayini kullanılmıştır ve TTR
tetramerinin stabilitesi değerlendirilmiştir.
Tafamidis hem vahşi tip TTR tetrameri hem de klinik olarak test edilen 14 TTR varyantını günlük bir doz tafamidis verilmesinin ardından dengelemiştir. Tafamidis ayrıca ex vivo test edilen 25 değişkenin TTR tetramerini dengeleyerek 40 amiloidojenik TTR genotipi için TTR dengeleme özelliği göstermiştir.
Çok merkezli, uluslararası, çift kör, plasebo kontrollü, randomize bir çalışmada (bkz. Klinik etkililik ve güvenlilik bölümü), 1. ayda TTR dengelemesi gözlenmiş ve 30. ay boyunca korunmuştur. Kalp yetmezliği (NT-proBNP ve Troponin I) ile ilişkili biyobelirteçler, plasebo yerine VYNDAQEL lehinde olmuştur.
Klinik etkililik ve güvenlilik
Primer analiz
| Toplam Tafamidis | Plasebo N=177 |
30. ayda hayatta olanların 30 ay boyunca (yıllık hasta | 0,297 | 0,455 |
Etkililik, vahşi tip veya kalıtsal ATTR-KM bulunan 441 hastada yapılan çok merkezli, uluslararası,
çift kör, plasebo kontrollü, randomize 3 kollu bir çalışmada gösterilmiştir.
Hastalar standart bakıma (örn. diüretikler) ek olarak, 30 ay boyunca randomize bir şekilde günde bir kez 20 mg (n=88) veya 80 mg [dört adet 20 mg tafamidis meglumin kapsülü şeklinde verilmiştir] (n=176) tafamidis meglumine veya bunlara karşılık gelen plasebo (n=177) gruplarına ayrılmıştır. Tedavi ataması, varyant bir TTR genotipinin varlığı ya da yokluğuna ve hastalığın başlangıç düzeyi şiddetine (NYHA Sınıfı) göre yapılmıştır. Tablo 1, hasta demografik özelliklerini ve başlangıç düzeyi özelliklerini açıklamaktadır.
Tablo 1: Hasta demografisi ve başlangıç düzeyi özellikleri
Özellik | Toplam tafamidis N=264 | Plasebo N=177 |
Yaş — yıl | ||
Ortalama (standart sapma) | 74,5 (7,2) | 74,1 (6,7) |
Medyan (minimum, maksimum) | 75 (46, 88) | 74 (51, 89) |
Cinsiyet — sayı (%) | ||
Erkek | 241 (91,3) | 157 (88,7) |
Kadın | 23 (8,7) | 20 (11,3) |
TTR genotipi — sayı (%) | ||
ATTRm | 63 (23,9) | 43 (24,3) |
ATTRwt | 201 (76,1) | 134 (75,7) |
NYHA Sınıfı — sayı (%) |
|
|
NYHA Sınıf I | 24 (9,1) | 13 (7,3) |
NYHA Sınıf II | 162 (61,4) | 101 (57,1) |
NYHA Sınıf III | 78 (29,5) | 63 (35,6) |
Kısaltmalar: ATTRm = değişken transtiretin amiloid, ATTRwt = vahşi tip transtiretin amiloid, NYHA = New York Kalp Derneği.
Primer analiz, tüm nedenlere bağlı ölüm ve kardiyovasküler nedenlere bağlı hospitalizasyon (kişinin kardiyovasküler morbiditeden dolayı hastaneye yatma sayısı olarak tanımlanır. Mesela hastaneye kabul) sıklığına Finkelstein-Schoenfeld (F-S) metodu uygulayarak hiyerarşik bir kombinasyon kullanmıştır. Bu yöntem her bir hastayı aynı sınıftaki diğer hastalar ile çiftler halinde karşılaştırmaktadır. Hastaların mortaliteye bağlı ayrıştırılamadığı zamanlarda tüm nedenlere bağlı ölüm ve bunu takip eden kardiyovasküler nedenlere bağlı hospitalizasyon sıklığını kullanarak hiyerarşik bir şekilde gerçekleştirmektedir.
Bu analiz, plaseboya göre toplam tafamidis 20 mg ve 80 mg doz grubunda tüm nedenlere bağlı ölümlerde ve kardiyovasküler nedenlere bağlı hospitalizasyon sıklığında önemli bir azalma (p = 0,0006) göstermiştir (Tablo 2).
Tablo 2: Tüm nedenlere bağlı ölüm ve kardiyovasküler nedenlere bağlı hospitalizasyon sıklığının Finkelstein-Schoenfeld (F-S) Yöntemi kullanılarak yapılan birincil analizi
başına) ortalama kardiyovasküler nedenlere bağlı hospitalizasyon sayısı |
|
|
F-S yöntemiyle elde edilen p değeri | 0,0006 | |
*Kalp nakli ve mekanik kalp yardımcı cihaz implantasyonu, son aşamaya yaklaşmanın göstergeleri olarak kabul edilir. Dolayısıyla, bu gönüllüler analizde ölüme eşdeğer olarak ele alınır. Bu nedenle bu gönüllüler 30 aylık yaşamsal durum takip değerlendirmesine göre hayatta olsalar bile, "30. aydaki Hayatta Olan Gönüllü Sayısı"na dahil edilmezler.
†30 ay hayatta kalanların betimsel ortalamasıdır.
Primer analizin (tüm nedenlere bağlı ölüm ve kardiyovasküler nedenlere bağlı hospitalizasyon) her bir komponentinin özel olarak değerlendirmesi plaseboya kıyasla tafamidis için önemli düşüşler göstermiştir.
Toplam tafamidis için tüm nedenlere bağlı ölüm oranının Cox orantılı tehlike modelinden elde edilen tehlike oranı 0,698 (%95 GA 0,508, 0,958) olmuştur; bu da plasebo grubuna (p=0,0259) göre ölüm riskinde %30,2'lik bir düşüşe işaret etmektedir. Tüm nedenlere bağlı ölüm oranının Kaplan- Meier zaman-olay grafiği Şekil 1'de verilmiştir.
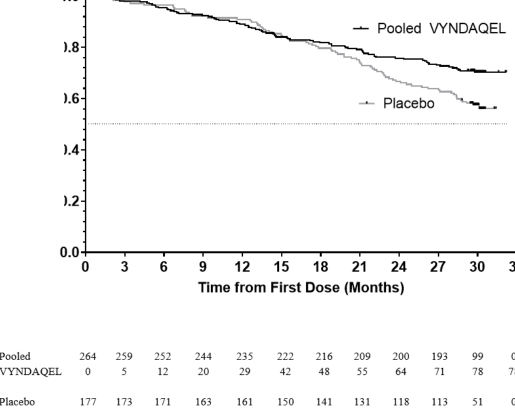
Risk altında kalan hastalar (kümülatif olaylar)
İlk Doz Zamanı (aylar)
Hayatta Kalma Olasılığı
Şekil 1: Tüm nedenlere bağlı ölüm oranı
* Kalp nakline ve mekanik kalp yardımcı cihazlarına ölüm olarak değerlendirilmiştir. Tedavi, TTR genotipi (değişken ve vahşi tip) ve New York Kalp Derneği (NYHA) Başlangıç düzeyi sınıflandırması (birleştirilmiş NYHA Sınıf I ve II ve NYHA Sınıf III) faktörleriyle yapılan Cox orantılı tehlike modelinden elde edilen tehlike oranı.
Plasebo ile karşılaştırıldığında %32,4 oranında risk azalmasıyla tafamidis kardiyovasküler nedenlere bağlı hospitalizasyon sayıları çok daha düşük olmuştur (Tablo 3).
Tablo 3: Kardiyovasküler nedenlere bağlı hospitalizasyon sıklığı
| Toplam Tafamidis N=264 | Plasebo N=177 |
Kardiyovasküler nedenlere bağlı hospitalizasyon toplam hasta sayısı (%) | 138 (52,3) | 107 (60,5) |
Yıllık kardiyovasküler nedenlere bağlı hospitalizasyon sayısı* | 0,4750 | 0,7025 |
Plasebo tedavisiyle karşılaştırıldığında birleştirilmiş tafamidis farkı (bağıl risk oranı)* | 0,6761 | |
p değeri* | <0,0001 | |
Kısaltma: NYHA=New York Kalp Derneği.
Bu analiz için tedavi, TTR genotipi (değişken ve doğal fenotip), New York Kalp Derneği (NYHA) Başlangıç düzeyi sınıflandırması (birleştirilmiş NYHA Sınıf I ve II ve NYHA Sınıf III), TTR genotip etkileşimine göre tedavi ve NYHA Başlangıç düzeyi sınıflandırması etkileşim terimleri faktörleriyle yapılan bir Poisson gerileme modeli esas alınmıştır.
Tafamidisin fonksiyonel kapasite ve sağlık durumu üzerindeki tedavi etkisi 6 Dakika Yürüyüş Testi (6MWT) ve Kansas Şehri Kardiyomiyopati Anketi Genel Özet (KCCQ-OS) skoru (toplam semptom, fiziksel kısıt, yaşam kalitesi ve sosyal kısıt alanlarından oluşur) ile değerlendirilmiştir. Tafamidis lehine belirgin bir tedavi etkisi ilk olarak 6. ayda gözlenmiştir ve hem 6MWT mesafesi hem de KCCQ-OS skoru bakımından 30. aya kadar tutarlı kalmıştır (Tablo 4).
Tablo 4: 6MWT ve KCCQ-OS ve bileşen alan skorları
Sonlanım | Başlangıç | Düzeyi | Başlangıç düzeyinden 30. | Tedavinin | p değeri | |
noktaları | Ortalaması (SD) |
| aya kadar olan değişiklik, | plasebodan |
| |
|
|
| LS ortalaması (SE) | farkı |
| |
| Toplam | Plasebo | Toplam | Plasebo | LS |
|
| Tafamidis | N=177 | Tafamidis |
| ortalaması |
|
| N=264 |
|
|
| (%95 GA) |
|
6MWT | 350,55 | 353,26 | -54,87 | -130,55 | 75,68 | p<0,0001 |
(metre) | (121,30) | (125,98) | (5,07) | (9,80) | (57,56, 93,80) |
|
KCCQ- | 67,27 | 65,90 | -7,16 | -20,81 | 13,65 | p<0,0001 |
OS | (21,36) | (21,74) | (1,42) | (1,97) | (9,48, 17,83) |
|
5.2. Farmakokinetik özellikler
Genel özelliklerEmilim
Yumuşak kapsülün günde bir kez ağız yoluyla uygulanmasından sonra, en yüksek pik konsantrasyona (C) açlık durumunda dozlandıktan sonra 4 saatlik bir medyan sürede (t) ulaşılmıştır. Birlikte verilen yüksek yağlı, yüksek kalorili bir öğün, emilim oranını değiştirmiştir, fakat emilim miktarını değiştirmemiştir. Bu sonuçlar, tafamidisin yiyecekle beraber ya da ayrı verilmesini desteklemektedir.
Dağılım
Tafamidis, plazma içinde yüksek oranda proteine bağlıdır (>%99). Görünür kararlı hal dağılım hacmi 18,5 litredir.
Tafamidisin plazma proteinlerine bağlanma derecesi, hayvan ve insan plazması kullanılarak değerlendirilmiştir. Tafamidisin TTR'ye yatkınlığı, albümine kıyasla daha fazladır. Bu nedenle tafamidis plazmadaki TTR'ye (3.6 μM) göre oldukça yüksek albümin (600 μM) konsantrasyonuna rağmen tercihli olarak TTR'ye bağlanır.
Biyotransformasyon
5.3. Klinik öncesi güvenlilik verileri
e dayanarak tafamidisin glukuronidasyon ile metabolize edildiği ileri sürülmektedir.
Eliminasyon
Tafamidisin insanlarda safra yolu ile vücuttan dışarı atıldığına dair somut bir kanıt yoktur. Klinik öncesi güvenlilik verilerie dayanarak tafamidisin safra yoluyla vücuttan dışarı atıldığı ileri sürülmektedir. Uygulanan toplam dozun yaklaşık %59'u dışkıda ve yaklaşık %22'si idrarda geri kazanıldığı için bu biyolojik dönüşüm yolu insanlarda olasıdır. Popülasyon farmakokinetik sonuçlarına dayanarak, tafamidisin ağız yoluyla görünür klerensi 0,263 l/saattir ve popülasyonun ortalama yarılanma ömrü yaklaşık 49 saattir.
Doğrusallık/Doğrusal olmayan durum
Tek dozun 480 mg'a kadar ve çoklu dozların 80 mg/güne kadar arttırılmasıyla günde bir defa tafamidis meglumin doz maruziyeti de artmıştır. Genel olarak artışlar doza orantılı veya yakın orantılı olmuştur ve tafamidis klerensi zamanla sabit hale gelmiştir.
Tafamidis 61 mg bağıl biyoyararlanımı, kararlı halde 80 mg tafamidis meglumine benzerdir.
Tafamidis ve tafamidis meglumin, mg bazında birbirinin yerine geçmez.
Farmakokinetik parametreler, tek ve tekrarlanan 20 mg tafamidis meglumin dozu uygulamasından sonra benzer olmuştur ve bu da tafamidis metabolizmasının indüklenmediğini veya inhibe edilmediğini göstermektedir.
14 gün boyunca ağız yoluyla günde bir kez 15 mg ila 60 mg tafamidis meglumin solüsyon doz
uygulaması sonuçları kararlı hale 14. günde ulaşıldığını göstermiştir. Özel popülasyonlar
Karaciğer yetmezliği
Farmakokinetik veriler, sağlıklı gönüllülerle karşılaştırıldığında tafamidis serbest fraksiyonunun daha yüksek olmasından dolayı orta derecede karaciğer yetmezliği olan (7-9 Child-Pugh skoru dahil) hastalarda tüm vücudu etkileyen maruziyetin azaldığını (yaklaşık %40) ve tafamidis meglumin toplam klerensinin arttığını (0,52 l/sa ve 0,31 l/sa farkı) göstermiştir. Orta derecede karaciğer yetmezliği olan hastalar sağlıklı gönüllülere göre daha düşük TTR seviyelerine sahip olduğundan dolayı dozun ayarlanması gerekli değildir, çünkü tafamidisin hedef proteini TTR ile birlikte stokiyometrisi, TTR tetramerinin dengelenmesi için yeterli olacaktır. Şiddetli karaciğer yetmezliği olan hastalarda tafamidis maruziyeti bilinmemektedir.
Böbrek yetmezliği
Tafamidis, böbrek yetmezliği olan hastalarla ayrıca yapılan bir çalışmada özel olarak
değerlendirilmemiştir. Kreatinin klerensinin tafamidis farmakokinetiği üzerindeki etkisi, kreatinin
klerensi 18 ml/dk'dan büyük olan hastalarda yapılan bir popülasyon farmakokinetik analizinde değerlendirilmiştir. Farmakokinetik tahminler, kreatinin klerensi 80 ml/dk'dan küçük olan hastalar ile kreatinin klerensi 80 ml/dk'ya eşit veya büyük olan hastalar kıyaslandığında tafamidisin görünür oral klerensinde hiçbir farklılık göstermemiştir. Böbrek yetmezliği olan hastalar için doz ayarlaması gerekmez. Şiddetli böbrek yetmezliği olan hastalara dair sınırlı veri mevcuttur (kreatinin klerensi 30 ml/dk'ya eşit veya daha az).
Yaşlılar
Popülasyon farmakokinetiği sonuçlarına göre 65 yaş altındaki gönüllülere kıyasla 65 yaş ve üstündeki gönüllülerin kararlı haldeki tahmini görünür oral klerens ortalamasına göre %15 daha düşük olmuştur. Bununla birlikte, klerens farkı daha genç gönüllülere kıyasla ortalama Cve EAA değerlerinde %20'den düşük bir artışa neden olmaktadır ve klinik açıdan anlamlı değildir.
Farmakokinetik/farmakodinamik ilişkiler
In vitro ortamda elde edilen veriler, tafamidisin sitokrom P450 enzimleri olan CYP1A2, CYP3A4, CYP3A5, CYP2B6, CYP2C8, CYP2C9, CYP2C19 ve CYP2D6'yı önemli ölçüde inhibe etmediğini göstermiştir. CYP1A2, CYP2B6 veya CYP3A4'ün indüklenmesi nedeniyle tafamidisin klinik açıdan anlamlı ilaç etkileşimine neden olması beklenmemektedir.
In vitro ortamda yapılan çalışmalar, tafamidisin UDP glukuronosiltransferaz (UGT) substratları ile tüm vücudu etkileyen klinik açıdan anlamlı ilaç etkileşimlerine neden olmasının olası olmadığını göstermektedir. Tafamidis, UGT1A1'in bağırsak etkinliklerini inhibe edebilmektedir.
Tafamidis, tüm vücutta ve gastrointestinal (GI) kanalda Çoklu İlaç Dirençli Proteini (MDR1) (P-glikoprotein; P-gp olarak da bilinir) organik katyon taşıyıcı 2'yi (OCT2), çoklu ilaç ve toksin ekstrüzyon taşıyıcı 1'i (MATE1) ve MATE2K'yi, organik anyon taşıyan polipeptit 1B1'i (OATP1B1) ve OATP1B3'ü klinik açıdan anlamlı konsantrasyonlarda inhibe etme açısından düşük bir potansiyel göstermiştir.
5.3. Klinik öncesi güvenlilik verileri
e dayanarak tafamidisin glukuronidasyon ile metabolize edildiği ileri sürülmektedir.
Klinik dışı veriler, geleneksel güvenlilik farmakolojisi, doğurganlık ve erken embriyo gelişimi, genotoksisite ve kanserojenlik potansiyeli çalışmalarına göre insanlar için özel bir tehlike göstermemiştir. Tekrarlı doz zehirli (toksik) olma durumu ve karsinojenisite çalışmalarında karaciğer test edilen farklı türlerde zehirli (toksik) olma durumu için bir hedef organ olarak görülmüştür. Karaciğer etkileri, tafamidisin 61 mg klinik dozunda kararlı halde insan EAA değerine eşit maruziyetlerde görülmüştür.
Tavşanlarda yapılan bir gelişime yönelik zehirli (toksik) olma durumu çalışmasında tafamidisin 61 mg klinik dozunda kararlı halde insan EAA değerinin yaklaşık 2,1 katı ve üzerindeki maruziyetlerde iskelet yapısal bozuklukları ve varyasyonlarında hafif bir artış, birkaç dişide düşük yapma, embriyo-fetal sağkalımda düşüş ve fetal ağırlıklarda azalma gözlenmiştir.
Tafamidis ile sıçanlarda yapılan doğum öncesi ve sonrası gelişim çalışmasında hamilelik ve emzirme sırasında annelere 15 ve 30 mg/kg/gün dozlar verilmesinin ardından yavru sağkalımının azaldığı ve yavru ağırlıklarının düştüğü kaydedilmiştir. Erkeklerde yavru ağırlıklarının düşmesi, 15 mg/kg/gün dozda cinsel olgunlaşmadaki gecikme (preputial ayrılma) ile ilişkilendirilmiştir. 15 mg/kg/gün dozda öğrenme ve hafıza için yapılan bir su labirenti testinde performans bozukluğu gözlenmiştir. Hamilelik ve emzirme sırasında annelere tafamidis dozu verilmesinin ardından F1
nesli yavrulardaki canlılık vebüyümeNOAEL'i5mg/kg/gün(insan eşdeğeri tafamidis dozu = 0,8
 Depresyonu Anlamak
Depresyon farklı kişileri farklı biçimlerde etkiler. Duygusal veya fiziksel
olmak üzere geniş alanda belirtilere sebep olabilir.Depresyona neler sebep olur?
Depresyonu Anlamak
Depresyon farklı kişileri farklı biçimlerde etkiler. Duygusal veya fiziksel
olmak üzere geniş alanda belirtilere sebep olabilir.Depresyona neler sebep olur? |
 HIV ve Aids
HIV, Human Immunodeficiency Virus’dür (İnsanlarda Bağışıklık Sistemini Bozan
Virüsdür). Bu virüs AIDS hastalığına sebep olur.
HIV ve Aids
HIV, Human Immunodeficiency Virus’dür (İnsanlarda Bağışıklık Sistemini Bozan
Virüsdür). Bu virüs AIDS hastalığına sebep olur. |
İLAÇ GENEL BİLGİLERİ
Pfizer İlaçları Ltd.Şti.
| Satış Fiyatı | 256034.78 TL [ 17 Dec 2024 ] |
| Önceki Satış Fiyatı | 256034.78 TL [ 2 Dec 2024 ] |
| Original / Jenerik | Original İlaç |
| Reçete Durumu | Normal Reçeteli bir ilaçdır. |
| Barkodu | 8681308191007 |
| Etkin Madde | Tafamidis |
| ATC Kodu | N07XX08 |
| Birim Miktar | 61 |
| Birim Cinsi | MG |
| Ambalaj Miktarı | 30 |
| Sinir Sistemi > Diğer İlaçlar |
| İthal ( ref. ülke : Fransa ) ve Beşeri bir ilaçdır. |
İLAÇ EŞDEĞERLERİ
| Eşdeğer İlaç Adı | Barkodu | İlaç Fiyatı |
|---|---|---|
| Eşdeğer bir ilaç bulunamadı |
 |
Ağız Kanseri Ağız kanserinin en yaygın türleri, dudak, dil, dişetidir. Nadiren yanak içi veya damak bölgelerini de içine alır. |
 |
Travma Sonrası Bunalımı Travmatik bir olay, günlük olağan olayların dışında olan ve kişiyi derinden rahatsız eden bir olaydır.Birçok olay böyle bir etki gösterebilir. |
 |
Sırt Ağrısı Sırt ağrısı birden bire ortaya çıkıp şiddetli (akut) olabilir veya zamanla gelişip daha uzun süreli sorunlara (kronik) neden olabilir. |