YULAREB 100 mg film kapl� tablet (42 tablet) K�sa �r�n Bilgisi
{ Abemasiklib }
1. BE�ER� TIBB� �R�N�N ADI
YULAREB 100 mg film kapl� tablet
2. KAL�TAT�F VE KANT�TAT�F B�LE��M
Etkin madde
Her bir film kapl� tablet 100 mg abemasiklib i�erir.
Yard�mc� maddeler
Her bir film kapl� tablet 28 mg s���r kaynakl� laktoz monohidrat i�erir. Yard�mc� maddelerin tamam� i�in 6.1'e bak�n�z.
3. FARMAS�T�K FORMU
Film kapl� tablet (tablet).
Bir taraf�nda “Lilly”, di�er taraf�nda “100” bask�s� bulunan, 6.6 x 12.0 mm boyutunda beyaz, modifiye oval tablet.
4. KL�N�K �ZELL�KLER
4.1. Terap�tik endikasyonlar
Erken evre meme kanseri
YULAREB, endokrin tedavi ile kombinasyon halinde, hormon resept�r� (HR) pozitif, insan epidermal b�y�me fakt�r� resept�r� 2 (HER2) negatif, n�ks riski y�ksek erken evre meme kanseri olan yeti�kin hastalar�n adjuvan tedavisinde endikedir (bkz. B�l�m 5.1) YULAREB, iki y�l boyunca veya hastal���n n�ks�ne dek veya kabul edilemez toksisite geli�ene dek s�rekli olarak al�nmal�d�r.
Rek�rrens riski y�ksek olan hastalarda a�a��daki klinik ve patolojik �zelliklerin bulunmas� gerekmektedir:
4 veya daha �zeri aksiller LN metastaz� olan veya
4.2. Pozoloji ve uygulama �ekli
YULAREB tedavisi anti-kanser tedavilerinin kullan�m� konusunda deneyimli hekimler taraf�ndan ba�lat�lmal� ve bu hekimlerin g�zetimi alt�nda uygulanmal�d�r.
Pozoloji/uygulama s�kl��� ve s�resi:
Endokrin tedaviyle kombinasyon halinde YULAREB
Endokrin tedaviyle kombinasyon halinde uyguland���nda, �nerilen abemasiklib dozu g�nde iki kez 150 mg'd�r. Birlikte kullan�laca�� di�er �r�n�n �nerilen pozolojisi i�in ilgili �r�n�n K�sa �r�n Bilgisine bak�n�z.
Tedavi s�resi
Erken evre meme kanseri
YULAREB, iki y�l boyunca veya hastal���n n�ks�ne dek veya kabul edilemez toksisite geli�ene dek s�rekli olarak al�nmal�d�r.
�leri evre veya metastatik meme kanseri
YULAREB, hasta tedaviden klinik yarar sa�lad��� s�rece veya kabul edilemez toksisite geli�ene dek s�rekli olarak kullan�lmal�d�r.
E�er hasta kusarsa veya bir YULAREB dozunu atlarsa, bir sonraki dozu planlanan zamanda almas� gerekti�i konusunda bilgilendirilmelidir; ek doz al�nmamal�d�r.
Doz ayarlamalar�
Baz� advers reaksiyonlar�n y�netilmesi i�in Tablo 1-7'de g�sterilen �ekilde doza ara verme ve/veya doz azalt�m� gerekebilir.
Tablo 1. Advers reaksiyonlar i�in doz ayarlama �nerileri
| Kombinasyon tedavisinde YULAREB dozu |
�nerilen doz | G�nde iki kez 150 mg |
�lk doz ayarlamas� | G�nde iki kez 100 mg |
�kinci doz ayarlamas� | G�nde iki kez 50 mg |
Tablo 2. Hematolojik toksisiteler i�in y�netim �nerileri
YULAREB tedavisi ba�lat�lmadan �nce, tedavinin ilk iki ay� boyunca iki haftada bir, sonraki iki ay boyunca ayda bir ve klinik olarak endike oldu�u �ekilde tam kan say�m� kontrol edilmelidir. Tedavi ba�lat�lmadan �nce mutlak n�trofil say�s� (ANC) ≥1500/mm, platelet d�zeyi ≥100.000/mm ve hemoglobin d�zeyi ≥8 g/dL olmas� �nerilmektedir.
Toksisite | Y�netim �nerileri |
GRADE 1 veya 2 | Doz ayarlamas� gerekli de�ildir. |
GRADE 3 | Toksisite GRADE 2 veya daha d���k GRADE'e gerileyene kadar doza ara verilmelidir. Doz azalt�m� gerekli de�ildir. |
GRADE 3, rek�rren veya GRADE 4 | Toksisite GRADE 2 veya daha d���k GRADE'e gerileyene kadar doza ara verilmelidir. Tedavi bir sonraki d���k dozda tekrar ba�lat�lmal�d�r. |
Hematopoetik b�y�me fakt�rlerinin uygulanmas� gereken hastalar | Hematopoetik b�y�me fakt�rlerinin son dozu uyguland�ktan sonra en az 48 saat boyunca ve toksisite GRADE 2 veya daha d���k GRADE'e gerileyene kadar abemasiklib dozuna ara verilmelidir. Daha �nce b�y�me fakt�r� kullan�m�na yol a�an toksisite i�in doz azalt�m� uygulanm�� oldu�u s�rece, tedavi bir sonraki d���k dozda tekrar ba�lat�lmal�d�r. |
LLN: Normal alt limiti
Tablo 3. Diyare i�in y�netim �nerileri
�lk sulu d��k� belirtisi tespit edildi�inde, loperamid gibi antidiyare ila�lar�yla tedavi ba�lat�lmal�d�r.
Toksisite | Y�netim �nerileri |
GRADE 1 | Doz ayarlamas� gerekli de�ildir. |
GRADE 2 | Toksisite 24 saat i�inde GRADE 1 veya daha d���k GRADE'e gerilemedi�i takdirde, toksisite ortadan kalkana kadar doza ara verilmelidir. Doz azalt�m� gerekli de�ildir. |
Maksimum destekleyici �nlemlere ra�men s�ren veya ayn� doz tekrar ba�lat�ld�ktan sonra tekrarlayan GRADE 2 |
Toksisite GRADE 1 veya daha d���k GRADE'e gerileyene kadar doza ara verilmelidir. Tedavi bir sonraki d���k dozda tekrar ba�lat�lmal�d�r. |
GRADE 3 veya 4 veya hastaneye yat�� gereklili�i |
Tablo 4. Aminotransferazlar�n y�kselmesi i�in y�netim �nerileri
YULAREB tedavisi ba�lat�lmadan �nce, tedavinin ilk iki ay� boyunca iki haftada bir, sonraki iki ay boyunca ayda bir ve klinik olarak uyguland��� �ekilde alanin aminotransferaz (ALT) ve aspartat aminotransferaz (AST) kontrol edilmelidir.
Toksisite | Y�netim �nerileri |
GRADE 1 (>ULN-3,0 x ULN) GRADE 2 (>3,0-5,0 x ULN) | Doz ayarlamas� gerekli de�ildir. |
Persistan ya da Rek�rren GRADE 2 veya 3 (>5,0-20,0 x ULN) | Toksisite ba�lang�ca veya GRADE 1'e gerileyene kadar doza ara verilmelidir. Tedavi bir sonraki d���k dozda tekrar ba�lat�lmal�d�r. |
Kolestaz yoklu�unda AST ve/veya ALT >3 x ULN ile total bilirubin >2 x ULN'de y�kselme | Abemasiklib kesilmelidir. |
GRADE 4 (>20,0 x ULN) | Abemasiklib kesilmelidir. |
ULN: Normal �st limit
Tablo 5. �nterstisyel Akci�er Hastal���/Pn�monit i�in y�netim �nerileri
Toksisite | Y�netim �nerileri |
GRADE 1 veya 2 | Doz ayarlamas� gerekli de�ildir. |
Maksimum destekleyici �nlemlerle 7 g�n i�inde ba�lang�ca veya GRADE 1'e |
Toksisite GRADE 1'e veya daha d���k GRADE'e gerileyene kadar doza ara verilmelidir. |
gerilemeyen persistan ya da rek�rren GRADE 2 toksisite | Tedavi bir sonraki d���k dozda tekrar ba�lat�lmal�d�r. |
GRADE 3 veya 4 | YULAREB'i kesiniz. |
Tablo 6. Ven�z tromboembolik olaylar (VTE'ler) i�in y�netim �nerileri
Toksisite | Y�netim �nerileri |
Erken evre meme kanseri |
|
T�m GRADE'ler (1, 2, 3 veya 4) | Doza ara verilmelidir ve klinik olarak endike oldu�u �ekilde m�dahale edilmelidir. Hasta klinik olarak stabil oldu�unda abemasiklib tekrar ba�lat�labilir. |
�leri evre veya metastatik meme kanseri |
|
GRADE 1 veya 2 | Doz ayarlamas� gerekli de�ildir. |
GRADE 3 veya 4 | Doza ara verilmelidir ve klinik olarak endike oldu�u �ekilde m�dahale edilmelidir. Hasta klinik olarak stabil oldu�unda abemasiklib tekrar ba�lat�labilir. |
Tablo 7. Hematolojik olmayan toksisiteler (diyare, artm�� aminotransferazlar ve interstisyel akci�er hastal���/pn�monit ve VTE'ler hari�) i�in y�netim �nerileri
Toksisite | Y�netim �nerileri |
GRADE 1 veya 2 | Doz ayarlamas� gerekli de�ildir. |
Maksimum destekleyici �nlemlerle 7 g�n i�inde ba�lang�ca veya GRADE 1'e gerilemeyen persistan ya da rek�rren GRADE 2 toksisite |
Toksisite GRADE 1'e veya daha d���k GRADE'e gerileyene kadar doza ara verilmelidir. Tedavi bir sonraki d���k dozda tekrar ba�lat�lmal�d�r. |
GRADE 3 veya 4 |
CYP3A4 inhibit�rleri
G��l� CYP3A4 inhibit�rlerinin e�zamanl� kullan�m�ndan ka��n�lmal�d�r. E�er g��l� CYP3A4 inhibit�r� kullan�m�ndan ka��n�lamazsa, abemasiklib dozu g�nde iki kez 100 mg'a d���r�lmelidir.
Abemasiklib dozu g�nde iki kez 100 mg abemasiklibe d���r�lm�� ve g��l� bir CYP3A4 inhibit�r�n�n e�zamal� kullan�m�ndan ka��n�lamayan hastalarda, abemasiklib dozu g�nde iki kez 50 mg'a d���r�lmelidir.
Dozu g�nde iki kez 50 mg abemasiklibe d���r�lm�� ve g��l� bir CYP3A4 inhibit�r�n�n e�zamanl� kullan�m�ndan ka��n�lamayan hastalarda, toksisite belirtileri yak�ndan izlenerek abemasiklib dozu s�rd�r�lebilmektedir. Alternatif olarak, abemasiklib dozu g�nde bir kez 50 mg'a d���r�lebilir veya kesilebilir.
CYP3A4 inhibit�r� kesilirse, abemasiklib dozu, CYP3A4 inhibit�r�n�n ba�lat�lmas�ndan �nce kullan�lan doza y�kseltilmelidir (CYP3A4 inhibit�r�n�n 3 ila 5 yar� �mr�nden sonra).
Uygulama �ekli:
YULAREB oral kullan�m i�indir.
Doz a� veya tok karn�na al�nabilir. Abemasiklib greyfurt veya greyfurt suyu ile birlikte al�nmamal�d�r (bkz. B�l�m 4.5).
Hastalar dozlar� her g�n yakla��k olarak ayn� saatlerde almal�d�r.
Tablet b�t�n olarak yutulmal�d�r (tabletler yutulmadan �nce �i�nenmemeli, ezilmemeli veya b�l�nmemelidir).
�zel pop�lasyonlara iliskin ek bilgiler:
B�brek yetmezli�i:
Hafif veya orta derece b�brek yetmezli�i olan hastalarda doz ayarlamas� gerekli de�ildir. �iddetli b�brek yetmezli�i, son d�nem b�brek hastal��� olan veya diyaliz uygulanan hastalarda abemasiklib uygulamas� ile ilgili veri yoktur (bkz. B�l�m 5.2). �iddetli b�brek yetmezli�i olan hastalarda, abemasiklib toksisite belirtileri yak�ndan izlenerek dikkatli bir �ekilde uygulanmal�d�r.
Karaci�er yetmezli�i:
Hafif (Child Pugh A) veya orta derece (Child Pugh B) karaci�er yetmezli�i olan hastalarda doz ayarlamas� gerekli de�ildir. �iddetli karaci�er yetmezli�i (Child Pugh C) olan hastalarda dozlama s�kl���n�n g�nde bir defaya d���r�lmesi �nerilmektedir (bkz. B�l�m 5.2).
Pediyatrik pop�lasyon:
18 ya� alt� �ocuklarda abemasiklibin g�venlili�i ve etkilili�i belirlenmemi�tir. Bu konuda veri yoktur.
Geriyatrik pop�lasyon:
Ya�a g�re doz ayarlamas� gerekli de�ildir (bkz. B�l�m 5.2).
4.3. Kontrendikasyonlar
Etkin madde
4.4. �zel kullan�m uyar�lar� ve �nlemleri
N�tropeni
Abemasiklib kullanan hastalarda n�tropeni bildirilmi�tir. GRADE 3 veya 4 n�tropeni geli�en hastalarda doz modifikasyonu �nerilmektedir (bkz. B�l�m 4.2). N�tropenik sepsis �l�mc�l olaylar�, metastatik meme kanseri hastalar�n�n <% 1'inde meydana gelmi�tir. Hastalar herhangi bir ate� epizodunu sa�l�k uzmanlar�na bildirmeleri konusunda bilgilendirilmelidir.
Enfeksiyonlar / enfestasyonlar
Abemasiklib art� endokrin tedavi alan hastalarda, endokrin tedavi alan hastalardan daha y�ksek oranda enfeksiyon bildirilmi�tir. E� zamanl� n�tropenisi olmayan abemasiklib alan hastalarda akci�er enfeksiyonu bildirilmi�tir. �l�mc�l olaylar, metastatik meme kanseri
hastalar�n�n <% 1'inde meydana gelmi�tir. Hastalar enfeksiyonun belirtileri ve semptomlar� a��s�ndan izlenmeli ve t�bbi a��dan uygun olan �ekilde tedavi edilmelidir.
Ven�z Tromboembolizm
Ven�z tromboembolik olaylar abemasiklib art� endokrin tedavi ile tedavi edilen hastalarda bildirilmi�tir. Hastalar derin ven trombozu ve pulmoner embolizm belirti ve semptomlar� a��s�ndan izlenmeli ve t�bbi a��dan uygun olan �ekilde tedavi edilmelidir. VTE GRADE'ine ba�l� olarak, abemasiklib doz ayarlamas� gerekebilir (bkz. B�l�m 4.2).
Artm�� Aminotransferazlar
Abemasiklib kullanan hastalarda ALT ve AST y�kselmesi bildirilmi�tir. ALT ve AST art�� d�zeyine ba�l� olarak, abemasiklib dozunun de�i�tirilmesi gerekebilir (bkz. B�l�m 4.2).
Diyare
Diyare en yayg�n advers reaksiyondur. Klinik �al��malarda, ilk diyare olay�n�n ba�lang�c�na kadar ge�en medyan s�re yakla��k 6-8 g�n, medyan diyare s�resi 7-12 g�n (GRADE 2) ve 5-8 g�n (GRADE 3) olarak belirlenmi�tir. Diyare dehidrasyon ile ili�kili olabilir. Hastalar ilk sulu d��k� bulgusu tespit etti�inde loperamid gibi bir antidiyareik tedavisine ba�lamal�, oral s�v� al�m�n� art�rmal� ve doktorunu bilgilendirmelidir. ≥ GRADE 2 diyare geli�en hastalarda doz modifikasyonu �nerilmektedir (bkz. B�l�m 4.2).
CYP3A4 ind�kleyicileri ile e�zamanl� kullan�m
Abemasiklib etkilili�inde azalma riski nedeniyle CYP3A4 ind�kleyicilerinin e�zamanl� kullan�m�ndan ka��n�lmal�d�r (bkz. B�l�m 4.5).
Viseral kriz
Viseral kriz geli�en hastalarda abemasiklibin etkilili�i ve g�venlili�i hakk�nda veri yoktur. �nterstisyel akci�er hastal���/pn�monit
YULAREB ve di�er CDK4/6 inhibit�rleri ile tedavi edilen hastalarda ciddi, hayat� tehdit edici veya �l�mc�l interstisyel akci�er hastal��� ve/veya pn�monit olu�abilir. Klinik �al��malarda (MONARCH 1, MONARCH 2 ve MONARCH 3), YULAREB ile tedavi edilen hastalar�n
%3,3'� herhangi bir GRADE, %0,6's� GRADE 3 veya 4, ve %0,4'� �l�mc�l sonu�lara sahip interstisyel akci�er hastal���/pn�monit ya�am��t�r.
Pazarlama sonras� ortamda, bildirilen �l�mlerle birlikte ilave interstisyel akci�er hastal���/pn�monit vakalar� g�zlemlenmi�tir (bkz. B�l�m 4.8).
Hastalar� interstisyel akci�er hastal���/pn�moniti i�aret eden pulmoner semptomlar a��s�ndan izleyiniz. Semptomlar hipoksi, �ks�r�k, nefes darl��� veya radyolojik incelemelerdeki interstisyel infiltratlar� i�erebilir. Enfeksiy�z, neoplastik ve bu gibi semptomlar�n di�er nedenleri uygun ara�t�rmalarla d��lanmal�d�r.
�nterstisyel akci�er hastal���/pn�monit derecesine ba�l� olarak abemasiklib doz modifikasyonu gerekebilir.
Kal�c� veya tekrarlayan GRADE 2 interstisyel akci�er hastal���/pn�monit geli�en hastalarda doz kesilmesi veya doz azalt�lmas� �nerilmektedir. GRADE 3 veya 4 interstisyel akci�er hastal��� veya pn�moniti olan t�m hastalarda YULAREB'i kal�c� olarak sonland�r�n�z (bkz. B�l�m 4.2).
Laktoz
Nadir kal�t�msal galaktoz intolerans�, total laktaz yetmezli�i ya da glukoz-galaktoz malabsorpsiyon problemi olan hastalar�n bu ilac� kullanmamalar� gerekir.
4.5. Di�er t�bbi �r�nler ile etkile�imler ve di�er etkile�im �ekilleri
Di�er t�bbi �r�nlerin abemasiklib farmakokinetikleri �zerindeki etkileri Abemasiklib primer olarak CYP3A4 taraf�ndan metabolize edilir.CYP3A4 inhibit�rleri
Abemasiklibin baz� CYP3A4 inhibit�rleriyle birlikte uygulanmas� abemasiklib plazma konsantrasyonlar�n� art�rabilir. �leri evre ve/veya metastatik kanser hastalar�nda bir CYP3A4 inhibit�r� olan klaritromisin ile birlikte uygulama, abemasiklibin plazma maruziyetinde 3,4 kat art��, abemasiklib ve aktif metabolitlerinin kombine ba�l� olmayan potansiyel plazma maruziyetinde ise 2,5 kat art��a yol a�m��t�r.
Abemasiklib ile birlikte g��l� CYP3A4 inhibit�rlerinin kullan�lmas�ndan ka��n�lmal�d�r. E�er g��l� CYP3A4 inhibit�rlerinin birlikte uygulanmas� gerekiyorsa, abemasiklib dozu azalt�lmal�d�r (bkz b�l�m 4.2), ard�ndan toksisitenin dikkatlice izlenmesi gerekir. G��l� CYP3A4 inhibit�rlerinin �rnekleri bunlarla birlikte ama bunlarla s�n�rl� olmayan: klaritromisin, itrakonazol, ketokonazol, lopinavir/ritonavir, posakonazol veya vorikonazolu i�ermektedir. Greyfurt veya greyfurt suyundan ka��n�lmal�d�r.
Orta veya zay�f CYP3A4 inhibit�rleri ile tedavi edilen hastalar i�in doz ayarlamas� gerekmez. Bununla birlikte, toksisite belirtileri i�in yak�n izleme yap�lmal�d�r.
CYP3A4 ind�kleyicileri
Abemasiklibin g��l� CYP3A4 ind�kleyicisi rifampisin ile birlikte uygulanmas�, abemasiklibin plazma konsantrasyonunu %95 ve ba�l� olmayan potansiyel abemasiklibin konsantrasyonunu ve aktif metabolitlerini EAA0-∞ de�erine g�re %77 oran�nda azaltm��t�r. G��l� CYP3A4 ind�kleyicilerinin birlikte kullan�m�ndan (karbamazepin, fenitoin, rifampisin ve St. John's wort dahil, ancak bunlarla s�n�rl� olmamak �zere), abemasiklibin etkilili�inin azalt�lmas� riski nedeniyle ka��n�lmal�d�r.
Abemasiklibin di�er t�bbi �r�nlerin farmakokinetikleri �zerindeki etkileri
Ta��y�c� substrat� olan t�bbi �r�nler
Abemasiklib ve maj�r aktif metabolitleri renal ta��y�c�lar olan organik katyon ta��y�c� 2 (OCT2), �oklu ila� ve toksin ekstr�zyon proteini (MATE1) ve MATE2-K'yi inhibe eder. Bu ta��y�c�lar�n dofetilid veya kreatinin gibi klinik olarak anlaml� substratlar� ile abemasiklib aras�nda in vivo etkile�imler ger�ekle�ebilir (bkz. B�l�m 4.8). Abemasiklib 400 mg ve metforminin (OCT2, MATE1 ve 2 substrat�) birlikte uyguland��� bir klinik ila� etkile�imi �al��mas�nda, metformin plazma maruziyetinde k���k ancak klinik a��dan anlaml� olmayan bir
art�� (%37) g�zlemlenmi�tir. Bu art���n, glomer�ler filtrasyondan etkilenmedi�i renal sekresyon azalmas�na ba�l� oldu�u tespit edilmi�tir.
Sa�l�kl� bireylerde abemasiklib ile bir P-glikoprotein (P-gp) substrat� olan loperamidin birlikte uygulanmas�, loperamid plazma maruziyetinde EAAde�erine g�re %9, Cde�erine g�re
%35 art��a yol a�m��t�r. Bu art�� klinik a��dan anlaml� bulunmam��t�r. Bununla birlikte, abemasiklib ile g�zlemlenen in vitro P-gp ve meme kanseri diren� proteini (BCRP) inhibisyonu g�z �n�nde bulunduruldu�unda, bu ta��y�c�lar�n digoksin veya dabigatran eteksilat gibi dar terap�tik indeksli substratlar� ile abemasiklib aras�nda in vivo etkile�im ger�ekle�ebilir.
Meme kanseri hastalar�n�n yer ald��� bir klinik �al��mada, abemasiklib ile anastrozol, fulvestrant, eksemestan, letrozol veya tamoksifen aras�nda klinik a��dan anlaml� farmakokinetik ila� etkile�imi g�zlenmemi�tir.
Abemasiklibin sistemik etki g�steren hormonal kontraseptiflerin etkinli�ini azalt�p azaltmad��� hen�z bilinmemektedir.
�zel pop�lasyonlara ili�kin ek bilgiler:
Hi�bir etkile�im �al��mas� yap�lmam��t�r.
Pediyatrik pop�lasyon:
Hi�bir etkile�im �al��mas� yap�lmam��t�r.
4.6. Gebelik ve laktasyon
Gebelik kategorisi C'dir.
�ocuk do�urma potansiyeli bulunan kad�nlar/Do�um kontrol� (Kontrasepsiyon)
�ocuk do�urma potansiyeli olan kad�nlar tedavi s�ras�nda ve tedavi tamamland�ktan sonra en az 3 hafta boyunca y�ksek oranda etkili kontrasepsiyon y�ntemleri (�r. �ift bariyer kontrasepsiyon) kullanmal�d�r (bkz. B�l�m 4.5).
Gebelik d�nemi
Gebe kad�nlarda abemasiklib kullan�m�yla ilgili veri yoktur. Hayvanlarda yap�lan �al��malarda �reme toksisitesi g�sterilmi�tir (bkz. B�l�m 5.3). �nsanlara y�nelik potansiyel risk bilinmemektedir. YULAREB, gebelik s�ras�nda ve kontrasepsiyon kullanmayan �ocuk do�urma potansiyeli olan kad�nlarda �nerilmemektedir.
Laktasyon d�nemi
Abemasiklibin anne s�t�ne ge�ip ge�medi�i bilinmemektedir. Yenido�ana/bebe�e y�nelik risk d��lanamaz. Abemasiklib kullanan hastalar emzirmemelidir.
�reme yetene�i /Fertilite
Abemasiklibin insanlarda fertilite �zerindeki etkisi bilinmemektedir. S��anlarda erkek fertilitesi �zerine hi�bir etki kaydedilmezken; farelerde, s��anlarda ve k�peklerde erkek �reme sistemindeki sitotoksik etkiler abemasiklibin erkeklerde fertilite bozuklu�una neden olabilece�ine i�aret etmektedir. Farelerde, s��anlarda veya k�peklerde di�i �reme organlar�
�zerine herhangi bir advers etki g�zlenmemi�tir, veya s��anlarda di�i fertilitesi ve erken embriyonik geli�im �zerine hi�bir etki g�zlenmemi�tir (bkz. B�l�m 5.3).
4.7. Ara� ve makine kullan�m� �zerindeki etkiler
YULAREB'in ara� ve makine kullan�m� �zerindeki etkisi �ok azd�r. YULAREB ile tedavi s�ras�nda hastalara yorgunluk veya ba� d�nmesi ya�amalar� durumunda araba s�rerken veya kullan�rken dikkatli olmalar� �nerilmelidir (bkz. B�l�m 4.8).
4.8. �stenmeyen etkiler
G�venlilik profili �zeti
En s�k geli�en advers reaksiyonlar diyare, enfeksiyonlar, n�tropeni, l�kopeni, anemi, yorgunluk, bulant�, kusma, alopesi ve i�tah kayb�d�r.
En yayg�n advers reaksiyonlardan, n�tropeni, l�kopeni ve diyare haricindeki GRADE ≥ 3 olaylar %5'ten azd�r.
Advers reaksiyonlar�n tablo halinde listesi
A�a��daki tabloda, advers reaksiyonlar MedDRA v�cut sistem organ s�n�f� ve s�kl�k derecesine g�re listelenmi�tir. S�kl�k dereceleri: �ok yayg�n (≥1/10); yayg�n (≥1/100 ila <1/10); yayg�n olmayan (≥1/1.000 ila <1/100); seyrek (≥1/10.000 ila <1/1.000); �ok seyrek (<1/10.000), bilinmiyor (eldeki verilerden hareketle tahmin edilemiyor). Her s�kl�k grubunda, advers reaksiyonlar azalan s�kl�kta sunulmaktad�r.
Tablo 8. Endokrin tedavisiile kombinasyon halinde abemasiklibin faz 3 �al��malar�nda bildirilen advers reaksiyonlar (N = 3559)
MedDRA Sistem organ s�n�f� | �ok yayg�n | Yayg�n | Yayg�n olmayan |
Enfeksiyonlar ve enfestasyonlar | Enfeksiyonlar |
|
|
Kan ve lenf sistemi hastal�klar� | N�tropeni L�kopeni Anemi Trombositopeni Lenfopeni |
| Febril n�tropeni |
Metabolizma ve beslenme hastal�klar� | ��tah azalmas� |
|
|
Sinir sistemi hastal�klar� | Ba� a�r�s� Disguzi Ba� d�nmesi |
|
|
G�z hastal�klar� |
| Lakrimasyon art��� |
|
Vask�ler hastal�klar |
| Ven�z tromboembolizm |
|
Solunum, g���s bozukluklar� ve mediastinal hastal�klar |
| �nterstisyel akci�er hastal���/pn�monit |
|
Gastrointestinal hastal�klar | Diyare Kusma Bulant� Stomatit | Dispepsi |
|
Deri ve deri alt� doku hastal�klar� | Alopesi Ka��nt� D�k�nt� | T�rnak bozuklu�u Deride kuruluk |
|
Kas-iskelet bozukluklar�, ba� doku ve kemik hastal�klar� |
| Kas g��s�zl��� |
|
Genel bozukluklar ve uygulama b�lgesine ili�kin hastal�klar | Pireksi Yorgunluk |
|
|
Ara�t�rmalar | Alanin aminotransferaz art��� Aspartat aminotransferaz art��� |
|
|
obliterans yer al�r.
Se�ili advers reaksiyonlar�n tan�m�
N�tropeni
�al��malarda n�tropeni s�kl�kla bildirilmi�tir. MonarchE �al��mas�nda, hastalar�n % 45,8'inde n�tropeni bildirilmi�tir. Endokrin tedavi ile kombinasyon halinde abemasiklib alan hastalar�n
% 19,1'inde n�trofil say�lar�nda GRADE 3 veya 4 azalma (laboratuvar bulgular�na g�re), ba�lamas�na kadar ge�en medyan s�re 30 g�n ve iyile�meye kadar ge�en medyan s�re 16 g�n olarak bildirilmi�tir. Hastalar�n % 0,3'�nde febril n�tropeni bildirilmi�tir MONARCH 2 ve MONARCH 3 �al��malar�nda hastalar�n % 45,1'inde n�tropeni bildirilmi�tir. Aromataz inhibit�rleri veya fulvestrant ile kombinasyon halinde abemasiklib alan hastalar�n % 28,2'sinde n�trofil say�s�nda GRADE 3 veya 4 azalma (laboratuvar bulgular�na g�re) bildirilmektedir. GRADE 3 veya 4 n�tropeni ba�lang�c�na kadar ge�en medyan s�re 29-33 g�n, iyile�meye kadar
ge�en medyan s�re 11-15 g�n olarak belirlenmi�tir. Hastalar�n % 0,9'unda febril n�tropeni bildirilmi�tir. GRADE 3 veya 4 n�tropeni geli�en hastalarda doz modifikasyonu �nerilmektedir (bkz. B�l�m 4.2).
Diyare
Diyare en s�k bildirilen advers reaksiyondur (bkz. Tablo 8). Abemasiklib tedavisinin ilk ay� i�inde en y�ksek d�zeyde kaydedilen insidans daha sonra d��m��t�r. MonarchE �al��mas�nda, herhangi bir GRADE'de ilk diyare olay�n�n ba�lang�c�na kadar ge�en medyan s�re 8 g�n olmu�tur. Medyan diyare s�resi GRADE 2 i�in 7 g�n ve GRADE 3 i�in 5 g�n olmu�tur. MONARCH 2 and MONARCH 3 �al��malar�nda, herhangi bir GRADE'de ilk diyare olay�n�n ba�lang�c�na kadar ge�en medyan s�re yakla��k 6-8 g�n olmu�tur. Medyan diyare s�resi GRADE 2 i�in 9-12 g�n ve GRADE 3 i�in 6-8 g�n olmu�tur. Diyare, loperamid gibi destekleyici tedaviler ve/veya doz ayarlamas� sonucunda ba�lang�ca veya daha d���k GRADE'e gerilemi�tir (bkz. B�l�m 4.2).
Artm�� Aminotransferazlar
MonarchE �al��mas�nda, endokrin tedavi ile kombinasyon halinde abemasiklib alan hastalarda ALT ve AST y�kselmeleri s�k bildirilmi�tir (s�ras�yla % 12,3 ve % 11,8). GRADE 3 veya 4, ALT veya AST y�kselmeleri (laboratuvar bulgular�na g�re) hastalar�n % 2,6 ve % 1,6's�nda bildirilmi�tir. GRADE 3 veya 4 ALT y�kselmesinin ba�lamas�na kadar ge�en medyan s�re 118 g�n ve iyile�meye kadar ge�en medyan s�re 14,5 g�n olmu�tur. GRADE 3 veya 4 AST y�kselmesinin ba�lamas�na kadar ge�en medyan s�re 90,5 g�n ve iyile�meye kadar ge�en medyan s�re 11 g�n olmu�tur. MONARCH 2 ve MONARCH 3 �al��malar�nda, aromataz inhibit�rleri veya fulvestrant ile kombinasyon halinde abemasiklib alan hastalarda ALT ve AST art��� s�k bildirilmi�tir (s�ras�yla %15,1 ve %14,2). GRADE 3 veya 4 ALT veya AST art��lar� (laboratuvar bulgular�na g�re) hastalar�n %6,1 ve %4,2'sinde bildirilmi�tir. GRADE 3 veya 4 ALT art��� ba�lang�c�na kadar ge�en medyan s�re 57-61 g�n, iyile�meye kadar ge�en medyan s�re 14 g�n olmu�tur. Grade 3 veya 4 AST art��� ba�lang�c�na kadar ge�en medyan s�re 71 ila 185 g�nd�r ve normale d�nmesi i�in ge�en medyan s�re 13 ila 15 g�nd�r. GRADE 3 veya 4 ALT veya AST art��� geli�en hastalarda doz modifikasyonu �nerilmektedir (bkz. B�l�m 4.2).
Kreatinin
Advers reaksiyon olarak kabul edilmese de, abemasiklibin serum kreatinin art���na yol a�t��� g�sterilmi�tir. MonarchE �al��mas�nda, hastalar�n %99,3'�nde serum kreatinin art��� (laboratuvar bulgular�na g�re) kaydedilmi�tir ve bunlar�n %0,5'inde GRADE 3 veya 4 art��lar olmu�tur. Yaln�zca endokrin tedavi alan hastalar�n %91,0'�nda serum kreatininde art�� bildirmi�tir (t�m laboratuvar GRADE'leri). MONARCH 2 ve MONARCH 3 �al��malar�nda, hastalar�n %98,3'�nde serum kreatinin art��� kaydedilmi�tir (laboratuvar bulgular�na g�re) ve bu hastalar�n %1,9'unda GRADE 3 veya 4 art�� kaydedilmi�tir. Tek ba��na aromataz inhibit�r� veya fulvestrant alan hastalar�n %78,4'�nde serum kreatinin art��� bildirilmi�tir (t�m laboratuvar derecelerinde). Abemasiklibin, renal t�b�ler sekresyon ta��y�c�lar�n�n inhibisyonu arac�l���yla glomer�ler fonksiyonu etkilemeden (ioheksol klerensine g�re �l��len) serum kreatinin d�zeyini art�rd��� g�sterilmi�tir (bkz. B�l�m 4.5). Klinik �al��malarda, serum kreatinin art��lar� abemasiklib dozlamas�n�n ilk ay�nda ortaya ��km��, tedavi d�nemi boyunca y�ksek ancak stabil kalm��, tedavi b�rak�ld�ktan sonra geri d�n���ml� seyir izlemi� ve buna kan �re azotu (BUN), sistatin C veya sistatin C baz al�narak hesaplanan glomer�ler filtrasyon h�z�
gibi b�brek fonksiyonu belirte�lerinde de�i�iklikler e�lik etmemi�tir. ��pheli advers reaksiyonlar�n raporlanmas�
Ruhsatland�rma sonras� ��pheli ila� advers reaksiyonlar�n�n raporlanmas� b�y�k �nem ta��maktad�r. Raporlanma yap�lmas�, ilac�n yarar/risk dengesinin s�rekli olarak izlenmesine olanak sa�lar. Sa�l�k mesle�i mensuplar�n�n herhangi bir ��pheli advers reaksiyonu T�rkiye Farmakovijilans Merkezi (T�FAM)'ne bildirmeleri gerekmektedir (www.titck.gov.tr, e-posta: tufam@titck.gov.tr; tel: 0 800 314 00 08; faks: 0 312 218 35 99).
4.9. Doz a��m� ve tedavisi
Abemasiklib doz a��m� durumunda, yorgunluk ve diyare geli�ebilir. Genel destekleyici tedavi uygulanmal�d�r.
5. FARMAKOLOJ�K �ZELL�KLER
5.1. Farmakodinamik �zellikler
Farmakoterap�tik grup: Antineoplastik ajanlar, Protein kinaz inhibit�rleri, ATC kodu: L01EF03
Etki mekanizmas�
Abemasiklib, siklin ba��ml� kinaz 4 ve 6'n�n (CDK4 ve CDK6) potent ve se�ici bir inhibit�r� olup, enzimatik testlerde en �ok Siklin D1/CDK4'e kar�� aktif oldu�u bulunmu�tur. Abemasiklib retinoblastom proteininin (Rb) fosforilasyonunu �nleyerek h�cre d�ng�s�n�n G1'den h�cre b�l�nmesi S faz�na ilerlemesini bloke eder ve b�ylece t�m�r b�y�mesinin bask�lanmas�n� sa�lar. �strojen resept�r� pozitif meme kanseri h�cre soylar�nda abemasiklib ile sa�lanan uzun s�reli hedef inhibisyonu Rb fosforilasyonunun geri d�n���n� �nleyerek h�cre ya�lanmas�na ve apoptoza yol a�m��t�r. �n vitro, Rb-negatif ve Rb-depleted kanser h�cre serileri, genellikle abemasiklibe kar�� daha az hassast�r. Meme kanseri ksenogreft modellerinde, klinik a��dan anlaml� konsantrasyonlarda tek ba��na veya anti-�strojenlerle kombinasyon halinde kesintisiz olarak her g�n dozlama yap�larak uygulanan abemasiklib t�m�r boyutunda k���lme sa�lam��t�r.
Farmakodinamik etkiler
G1 restriksiyon noktas�ndan �nce h�cre d�ng�s� inhibisyonuyla sonu�lanan Rb fosforilasyonu ve topoizomeraz II alfa inhibisyonundan anla��ld��� �zere, abemasiklib kanser hastalar�nda CDK4 ve CDK6'y� inhibe eder.
Kardiyak elektrofizyoloji
Abemasiklibin QTcF aral��� �zerindeki etkisi 144 ileri evre kanser hastas�nda de�erlendirilmi�tir. Terap�tik dozlama program�n�n ard�ndan g�zlemlenen ortalama maksimum kararl� durum abemasiklib konsantrasyonunda QTcF aral���nda b�y�k bir de�i�iklik (>20 ms) saptanmam��t�r.
Sa�l�kl� bireylerde g�nde iki kez 200 mg dozuna benzer maruziyet d�zeylerinde yap�lan maruziyet-yan�t analizinde, abemasiklibin QTcF aral���n� klinik a��dan anlaml� derecede uzatmad��� belirlenmi�tir.
Klinik etkililik ve g�venlilik
Erken evre meme kanseri
Randomize Faz 3 �al��ma monarchE: Endokrin tedavi ile kombinasyon halinde abemasiklib
Adjuvan endokrin tedavi ile kombinasyon halinde abemasiklib'in etkilili�i ve g�venli�i, HR pozitif, HER2 negatif, nod pozitif, n�ks riski y�ksek erken evre meme kanseri olan kad�n ve erkeklerde, randomize, a��k etiketli, iki kohortlu bir faz 3 �al��ma olan monarchE �al��mas�nda de�erlendirilmi�tir. Y�ksek n�ks riski, �u klinik ve patolojik �zelliklerle tan�mlanm��t�r: ≥ 4 pALN (pozitif aksiller lenf d���mleri) veya 1-3 pALN ve takip eden kriterlerden en az biri: t�m�r boyutu ≥5 cm veya histolojik grade 3 veya y�ksek Ki-67 indeksi (≥%20).
Toplam 5637 hasta, 2 y�l g�nde iki kez abemasiklib 150 mg art� doktor se�imi standart endokrin tedavi veya tek ba��na standart endokrin tedavi alacak �ekilde 1:1 oran�nda randomize edilmi�tir. Randomizasyon, �nceki kemoterapi, menopoz durumu ve b�lgeye g�re ger�ekle�tirilmi�tir. Erkekler postmenopozal olarak s�n�fland�r�lm��t�r. Hastalar definitif lokorejyonal tedaviyi (neoadjuvan veya adjuvan kemoterapi olsun veya olmas�n) tamamlam��t�r. Hastalar, �nceki herhangi bir kemoterapi veya radyoterapinin akut yan etkilerinden kurtulmu� olmal�d�r. Randomizasyondan �nce, kemoterapiden sonra 21 g�n ve radyoterapiden sonra 14 g�nl�k bir ar�nma periyodu gerekli olmu�tur. Randomizasyondan �nce hastalar�n 12 haftaya kadar adjuvan endokrin tedavisi almalar�na izin verilmi�tir. Standart endokrin tedavisi olarak fulvestrant ile adjuvan tedaviye izin verilmemi�tir. Do�u Kooperatifi Onkoloji Grubu (Eastern Cooperative Oncology Group - ECOG) Performans Durumu 0 veya 1 olan hastalar dahil edilmi�tir. VTE �yk�s� olan hastalar �al��maya dahil edilmemi�tir. �al��ma tedavi periyodunun bitiminden sonra, her iki tedavi kolunda hastalar, k�m�latif en az 5 y�l ve t�bbi olarak uygunsa 10 y�la kadar adjuvan endokrin tedavisi almaya devam etmi�tir.
LHRH agonistleri, erkekler ve premenopozal ve perimenopozal kad�nlar i�in klinik olarak endike oldu�unda verilmi�tir.
Randomize pop�lasyon, sadece y�ksek risk klinik ve patolojik �zelliklerine g�re �al��maya al�nan 5120 (%91) hastay� ve 1-3 pALN ve y�ksek Ki-67 indeksine dayal� olarak �al��maya al�nan 517 (%9) hastay� i�ermektedir.
Hasta demografikleri ve ba�lang��taki t�m�r �zellikleri tedavi kollar� aras�nda dengelidir. �al��maya al�nan hastalar�n medyan ya�� yakla��k 51'dir (aral�k, 22-89 y�l); hastalar�n %15'i 65 ya� veya �zeri, %99'u kad�n, %71'i beyaz �rk, %24'� asyal� ve %5'i di�erdir. Hastalar�n %44'� premenopozal veya perimenopozald�r. Hastalar�n �o�u �ncesinde kemoterapi (%37 neoadjuvan, %62 adjuvan) ve radyoterapi (%95) alm��t�r. Hastalar�n ald��� ba�lang�� endokrin tedavi letrozol (%38), tamoksifen (%31), anastrozol (%22) veya eksemestan� (%8) i�ermektedir. Hastalar�n %60'�nda 4 veya daha fazla pozitif lenf nodu, %38'inde GRADE 3 t�m�r ve %22'sinde ameliyatta patolojik t�m�r boyutu ≥5 cm ve %44'� tedavisi ama�lanan pop�lasyonda (ITT) y�ksek Ki-67 indeksine sahiptir.
Birincil sonlan�m noktas� randomizasyondan itibaren; ipsilateral invaziv meme t�m�r� n�ks�, b�lgesel invaziv meme kanseri n�ks�, uzak n�ks, kontralateral invaziv meme kanseri, primeri meme olmayan ikinci bir invazif kanserin ilk olu�umuna kadar ge�en s�re veya herhangi bir
nedene ba�lanabilecek �l�m olarak tan�mlanan �nvazif Hastal�ks�z Sa�kal�m (Invasive Disease- Free Survival - IDFS)'d�r. Anahtar ikincil sonlan�m noktas�, randomizasyondan ilk uzak n�ks olu�umuna veya herhangi bir nedene atfedilebilen �l�me kadar ge�en s�re olarak tan�mlanan Uzak N�kss�z Sa�kal�m (Distant Relapse Free Survival - DRFS)'d�r.
�al��man�n birincil amac�na, �nceden planlanm�� interim analizde (veri kesim tarihi 16 Mart 2020), medyan 15,5 ayl�k takip s�resiyle ula��lm��t�r.
Abemasiklib art� endokrin tedavi alan hastalarda tek ba��na endokrin tedavi alanlara k�yasla IDFS'de istatistiksel olarak anlaml� bir iyile�me g�zlenmi�tir (HR = 0,747, %95 CI [0,598, 0,932], p = 0,0096).Daha ileri bir analizde (01 Nisan 2021 veri kesim tarihli), hastalar�n %90� 2 y�ll�k �al��ma tedavi s�resinden uzakt�r ve medyan takip s�resi 27,1 ayd�r.
Etkililik sonu�lar� Tablo 9 ve �ekil 1'de �zetlenmi�tir.
Tablo 9. monarchE: Etkililik verilerinin �zeti (Tedavisi ama�lanan pop�lasyon)
| Abemasiklib art� endokrin tedavi N = 2808 | Yaln�zca endokrin tedavi N = 2829 |
�nvazif Hastal�ks�z Sa�kal�m (IDFS) |
|
|
Olay g�r�len hasta say�s� (n, %) | 232 (8,3) | 333 (11,8) |
Tehlike oran� (%95 CI) ve p de�eri | 0,696 (0,588, 0,823), p < 0,0001 | |
24. ayda IDFS (%, %95 CI) | 92,7 (91,6, 93,6) | 90,0 (88,8, 91,1) |
36. ayda IDFS (%, %95 CI) | 88,8 (87,0, 90,3) | 83,4 (81,3, 85,3) |
Uzak N�kss�z Sa�kal�m (Distant Relapse Free Survival - DRFS) |
|
|
Olay g�r�len hasta say�s� (n, %) | 191 (6,8) | 278 (9,8) |
Tehlike oran� (%95 CI) | 0,687 (0,571, 0,826) | |
24. ayda DRFS (%, %95 CI) | 94,1 (93,2, 95,0) | 91,6 (90,5, 92,6) |
36. ayda DRFS (%, %95 CI) | 90,3 (88,6, 91,8) | 86,1 (84,2, 87,9) |
K�saltma: CI = G�ven aral��� Veri kesim tarihi 01 Nisan 2021
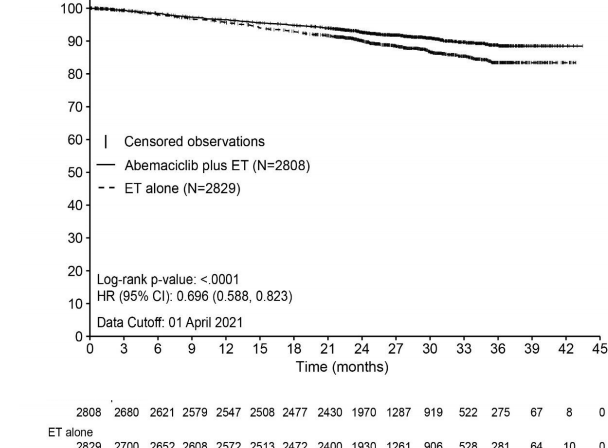
Zaman (ay)
Log-s�ra p-de�eri: <.0001
HR (%95 CI): 0,696 (0,588, 0,823)
Veri kesim: 01 Nisan 2021
Sans�rlenmi� g�zlemler Abemasiklib art� ET (N=2808) Yaln�zca ET (N=2829)
�nvazif Hastal�ks�z Sa�kal�m (%)
�ekil 1. monarchE: IDFS'ye ili�kin Kaplan-Meier grafi�i (Ara�t�rmac� de�erlendirmesi, tedavisi ama�lanan pop�lasyon)
K�saltmalar: CI = g�ven aral���; ET = endokrin tedavi; HR = tehlike oran�; IDFS = invazif hastal�ks�z sa�kal�m; N = pop�lasyondaki hasta say�s�
Veri kesim tarihi 01 Nisan 2021
Co�rafi b�lge, menopoz durumu ve �nceki kemoterapi ile tan�mlanan hasta alt gruplar�nda fayda g�zlemlenmi�tir.�leri evre veya metastatik meme kanseri
Randomize Faz 3 �al��ma MONARCH 3: Aromataz inhibit�rleriyle kombinasyon halinde abemasiklib
Bir aromataz inhibit�r� (anastrozol veya letrozol) ile kombinasyon halinde abemasiklib'in etkilili�i ve g�venlili�i, bu hastal�k ko�ullar�nda �nceden sistemik tedavi uygulanmam�� HR pozitif, HER2 negatif, lokal olarak ilerlemi� veya metastatik meme kanseri olan kad�nlar�n yer ald��� randomize, �ift k�r, plasebo kontroll� bir faz 3 �al��ma olan MONARCH 3 �al��mas�nda de�erlendirilmi�tir. Hastalar, g�nde iki kez 150 mg abemasiklib art� ayn� programa g�re plasebo art� nonsteroid aromataz inhibit�r�ne kar�� �nerilen dozda g�nl�k olarak uygulanan nonsteroid aromataz inhibit�r� almak �zere 2:1 oran�nda randomize edilmi�tir. Primer sonlan�m noktas� RECIST 1.1 uyar�nca ara�t�rmac� taraf�ndan de�erlendirilen progresyonsuz sa�kal�m (PFS), temel sekonder etkililik sonlan�m noktalar� ise objektif yan�t oran� (ORR), klinik yarar oran� (KYO) ve genel sa�kal�m (GS) olarak belirlenmi�tir.
�al��maya al�nan hastalar�n medyan ya�� 63 (aral�k: 32-88) olarak kaydedilmi�tir. Neo(adjuvan) ko�ullarda hastalar�n yakla��k %39'u kemoterapi ve %44'� antihormonal tedavi alm��t�r. �nceden (neo) adjuvan endokrin tedavi alan hastalar, bu tedaviyi �al��ma randomizasyonundan en az 12 ay �nce tamamlam�� olmal�d�r. Hastalar�n b�y�k b�l�m�nde (%96) ba�lang��ta metastatik hastal�k tespit edilmi�tir. Hastalar�n yakla��k %22'sinde yaln�zca kemikte hastal�k g�zlenirken, %53'�nde viseral metastazlar belirlenmi�tir.
�al��ma, PFS'nin iyile�tirilmesi olarak belirlenen primer sonlan�m noktas�n� kar��lam��t�r. Primer etkililik bulgular� Tablo 10 ve �ekil 2'de �zetlenmektedir.
Tablo 10. MONARCH 3: Etkililik verilerinin �zeti (Ara�t�rmac� de�erlendirmesi, tedavisi ama�lanan pop�lasyon)
| Abemasiklib art� aromataz inhibit�r� | Plasebo art� aromataz inhibit�r� |
Progresyonsuz sa�kal�m | N=328 | N=165 |
Ara�t�rmac� de�erlendirmesi, olay say�s� (%) | 138 (42,1) | 108 (65,5) |
Medyan [ay] (%95 CI) | 28,18 (23,51; NR) | 14,76 (11,24; 19,20) |
PFS'deki fark (ay) | NR | |
Tehlike oran� (%95 CI) ve p de�eri | 0,540 (0,418; 0,698); p <0,000002 | |
Ba��ms�z radyografik inceleme, olay say�s� (%) | 91 (27,7) | 73 (44,2) |
Medyan [ay] (%95 CI) | NR (NR; NR) | 19,36 (16,37; 27,91) |
Tehlike oran� (%95 CI) ve p de�eri | 0,465 (0,339; 0,636); p < 0,000001 | |
Objektif yan�t oran�[%] (%95 CI) | 49,7 (44,3; 55,1) | 37,0 (29,6; 44,3) |
Yan�t s�resi [ay] (%95 CI) | 27,39 (25,74; NR) | 17,46 (11,21; 22,19) |
�l��lebilir hastal��� olan hastalarda objektif yan�t |
N=267 |
N=132 |
Objektif yan�t oran� [%] (%95 CI) | 61,0 (55,2 – 66.9) | 45,5 (37,0 ; 53,9) |
Tam yan�t, (%) | 3,4 | 0 |
K�smi yan�t, (%) | 57,7 | 45.5 |
Klinik yarar oran�(�l��lebilir hastal�k) [%] (%95 CI) | 79,0 (74,1; 83,9) | 69,7 (61,9; 77,5) |
�ekil 2. MONARCH 3: Progresyonsuz sa�kal�ma ili�kin Kaplan-Meier grafi�i (Ara�t�rmac� de�erlendirmesi, tedavisi ama�lanan pop�lasyon)
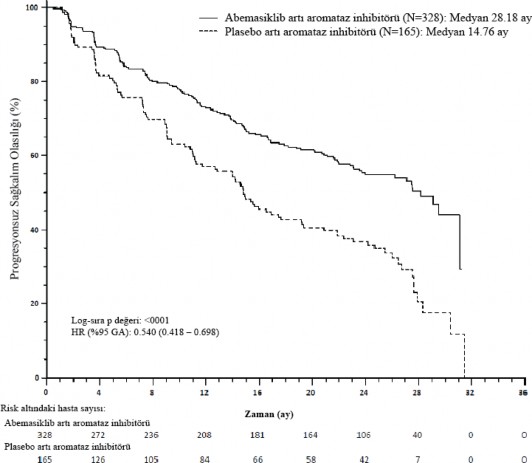
Progresyonsuz sa�kal�m (PFS) abemasiklib art� aromataz inhibit�r� (A�) kolunda anlaml� �l��de uzam��t�r (HR 0,540 [%95 GA, 0,418, 0,698]); medyan PFS abemasiklib art� A� kolunda 28,18 ay, plasebo art� A� kolunda 14,76 ay olarak belirlenmi�tir. Bu bulgular, abemasiklib art� aromataz inhibit�r� ile tedavi edilen hastalarda hastal�k progresyonu veya �l�m riskinde %46 oran�nda klinik a��dan anlaml� bir azalmaya kar��l�k gelmektedir.
Son PFS analizi s�ras�nda genel sa�kal�m verileri olgunla�mam��t�r (iki kolda 93 olay g�zlemlenmi�tir). HR 1,057 (%95 GA: 0,683, 1,633), p=0,8017 olarak bildirilmi�tir.
�nceden belirlenmi� bir dizi alt grup PFS analizi g�stermi�tir ki, ya� (<65 veya ≥65 y�l), hastal�k b�lgesi, hastal�k durumu (de novo metastatik veya rek�rren metastatik ya da lokal olarak ilerlemi� rek�rren), �l��lebilir hastal���n varl���, progesteron resept�r� durumu dahil olmak �zere hasta alt gruplar� aras�nda ve temel ECOG performans durumu parametrelerinde sonu�lar tutarl�d�r. Hastal�k progresyonu veya �l�m riskinde azalma viseral hastal�k bulunan hastalar (HR 0,567 [%95 GA: 0,407, 0,789], medyan PFS 21,6 ay ve 14,0 ay), yaln�zca kemikte
hastal�k bulunan hastalar (HR 0,565, [%95 GA: 0,306, 1,044]) ve �l��lebilir hastal�k bulunan
hastalarda (HR 0,517, [%95 GA: 0,392, 0,681]) g�zlenmi�tir.
�lk genel sa�kal�m (OS) interim analizinde, her iki kolda 197 olay g�zlemlenmi�tir ve HR, 0,786 (%95 CI: 0,589, 1,049) olarak bildirilmi�tir.
�kinci OS interim analizinde, her iki kolda 255 olay g�zlemlenmi�tir. Medyan OS, abemasiklib art� A� kolunda 67,1 ay ve plasebo art� A� kolunda 54,5 ayd�r. 0,754 (%95 GA: 0,584, 0,974) olarak g�zlemlenen HR, istatistiksel anlaml�l��a ula�mad���ndan (�ekil 3), �al��ma genel sa�kal�m� tam olarak karakterize etmeye devam etmektedir.
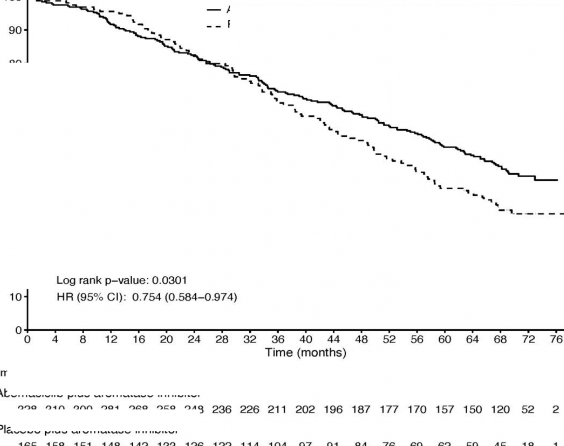
Zaman (ay)
Log s�ra p-de�eri: 0,0301
HR (%95 GA): 0,754 (0,584 – 0,974)
Genel Sa�kal�m Olas�l��� (%)
�ekil 3. MONARCH 3: Genel sa�kal�ma ili�kin Kaplan-Meier grafi�i (Tedavisi ama�lanan pop�lasyon)
Randomize Faz 3 �al��ma MONARCH 2: Fulvestrant ile kombinasyon halinde abemasiklib
Fulvestrant ile kombinasyon halinde abemasiklib'in etkilili�i ve g�venlili�i HR pozitif, HER2 negatif, lokal olarak ilerlemi� veya metastatik meme kanseri olan kad�nlar�n yer ald��� randomize, �ift k�r, plasebo kontroll� bir faz 3 �al��ma olan MONARCH 2 �al��mas�nda de�erlendirilmi�tir. Hastalar, g�nde iki kez 150 mg abemasiklib art� ilk dozdan iki hafta sonra uygulanan ek 500 mg dozla birlikte bir ayl�k aral�klarla 500 mg fulvestrant ve plasebo art� ayn� programa g�re tek ba��na fulvestrant almak �zere 2:1 oran�nda randomize edilmi�tir. Primer sonlan�m noktas� RECIST 1.1 uyar�nca ara�t�rmac� taraf�ndan de�erlendirilen PFS, temel sekonder etkililik sonlan�m noktalar� ise objektif yan�t oran� (ORR), klinik yarar oran� (KYO) ve genel sa�kal�m (GS) olarak belirlenmi�tir.
�al��maya al�nan hastalar�n medyan ya�� 60 (aral�k: 32-91) olarak kaydedilmi�tir. Her tedavi kolunda hastalar�n b�y�k b�l�m� beyaz �rktand�r ve daha �nce metastatik hastal�k i�in
kemoterapi almam��t�r. GnRH agonisti ile overi bask�lanan hastalar�n %17'si pre/perimenopozal d�nemdedir. Hastalar�n yakla��k %56'�nda viseral Hastalar�n yakla��k % 25'i primer endokrin direncine sahiptir (adjuvan endokrin tedavinin ilk 2 y�l�nda endokrin terapisinde ilerleme veya metastatik meme kanseri i�in ilk s�radaki endokrin tedavinin ilk 6 ay�nda) ve �o�unlu�unda endokrin direnci daha sonra geli�mi�tir. Hastalar�n %59'u (neo) adjuvan basamakta ve %38'i metastatik basamakta en son endokrin tedaviyi alm��t�r.
�al��ma, PFS'de primer sonlan�m noktas�n� kar��lam��t�r. Primer etkililik bulgular� Tablo 11 ve �ekil 4'te �zetlenmektedir.
Tablo 11. MONARCH 2: Etkililik verilerinin �zeti (Ara�t�rmac� de�erlendirmesi, tedavisi ama�lanan pop�lasyon)
| Abemasiklib art� fulvestrant | Plasebo art� fulvestrant |
Progresyonsuz sa�kal�m | N=446 | N=223 |
Ara�t�rmac� de�erlendirmesi, olay say�s� (%) | 222 (49,8) | 157 (70,4) |
Medyan [ay] (%95 CI) | 16,4 (14,4; 19,3) | 9,3 (7,4; 12,7) |
Tehlike oran� (%95 CI) ve p de�eri | 0,553 (0,449; 0,681), p=0,0000001 | |
Ba��ms�z radyografik inceleme, olay say�s� (%) | 164 (36,8) | 124 (55,6) |
Medyan [ay] (%95 CI) | 22,4 (18,3; NR) | 10,2 (5,8; 14,0) |
Tehlike oran� (%95 CI) ve p de�eri | 0,460 (0,363; 0,584); p <0,000001 | |
Objektif yan�t oran� [%] (%95 CI) | 35,2 (30,8; 39,6) | 16,1 (11,3; 21,0) |
Yan�t s�resi [ay] (%95 CI) | NR (18,05; NR) | 25,6 (11,9; 25,6) |
�l��lebilir hastal��� olan hastalarda objektif yan�t |
N=318 |
N=164 |
Objektif yan�t oran� [%] (%95 CI) | 48,1 (42,6; 53,6) | 21,3 (15,1; 27,6) |
Tam yan�t, (%) | 3,5 | 0 |
K�smi yan�t, (%) | 44,7 | 21,3 |
Klinik yarar oran� (�l��lebilir hastal�k) [%] (%95 CI) | 73,3 (68,4; 78,1) | 51,8 (44,2; 59,5) |
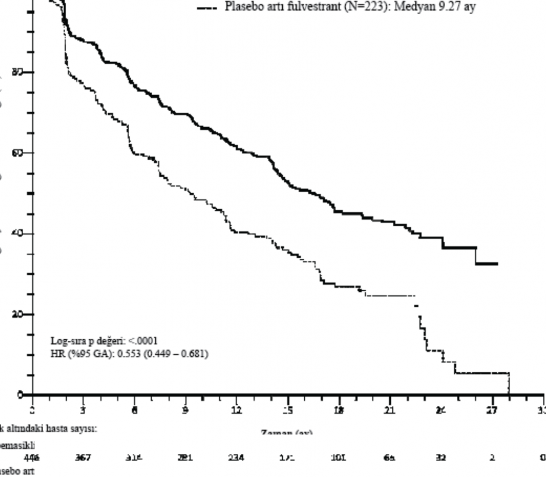
�ekil 4. MONARCH 2: Progresyonsuz sa�kal�ma ili�kin Kaplan-Meier grafi�i (Ara�t�rmac� de�erlendirmesi, tedavisi ama�lanan pop�lasyon)
|
|
|
|
|
|
|
|
|
|
|
Medyan PFS abemasiklib art� fulvestrant kolunda anlaml� �l��de uzam�� (HR 0,553 [%95 GA 0,449, 0,681]) ve abemasiklib art� fulvestrant kolunda medyan PFS 16,4 ay, plasebo art� fulvestrant 9,3 ay olarak belirlenmi�tir. Bu bulgular, abemasiklib art� fulvestrant ile tedavi edilen hastalarda hastal�k progresyonu veya �l�m riskinde klinik a��dan anlaml� olan %44,7 azalmaya ve medyan PFS'de 7,2 ayl�k art��a kar��l�k gelmektedir. Abemasiklib art� fulvestrant sa�l�kla ilgili ya�am kalitesinde klinik a��dan anlaml� veya �nemli bir zarara yol a�madan progresyonsuz sa�kal�m� uzatm��t�r.
�nceden belirlenmi� bir dizi alt grup PFS analiziyap�lm��t�r, ya� (<65 veya ≥65 y�l), �rk, co�rafi b�lge, hastal�k b�lgesi, endokrin tedavi direnci, �l��lebilir hastal�k varl���, progesteron resept�r� durumu ve menopozal durum dahil olmak �zere hasta alt gruplar� aras�nda tutarl� sonu�lar g�stermi�tir. Hastal�k progresyonu veya �l�m riskinde azalma viseral hastal�k bulunan hastalar (HR 0,481 [%95 GA: 0,369, 0,627], medyan PFS 6,5 aya kar��l�k 14,7 ay ), yaln�zca
kemikte hastal�k bulunan hastalar (HR 0,543, [%95 GA: 0,355, 0,833]) ve �l��lebilir hastal�k
bulunan hastalarda (HR 0,523, [%95 GA: 0,412, 0,644]) g�zlemlenmi�tir. Tehlike oran�,
pre/perimenopozal d�nemdeki hastalarda 0,415 (%95 GA: 0,246, 0,698), progesteron resept�r�
negatif hastalarda ise 0,509 [%95 GA: 0,325, 0,797]) olarak belirlenmi�tir.
PFS, lokal olarak ilerlemi� veya metastatik hastal��� olan ve �nceden endokrin tedavi almayan alt pop�lasyonda da tutarl�d�r.
ITT pop�lasyonundaki genel sa�kal�m (OS) analizi, plasebo art� fulvestrant alanlara k�yasla abemasiklib art� fulvestrant alan hastalarda istatistiksel olarak anlaml� bir iyile�me g�stermi�tir. Genel sa�kal�m sonu�lar� Tablo 12 ve �ekil 5'te �zetlenmi�tir.
Tablo 12. MONARCH 2: Genel sa�kal�m verilerinin �zeti (Tedavisi ama�lanan pop�lasyon)
| Abemasiklib art� fulvestrant | Plasebo art� fulvestrant |
Genel sa�kal�m | N = 446 | N = 223 |
Olaylar�n say�s� (n, %) | 211 (47,3) | 127 (57,0) |
Medyan OS [ay] (95 % CI) | 46,7 (39,2, 52,2) | 37,3 (34,4, 43,2) |
Tehlike oran� (95 %CI) | 0,757 (0,606, 0,945) | |
p de�eri | 0,0137 | |
N = hasta say�s�; CI = g�ven aral���; OS = genel sa�kal�m
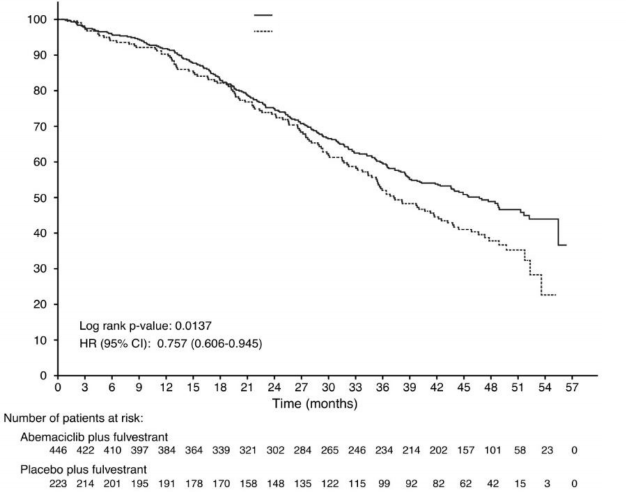
Abemasiklib art� fulvestrant (N=446): Medyan 46,72 ay Plasebo art� fulvestrant (N=223): Medyan 37,25 ay
Plasebo art� fulvestrant
Zaman (ay)
Risk alt�ndaki hasta say�s�: Abemasiklib art� fulvestrant
Log-s�ra p de�eri: 0,0137
HR (%95 GA): 0,757 (0,606-0,945)
Genel Sa�kal�m Olas�l��� (%)
�ekil 5. MONARCH 2: Genel sa�kal�ma ili�kin Kaplan-Meier e�risi (Tedavisi ama�lanan pop�lasyon)
S�n�fland�rma fakt�rlerine g�re OS analizleri, viseral hastal��� olan hastalarda OS HR'nin 0,675 (%95 GA: 0,511, 0,891) ve primer endokrin direnci olan hastalarda 0,686 (%95 GA: 0,451,
1,043) oldu�unu g�stermi�tir.
5.2. Farmakokinetik �zellikler
Genel �zelliklerEmilim:
Abemasiklib, Tde�eri 8 saat ve ortalama mutlak biyoyararlan�m� yakla��k %45 olan yava� emilimli bir ila�t�r. 50-200 mg terap�tik doz aral���nda, plazma maruziyeti (EAA) ve Cde�erindeki art�� dozla yakla��k olarak orant�l�d�r. Tekrarlanan g�nde iki kez dozlamadan sonra kararl� duruma 5 g�n i�inde ula��l�rken, abemasiklibin Cve EAA'ya g�re s�ras�yla 3,7 (%58 CV) ve 5,8 (%65 CV) geometrik ortalama birikim oran�yla birikti�i belirlenmi�tir. Y�ksek ya� i�erikli ���n abemasiklib ve aktif metabolitlerinin kombine EAA de�erini %9, Cde�erini
%26 art�rm��t�r. Bu de�i�iklikler klinik a��dan anlaml� bulunmam��t�r. Dolay�s�yla, abemasiklib a� veya tok karn�na al�nabilir.
Da��l�m:
Abemasiklib insanlarda plazma proteinlerine y�ksek oranda ba�lan�r (ortalama ba�l� fraksiyon yakla��k %96-98). Yakla��k 750 L (%69 CV) olarak belirlenen geometrik ortalama sistemik da��l�m hacmi abemasiklibin dokulara da��ld���n� g�stermektedir.
Abemasiklib ve aktif metabolitlerinin beyin-omurilik s�v�s�ndaki konsantrasyonlar� ba�lanmam�� plazma konsantrasyonlar�na benzerdir.
Biyotransformasyon:
Abemasiklibin temel klerens yolu hepatik metabolizmad�r. Abemasiklib, a��rl�kl� olarak sitokrom P450 (CYP) 3A4 taraf�ndan �e�itli metabolitlere metabolize edilir. Primer biyotransformasyon, ana ilac�n % 77'si olan bir EAA ile sirk�le olan bir metabolite hidroksilasyondur. Ek olarak, N-desetil ve N-desetilhidroksi metabolitleri, ana ilac�n % 39 ve
% 15'i olan EAA'larda sirk�le olmaktad�r. Bu sirk�le olan metabolitler, abemasiklibe benzer bir potansiyele sahiptir.
Eliminasyon:
Abemasiklibin geometrik ortalama hepatik klerensi (CL) 21,8 L/sa. (%39,8 CV) olarak hesaplan�rken, hastalardaki ortalama plazma eliminasyon yar�lanma �mr� 24,8 saat (%52,1 CV) olarak belirlenmi�tir. [C]-abemasiklibin tek oral dozundan sonra dozun yakla��k %81'i fe�es ve %3,4'� idrar ile at�l�r. Fe�este elimine edilen dozun b�y�k k�sm� metabolitlerdir.
Do�rusall�k/do�rusal olmayan durum: Veri bulunmamaktad�r.
Hastalardaki karekteristik �zellikler
�zel pop�lasyonlar:
Ya�, cinsiyet ve v�cut a��rl���:
Kanser hastalar�na ili�kin pop�lasyon farmakokineti�i analizinde (135 erkek, 859 kad�n; ya� aral��� 24-91 ya�, v�cut a��rl��� aral��� 36-175 kg) ya�, cinsiyet ve v�cut a��rl���n�n abemasiklib maruziyeti �zerinde etki g�stermedi�i saptanm��t�r.
Karaci�er yetmezli�i:
Abemasiklib karaci�erde metabolize edilir. Hafif (Child Pugh A) ve orta derece (Child Pugh B) karaci�er yetmezli�inin abemasiklib maruziyeti �zerinde etkisi olmad��� belirlenmi�tir. �iddetli karaci�er yetmezli�i (Child Pugh C) bulunan hastalarda ba�lanmam�� abemasiklib art� aktif metabolitleri s�ras�yla 2,1 kat ve 2,4 kat artm��t�r. Abemasiklibin yar� �mr� 24 saatten 55 saate y�kselmi�tir (Bkz. B�l�m 4.2).
B�brek yetmezli�i:
Abemasiklib ve metabolitlerinin renal klerensi min�r d�zeydedir. Hafif ve orta derece b�brek yetmezli�inin abemasiklib maruziyeti �zerinde etkisi olmad��� belirlenmi�tir. �iddetli b�brek yetmezli�i, son d�nem b�brek hastal��� olan veya diyaliz uygulanan hastalarla ilgili veri yoktur.
5.3. Klinik �ncesi g�venlilik verileri
�nsanlarla potansiyel olarak ilgili olan primer hedef organ bulgular�, 13 haftaya kadar s�rd�r�len �al��malarda fare, s��an ve k�peklerde g�r�len gastrointestinal kanal, hematolenfopoetik organlar ve erkek �reme sisteminde g�r�lm��t�r. G�zlerdeki ve kalp kapak��klar�ndaki etkiler, klinik olarak ili�kili maruziyet seviyelerinde yaln�zca kemirgenlerde meydana gelmi�tir. Akci�er ve iskelet kas� �zerindeki etkiler, yaln�zca kemirgenlerde insan maruziyet seviyelerinden en az 2 kat daha y�ksek maruziyet seviyelerinde ve b�breklerdeki etkiler, yaln�zca kemirgenlerde insan maruziyet seviyelerinden en az 6 kat daha y�ksek maruziyet seviyelerinde meydana gelmi�tir. 28 g�nl�k iyile�me s�resinin sonunda, erkek �reme sistemindeki etkiler istisnas� d���nda t�m hedef organ bulgular�nda tam veya k�smi iyile�me g�zlenmi�tir.
Genotoksisite
Abemasiklib bakteriyel ters mutasyon (Ames) testinde mutajenik, insan periferik kan lenfositlerindeki in vitro kromozomal aberasyon testinde klastojenik ve in vivo s��an kemik ili�i mikron�kleus testinde klastojenik bulunmam��t�r.
Karsinojenisite
Abemasiklib, s��anlarda ve farelerde yap�lan 2 y�ll�k �al��malarda kanserojenisite a��s�ndan de�erlendirilmi�tir. Erkek s��anlarda abemasiklibin g�nl�k oral uygulamas�, insan klinik maruziyetinin yakla��k 1,5 kat� maruziyetlerde benign testik�ler interstisyel h�cre adenomlar� ile sonu�lanm��t�r. �lave olarak, insan klinik maruziyetinin yakla��k 0,1 kat� maruziyetlerde interstisyel h�cre hiperplazisi g�zlemlenmi�tir. Bu etkilerin insanlardaki yans�mas� bilinmemektedir. Farelerde veya di�i s��anlarda abemasiklib uygulamas�na ba�l� neoplastik bulguya rastlanmam��t�r.
Fertilite bozuklu�u
Abemasiklib, �reme potansiyeli olan erkeklerde fertilite bozuklu�una neden olabilir. 3 aya kadar tekrarlanan doz toksisite �al��malar�nda abemasiklib ile ili�kili bulgular, testis, epididimis, prostat ve seminal vezik�ldeki azalm�� organ a��rl�klar�, intratub�ler h�cresel debris, hipospermi, t�b�ler dilatasyon, atrofi ve dejenerasyon/nekrozu i�ermektedir. Bu etkiler, s��anlarda ve k�peklerde insan klinik maruziyetinin s�ras�yla yakla��k 2 ve 0,02 kat� maruziyetlerde meydana gelmi�tir. Bir s��an erkek fertilite �al��mas�nda, abemasiklibin �reme performans� �zerinde herhangi bir etkisi olmam��t�r.
Bir s��an di�i fertilite ve erken embriyonik geli�im �al��mas�nda ve tekrarlanan doz toksisite �al��malar�nda, abemasiklibin �reme performans� �zerinde herhangi bir etkisi olmam��t�r veya di�ilerde fertilitenin bozulma riskinin g�stergesi olan, di�i �reme sistemi �zerinde herhangi bir �nemli etkisi olmam��t�r.
Geli�im toksisitesi
Abemasiklib, insanlar i�in �nerilen doza benzer maternal maruziyetlerde teratojenik bulunmu� ve fetus a��rl���nda azalmaya neden olmu�tur.
6. FARMAS�T�K �ZELL�KLER
6.1. Yard�mc� maddelerin listesi
Tablet �ekirde�i Kroskarmelloz sodyum
Laktoz monohidrat; Laktoz Hidrat (s���r kaynakl�) Mikrokristalin sel�loz 101
Mikrokristalin sel�loz 102
Silikon Dioksit; Silika, Sulu Kolloidal; Sulu Silikon Dioksit Sodyum stearil fumarat
Film kaplama
Polivinil alkol - K�smen Hidrolize Edilmi� (E1203) Titanyum dioksit (E171)
Makrogol 4000 / PEG MW 3350 (E1521)
Talk (E553b)
6.2. Ge�imsizlikler
Ge�erli de�ildir.
6.3. Raf �mr�
36 ay
6.4. Saklamaya y�nelik �zel tedbirler
30°C alt�ndaki oda s�cakl���nda saklay�n�z.
6.5. Ambalaj�n niteli�i ve i�eri�i
Al�minyum folyo ile kapat�lm�� PCTFE/PE/PVC blisterlerde 28, 42 veya 56 film kapl� tabletlik ambalajlarda
T�m ambalaj boyutlar�nda pazarlanmayabilir.
6.6. Be�eri t�bbi �r�nden arta kalan maddelerin imhas� ve di�er �zel �nlemler
Kullan�lmam�� olan �r�nler ya da at�k materyaller ‘T�bbi At�klar�n Kontrol� Y�netmeli�i' ve ‘Ambalaj ve Ambalaj At�klar�n�n Kontrol� Y�netmelikleri'ne uygun olarak imha edilmelidir.7. RUHSAT SAH�B�
Lilly �la� Ticaret Ltd �ti Ac�badem Mah. �e�en Sokak Akasya Ac�badem Kent Etab� A Blok Kat: 3
34660 �sk�dar / �stanbul
Tel : 0 216 554 00 00
Faks : 0 216 474 71 99
 Parkinson Hastal���
Hastal�k ilk kez 1817 de �ngiliz doktor James Parkinson taraf�ndan tan�mlanm�� ve Dr. Parkinson hastal��� “sallay�c� fel�” olarak kaleme alm��.
Parkinson Hastal���
Hastal�k ilk kez 1817 de �ngiliz doktor James Parkinson taraf�ndan tan�mlanm�� ve Dr. Parkinson hastal��� “sallay�c� fel�” olarak kaleme alm��. |
 S�rt A�r�s�
S�rt a�r�s� birden bire ortaya
��k�p �iddetli (akut) olabilir veya zamanla geli�ip daha uzun
s�reli sorunlara (kronik) neden olabilir.
S�rt A�r�s�
S�rt a�r�s� birden bire ortaya
��k�p �iddetli (akut) olabilir veya zamanla geli�ip daha uzun
s�reli sorunlara (kronik) neden olabilir. |
�LA� E�DE�ERLER�
| E�de�er �la� Ad� | Barkodu | �la� Fiyat� |
|---|---|---|
| YULAREB | 8699673098289 | 42,820.01TL |
| Di�er E�de�er �la�lar |
 |
En Yayg�n Alerji T�rleri Ba����kl�k sistemi, polen, ar� zehiri veya evcil hayvan gibi yabanc� bir maddeye veya �o�u insanda reaksiyona neden olmayan bir yiyece�e tepki g�sterdi�inde alerjiler meydana gelir. |
 |
Deri Kanseri Deri kanseri �ok rastlanan bir hastal�kt�r. �� ana t�r� bulunur ;genelde kemirici �lser olarak bilinen bazal h�creli karsinom, yass� h�creli karsinom ve k�t� huylu t�m�r. |
 |
Ruh ve Ak�l Sa�l���m�z� Geli�tirmek �yi ak�l ve ruh sa�l��� sahip olmaktan ziyade, yapt���n�z �eylerdir. Ak�l ve ruhsal olarak sa�l�kl� olmak i�in kendinize de�er vermeli ve kendinizi kabul etmelisiniz. |
�LA� GENEL B�LG�LER�
Lilly �la� Ticaret Ltd.�ti.
| Sat�� Fiyat� | 42820.01 TL [ 17 Dec 2024 ] |
| �nceki Sat�� Fiyat� | 42820.01 TL [ 2 Dec 2024 ] |
| Original / Jenerik | Original �la� |
| Re�ete Durumu | K�s�tlanm�� Beyaz Re�eteli bir ila�d�r. |
| Barkodu | 8699673098289 |
| Etkin Madde | Abemasiklib |
| ATC Kodu | L01EF03 |
| Birim Miktar | 100 |
| Birim Cinsi | MG |
| Ambalaj Miktar� | 42 |
| Antineoplastik ve �mm�nomod�lat�r Ajanlar |
| �thal ( ref. �lke : Fransa ) ve Be�eri bir ila�d�r. |